Изобретение относится к получению белка, обладающего способностью стимулировать рост и дифференциацию первичных кроветворных прогениторных клеток, в частности фактора стимуляции колонии (ФСК). В одном аспекте изобретение обеспечивает способ получения ФСК-белка путем технологии рекомбинантной ДHК, векторы, содержащие ген экспрессии указанного белка, микроорганизмы и клеточные линии, трансформированные указанными векторами, и ФСК-белок, полученный таким образом. Второй аспект изобретения обеспечивает способ выделения и очистки ФСК-белка из природных или рекомбинантных источников и очищенный таким образом ФСК-белок, имеющий степень чистоты и уровень активности выше тех, что были описаны ранее.
Найдено, что многие различные типы клеток крови происходят из многопотенциальных кроветворящих клеток спинного мозга. Клетки спинного мозга выполняют две функции: /1/ они репродуцируют сами себя, в результате чего поддерживается популяция клеток спинного мозга в организме и /2/ они обеспечивают потомство клеток, передающее различия в любых типах зрелых клеток крови. Клетка, которая передает различия по конкретному кроветворному пути, называется клеткой-предшественником. Клетки-предшественники для T-лимфоцитов, B-лимфоцитов, гранулоцитов, красных кровяных клеток, тромбоцитов и эозинофилов, так же как и более ранние предшественники, которые могут индивидуально приводить к увеличению некоторых типов зрелых клеток, были экспериментально изучены как in vivo, так и in vitro /Dexter, T.M., 1983, J. Patology 141, 415-433/. Уже было определено in vitro, что пролиферация и/или дифференциация предшественника каждого типа клеток зависит от определенных "факторов", которые происходили из различных источников. Например, последние предшественники красных кровяных клеток требуют фактора, называемого эритропоиэтином. Факторы, требующиеся для выживания, пролиферации и дифференциации миелоидных предшественников, переходящих в форму зрелых нейтрофильных гранулоцитов, моноцитов и зрелых макрофагов, называют факторами стимуляции колоний (ФСК).
ФСК активность экстенсивно изучалась на мышах. Большинство органов взрослых мышей продуцирует ФСК активность. Однако, композиции, содержащие ФСК активность, которые были получены из различных тканей и различными методами, различаются по своим биохимическим характеристикам. Так, структурное соотношение между различными факторами остается неизвестным. Кроме того, ФСК активность действует на более, чем одной стадии развития гранулоцита и макрофага, и снова точно не известно, единственный ли фактор является ответственным за все наблюдаемые активности или же различные факторы действуют на каждой стадии. / Burgess, A. и Metealf, D. 1980 Blood 56, 947-957/.
Человеческая ФСК активность была получена из плаценты некоторых плодных тканей, макрофагов и стимулированных T-клеток. Линия T-клеток (Mo), которая продуцирует одну или несколько мощных ФСК активностей, была установлена от пациента с вариантом T-клетки "волосатой" клетки лейкемии (лейкемический ретикулоэндотелиозис) /bolde et al, 1978, Blood, 52, 1068-1072).
Способность СК активности стимулировать продуцирование гранулоцитов и макрофагов указывает, что фармацевтические композиции, обладающие ФСК активностью, являются клинически полезными в ситуациях, когда требуется повышенное продуцирование таких типов /миелоидных/ клеток. Действительно, показано, что некоторые пациенты с крайне высокими уровнями по-видимому нормальных циркулирующих гранулоцитов имеют опухоли, которые свврх-продуцируют ФСК. В одном случае, при хирургическом удалении опухоли количество гранулоцитов быстро падает к нормальному уровню, четко подтверждая, что ФСК может быть полезным при регулировании количеств циркулирующих гранулоцитов. /Hockiug, W. Goodinau, J., и Golde, D., Blood, 61, 600 /1983//. В частности, ФСК композиции являются клинически полезными для лечения миело-супрессии, вызванной хемотерапевтическим лечением рака или его лечением с помощью облучения. Кроме того, ФСК композиции являются полезными при лечении сильных инфекций, потому что ФСК может увеличивать и/или активировать количество гранулоцитов и/или моноцитов.
Имеются различные дифференцированные типы известных ФСК активностей, включая гранулоциты. ФСК /G-ФСК/, макрофаг-ФСК/M-ФСК/, гранулоцит-макрофаг ФСК /GM-ФСК/ и мульти-ФСК. Настоящее изобретение в частности относится к GM-ФСК. ФСК-белки являются известными из различных животных источников. Однако настоящее изобретение в частности относится к приметному ФСК, более конкретно к человеческому ФСК и к обезьяньему ФСК.
Биологическая и биохимическая характеристика композиций, обладающих ФСК активностью, и изучение этих композиций в клинических условиях было затруднено до настоящего времени недостаточным количеством и примесями ФСК-композиций человека и/или других приматов. Следует учитывать, что должно быть желательным идентифицировать белок или белки, ответственные за ФСК активность. Кроме того, желательно иметь приматный, в частности человеческий источник такого ФСК, который может легко снабжать такими белками в таких количествах и такой чистоты, которые достаточны для биологической и биохимической характеристики и для использования их в качестве терапевтических агентов.
Разработанные ранее методики молекулярного клонирования делают возможным клонирование нуклеотидной последовательности, которая кодирует белок, и получение такого белка в достаточном количестве, используя подходящую систему хозяин-вектор, /Т. Маниатис "Молекулярное клонирование - Лабораторное руководство", Колд Спринг Харбор Лаборатору, Колд Сиринг Харбор, 1982 г./. Затем белок может быть извлечен по известным методикам выделения и очистки. Методы клонирования, используемые до настоящего времени, могут быть сгруппированы в три основные категории: /1/ способы, основанные на знании структуры белка, например, его аминокислотной последовательности, /2/ способы, основанные на идентификации белка, экспрессированного клонированным геном, с использованием специфического к такому белку антителу; и /3/ способы, основанные на идентификации видов РНК, которые могут быть транслированы для получения белка или активности, кодируемых интересующим геном.
Каждый из этих классов способов становится трудным для применения, когда интересующий белок, такой как ФСК-белок, доступен в очень малом количестве. Следовательно, если трудно получить адекватное количество очищенного белка, то трудно и определить аминокислотную последовательность или даже частичные последовательности белка. Подобным образом, идентификацию экспрессированного белка связывающим антителом предпочтительно проводят при использовании поликлональной антисыворотки с высоким титром. Такая антисыворотка не может быть получена при отсутствии достаточных количеств чистого белка (антигена). Моноклональное антитело предполагает альтернативную попытку, но требуемое антитело также может быть получено с большим трудом при отсутствии подходящего антигена и такое моноклональное антитело не может взаимодействовать с белком в том виде, в каком белок экспрессирован доступной рекомбинантной системой хозяин-вектор. Наконец, трансляция видов РНК для получения идентифицируемого белка или активности требует, чтобы искомая РНК находилась в источнике РНК в достаточном избытке, чтобы получить достоверный белок или сигнальную активность. Относительный избыток РНК, кодирующей конкретный белок, обычно параллелен избытку белка, так что редкий белок обычно кодируется редкой РНК.
Моноклеточную линию использовали как в качестве исходного материала для очистки человеческих ФСК, так и для идентификации соответствующих матричных РНК. Однако даже при таком относительно хорошем источнике ФСК активности оказалось очень трудно выделить белок даже для структурных исследований.
Для того, чтобы решить проблемы, присущие клонированию нуклеотидной последовательности, кодирующей редкий белок, такой как ФСК, с помощью описанных выше способов, разработан новый способ. Этот способ требует только, чтобы генный продукт или его активность могли быть достоверно измерены. Подходящие способы определения ФСК описаны в примере 2 ниже. Во втором аспекте, разработан способ очистки, который пригоден для выделения и очистки белка ФСК как из рекомбинантных, так и природных источников при уровне очистки и активности намного более высоком, чем был ранее возможен.
В его первом аспекте настоящее изобретение решает проблемы известного уровня техники и обеспечивает источник белка, обладающего ФСК активностью, при использовании технологии с рекомбинантной ДНК. В соответствии с настоящим изобретением используется новая методика клонирования, которая требует только пробу для ФСК активности, чтобы клонировать кДНК, кодирующую белок, обладающий ФСК активностью. Итак, настоящее изобретение обеспечивает кДНК, кодирующую белок, обладающий ФСК активностью /т.е. ФСК/кДНК/, микроорганизм или клеточную линию, трансформированную рекомбинантным вектором, содержащим такой ФСК/кДНК, и способ получения ФСК белка путем экспрессии указанной ФСК/кДНК при культивировании микроорганизма или клеточной линии. Поскольку ФСК белок продуцируется из клона в соответствии с настоящим изобретением, мы может быть уверены, что это белок, который обладает ФСК активностью. Далее изобретение заключается в способе получения и изоляции вектора трансформации, содержащего ФСК/кДНК, указанный способ состоит из получения РНК из клетки, продуцирующей ФСК; получения полиаденилированной матричной РНК из указанной РНК; получения однониточной кДНК из указанной матричной РНК; превращения однониточной кДНК в двуниточную кДНК; вставки двуничтоной кДНК в векторы трансформации и трансформирование бактерий указанным вектором для образования колоний; отбора пулов из 200-500 колоний каждый и изоляции плазмиды ДНК из каждого пула; трансфекции плазмиды ДНК в подходящую клетку-хозяина для, экспрессии ФСК белка; культивирования трансфецированных клеток и испытания надосадочного слоя на ФСК активность; отбора ФСК положительных пулов и скринирования колоний, использованных для образования пула, чтобы идентифицировать колонии, обладающие ФСК активностью.
ФСК-белки настоящего изобретения обеспечивают рост и дифференциацию гормонов для клеток миелоидной системы. Например, указывалось на их клиническое использование при лечении миелосупрессии, особенно (симптоматической) гранулоцитопении после хемотерапевтического лечения рака или после его лечения облучением.
На фиг.1 представлены последовательности ДНК, которые кодируют ФСК-белок в соответствии с настоящим изобретением. Последовательность ДНК, представленная полностью, кодирует один вариант человеческого ФСК, упоминаемый как ФСК-Thr. Другой аллель кодирует идентичный продукт с тем исключением, что Thr в положении 100 заменен Ile /ФСК-Ile/. Изменения, показанные выше для человеческой последовательности, представляют собой различия в последовательности ДНК, кодирующей ФСК гиббона /ФСК обезьяны гиббона/ /ФСК-G/. Также показаны уменьшенные последовательности аминокислот.
На фиг. 2 схематически представлено получение плазмиды pTP из плазмиды pAd D26 SV pA /3/.
На фиг. 3 схематически представлено продолжение фиг. 2 и иллюстрируется получение плазмиды p91023 из плазмиды pTPL.
На фиг. 4 схематически представлено продолжение фиг. 3 и показана плазмида p91023 /B/.
На фиг. 6 схематически представлен вектор pTALC-185P.
На фиг. 7 схематически представлен вектор AJ-14.
Следующие определения приведены для облегчения понимания настоящей заявки. По мере того, как определения меняются в зависимости от значений, применяемых на данном уровне техники, приведенные ниже определения даны для контроля.
Амплификация означает процесс, при котором клетки продуцируют копии генов внутри их хромосомальной ДНК.
ФСК представляет собой биологическую активность, определенную путем анализа, описанного здесь.
ФСК-белок представляет собой белок из приматного источника, который проявляет ФСК активность. Для целей настоящего изобретения термин ФСК-белок, включает модифицированный ФСК-белок, аллальные вариации ФСК-белка и ФСК-белок, предшествующий MET-остатку.
Направление вниз означает направление к 3'-концу нуклеотидной последовательности.
Усилитель представляет собой нуклеотидную последовательность, которая может сделать возможной транскрипцию гена независимо от положения усилителя по отношению к гену или от ориентации последовательности.
Ген представляет собой деоксирибонуклеотидную последовательность, кодирующую данный белок. Для целей настоящей заявки ген не должен включать нетранслируемые боковые области, такие как сигналы начала транскрипции РНК, сайты полиаденильного присоединения, промоторы и усилители.
Связывание представляет собой процесс образования фосфоди/сложно/эфирной связи между 5'- и 3'-концами двух нитей ДНК. Оно может быть осуществлено несколькими хорошо известными ферментативными методами, включая связывание тупого конца T4 лигазой.
Ориентация относится к порядку нуклеотидов в последовательности ДНК. Обратная ориентация последовательности ДНК представляет собой последовательность, у которой порядок последовательности 5' к 3' по отношению к другой последовательности является обратным при сравнении указанного места в ДНК, из которой последовательность была получена. Такие указанные точки (места) могут включать направление транскрипции других определенных последовательностей ДНК в источнике ДНК или в источнике репликации реплицируемых векторов, содержащих последовательность.
Транскрипция означает изменение генотипа клеток путем клеточного поглощения экзогенной ДНК. Трансформация может быть детектирована в некоторых случаях путем изменения фенотипа клетки. Трансформированные клетки называются трансформантами. Пре-трансформация клеток указывается в отношении родительских клеток.
Трансляция означает синтез полипептида из матричной РНК.
Активность фактора стимуляции колоний (ФСК) может происходить из ряда клеточных источников, включая кондиционированную среду из периферических моноядерных клеток крови, ткани легких и плаценты, и костного мозга, мочи от анемичных пациентов, сыворотки, и нормальных и неопластичных клеток T-лимфоцита и моноядерного фагоцита. Одна клеточная линия, которая продуцирует ФСК, представляет собой Mo клеточную линию, депонированную и доступную публике из ATCC под кодовым номером CP 8066. ФСК, продуцированный этой клеточной линией, известен как гранулоцитный макрофаг ФСК (или GM-ФСК), и, разумеется, как человеческий ФСК. Одним источником ФСК гиббона является линия Т-клеток, обозначенных ИСД M A-144 и депонированных и доступных для публики из ATCC под кодовым номером HB 9370, депонированы 29 сентября 1983 г.
Для того, чтобы изолировать ФСК клон в соответствии с настоящим изобретением, была использована новая процедура, которая требует только техники определения ФСК-активности. Сначала идентифицируют клетку, которая продуцирует ФСК активность, такую как T-лимфоцитные клетки (или другие источники, такие как представлены выше). Затем собирают мРНК клетки. Предпочтительно используют Т-лиффоцитные клетки. В таком случае отделяют связанную с мембраной мРНК, которая содержит мРНК для лимфокина, от свободной мРНК в клетках. Это отделение, как полагают, обогащает собранную мРНК в 5-10 раз последовательностями для лимфокина и таким образом сокращает усилия, вкладываемые в идентификацию целевого ФСК клона. Затем получают полиаденилированную матричную РНК хроматографией на олиго-dT - целлюлозе.
Готовят банк кДНК из мРНК, используя вектор, подходящий для трансфекции в хозяина для экспрессии целевого белка, обладающего ФСК активностью. Сначала получают нить кДНК с использованием стандартных методик, применяя полученную выше мРНК. Затем превращают гибрид РНК/кДНК в двуниточную форму кДНК. Затем кДНК может быть вставлена в подходящий вектор.
Предпочтительная систем хозяин-вектор для изоляции клона ФСК основана на экспрессии ФСК кДНК в подходящем векторе трансформации. Подходящий вектор трансформации может обеспечить случайное введение ДНК в клетки млекопитающих. /Mellon, P., V. Parker, Y. Gluzman T. Maniatis, 1981 Cell, 27, 279-288/. Для изоляции целевых ФСК-трансформантов не требуется, чтобы все клетки популяции стабильно содержали экзогенные гены, которые экспрессируют целевой ФСК-продукт. Возможно временное вхождение экзогенных генов в субпопуляцию клеток, так что субпопуляция будет экспрессировать целевой продукт в течение нескольких дней. Поскольку нет нужды в отбираемом маркере в векторе трансформации для трансфекции ДНК и системы экспрессии в соответствии с настоящим изобретением, экзогенная ДНК может быть потеряна при росте клеток в течение 1-2 недель. Однако через 2-3 дня после трансфекции подходящих клеток млекопитающих, как было обнаружено, целевые продукты могут быть синтезированы и могут быть детектированы.
Выбор системы хозяин-вектор основан на развитии клеточных линий CV-1 обезьян, трансформированных молекулой ДНК репликация-происхождение-дефектных SV 40/Glusman, Y., Cell, 23, 175-182, 1981/. Трансформированные CV-1 клетки обезьян, содержащие дефектную SV 40 ДНК, обозначенные COS /CV-1, дефектное происхождение, SV 40/, не содержат полной копии генома SV 40, но продуцируют высокие уровни широкого T антигена и разрешают репликацию ДНК 40. Они также эффективно поддерживают репликацию SV 40, содержащих делеции в ранней области, и бактериальных плазмид, которые содержат 40 источник репликации /Myers, R. M. and Tjian, R. 1980, PNA 77, 6491-6495/. Следовательно, такая система обеспечивает средство амплификации трансфецированной экзогенной ДНК через репликацию ДНК медиированных SV 40, чтобы повысить уровень мРНК и белка, экспрессированного из экзогенной ДНК. Однако также являются полезными другие подобные системы.
Векторы, использованные для ФСК экспрессии, обычно содержат различные элементы, такие как усилители, промоторы, интроны, сайты полиаденилирования, 3'-некодирующие области и активаторы трансляции, как будет описано ниже.
Здесь векторы могут включать усилители. Усилители функционально отличаются от промоторов, но очевидно работают совместно с промоторами. Их функция на клеточном уровне еще недостаточно понятна, но их уникальной характерной чертой является способность активировать или делать возможной транскрипцию независимо от положения или ориентации. Промоторы должны быть расположены вверх от гена, тогда как усилители могут находиться вверх или 5' от промотора, внутри гена как интрона, или вниз от гена между геном и сайтом полиаденилирования. Вставленные промоторы не являются функциональными, а вставленные усилители являются. Усилители являются цис-активными, а именно они действуют на промоторы, только если они находятся в одной и той же нити ДНК. Общую дискуссию об усилителях смотри у Khoury et al., Cell, 33, 313-314 /1983/.
Предпочтительные усилители для использования в клетках млекопитающих получают из вирусов животных, таких как обезьяний вирус 40, вирус полиомы, вирус бычьей папилломы, ретровирус и аденовирус. Идеально, усилитель должен быть из вируса, для которого клетка-хозяин является рекомендованной, т.е. который обычно заражает клетки хозяина. Вирусные усилители могут быть легко получены из публично доступных вирусов. Усиливающие области для некоторых вирусов, а именно вируса саркомы Рауса и обезьяньего вируса 40, хорошо известны. Смотри Lueiu et al., Cell 33, 705-716 (1983). Из традиционной молекулярной биологии известно расположение этих областей на основе опубликованных карт рестрикции для указанных вирусов и, в случае необходимости, можно модифицировать сайты, чтобы сделать возможной сращивание усилителя с вектором, как желательно. Например, смотри Кауфман и др., J. Mol. Biol., 159, 601 - 621 /1982/ и Mol. Cell Biol. 2 /II/, 1304-1319 /1982/. Альтернативно усилитель может быть синтезирован из данных последовательностей; размеры вирусных усилителей (обычно менее примерно 150 пар оснований/ являются достаточно маленькими, чтобы это могло быть осуществлено на практике.
Другим элементом, который должен присутствовать в векторе, является сайт полиаденилированного сращивания /или присоединения/. Он представляет собой последовательность ДНК, расположенную вниз от транслируемых областей гена, вскоре вниз от которого в свою очередь добавляются ринонуклеотиды остановки транскрипции и аденина для образования полиаденинового нуклеотидного хвоста на 3' конце матричной РНК. Полиаденилирование является важным при стабилизации матричной РНК против разложения в клетке, ситуация, при которой снижается уровень матричной РНК и, следовательно, уровень белкового продукта.
Эукариотные сайты полиаденилирования хорошо известны. Consensus-последовательность существует среди эукариотных генов: гексануклеотид 5'-AAUAAA-3' найден 11-30 нуклеотидов от точки, в которой начинается полиаденилирование. Последовательности ДНК, содержащие сайты полиаденилирования, могут быть получены из вирусов в соответствии с опубликованными сообщениями. Типичные последовательности полиаденилирования могут быть получены из бета-глобина мыши и поздней или ранней областей генов обезьяньего вируса 40, но предпочтительными являются вирусные сайты полиаденилирования. Поскольку эти последовательности являются известными, они могут быть синтезированы in vitro и связаны в вектор традиционным способом.
Последовательность, которая отделяет сайт полиаденилирования от трансляционного стор-кодона, является предпочтительно нетранслируемой последовательностью ДНК, такой как непромотированный эукариотический ген. Поскольку такие последовательности и гены не обеспечены промотором, они не будут экспрессироваться. Последовательность должна простираться на значительное расстояние, порядка примерно 1000 оснований, от стоп-кодона до сайта полиаденилирования. Такая 3'-нетранслируемая последовательность обычно в результате приводит к повышению выхода продукта. Вектор может заканчиваться примерно за 30 пар оснований вниз от consensus-последовательности полиаденилирования, но предпочтительно сохранить 3'-последовательности, найденные вниз по ходу от сайта полиаденилирования, в окружении их дикого типа. Эти последовательности обычно протягиваются примерно на 200-600 пар оснований вниз от сайта полиаденилирования.
Наличие интронов в нетранслируемом транскрибируемом участке вектора может увеличить выход продукта. Такие интроны могут быть получены из других источников, чем клетки хозяина или источники генов. Например, гибридный интрон, состоящий из 5'-сайта сращивания от второго интрона трехчастного лидера аденовируса и 3'-сайта сращивания от гена иммуноглобулина, вставленного вниз от сайта старта транскрипции в основной последний промотор аденовируса, приводит в результате к увеличению выхода продукта.
В предпочтительном варианте вектора клонирования ФСК и экспрессии имеется ген активатора трансляции. Активаторы трансляции являются генами, которые кодируют или белок иди продукты РНК, которые влияют на трансляцию целевой мРНК. Лучшим примером является аденовирус-ассоциированный /VA/ ген /VAI/, который считывается в коротких типах РНК, которые взаимодействуют с последовательностями в 5' нетранслируемой области основных поздних мРНК аденовируса /Thimmuappaya et al., 1982, Ce, 3, 543/. Необходимые последовательности трансляционной активации с помощью VA РНК лежат внутри трехчастного лидера последней мРНК аденовируса. Трехчастный лидер аденовируса сращивают вместе с несоприкасающимися областями генома аденовируса и находится на 5'-конце основных последних транскриптов аденовируса. VA РНК может взаимодействовать для активации трансляции мРНК, которые содержат последовательность трехчастного лидера. Итак, предпочтительный вектор клонирования кДНК и экспрессии содержит соединенную форму трехчастного лидера и гены VA аденовируса.
Эти векторы могут быть синтезированы по методикам, хорошо известным специалистам в данной области. Компоненты векторов, такие как усилители, промоторы и т. п., могут быть получены из природных источников или синтезированы, как описано выше. В основном, если найдено, что компоненты в ДНК доступны в большом количестве, а именно, такие компоненты, как вирусные функции, или если они могут быть синтезированы, например, сайты полиаденилирования, тогда при соответствующем использовании рестрикционных ферментов могут быть получены большие количества вектора при простом культивировании организма-источника, переваривании его ДНК соответствующей эндонуклеазой, отделении фрагментов ДНК, идентификации ДНК, содержащей интересующий элемент, и его извлечении. Обычно вектор трансформации должен быть введен в малом количестве и затем связан в подходящий автономно реплицирующийся синтетический вектор, такой как прокариотная плазмида или фаг. В большинстве случаев может быть использована плазмида pBP322. Смотри Кауфман и др., выше.
Синтетический вектор используют для клонирования связанных векторов трансформации обычным образом, а именно путем трансфекции возможного прокариотного организма, репликации синтетического вектора с большим числом копий и извлечения синтетического вектора при лизисе клеток и отделения синтетического вектора от клеточного дебриса.
Векторы, содержащие кДНК, приготовленную из клетки, которая продуцирует ФСК активность, затем трансфецируют в E.coli и помещают на чашки Петри приблизительно 2000 колоний на чашку. Колонии вынимают на нитроцеллюлозный фильтр и фильтр переносят на новую пластину, которую хранят как первый оригинал. После выращивания этих колоний делают реплики и сравнивают с оригиналом, тщательно отмечая, чтобы секции фильтров реплик могли быть идентифицированы с соответствующим участком пластины оригинала.
Каждый фильтр реприку разрезают на секции, содержащие заранее определенное число колоний на секцию, предпочтительно 200-500 колоний на секцию. Колонии с каждой секции соскабливают в среду, такую как L-бульон, бактерии собирают центрифугирование и отделяют плазмиду ДНК. Плазмиду ДНК каждой секции трансфецируют в подходящего хозяина для экспрессии белка. Предпочтительный синтетический вектор здесь является мутантом E.coli плазмиды pBP 322, в которой были делецированы последовательности, которые являются вредными для эукариотных клеток. Смотри Кауфман и др., выше. Использование этого мутанта устраняет необходимость в делении остатка плазмиды перед трансфекцией. После выращивания трансфецированных клеток среды проверяют на ФСК активность. Положительная проба показывает, что колония, содержащая ФСК/кДНК, находится на конкретной секции на фильтре.
Для определения, какой из клонов на секции исходного первого оригинала фильтра содержит ФСК/кДНК, каждый клон на секции фильтра пересаживают и выращивают. Затем культуры помещают на матрицу Пулы получают от каждого горизонтального ряда и вертикальной колонки матрицы. Готовят образцы ДНК из каждого пула культуры и трансфецируют в клетку-хозяина для экспрессии. Надосадочные слои для каждого пула проверяют на ФСК активность. Одна вертикальная колонка пула и горизонтальный ряд пула должны продуцировать ФСК активность. Клон, общий для этих пулов, будет содержать ФСК/кДНК. Если матрица, содержит больше одного положительного клона, больше чем одна колонка и ряд должны быть положительными. В таком случае может быть необходимым дальнейший скрининг малого количества клонов.
Вырезают ФСК/кДНК из клонов рестрикционными ферментами и можно провести определение аминокислотной последовательности обычными методами. Можно легко оценить что описанная здесь процедура может быть использована для получения ФСК/кДНК из любого источника. Полная последовательность ФСК/кДНК в соответствии с изобретением представлена на фиг. 1 вместе с предсказанной аминокислотной последовательностью транслированного ФСК белка.
Последовательность ДНК, кодирующая белок, проявляющий ФСК активность, в соответствии с настоящим изобретением, такая как представлена на фиг. 1, может быть модифицирована с помощью традиционных методик для получения вариантов в конечном ФСК белке, который еще обладает ФСК активностью в описанных здесь ниже пробах. Так, например, одна, две, три, четыре или пять аминокислот могут быть заменены другими аминокислотами. В бельгийском патенте N 898016, приведенном здесь в качестве уровня техники, описана одна такая типичная методика для замены цистеина, например, серином.
В соответствии с настоящим изобретением ФСК/кДНК включает природный ФСК/кДНК ген, предшествующий АТС кодону, и ФСК/кДНК, кодирующей аллельные вариации ФСК-белка. Один аллель представлен на фиг. 1. Другой аллель, который мы обнаружили, имеет тимидиновый остаток в положении 365 вместо цитозинового остатка, показанного на фиг. 1. ФСК-белок настоящего изобретения включает 1-метиониновое производное ФСК-белка/Met-ФСК/ и аллельные вариации ФСК-белка. Зрелый ФСК-белок, представленный последовательностью на фиг. 1 начинается с последовательности Ala. Pro. Ala Arg ..., начало которой обозначено стрелкой после нуклеотида номер 59 на фиг. 1. Met-ФСК - будет начинаться с последовательности Met. Ala. Pro. Ala. Arg ... Аллельная вариация, представленная на фиг. 1, имеет Thr у аминокислотного остатка номер 100 (начиная от Ala после стрелки) и может быть упомянута как ФСК/Thr/. Другая вариация имеет Ile остаток у положения 100 и может быть упомянута как ФСК/Ile/. Очищенный ФСК-белок настоящего изобретения проявляет удельную активность по крайней мере 107 единиц/мг белка и предпочтительно по крайней мере 4•107 единиц/мг при пробе с человеческими клетками костного мозга.
Системы вектор-хозяин для экспрессии ФСК могут быть прокариотическими или эукариотическими, но сложность ФСК может сделать предпочтительной систему экспрессии млекопитающих. Экспрессия легко осуществляется при трансформации прокариотических или эукариотических клеток подходящим вектором ФСК. Последовательность ДНК, полученная по описанной выше процедуре, может быть экспрессирована. непосредственно в клетках млекопитающих под контролем подходящего промотора. Гетерологические промоторы, хорошо известные специалистам в данной области, могут быть использованы. Для экспрессии ФСК в прокариотических или дрожжевых клетках должна быть удалена лидерная последовательность /или секреторная последовательность/. Положение кодона для N-терминала зрелого ФСК белка показано на фиг. 1. Это может быть сделано с использованием стандартных методик, известных специалистам в данной области. Как только получают целевой ФСК/кДНК клон, используют известные и подходящие средства для экспрессии ФСК белка, а именно, вставку в подходящий вектор и трансфекцию вектора в подходящую клетку-хозяин, отбор трансформированных клеток и культивирование этих трансформантов для экспрессии ФСК активности. Подходящими клетками-хозяевами являются бактерии, например, E.coli, дрожжи, клетки млекопитающих, например CHO, и насекомых. Полученный таким образом ФСК белок может иметь метиониновую группу у N-терминала белка /здесь называемого Met-ФСК/. Зрелый белок, полученный из прокариотических или эукариотических клеток, иначе, должен быть идентичным по аминокислотной последовательности, но эукариотический продукт может быть гликозилированным в той же самой степени или в другой, чем природный продукт. Различные методы получения ФСК-белка в соответствии с соглашением показаны в приведенных ниже примерах. Другие способы или материалы, например, векторы, будут легко оценены специалистами в данной области на основе примеров и последующего описания.
ФСК-белок, экспрессированный в соответствующих прокариотных или эукариотных клетках, может быть извлечен с помощью методик очистки и разделения, известных специалистам в данной области. Однако, как указано, настоящее изобретение также обеспечивает способ очистки, пригодный для ФСК белка как из рекомбинантного, так и природного источников, с помощью которого ФСК-белок может быть получен с высокой степенью чистоты и активности.
Настоящее изобретение разрешает проблемы известного уровня техники и обеспечивает способ очистки белка, обладающего ФСК-активностью. ФСК-белок в соответствии с настоящим изобретением обладает удельной активностью по крайней мере 1•107 единиц/мг белка, предпочтительно по крайней мере 2•107 единиц/мг белка и более предпочтительно по крайней мере примерно 4•107 единиц/мг белка при пробе с человеческим костным мозгом.
В соответствии с настоящим изобретением способ очистки ФСК-белка состоит из: осаждения белка сульфатом аммония при 80% насыщении для образования шарика, содержащего ФСК-белок; повторного суспендирования шарика в буферном растворе при pH в интервале от примерно 6 до примерно 8; нанесения буферного раствора, содержащего ФСК, на хроматографическую колонку, элюирования буферным раствором, содержащим хлористый натрий, и сбора фракций, обладающих ФСК активностью; объединения активных фракций, нанесения их на колонку с C4 обратимой фазой и элюирования 0 - 50% градиентом ацетонитрила для сбора активной фракции.
Рис. 5 иллюстрирует СДС-ПАГЭ-анализ очищенного ФСК-белка.
ФСК-белок, очищаемый в соответствии со способом изобретения, может происходить из любого природного источника, описанного выше в качестве исходного источника для рекомбинантного способа ДНК, например, Mo клеточной линии или UCD MLA-144 гиббоновой клеточной линии.
Альтернативно ФСК-белок может быть получен с использованием методик рекомбинантной ДНК изобретения.
ФСК из любого источника может быть очищен по способу настоящего изобретения. Кондиционированную среду из любого источника ФСК белка предпочтительно концентрируют ультрафильтрацией до концентрации белка по крайней мере около 0,1 мг белка/мл. Затем белок осаждают при добавлении сульфата аммония до 80% насыщения. Полученный шарик повторно суспендируют в водном растворе, забуферированном при pH в интервале от примерно 6 до примерно 8. Примерами подходящих буферов являются Трис-HCl, HEPES, цитрат натрия и т.п.
Буферный раствор фракционируют хроматографией на колонке. Подходящими материалами для использования при колоночной хроматографии являются октилсефароза, DEAE-ультрогель, AcA44-ультрогель, AcA-54 ультрогель и т.п. Один или несколько из этих материалов могут быть использованы последовательно для получения более высокой чистоты.
Фракции от каждой колонки собирают и проверяют на ФСК активность. Активные фракции объединяют и разбавляют трифторуксусной кислотой (ТФУК), гептафтормасляной кислотой (ГФМК) или т.п. и наносят на колонку с C4 обратимой фазой. ФСК активность затем элюируют, используя 0-90% ацетонитрильный градиент в ТФУК или ГФМК, предпочтительно при концентрации от 0,10% или 0,15% (объем/объем), соответственно, в зависимости от того, какая кисло та была использована при нанесении объединенных фракций на колонку.
Фракции, имеющие ФСК активность, анализируют СДС-электрофорезом на полиакриламидном геле (13,5% гель, как описано Лэммли, wature 227, 6810/1970/. Дополнительные обработки с использованием указанных выше материалов для хроматографических колонок могут дополнительно очистить ФСК белок для гомогенности.
Очищенный ФСК белок, фракционированный на СДС-ПАГЗ, показывает гетерогенный ФСК белок, имеющий кажущуюся молекулярную массу в интервале от примерно 15000 до примерно 26000 дальтон. Такой кажущийся размер гетерогенности имеется благодаря экстенсивному гликозилированию белка и представляет собой обычную характеристику гликопротеинов. Фракционирование менее очищенных образцов из Mo клеток кондиционированной среды с помощью СДС-ПАГЭ /в невосстановительных условиях/ и проверка белка, элюированного из геля, показывает наличие второго белка, обладающего ФСК активностью, имеющего кажущуюся молекулярную массу от примерно 28000 до 30000.
ФСК активность связывается и элюируется из октилсефарозы, ДЕАЕ ультрогеля и колонки с C4 обратимой фазы. Примерно 60% ФСК активности связывается Кон-A сефарозой /40% протекает через/ и может быть элюировано альфаметилманнозидом.
Молекулярно-массовый анализ рекомбинантного ФСК гельфильтрацией при низком содержании соли показывает, что примерно 30% активности элюируется с определенной молекулярной массой около 19000, но 70% материала находится в качестве димера, элюируется в положении, соответствующем молекулярной массе примерно 38000. Если 1 м хлористого натрия включают в эту колонку, вся активность элюируется в виде широкого пика примерно при 19000.
Очищенный ФСК является стабильным в течение по крайней мере 16 часов при инкубировании при 4oC /pH 7,4/ в 4 М гуанидин гидрохлориде, в 10 мМ ЭДТА; 10 мМ 2-меркаптоэтанола; и в 30% (объем/объем) этаноле. ФСК активность также является стабильной в 0,1% трифторуксусной кислоте (ТФУК) /pH 2,0/ и 0,1% ТФУК плюс 25% (объем/объем) ацетонитрила.
Как указывалось ранее, ФСК белок в соответствии с настоящим изобретением используется при лечении миелосупрессии, такой как (симптоматическая) гранулоципения, например, вызываемая химиотерапевтическим лечением рака или его лечением при облучении. В дополнение к этому, ФСК белки изобретения, как указывалось, используются при лечении серьезной инфекции. Для такой цели обычно показана дозировка примерно 200-1000 мкг/пациента. ФСК-белок предпочтительно вводят пациенту внутривенно с подходящим фармакологическим носителем. Примерами таких носителей являются фармакологический физиологический раствор и человеческий сывороточный альбумин в физиологическом растворе.
Кроме того, ФСК белки изобретения обладают другими активностями и применениями. Например, было показано, что мышиные ФСК активируют нейтрофилы. Следовательно, следует ожидать, что приматные ФСК настоящего изобретения также будут активировать нейтрофилы. Поэтому физиологические функции ФСК могут быть разнообразными (?). В костном мозге этот лимфокин может стимулировать пролиферацию и дифференциацию эффекторных клеток для защиты хозяина, тогда как в периферии могут быть активированы новые и существующие клетки. В локализованном иммунологическом ответе ФСК может сохранять циркулирующие нейтрофилы внутри или вне площадей воспаления. Несоответствующая локализация и/или активация нейтрофилов может быть включена в патофизиологию различных иммуно-медиированных болезней, таких как равматоидный артрит.
Изобретение будет более понятно при ссылке на следующие иллюстративные варианты, которые являются чисто примерными и не должны рассматриваться как ограничивающие область настоящего изобретения, описанную в формуле изобретения.
В примерах, если нет других указаний, температура дана в oC.
Рестрикционные эндонуклеазы используются в таких условиях и по методике, рекомендуемой их коммерческими поставщиками. Реакции связывания проводят, как описано Маниатисом и др., выше, на стр. 245-6, описание которых приведено здесь в качестве уровня техники, используется буферный раствор, описанный на стр. 246, и концентрация ДНК 1-100 мкг/мл при температуре 23oC для ДНК с тупыми концами и 16oC для ДНК с липкими концами. Проводят электрофорез в 0,5 - 1,5% агалозных гелях, содержащих 90 мМ Трис-бората, 10 мМ ЭДТА. Всю радиомеченную ДНК метят 32p, какая бы методика метки не использовалась.
"Быстрый преп" означает быстрое, маломасштабное продуцирование бактериофага или плазмиды ДНК, например, как описано Маниатисом и др., выше. стр. 365-373.
Пример A (I).
Стадия 1. Культивирование Mo-клеточной линии.
Mo-клетки /ATCC CRZ 8066/ выращивают традиционным образом на Альфа /6% CO2/ среде или на среде Искова /10% CO2/, содержащей 20% сыворотки зародыша теленка /СЗТ/, 2 мМ глютамина, 100 U/мл стрептомицина и 100 мкг/мл пенициллина. Клетки должны быть субкультивированы каждые 4-5 дней. Клетки подсчитывают и высевают в колбы Фалькона T-175 в 100-150 мл среды при плотности 3-4•105 клеток /мл. Клетки должны удваиваться в 20% СЗТ каждые 4-7 дней. Скорость роста не является постоянной и клетки могут иногда казаться остановившимися в росте, затем проходят через вспышки роста. Mo клетки могут быть выращены на среде, не содержащей сыворотки. Выживание намного лучше, когда клетки не промывают при переносе из СЗТ на среду, не содержащую сыворотки. Оптимальная плотность на среде, не содержащей сыворотки /СНС/ составляет 5•105 клеток/мл. Клетки будут расти медленно /или по крайней мере сохранять постоянное число/ в течение 3 дней в среде, не содержащей сыворотки, а затем должны быть подпитаны 20% СЗТ в течение по крайней мере 4 дней. Рост по такому графику /3 дня СНС, 4 дня 20% СЗТ/ может быть повторен еженедельно, если требуется СНС среда, без какого-либо ущерба для клеток в течение нескольких месяцев.
Стадия 2. Проба на ФСК-активность.
A. Проба с костным мозгом
Получают свободный костный мозг. Отделяют спикулы вытягиванием через иглу 20, 22, а затем 25 калибра. Разбавляют 1:1 стерильным забуферированным фосфатом физиологическим раствором /ФБР/ /комнатная температура/ и наслаивают Фиколл-Пак /примерно 30 мл ВМ-ФБР на 6 мл Фиколла/. Перемешивают при 1500 об/мин в течение 30 минут при комнатной температуре. Удаляют жир и ФБР слой и отбрасывают. Отбирают пипеткой слой малой плотности. Промывают 2 раза ФБР и считают. Располагают клетки на пластине в RPMI /получен от ГИБКО как PPMI 1640/ плюс 10% HTFCS /инактивированная теплом СЗТ/ в течение 3 часов для удаления приклеившихся клеток.
Среда для пластины /готовится свежая/:
20% СЗТ
0,3% агара, растворенного в воде, охлажденного до 40o
2x Искова /1:1 объем/объем с агаром/
1% P/S конечная концентрация 100 U/мл стрептомицина, 100 мкг/мл пенициллина
10-4 M альфа-тиоглицерина в 2x Искова из 10-2 M исходного Агар, охлажденный до 40o. Смесь с другими ингредиентами Охлаждение на водяной бане до 37-38o и хранение при этой температуре.
Через 3 часа отбирают пипеткой неприклеившиеся клетки. Перемешивают и подсчитывают. Добавляют 2.10 клеток/мл посевной среды и хранят при контролируемой температуре водяной бани 37-38oC. Прибавляют образцы /например, среды от трансфецированных клеток, обычно 10 мкл образца/ в первый ряд углублений пластины микротитратора в двойной повторности. Прибавляют 100 мкл суспензии клеток в каждое углубление. Прибавляют дополнительные 50 мкл суспензии клеток в каждое углубление в первом ряду. Тщательно смешивают и переносят 50 мкл раствора из первого ряда в следующий ряд и т.д. и продолжают разбавления 1:3 поперек пластины. Обертывают пластину парафильмом. Инкубируют 10-14 дней при 10% CO2, 37oC в полностью влажной атмосфере и подсчитывают колонии.
Для подсчета колоний считают общее число колоний, которое выросло в каждом углублении. В каждой пробе несколько углублений засевают без включения образца /холостой/ для получения основы для отсчета колоний. Среднее число колоний, которые выросли в контрольных углублениях, вычитают из числа колоний, найденных в каждом углублении, содержащем образцы. Одна единица СЗТ представляет собой количество, которое будет стимулировать образование одной колонии больше контрольного уровня на 105 клеток человеческого костного мозга /засеивается 105 клеток/мл/, когда концентрация СЗТ является суб-насыщенной. Суб-насыщенная концентрация определяется разбавлением и сравнением числа колоний при различных разбавлениях для нахождения концентрации чуть ниже уровня насыщения.
Для этой пробы подсчитывают колонии, содержащие гранулоциты, моноциты или оба типа клеток. Типы клеток в колониях определяются отбором колоний и окрашиванием индивидуальных клеток.
B. Проба с KG-1 клетками
KG-1 клетки /Blod, 56, N 3 /1980// выращивают в среде Искова + 10% СЗТ, переносят 2 раза в неделю и высевают каждый пассаж 2•105 клеток/мл. Клетки используют для пробы только между пассажем 30-35. Проба является такой же, как описанная выше для костного мозга, с тем исключением, что KGI клетки высевают в агаровую смесь при 4•103 клеток/мл.
Число колоний, выросших в каждом углублении, определяют и вычитают контрольный счет холостого опыта, как и в описанном выше опыте с костным мозгом. Одна KG-1 СЗТ единица/мл означает, такую концентрацию СЗТ, которая будет стимулировать половину максимального числа /насыщение/ KG-1 колоний для роста. Максимальное число получают при включении уровня насыщения СЗТ в нескольких углублениях.
Стадия 3. Конструирование вектора p91023/B/.
Вектор трансформации представляет собой pAdD26SUpA /3/, описанную Кауфманом и др., Mol. Cell Biol. 2 /11/: 1304-1319 /1982/. Он имеет структуру, представленную на фиг. 2. Короче, эта плазмида содержит мышиный ген кДНК дигидрофолат редуктазы /ДГФР/, который является основным последним промотором аденовируса 2 /Ad2/ при транскрипционном контроле. 5' сайт сращивания включен в ДНК аденовируса, а 3' сайт сращивания, происходящий из гена иммуноглобулина, находится между Ad2 основным последним промотором и последовательностью, кодирующей ДГФР. SV40 ранний сайт полиаденилирования находится вниз от последовательности, кодирующей ДГФР. Секция прокариотного происхождения pAd26SVpA /3/ взята из /Mellon P., Parker V., Gluzman J. and Maniatis T., 1981, Cell 27: 279-288/ и не содержит pBP322 последовательностей, известных для ингибирования репликации в клетках млекопитающих /Lusky M. and Botchan M., 1981, Mature (London) 293: 79-81/.
pAdD26SUpA /3/ превращают в плазмиду pCSV2, как показано на фиг. 2. pAdD26SVpA /3/ превращают в плазмиду pAdD26SVpA /3/ путем делении одного или двух Pst сайтов в pAdD26SVpA /3/. Это осуществляется при частичном переваривании PstI /используя недостаточность ферментной активности, чтобы таким образом могла быть получена субпопуляция линеаризированных плазмид, в которых отщеплен только один Pst сайт/, затем проводят обработку по Клейноу, связывание для рециркуляризации плазмиды, трансформацию E. coli и скринирование для делении P I сайта, локализованного у 3'SV40 последовательности полиаденилирования.
Трехчастный лидер аденовируса и гены ассоциированных вирусов /VA гены/ вставляют в pAdG26SVpA /3/ /d/, как показано на фиг. 2. Сначала pAdD26SVpA /3/ /d/ расщепляют PVUII, чтобы сделать линейную молекулу открытой внутри 3' участка первого из трех элементов, составляющих трехчастный лидер. Затем PJAW 43 /Zain et al. 1979, Cell, 16, 851/ переваривают Xho I, обрабатывают по Клейноу, переваривают P II и изолируют фрагмент 140 пар оснований, содержащий второй и часть третьего лидеров, с помощью электрофореза на полиакриламидном геле /6% в Трис-боратном буфере; Маниатис и др. /1982/ выше/. Фрагмент 140 пар оснований затем связывают с PVUII переваренной pAdD26SVpA /3/ /d/. Продукт связывания используют для трансформации E. coli для резистентности к тетрациклину и скринируют колонии, используя процедуру Грюнщтейна-Хогнесса с примерением 32P-меченного зонда гибридизации для фрагиента 140 пар оснований. Получают ДНК из положительно гибридизованных колоний, чтобы проверить, находится ли реконструированный PVUII сайт в 5'-или в 3'-концах вставленной определенной ДНК 140 пар оснований во 2-м или 3-м лидерах последних аденовируса. При правильной ориентации PVUII сайт находится на 5'-стороне вставки 140 пар оснований. Эту плазмиду обозначают pTPL на фиг. 2.
AVaII D фрагмент SV 46, содержащий SV40 усиливающую последовательность, получают при переваривании SV40 ДНК ферментом AVaII, затуплении концов фрагментом Клейноу Pol I, связывании Xho I линкеров с фрагментами, переваривании Xho I для открытия Xho I сайта и изоляции четвертого самого большого /D/ фрагмента гельэлектрофорезом. Затем этот фрагмент связывают с разрезанной Xho I pTPL, получая плазмиду pCVSVL2-TPL. Ориентация SV40 D фрагмента в pCVSVL2-TPL будет такой, что SV40 последний промотор находится в той же ориентации, как основной последний промотор аденовируса.
Для введения генов ассоциированного вируса /VA/ аденовируса в pCVSVL2-TPL сначала конструируют плазмиду pBR322, которая содержит фрагмент аденовируса типа 2 Hind III B. ДНК аденовируса типа 2 переваривают Hind III и изолируют фрагмент В после гельэлектрофореза. Затем этот фрагмент вставляют в pBR322, которую заранее переварили Hind III. После трансформации E. coli для резистенции к ампициллину скринируют рекомбинаты для вставки фрагмента Hind III и определяют ориентацию вставки при переваривании рестракционным ферментом. pB322 - AdHind III B содержит фрагмент Hind III B аденовируса типа 2 в ориентации, представленной на фиг. 3.
Как показано на фиг. 3, VA гены обычно получают из плазмиды pBR322-Ad Hind III B при переваривании HpaI, добавлении EcoRI линкеров и переваривании EcoRI и извлечении фрагмента 1,4 кв. Фрагмент, имеющий EcoRI липкие концы, затем связывают по EcoRI сайту pTRL /которая была ранее переварена EcoRI/. После трансформации E. coli HBIOI и отбора на резистентность к тетрациклину, колонии скринируют путем гибридизации на фильтре с специфическим зондом ДНК для VA генов. ДНК получают из положительно гибридизированных клонов и характеризуют перевариванием рестрикционными эндонуклеазами. Полученную плазмиду обозначают p91023.
Удаляют оба EcoRI сайта в p91023. p91023 разрезают полностью EcoRI, генерируют два фрагмента ДНК, один примерно 7 кв, а другой - пример 1,3 кв, содержащие VA гены. Концы обоих фрагментов являются заполненными при использовании фрагмента Клейноу PolI, а затем оба фрагмента, а именно 1,3 кв и 7 кв связывают вместе. Плазмиду p91023 /A/, содержащую VA гены, и подобную p91023, но делецированную на 2 сайта EcoRI, идентифицируют с помощью скрининга Грунштейна - Хогнесса с фрагментом VA гена и с помощью традиционного анализа сайтов рестрикции.
Затем удаляют единственный сайт PstI в p91023 /A/ и заменяют сайтом EcoRI. p91023 /A/ разрезают для завершения PstI, а затем обрабатывают фрагментом Клейноу PolI для генерации полных концов. EcoRI линкеры связывают с затупленным PstI сайтом p91023 /A/. Линейную p91023 /A/ с EcoRI линкерами, присоединенными к тупому PstI сайту, отделяют от неприсоединенных линкеров и переваривают для завершения EcoRI, а затем повторно связывают. Извлекают плазмиду p91023 /B/ и идентифицируют, чтобы иметь структуру, подобную p91023 /A/, но с EcoRI сайтом, расположенным на месте предыдущего PstI сайта.
Стадия 4. Получение кДНК банка.
Mo клетки индуцируют в течение 16-20 часов с помощью РНА и РМА для усиления продуцирования ими лимфокина. Эти клетки высевают при 5•105 клеток/мл в среду Искова с 20% СЗТ,0,3% /объем/объем/ РНСА и 5 нг/мл ТРА. Клетки собирают центрифугированием. Шарик клеток снова суспендируют в 20 мл охлажденного на льду гипотонического буфера /RSB буфер: 0,01 М Трис-HCl-, pH 7,4, 0,01 М KCl, 0,0015 М MgCl2, 1 мкг/мл циклогексимида, 50 единиц/мл РНК-син и 5 мМ дитиотрейнола/. Клеткам дают набухнуть на льду в течение 5 минут, затем механически разрывают 10 ударами плотной гарнитуры стеклянного гомогенизатора. Гомогенат цинтрифугируют при низкой скорости /2000 об/мин в центрифуге Бекман J6/ для удаления ядер и нелизированных клеток. Надосадочный слой хранят на льду до тех пор, пока шарик из ядер не суспендируют повторно в 10 мл BSB и снова не отцентрифугируют с низкой скоростью. Этот второй надосадочный слой объединяют с первым и центрифугируют объединенные надосадочные слои с низкой скоростью для удаления остаточного загрязнения ядрами и нелизированными клетками. Надосадочный слой из этой операции доводят до 0,15 М KCl добавлением 2М KCl, затем цинтрифугируют с высокой скоростью /25000 об/мин, Бекман SW ротор в течение 30 минут/, чтобы получить шарик из мембран. Мембранный шарик тщательно промывают холодным RSB, затем повторно суспендируют в 12 мл RSB, содержащем 2 М сахарозы и 0,15 М KCl. Готовят два прерывистых градиента в центрифужных трубках Бекман SW41 путем наслаивания 6 мл мембранного раствора в 2 М сахарозы на 2 мл RSB с 2,5 М сахарозы и 0,15 М KCl. Трубки заполняют доверху путем наслаивания сверху 2,5 мл PSB, содержащих 1,3 М сахарозы и 0,15 М KCl. Эти градиенты перемешивают в течение 4 часов при 27000 об/мин /Бекман, ротор SW 41/ при 4oC. Мембранный слой /при границе фаз между 2,0 М и 1,3 М сахарозы/ тщательно удаляют сбоку, используя иглу 18 калибра и шприц. Объединяют мембранные фракции из двух градиентов и разбавляют 1 объемом дистиллированной воды, затем смешивают с 0,5% Тритона X-100 и 0: 5% деоксихолата натрия, затем экстрагируют равным объемом фенола. Водный слой повторно экстрагируют смесью 1:1 фенола и хлороформа и, наконец, равным объемом хлороформа. Наконец, осаждают соединенную с мембраной РНК добавлением хлористого натрия до 0,25 М и 2,5 объемов холодного этанола и инкубируют всю ночь при -20oC. Осажденную РНК собирают центрифугированием /4000 об/мин в течение 10 минут в центрифуге Бекман J-6/ и повторно суспендируют в 1 мл дистиллированной воды. Из 2•109 клеток получают приблизительно 1 мг РНК. Матричную РНК /мРНК/ изолируют из всей РНК хроматографией на колонке с 0,5 мл олиго-dT-целлюлозой. Кратко, РНК нагревают в течение 5 минут, быстро охлаждают на льду, затем разбавляют в 5 раз при комнатной температуре связывающим буфером /0,5 MLiCI 0,01 М Трис-HCl, pH 7,4, 0,002 М ЭДТА, и 0,1% СДС/. РНК в связывающем буфере переносят на колонку в олиго-dT-целлюлозой, уравновешенную связывающим буфером, при комнатной температуре. Колонку промывают 5 мл связывающего буфера, затем 5 мкл 0,15 MLiCI Cl, 0,01 М Трис-HCl, pH 7,4, 0,002 М ЭДТА и 0,1% СДС. Наконец, элюируют мРНК 2 мл 0,01 М Трис-HCI, pH 7,4, 0,002 М ЭДТА и 0,1% СДС мРНК осаждают добавлением хлористого натрия до 0,25 М и 2,5 объемов этанола и инкубируют всю ночь при - 20oC. Осажденную мРНК собирают центрифугированием /30000 об/мин в течение 30 минут в роторе SW55 Векмана/. Трубку тщательно сливают и шарик мРНК повторно суспендируют в 50 мл воды. Повторно суспендированную мРНК доводят до 0,25 М NaCl; затем экстрагируют 1 раз смесью 1:1 фенола и хлороформа: затем 3 раза хлороформом. Осаждают мРНК добавлением 2,5 объемом этанола. Смесь замораживают и оттаивают несколько раз на бане сухой лед/этанол, затем центрифугируют 15 минут в центрифуге Эппендорфа. Трубку тщательно сливают и шарик мРНК повторно суспендируют в 20 мкл дистиллированной воды. Конечный выход составляет примерно 30 мкг мРНК.
Готовят первую нить кДНК, используя стандартные методики. Кратко, 10 мкг мембранной мРНК разбавляют в 100 мкл реакционной смеси синтеза кДНК, содержащей 300 мМ Трис, pH 8,4, 140 мМ KCl, 10 мМ MgCl2, 10 мМ β- меркаптоэтанола, 500 мМ каждой из dATF, dGTP, dCTP и dTTP, 5 мкг олиго-dT-/фосфорилированного и со средним размером 12-18/ в качестве праймера, 150 μ Ku32 dCTP /400 Ku/ммоль/ и 20 единиц ингибитора рибонуклеазы РНК-син. Реакцию инициируют добавлением 100 единиц обратной транскриптазы и инкубируют 30 минут при 42oC. Реакцию останавливают добавлением ЭДТА до 40 мМ и разлагают РНК инкубированием в течение 20 минут при 65oC в 0,2 М NaOH. Основание нейтрализуют добавлением 20 мкл Трис, pH 7,4. Реакционную смесь затем экcтpaгиpуют фенолом/хлороформом, снова экстрагируют 50 мкл 10 мМ Трис, pH 7,5 1 мМ ЭДТА /TE/ и объединяют водные фазы. Однониточную кДНК превращают в двуниточную инкубированием в течение 12 часов при 16oC с 40 единицами фрагмента Клейноу ДНК полимеразы 1 в 100 мкл реакционной смеси, содержащей 50 мМ фосфата калия, pH 7,4, 2,3 мМ ДТТ, 2-меркаптоэтанол, 10 мМ MgCl2, 150 μ Молей каждой из четырех деоксинуклеотидтрифосфатов и 25 μ Ku32P dCTP. Реакцию прекращают экстракцией фенолом/хлороформом и удаляют невошедшие трифосфаты пропусканием водной фазы через колонку с 1 мл сефадексом G-50. Выведенные фракции объединяют и осаждают этанолем.
Шарик кДНК промывают холодным этанолом, затем повторно суспендируют в 200 мкл 20 мМ Трис, pH 8,0, 1 мМ ЭДТА 80 μ Молярном 5-аденозил-метионине и 300 единицах EcoRI метилазы в течение 60 минут при 37oC. Реакцию останавливают экстрацией фенолом/хлороформом и собирают метилированную кДНК осаждением этанолом.
Шарик кДНК прорывают 70% этанола, затем повторно суспендируют в 200 мкл Sl буфера/Маниатис и др. / и инкубируют с 200 единицами Sl - нуклеазы при 30oC в течение 30 минут. Реакцию останавливают экстрацией фенолом/хлороформом и собирают кДНК осаждением этанолом.
Двуниточную кДНК притупляют инкубированием в 100 мкл 20 мМ Трис, pH 7,4 50 мМ NaCl, 10 мМ 2-меркаптоэтанола и 500 μ Молярных всех четырех деоксинуклеотидтрифосфатов с 25 единицами Клейноу при комнатной температуре в течение 30 минут. Реакцию останавливают экстракцией фенолом/хлороформом и собирают кДНК осаждением этанолом.
Связывают нДНК в 50 млк T4 лигазного буфера /Маниатис и др./ с 500 p Молей RI линкеров, полученных от Нью Инглэнд Биолабс /последовательность: pCGGAATTCCG/, используя 2000 единиц T4 лигазы в течение ночи при 16oC. Реакцию останавливают инкулированием при 70 в течение 20 минут, затем разбавляют до 300 мкл так, чтобы конечная концентрация соли составляла 0,1 М NaCl, 10 мМ MgCl2, 50 мМ Трис-Cl, pH 7,4. Затем кДНК переваривают 2 минуты при 37oC 700 единицами KcoRI. Реакцию останавливают экстракцией фенолом/хлороформом и собирают кДНК осаждением этанолом. Шарик повторно суспендируют в 50 мкл TE и пропускают через колонку 5 мл Cl-4B. Выведенные фракции собирают, объединяют и осаждают этанолом. Осажденную кДНК подвергают электрофорезу через 1% агарозный гель в Трис-ацетатном буфере в присутствии 1 мкг/мл этидинийбромида. Изолируют из гелия кДНК с размером в интервале 500-4000 пар оснований, используя стандартную методику со стеклянным порошком. Элюированную кДНК экстрагируют фенолом/ хлороформом, осаждают этанолом и шарик /после промывки этанолом/ повторно суспендируют в 60 мкл TE. Конечный выход составляет 100-500 нг кДНК.
Получение вектора экспрессии p91023/B/ описано выше. Связывают переваренный EcoRI и обработанный фосфатазой вектор /500 нг/ со 100 нг кДНК в 100 мкл реакционной смеси /стандартная T4 лигазная реакционная смесь/ в течение ночи при 16oC. Реакцию останавливают экстракцией фенолом/хлороформом, затем связанную кДНК собирают осаждением этанолом после добавления 5 мкг т-РНК в качестве носителя.
Осажденную этанолом ДНК промывают 70% этанола, затем повторно суспендируют в 100 мкл TE. Эту ДНК используют в 4 мкл аликвотов для трансформации E. coli MC 1061/4 мкл в 100 мкл трансформационной среды/. Каждую из 25 стансформаций переносят в 150 мм чашки Петри с 1% агара, L-бульоном и 10 мкг/мл тетрациклина /Tet-пластины/ и инкубируют всю ночь при 37oC. На каждой пластине вырастает приблизительно 2000 колоний, в результате получают около 50 000 колоний. После достижения примерно 0,5 мм в диаметре колонии переносят на нитроцеллюлозные диски /137 мм/, осторожно размещая сухой фильтр на поверхности пластины, затем мягко отщепляют фильтр. Все колонии на пластине переносят на фильтр, который затем помещают /колонии сбоку / Sideup/ на свежую Tet-пластину. После выращивания колоний в течение нескольких часов готовят реплику каждого из фильтров, помещая свежий влажный фильтр точно на первоначальный фильтр, прижимая их друг к другу, отщепляя их, затем возвращая каждый фильтр на свежую Tet-пластину и инкубируя пластины всю ночь при 37oC. Каждую реплику тщательно маркируют, чтобы ее можно было сравнить с оригинальным фильтром.
Стадия 5. Приготовление пула плазмид ДНК.
Каждый из 25 фильтров-реплик осторожно разрезают на восемь частей, используя скальпель и отмечая ориентацию каждой восьмой части относительно оригинального фильтра. Соскабливают колонии с каждой секции в 10 мл L-бульона. Бактерии собирают центрифурированием /3000 об/мин, 10 минут, центрифуга Бекман J-6/, повторно суспендируют в 0,6 мл 25% сахарозы, 50 М Трис-HCl, pH 8,0, и превращают в протопласты добавлением 0,12 мл 5 мг/мл лизоцима и инкубируют на льду в течение 5-10 минут. Протопласты снова инкубируют при комнатной температуре 10 минут, затем добавляют 0,125 мл 0,5 М ЭДТА, затем лизируют при добавлении 0,12 мл 10% СДС в 50 мМ Трис-HCl, pH 8,0. Лизат осторожно смешивают, инкубируют при комнатной температуре 15 минут, затем осаждают белок и хромосомальную ДНК добавлением 0,3 мл 5 М NaCl. После инкубирования на льду в течение 15 минут лизат центрифугуют на центрифуге эппендорфа в течение 30 минут на холоду. Осторожно удаляют недосадочный слой, оставляя внизу вязкий шарик ДНК/белок и разбавляют, добавляя 2,5 мл воды. Смесь экстрагируют 1 мл фенола, разделяют слои центрифугированием /IOK в течение 10 минут в роторе Серволл SS-34/ и удаляют водный слой в свежую трубку. Осаждают ДНК добавлением 0,5 мл 5 М NaCl и 7,5 мл холодного этанола, замораживают смесь несколько раз на бане сухой лед/ этанол. Осадок собирают центрифугированием /IOK, 15 минут в Сорволл SS-34/, повторно суспендируют в 0,3 мл 0,3 М ацетата натрия и снова осаждают /в трубке Эппендорфа/ добавлением 1 мл этанола. После 10-15 минут на бане сухой лед-этанол собирают осажденную ДНК центрифугированием/ 5 минут в центрифуге Эппендорфа/ и готовый шарик снова суспендируют в 100 мкл стерильного TE/10 мМ Трис, pH 8,0, 1 мМ ЭДТА/. Из типичной операции получают 5-10 мкг плазмиды ДНК. Каждое приготовление содержит ДНК из 200-500 колоний на первоначальном фильтре. Всего приготовлено 200 образцов ДНК из 25 фильтров.
Стадия 6. Изолирование ФСК клона.
Каждым из образцов ДНК со стадии 5 отдельно стансфецируют M6 COS клетки обезьяны, как описано ниже.
M6 клетки выращивают рутинно в среде Игла, модифицированной Дальбекко "ДМЕ, доступная из Джибко/, содержащей 10% инактивированной теплом сыворотки зародыша теленка (HIFCS), разделяют дважды в неделю при разбавлении 1:6. Через 24 часа после разделения M6 клетки готовы для трансфекции. За 24 часа до трансфекции высевают 1,2•108 M6 клеток /деление 1:6/ в Клеточный Фактор / доступный от Нунк/ в 1,5 л ДМЕ + 10% HIFCS. Непосредственно перед трансфекцией пластины отсасывают и дважды промывают 7 мл не содержащей сыворотки ДМЕ. ДНК растворяют в 0,1 М Трис /pH 7,3/ и прибавляют в ДМЕ среде, содержащей 2 мМ глютамина, 100 мкг/мл стрептомицина, 100 U/мл пенициллина и 0,25 мг/мл ДЕАЕ Декстрана, доводя до 4 мл раствором Трис-ДНК. Прибавляют 4 мл среды, содержащей растворенную ДНК, на пластину, содержащую M6 COS клетки, и инкубируют в течение 12 часов.
После инкубации клетки промывают один или два раза 7 мл SFDME. Затем прибавляют 5 мл ДМЕ с 10% HIFCS, 100 U/мл пенициллина, 100 мкг/мл стрептомицина, 2 мМ глютамина и 0,1 мМ хлорокина и инкубируют клетки 2,5 часа.
Через 2,5 часа промывают один раз SF ДМЕ и прибавляют 10 мл ДМЕ + 10% HIFCS /пластину. Через 30 часов отсасывают среду и подают 4 мл/пластину ДМЕ + 10% HIFCS. Собирают урожай, удаляя кондиционированную среду после 24-26 часов дополнительной инкубации.
Кондиционированную среду после каждой трансфекции проверяют на ФСК активность, используя KG-I пробу. Для каждого образца, положительного на ФСК активность, должен быть идентифицирован клон на первоначальном основном фильтре, ответственный за ФСК активность. Например, для одной трансфекции, положительной на ФСК активность, пересаживают все колонии с секции первоначального основного фильтра, с которого происходит образец трансфекции ДНК. Некоторые из этих 320 колоний пересаживают в 3 мл L-бульона плюс 10 мкг/мл тетрациклина. Культуры выращивают в течение ночи. 320 колоний помещают на матрицу 18 х 18. Готовят пулы из каждого горизонтального ряда и вертикальной колонки матрицы/ всего 36 пулов/ /примечание: последний горизонтальный ряд имеет только 14 клонов/. Готовят образцы ДНК из каждой объединенной в пул культуры, затем используют для трансфекции COS-клеток. Проверяют надосадочные слои этих трансфекции, используя пробу KG-1 колонии. Из этой группы трансфекции получают два положительных: один - в вертикальной колонке, другой - в горизонтальном ряду. Общая культура этих пулов содержит ФСК-клон.
Изолируют 12 индивидуальных клонов из этой культуры и готовят минипрер ДНК из 10 мл культуры в L-бульоне, как описано выше. Образцы 10 мкг ДНК из этих приготовлений переваривают EcoRI и анализируют полученные в результате фрагменты ДНК с помощью электрофореза на агарозном геле. Девять из двенадцати клонов имеют общую вставку приблизительно 750 пар оснований. ДНК из четырех из этих клонов и остальные три клона вводят в M6 COS клетки, как описано выше. Надосадочные слои от этих трансфекций проверяют, используя KG-1 пробу, а также пробу на ФСК с костным мозгом. Четыре клона, каждый из которых содержит фрагмент 750 пар оснований, все направляют экспрессию M6 COS клеток с высоким уровнем ФСК активности, как определено в любой пробе, тогда как другие три клона нет. Следовательно, кодирующая область для ФСК должна быть локализована внутри вставки 750 пар оснований.
Последовательность ДНК, кодирующая ФСК, была удалена из вектора трансформации в положительном клоне путем переваривания EcoRI и была определена ее аминокислотная последовательность с использованием стандартных методов дидеоксисеквенсирования после субклонирования фрагментов в M13 векторы для получения последовательности, показанной на фиг.1. Плазмида, p91023/B/-ФСК, которая сначала показала направленную ФСК-экспрессию в COS клетках, была обозначена pCSF-1. Эта плазмида была депонирована в Коллекции культур американского типа в штамме E.coli -MC1061 под номером хранения ATCC 39754 2 июля 1984 года.
Стадия 7. Экспрессия ФСК-белка.
M6 COS клетки обезьяны, трансформированные вектором p91023/B/, содержащим ФСК/кДНК, как выделено на стадии 6, выращивают, как описано на стадии 6, для получения ФСК-белка в культуральной среде.
А именно, 1 мг этой ДНК /pC5F/ растворяют в 1 мл 0,1 М Трио pH 7,3 и прибавляют к 600 мл ДМЕ, содержащим 2 мМ глютамина, 100 11/мл стрептомицина, 100 мкг/мл пенициллина /P/S/ и 0,25 мг/мл ДЕАЕ Декстрана /молекулярная масса 500 000, получено из Фармациа/. 600 мл раствора ДНК ДЕАЕ Декстрана прибавляют к M6 COS клеткам в установку для культивирования клеток и инкубируют при 37oC в течение 12 часов. После инкубирования клетки промывают один раз 900 мл SF ДМЕ, затем инкубируют 2,5 часа с 600 мл ДМЕ, содержащими 0,1 мМ хлорокина, 10% HIFCS, 2 мМ глютамина и P/S. После отсасывания среды, содержащей хлорокин, клетки промывают SF ДМЕ и подают 1500 мл ДМЕ с 10% HIFCS. Через 30 часов клетки промывают SF ДМЕ, среду заменяют 800 мл SF ДМЕ и помещают трансфецированные клетки в условия среды при 37oC на 24 часа. Отработанную кондиционированную среду отсасывают и заменяют другими 800 мл SF ДМЕ. Клетки оставляют на 24 часа в этой среде, затем собирают отработанную среду. По возможности быстро после сбора концентрируют образец отработанной среды в 20 раз ультрафильтрацией под давлением, используя камеру Амикон на 2,5 л с YM5 мембраной/ 5000 MW отрезок/.
Стадия 8. Очистка рекомбинантного ФСК.
200 мл концентрированной отработанной среды /из 4 л исходного материала - стадия 7/ доводят до 30% насыщения сульфатом аммония при добавлении твердого сульфата аммония и удаляют осажденный белок центрифугированием. Надосадочный слой доводят до 80% насыщения сульфатом аммония добавлением более твердого сульфата аммония и осажденный белок собирают центрифугированием. Шарик повторно суспендируют в 5 мл 20 мМ цитрата натрия, pH 6,1, содержащем 1 М NaCl. Растворенный белок наносят на колонку 1,6 x 100 см Ультрогель AcA54, уравновешенную тем те самым буфером, ВСК активность, элюированная с колонки, имеет кажущийся молекулярный вес 19 к дальтон или после примерно 90 мл. Наблюдали, что если проводить гель-фильтрацию с низкой ионной силой, ФСК активность элюируют с колонки в двух положениях с кажущимися молекулярными массами примерно 19 к дальтон и 38 к дальтон, подтверждая, что GM-ФСК может легко образовать димеры/. Объединяют активные фракции и доводят до 0,15% ТФУК /добавлением 10% ТФУК/ и наносят на колонку Видак C4 /0,46 х 25 см/, уровновешенную 0,1% ТФА. Колонку проявляют при линейном градиенте 0-90% ацетонитрила /1 мл/мин, всего 340 мл/ в 0,1% ТФУК. ФСК-активность элюируется между 39% и 43% ацетонитрила /фракции 16-активность элюируется между 39% и 43% ацетонитрила/ /фракции 16-20/. Анализируют образец 20 мкл фракции 19 с помощью электрофореза на СДС-полиакриламидном геле/ 13,5% гель, как описано Леммли, Nature 227, 680 /1970//. Наблюдалась одна широкая полоса белка с кажущейся молекулярной массой 18-26 к дальтон. Более широкий размер полосы для ФСК является общим признаком гликопротеинов и утончается, отражая экстенсивное, но переменное добавление углевода. Белок из фракции 19 подвергают разложению на Эдману, используя газофазный микросеквенатор Апплайд Биосистемс. Из приблизительно 20 мкг нанесенного белка получают последовательность из первых 16 аминокислот /A-P-A-R-S-P-S-P-S-T-Q-P-W-E-H/. Высокий выход этой единственной белковой последовательности хорошо подтверждает, что ФСК-белок во фракции 19 был очищен до гомогенности. Биопроба показывает, что фракция 19 имеет 3•107 единиц на A280 единиц поглощения. Поскольку типичные белки в водном растворе дают коэффициенты экстинкции в интервале от 0,8 до 1,2 A280 единиц поглощения на миллиграмм белка, удельная активность очищенного ФСК находится между примерно 1•107 и примерно 4•107 единиц/мг при испытании с использованием пробы с человеческим костным мозгом.
Пример B (II). Клонирование ФСК гиббона
Стадия 1. Получение мРНК из T-клеток гиббона.
Образец линии T-клеток гиббона, обозначенной ИСД-MLA 144, культивируют в течение нескольких недель в RPMI 1640 /полученной от Гибко/ и 20% сыворотки зародыша теленка /СЗТ/ до тех пор, пока не будет получено 1•109 клеток всего. Клетки индуцируют для продуцирования высоких уровней ФСК путем активации в течение 24 часов в присутствии 10 нг/мл 12-O-тетрадеканоилфорбол-13-ацетата /ТФА/ в RPMI 1640 плюс 1% СЗТ. Собирают выращенные клетки центрифугированием / 1000 об/мин, 5 минут/, промывают один раз фосфатным буферным солевым раствором /ФБР/ и снова собирают центрифугированием.
Из этих клеток готовят связанную с мембраной полисомальную /MBP/ мРНК, используя ту же самую процедуру, что описана в примере A для получения РНК Mo клеток.
Стадия 2. Реакция однониточной кДНК.
Разбавляют 6 мгк MBP мРНК /из стадии 1/ в 50 мкл реакционной смеси дм синтеза кДНК /смотри пример A - стадия 4/ и инициируют реакцию добавлением обратной транскриптазы. После 30 минут инкубирования при 42oC реакцию останавливают добыванием ЭДТА до 50 мМ и разбавляют водой до 100 мкл. Смесь экстрагируют фенолом/хлороформом и снова экстрагируют хлороформом. Отделяют гибриды кДНК/РНК от непрореагировавших трифосфатов хроматографией на колонке с Сефарозой CL-4B. Выведенные фракции объединяют и собирают гибриды осаждением этанолом. Конечный выход составляет 570 нг.
Стадия 3. Реакция двуниточной кДНК.
Снова суспендируют шарик однониточной кДНК /стадия 2/ в 50 мл воды и проводят синтез второй нити в стандартной реакционной смеси с E.coli. Полимеразой I, E.coli лигазой и РНКазой H. Реакционную смесь инкубируют в течение ночи при 16oC и затем инкулируют 1 час при 37oC. Реакцию останавливают добавлением ЭДТА и экстрагируют фенолом/хлороформом. Отделяют кДНК от непрореагировавших трифосфатов хроматографией на колонке с Сефарозой CL-4B, выведенные фракции объединяют и собирают кДНК осаждением этанолом.
Стадия 4. Получение рекомбинантной кДНК.
Снова суспендируют шарик кДНК /стадия 3/ в 75 мкл воды. Гомополимерные C "хвосты" присоединяют к концам кДНК при добавлении 10 мкл раствора кДНК к 25 мкл стандартной реакционной смеси с концевой трансферазой и инкубируют при 30oC в течение 5 минут. Реакцию останавливают добавлением ЭДТА до 40 мМ и тепловой инактивацией при 68o в течение 10 минут. Закаливают 10 нг этой кДНК с хвостами с 50 нг G-хвостовой pBR322 /получена от HEH/ в 10 мкл 10 мМ Трис, pH 7,5, 1 мМ ЭДТА и 100 мМ NaCl. Закаленную реакционную смесь инкубируют в течение 10 минут при 68oC, а затем 2 часа при 57oC.
Стадия 5. Трансформация бактерий.
Выращивают E.coli штамм MC1061 в L-бульоне, охлаждают на льду, собирают центрифугированием и обрабатывают CACl2 для приготовления их для трансформации. Затем инкубируют 5 мкл зазаленной реакционной смеси кДНК с 200 мкл обработанных CACl2 бактерий. Проводят 50 таких трансформаций, используя всю закаленную кДНК, и наносят на пластины с 1% агаром L-бульоном, размером 15 см, содержащие 10 мкг/мл тетрациклина. На каждой пластине вырастает приблизительно 1000 колоний.
Стадия 6. Посев реплик.
Пересаживают 10 000 колоний из трансформации каждую с помощью зубочистки, переносят на свежие пластины /500 на пластину в решетке/ и выращивают всю ночь при 37oC. Затем колонии снимают с каждой пластины, прижимая сухой нитроцеллюлозный фильтр плотно к поверхности пластины. Для каждого из этих основных исходных фильтров готовят два фильтра-реплики. Основные исходные фильтры хранят при 4oC, а фильтры-реплики обрабатывают основанием и сушат, чтобы подготовить их к гибридизации.
Стадия 7. Приготовление 32P-меченых зондов гибридизации.
Изолируют вставку кДНК из pCSF-1 перевариванием рестрикционным ферментом EcoRI и электрофорезом на агарозном геле с Трис-ацетатом и этидинийбромидов. Полосу, содержащую фрагмент кДНК, вырезают из геля и очищают по методике со стеклянным порошком.
Затем прибавляют 300 нг фрагмента кДНК к 1 мкл 10 х T4 ДНК Полимеразного буфера /0,33 М Трис-ацетата, pH 7,9,0,66 М ацетата калия, 0,1 М ацетата магния и 10 мМ дитиотрейтола", и 3 единицам T4 ДНК Полимеразы "Нью Ингленд Биолабс" и разбавляют водой до 10 мкл. После инкулирования 5-10 минут при 37oC, эту смесь объединяют с 1 мкл 10 х T4 ДНК Полимеразного буфера; 1 мкл 2 мМ раствора каждого из dCTP, dTTP, dGTP, 10 мкл 32PdATP/10 μ Ku мкл 3000 Ku/ммоль" и 3 единицами Tr ДНК Полимеразы. Реакционную смесь инкубируют в течение 20 минут при 37oC. Затем прибавляют 1 мкл 2 мМ dATP и реакционную смесь инкубируют еще дополнительные 10 минут при 37oC.
Отделяют не включенные трифосфаты от меченной кДНК хроматографией на колонке с Сефадексом GIOO. Готовят второй зонд из синтетического олигонуклеотида, имеющего последовательность:
ATC TGG CTG CAC AG,
которая комплементарна аминоконцу области, кодирующей ФСК. Этот олигонуклетид мечен по 32P dATP на его 5'-конце с использованием реакции полинуклеотидкиназы.
Стадия 8. Изоляция клонов ФСК кДНК.
В стандартной процедуре скрининга гибридизацией гибридизуют некоторые 45 клонов с T4 меченной pCSF-1 кДНК. Из этих приблизительно 20 также гибридизуется с меченным олигонуклеотидным зондом. Кодирующую область одного из них секвенсировали и данные последовательности показывают число замещений основания, некоторые из которых являются результатом в различии аминокислот в экспрессированном белке. Эти различия представлены на фиг. 1 выше последовательности ДНК для гена человеческого ФСК, клонированного в примере A.
Пример C. Клонирование ФСК из мРНК лимфоцита периферического кровотока.
Стадия 1. Получение мРНК из лимфоцитов периферического кровотока.
Лимфоциты периферического кровотока были получены из четырех побочных продуктов плазмафореза "получены от Ред Кромм/ при фракционировании на градиенте Фиколл-Гипак. Малая плотность в RPMI 1640 в присутствии 5% сыворотки зародыша теленка, 0,17% фитогеммаглютинина и 10 нг/мл форбал миристат ацетата /РМА/ при плотности 2•106 клеток /мл/ всего получено 6•109 клеток/. Собирают клетки центрифугированием /1000 об/мин, 5 минут/, один раз промывают солевым фосфатным буфером /PBS/ и снова собирают центрифугированием. Готовят цитоплазматическую РНК при осторожном лизисе, при котором клетки снова суспендируют в 50 мл холодного Тритонового буфера для лизиса /140 мМ NaCl, 1,5 мМ MgCl2, 10 мМ Трис, pH 8,6, 0,5% Тритон X-100/ с 10 мМ дитиотрейтола /ДТТ/ и 50 единиц/мл РНКсин/ получена от Биотек/. Этот лизат делят на 2 равные части и каждую часть наслаивают на 10 мл подушки лизисного буфера, содержащего 20% сахарозы. Удаляют ядра клеток центрифугированием на холоду /4oC, 400 об/мин в течение 5 минут/. Осторожно удаляют верхний слой /цитоплазматический экстракт/ и прибавляют додецилсульфат натрия /СДС/ до конечной концентрации 1%. Этот раствор дважды экстрагируют равным объемом фенола/хлороформа" смесь 1: 1/ и осаждают РНК добавлением 2,5 объемов этанола. Осажденную РНК собирают центрифугированием /15 минут при 4000 об/мин./ и снова суспендируют в 0,01 М Трис, pH 7.5 1 мМ ЭДТА, 0,25 М NaCl/TE буфер плюс 0,25 М NaCl/ и снова осаждают добавлением 2,5 объемов холодного этанола. Наконец собирают РНК центрифугированием и снова суспендируют в 5 мл воды. Конечный выход 7,5 мг.
Изолируют матричную РНК из всей цитоплазматической РНК селекцией на олиго-dT-целлюлозе. Нагревают 2,5 мг всей РНК до 65o в течение 5 минут. Прибавляют NaCl до 0,5 М и дают РНК остыть до комнатной температуры. Эту РНК пропускают через колонку с 1 мл олиго-dT-целлюлозы, уравновешенную в TE + 0,5 М NaCl/связующий буфер/. Удаляют несвязанную РНК экстенсивным промыванием колонки связующим буфером. Связанную матричную РНК элюируют 3 мл воды и осаждают добавлением 0,2 мл 4 М NaCl и 2,5 объемов холодного этанола. Осажденную мРНК собирают центрифугированием /30 минут при 25000 об/мин/. Конечный шарик /приблизительно 100 мгк/ повторно суспендируют в 50 мкл воды.
Стадия 2. Реакция однониточной кДНК.
Разбавляют 20 мкг PBL мРНК в 50 мкл реакции синтеза кДНК, содержащей 100 мМ Трис, pH 8,4, 140 мМ KCl, 10 мМ MgCl2, 10 мМ 2-меркаптоэтанола, 400 мкмМ каждого из dATP, dGTP, dCTP и dTTP, 5 мкг олиго-dT /средний размер 12-18/ в качестве праймера, 25 μ Ku 32PdCTP /400 μ Ku/моль/ и 20 единиц ингибитора рибонуклеазы РНК син. Реакцию инициируют добавлением 60 единиц обратной транскриптазы при 37oC и инкубируют 30 минут при 42oC. Реакцию останавливают добавлением ЭДТА до 40 мМ и экстрагируют равным объемом насыщенного водой фенола. Фенольную фазу снова экстрагируют 50 мкл TE буфера. Водные фазы объединяют. Отделяют гибриды кДНК/РНК от непрореагировавших трифосфатов, пропуская объединенные водные фазы через колонку с 5 мл Сефарозы CL-4B. /получена от Сигмы/, уравновешенную TE. Фракции, которые отводят из колонки, объединяют, доводят до 2500 мМ NaCl и осаждают нуклеиновые кислоты добавлением 2,5 объемов холодного этанола. Гибриды собирают центрифугированием в течение 30 минут при 4000 об/м. Конечный шарик /2,5 мкг кДНК/ снова суспендируют в 50 мкл воды.
Стадия 3. Реакция двуниточной кДНК.
Синтезируют двуниточную кДНК при совместном действии ферментов E.coli ДНК Полимеразы 1, E.coli ДНК лигазы и E.coli РНКазы Н. Реакционная смесь /50 мкл/ содержит 20 мМ Трис, pH 8,0, 4 мМ MgCl2, 1,2 мм ЭДТА, 25 М НАД, 100 μ М каждого из dATP, dGTP, dCTP и dTTP, и 50 μ Ku 32PdCTP/3000 Ku / ммоль/.
Проводят реакцию при добавлении 3 единиц ДНК Полимеразы 1,05 единиц ДНК лигазы и 0,75 единиц РНКазы H и инкубировании при 16o в течение 18 часов, затем 1 час при 37oC, а затем останавливают добавлением ЭТА до 40 мМ экстрагируют равным объемом фенола. Фенольную фазу снова экстрагируют 50 мкл TE, объединяют водные фазы и отделяют к ДНК от непрореагировавших трифосфатов хроматографией на колонке с Сефарозой CL-4B, как описано выше для однониточной кДНК. Основываясь на включенном 32P, однониточная кДНК количественно превращается в двуниточную форму.
Стадия 4. Получение рекомбинантной кДНК.
Прибавляют гомополимерные C "хвосты" к конца кДНК при осторожном нагревании 400 нг кДНК в 50 мкл реакционной смеси, содержащей 1 мМ 2-меркаптоэтанола, 1 мМ CoCl2 и 9 единиц концевой деоксинуклеотидилтрансферазы, при 30oC в течение 5 минут. Реакцию прекращают добавлением ЭДТА до 40 мМ и нагревают до 68oC в течение 10 минут. Закаливают 200 нг этой хвостовой кДНК с 500 нг G-хвостового pAT153 /получена от Амершем/ в 100 мкл 10 мМ Трис, pH 7,5, 1 мМ ЭДТА и 100 мМ NaCl. Реакцию закаливания проводят при 57oC в течение 2 часов после 3 минут предварительной инкубации при 68oC.
Стадия 5. Трансформация бактерий.
Продукт реакции закаливания кДНК используют непосредственно для трансформации E.coli штамм MC1061. Используют свежую колонию бактериальных клеток для инокуляции 50 мл L-бульона и выращивают несколько часов до тех пор, пока оптическая плотность при 550 нм не достигнет 0,25. Клетки замораживают на льду и собирают центрифугированием /2000 об/мин в течение 10 минут/. Шарик повторно суспендируют в 10 мл холодного 0,1 м CaCl2 и оставляют на льду на 10 минут. Клетки собирают центрифугированием /2000 об/мин в течение 5 мин/ и повторно суспендируют в 2,5 мл 0,1 М CaCl2. Затем 10 мкл реакционной смеси закаливания кДНК инкубируют с 200 мкл обработанных CaCl2 бактерий в течение 30 минут на льду, а затем 2 минуты при 37oC, затем добавляют 0,8 мл L-бульона и наконец инкубируют 30 минут при 37oC.
Осуществляют 20 из этих трансформаций, используя всю закаленную кДНК. Каждую трансформированную смесь наливают на пластины с 1% агаром L-бульоном / 15 см диаметр/, содержащее 10 мкг/мл тетрациклина. Из 20 трансформаций все 20 таких пластин были залиты и инкубированы всю ночь при 37oC. В среднем приблизительно 1500 бактириальных колоний выросло на каждой пластине, всего 30 000 клонов.
Стадия 6. Посев реплик.
Первоначальные колонии, выросшие на каждой пластине, переносят на 137 мм нитроцеллюлозные фильтры прижиманием сухого фильтра к верхушкам колоний и снятием их с пластины. Готовят две идентичных реплики для каждого исходного фильтра по стандартной методике посева реплик, в которой каждый оригинальный фильтр осторожно помещают сбоку колонии на стерильный квадрат фильтровальной бумаги /Ватман 3ММ/, оставляя на квадратном кусочке стекла. Новый предварительно увлажненный нитроцеллюлозный фильтр осторожно накладывают поверх основного фильтра, покрывают вторым стерильным квадратом фильтровальной бумаги и полный сэндвич затем зажимают вместе с первым и вторым куском стекла. Нумеруют сэндвичевые фильтры и 3 отверстия малого диаметра пробивают через них асимметрично, чтобы можно было точно выровнять в будущем. Затем удаляют реплики с основы и помещают колонии сбоку на новые пластины с L-бульоном агаром, содержащие тетрациклин. Немедленно готовят вторую реплику идентичным образом. Каждый основной фильтр возвращают на пластину и все пластины инкубируют при 37oC в течение нескольких часов до тех пор, пока бактериальные колонии не достигнут примерно 1 мм в диаметре. Основные исходные фильтры хранят при 4oC и готовят реприки для гибридизации, как описано ниже.
Стадия 7. Приготовление фильтров для гибридизации.
Каждый фильтр-реплику /стадия 6/ помещают сбоку колонии на фильтровальную бумагу /Ватман 3 MM/, смоченную в 0,5 М NaOH, 1,5 М NaCl в течение нескольких минут. Фильтры переносят для нейтрализации на фильтровальную бумагу, смоченную в 1 м Трис, pH 7,5 1,5 М NaCl в течение 2 минут, а затем переносят на вторую группу фильтров для нейтрализации в течение 5-10 минут. Наконец фильтры помещают на фильтры, смоченные SSC-буфером /0.015 М цитрата натрия, 0,15 М NaCl, pH 7,4/ в течение 5 минут, сушат на воздухе и прогревают в вакууме при 80oC в течение 1-2 часов.
Стадия 8. Изоляция клонов ФСК к ДНК.
Дубликатные фильтры зондируют с радиоактивно меченной вставкой рФСК-1 кДНК, приготовленной как описано выше в примере B. Гибридизуют в кДНК 20 колоний. Пересаживают 20 из них с основного фильтра и выращивают всю ночь в L-бульоне для дальнейшего анализа. Рестрикционный фермент переваривает /PstI/ образцы ДНК /быстрый преп/ из этих клонов, показывая что 3 близки к полной длине. Один из них был секвенсирован. Последовательность области, кодирующей ФСК, этого клона идентична соответствующей последовательности pCSF-1 /а именно, имеет T в положении 365-CSF/Ile//.
Пример D (III). Очистка ФСК из линии Mo-клеток.
Инкубируют отработанную кондиционированную MO среду, не содержащую сыворотки /40 л/, при 55oC в течение 30 минут для инактивации HTZV-II вируса, ассоциированного с клеточной линией. Эту среду концентрируют ультрафильтрацией по давлениям, используя Пелликон Газетт с мембраной PTGC /1,5 кв. фута/, которая имеет отрезок с молекулярной массой 10000. Затем белок концентрируют осаждением сульфатом аммония /80% насыщения/. Повторно суспендируют конечный шарик белка /800 мг/ в 100 мл 20 мМ трис /оксиметил /аминометана гидрохлорида/Трис-HCl/, pH 7,4, и диализуют против того же самого буфера /3 раза с 4 л загрузки каждый раз/. Диализованный белок наносят на колонку 2,5 х 10 см с ДЕАЕ /диэтиламиноэтил/ - ультрагелем, уравновешенным в том же буфере. Колонку промывают 800 мл 20 мМ Трис-HCl, pH, 7,4, затем элюируют ФСК-активность 800 мл 20 мМ Трим-HCl, pH 7,4, содержащего 0,12 М NaCl. Собирают фракции 10 мл и проверяют на ФСК. Объединяют активные фракции /3/ и концентрируют в 6 раз /до 5 мл/ ультрафильтрацией под давлением "мембрана Амикон УМ5, отрезок с молекулярной массой 5000/. Концентрированный образец из ДЕАЕ колонки наносят на колонку 1,6 х 100 см с AcA44 ультрагелем/акриламид-агарозный ультрогель, имеющий фракционирование 10-130 к дальтон/, уравновешенным 20 мМ N-2-оксиэтилпиперазн-N-2-этансульфоновой кислотой /HEPES /, pH 7,4, 50 мМ NaCl и 0,01% полиэтиленгликоля /ПЭГ-8000/. ФСК активность элюируют с колонки с кажущейся молекулярной массой 30 к дальтон. Объединяют активные фракции и доводят до 0,15% /объем/объем/трифторуксусной кислоты /ТФУК/ добавлением 10% ТФУК и наносят на колонку 1 х 25 см с Видак C4 обратной фазой. Колонку проявляют с линейным градиентом 0-90% ацетонитрила в 0,1% ТФУК /объем/объем/ при 4 мл/мин/всего 1000 мл/. ФСК активность элюируется приблизительно при 47% объем/объем/ацетонитрила/. Объединенные активные фракции доводят до 0,05% /объем/объем/гептафтормасляной кислоты /ГФМК/ при добавлении половины объема 0,15%/объем/объем/ГМФК/ и наносят на колонку /0,46 х 25 см/ с Видак C4, уравновешенной 0,15% объем/объем/ГФМК. Колонку проявляют с линейным градиентом 0-90% /объем/объем/ацетонитрила в 0,15% /объем/объем/ГФМК при 1 мл/мин. /Всего 340 мл/. ФСК активность элюируется примерно при 53% /объем/объем/ацетонитрила. Было найдено, что активными являются фракции 37-44 /1 мл каждая". Концентрируют 0,15 мл фракции 40 в 4 раза /используя САВАНТ Спид Вак Концентратор/ и прибавляют 40 мкл 2 х СДС гель образца буфера /0,125 М Трис-HCl, pH 6,8, 4% СДС, 20% глицерина и 0,004% бромфенола голубого/. Эти образцы кипятят 2 минуты и наносят на 13,5% СДС гель /Лэммли И., Nature 227, 680 /1970/ /см. фиг.2/. Было определено, что фракция 40 имеет 110 000 единиц ФСК костного мозга мл. Это соответствует примерно 3,0•107 единиц на A280 единиц поглощения. Поскольку типичные белки имеют коэффициенты экстинкции в интервале между 0,8 и 1,2 A280 единиц/мг, очищенный ФСК имеет удельную активность в интервале от примерно 1•107 до примерно 4•107 единиц/мг в пробе с костным мозгом. Подвергают разложению по Эдману 1 мкг образца очищенного GM-ФСК, используя газофазный микросексенсатор нанесенный биосистем. Была определена последовательность остатков 3 - 5, являющаяся AIa Arg Ser.
Пример E (IV). Сотрансформация и амплификация ФСК последовательности в CHO клетках. Пдазмиду p91023/B/-CSF, вводят в CHO ДГФР-дефицитные клетки ДИКХ-BII /Chasin and Urlaub PVAS 77: 4216, 1980/ путем слияния протопластов, как описано /Sandri-goldin et al. Mol. Cell Biol I, 743-752, 1981/. Рост и поддержание CHO клеток описаны /Кауфман и Шарп, J. Mol. Bio, 150, 501-621 /1981/. Для слияния протопластов вводят p91023/B/-CSF-1 в E.coli HB101 / и выращивают бактерии в 50 мл м9 солей, содержащих 0,5% казаининовых кислот, 0,5% глюкозы, 0,012% MgSO4, 5 мкг/мл тиамина, и 10 мкг/мл тетрациклина, до поглощения 0,6 при 600 нм. Добавляют хлорамфеникол до 250 мкг/мл и инкубируют культуру при 37oC дополнительно 16 часов для того, чтобы амплифицировать число копий плазмиды. Клетки центрифугируют при 3000 g в течение 10 минут при 4oC и суспендируют в 2,5 мл охлажденной 20% сахарозы в 50 мМ Трис-Cl, pH 8,0. Прибавляют лизоцим /0,5 мл 5 мл/мл раствора в 0,25 М Трис-Cl, pH 8,0/ и смесь выдерживают на льду в течение 5 минут. Прибавляют ЭДТА /1 мл 0,025 М ЭДТА, pH 8,0/ и выдерживают на льду еще 5 минут, затем медленно прибавляют 1,0 мл 0,05 М Трис-Cl, pH 8,0. Инкубируют суспензию в течение 15 минут при 37oC до тех пор, пока бактерии не превратятся в протопласты. Затем суспензию медленно разбавляют 20 мл предварительно подогретой среды, содержащей 10% сахарозы и 10 мМ MgCl2, и выдерживают 15 минут при 37oC. Раствор протопластов /приблизительно 109/мл/ прибавляют к CHO, ДГФР дефицитным ДТКХ-BII клеткам в пластине с 6 углублениями /приблизительно 1•106 меток /углубление/ при соотношении примерно 1-2•104 протопластов/ клетку и протопласты собирают в шарик в клетки при центрифугировании при 2000 об/мин в течение 8 минут в дисковом роторе вращающегося микротитратора центрифуги IEC Модель K. После центрифугирования удаляют надосадочный слой отсасыванием. Прибавляют 2 мл раствора полиэтиленгликоля 50 г PEO - 1450 /Baker Chem Co/ в 50 мл среды в каждое углубление пластины с 6 углублениями. Клетки снова центрифугируют при 2000 об/мин в течение 90 секунд, удаляют раствор полиэтиленгликоля и пластины три раза промывают 4 мл среды/углубление. Затем клетки трипсинизируют, суспендируют в 10 мл среды, содержащей 10% сыворотки зародыша теленка, и центрифугируют в конической трубке при 500 об/мин в клинической центрифуге. Шарики клеток из 3 углублений объединяют и высевают в чашку 10 см для культуры ткани. К каждой пластине добавляют свежую среду, содержащую 100 мкг/мл канамицина, тимидина, аденоксина, деоксиаденозина, пенициллина и стрептомицина и 10% диализованной сыворотки зародыша теленка. Канамицин вводят для предотвращения роста любых бактерий, которые имеют способность превращаться в протопласты.
Через 2 дня клетки подкультивируют 1:15 в альфа-среде с 10% диализованной сыворотки теленка, пенициллином и стрептомицином, но без нуклеозидов. Затем клетки снова подают в ту же самую селективную среду /лишенную нуклеозидов/ через 4-5 дней.
Колонии появляются через 10-12 дней после субкультивирования в селективной среде. Следовали двум схемам отбора на метотрексат /MTX/ и амплификации. В первой схеме изолируют единые независимо клонированные трансформанты на основе экспрессии ДГФР и выращивают последовательно каждый клон в условиях для амплификации числа копий вышеуказанной ДНК, а именно рост при увеличивающейся концентрации метотрексата. По второй схеме изолируют пул из множественных независимых трансформантов на основе ДГФР экспрессии и размножают вместе в условиях амплификации указанной выше ДНК, а именно рост при повышающихся концентрациях метотрексата. Затем изолируют индивидуальные клоны из массы отобранной популяции и анализируют на GM-ФСК экспрессию. Эти клоны, показывающие самые высокие уровни экспрессии, снова выращивают в условиях дальнейшей амплификации вышеуказанной ДНК /а именно рост в условиях повышающейся концентрации метотрексата в культуральной среде/.
В одном эксперименте семь ДГФР+ трансформантов объединяют в альфа-среду, лишенную нуклеозидов. Эти клетки последовательно выращивают при постепенном увеличении концентраций MTX, начиная с 0,02 μ М, затем 0,1, 0,5 и 2,О μ М MTX. При пробе на GM-ФСК-активность в KG-1 пробе клеток, эти клетки продуцируют от 3000 до 12000 единиц/мл. Отобранную популяцию клонируют при 0.02 μ M. MTX и в 2,0 μ M.MTX. Клоны, полученные в 0,5 μ M.MTX O10, D2 и B6/ последовательно отбирает для роста в 2,О μ M.MTX. При испытании на GM-ФСК активность в пробе на KG-1 клетках, клонированные клеточные линии продуцируют от 15 000 до 300 000 единиц/мл GM-ФСК активности. GM-ФСК, продуцированный согласно этому примеру, имеет аминокислотную последовательность, приведенную для ФСК-Thr на фиг.1.
Пример G (X),
Экспрессия GM-ФСК в E.coli.
GM-ФСК экспрессируется в E.coli из вектора pTALC.-185R, схематическое описание которого приведено на фиг. 6. Последовательность, кодирующая GM-ФСК, начинается с синтетической последовательности ATG.CCA.CCA.CCT.CCT.TCT. CCA.TCT.CCA.CTC.ACT, которая определяет начальные II аминокислотных остатков зрелого GM-ФСК. Остальная последовательность, кодирующая GM-ФСК, в pTALC.-185R является идентичной последовательности pCST-1, нуклеотиды 97-447 вслед за последовательностью TAR. TAR. TAG. Сразу после триплетного терминатора имеется pUM-18 полилинкер. Ген резистентности к тетрациклину из pBP322 был вставлен в противоположной ориентации к ФСК гену, 100 оснований вниз от pUC-18 полилинкера. Ген резистентности к тетрациклину несет свой собственный просмотр. Продолжая движение против часовой стрелки имеется следующий ген для β-лактамазы вслед за pUC-18/CdZEI/ источником репликации.
Конечным структурным признаком плазмиды перед возвращением к ФСК последовательностям является PL промотор. Этот промотор по существу описан А. Скатцманом и М. Розенбергом /в "Лабораторном руководстве по молекулярному клонированию" /1982/, Колд Спринг Харбор Лаборатори, с.419/. ФСК экспрессия обеспечивается PL промотором после термической индукции в подходящем штамме-хозяине E.coli.
Родительский штамм, используемый для конструирования всех штаммов, представляет собой W 3110 IacIoL8 /R. Brent and M. Ptashne PNAS 78 /1981/ 4204-4208/.
Фрагментλ ДНК / λ нуклеотиды 34499 - 38214/ интегрируют в хромосому W 3110 Iac1oL8 у IacL локуса. Интеграцию осуществляют с использованием вектора интеграции, состоящего из pBR325 последовательностей, несущих гены для резистентности к хлорамфениколу и амипициллину, а также pBR322 источника репликации. /F. Bolivar, Gene, 4: /1978/, с. 121-136/. Вставляют λ ДНК фрагмент в IacL ген, который сам находится в плазмиде в качестве фрагмента, простирающегося от сайта Bst Eilb LacI до сайта IthillI вниз от lacL.
Интеграция λ ДНК в хромосомальную копию lacL достигается гомологической рекомбинацией и находят Iac+, чувствительные к ампициллину, резистентные к хлорамфениколу колонии. Второй рекомбинационный случай приводит к удалению всех экстра-плазмидных последовательностей, но приводит к тому, что интегрированный λ ДНК фрагмент скринируется на лактозных пластинах МакКонкея. Во втором рекомбинантном случае исходный Iac+, amp, camP фенотип изменяется на Iac-, amps, cams фенотип. Полученный в результате штамм назван GZ400 и является λp при 30o и λs при 42oC. Этот фенотип демонстрирует существование функциональной хромосомальной копии Cl857 аллеля.
GL400 дает lon при PL трансдукции из лизата, выросшего на штамме SG20252 /lac. Δ и 1169, ara 139 гр. sl lon Δ, T h 10/ Th10 заготавливают скринированием на Tets на селективной среде. /S. Maloy, W. Nunn, J. Bacterial. 145/1981/ 1110-1112/
Готовый штамм-хозяин называется G.1413 /Iac1oL8, LacZ Δ / λ Cl, REX, N/, lon Δ 100/.
pTALC-185R, транспортируют в G1413. Культуру этого штамма выращивают всю ночь при 30oC в 5 мл индукционной среды, содержащей 7 мкг/м тетрациклина. Индукционная среда содержит, на 1 л: 20 г казаининовых кислот, 6 г Na2HPO4 • 7H2O, 3 г KH2PO4, 0,5 г NaCl, 1 г NH4Cl 1% глицерина, 2 мг витамина B1, 2 мг CaCl2 • 2H2O, 0,2 г MgCl2 • 6H2O.
Инокулируют 25 мл этой среды, содержащей 7 мкг/мл тетрациклина, 125 мкл ночной культуры и встряхивают при 30oC на водяной бане до тех пор, пока культура не достигнет плотности при A550 0,5. Затем быстро переходит на 40o водяную баню и встряхивают еще 2 часа, чтобы дать возможность пройти синтезу GM-ФСК. Собирают урожай клеток и проверяют их на содержание ФСК электрофорезом на СДС-полиакриламидном геле. В этих условиях GM-ФСК аккумулируется приблизительно до 5% от клеточного белка.
Пример C (VI). Экспрессия GM-ФСК в Saceharomyus Cerevisial.
A. Вектор конструирования.
Конструируют плазмиду, которая содержит ген для фермента в урацил биосинтетическом пути /UPA3/ в качестве гена селекции и 2 источника репликации. Эта плазмида происходит из VIp5 /Botstein et al Gene, 8, с.с. 17-24 /1979// с добавлением фрагмента, содержащего источник репликации из 2 микрон плазмиды дрожжей.
B. Изоляция гена для глицеральдегид фосфат дегидрогеназы /SPDH/.
Изолировали из дрожжей два гена для GFDH /Holl and and Hol land Jarnal of Bidogical Chemistry 225, с.с. 2596-2605 /1980// Олигонуклеотидный зонд, синтезированный из опубликованной последовательности, используют для изоляции GFDH гена из плазмидной библиотеки дрожжевой геномной ДНК по стандартным методикам. Плазмида, содержащая целый GAP491 ген, была депонирована ранее /ATCC N 39777/.
C. Получение промотора глицеральдегид фосфат дегидрогеназы для экспрессии гетерологического гена.
Конструируют плазмиду, которая позволяет природное распределение GPDH промотора с начала целевого гетерологического структурального гена. Это осуществляется при введении Kp I сайта в непосредственной близости к инициирующему метиониновому кодону GPDH структурального гена. Затем вставляют промотор "cas sette" в дрожжевой вектор экспрессии YOpI.
D. Изоляция гена для α- фактора.
Из дрожжей изолировали ген для фактора α зреющего феромона /Kurjan and Herskowitz, Cell 30, с.с. 933-943 /1982//. Олигонуклеотидный зонд, синтезированный из этой последовательности, используют для изоляции гена из плазмидной библиотеки дрожжевой геномной ДНК по стандартным методикам.
E. Получение плазмиды экспрессии ФСК.
Конструируют по стандартным методикам из описанных выше элементов и гена человеческого ФСК вектор экспрессии /AJ 14, фиг. 7/. В этом векторе удалили природную лидерную последовательность ФСК и вставили последовательность, кодирующую зрелый ФСК, вблизи пре-про последовательности λ фактора. Соединения между GPDH промотором, пре-про последовательностью λ фактора и последовательностью зрелого ФСК уточнены /ниже/ и были подтверждены деоксинуклеотидным секвенсированием. AAATAAACAAAATG.CGTTTTCCTTCA....... AAA AGA GAG GCG GAA GCT.GCA CCC GCC CGC TCG...
F. Экспрессия GM-ФСК
Плазмиду AJ 14 трансформируют в штамм Saccharowyces Cerevisial Культивируют клетки для продуцирования ФСК.
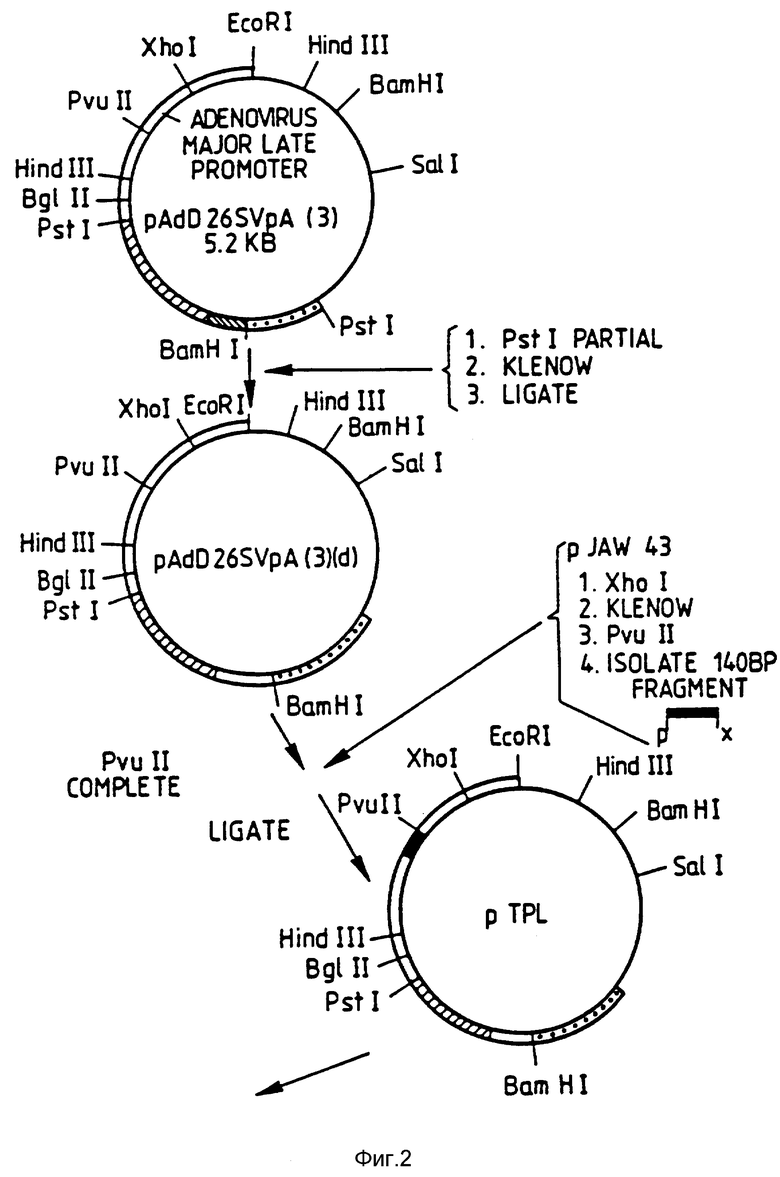
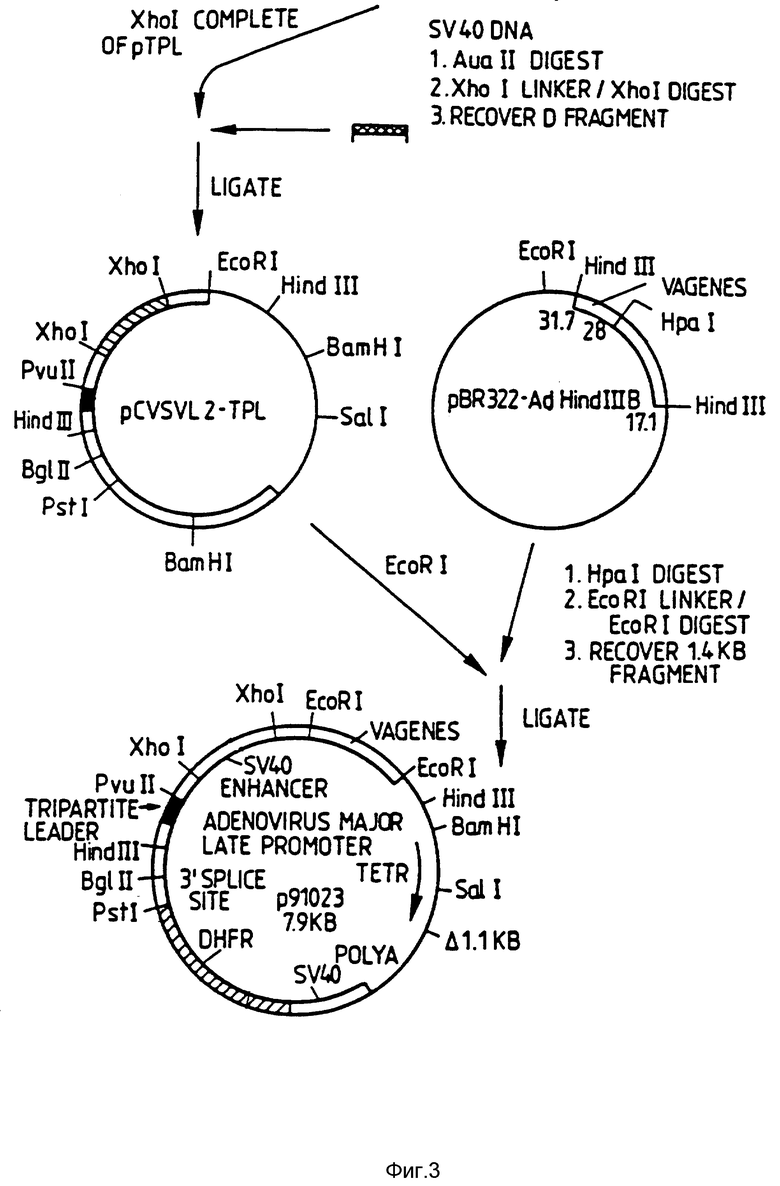
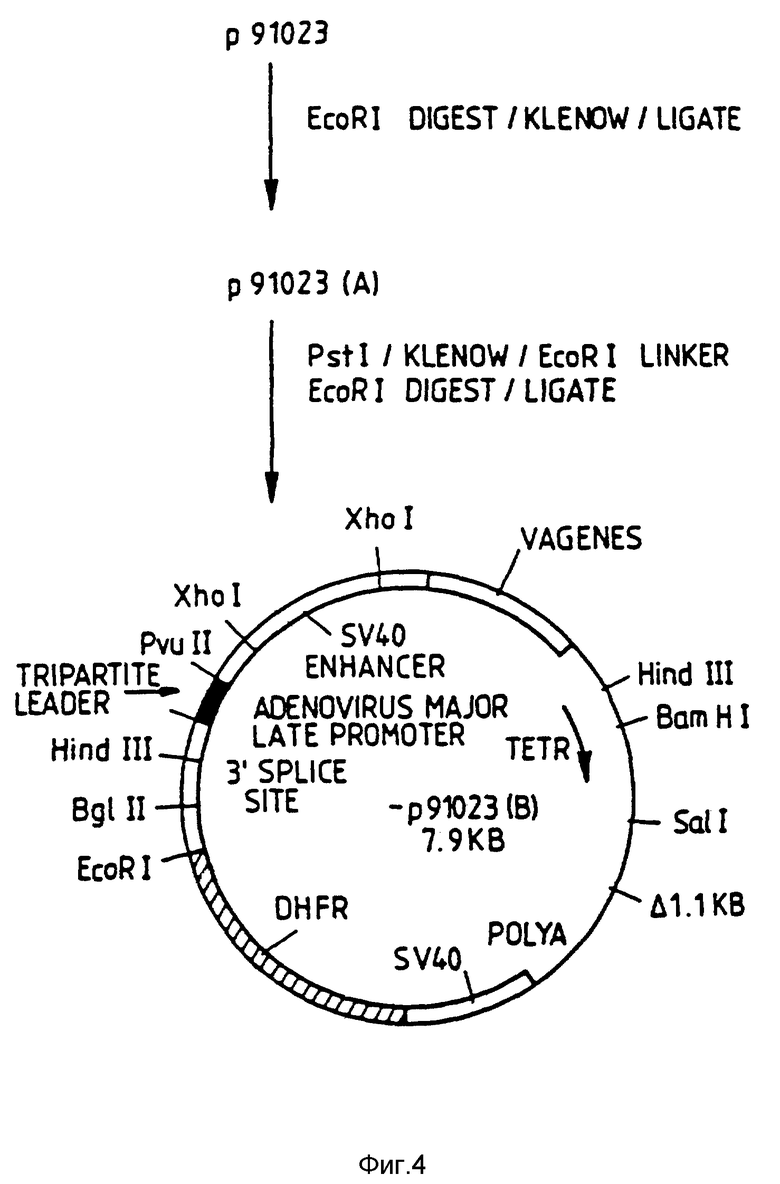

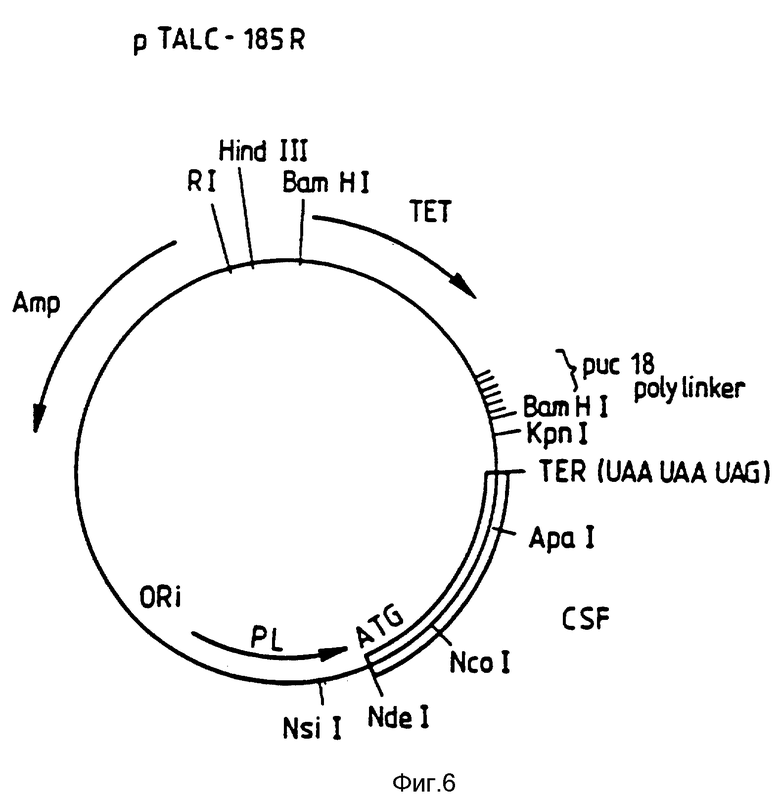
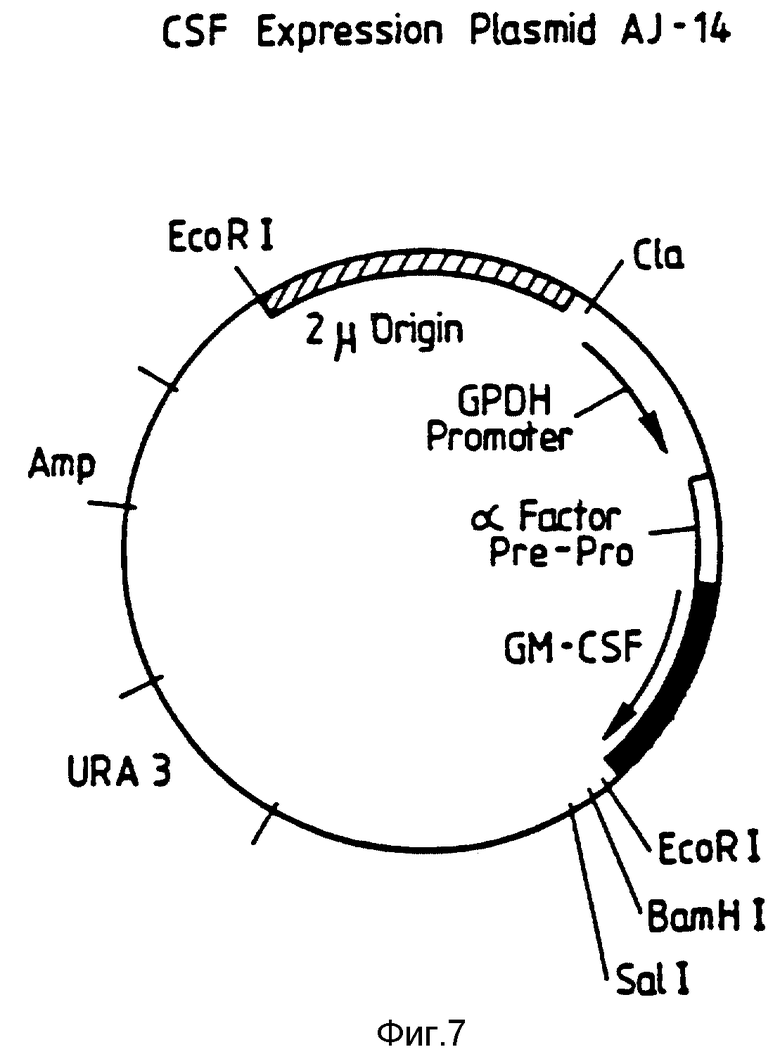
Изобретение относится к генной инженерии. Разработан способ получения белка с активностью гранулоцитмакрофагколониестимулирущего фактора (GМ - СSF) приматов. В процессе способа осуществляют культивирование дрожжевых или прокариотических клеток после их трансформации рекомбинантным вектором с геном, кодирующим полипептид с установленной аминокислотной последовательностью. Продуцируемый белок представляет собой указанный фактор человека (СSF - Th2 или СSF - Ile ) или гиббона (СSF - G). После культивирования белок выделяют и очищают. Полученный рекомбинантный белок имеет более высокие степень чистоты и уровень биологической активности. 6 з.п.ф-лы, 7 ил.
| US 4438032, 20.03.84 | |||
| J | |||
| Blood | |||
| Чугунный экономайзер с вертикально-расположенными трубами с поперечными ребрами | 1911 |
|
SU1978A1 |
| J | |||
| Blood | |||
| Способ получения фтористых солей | 1914 |
|
SU1980A1 |
| J | |||
| Blood | |||
| Гребенчатая передача | 1916 |
|
SU1983A1 |
Авторы
Даты
1999-05-20—Публикация
1985-07-04—Подача