1. Область изобретения.
Область настоящего изобретения включает кристаллические формы известного соединения - соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4-[3- (1-метилэтиламино)-2-пиридинил] пиперазина, которая является фармацевтически полезным соединением при лечении пациентов с положительной ВИЧ-реакцией (ВИЧ-вирус иммунодефицита человека).
2. Описание уровня техники.
Специалистам известно, что твердые вещества, включая фармацевтические препараты, часто имеют более одной кристаллической формы, что называется полиморфизмом. В типичных работах по свойствам твердых фармацевтических препаратов приведены многочисленные примеры: Byrn, S.R., Solid-State Chemistry of Drugs, New York, Academic Press (1982); Kuhnert-Brandstatter, M., Thermomicroscopy In The Analysis of Pharmaceuticals, New York, Pergamon Press (1971) и J.Pharm.Sci., 58, 911 (1969). Byrn утверждает, что полиморфные вещества в основном демонстрируют разные физические характеристики, включая растворимость и физическую и химическую устойчивость. Важно отметить, что не существует надежного способа предсказания различимых кристаллических структур данного лекарства или предсказать наличие полиморфного соединения с подходящими физическими свойствами.
Патент США 3565924 раскрывает и заявляет твердое соединение 25-гидроксикокальциферол (25-hydroxycocalciferol = 25-HCC). Даже принимая во внимание этот прототип Патентное Ведомство США выдало Патент США 3833622 на новую кристаллическую форму полугидрата 25-HCC.
Патент США 4521431 раскрывает формы 1 и 2 гидрохлорида ранитидина (ranitidine hydrochloride).
Патент США 4504657 заявляет кристаллический моногидрат 7-[D-a-(пара-гидроксифенил)ацетамидо]-3-метил-3-цефем-4-карбоновой кислоты.
Международная публикация N WO 91/09849 (Пример 105) раскрывает 1-[5-метан-сульфонамидоиндолил-2-карбонил] -4-[3-(1-метилэтиламино)-2- пиридинил] пиперазин.
В журналах Journal of Medicinal Chemistry, 36, 1505 (1993) и Antimicrobial Agents & Chemotherapy, 1127-31 (Май 1993) раскрыта соль монометансульфонат 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил] - пиперазина в кристаллической форме, отличающейся от заявленной здесь.
3. Краткое описание изобретения.
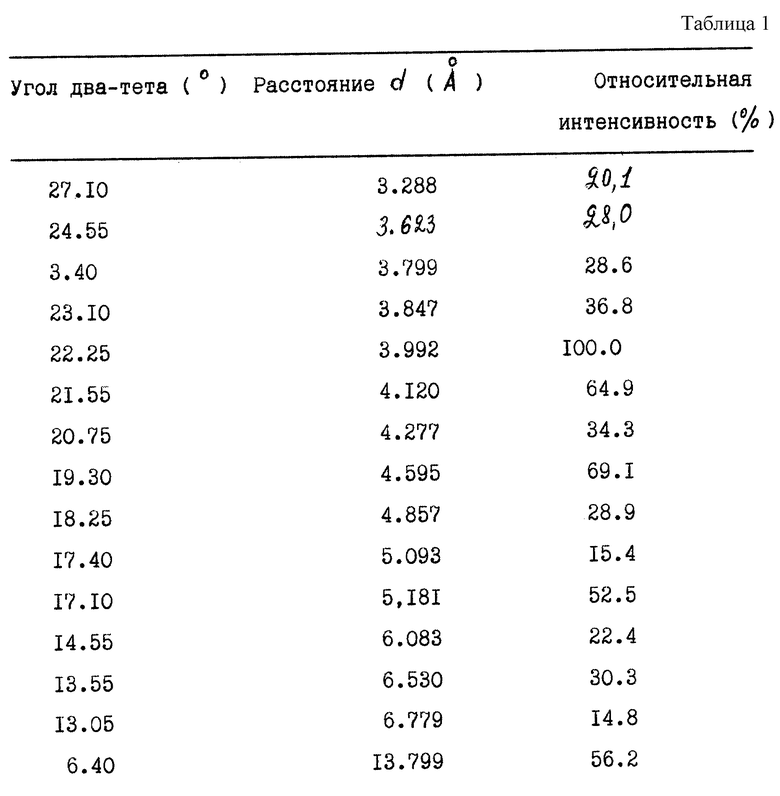
Раскрыта соль монометансульфонат 1-[5-метансульфонамидоиндолил- 2-карбонил] -4-[3-(1-метилэтиламино)-2-пиридинил] - пиперазина, известная как "S" форма, для которой в формуле изобретения приведены рентгеновские диффракционные спектры порошка.
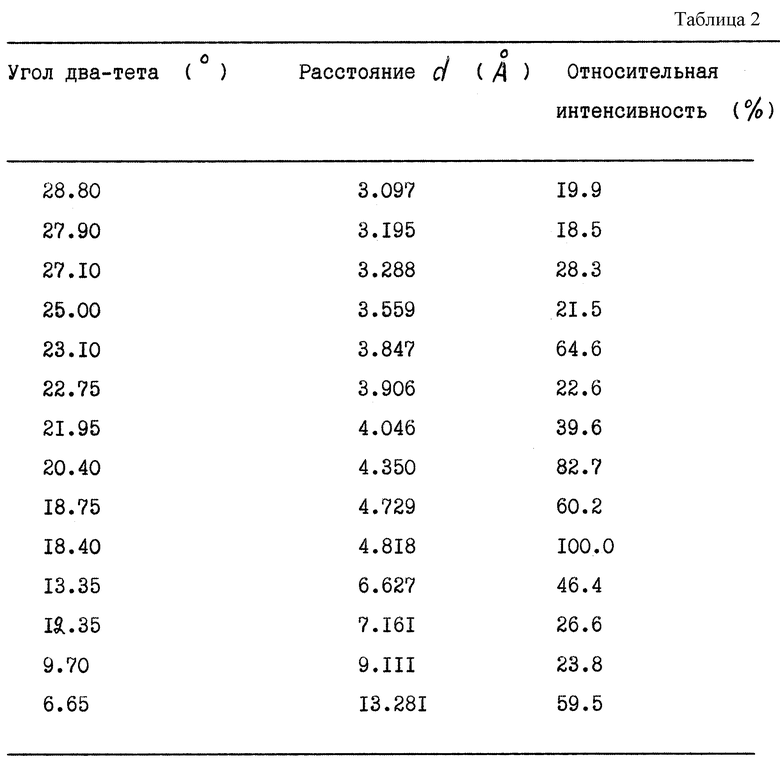
Также раскрыта соль монометансульфонат 1-[5-метансульфонамидолил- 2-карбонил] -4-[3-(1-метилэтиламино)-2-пиридинил] пиперазина, известная как "T" форма, для которой в формуле изобретения приведены рентгеновские диффракционные спектры порошка.
4. Подробное описание изобретения.
Известен 1-[5-метансульфонамидоиндолил-2-карбонил]-4- [3-(1-метилэтиламино)-2-пиридинил] пиперазин, смотри Международную публикацию N WO 91/09849 (Пример 105). Известна также соль монометансульфонат 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил] пиперазина, смотри журналы Journal of Medicinal Chemistry, 36, 1505 (1993) и Antimicrobial Agents & Chemotherapy, 1127-31 (Май 1993).
Кристаллическую "S" форму (известную так же, как форму VIII) соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил]-4- [3-(1-метилэтиламино)-2-пиридинил] пиперазина получают, исходя из соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил] пиперазина, которая отличается от "S" формы, растворяя ее в растворяющем растворителе, выбранном из группы, состоящей из метанола, этанола, ацетонитрила, диметилсульфоксида и диметилформамида или их смесей; предпочтительным растворяющим растворителем является метанол. Если исходят из свободного амина, то в качестве совместно действующего растворяющего растворителя можно использовать метиленхлорид, предпочтительно с метанолом, хотя сам по себе метиленхлорид не растворяет исходное вещество в заметной степени. К раствору соли в растворяющем растворителе добавляют достаточное количество кристаллизующего растворителя или смеси таких растворителей, которые выбирают из группы, состоящей из ацетона, ацетонитрила, изопропанола, н-пропанола, метил-трет-бутилового эфира, этилацетата, н-пропилацетата, изопропилацетата, тетрагидрофурана, толуола или любых изомеров ксилола, гексана или гептана; предпочтительным кристаллизующим растворителем является ацетон. Предпочтительно добавлять очень небольшое количество требуемой кристаллической формы, так как это ускоряет кристаллизацию требуемой "S" формы. После кристаллизации соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил]-4-[3-(1-метилэтиламино)-2- пиридинил]пиперазина ее фильтруют и сушат известным специалистам способом.
Когда требуется "S" кристаллическая форма соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил] пиперазина, предпочтительно растворять соль монометансульфоната 1-[5-метансульфонамидоиндолил-2- карбонил] -4-[3-(1-метилэтиламино)-2-пиридинил] пиперазина в метаноле до концентрации примерно 1 г соединения на 5 мл метанола. Эту смесь затем концентрируют при нагревании с обратным холодильником при атмосферных условиях примерно до одномолярной концентрации. Во время нагревания с обратным холодильником за небольшой отрезок времени, например, пять или десять минут, добавляют ацетон (примерно 4 мл/г соли монометансульфоната 1-[5-метансульфонамидоиндолил- 2-карбонил] -4-[3-(1-метилэтиламино)-2-пиридинил] пиперазина). В этот момент желательно и предпочтительно инициировать кристаллизацию небольшим количеством "S" кристаллической формы. Пока происходит кристаллизация смесь перемешивают при нагревании с обратным холодильником. Смесь можно фильтровать в горячем или холодном виде.
Альтернативной является процедура, когда исходят из свободного основания 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил]пиперазина и получают соль метансульфокислоты одновременно с кристаллизацией (смотри Примеры 2 и 8), что является предпочтительным способом осуществления изобретения в больших масштабах. Для небольшого производства (в лабораторных или стендовых условиях) и нечастых процессов предпочтительными являются способы Примеров 1, 4 и 6.
Если необходимо исходить из свободного основания и ацетонитрила в качестве растворяющего растворителя, то при температуре ниже 40oC получают сольватированную кристаллическую форму. После высушивания из твердого продукта удаляют ацетонитрил, и в результате образуется десольватированная кристаллическая форма. Если исходят из свободного основания и метанола в качестве растворяющего растворителя и используют изопропанол в качестве кристаллизующего растворителя, то образования нежелательных кристаллических форм (как в случае ацетонитрила и при низкой температуре) не происходит, но кристаллы могут аггломерировать, что может затруднять высушивание. Если в качестве кристаллизующего растворителя используют ацетон, проблем, связанных с аггломерацией, не возникает.
Кристаллическую "T" форму (известную так же, как форму XI) соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил]-4- [3-(1-метилэтиламино)-2-пиридинил] пиперазина получают, исходя из соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил]пиперазина в отличающейся от "T" форме и проводя перекристаллизацию из растворяющего растворителя (как указано выше). Использование кристаллизующего растворителя (указано выше) является произвольным. "T" форму соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4-[3-(1-метилэтиламино)- 2-пиридинил] пиперазина можно получить либо из свободного основания, либо из другой кристаллической соли мезилата (mesylate), как описано выше для кристаллической формы "S". Для получения "T" формы предпочтительно иметь концентрацию примерно 1 г соединения на мл растворяющего растворителя, особенно, когда растворяющим растворителем является метанол. При получении кристаллической "T" формы предпочтительно вносить в реакционную смесь затравку полученного ранее "T" кристалла.
Обе формы ("S" и "T") соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил]-4-[3-(1-метилэтиламино)-2- пиридинил]пиперазина применяют таким же образом, как описано для 1-[5-метансульфонамидоиндолил-2-карбонил] -4-[3-(1- метилэтиламино)-2-пиридинил] пиперазина в Международной публикации N WO 91/09849. Более подробно, "S" и "T" формы монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4-[3-(1-метилэтиламино)-2- пиридинил]пиперазина полезны при лечении СПИД (AIDS).
Термин ретровирус человека (HRV) обозначает тип I вируса иммунодефицита человека или его штаммы, очевидные для специалистов, которые принадлежат к тому же семейству вирусов и оказывают аналогичные физиологические действия на людей, как и различные ретровирусы человека.
Пациентами, нуждающимися в таком лечении, являются (1) лица, инфицированные одним или более штаммами ретровируса человека, что определяют по присутствию измеримого количества вирусных антител или антигенов в сыворотке, и (2) лица с какой-либо инфекцией, симптоматически определяющей СПИД, такой как: (a) распространенный гистоплазмоз, (b) изопсориаз, (c) бронхиальный и легочный кандидоз, включая пневмоцистную пневмонию, (d) лимфома non-Hodgkin's lymphoma или (e) саркома Капози (Kaposi's sarcoma), и моложе шестидесяти лет; или имеющие абсолютное число CD4 лимфоцитов менее 200/м3 в периферической крови. "S" и "T" формы монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4-[3-(1-метилэтиламино)-2- пиридинил] пиперазина можно применять орально. Подходящие дозированные формы включают таблетки, капсулы, суспензии, растворы и эликсиры. Эффективное количество составляет примерно от 0.1 до 500 мг/кг в день. Типичная разовая доза для человека весом 70 кг должна составлять примерно от 10 до 2000 мг, предпочтительно примерно от 100 до 1000 мг в день за один - шесть приемов.
Точная дозировка и частота приема зависят от того, используют ли "S" или "T" форму монометансульфоната 1-[5-метансульфонамидоиндолил- 2-карбонил]-4-[3-(1-метилэтиламино)-2-пиридинил] пиперазина, конкретных условий приема, тяжести заболевания, возраста, веса, общего физического состояния конкретного пациента, другого возможного хорошо известного специалистам медикаментозного лечения пациента, более точно дозировку и частоту приема можно определить, определяя уровень или концентрацию соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4-[3-(1-метилэтиламино)-2- пиридинил] пиперазина в крови пациента и/или реакцию пациента на конкретное подвергающееся лечению состояние.
Пациенты с положительной реакцией на HIV (вирус иммунодефицита человека), но без симптомов обычно должны принимать меньшие оральные дозы (примерно от 0.2 до 100 мг/кг в день). ARC-пациенты (ARC = AIDS-related complex = комплекс, родственный СПИД) и СПИД пациенты обычно должны принимать большие оральные дозы (примерно от 1 до 500 мг/кг в день).
"S" и "T" формы соли настоящего изобретения монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4-[3-(1-метилэтиламино)-2- пиридинил] пиперазина можно применять вместе с другими противовирусными агентами, такими как AZT.
Точная дозировка и частота приема зависят от конкретных условий приема, тяжести заболевания и состояния, возраста, веса, общего физического состояния конкретного пациента, другого возможного хорошо известного специалистам медикаментозного лечения пациента; более точно дозировку и частоту приема можно определить, установив уровень или концентрацию CD4 в крови пациента и/или клиническую реакцию пациента.
5. Определения.
Приведенные ниже определения и терминология использованы во всем документе, включая описание и формулу изобретения.
Все температуры приведены в градусах Цельсия.
При использовании пары растворителей указывают их объемные соотношения.
При использовании понятия растворимость твердого вещества в растворителе указывают на соотношение твердого соединения к растворителю в виде отношения веса к объему.
6. Примеры.
Без дополнительных уточнений очевидно, что специалист, используя предыдущее описание, может воплотить на практике настоящее изобретение во всей его полноте. Следующие подробные примеры описывают, как получить различные соединения и/или осуществить различные способы, и являются лишь иллюстративными, не ограничивая ни коим образом предшествующее описание.
ПРИМЕР 1. Получение кристаллической "S" формы соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил]пиперазина из другой кристаллической формы.
Соль монометансульфонат 1-[5-метансульфонамидоиндолил-2- карбонил]-4-[3-(1-метилэтиламино)-2-пиридинил] пиперазина (кристаллическая форма XI, 25 г) растворяют в метаноле (125 мл) при нагревании с обратным холодильником. Смесь концентрируют в атмосферных условиях до объема 40 - 45 мл. Продолжая нагревание с обратным холодильником, добавляют теплый ацетон (100 мл) за 5 минут. Смесь выдерживают при нагревании с обратным холодильником и в течение 30 минут наблюдают кристаллизацию. Суспензию перемешивают при нагревании с обратным холодильником в течение полных 60 минут и затем фильтруют. Отжатый осадок промывают ацетоном (100 мл) и сушат, получая указанное в названии соединение, т.пл. 228 - 232oC.
ПРИМЕР 2. Получение кристаллической "S" формы соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил]пиперазина из свободного основания.
Готовят суспензию 1-[5-метансульфонамидоиндолил-2-карбонил]-4- [3-(1-метилэтиламино)-2-пиридинил] пиперазина (сольват ТГФ, 100 г, 0.18 моля) в метаноле, к которому добавлена метансульфокислота (19.6 г, 0.20 моля). Смесь нагревают до 40oC и добавляют изопропанол (325 мл). Смесь выдерживают при 37 - 42oC и в течение 2 - 3 часов наблюдают кристаллизацию. Суспензию охлаждают за 2 часа до 15oC и фильтруют. Отжатый осадок промывают изопропанолом (100 мл) и метил-трет-бутиловым эфиром (250 мл), затем сушат, получая указанное в названии соединение, т.пл. 221 - 228oC.
ПРИМЕР 3. Получение кристаллической "S" формы соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил]пиперазина из свободного основания.
1-[5-метансульфонамидоиндолил-2-карбонил] -4-[3- (1-метилэтиламино)-2-пиридинил] пиперазин (сольват ТГФ, 6.58 кг, 12.77 моля) в метаноле (50 л) и метиленхлориде (150 л) фильтруют через 0.6 микронный фильтр, затем промывают метиленхлоридом (50 л). Смесь концентрируют при пониженном давлении и 10oC до объема 10 л, разбавляют ацетонитрилом (160 кг) и концентрируют до 10 л. Затем остаток смешивают с ацетонитрилом (240 л), получая суспензию, смесь нагревают до 63oC и добавляют метансульфокислоту (1.29 кг, 13.4 моля). Затем смесь нагревают до 70 - 75oC и после перемешивания при этой температуре в течение 4.5 часов охлаждают до 32oC. Продукт собирают на фильтре, промывают ацетонитрилом (50 л) и сушат, получая указанное в названии соединение, т.пл. 222 - 229oC.
ПРИМЕР 4. Получение кристаллической "T" формы соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил]пиперазина из кристаллической формы VIII.
Соль монометансульфонат 1-[5-метансульфонамидоиндолил-2- карбонил]-4-[3-(1-метилэтиламино)-2-пиридинил] пиперазина (кристаллическая форма VIII, 25.0 г, 0.045 моля) растворяют в метаноле (25 мл) при нагревании с обратным холодильником. Через час нагревания с обратным холодильником наблюдают образование кристаллов. Суспензию фильтруют, не охлаждая, и сушат, получая указанное в названии соединение, т.пл. 213 - 233oC.
ПРИМЕР 5. Получение кристаллической "T" формы соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил]пиперазина из свободного основания.
Готовят суспензию 1-[5-метансульфонамидоиндолил-2-карбонил]-4- [3-(1-метилэтиламино)-2-пиридинил] пиперазина (сольват ТГФ, 100 г, 0.18 моля) в метаноле (250 мл), к которому добавлена метансульфокислота (19.0 г, 0.21 моля). Смесь нагревают с обратным холодильником до растворения и затем концентрируют при атмосферных условиях до объема 150 мл. В смесь вносят затравку 10 мг полученной ранее кристаллической "T" формы и продолжают нагревание с обратным холодильником до тех пор, пока наблюдается кристаллизация. Суспензию выдерживают при нагревании с обратным холодильником в течение 16 часов, фильтруют, не охлаждая, и затем сушат, получая указанное в названии соединение.
ПРИМЕР 6. Получение кристаллической "T" формы соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил]пиперазина из кристаллической формы VIII.
Соль монометансульфонат 1-[5-метансульфонамидоиндолил-2- карбонил]-4-[3-(1-метилэтиламино)-2-пиридинил] пиперазина (кристаллическая форма VIII, 104.9 г, 0.19 моля) растворяют в метаноле (150 мл) при нагревании с обратным холодильником. Раствор концентрируют при атмосферных условиях до объема 175 мл. Продолжая нагревание с обратным холодильником, добавляют теплый ацетон (100 мл) за 15 минут. В течение 30 минут наблюдают кристаллизацию, во время которой добавляют дополнительное количество ацетона (175 мл) за 70 минут. Суспензию перемешивают при нагревании с обратным холодильником в течение полных 2 часов, охлаждают до 15oC и затем фильтруют. Отжатый осадок промывают ацетоном (200 мл) и сушат, получая указанное в названии соединение, т.пл. 212 - 228oC.
ПРИМЕР 7. Получение кристаллической "T" формы соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил]пиперазина из кристаллической формы VIII.
Готовят суспензию соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил]-4-[3-(1-метилэтиламино)-2- пиридинил]пиперазина (кристаллическая форма VIII, 25.0 г, 0.045 моля) в смеси метанол/ацетон (1/1, 50 мл) при нагревании с обратным холодильником. В суспензию вносят затравку 10 мг выделенной ранее кристаллической "T" формы. После нагревания с обратным холодильником в течение 2 - 3 часов суспензию охлаждают до 15oC, фильтруют, промывают ацетоном (50 мл) и сушат, получая указанное в заглавии соединение, т.пл. 213 - 228oC.
ПРИМЕР 8. Получение кристаллической "T" формы соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил]пиперазина из свободного основания.
Готовят суспензию 1-[5-метансульфонамидоиндолил-2-карбонил]-4- [3-(1-метилэтиламино)-2-пиридинил] пиперазина (свободное основание, сольват ТГФ, 100.0 г, 0.18 моля) в метаноле (250 мл), к которому добавлена метансульфокислота (17.65 г, 0.18 моля). Смесь нагревают с обратным холодильником до растворения и затем концентрируют при атмосферных условиях до объема примерно 300 мл, во время чего вносят затравку 10-15 мг выделенной ранее кристаллической "T" формы соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил]пиперазина. Продолжают концентрирование при атмосферных условиях до объема 200 мл. Продолжая нагревание с обратным холодильником, добавляют ацетон (175 мл) за 10 минут. В смесь снова вносят затравку 10 - 15 мг выделенной ранее кристаллической "T" формы соли монометансульфоната 1-[5-метансульфонамидоиндолил-2-карбонил]-4-[3-(1-метилэтиламино)-2- пиридинил]пиперазина и выдерживают при нагревании с обратным холодильником. В течение 30 минут наблюдают кристаллизацию и выдерживают суспензию при нагревании с обратным холодильником еще в течение 30 минут. В это время снова начинают перегонку при атмосферных условиях и добавляют ацетон, поддерживая постоянный объем. Когда добавлено 250 мл ацетона, перегонку заканчивают и смесь охлаждают до 15oC. После перемешивания суспензии в течение примерно двух часов ее фильтруют и отжатый осадок промывают ацетоном. Продукт сушат, получая 88.96 г указанного в названии соединения, т.пл. 214 - 227oC.
СХЕМА А
1-[5-метансульфонамидоиндолил-2-карбонил] -4- [3-(1-метилэтиламино)-2-пиридинил]пиперазин имеет следующую структурную формулу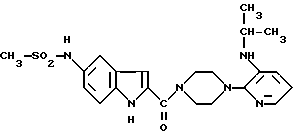 л
л
Изобретение относится к двум новым кристаллическим формам известного соединения - монометансульфонат-1-[5-метансульфонамидоиндолил-2-карбонил]-4-[3-(1-метилэтиламино)-2-пиридинил] пиперазина. Новые кристаллические формы обозначены как "S" и "T" формы и идентифицированы рентгеновскими дифракционными спектрами порошков. Новые кристаллические формы являются фармацевтически полезными соединениями при лечении пациентов с положительной ВИЧ-реакцией (ВИЧ - вирус иммунодефицита человека), 2 с.п. ф-лы.
Приоритет по пунктам:
15.04.94 по пп.1 и 2;
23.09.94 по пп.1 и 2.
| WO 9109849 A, 1991 | |||
| Обзорная информация | |||
| Медицина и здравоохранение | |||
| Серия: Эпидемиология, вирусология и инфекционные заболевания | |||
| Синдром приобретенного иммунодефицита: этиология, патогенез, клиника, диагностика, лечение | |||
| - М.: ВНИИМИ, 1988, выпуск 4, с | |||
| Железобетонный фасонный камень для кладки стен | 1920 |
|
SU45A1 |
Авторы
Даты
1999-09-10—Публикация
1995-03-01—Подача