Изобретение относится к электролюминесцентному материалу, содержащему органическое люминесцентное вещество.
Известен электролюминесцентный материал (ЭЛМ), содержащий в качестве люминесцентного слоя испаренный слой органического соединения - 8-оксихинолината (q) алюминия (Alq3) [C.W. Tang, S.A.Van Slike, Appl.Phys.Letter, v. 51, pp. 913-915 (1987)] . При этом в качестве дырочно-инжектирующего слоя (анода) применяется прозрачный низкоомный слой на основе смешанного оксида индия и олова, In2O3 - SnO2 (ITO), а в качестве электронно-инжектирующего слоя (катода) - сплав Mg-Ag.
Наиболее близким по технической сущности к предлагаемому устройству является ЭЛМ, состоящий из электронно-инжектирующего слоя (катода) (сплав Mg-In с массовым соотношением 10:1), активного люминесцентного слоя, дырочно-транспортного слоя, содержащего N,N'-дифенил-N,N'-(3-метилфенил)-1,1'-бифенил-4,4'-диaмин (TPD) и дырочно-инжектирующего слоя (анода) (In2O3 - SnO2), который содержит в качестве активного люминесцентного слоя хелатные комплексы 8-оксихинолина (q) с металлами 2B или 3A группы Периодической системы (М= Al, Be, Zn, Mg) (Мq3) [С.Токито, Материалы для органических электролюминесцентных элементов на основе металлокомплексов, 6-ой Семинар Органические электролюминесцентные элементы - от базовых знаний к практическим технологиям. Институт технологии, префектура Сайтама, г.Хиросава; Y.Hamada et al. Organic electroluminescent devices with 8-Hydroxyquinoline derivative -metal complexes as an emitter, Japanese Journal of Applied Physics, Part 2, vol.32, no.4 A, 1 April 1993, pp.L514-L515]. Структура на основе такого слоистого материала обладает фото- и электролюминесценцией от зеленого до желтого цвета (λmax = 503-567 нм) в зависимости от выбора металла (Al, Be, Zn, Mg), которая пропорциональна плотности тока в интервале 1-103 мА/см2, причем спектры фото- и электролюминесценции практически идентичны. Для комплексов цинка максимум излучения находится в желтой области. Недостатком материалов на основе Mq3 является высокая чувствительность к влаге и кислороду, что затрудняет работу с ними как при изготовлении так и при эксплуатации приборов (высокие требования к герметичности). Хотя 8-оксихинолинаты имеют высокую термостойкость (в частности Alq3 имеет точку плавления 360oC), но морфология дырочно-транспортного слоя, состоящего из TPD, изменяется уже при комнатной температуре вследствие низкой температуры стеклования (<60oC). Разогрев при работе прибора приводит к изменению электрических свойств транспортного слоя и, как следствие, - потере электролюминесценции устройства, то есть снижению срока службы устройства.
Задачей настоящего изобретения является создание электролюминесцентного материала с излучением в зеленой области спектра, меньшей чувствительностью к влаге и с повышенной термостабильностью.
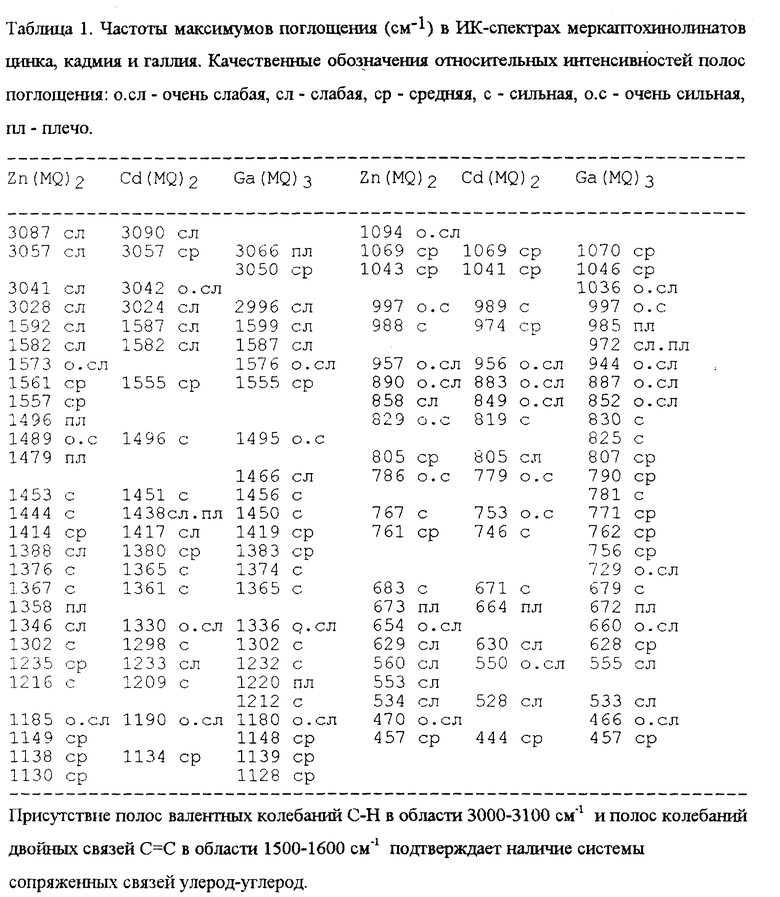
Поставленная задача решается тем, что согласно изобретению электролюминесцентный материал состоит из электронно-инжектирующего слоя, активного люминесцентного слоя, содержащего хелатный комплекс производного 8-меркаптохинолина с металлом 2B или 3A Периодической системы, с общей формулой
где n=2-3, M=Zn, Cd, Ga, R1-R6 независимо друг от друга H, метил; R3, R4 независимо друг от друга фенил, незамещенный или замещенный метилом, трет. бутилом, R3-R5 независимо друг от друга метоксигруппа, этоксигруппа, диметиламиногруппа, диэтиламиногруппа, нитрил, дырочно-транспортного слоя и дырочно-инжектирующего слоя.
Группы R1-R6 в производном 8-меркаптохинолина не изменяют способность вещества к электролюминесценции, но влияют на его растворимость в органических растворителях и позволяют в небольших пределах сдвигать максимум длины волны фото- и электролюминесценции, то есть осуществлять тонкую настройку люминесцентных свойств.
Введение меркаптогруппы вместо оксигруппы приводит к сдвигу излучения в коротковолновую область. Кроме того, меркаптогруппа проявляет меньшую гидрофильность чем оксигруппа.
Предлагаемый электролюминесцентный материал в качестве дырочно-транспортного слоя содержит смесь олигомеров с общей формулой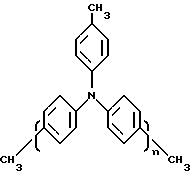
где n= 8-9, при молекулярно-массовом распределении: Mn=2332 (около 9 звеньев), Mw= 3586 и полидисперсности Mw/Mn=1,54, с высокой температурой стеклования 185oC по сравнению с TPD, что обеспечивает сохранение морфологии дырочно-транспортного слоя даже при повышенных температурах [Якущенко И.К., Каплунов М. Г. , Шамаев С.Н., Ефимов О.Н., Николаева Г.В., Белов М.Ю., Марченко Е. П., Скворцов А.Г., Воронина В.А. "Способ получения смеси олиготрифениламинов и 3-(4-бифенилил)-4-(4-третбутилфенил)- 5-(4-диметиламинофенил)-1,2,4-триазола в качестве материалов для электролюминесцентного устройства и электролюминесцентное устройство на их основе" Заявка на патент РФ N 97118798/04 от 20.11.97, положительное решение от 2.06.98].
Пример 1. Синтез 8-меркаптохинолинатов.
Бис(8-хинолинтиолато)цинк(II), Zn(MQ)2
В колбу емкостью 100 мл, снабженную магнитной мешалкой, капельной воронкой и обратным холодильником, помещали 4,03 г (0,022 моль) натриевой соли 8-меркаптохинолина и 35 мл метанола. Смесь нагревали в атмосфере аргона при перемешивании до полного растворения соли (температура смеси около 50oC). Затем к полученному раствору прибавляли по каплям раствор 1,36 г (0,01 моль) безводного хлорида цинка в 20 мл метанола. После окончания прибавления соли цинка реакционную смесь нагревали до 55-60oC в течение 20 мин, охлаждали до комнатной температуры и разбавляли равным объемом воды. Выпавший осадок отфильтровывали, промывали водой (2х20 мл), сушили в вакууме над безводным MgSO4. Получали 3,35 г комплекса. Выход 87,0% от теоретического (считая на хлорид цинка). Тпл =292-293oC.
Элементный анализ.
Найдено, %: C 55,80; H 3,21; N 7,52; S 16,62; Zn 17,05.
Брутто-формула C18H12N2S2Zn.
Вычислено, %: C 56,10; H 3,11; N 7,27; S 16,61; Zn 16,91.
ИК-спектр (таблетка KBr) приведен в таблице.
Бис(8-хинолинтиолато) кадмий (II), Cd(MQ)2
В колбу емкостью 100 мл, снабженную магнитной мешалкой, капельной воронкой и обратным холодильником, помещали 4,03 г (0,022 моль) натриевой соли 8-меркаптохинолина и 35 мл метанола. Смесь нагревали при перемешивании в атмосфере аргона до полного растворения соли (температура раствора около 50oC), после чего прибавляли по каплям раствор 3,44 г (0,01 моль) кадмий дибромид тетрагидрата в 15 мл метанола. Выпадал желтый осадок. Смесь перемешивали еще в течение 20 мин при 55-60oC, затем охлаждали до комнатной температуры и разбавляли равным объемом воды. Осадок отфильтровывали, промывали метанолом (2х20 мл), водой (2х20 мл), сушили в вакууме над безв. MgSO4. Получали 3,93 г комплекса. Выход 91% от теоретического (считая на соль кадмия). Тпл = 382-384oC.
Элементный анализ.
Найдено, %: C 49,80; H 3,01; N 6,41; S 14,27; Cd 26,36.
Брутто-формула C18H12N2S2Cd.
Вычислено, %: C 49,95; H 2,76; N 6,48; S 14,80; Cd 25,99.
ИК-спектр Cd(MQ)2 (таблетка KBr) приведен в таблице. Сходство с ИК-спектром Zn(MQ)2 подтверждает одинаковый состав органической части этих молекул.
Трис (8-хинолинтиолато) галлий (III), Ga(MQ)3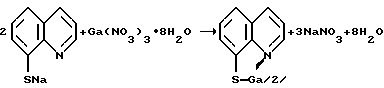
В колбу емкостью 100 мл, снабженную магнитной мешалкой, капельной воронкой и обратным холодильником, помещали 4,58 г (0,025 моль) натриевой соли 8-меркаптохинолина, растворенного в 100 мл 50%-ного водного этанола. Смесь нагревали до 35-40oC и прибавляли по каплям 2,8 г (0,007 моль) галлия нитрата октагидрата, растворенного в 15 мл воды. Затем смесь перемешивали в течение 1 часа при температуре 50-55oC. После этого смесь охлаждали до комнатной температуры, отфильтровывали осадок, промывали его последовательно эфиром (30 мл), метанолом (20 мл), водой (2х20 мл), сушили в вакууме над безв. MgSO4. Получали 3,63 г комплекса. Выход 94,3% от теоретического (считая на нитрат галлия). Тпл= 271-272oC.
Элементный анализ.
Найдено, %: C 58,10; H 3,73; N 7,29; S 17,34; Ga 13,12.
Брутто-формула C27H18N3S3Ga.
Вычислено, %: C 58,90; H 3,28; N 7,64; S 17,46; Ga 12,68.
ИК-спектр (таблетка KBr) приведен в таблице. Спектр Ga(MQ)3 близок к ИК-спектрам Zn(MQ)2 и Cd(MQ)2, хотя в ряде случаев наблюдается расщепление сильных полос поглощения, что согласуется с увеличением числа меркаптохинолинатных групп в составе этой молекулы.
Пример 2. Синтез смеси олигомеров трифениламина для дырочно-транспортного слоя.
Схема синтеза смеси олигомеров трифениламина (I)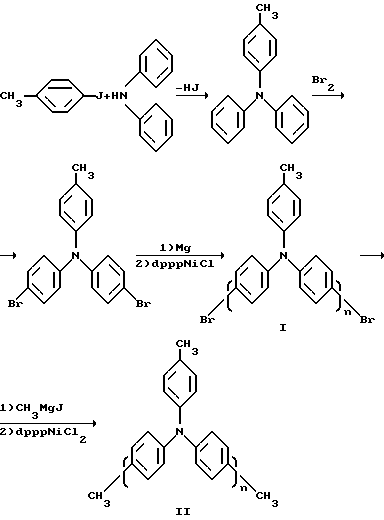
1) Синтез мономера.
4-Метилтрифениламин получали согласно известной методике.
Смесь 66,68г (30,6 моль) 4-иод-толуола, 43,94 г (0,26 моль) дифениламина, 41,4 г (0,30 моль) безводного K2CO3 и 2,0 г порошка меди нагревали в 75 мл нитробензола до кипения и при непрерывном перемешивании кипятили с обратным холодильником в течение 24 ч. По охлаждении реакционную массу отфильтровывали, осадок промывали 100 мл бензола. Из объединенного фильтрата перегонкой при пониженном давлении удаляли бензол, нитробензол, остатки 4-иодтолуола, а остаток перегоняли в вакууме, собирая фракцию, кипящую при 180-200oC / 3 мм рт. ст. По охлаждении вещество закристаллизовывалось. Его очищали хроматографированием на короткой колонке с Al2O3 элюент бензол : гексан (1: 1 об.), с последующей кристаллизацией из 90%-ной водной уксусной кислоты. Получили 47,2 г чистого вещества. Выход 70,1% от теоретического. Т. пл. 68,0oC (т. пл. 68,8oC ).
2) 4,4'-Дибpoм-(4''-метил)тpифенилaмин получали согласно известной методике.
К раствору 28,72 г (0,11 моль) 4-метилтрифениламина в 140 мл диэтилового эфира, охлажденному до -10oC, прибавляли малыми порциями в течение 2-х часов 55 г (0,22 моль) диоксандибромида при непрерывном перемешивании. Исходную температуру (-10oC) поддерживали весь период прибавления реагента и далее, до прекращения выделения газообразного HBr (всего 2,5-3 ч), после чего смесь нагрели до комнатной температуры и оставили на 24 ч. Затем реакционную смесь обрабатывали 20%-ным водным раствором NaOH (до pH 8-9 водной фазы). Выделившийся органический слой отделяли, промывая 5% водной уксусной кислотой, затем водой, затем отгоняли растворитель при пониженном давлении. Полученный кристаллический остаток очищали на короткой колонке с Al2O3, элюент бензолгексан (1: 4 объемн.), с последующей перекристаллизацией из 90%-ной водной уксусной кислоты. Получили 38,2 г продукта. Выход 82,6% от теоретического. Т.пл. 107oC.
Элементный анализ.
Найдено, %: C 57,37; H 3,69; Br 37,22.
C19H15NBr2.
Вычислено, %: C 57,71; H 3,62; Br 38,31.
3) Синтез олигомеров.
Олигомеризацию мономера [4,4'-дибром-(4''-метил)трифениламина] проводили согласно модифицированной методике [1].
Oлиго(4,4'-(4''-метил)тpифенилaмин (бромсодержащий), (I).
5,21 г (0,133 моль) металлического калия прибавляли небольшими кусочками к раствору 5,54 г (0,058 моль) MgCl2 безводного в 300 мл сухого ТГФ в атмосфере сухого аргона в течение 0,5 часа. Затем смесь кипятили с обратным холодильником при непрерывном перемешивании в течение 2-х часов (до образования мелкодисперсного металлического магния). Смесь охлаждали до комнатной температуры и в течение 0,5 ч прибавляли раствор 24,52 г (0,059 моль) 4,4'-дибром-(4''-метил)трифениламина в 50 мл сухого ТГФ. Смесь перемешивали при комнатной температуре в течение 3-х часов, затем добавляли 0,35 г катализатора ([1,3-бис(дифенилфосфино)пропан] никель(II)хлорида) (dpppNiCl). Смесь самопроизвольно нагревалась до кипения, которое затем поддерживали в течение еще 2 часов. По охлаждении к смеси осторожно прибавляли 10 мл этанола и спустя 0,5 часа реакционную смесь выливали в 1 л холодного этанола. Образовывался мелкий хлопьевидный осадок желтовато-коричневого цвета. Его отфильтровывали, промывали порциями 4х100 мл 2% соляной кислотой, затем водой до нейтральной реакции промывных вод, сушили в вакууме при 50oC. Получили 15,95 г неочищенного продукта. Его растворяли в 60 мл бензола, отфильтровывали от нерастворимого остатка, выливали в 350 мл гексана. Выпавший желтый осадок отфильтровывали, сушили в вакууме при 50oC. Получили 6,35 г продукта. Выход очищенного продукта 39% от теоретического. Т. пл. 183-187oC.
Элементный анализ.
Найдено, %: C 82,18; H 4,87; N 5,15; Br 7,03.
Брутто-формула (C18,6H13,2NBr0,24)n.
Вычислено, %: C 82,29; H 5,45; N 5,05; Br 7,20.
Для брутто-формулы (C19H15N)8Br2. Молекулярно-массовое распределение: Mn= 1812, Mw= 2802, полидисперсность Mn/Mw= 1,55. Температура стеклования (измерена на дифференциальном сканирующем калориметре DTAS-1300) равна 175oC.
4) Дебромирование олигомера (I).
Oлигo(4,4'-(4''-метил)тpифенилaмин (диметилзамещенный) (II).
К суспензии 4,13 г (0,17 моль) металлического магния в 60 мл сухого ТГФ прибавляли в атмосфере аргона и при непрерывном перемешивании 16,1г (0,11 моль) йодистого метила с такой скоростью, чтобы реакционная смесь спокойно кипела (время прибавления около 0,5 часа). К полученной массе прибавляли 0,15 г катализатора ([1,3-бис(дифенилфосфино)пропан] никель(II)хлорида) (dpppNiCl2) и раствор 6,0 г (около 0,003 моль) бромсодержащего олигомера (I) в 95 мл ТГФ. Реакционную смесь перемешивали при комнатной температуре в течение 24 ч, затем кипятили с обратным холодильником в течение еще 2 ч. По охлаждении реакционную массу осторожно выливали в 1,5 л 2% раствора соляной кислоты. Выпадал осадок светло-желтого цвета. Его промывали последовательно 2% раствором соляной кислоты, водой, гидроксидом аммония, водой, затем сушили в вакууме при 50oC. Получили 5,54 г сухого продукта. Очистка: полученный ранее продукт растворяли в 60 мл бензола и хроматографировали на короткой колонке с силикагелем (элюент-бензол). Собранный элюат концентрировали до объема около 40 мл и выливали при перемешивании в 100 мл гексана. Выпадал светло-желтый осадок. Его отфильтровывали, промывали гексаном, сушили в вакууме при 50oC. Получили 3,47 г вещества. Выход очищенного продукта 61,4% от теоретического. Температура плавления 206-210oC. Температура стеклования по методу дифференциального термического анализа 185oC.
Элементный анализ.
Найдено, %: C 88,47; H 5,71; N 5,83.
Для брутто-формулы (C17,7H13,6N)n.
Вычислено, %: C 88,56; H 6,08; N 5,36.
Для брутто-формулы (C19H15N)8(CH3)2. Молекулярно-массовое распределение: Mn= 2332 (около 9 звеньев), Mw=3586, полидисперсность Mw/Mn=1,54. УФ-спектр поглощения (раствор в хлороформе) 313, 372 нм.
Пример 3. Использование 8-меркаптохинолината цинка, Zn(MQ)2.
Максимум поглощения для напыленной пленки 420 нм. Максимум фотолюминесценции (порошок, возбуждающее излучение 440 нм) при 525 нм, полуширина спектра фотолюминесценции 58 нм. Квантовый выход фотолюминесценции, измеренный для раствора в этаноле около 3%.
Для изготовления электролюминесцентного устройства со структурой ITO/PTA/Zn(MQ)2/Mg: Ag, где ITO - дырочно-инжектирующий слой, PTA - дырочно-транспортный слой, Zn(MQ)2 - электролюминесцентный слой и Mg:Ag - электронно-инжектирующий слой, используют стеклянную подложку с полупрозрачным слоем смешанного оксида индия и олова с сопротивлением 20-25 Ом/квадрат, на которую методом центрифугирования из раствора в толуоле наносят слой PTA толщиной 0,05 - 0,1 мкм. Затем путем испарения Zn(MQ)2, полученного по примеру 1, в вакууме при температуре около 300oC и базовом давлении 5•10-6 мм рт.ст. наносят активный электролюминесцентный слой толщиной 0,02-0,05 мкм. Образец помещают в вакуумную установку ВУП-4, откачивают в динамическом режиме до вакуума 5•10-6 мм рт.ст. и напыляют металлический электрод путем испарения сплава, содержащего магний (90 мас.%) и серебро (10 мас.%). Толщина металлического электрода порядка 0,1 мкм.
Площадь светящейся поверхности 4-5 мм2. Полученное ЭЛУ обладает следующими параметрами: яркость 121 кд/м2 достигается при напряжении 14,1 B и плотности тока 24 мА/см2.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭЛЕКТРОЛЮМИНЕСЦЕНТНЫЙ МАТЕРИАЛ, СОДЕРЖАЩИЙ ОРГАНИЧЕСКОЕ ЛЮМИНЕСЦЕНТНОЕ ВЕЩЕСТВО | 1998 |
|
RU2140956C1 |
| ОРГАНИЧЕСКИЙ ЭЛЕКТРОЛЮМИНЕСЦЕНТНЫЙ МАТЕРИАЛ, ИЗЛУЧАЮЩИЙ В КРАСНОЙ ОБЛАСТИ СПЕКТРА | 1998 |
|
RU2155204C2 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕСИ ОЛИГОТРИФЕНИЛАМИНОВ, СПОСОБ ПОЛУЧЕНИЯ 3-(4-БИФЕНИЛИЛ)-4- (4-ТРЕТ-БУТИЛФЕНИЛ)-5-(4-ДИМЕТИЛАМИНОФЕНИЛ)-1,2,4-ТРИАЗОЛА И ЭЛЕКТРОЛЮМИНЕСЦЕНТНОЕ УСТРОЙСТВО | 1997 |
|
RU2131411C1 |
| ЭЛЕКТРОЛЮМИНЕСЦЕНТНЫЙ МАТЕРИАЛ, СОДЕРЖАЩИЙ ОРГАНИЧЕСКОЕ ЛЮМИНЕСЦЕНТНОЕ ВЕЩЕСТВО | 2004 |
|
RU2265040C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИ(2-МЕТОКСИ-5-(2'-ЭТИЛГЕКСИЛОКСИ)-1,4-ФЕНИЛЕНВИНИЛЕНА), ЭЛЕКТРОЛЮМИНЕСЦЕНТНОЕ УСТРОЙСТВО И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 1999 |
|
RU2186821C2 |
| ЭЛЕКТРОЛЮМИНЕСЦЕНТНЫЙ МАТЕРИАЛ, СОДЕРЖАЩИЙ ОРГАНИЧЕСКОЕ ЛЮМИНЕСЦЕНТНОЕ ВЕЩЕСТВО | 2006 |
|
RU2310676C1 |
| ЭЛЕКТРОЛЮМИНЕСЦЕНТНЫЙ МАТЕРИАЛ, СОДЕРЖАЩИЙ ОРГАНИЧЕСКОЕ ЛЮМИНЕСЦЕНТНОЕ ВЕЩЕСТВО | 2007 |
|
RU2368641C2 |
| ПОЛУПРОВОДНИКОВЫЙ ЭЛЕКТРОЛЮМИНЕСЦЕНТНЫЙ ИСТОЧНИК СВЕТА С ПЕРЕСТРАИВАЕМЫМ ЦВЕТОМ СВЕЧЕНИЯ | 2001 |
|
RU2202843C2 |
| ОРГАНИЧЕСКОЕ ЛЮМИНЕСЦЕНТНОЕ ВЕЩЕСТВО НА ОСНОВЕ ПРОИЗВОДНЫХ ПИРЕНА И ЭЛЕКТРОЛЮМИНЕСЦЕНТНОЕ УСТРОЙСТВО, СОДЕРЖАЩЕЕ ЭТО ВЕЩЕСТВО | 2013 |
|
RU2572414C2 |
| СОПРЯЖЕННЫЙ ПОЛИМЕР НА ОСНОВЕ КАРБАЗОЛА И ЦИКЛОПЕНТАДИТИОФЕНА И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЭЛЕКТРОЛЮМИНЕСЦЕНТНОГО МАТЕРИАЛА В ОРГАНИЧЕСКИХ СВЕТОИЗЛУЧАЮЩИХ ДИОДАХ | 2013 |
|
RU2568489C2 |
Изобретение относится к электролюминесцентным материалам, содержащим органическое люминесцентное вещество. Описывается новый электролюминесцентный материал, состоящий из электронного инжектирующего слоя, активного люминесцентного слоя на основе хелатного комплекса металла 2В или 3А группы Периодической системы, дырочно-транспортного слоя и дырочно-инжектирующего слоя. В качестве люминесцентного слоя содержит комплекс производного 8-меркаптохинолина общей формулы I, где n = 2-3, М = Zn, Сd, Ga; R1-R6 независимо друг от друга Н, метил; R3, R4 независимо друг от друга фенил, незамещенный или замещенный метилом, трет.бутилом; R3-R5 независимо друг от друга метоксигруппа, этоксигруппа, диметиламиногруппа, диэтиламиногруппа, нитрил. Технический результат - создание электролюминесцентного материала с излучением в зеленой области спектра, меньшей чувствительностью к влаге и с повышенной термостабильностью. 2 з.п. ф-лы, 1 табл.

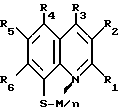
где n = 2 - 3;
M - Zn, Cd, Ga;
R1 - R6 - независимо друг от друга H, метил;
R3, R4 - независимо друг от друга фенил, незамещенный или замещенный метилом, трет.бутилом;
R3 - R5 - независимо друг от друга метоксигруппа, этоксигруппа, диметиламиногруппа, диэтиламиногруппа, нитрил.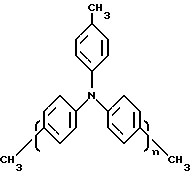
где n = 8 - 9,
при молекулярно-массовом распределении: Mn = 2332, Mw = 3586.
| Y.Hamada et al, Japanese Journal of Applied Physics, P | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ образования коричневых окрасок на волокне из кашу кубической и подобных производных кашевого ряда | 1922 |
|
SU32A1 |
| Способ и прибор для электролитической очистки серной кислоты от мышьяка | 1922 |
|
SU1514A1 |
| C.W.Tang et al | |||
| Appl | |||
| Phys | |||
| Letter, v | |||
| Способ запрессовки не выдержавших гидравлической пробы отливок | 1923 |
|
SU51A1 |
| Плавучий цепной ветро-водяной двигатель | 1923 |
|
SU913A1 |
| RU 94020885 A1, 1997 | |||
| Электролюминсцентная ячейка | 1973 |
|
SU469225A1 |
| Электролюминесцентная структура | 1982 |
|
SU1327810A3 |
Авторы
Даты
1999-09-20—Публикация
1998-05-07—Подача