Изобретение относится к производным N-(3- аминопропил)-N-фенил-5,6,7,8-тетрагидронафталин-2-карбоксамида, их получению и применению в терапевтической практике.
Согласно изобретению предложены производные N-(3-аминопропил)-N- фенил-5,6,7,8-тетрагидронафталин-2-карбоксамида общей формулы (I)
возможно в форме чистого оптического изомера либо смеси таких изомеров,
где R1 является атомом водорода или галогена, метильной группой или C1-C4 алкокси группой,
R1' является атомом водорода или галогена,
R1'' является атомом водорода или метокси группой,
R3 отдельно является C1-C3 алкильной группой,
R4 отдельно является 2,3-дигидро-1H-инден-2-ил группой, 2,3-дигидро-1H-инден-1-ил группой или 1,2,3,4-тетрагидронафталин- 1-ил группой, либо альтернативно
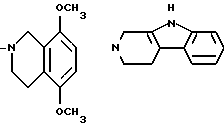
R3 и R4 вместе, и с несущим их атомом азота, образуют 1,2,3,4-тетрагидроизохинол-2-ил группу, 6,7-диметокси-1,2,3, 4-тетрагидроизохинол-2-ил группу, 5,8-диметокси-1,2,3,4- тетрагидроизохинол-2-ил группу, 1,2,3,4-тетрагидро-9H- пиридо[3,4-b] индол-2-ил гриппу, 1,2,3,4-тетрагидро-9H-пиридо[4,3- b] индол-3-ил гриппу, 4, 5, 6, 7-тетрагидротиено [2, 3-c] -пирид-6-ил группу, 2,3-дигидро-1H-изоиндол-2-ил группу или 2,3,4,5- тетрагидро-1H-3-бензазепин-3-ил группу, соответствующие формулы которых имеют вид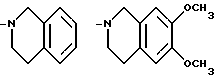
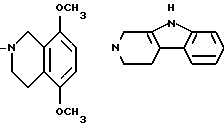
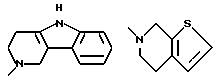
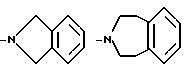
за исключением соединений, в которых R1 является алкоксигруппой, R1' и R1'' каждый является водородом, а R3 и R4 вместе с атомом азота являются замещенной или незамещенной 1,2,3,4- тетрагидроизохинолин-2-ил группой,
в форме основания или соли, полученной присоединением кислоты.
Предпочтительны соединения, в которых
R1 является атомом галогена,
R1' является атомом водорода или галогена,
R1'' является атомом водорода,
R3 отдельно является C1-C3 алкильной группой,
R4 отдельно является 2,3-дигидро-1H-инден-2-ил группой, 2,3-дигидро-1H-инден-1-ил группой или 1,2,3,4-тетрагидронафталин-1-ил группой, либо альтернативно
R3 и R4 вместе, и с несущим их атомом азота, образуют 1,2,3,4-тетрагидроизохинол-2-ил группу, 6, 7-диметокси-1,2,3,4-тетрагидроизохинол-2-ил группу или 5, 8-диметокси-1,2,3,4-тетрагидроизохинол-2-ил группу.
Среди указанных соединений наиболее предпочтительными являются N-[3-[(2,3-дигидро-1H-инден-2-ил) метиламино] пропил] - N-(3,4-дихлорфенил)-5,6,7,8-тетрагидронафталин-2-карбоксамид в форме основания или соли, полученной присоединением кислоты;
N-[3-[(2,3-дигидро-1Н-инден-1-ил)метиламино] пропил]-N- (3,4-дихлорфенил)-5,6,7,8-тетрагидронафталин-2-карбоксамид в форме чистого оптического изомера или смеси таких изомеров и в форме основания или соли, полученной присоединением кислоты; и
N-[3-[(1,2,3,4-тетрагидронафталин-1-ил) метиламино] пропил] -N-(3,4-дихлорфенил)-5,6,7,8-тетрагидронафталин-2-карбоксамид в форме чистого оптического изомера или смеси таких изомеров и в форме основания или соли, полученной присоединением кислоты.
Согласно изобретению предложен также способ получения указанных производных N-(3-аминопропил)-N-фенил-5,6,7,8- тетрагидронафталин-2-карбоксамида формулы (I), при котором бензоламин общей формулы (II)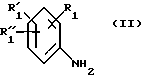
в которой R1, R1' и R1'' такие, как определено выше, подвергают взаимодействию с метиловым эфиром 5,6,7,8-тетрагидронафталин-2-карбоновой кислоты формулы (III)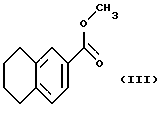
с образованием амида общей формулы (IV)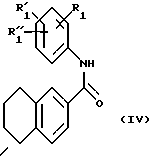
который затем подвергают взаимодействию с 1-бром-3-хлор- пропаном формулы (V)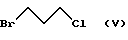
с образованием хлорпроизводного общей формулы (VI), которое, наконец, подвергают взаимодействию с амином общей формулы HNR3R4, в которой R3 и R4 такие, как определено выше.
Согласно данному изобретению предложена также фармацевтическая композиция, проявляющая антиишемическую активность, включающая активное вещество и эксципиент, отличающаяся тем, что в качестве активного вещества она содержит соединение по пп. 1-5 в количестве 1-1000 мг.
Соединения по изобретению могут существовать в форме оснований либо солей, полученных в результате присоединения кислот.
Кроме того, в случае, когда R4 содержит асимметричный атом углерода, то есть R4 является 2,3-дигидро-1H-инден-1-ил группой или 1,2,3,4-тетрагидронафталин-1-ил группой, соединения могут существовать в форме чистых оптических изомеров или смесей таких изомеров.
Соединения, отвечающие общей формуле (I), могут быть получены в результате реакции, описываемой следующей схемой:
Бензоламин общей формулы (II), в которой R1, R1' и R1'' определены ранее, подвергают взаимодействию с метиловым эфиром 5,6,7,8-тетрагидронафталин-2-карбоновой кислоты формулы (III), например в присутствии гидрида натрия и в растворителе, таком как диметилсульфоксид. В результате получают амид общей формулы (IV), который затем подвергают взаимодействию с 1-бром-3-хлорпропаном формулы (V), например в присутствии гидрида натрия и в растворителе, таком как N,N-диметилформамид.
В результате получают хлорпроизводное общей формулы (VI), которое, наконец, подвергают взаимодействию с амином общей формулы HNR3R4 в которой R3 и R4 такие, как определены выше, например в присутствии иодида калия и основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид.
Бензоламины общей формулы (II) имеются в продаже и описаны в литературе, например в заявках ЕР-0144730 и ЕР-0300865, либо могут быть получены способами, описанными в литературе или известными специалистам.
Метиловый эфир 5,6,7,8-тетрагидронафталин-2-карбоновой кислоты описан в J. Amer. Chem. Soc. (1943), 65, 1097.
Амины общей формулы (VII), в которой R4 является 2,3-дигидро- 1Н-инден-2-ил группой, описаны в J. Med. Chem. (1980), 23, 745.
Амины общей формулы (VII), в которой R4 является 2,3-дигидро- 1Н-инден-1-ил группой, описаны в J. Amer. Chem. Soc. (1966), 88, 2233.
Амины общей формулы (VII), в которой R4 является 1,2,3,4- тетрагидронафталин-1-ил группой, описаны в J. Amer. Chem. Soc. (1960), 82, 459, в C. R. Hebd. Seances Acad. Sci. Ser. C. (1969), 268, 2225 и в J. Med. Chem. (1966), 9, 830.
1,2,3,4-тетрагидроизохинол-2-илы, соответствующие общей формуле (VII), имеются в продаже либо описаны в литературе.
1, 2, 3, 4-тетрагидро-9Н-пиридо[3,4-b]индол, соответствующий общей формуле (VII), описан в Organic Synthesis (1971), 51, 136.
1,2,3,4-тетрагидро-9Н-пиридо[4,3-b] индол, соответствующий общей формуле (VII), описан в J. Chem. Soc. (1968), 1235.
4,5,6,7-тетрагидротиено [2, 3-c]пиридин, соответствующий общей формуле (VII), описан в Arkiv. Kemi (1970), 13 (19), 217.
2,3-дигидро-1H-изоиндол, соответствующий общей формуле (VII), описан в Organic Synthesis Coil. (1973), 5, 406.
2,3,4,5-тетрагидро-1H-3-бензазепин, соответствующий общей формуле (VII), описан в Helv. Chim. Acta (1935), 18, 1388.
Следующие примеры детально иллюстрируют получение нескольких соединений согласно изобретению.
Элементные микроанализы и ИК и ЯМР спектры подтверждают структуры полученных соединений.
Номера, приводимые в круглых скобках в заголовках примеров, соответствуют номерам в 1-ой колонке приводимой ниже таблицы.
Пример 1 (Соединение N 2).
N-[3-[(2,3-дигидро-1H-инден-2-ил)метиламино] пропил] -N- (3,4-дихлорфенил)-5,6,7,8-тетрагидронафталин-2-карбоксамида этандиоат (1:1) и (E)-2-бутендиоат (1:1).
1.1. N-(3,4- Дихлорфенил)-5,6,7,8-тетрагидронафталин-2-карбоксамид.
К суспензии 1,008 г (0,021 моль) гидрида натрия (при содержании 50% в масле) в 8 мл диметилсульфоксида в атмосфере аргона добавляют одну каплю метанола, смесь оставляют перемешиваться в течение 10 минут, а затем добавляют 1,94 г (0,012 моль) 3,4-дихлорбензоламина. Смесь перемешивают в течение 15 минут, затем 2,0 г (0,0105 моль) метилового эфира 5,6,7,8- тетрагидронафталина-2-карбоновой кислоты, растворенного в 8 мл диметилсульфоксида, добавляют по каплям, а затем перемешивание продолжается при комнатной температуре в течение 3 часов. Медленно добавляют 150 мл воды, 50 мл диэтилового эфира и 50 мл этилацетата, органическую фазу отделяют, промывают последовательно 50 мл воды и 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и фильтруют, а растворитель выпаривают.
Остаток кристаллизуют из смеси диэтилового эфира и гексана, получают при этом 2,09 г продукта, который используют на следующей стадии.
1.2. N-(3-Хлорпропил)-N-(3,4-дихлорфенил)-5,6,7,8-тетрагидронафталин- 2-карбоксамид.
К раствору 2,05 г (0,0064 моль) N-(3,4-дихлорфенил)-5,6, 7,8-тетрагидронафталин-2-карбоксамида в 1 1 мл N, N-диметилформамида в атмосфере азота медленно добавляют небольшими порциями 0,369 г (0,0077 моль) гидрида натрия в виде 50% суспензии в масле, смесь охлаждают до 0oC, по каплям добавляют 1,26 г (0,008 моль) 1-бром-3-хлорпропана, смесь оставляют нагреваться до комнатной температуры и перемешивают в течение 4 часов.
Смесь охлаждают, медленно добавляют 50 мл воды и 50 мл диэтилового эфира, фазы разделяют и экстрагируют водную фазу 50 мл диэтилового эфира. Органические фазы объединяют и последовательно промывают дважды 50 мл воды, 50 мл 1N соляной кислоты, дважды 50 мл воды и 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния, а растворитель выпаривают.
Получают 2,51 г продукта, который используют на следующей стадии.
1.3. N-[3-[(2,3-Дигидро-1H-инден-2-ил)метиламино]-пропил]- N-(3,4-дихлорфенил)-5,6,7,8- тетрагидронафталин-2-карбоксамида этандиоат (1: 1).
К раствору 2,45 г (0,0062 моль) М-(3-хлорпропил)-N-(3, 4- дихлорфенил)-5,6,7,8-тетрагидронафталина-2-карбоксамида в 9 мл N,N-диметилформамида в атмосфере аргона добавляют 1,71 г (0,0124 моль) карбоната калия и 1,03 г (0,0062 моль) иодида калия, а затем, через 5 минут, 1,14 г (0,0062 моль) N-метил-2,3-дигидро- 1H-инден-2-амина солянокислого, а смесь прогревают при 85oC в течение 4 часов.
Смесь охлаждают, добавляют 50 мл воды и 50 мл диэтилового эфира, фазы разделяют, а водную фазу экстрагируют дважды 50 мл диэтилового эфира. Органические фазы объединяют и промывают 50 мл насыщенного водного раствора хлорида натрия, а затем сушат над сульфатом магния, а растворитель выпаривают.
Получают 3,04 г маслянистого продукта, который затем очищают путем хроматографии на колонке с силикагелем, элюируя смесью 97/3 дихлорметан/метанол.
Получают 0,930 г чистого основания в виде масла.
Оксалат получают в 2-пропаноле путем добавления 0,165 г (0,0018 моль) щавелевой кислоты к 0,930 г (0,0018 моль) основания, продукт выделяют и перекристаллизовывают из этилацетата.
Окончательно получают 0,64 г оксалата в виде белых кристаллов.
Точка плавления: 140-141 oC.
1.4. N-[3-[(2,3-Дигидро-1H-инден-2-ил)метиламино] пропил] - N-(3,4-дихлорфенил)-5,6,7,8-тетрагидронафталин-2-карбоксамида (E)-2-бутендиоат (1:1).
Фумарат получают в смеси 2-пропанола и диизопропилового эфира путем добавления 1,05 г (0,009 моль) фумаровой кислоты к 4,58 г (0,009 моль) основания; соль выделяют и перекристаллизовывают из смеси 2-пропанола и диизопропилового эфира.
Окончательно получают 4,28 г фумарата в виде белых кристаллов. Точка плавления: 160-161oC.
Пример 2 (Соединение N 13).
N-(4-Хлорфенил)-N-[3-(6,7-диметокси-1,2,3,4-тетрагидроизохинолин-2-ил) пропил]-5,6,7,8-тетрагидронафталин-2-карбоксамида этандиоат.
2.1. N-(4-Хлорфенил)-5,6,7,8-тетрагидронафталин-2-карбоксамид.
К суспензии 0,912 г (0,019 моль) гидрида натрия (содержание - 50% в масле) в 7 мл диметилсульфоксида в атмосфере аргона добавляют одну каплю метанола, смесь подвергают перемешиванию в течение 10 минут и добавляют 1,40 г (0,011 моль) 4-хлорбензоламина. Смесь перемешивают в течение 15 минут, добавляют по каплям 1,8 г (0,0095 моль) метил-5,6,7,8-тетрагидронафталин- 2-карбоксилата, растворенного в 7 мл диметилсульфоксида, и перемешивают при комнатной температуре в течение 3 часов. Медленно добавляют 150 мл воды, 50 мл диэтилового эфира и 50 мл этилацетата, органическую фазу отделяют, промывают последовательно 50 мл воды и 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и фильтруют, а растворитель выпаривают.
Остаток кристаллизуют из диэтилового эфира и получают 1,96 г продукта, который используют на следующей стадии.
2.2. N-(4- Хлорфенил)-N-(3-хлорпропил)-5,6,7,8-тетpaгидронафталин-2-карбоксамид.
К раствору 1,92 г (0,0067 моль) N-(4-хлорфенил)-5,6,7,8- тетрагидронафталин-2-карбоксамида в 11 мл N,N-диметилформамида в атмосфере азота медленно добавляют небольшими порциями 0,384 г (0,0080 моль) гидрида натрия в виде 50% суспензии в масле, смесь охлаждают до 0 oC, по каплям добавляют 1,325 г (0,0084 моль) 1-бром-3-хлорпропана, смесь оставляют нагреваться до комнатной температуры и перемешивают в течение 4 часов.
Смесь охлаждают, медленно добавляют 50 мл воды и 50 мл диэтилового эфира, фазы разделяют и водную фазу экстрагируют 50 мл диэтилового эфира. Органические фазы объединяют и последовательно промывают дважды - 50 мл воды, 50 мл 1 N соляной кислоты, дважды - 50 мл воды и 50 мл насыщенного водного раствора хлорида натрия, затем сушат над сульфатом магния, а растворитель выпаривают.
Получают 2,29 г продукта, используемого на следующей стадии.
2.3. N-(4-Хлорфенил)-N-[3-(6,7-диметокси-1,2,3,4-тетрагидроизохинолин-2-ил)пропил]-5,6,7,8-тетрагидронафталин-2- карбоксамида этандиоат.
К раствору 2,29 г (0,0063 моль) N-(4-хлорфенил)-N-(3- хлорпропил)-5,6,7,8-тетрагидронафталин-2-карбоксамида в 9 мл N, N-диметилформамида в атмосфере аргона добавляют 1,738 г (0,0126 моль) карбоната калия (углекислого калия) и 1,04 г (0,0063 моль) иодида калия, а затем, спустя 5 минут, 1,45 г (0,0063 моль) солянокислого 6,7-диметокси-1,2,3,4-тетрагидроизохинолина, смесь прогревают при 85oC в течение 4 часов.
После остывания смеси к ней добавляют 50 мл воды и 50 мл диэтилового эфира, фазы разделяют и водную фазу экстрагируют дважды 50 мл диэтилового эфира. Органические фазы объединяют и промывают 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния, а растворитель выпаривают.
В результате получают 3,1 г маслянистого продукта, который чистят хроматографически на колонке с силикагелем, элюируя смесью 97/3 дихлорметан/метанол.
Получают 1,33 г чистого основания в виде масла.
Оксалат получают в 2-пропаноле путем добавления 0,230 г (0,0025 моль) щавелевой кислоты к 1,32 г (0,0025 моль) основания, продукт выделяют и перекристаллизовывают из 2- пропанола.
Окончательно получают 1,0 г оксалата в виде белых кристаллов. Точка плавления: 162-163oC.
Пример 3 (Соединение N 17).
N-[3-(6,7-Диметокси-1,2,3,4-тетрагидроизохинолин-2- ил)пропил]-N(4-метилфенил)-5,6,7,8-тетрагидронафталин-2-карбоксамида этандиоат.
3.1. N-(4-Метилфенил)-5, 6,7,8-тетрагидронафталин-2- карбоксамид.
К суспензии 0,912 г (0,019 моль) гидрида натрия (при содержании 50% в масле) в 7 мл диметилсульфоксида в атмосфере аргона добавляют одну каплю метанола, смесь перемешивают в течение 10 минут и добавляют 1,177 г (0,011 моль) 4-метилбензамина. Смесь перемешивают в течение 15 минут, добавляют по каплям 1,8 г (0,0095 моль) метил-5,6,7,8-тетрагидронафталин-2- карбоксилата, растворенного в 7 мл диметилсульфоксида, и продолжают перемешивание при комнатной температуре в течение 3 часов. Медленно добавляют 150 мл воды, 50 мл диэтилового эфира и 50 мл этилацетата, органическую фазу отделяют, промывают последовательно 50 мл воды и 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и фильтруют, растворитель выпаривают. Остаток кристаллизуют из диэтилового эфира и получают 1,43 г продукта, используемого на следующей стадии.
3.2. N-(3-Хлорпропил)-N-(4-метилфенил)-5,6,7,8-тетрагидронафталин- 2-карбоксамид.
К раствору 1,4 г (0,0053 моль) N-(4-метилфенил)-5,6,7,8-тетрагидронафталин-2-карбоксамида в 9 мл N,N-диметилформамида в атмосфере азота медленно добавляют, небольшими порциями, 0,307 г (0,0064 моль) гидрида натрия в виде 50% суспензии в масле, смесь охлаждают до 0 oC, по каплям добавляют 1,048 г (0,0066 моль) 1-бром-3-хлорпропана и после остывания до комнатной температуры смесь перемешивают в течение 4 часов.
Смесь охлаждают, медленно добавляют 50 мл воды и 50 мл диэтилового эфира, фазы разделяют и экстрагируют водную фазу 50 мл диэтилового эфира. Органические фазы объединяют и промывают последовательно дважды 50 мл воды, 50 мл 1N соляной кислоты, дважды 50 мл воды и 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния, растворитель выпаривают.
Получают 1,55 г продукта, используемого на следующей стадии.
3.3. N-[3-(6,7-Диметокси-1,2,3,4-тетрагидроизохинолин-2-ил) пропил]-N-(4-метилфенил)-5,6,7,8-тетрагидронафталин-2- карбоксамида этандиоат.
К раствору 1,55 г (0,0045 моль) N-(3-хлорпропил)-N-(4-метилфенил)- 5,6,7,8-тетрагидронафталин-2-карбоксамида в 7 мл N,N- диметилформамида в атмосфере аргона добавляют 1,24 г (0,009 моль) углекислого калия и 0,747 г (0,0045 моль) иодида калия, а затем, спустя 5 минут, добавляют 1,03 г (0,0045 моль) соляно- кислого 6,7-диметокси-1,2,3,4-тетрагидроизохинолина, смесь прогревают при 85oC в течение 4 часов.
После охлаждения к смеси добавляют 50 мл воды и 50 мл диэтилового эфира, фазы разделяют, водную фазу экстрагируют дважды 50 мл диэтилового эфира. Органические фазы объединяют и промывают 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния, а растворитель выпаривают.
Получают 2,07 г маслянистого продукта, который очищают хроматографически на колонке с силикагелем, элюируя смесью 97/3 дихлорметан/метанол.
Получают 0,920 г чистого основания в виде масла.
Оксалат получают в 2-пропаноле путем добавления 0,162 г (0,0018 моль) щавелевой кислоты к 0,9 г (0,0018 моль) основания, продукт выделяют и перекристаллизовывают из 2-пропанола.
Окончательно получают 0,797 г оксалата в виде белых кристаллов.
Точка плавления: 159-160oC.
Пример 4 (Соединение N 26).
N-[4-(2-Метилпропокси)фенил] -N-[3-(1,2,3,4-тетрагидро-9Н- пиридо[4,3-b] индол-3-ил) пропил]-5,6,7,8-тетрагидронафталин-2-карбоксамида этандиоат.
4.1. N-[4-(2-Метилпропокси) фенил]ацетамид.
К раствору 23 г (0,15 моль) N-(4-гидроксифенил) ацетамида в 124 мл N, N-диметилформамида добавляют 32,6 мл (0,3 моль) 1-бром-2-метилпропана и 31 г (0,225 моль) углекислого калия, смесь прогревают при 100oC в течение 5 часов.
Смесь охлаждают, растворитель выпаривают) а остаток собирают в 400 мл диэтилового эфира и 200 мл 1N гидроксида натрия. Органическую фазу отделяют и промывают последовательно три раза 50 мл 1N гидроксида натрия, три раза 100 мл воды и 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и фильтруют, растворитель выпаривают.
Получают 30,96 г продукта, используемого на следующей стадии.
4.2. 4-(2-Метилпропокси) бензоламин.
К раствору 30,35 г (0,146 моль) М-[4-(2-метилпропокси) фенил]ацетамида в 157 мл этанола добавляют 41,5 мл (0,309 моль) 30%-ного гидроксида натрия, смесь прогревают в сосуде с обратным холодильником в течение 5 часов.
Растворитель выпаривают, а остаток собирают в 400 мл диэтилового эфира и 350 мл воды. Органическую фазу отделяют и промывают последовательно три раза 100 мл воды и 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и фильтруют, растворитель выпаривают.
Получают 23,64 г продукта, который затем чистят хроматографически на колонке с силикагелем, элюируя 7/3 смесью циклогексан/этилацетат.
Получают 22,43 г продукта.
4.3. N-[4- (2-Метилпропокси)фенил] -5,6,7,8-тетрагидронафталин-2-карбоксамид.
К суспензии 1,25 г (0,026 моль) гидрида натрия (содержание 50% в масле) в 10 мл диметилсульфоксида в атмосфере аргона добавляют одну каплю метанола, смесь перемешивают в течение 10 минут и добавляют 2,6 г (0,015 моль) 4-(2-метилпропокси)бензоламина. Смесь перемешивают в течение 15 минут, добавляют по каплям 2,5 г (0,013 моль) метил-5,6,7,8-тетрагидронафталина-2-карбоксилата, растворенного в 10 мл диметилсульфоксида, и продолжают перемешивание при комнатной температуре в течение 3 часов. Медленно добавляют 200 мл воды, 100 мл диэтилового эфира и 100 мл этилацетата, органическую фазу отделяют и промывают последовательно 100 мл воды, 100 мл 1N соляной кислоты, дважды 50 мл воды и 100 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и фильтруют, растворитель выпаривают.
Остаток кристаллизуют из смеси диэтилового эфира и гексана, получают 3,10 г продукта, используемого на следующей стадии.
4.4. N-(3-Хлорпропил)-N-[4-(2-метилпропокси)фенил]-5,6, 7,8-тетpaгидронафталин-2-карбоксамид.
К раствору 2,5 г (0,008 моль) N-[4-(2-метилпропокси)фенил]- 5,6,7,8-тетрагидронафталин-2-карбоксамида в 13 мл N,N-диметилформамида в атмосфере азота медленно добавляют небольшими порциями 0,5 г (0,010 моль) гидрида натрия в виде 50% суспензии в масле, смесь охлаждают до 0oC, по каплям добавляют 1,6 г (0,010 моль) 1-бром-3-хлорпропана и после нагрева до комнатной температуры продолжают перемешивание в течение 4 часов.
Смесь охлаждают, медленно добавляют 100 мл воды и 100 мл диэтилового эфира, фазы разделяют, а водную фазу экстрагируют 100 мл диэтилового эфира. Органические фазы объединяют и промывают последовательно дважды 50 мл воды, 50 мл 1N соляной кислоты, дважды 50 мл воды и 50 мл насыщенного водного раствора хлорида натрия и сушат над сульфатом магния, растворитель выпаривают.
Получают 3,13 г продукта, используемого на следующей стадии.
4.5. N-[4-(2-Метилпропокси)фенил] -N-[3-(1,2,3,4-тетрагидро- 9H-пиридо[4,3-b] индол-3-ил) пропил] -5,6,7,8- тетрагидронафталин-2-карбоксамида этандиоат.
К раствору 3,13 г (0,008 моль) N-(3-хлорпропил)-N-[4-(2- метилпропокси)фенил] -5,6,7,8-тетрагидронафталин-2- карбоксамида в 11 мл N,N-диметилформамида в атмосфере аргона добавляют 2,21 г (0,016 моль) углекислого калия и 1,33 г (0,008 моль) иодида калия, а затем, спустя 5 минут, добавляют 1,67 г (0,008 моль) солянокислого 1,2,3,4-тетрагидро-9H-пиридо[4,3- b] индола и прогревают смесь при 85oC в течение 4 часов.
После охлаждения к смеси добавляют 100 мл воды и 100 мл диэтилового эфира, фазы разделяют и водную фазу экстрагируют дважды 50 мл диэтилового эфира. Органические фазы объединяют и промывают 100 мл насыщенного водного раствора хлорида натрия и сушат над сульфатом магния, растворитель выпаривают.
Получают 4,29 г маслянистого продукта, который подвергают хроматографической очистке на колонке с силикагелем, элюируя 95/5 смесью дихлорметан/метанол.
Получают 1,63 г чистого основания в виде масла.
Оксалат получают в 2-пропаноле путем добавления 0,221 г (0,0025 моль) щавелевой кислоты к 1,32 г (0,0025 моль) основания, продукт выделяют и перекристаллизовывают из 2-пропанола.
Окончательно получают 1,0 г оксалата в виде белых кристаллов.
Точка плавления: 121-122oC.
Пример 5 (Соединение N 20).
N-(4-Метоксифенил)-N-[3-(1,2,3,4-тетрагидро-9H-пиридо [3, 4-b] индол-2-ил)-пропил]-5,6,7,8-тетрагидронафталин -2- карбоксамида этандиоат.
5.1. N-(4-Метоксифенил)-5,6,7,8 - тетрагидронафталин-2-карбоксамид.
К суспензии 1,25 г (0,026 моль) гидрида натрия (содержание в масле - 50%) в 10 мл диметилсульфоксида в атмосфере аргона добавляют одну каплю метанола, смесь перемешивают 10 минут и добавляют 1,92 г (0,015 моль) 4-метоксибензоламина. Смесь перемешивают 15 минут, по каплям добавляют 2,5 г (0,013 моль) метил-5,6,7,8- тетрагидронафталин-2-карбоксилата, растворенного в 10 мл диметилсульфоксида и продолжают перемешивание при комнатной температуре в течение 3 часов. Медленно добавляют 200 мл воды, 100 мл диэтилового эфира и 100 мл этилацетата, органическую фазу отделяют и промывают последовательно 100 мл воды, 100 мл 1N соляной кислоты, дважды 50 мл воды и 100 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и фильтруют, а растворитель выпаривают.
Получают 3,34 г остатка, этот остаток кристаллизуют из смеси диэтилового эфира и гексана.
Получают 2,69 г продукта, используемого на следующей стадии.
5.2. N-(3-Хлорпропил)-N-(4-метоксифенил)-5,6,7,8-тетрагидронафталин- 2-карбоксамид.
К раствору 2,47 г (0,0088 моль) N-(4- метоксифенил)-5,6,7,8- тетрагидронафталин-2-карбоксамида в 14 мл N,N-диметилформамида в атмосфере азота медленно добавляют небольшими порциями 0,506 г (0,0105 моль) гидрида натрия в виде 50% масляной суспензии, смесь охлаждают до 0oC, по каплям добавляют 1,73 г (0,011 моль) 1- бром-3-хлорпропана, после возвращения температуры смеси к комнатной продолжают перемешивание в течение 4 часов. Смесь охлаждают, медленно добавляют 100 мл воды и 100 мл диэтилового эфира, фазы разделяют, водную фазу экстрагируют 100 мл диэтилового эфира. Органические фазы объединяют и промывают последовательно дважды 50 мл воды, 50 мл 1N соляной кислоты, дважды 50 мл воды и 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и выпаривают растворитель.
Получают 3,11 г продукта, используемого на следующей стадии.
5.3. N-(4-Метоксифенил)-N-[3 -(1,2,3,4-тетрагидро-9H-пиридо[3,4-b] индол-2-ил) пропил]-5,6,7,8-тетрагидронафталин-2- карбоксамида этандиоат.
К раствору 2,28 г (0,0064 моль) N-(3-хлорпропил)-N-(4-метоксифенил) -5,6,7,8-тетрагидронафталин-2-карбоксамида в 8 мл N,N-диметилформамида в атмосфере аргона добавляют 1,76 г (0,0128 моль) углекислого калия и 1,06 г (0,0064 моль) иодида калия, а затем, спустя 5 минут, 1,1 г (0,0064 моль) солянокислого 1,2,3,4-тетрагидро-9H-пиридо[3,4-b] индола и прогревают смесь в течение 4 часов при 85oC.
После остывания к смеси добавляют 100 мл воды и 100 мл диэтилового эфира, фазы разделяют, водную фазу экстрагируют дважды 50 мл диэтилового эфира. Органические фазы объединяют и промывают 100 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния, а растворитель выпаривают.
Получают 2,66 г маслянистого продукта, очищают его хроматографически на колонке с силикагелем, элюируя 97/3 смесью дихлорметан/метанол.
Получают 0,930 г чистого основания в виде масла.
Оксалат получают в 2-пропаноле путем добавления 0,170 г (0,0019 моль) щавелевой кислоты к 0,930 г (0,0019 моль) основания, продукт выделяют и перекристаллизовывают из 2-пропанола.
Окончательно получают 0,515 г оксалата в виде белых кристаллов.
Точка плавления: 245 oC.
Пример 6 (Соединение N 28).
N-(4-Хлорфенил)-N-[3-(2,3,4,5-тетрагидро-1 H-3-бензазепин-3- ил)пропил] -5,6,7,8-тетрагидронафталин-2-карбоксамида этандиоат.
6.1. N-(4-Хлорфенил)-5,6,7,8-тетpaгидронафталин-2-карбоксамид.
К суспензии 0,912 г (0,019 моль) гидрида натрия (содержание в масле - 50%) в 7 мл диметилсульфоксида в атмосфере аргона добавляют одну каплю метанола, смесь перемешивают 10 минут и добавляют 1,40 г (0,011 моль) 4-хлорбензоламина. Смесь перемешивают в течение 15 минут, добавляют по каплям 1,8 г (0,0095 моль) метил-5,6,7,8-тетрагидронафталин-2-карбоксилата, растворенного в 7 мл диметилсульфоксида, и перемешивают смесь при комнатной температуре в течение 3 часов. Медленно добавляют 150 мл воды, 50 мл диэтилового эфира и 50 мл этилацетата, органическую фазу отделяют и промывают последовательно 50 мл воды и 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и фильтруют, а растворитель выпаривают.
Получают 2,5 г остатка, этот остаток кристаллизуют из диэтилового эфира.
Получают 1,96 г продукта, используемого на следующей стадии.
6.2. N-(4-Хлорфенил)-N-(3-хлорпропил)-5,6,7, 8-тетрагидронафталин- 2-карбоксамид.
К раствору 1,92 г (0,0067 моль) N-(4-хлорфенил)-5,6,7,8- тетрагидронафталин-2-карбоксамида в 11 мл N,N-диметилформамида в атмосфере азота медленно добавляют небольшими порциями 0,384 г (0,008 моль) гидрида натрия в виде 50%-ной суспензии в масле, смесь охлаждают до 0 oC, по каплям добавляют 1,325 г (0,0084 моль) 1-бром-3-хлорпропана, после возвращения температуры смеси к комнатной продолжают перемешивание в течение 4 часов. Смесь охлаждают, медленно добавляют 50 мл воды и 50 мл диэтилового эфира, фазы разделяют, а водную фазу экстрагируют 50 мл диэтилового эфира. Органические фазы объединяют и промывают последовательно дважды 50 мл воды, 50 мл 1N соляной кислоты, дважды 50 мл воды и 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния, а растворитель выпаривают.
Получают 2,29 г продукта, используемого на следующей стадии.
6.3. N-(4-Хлорфенил)-N-[3-(2,3,4,5-тетрагидро-1H-3- бензазепин-3-ил)пропил]-5,6,7,8-тетрагидронафталин-2- карбоксамида этандиоат.
К раствору 2,5 г (0,0069 моль) N-(4-хлорфенил)-N-(3- хлорпропил)-5,6,7,8-тетрагидронафталин-2-карбоксамида в 9 мл N, N-диметилформамида в атмосфере аргона добавляют 1,9 г (0,0138 моль) углекислого калия и 1,14 г (0,0069 моль) иодида калия, а затем, спустя 5 минут, добавляют 1,26 г (0,0069 моль) солянокислого 2,3,4,5-тетрагидро-1H-3-бензазепина и прогревают смесь при 85oC в течение 4 часов.
После охлаждения к смеси добавляют 50 мл воды и 50 мл диэтилового эфира, фазы разделяют и экстрагируют водную фазу дважды 50 мл диэтилового эфира. Органические фазы объединяют и промывают 50 мл насыщенного водного раствора хлорида натрия и сушат над сульфатом магния, а растворитель выпаривают.
Получают 3,04 г маслянистого продукта, который очищают хроматографически на колонке с силикагелем, элюируя 97/3 смесью дихлорметан/метанол.
Получают 1,18 г чистого основания в виде масла.
Оксалат получают в 2-пропаноле путем добавления 0,225 г (0,0025 моль) щавелевой кислоты к 1,18 г (0,0025 моль) основания, продукт выделяют и перекристаллизовывают из 2-пропанола.
Окончательно получают 1,04 г оксалата в виде белых кристаллов.
Точка плавления: 180oC.
Пример 7 (Соединение N 27).
N-(4-Хлорфенил)-N-[3-(4,5,6,7-тетрагидротиено-[2,3-c] пирид-6-ил)пропил] -5,6,7,8-тетpагидpoнафталин-2-карбоксамида этандиоат (1:1).
К раствору 2,37 г (0,0065 моль) N-(4-хлорфенил)-N-(3- хлорпропил)-5,6,7,8-тетрагидронафталин-2-карбоксамида в 10 мл N, N-диметилформамида в атмосфере аргона добавляют 2,69 г (0,0195 моль) углекислого калия и 1,1 г (0,0065 моль) иодида калия, а затем, спустя 5 минут, 1,49 г (0,0065 моль) 4,5,6,7- тетрагидротиено [2,3-c] пиридин оксалата и прогревают смесь при 85oC в течение 4 часов.
После остывания к смеси добавляют 50 мл воды и 50 мл диэтилового эфира, фазы разделяют и водную фазу экстрагируют дважды 50 мл диэтилового эфира. Органические фазы объединяют и промывают 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния, растворитель выпаривают.
Получают 3,0 г маслянистого продукта, который затем очищают хроматографически на колонке с силикагелем, элюируя 97/3 смесью дихлорметан/метанол.
Получают 1,16 г чистого основания в виде масла.
Оксалат получают в 2-пропаноле путем добавления 0,26 г (0,0022 моль) щавелевой кислоты к 1,16 г (0,0022 моль) основания, продукт выделяют и перекристаллизовывают из 2-пропанола.
Окончательно получают 1,09 г оксалата в виде белых кристаллов.
Точка плавления: 164-165oC.
Пример 8 (Соединение N 31).
N-(4-Хлорфенил)-N-[3-(2,3-дигидро-1H-изоиндол-2-ил) пропил] -5,6,7,8-тетрагидронафталин-2-карбоксамид (Е)-2-бутендиоат (1:1).
К раствору 2,0 г (0,0055 моль) N-(4-хлорфенил)-N-(3-хлорпропил)- 5,6,7,8-тетрагидронафталин-2-карбоксамида в 10 мл N,N- диметилформамида в атмосфере аргона добавляют 1,15 г (0,0083 моль) углекислого калия и 0,92 г (0,0055 моль) иодида калия, а затем, спустя 5 минут, 0,66 г (0,0055 моль) 2,3-дигидро-1H-изоиндола, смесь прогревают при 85oC в течение 4 часов.
После остывания в смесь добавляют 50 мл воды и 50 мл диэтилового эфира, фазы разделяют и экстрагируют водную фазу дважды 50 мл диэтилового эфира. Органические фазы объединяют и промывают 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния, растворитель выпаривают.
Получают 2,8 г маслянистого продукта, который очищают хроматографически на колонке с силикaгелем, элюируя 97/3 смесью дихлорметан/метанол.
Получают 0,82 г чистого основания в виде масла.
Фумарат получают в 2-пропаноле путем добавления 0,21 г (0,0018 моль) фумаровой кислоты к 0,82 г (0,0018 моль) основания, продукт выделяют и перекристаллизовывают из 2-пропанола.
Окончательно получают 0,43 г фумарата в виде белых кристаллов.
Точка плавления: 141-142 oC.
Пример 9 (Соединение N 44).
(±)-N-[3-[(2, З-Дигидро-1H-инден-1-ил)метиламино] - пропил]-N-(3,4-дихлорфенил) -5,6,7,8-тетpaгидронафталин-2- карбоксамида этандиоат (1:1).
К раствору 3 г (0,0075 моль) N-(3-хлорпропил)-N-(3,4-дихлорфенил)- 5,6,7,8-тетрагидронафталин-2-карбоксамида в 12 мл N,N- диметилформамида в атмосфере аргона добавляют 2,07 г (0,015 моль) углекислого калия и 1,25 г (0,0075 моль) иодида калия, а затем, после перемешивания в течение 5 минут, добавляют 1,37 г (0,0075 моль) солянокислого N-метил-2,3-дигидро-1H-инден-1-амина, смесь прогревают при 85oC в течение 3 часов 30 минут.
После остывания к смеси добавляют 50 мл воды и отделяют коричневый осадок посредством фильтрации, промывают водой и сушат.
Получают 3,58 г продукта, который очищают хроматографически на колонке с силикагелем, элюируя 96/4 смесью дихлорметан/метанол.
Получают 1,12 г чистого основания.
Для получения оксалата 0,73 г (0,0014 моль) основания и 0,13 г (0,0014 моль) щавелевой кислоты растворяют в 10 мл 2-пропанола, смесь нагревают с обратным холодильником до тех пор, пока материалы не растворятся, охлаждают, собирают белый осадок и перекристаллизовывают из 2-пропанола. После фильтрации и сушки окончательно получают 0,58 г оксалата.
Точка плавления: 142-143oC.
Пример 10 (Соединение N 45).
(±)-N-[3-[(1,2,3,4-Тетрагидронафталин-1-ил) метиламино] пропил] -N-(3,4-дихлорфенил)-5,6,7, 8-тетрагидронафталин-2- карбоксамида этандиоат (1: 1).
К раствору 3 г (0,0075 моль) N-(3-хлорпропил)-N-(3,4-дихлорфенил)- 5,6,7,8-тетрагидронафталин-2-карбоксамида в 12 мл N,N-диметилформамида в атмосфере аргона добавляют 2,07 г (0,015 моль) углекислого калия и 1,25 г (0,0075 моль) иодида калия, а затем, спустя 5 минут, добавляют 1,48 г (0,0075 моль) солянокислого N-метил-1,2,3,4-тетрагидронафталин-1-амина, смесь прогревают при 85oC в течение 3 часов 30 минут.
После остывания добавляют 50 мл воды и отделяют посредством фильтрации желтый осадок, промывают его водой и сушат.
Получают 4,32 г продукта, который очищают хроматографически на колонке с силикагелем, элюируя 96/4 смесью дихлорметан/метанол.
Получают 1,34 г чистого основания в виде масла.
Для получения оксалата 1,34 г (0,0026 моль) основания и 0,23 г (0,0026 моль) щавелевой кислоты растворяют в 15 мл 2-пропанола, смесь нагревают с обратным холодильником до полного растворения веществ и выпаривают растворитель. Остаток перекристаллизовывают из большого объема диизопропилового эфира и посредством фильтрации собирают белый осадок и сушат его. Окончательно получают 0,71 г оксалата.
Точка плавления: 116-117oC.
Приводимая ниже таблица иллюстрирует химические структуры и физические свойства нескольких соединений по изобретению. В колонке "соль" "-" обозначает соединение в форме основания, "окс." обозначает оксалат или этандиоат, "фум." обозначает фумарат или (Е)-2-бутендиоат, "цит." обозначает цитрат или 2-гидрокси- 1,2,3-пропантрикарбоксилат, а "мез. " обозначает мезотартрат или 2,3-дигидроксибутандиоат; соотношение, приводимое в круглых скобках, является молярным соотношением кислота: основание.
Соединения по изобретению подвергали различным испытаниям, которые продемонстрировали их терапевтическую перспективность.
Так, их испытывали в тесте на общую церебральную ишемию на мышах. Ишемия наступает из-за сердечной приостановки, вызванной быстрым внутривенным введением хлорида магния. В этом тесте измеряют "время выживания", представляющее собой интервал между моментом введения хлорида магния и последним наблюдавшимся дыхательным движением каждой мыши. Это последнее движение считают знаком окончания функционирования центральной нервной системы.
Остановка дыхания происходит приблизительно через 19 секунд после введения хлорида магния.
Изучали группы из 10 самцов мышей (Swiss OF1 IFFA CREDO). Перед тестами им давали свободный доступ к пище и воде. Время выживания измеряют через 10 минут после внутрибрюшинного введения соединений по изобретению. Результаты представляют в виде разницы между временем выживания, измеренным в группе из 10 мышей, которые получили соединение, и временем выживания, измеренным в группе из 10 мышей, которые получили растворитель. Соотношения между изменениями во времени выживания и дозами соединения представляют графически в виде полулогарифмической кривой.
Эта кривая позволяет вычислить "3-х секундную эффективную дозу" (ЭДз), обозначающую дозу (в мг/кг), которая обеспечивает 3- х секундное увеличение времени выживания относительно контрольной группы из 10 необработанных мышей.
Это 3-х секундное увеличение времени выживания является как статистически значимым, так и воспроизводимым.
ЭДз соединений по изобретению варьирует от 0,1 до 30 мг/кг при внутрибрюшинном введении.
Соединения по изобретению являлись также объектом изучения потенциал-зависимых ("вольтаж-зависимых") бариевых токов путем так называемой техники "пэтч-кламп".
Бариевые токи, идущие через потенциал-зависимые кальциевые каналы, измеряют на препаратах клеток коры головного мозга только что родившихся крысят (Sprague - Dawley) в культуре (культивировавшихся от 6 до 10 дней); в случае этих клеток, это составные токи, которые включают L, N и P каналы, как описано в Soc. Neurosci. Abstr. (1989), 15, 823.
Измеряющие ячейки, объемом 800 мкл, содержащие клетки коры головного мозга, помещают на столик Olympus 1ТМ - 2TM инвертированного микроскопа и наблюдают за клетками при увеличении 400х. Ячейки непрерывно перфузируются (4-5 мл/мин) с использованием устройства для распределения растворов, имеющего 9 входов (мертвый объем < 50 мкл), единственный выход которого, состоящий из полиэтиленовой трубки с отверстием 500 мкм, находится менее чем в 3 мм от изучаемой клетки. Преимуществом этого устройства является то, что оно позволяет быстро менять раствор на изучаемых клетках.
Используемый "пэтч-кламп" метод описан в Pfluegers Archives (1981), 391, 85-100. Axopatch - 1DTM усилитель, соединенный с компьютером типа AT 386-33 МГц с PCLAMPTM программным обеспечением Axon InstrumentsTM используют для стимуляции клеток, сбора данных и анализа результатов. Для регистрации бариевых токов пипетки из боросиликатного стекла закрепляют в непосредственной близости от клеток посредством Narishige WR 60TM гидравлического микроманипулятора. Концы пипеток заполнены соответствующим внутриклеточным раствором, имеющим следующий состав (в мМ): CsCI (140), CaCI2 (1) Na2ATФ (4), ЭДТА (11; pCa = 8), Hepes (10), Трис-OH (pH 7,2).
После того как получают так называемую конфигурацию "целая клетка", эту клетку перфузируют так называемым ТЕА- бариевым раствором, имеющим следующий состав: ТЕА-C1 (144), BaCI2 (5), MgCl2 (2), CsCI (3), глюкоза (10), Hepes (10), Трис-OH (pH 7,4).
Раствор делает возможным измерять кальциевый ток (аналогичный бариевому току, проходящему через потенциал-зависимые кальциевые каналы), тогда как в то же самое время он является независимым от натриевого и калиевого тока.
Общий потенциал-зависимый бариевый ток получают путем приложения деполяризующего потенциала длительностью 250 мс, переводящего мембранный потенциал с -80 до 0 мВ. Частота стимуляции составляет 0,25 Гц.
Соединения по изобретению растворяют в TEA-бариевой среде и наносят после того, как амплитуда бариевого тока стабилизируется. После получения стабильного ингибиторного эффекта клетку снова перфузируют контрольным ТЕА-бариевым раствором для того, чтобы наблюдать аннулирование эффекта.
Величина получаемого эффекта сравнима с величиной эффекта 100 мкМ кадмиевого раствора. Ингибирование потенциал-зависимого бариевого тока изменяется как функция доз исследуемых соединений и, для наиболее активных соединений, составляет порядка 49% при концентрации 1 мкМ и 83% при концентрации 10 мкМ.
Результаты тестов, проводившихся с соединениями по изобретению, показывают, что in vitro они обладают антагонистическими свойствами по отношению к нейронному кальцию, a in vivo они обладают нейрозащитными и антиишемическими свойствами.
Эти результаты подтверждают, что соединения могут быть использованы для лечения и профилактики церебральных нарушений, таких как, например, приступы ишемической болезни, остановка сердца или дыхания, церебральная эмболия или тромбоз, для лечения церебрального старения, слабоумия, следующего за множественными инфарктами, старческого слабоумия, например болезни Альцгеймера или болезни Пика, для лечения оливомостомозжечковой атрофии и других нейродегенеративных заболеваний, таких как хорея Гентингтона и амиотрофного латерального склероза, для лечения черепных или спинно-мозговых травм, для профилактики нейронных расстройств, наступающих после конвульсивных состояний, для лечения некоторых раков, для лечения неврологических расстройств, вызываемых СПИДом, и для профилактики и для лечения диабетических ретинопатий, дегенерации оптического нерва и ретинопатий, связанных с глаукомой, и в общем, для лечения любой патологии, связанной с дисфункцией гомеостаза нейронного кальция.
Таким образом, соединения могут использоваться во всех фармацевтических формах, приспособленных для энтерального или парэнтерального введения, в сочетании с соответствующими эксципиентами, например в форме таблеток, таблеток, покрытых сахаром, желатиновых капсул, капсул-облаток, суппозиториев, либо растворов или суспензий для питья или инъекций, которые дозированы таким образом, что позволяют вводить от 1 до 1000 мг активного вещества в сутки.
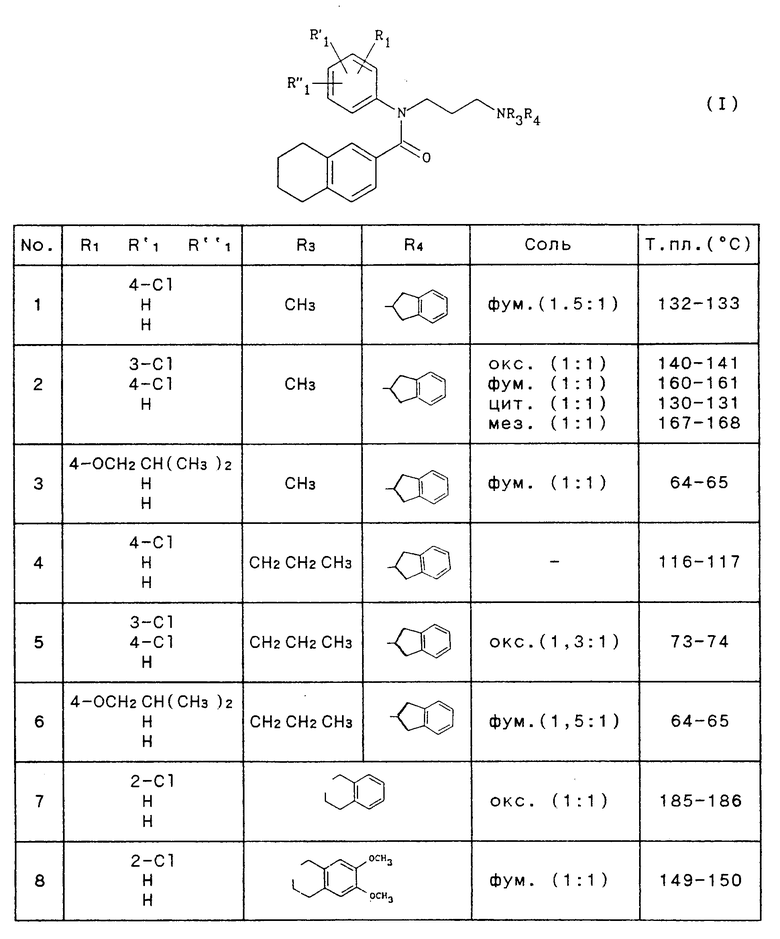



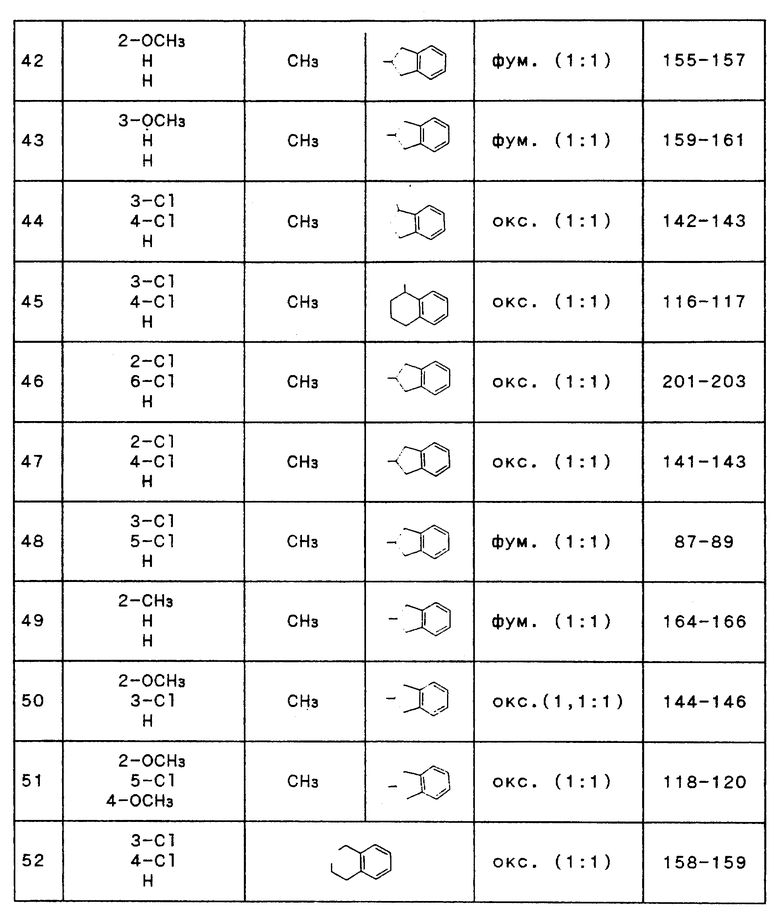
Производные N-(3-аминопропил)-N-фенил-5,6,7,8-тетрагидронафталин-2-карбоксмида формулы I, где R1 - атом водорода, галоген, метил или алокси, R'1 - водород, галоген, R''1 - Н или метокси, R3 - С1-3-алкил, R4 - 2,3-дигидро-1Н-инден-2-ил, 2,3-дигидро-1Н-инден-1-ил, 1,2,3,4-тетрагидронафталин-1ил-, либо R3 и R4 вместе с несущим атомом азота образуют 1,2,3,4-тетрагидроизохинолил, 6,7-диметокси-1,2,3,4-тетрагидроизохинолил (другие обозначения см. в п.1 ф-лы изобретения), в форме основания или соли, в форме чистого изомера либо смеси таких изомеров, проявляют антиишемическую активность. 6 с. и 1 з.п. ф-лы, 1 табл.

возможно в форме чистого оптического изомера либо смеси таких изомеров,
где R1 - атом водорода или галогена, метильная группа или С1-С4-алкоксигруппа;
R'1 - атом водорода или галогена;
R"1 - атом водорода или метоксигруппа;
R3 отдельно - С1-С3-алкильная группа;
R4 - отдельно - 2,3-дигидpo-IH-индeн-2-ил-гpуппа, 2,3-дигидро-1Н-инден-1-ил-группа или 1,2,3,4-тетрагидронафталин-1-ил-группа,
либо альтернативно R3 и R4 вместе с несущим их атомом азота образуют 1,2,3,4-тетрагидроизохинол-2-ил- группу, 6,7-диметокси-1,2,3,4- тетрагидроизохинол-2-ил-группу, 5,8-диметокси-1,2,3,4-тетрагидроизохинол-2-ил-группу, 1,2,3,4-тетрагидро-9Н-пиридо[3,4-b]инодол-2-ил-группу, 1,2, 3,4-тетрагидро-9Н-пиридо[4,3-b] индол-3-ил-группу, 4,5,6,7-тетрагидротиено[2,3-с] -пирид-6-ил-группу, 2,3-дигидро-1Н-изоиндол-2-ил-группу или 2,3,4,5-тетрагидро-1Н-бензазепин-3-ил-группу, соответствующие формулы которых имеют вид 
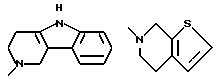
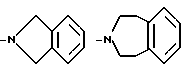
за исключением соединений, в которых R1 является алкоксигруппой, R'1 и R"1 каждый -, а R3 и R4 вместе с атомом азота являются замещенной или незамещенной 1,2,3,4-тетрагидроизохинолин-2-ил-группой, в форме основания или соли, полученной присоединением кислоты.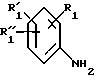
в которой R1, R'1 и R"1 определены в п.1,
подвергают взаимодействию с метиловым эфиром 5,6,7,8-тетрагидронафталин-2-карбоновой кислоты формулы III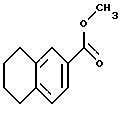
с образованием амида общей формулы IV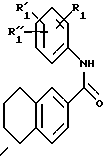
который затем подвергают взаимодействию с 1-бром-3-хлор-пропаном формулы (V)
с образованием хлорпроизводного общей формулы VI
которое подвергают взаимодействию с амином общей формулы HNR3R4, в которой R3 и R4 определены в п.1.
| СПОСОБ ПОЛУЧЕНИЯ Л/-МЕТИЛ-Я-[(р-АРОИЛАМИДО)-ЭТИЛ]--АНИЛИНОВ | 0 |
|
SU289084A1 |
| Способ получения производных 3,5-диметилбензойной кислоты | 1974 |
|
SU578862A3 |
| КРАНОВОЕ КОЛЕСО;.-•*', — '~v^4 .-*-\*-* 4 § л лл.:.-..,,с 1.,.^ -^.X^ClHA лi^-:im^rim^tmi;^;':Бл;->&отЕг"^? | 0 |
|
SU367040A1 |
| КЛАВИШНЫЙ ПЕРЕКЛЮЧАТЕЛЬ | 0 |
|
SU233762A1 |
| КОМБИНИРОВАННАЯ МАШИНА ДЛЯ ОДНОВРЕМЕННОГО ЛЕНТОЧНОГО ВНЕСЕНИЯ ГЕРБИЦИДОВ, ВЫСЕВА МИНЕРАЛЬНЫХ УДОБРЕНИЙ И ПОСЕВА | 0 |
|
SU352613A1 |
Авторы
Даты
1999-09-27—Публикация
1995-02-02—Подача