Настоящее изобретение относится к антагонистам эндотелина, применяемым (между прочим) для лечения гипертензии.
Соединение формулы I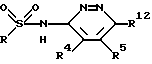
и их фармацевтически пригодные соли являются антагонистами рецептора эндотелина, применяемыми (между прочим) в качестве гипотензивных средств. На всем протяжении настоящего описания изобретения символы имеют следующие значения:
R представляет собой фенил, нафтил или дифенилил, каждый из которых может быть замещен радикалами R1, R2 и R3,
R1, R2 и R3 независимо друг от друга представляют собой
(a) водород,
(b) алкил, алкенил, алкинил, алкоксигруппу, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил, арилоксигруппы, аралкил или аралкоксигруппу, каждый из которых может быть замещен радикалами Z1, Z2 и Z3,
(c) галоген,
(d) гидроксигруппу,
(e) цианогруппу,
(f) нитрогруппу,
(q) C(O)H или C(O)R6,
(h) CO2H или CO2R6,
(i) SH, S/O/nR6, S/O/mOH, S/O/mOR6, OS/O/mR6, OS/O/mOH или OS/O/mOR6,
(j) Z4NR7R8 или
(k) Z4N(R11)Z5NR9R10,
R4, R5 и R12 независимо друг от друга представляют собой (a) водород,
(b) алкил, алкенил, алкинил, алкоксигруппу, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил, арилоксигруппу, аралкил или аралкоксигруппу, каждый из которых может быть замещен радикалом Z1, Z2 и Z3,
(c) галоген,
(d) гидроксигруппу,
(е) цианогруппу,
(f) нитрогруппу,
(g) C(O)H или C(O)R6,
(h) CO2H или CO2R6,
(i) SH, S(O)nR6, S(O)mOH, S(O)mOR6, OS(O)mR6, OS(O)mOH или OS(O)mOR6,
(j) Z4NR7R8,
(k) Z4N(R11)ZNR9R10 или
(l) R4 и R5 или R5 и R12 вместе образуют алкилен или алкенилен (каждый из них может быть замещен радикалом Z1, Z2 и Z3), замыкающий вместе с атомами углерода, к которым присоединены R4 и R5 или R5 и R12, 4-8-членное насыщенное, ненасыщенное или ароматическое ядро, причем, если R является фенилом, то по меньшей мере два из радикалов R4, R5 и R12 не являются водородом,
R6 представляет собой алкил, алкенил, алкинил, алкоксигруппу, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил или аралкил, каждый из которых может быть замещен радикалами Z1, Z2 и Z3,
R7 представляет собой
(a) водород,
(b) алкил, алкенил, алкинил, алкоксигруппу, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил или аралкил, каждый из которых может быть замещен радикалами Z1, Z2 и Z3,
(c) цианогруппу,
(q) гидроксигруппу,
(e) C(O)H или C(O)R6,
(f) CO2R6 или
(g) SH, S(O)nR6, S(O)mOR6, OS(O)mR6 или OS(O)mOR6, за исключением случая, когда Z4 является группой S(O)n,
R8 представляет собой
(a) водород,
(b) C(O)H или C(O)R6, за исключением случая, когда Z4 является группой C(O) и R7 является группой C(O)H, C(O)R6 или CO2R6, или
(c) алкил, алкенил, алкинил, алкоксигруппу, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил или аралкил, каждый из которых может быть замещен радикалами Z1, Z2 и Z3, или
R7 и R8 вместе образуют алкилен или алкенилен (каждый из них может быть замещен радикалами Z1, Z2 и Z3), замыкающий вместе с атомом азота, к которому присоединены R7 и R8, 3-8-членное насыщенное, ненасыщенное или ароматическое ядро,
R9 представляет собой
(a) водород,
(b) гидроксигруппу,
(c) C(O)H или C(O)R6,
(d) CO2R6,
(e) SH, S(O)nR6, S(O)mOR6, OS(O)mR6 или OS(O)mOR6 или
(f) алкил, алкенил, алкинил, алкоксигруппу, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил или аралкил, каждый из которых может быть замещен радикалами Z1, Z2 и Z3,
R10 представляет собой
(a) водород,
(b) C(O)H или C(O)R6, за исключением случая, когда Z5 является группой C(O) и R9 является группой C(O)H, C(O)R6 или CO2R6, или
(c) алкил, алкенил, алкинил, алкоксигруппу, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил или аралкил, каждый из которых может быть замещен радикалами Z1, Z2 и Z3,
R11 представляет собой
(a) водород,
(b) гидроксигруппу или CO2R6, за исключением случая, когда один из R9 и R10 является гидроксигруппой или CO2R6,
(c) C(O)H или C(O)R6 или
(d) алкил, алкенил, алкинил, алкоксигруппу, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил или аралкил, каждый из которых может быть замещен радикалами Z1, Z2 и Z3,
или два любых радикала из R9, R10 и R11 вместе образуют алкилен или алкенилен (каждый из них может быть замещен радикалами Z1, Z2 и Z3), замыкающий вместе с атомами, к которым они присоединены, 3-8-членное насыщенное, ненасыщенное или ароматическое ядро,
Z1, Z2 и Z3 представляют собой независимо друг от друга
(a) водород,
(b) галоген,
(c) гидроксигруппу,
(d) алкил, алкенил, аралкил, алкоксигруппу, арилоксигруппу или аралкоксигруппу,
(e) SH, S(O)nZ6, S(O)mOH, S(O)mOZ6, OS(O)mZ6, OS(O)mOH или OS(O)mOZ6,
(f) оксогруппу,
(g) нитрогруппу,
(h) цианогруппу,
(i) C(O)H или C(O)Z6,
(j) CO2H или CO2Z6 или
(k) Z4NZ7Z8, Z4N(Z11)Z5Z6 или Z4N(Z11)Z5NZ7Z8
Z4 и Z5 представляют собой независимо друг от друга
(a) прямую одинарную связь,
(b) Z9S(O)mZ10,
(c) Z9C(O)Z10,
(d) Z9C(S)Z10,
(e) Z9OZ10,
(f) Z9SZ10,
(g) Z9OC(O)Z10 или
(h) алкил, алкенил, алкинил, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил или аралкил, каждый из которых может быть замещен радикалами Z1, Z2 и Z3,
Z6, Z7 и Z8 представляют собой независимо друг от друга водород, алкил, алкенил, алкинил, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил или аралкил или Z7 и Z8 вместе образуют алкилен или алкенилен, который вместе с атомом азота, к которому присоединены Z7 и Z8, замыкает 3-8-членное насыщенное, ненасыщенное или ароматическое ядро, Z9 и Z10 представляют собой независимо друг от друга прямую одинарную связь, алкилен, алкенилен или алкинилен,
Z11 представляет собой
(a) водород,
(b) гидроксигруппу,
(c) C(O)H, C(O)Z6 или CO2Z6, причем, если Z11 является группой CO2Z6, то Z6 не может быть водородом, или
(d) алкил, алкенил, алкинил, алкоксигруппу, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил или аралкил,
или любые два из радикалов Z7, Z8 и Z11 вместе образуют алкилен или алкенилен, который вместе с атомами, к которым они присоединены, замыкает 3-8-членное насыщенное, ненасыщенное или ароматическое ядро,
m = 1 или 2 и
n = 0, 1 или 2.
Для соединения формулы I, у которого
R является радикалом формулы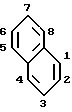
предпочтительно сульфамидогруппа присоединена в положении 1 или 2 и один из радикалов R1, R2 и R3 присоединены в положении 5 или 6.
один из R1, R2 и R3 является радикалом NR7R8,
R4, R5 и R12 представляют собой независимо друг от друга водород, алкил или галоген и
R7 и R8 представляют собой независимо друг от друга водород, алкил или C(O)R6 (R6 является алкилом).
Наиболее предпочтительны соединения, у которых один из R1, R2 и R3 является радикалом NR7R8 и два других являются водородом, радикал NR7R8 присоединен в положении 5 и сульфамидогруппа присоединена в положении 1, R4 и R5 независимо друг от друга представляют собой водород или метил, R12 является галогеном и R7 и R8 представляют собой водород, метил, метилэтил или ацетил.
Для соединения 1, у которого R является дифенилилом, один из R1, R2 и R3 предпочтительно является алкилом нормального или разветвленного строения в положении 4'.
Ниже указаны значения терминов, применявшихся в этом описании изобретения. Эти значения применяли на протяжении всего описания изобретения по отдельности или как часть группы, если не приведены ограничения в конкретных примерах.
Термины "алкил" и "алкоксигруппа" обозначают углеводородные радикалы с цепью нормального или разветвленного строения, имеющие 1 - 10 атомов углерода.
Термины "низший алкил" и "низшая алкоксигруппа" обозначают предпочтительно группы с 1 - 4 атомами углерода.
Термин "арил" или "ар-" обозначает фенил, нафтил и дифенилил.
Термин "алкенил" обозначает углеводородные радикалы с 2 - 10 атомами углерода и цепью нормального или разветвленного строения, имеющие по меньшей мере одну двойную связь. Предпочтительны радикалы с 2 - 4 атомами углерода.
Термин "алкинил" обозначает радикалы с 2 - 10 атомами углерода и цепью нормального или разветвленного строения, имеющие по меньшей мере одну тройную связь. Предпочтительны радикалы с 2 - 4 атомами углерода.
Термин "алкилен" обозначает мостиковую группу с цепью нормального строения из 1 - 5 атомов углерода, которая соединена одинарными связями (например, , группу (CH2)m, в которой m = 1 - 6) и может быть замещена 1 - 3 низшими алкилами.
Термин "алкенилен" обозначает мостиковую группу с цепью нормального строения из 2 - 5 атомов углерода, имеющей 1 или 2 двойные связи, которая соединена одинарными связями (например, -CH=CH2CH=CH, -CH2CH=CH-, -CH2CH= CHCH2-, C(CH3)2CH=CH- и CH(C2H5)-CH=CH-) и может быть замещена 1 - 3 низшими алкилами.
Термин "алкинилен" обозначает мостиковую группу с цепью нормального строения из 2 - 5 атомов углерода, имеющей тройную связь, которая соединена одинарными связями и может быть замещена 1 - 3 низшими алкилами. Примерами алкиниленов являются -C≡C, -CH2C≡C-, -CH(CH3)C≡C и -C≡CCH(C2H5)CH2-.
Термин "алканоил" обозначает группы формулы C(O)алкил.
Термины "циклоалкил" и "циклоалкенил" обозначает циклические углеводородные радикалы с 3 - 8 атомами углерода.
Термин "аралкил" обозначает алкил, замещенный одним или несколькими арилами.
Термин "галоген" обозначает фтор, хлор, бром и йод.
Соединения формулы I образуют соли, которые также входят в объем настоящего изобретения. Предпочтительны фармацевтически пригодные (т.е. нетоксичные, физиологически пригодные) соли, хотя применяют также другие соли, например для выделения или очистки соединений изобретения.
Соединения формулы I могут образовать соли со щелочными металлами, например натрием, калием и литием, со щелочноземельными металлами, например кальцием и магнием, с органическими основаниями, например дициклогексиламином, бензатином, N-метил-D-глюкамидом и гидрабамином, и с аминокислотами, например аргинином, лизином и подобными аминокислотами. Такие соли можно получить реакцией соединения формулы I с желаемым ионом в среде, в которой соль осаждается, или в водной среде с последующей лиофилизацией.
Когда заместители R1 - R5 или R12 содержат группу основного характера, например, аминогруппу или замещенную аминогруппу, то соединение 1 может образовать соли с различными органическими и неорганическими кислотами. Такие соли включают соли, образованные соляной, бромистоводородной кислотой, метансульфокислотой, серной, уксусной, малеиновой кислотой, бензолсульфокислотой, толуолсульфокислотой, и различными другими сульфокислотами, нитраты, фосфаты, бораты, ацетаты, тертраты, малеинаты, цитраты, сукцинаты, бензоаты, аскорбинаты, салицилаты и подобные соли. Эти соли получают реакцией соединения 1 с эквивалентным количеством кислоты в среде, в которой соль осаждается, или в водной среде с последующей лиофилизацией.
Кроме того, если заместители R1 - R5 или R12 имеют остаток основного характера, например аминогруппу, то можно получить цвиттерионы ("внутренние соли").
Некоторые из заместителей R1 - R5 и R12 соединения 1 могут содержать асимметричные атомы углерода. Такие соединения формулы I могут быть поэтому в энантиомерной и диастереомерной формах и в виде их рацемических смесей. Все они включены в объем настоящего изобретения.
Соединения формулы I являются антагонистами ЕТ-1, ЕТ-2 и/или ЕТ-3, они пригодны для лечения состояний, связанных с повышенным содержанием ЕТ (например, диализа, травм и хирургических операций), и всех эндотелин-зависимых нарушений. Они, таким образом, пригодны в качестве гипотензивных средств. Введением препарата, содержащего одно или комбинацию соединений настоящего изобретения, снижают кровяное давление гипертензивного млекопитающего-хозяина (например, человека). Они пригодны также для лечения индуцированной беременностью гипертензии, комы (преэклампсии и эклампсии), острой портальной гипертензии и гипертензии, вторичной к лечению эритропоэтином.
Соединения настоящего изобретения пригодны также для лечения нарушений, связанных с функцией почечных, гломерулярных и механгиальных клеток, включая острую и хроническую почечную недостаточность, гломерулярное повреждение, почечное нарушение, вызванное старостью или связанное с диализом, нефросклероза (в частности, гипертензивного нефросклероза), нефротоксичности (включая нефротоксичность, связанную со средствами, применяемыми для получения изображений, и контрастными средствами), почечной ишемии, первичного везикоуретерального рефлекса, гломерулосклероза и подобных заболеваний. Они пригодны также для лечения нарушений, связанных с паракринной и эндокринной функцией.
Соединения настоящего изобретения пригодны для лечения эндотоксемии и эндотоксинового бактериально-токсического шока, а также геморрагического шока.
Соединения настоящего изобретения пригодны также для лечения гипоксического и ишемического заболевания и в качестве антиишемических средств для лечения, например, сердечной, почечной и церебральной ишемии и реперфузии (например, возникающей после сердечно-легочного шунтирования), коронарных и церебральных вазоконстрикций и подобных заболеваний.
Кроме этого, соединения настоящего изобретения пригодны в качестве антиаритмических средств, антистенокардических средств; антифибрилляционных средств; антиастматических средств; антиатеросклеротических и антиартериосклеротических средств; добавок в кардиоплегические растворы для сердечно-легочного шунтирования; вспомогательных средств для тромболитической терапии и средств против поноса. Соединения этого изобретения можно также применять для лечения инфаркта миокарда; лечения периферического сосудистого заболевания (например, симметричной гангрены и болезни отсутствия пульса); лечения сердечной гипертрофии (например, гипертрофической кардиомиопатии); лечения первичной легочной гипертензии (например, плексогенной, эмболической) у взрослых людей и новорожденных и легочной гипертензии, вторичной к сердечной недостаточности, радиации и химиотерапевтического повреждения или другой травмы; лечения васкулярных нарушений центральной нервной системы, например припадка, мигрени, и субарахноидального кровоизлияния; лечения поступательных нарушений центральной нервной системы; лечения желудочно-кишечных заболеваний, например неспецифического язвенного колита, гранулематозной болезни, повреждения слизистой оболочки желудка, язвы и ишемической болезни кишечника; лечения заболеваний желчного пузыря и желчных протоков, например холангита; лечения панкреатита; регулирования роста и миграции клеток; лечения доброкачественной гиперплазии и гипертрофии простаты; лечения липидных нарушений; лечения рестеноза после пластической операции на сосудах или любых процедур, включающих трансплантацию; лечения застойной сердечной недостаточности, включающей ингибирование фиброза; ингибирования левого вентрикулярного расширения, реконструкции и дисфункции; и лечения гепатотоксичности и скоропостижной смерти. Соединения этого изобретения пригодны для лечения серповидно-клеточной анемии, включая инициирование и/или развитие болевых кризисов этого заболевания; лечения вредных последствий ЕТ-продуцирующих опухолей, например гипертензии, являющейся результатом гемангиоперицитомы; лечения ранней и развитой формы заболевания и повреждения печени, включая сопутствующие осложнения (например, гепатотоксичность, фиброз и цирроз); лечения спастических заболеваний мочевых путей и/или мочевого пузыря; лечения гепаторенального синдрома; лечения иммунологических заболеваний, включая васкулит, например волчанки, системного склероза, смешанной криоглобулинемии; и лечения фиброза, связанного с почечной дисфункцией и гепатотоксичностью. Соединения настоящего изобретения можно применять в терапии метаболических и нейрологических нарушений; ракового заболевания; инсулинзависимого и инсулиннезависимого сахарного диабета; невропатии; ретинопатии; материнского респираторного дистресс-синдрома; дисменореи; эпилепсии; геморрагического и ишемического приступа; костного переделывания и хронических воспалительных заболеваний, например ревматического артрита, остеоартрита, саркоидоза и экзематозного дерматита (все типы дерматита).
Соединения этого изобретения можно также применять в комбинации с ингибиторами фермента, превращающего эндотелин (ECE), например фосфорамидоном; антагонистами рецептора тромбоксана; средствами, открывающими калиевые каналы; ингибиторами тромбина (например, гирудином и подобными средствами), ингибиторами фактора роста, например модуляторами фактора роста, полученного из тромбоцитов (PDGF); антагонистами фактора активации тромбоцитов (PAF); антагонистами рецептора ангиотензина II (All); ингибиторами ренина; ингибиторами фермента, превращающего ангиотензин (ACE), например каптоприлом, зофеноприлом, фозиноприлом, церанаприлом, алацеприлом, эналаприлом, лелаприлом, пентоприлом, хинаприлом, рамиприлом, лизиноприлом и солями таких соединений; ингибиторами нейтральной эндопептидазы (NEP), блокаторами кальциевых каналов, активаторами калиевых каналов; β -адренергическими средствами, антиаритмическими средствами; диуретиками, например хлоротиазидом, гидрохлоротиазидом, флуметиазидом, гидрофлуметиазидом, бендрофлуметиазидом, метилхлоротиазидом, трихлорметиазидом, политиазидом или бензотиазидом, а также этакриновой кислотой, трикринафеном, хлорталидоном, фуросемидом, музолимином, буметанидом, триамтереном, амилоридом и спиронолактоном и солями таких соединений; тромболитическими средствами, например тканевым активатором плазминогена (tPA), рекомбинантным tPA, стрептокиназой, урокиназой, проурокиназой и комплексом анизоилированного активатора стрептокиназы плазминогена (APSAC, Sminase, Beecham Laboratories). Если такие комбинации продуктов приготовляют в виде определенных доз, то они содержат соединения настоящего изобретения в описанном ниже дозированном пределе, а другое фармацевтически активное средство в его одобренном дозированном пределе. Соединения настоящего изобретения можно также выпускать или применять вместо с антигрибковым и иммунодепрессивными средствами, например, амфотерицином B, циклоспоринами и подобными соединениями для противодействия гломерулярному сокращению и нефротоксичности, вызванной побочным действием таких соединений. Соединения этого изобретения можно также применять в сочетании с гемодиализом.
Соединения изобретения можно вводить перорально или парентерально различным видам млекопитающих, которые, как известно, являются субъектами таких заболеваний, например людям, в эффективном количестве в пределах 0,1 - 100 мг/кг, предпочтительно 0,2 - 50 мг/кг, более предпочтительно 0,2 - 25 мг/кг (или 1 - 2500 мг, предпочтительно 5 - 2000 мг) в виде разовой дневной дозы или такой дневной дозы, разделенной на 2 - 4 введения.
Активное вещество можно применять в составе препарата, например в форме таблетки, капсулы, раствора или суспензии, содержащей 5 - 500 мг (на единицу дозы) соединения или смеси соединений формулы I, или в форме для местного введения, предназначенной для заживления ран (0,01 - 5% соединения формулы I, 1 - 5 введений в день). Их можно смешивать обычным способом с физиологически пригодным наполнителем или носителем, неактивным компонентом, связующим, консервантом, стабилизатором, отдушкой или с носителем для местного введения, например пластибазом (минеральным маслом, желатинированным полиэтиленом), как предусмотрено фармацевтической практикой.
Соединения изобретения можно также вводить местным способом для лечения периферических сосудистых заболеваний в составе препарата в виде крема и мази.
Соединения формулы I можно также вводить в состав препаратов в виде стерильных растворов или суспензий для парентерального введения. 1 - 500 мг соединения формулы I смешивают с физиологически пригодным наполнителем, носителем, неактивным компонентом, связующим, консервантом, стабилизатором для образования препарата в унифицированной дозе, как предусмотрено фармацевтической практикой. Количество активного вещества в этих составах или препаратах соответствует указанному дозированному пределу.
Соединения настоящего изобретения можно получить следующим образом.
Соединение формулы I получают конденсацией сульфамида формулы II
RSO2NH2
с соединением формулы III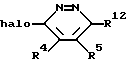
в безводном органическом растворителе в присутствии основания (например, Cs2CO3).
Сульфамид формулы II получают из PSO2-галоген и NH3.
Сульфамид формулы II, у которого R является дифенилилом, замещенным радикалами R1, R2 и R3, можно получить катализированной металлом (например, палладием (O)) конденсацией галогензамещенного соединения формулы
с арилметаллоидами (то-есть арилпроизводными олова, кремния, бора и подобных металлоидов, например фенилбороновой кислотой). Фенилбороновую кислоту можно получить обработкой арилгалогенида н-бутиллитием или магниевой стружкой в безводном органическом растворителе (например, тетрагидрофуране) с последующим добавлением в продукт триметилбората и затем водной соляной кислоты.
Реагенты, у которых любой из радикалов R1 - R5 и R12 содержит реакционноспособные функциональные группы, можно до конденсации обработать защищающими агентами. Используют известные защитные агенты и способы из применения. Примерами защитных групп являются бензил, галогенкарбобензилоксигруппа, тозил для гидроксигруппы и карбобензилоксигруппа, галогенкарбобензилоксигруппа, ацетил и бензоил для аминогруппы. Такие группы можно затем удалить у образованного защищенного аналога соединения 1 обработкой одним или несколькими средствами для удаления защитных групп. Используют известные такие средства и способы их применения.
Аналогично может быть необходимо, чтобы атом азота сульфамидогруппы был защищен в процессе получения соединения 1. Применяют также обычно известные защитные группы. Защитную группу присоединяют обработкой свободного амина галогенидом защитной группы при 0oC в присутствии основания (например, триэтиламина). Защитную группу можно удалять обработкой кислотой (например, трифторуксусной кислотой) в органическом растворителе (например, хлористом метилене) при 0oC.
Изобретение далее будет описано следующими рабочими примерами, которые являются предпочтительными примерами осуществления изобретения. Эти примеры предназначены для иллюстрации, а не для ограничения изобретения.
Пример 1
N-(6-Хлор-3-пиридазил)-5-(диметиламино)-1-нафталинсульфамид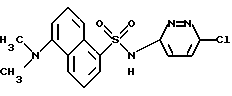
Раствор данзиламида (0,50 г, 2,00 ммоля), 3,6-дихлорпиридазина (0,37 г, 2,50 ммоля) и карбоната цезия (1,33 г, 4,10 ммоля) в диметилформамиде (2 мл) нагревали при 105oC в течение 6 ч, остудили и вылили в воду. Раствор подкислили до pH 3 и образованный коричневый осадок отделили фильтрованием, промыли водой и растворили в полунасыщенном водном растворе бикарбоната натрия. Раствор подкислили по pH 3 и образованный коричневый осадок отделили фильтрованием, промыли водой и растворили в 10% изопропанол/хлористый метилен. Раствор промыли соляным раствором, высушили (сульфатом магния) и выпарили. Остаток хроматографировали на диоксиде кремния с применением 2%, затем 3% метанол-хлористый метилен для выделения 0,29 г продукта, содержащего небольшое количество данзиламида. Твердый продукт растворили в полунасыщенном водном растворе бикарбоната натрия и раствор профильтровали. Фильтрат подкислили до pH 3 твердым кислым сульфатом калия и экстрагировали хлористым метиленом. Органический раствор сушили (сульфатом магния) и выпаривали для выделения 0,24 г (33%) продукта примера 1 в виде ярко-желтого твердого вещества. Т. пл. 92 - 100oC.
Элементный состав, рассчитанный для C16H15N4O2SCl - 0,41 H2O - 0,15 C4H10O
Подсчитано: C 52,29; H 4,58; N 14,69; 8,40; Cl 9,30.
Найдено: C 52,29; H 4,34; N 14,53; 8,32; Cl 9,38.
Пример 2
N-(6-Хлор-5-метил-3-пиридазил)-5-(диметиламино)-1- нафталинсульфамид
Раствор данзиламида (1,5 г 6,0 ммоля), 3,6-дихлор-4-метилпиридазина (0,98 г, 6,0 ммоля) и карбоната цезия (4,1 г, 12,6 ммоля) в диметилформамиде (8 мл) нагревали при 105oC в течение 8 ч, охладили и вылили в полунасыщенный раствор бикарбоната натрия (300 мл). После отделения фильтрованием большого количества черного смолистого твердого вещества фильтрат подкислили твердым кислым сульфатом калия и экстрагировали три раза хлористым метиленом. Объединенную органическую фазу сушили (сульфатом магния), выпаривали и нагревали в высоком вакууме для выделения 1,03 г черного смолистого вещества. Тонкослойной хроматографией на диоксиде кремния (30% затем 50% этилацетат/гексаны) получили 0,17 г неочищенного быстрее движущегося изомера (FMI; TCX, 50% этилацетат/гексаны, Rf = 0,60) в виде розового твердого вещества и 0,19 г почти чистого медленнее движущегося изомера (SMI; TCX, 50% этилацетат/гексаны, Rf = 0,43) в виде серо-зеленого смолистого вещества. SMI-изомер перекристаллизовали из смеси этилацетат/гексаны для выделения 93 мг (4%) продукта примера 2 в виде белого твердого вещества. Т. пл. 112 - 115oC.
Элементный состав, рассчитанный для C17H17N4O2SCl - 0,07 H2O
Подсчитано: C 53,99; H 4,57; N 14,81; 8,48; Cl 9,37.
Найдено: C 53,99; H 4,36; N 14,84; 8,36; Cl 9,35.
Пример 3
N-(6-Хлор-4-метил-3-пиридазил)-5-(диметиламино)-1- нафталинсульфамид
FMI-изомер примера 2 суспензировали в 5%-ном водном растворе бикарбоната натрия, в суспензию добавили метанол и раствор нагревали почти до полного растворения. Раствор выпаривали для удаления только метанола, оставшийся неоднородный раствор фильтровали для отделения нерастворимого данзиламида. Фильтрат подкислили твердым кислым сульфатом калия и экстрагировали этилацетатом. Органическую фазу сушили (сульфатом магния) и выпаривали для выделения 130 мг розового твердого вещества, которое растворили в небольшом количестве теплого этилацетата. В раствор добавили гексан и продукт выдерживали для кристаллизации. Кристаллический продукт отделили фильтрованием, промыли смесью этилацетат/гексаны и сушили для получения 96 мг (4%) соединения примера 3 в виде желтого твердого вещества. Т. пл. 192 - 194oC.
Элементный состав, рассчитанный для C17H17N4O2SCl
Подсчитано: C 54,18; H 4,55; N 14,87; 8,51; Cl 9,41.
Найдено: C 54,25; H 4,56; N 14,69; 8,22; Cl 9,40.
Пример 4
N-(6-Хлор-3-пиридазил)-1,1'-дифенил-2-сульфамид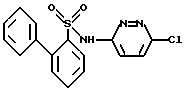
A. 1,1'-Дифенил-2-сульфамид
В дегазированный раствор 2-бромбензолсульфамида (0,7 г, 3,00 ммоля) и тетракис(трифенилфосфин)палладия (O) (0,21 г, 0,18 ммоля) в бензоле (25 мл) добавили 2М водный раствор карбоната натрия (15 мл) и затем раствор фенилбороновой кислоты (0,44 г, 3,6 ммоля) в 95%-ном водном этаноле. Двухфазный раствор кипятили 18 ч, охладили до комнатной температуры и разбавили водой. Смесь экстрагировали два раза этилацетатом. Объединенную органическую фазу промыли соляным раствором, сушили (сульфатом магния), фильтровали и выпаривали. Остаток хроматографировали (силикагель, смесь гексанов и этилацетата в соотношении 2: 1) для выделения 0,25 г (36%) соединения A в виде желтого твердого вещества.
B. N-(6-Хлор-3-пиридазил)-1,1'-дифенил-2- сульфамид
В раствор соединения A (0,30 г, 1,3 моля) и 3,6-дихлорпиридазина (0,21 г, 1,4 ммоля) в сухом диметилформамиде (4 мл) добавили карбонат цезия (0,46 г, 1,4 ммоля). Смесь нагревали при 105oC в течение 24 ч, охладили до комнатной температуры, разбавили водой (40 мл) и подкислили до pH 4 6N водной соляной кислотой. Образованный рыжевато-коричневый осадок отделили фильтрованием, промыли водой и растворили в этилацетате. Раствор экстрагировали 3 раза 2N водным раствором карбоната натрия (3 х 50 мл) и объединенный экстракт подкислили до pH 4 6N водной соляной кислотой. Образованный рыжевато-коричневый осадок отделили фильтрованием, промыли водой и сушили в вакууме для получения 0,24 г (54%) соединения примера 4 в виде рыжевато-коричневого твердого вещества с т. пл. 176 - 181oC. Элементный состав, рассчитанный для C16H12N3O2SCl - 1,11 H2O.
Подсчитано: C 52,53, H 3,92, N 11,49, 8,76; Cl 9,68.
Найдено: C 52,78, H 3,69, N 11,24, 8,70, Cl 9,39.
Пример 5
N-(6-Хлор-3-пиридазил)-4'-(2-метилпропил)-1,1'-дифенил- 2-сульфамид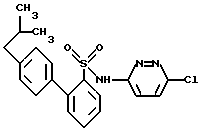
A. 4-(2-Метилпропил)бензолбороновая кислота
В суспензию 0,68 г (28,15 ммоля) магниевой стружки в 50 мл тетрагидрофурана в 50 мл тетрагидрофурана в атмосфере аргона добавили кристалл йода и раствор 4-бромизобутиленбензола (6,0 г, 28,15 ммоля) в 25 мл тетрагидрофурана с такой скоростью, чтобы поддерживалось спокойное орошение. Смесь кипятили с обратным холодильником еще 1 ч, охладили до комнатной температуры и добавили по частям в течение 15 мин в раствор триметилбората (2,93 г, 28,15 ммоля) в 50 мл простого эфира при -78oC в атмосфере аргона. После выдерживания смеси при -78oC в течение 30 мин раствор нагрели до комнатной температуры, перемешивали 90 мин и добавили 10%-ную водную соляную кислоту (10 мл). Через 10 мин после добавления раствор экстрагировали простым эфиром (3 х 100 мл) и объединенный эфирный экстракт экстрагировали 1М раствором едкого натра (3 х 100 мл). Водные экстракты подкислили разбавленной соляной кислотой до pH 2 и экстрагировали простым эфиром (3 х 100 мл). Объединенный эфирный экстракт промыли один раз водой (100 мл), сушили и выпаривали для выделения 3,5 г белого твердого вещества. Кристаллизацией из смеси простого эфира и гексанов получили 2,3 г (46%) белого твердого соединения A в виде двух порций с т. пл. 134 - 135oC.
В. N-(1,1-Диметилэтил)-4'-(2-метилпропил)-1,1'-дифенил-2- сульфамид
В раствор N-(1,1-диметилэтил)-2-бромбензолсульфамида (500 мг, 1,71 ммоля) в толуоле (14 мл), карбоната натрия (363 мг, 3,42 ммоля) в воде (7 мл) и соединения A (366 мг, 2,05 ммоля) в этаноле (7 мл), причем все растворители были дегазированы аргоном, добавили тетракис(трифенилфосфин)палладий(O) (119 мг, 0,103 ммоля). Желтую смесь нагревали с обратным холодильником 1 ч, охладили до комнатной температуры и вылили в полунасыщенный раствор бикарбоната натрия (30 мл). Смесь экстрагировали этилацетатом (2 х 50 мл). Объединенный органический слой сушили (сульфатом магния) и выпаривали. Хроматографией (диоксид кремния, 10% этилацетат/гексаны) выделили белое твердое соединение B (503 мг, 85%).
C. 4'-(2-Метилпропил)-1,1'-дифенил-2-сульфамид
Раствор соединения B (503 мг, 1,45 ммоля) в холодной трифторуксусной кислоте (5 мл) перемешивали в течение 5 ч при постепенном нагревании его до комнатной температуры. Растворитель выпаривали и остаток пропустили через колонку с диоксидом кремния с элюированием этилацетатом. После выпаривания элюата получили соединение C в виде масла (306 мг, 100%).
N-(6-Хлор-3-пиридазил)-4'-(2-метилпропил)-1,1'-дифенил-2- сульфамид
В раствор соединения C (300 мг, 1,73 ммоля) и 3,6-дихлорпиридазина (350 мг, 2,34 ммоля) в сухом диметилформамиде (4 мл) добавили карбонат цезия (770 мг, 2,34 ммоля). Смесь нагревали 3 ч при 100oC, охладили до комнатной температуры, разбавили водой (75 мл) и подкислили до pH 3 6N водной соляной кислотой. Смесь экстрагировали этилацетатом (3 х 50 мл) и объединенную органическую фазу промыли водой и соляным раствором и сушили (сульфатом магния). Остаток хроматографировали на силикагеле с применением смеси этилацетата и гексанов в соотношении 2:3 для выделения 200 мг (29%) рыжевато-коричневого твердого соединения примера 5. Т. пл. 108 - 110oC.
Элементный состав, рассчитанный для C20H20N3O2SCl - 0,15 H2O
Подсчитано: C 59,37; H 5,05; N 10,38, S 7,92; Cl 8,76
Найдено: C 59,37; H 4,99; N 10,03, S 7,94; Cl 9,09.
Данные по связыванию рецепторов ETA на клетках A10 у крыс
Пример - Ki, мкМ (uM)
1 - 0,46
2 - 7,1
3 - 1,6
4 - 2,8
5 - 0,4
Наименьшее значение Ki свидетельствует о том, что соединение высокоактивно при использовании в качестве гипотензивного агента. Эксперимент описан в Journal of Medicinal Chemistry, 1995, Vol.38, N.8. Все соединения являются малотоксичными.
Сульфамидные соединения общей формулы I, где R - нафтил или бифенил, возможно замещенные R1, R2; R1, R2 - С1-C4-алкил или -NR7R8; R4, R5 - H или С1-C4-алкил; R7, R8 - С1-C4-алкил; R12 - галоген, или их фармацевтически пригодные соли являются антагонистами рецептора энтотелина и могут использоваться в качестве гипотензивных средств. 2 с. и 12 з.п.ф-лы.
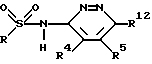
или их фармацевтически пригодные соли,
где R означает нафтил или бифенил, возможно замещенные группами R1 и R2, где R1 и R2 означают C1 - C4-алкильную или - NR7R8-группу;
R4 и R5 означают водород или C1 - C4-алкильную группу;
R7 и R8 означают C1 - C4-алкильную группу;
R12 означает галоген.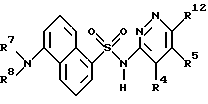
7. Соединение по п.6, где R7 и R8 означают C1 - C4-алкильную группу.
| Сталь | 1974 |
|
SU510526A1 |
| Релейный реверсивный распределитель | 1973 |
|
SU526708A1 |
| Автоматическое огнестрельное оружие | 1936 |
|
SU92945A3 |
| Способ получения производных пиридазина | 1982 |
|
SU1356960A3 |
Авторы
Даты
1999-11-27—Публикация
1994-08-29—Подача