Данная заявка является частичным продолжением заявки N 08/487308, поданной 7 июля 1995 года, которая, в свою очередь, является частичным продолжением заявки N 08/368285, поданной 5 января 1995 года, которая в свою очередь является частичным продолжением заявки N 08/297187, поданной 26 августа 1994 года. Содержание всех этих заявок включено в данное описание для сведения.
Данное изобретение относится к антагонистам эндотелина, полезным наряду с прочим для лечения гипертензии или артериальной гипертонии.
Соединения формулы I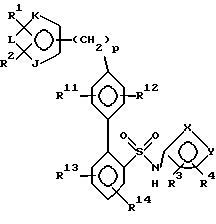
их энантиомеры и диастереомеры и их фармацевтически приемлемые соли являются антагонистами эндотелинового рецептора, полезными наряду с прочим в качестве противогипертензивных средств. На протяжении данного описания указанные выше символы имеют значения, определяемые следующим образом:
один из X и Y представляет N, а другой - O;
R1, R2, R3 и R4 каждый непосредственно связан с кольцевым углеродом и каждый представляет независимо:
/а/ водород,
/b/ алкил, алкенил, алкинил, алкокси, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил, арилокси, аралкил или аралкокси, любой из которых может быть замещен заместителями Z1, Z2 и Z3,
/c/ галоид,
/d/ гидрокси,
/e/ циано,
/f/ нитро,
/g/ - С/О/H или -С/О/R5,
/h/ - СО2H или - СО2R5,
/i/ - Z4-NR6, R7,
/j/ - Z4-N/R10-Z5-NR8R9, или
/k/ R3 и R4 вместе могут также представлять алкилен или алкенилен, любой из которых может быть замещен заместителями Z1, Z2 и Z3, завершающий 4- ... 8-членное насыщенное, ненасыщенное или ароматическое кольцо вместе с атомами углерода, к которым они присоединены.
R5 представляет алкил, алкенил, алкинил, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил или аралкил, любой из которых может быть замещен заместителями Z1, Z2 и Z3;
R6, R7, R8, R9 и R10 каждый независимо представляет
/a/ водород, или
/b/ алкил, циклоалкил, циклоалкилалкил, циклоалкенилалкил, арил или аралкил, любой из которых может быть замещен заместителями, Z1, Z2 и Z3, или
R6 и R7 вместе могут представлять алкилен или алкенилен, любой из которых может быть замещен заместителями Z1, Z2 и Z3, завершая 3- ... 8-членное насыщенное или ненасыщенное кольцо вместе с атомом азота, к которому они присоединены, или любые два из R8, R9 и R10 вместе представляют алкилен или алкенилен, любой из которых может быть замещен заместителями Z1, Z2 и Z3, завершая 3- ... 8-членное насыщенное или ненасыщенное кольцо вместе с атомами, к которому они присоединены;
R11, R12, R13 и R14 каждый независимо представляет
/а/ водород,
/b/ алкил, алкенил, алкинил, алкокси, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил, арилокси, аралкил или аралкокси, любой из которых может быть замещен заместителями Z1, Z2 и Z3,
/с/ гетероцикл, замещенный гетероцикл или гетероциклоокси,
/d/ галоид,
/e/ гидроксил,
/f/ циано,
/g/ нитро,
/h/ - С/О/H или -С/О/R5,
/i/ - СО2H или - СО2R5,
/j/ - SH, -S/O/nR5, - S/O/m-OH, -S/O/m- OR5, -O-S/O/m- OR5, -O-S/O/mOH или -O-S/O/m-OR5,
/k/ -Z4-NR6R7, или
/I/ - Z4-N/R10/-Z5/NR8R9,
Z1, Z2 и Z3 каждый независимо представляет:
/a/ водород,
/b/ галоид,
/c/ гидрокси,
/d/ алкил,
/e/ алкенил,
/f/ арил,
/g/ аралкил,
/h/ алкокси,
/i/ арилокси,
/j/ аралкокси,
/k/ гетероцикл, замещенный гетероцикл или гетероциклоокси,
/I/ -SH, -S/O/nZ6, -S/O/m-OH, -S/O/m-OZ6, -O-S/O/m-Z6, -O-S/O/mOH или -O-S/O/m-O6,
/m/ оксо,
/n/ нитро,
/o/ циано,
/p/ C/O/H или - С/О/Z6,
/q/ - CO2H или - СО2Z6;
/r/ -Z4 -NZ7 Z8;
/s/ -Z4-N/Z11/-Z5-H,
/t/ Z4-N/Z11/-Z5-Z6, или
/u/ -Z4-N/Z11/-Z5-NZ7 Z8,
Z4 и Z5 каждый независимо представляет
/a/ одинарную связь,
/b/ -Z9-S/O/n-Z10-,
/c/ Z9/C/O-Z10-,
/d/ -Z9-C/S/-Z10-,
/e/ Z9-O-Z10-,
/f/ Z9-S-Z10-,
/c/ -Z9-O-C/O/-Z10-, или
/h/ -Z9-C/O/-O-Z10-,
Z6 представляет алкил, алкил, замещенный одним, двумя или тремя галогенами, алкенил, алкинил, циклоалкил, циклоалкилалкил, циклоалкенил, циклоалкенилалкил, арил, арил, замещенный одним, двумя или тремя галогенами, арил, замещенный тригалоидалкилом, или аралкил;
Z7 и Z8 каждый независимо представляет водород, алкил, циклоалкил, циклоалкилалкил, циклоалкенилалкил, арил или аралкил, или Z7 и Z8 вместе представляют алкилен или алкенилен, завершающий 3- ... 8-членное насыщенное или ненасыщенное кольцо вместе с атомом азота, к которому они присоединены;
Z9 и Z10 каждый независимо представляет одинарную связь, алкилен, алкенилен или алкинилен;
Z11 представляет:
/a/ водород, или
/b/ алкил, алкил, замещенный одним, двумя или тремя галогенами, циклоалкил, циклоалкилалкил, циклоалкенилалкил, арил или аралкил или любые два из Z7, Z8 и Z11 вместе представляют алкилен или алкенилен, завершающий 3- ... 8-членное насыщенное или ненасыщенное кольцо вместе с атомами, к которым они присоединены;
J представляет O, S, N или NR15;
K и L представляют N или C, при условии, что, по крайней мере, один из K или L представляет C;
R15 представляет водород, алкил, гидроксиэтоксиметил или метоксиэтоксиметил;
каждый m независимо представляет 1 или 2;
каждый n независимо представляет 0, 1 или 2; и p = 0, 1 или 2.
Для соединения I предпочтительно, чтобы:
R1 и R2 каждый представлял независимо водород, алкил, алкокси, арил, гидроксиалкил, - СО2R5 или -Z4-NR6R7;
R3 и R4 каждый независимо представлял водород, гидрокси, амино, гетероцикло, алкенил, карбоксамид или замещенный низший алкил.
Наиболее предпочтительными соединениями являются соединения, в которых:
R1 и R2 каждый независимо представляет низший алкил или водород;
R3 и R4 каждый независимо представляет низший алкил, особенно метил;
и R11 и R12 каждый независимо представляет водород, гидрокси, гетероцикло, алкенил, карбоксамид, или замещенный низший алкил.
Ниже приводятся определения терминов, используемых в данном описании. Эти определения применимы к терминам, используемым по всему данному описанию, индивидуально или в виде части другой группы, если они не ограничиваются иным образом в конкретных случаях.
Термин "алкил" или "алк-" относится к углеводородным группам, с прямой или разветвленной цепью, имеющим 1-10 атомов углерода, предпочтительно 1-7 атомов углерода. Выражение "низший алкил" относится к алкильным группам с 1-4 атомами углерода.
Термин "алкокси" относится к группе алкил-О-.
Термин "арил" или "ар-" относится к фенилу, нафтилу и бифенилу.
Термин "алкенил" относится к углеводородным группам с прямой или разветвленной цепью, с 2-10 атомами углерода, имеющим, по крайней мере, одну двойную связь. Предпочтительными являются группы с двумя-четырьмя атомами углерода.
Термин "алкинил" относится к группам с прямой или разветвленной цепью с 2-10 атомами углерода, имеющим, по крайней мере, одну тройную связь. Предпочтительны группы с двумя - четырьмя атомами углерода.
Термин "алкилен" относится к мостику с прямой цепью с 1-5 атомами углерода, связанными одинарными связями /например, - /CH2/x-, где x представляет 1-5/, который может быть замещен 1-3 низшими алкильными группами.
Термин "алкенилен" относится к мостику с прямой цепью с 2-5 атомами углерода, имеющему одну или две двойные связи, который соединяется одинарными связями и может быть замещен 1-3 низшими алкильными группами. Примерами алкениленовых групп являются - CH=CH-CH=CH-, -CH2-CH=CH, -CH2- CH=CH-CH2-, -C/CH3/2CH=CH- и -CH/С2H5/-CH=CH-.
Термин "алкинилен" относится к мостику с прямой цепью из 2-5 атомов углерода, который имеет в себе тройную связь и присоединяется одинарными связями, и может быть замещен 1-3 низшими алкильными группами. Примерами алкиниленовых групп являются 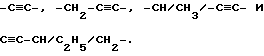
Термин "алканоил" относится к группам формулы -С/О/алкил.
Термин "циклоалкил" и "циклоалкенил" относятся к циклическим углеводородным группам с 3-8 атомами углерода.
Термин "гидроксиалкил" относится к алкильной группе, включающей один или более гидрокси радикалов, такой как - CH2CH2ОН, -CH2CH2OHCH2OH, - CH/CH2OH/2 и аналогичные.
Термины "галоген" и "галоид" относятся к фтору, хлору, брому и иоду.
Термины "гетероцикл", "гетероциклический" и "гетероцикло" относятся к необязательно замещенной, полностью насыщенной или ненасыщенной ароматической или неароматической циклической группе, например, которая представляет 4-7-членную моноциклическую, 7-11-членную бициклическую или 10-15-членную трициклическую кольцевую систему, которая имеет, по крайней мере, один гетероатом в кольце, содержащем, по крайней мере, один атом углерода. Каждое кольцо гетероциклической группы, содержащее гетероатом, может иметь 1, 2 или 3 гетероатома, выбранных из атомов азота, атомов кислорода или серы, при этом гетероатомы азота и серы могут быть необязательно окисленными, а гетероатомы азота могут быть необязательно кватернизованными. Гетероциклическая группа может присоединяться по любому гетероатому или атому углерода.
Примеры моноциклических гетероциклических групп включают пирролидинил, пирролил, пиразолил, оксетанил, пиразолинил, имидазолил, имидазолинил, имидазолидинил, оксазолил, оксасолидинил, изоксазолинил, изоксазолил, тиазолил, тиадиазолил, тиазолидинил, изотиазолил, изотиазолидинил, фурил, тетрагидрофурил, тиенил, оксадизолил, пиперидинил, пиперазинил, 2-оксопиперазинил, 2- оксопиперидинил, 2-оксопирролодинил, 2- оксоазепинил, азепинил, 4- пиперидонил, пиридил, пиразинил, пиримидинил, пиридазонил, тетрагидропиранил, морфолинил, тиаморфолинил, тиаморфолинил, сульфоксид, тиаморфолинилсульфон, 1,3- диоксолан и тетрагидро-1,1-диоксотиенил, и аналогичные.
Примеры бициклических гетероциклических групп включают индолил, бензотиазолил, бензоксазолил, бензотиенил, хинуклидинил, хинолинил, тетра-гидроизохинолинил, изохинолинил, бензимидазолил, бензопиранил, индолизинил, бензофурил, хромонил, кумаринил, бензопиранил, циннолинил, хиноксалинил, индазолил, пирролопиридил, фуропиридинил /такой как фуро/2,3-с/ пиридинил, фуро /3,2-b/пиридинил/ или фуро/2,3-b/пиридинил/, дигидроизоиндолил, дигидрохиназолинил /такой как 3,4-дигидро- 4-оксо-хиназолинил/ и аналогичные.
Примеры трициклических гетероциклических групп включают карбазолил, бензиндолил, фенантролинил, акридинил, фенантридинил, ксантенил и аналогичные.
Выражение "замещенный гетероцикл" относится к гетероциклу, замещенному 1, 2 или 3 из следующих заместителей:
/a/ алкил, особенно низший алкил;
/b/ гидрокси /или защищенный гидрокси/;
/c/ галоид;
/d/ оксо /т.е. = О/;
/e/ амино, алкиламино или диалкиламино;
/f/ алкокси;
/g/ карбоцикло, такой как циклоалкил;
/h/ карбокси;
/i/ гетероциклоокси;
/j/ алкоксикарбонил: такой как незамещенный низший алкоксикарбонил;
/k/ карбомил, алкилкарбамил или диалкилкарбамил;
/I/ меркапто,
/m/ нитро;
/n/ циано;
/о/ карбоалкокси;
/p/ сульфонамидо, сульфонамидоалкил или сульфонамидодиалкил;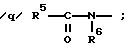

/s/ арил,
/t/ алкилкарбонилокси;
/u/ арилкарбонилокси;
/v/ арилтио;
/w/ арилокси;
/x/ алкилтио;
/y/ формил;
/z/ арилалкил; или
/a'/ арил, замещенный алкилом, циклоалкилом, алкокси, гидрокси, амино, алкиламино, диалкиламино, галоидом или тригалоидалкилом.
Термин "гетероциклоокси" обозначает гетероциклическую группу, связанную через кислородный мостик.
На протяжении описания группы и их заместители выбраны для обеспечения стабильных фрагментов и соединений.
Соединения формулы I образуют соли, которые также охватываются объемом данного изобретения. Предпочтительными являются фармацевтически приемлемые /т. е. нетоксичные, физиологически приемлемые/ соли, хотя полезны также и другие соли, например, при выделении или очистке соединений данного изобретения.
Соединения формулы I могут образовывать соли с щелочными металлами, такими, как натрий, калий и литий, со щелочноземельными металлами, такими как кальций и магний, с органическими основаниями, такими как дициклогексиламин, трет- бутиламин, бензатин, N-метил-Д-глюкамид и гидробамин, и с аминокислотами, такими как аргинил, лизин и аналогичные. Такие соли могут получаться с помощью реакции соединения I с желаемым ионом в среде, в которой соль осаждается, или в водной среде с последующей лиофилизацией.
Когда заместители R1-R4 или R11-R14 включают основной фрагмент, такой как амино или замещенный амино, соединение I может образовывать соли с различными органическими и неорганическими кислотами. Такие соли включают соли, образуемые с соляной кислотой, бромистым водородом, метансульфокислотой, серной кислотой, уксусной, малеиновой кислотой, бензолсульфонатом, толуолсульфонатом и различными другими сульфонатами, нитратами, фосфатами, боратами, ацетатами, тартратами, малеатами, цитратами, сукцинатами, бензоатами, аскорбатами, салицилатами и аналогичными. Такие соли могут образовываться с помощью реакции соединения I в эквивалентном количестве кислоты в среде, в которой соли выпадают в осадок, или в водной среде с последующей лиофилизацией.
В дополнение к сказанному, когда R1-R4 или R11-R14 заместители включают основной фрагмент, такой как амино, могут образовываться цвиттерионы /"внутренние соли"/.
Некоторые из заместителей R1-R4 и R11-R14 соединения I могут содержать асимметричные атомы углерода. Такие соединения формулы I могут существовать, следовательно, в энантиомерных и диастереомерных формах и в виде их рацемических смесей. Все они охватываются объемом данного изобретения. Дополнительно к сказанному соединения I могут существовать в виде энантиомеров даже в отсутствие асимметрических атомов углерода. Все такие энантиомеры также охватываются объемом данного изобретения.
Соединения формулы I являются антагонистами ET-1, ET-2 и/или ЕТ-3 и полезны при лечении состояний, связанных с увеличенными уровнями ET /например, при диализе, травмах и хирургическом вмешательстве/ и всех эндотелин-зависимых расстройствах. Таким образом, они полезны в качестве антигипертензивных агентов. При назначении композиции, имеющей одно из /или сочетание/ соединений данного изобретения, понижается кровяное давление у гипертензивных млекопитающих /например, у человека/. Они полезны также при гипертензии, вызванной беременностью, и при коме /преэклампсии и эклампсии/, при острой портальной гипертензии и гипертензии вторичной по отношению к лечению эритропоэтином.
Соединения настоящего изобретения полезны также при лечении нарушений, связанных с функцией ренальных, гломерулярных и мезангиальных клеток, включая острую и хроническую почечную недостаточность, гломерулярные повреждения, ренальные повреждения вторичные для пожилого возраста, или связанных с диализом, нефросклерозом /особенно гипертензивным нефросклерозом/, нефротоксичностью /включая нефротоксичность, связанную с визуализующими и контрастными агентами и с циклоспорином/, ренальную ишемию, первичный везикоуратеральный рефлюкс, гломерулосклероз и аналогичные. Соединения данного изобретения могут быть также полезными при лечении расстройств, связанных с функцией паракрина и эндокрина.
Соединения настоящего изобретения полезны также при лечении эндотоксемии или эндотоксинового шока, а также геморрагического шока.
Соединения настоящего изобретения являются полезными также в случае гипоксической или ишемической болезни и в качестве противо-ишемических агентов для лечения, например, сердечной, ренальной и церебральной ишемии и реперфузии /такой, как имеет место после хирургического вмешательства с использованием системы искусственного кровообращения/, спазмов коронарных и церебральных сосудов и аналогичных.
В дополнение к изложенному соединения данного изобретения могут быть также полезными в качестве анти-аритмических агентов, противоантигенных агентов; анти-фибрилляторных агентов; противоастматических агентов; противо-этеросклеротических и противоартериосклеротических агентов; добавок к кардиоплегическим растворам для искусственного кровообращения, вспомогательных средств для тромболитической терапии, и в качестве противо- диаррейных агентов. Соединения данного изобретения могут быть полезными при терапии инфаркта миокарда; лечения заболеваний периферических сосудов /например, болезни Ренод'а и болезни Такаясу/, для лечения сердечной гипертрофии /например, гипертрофической кардиомиопатии/; лечения первичной легочной гипертензии /например, плексогенической, эмболической/ у взрослых и у новорожденных и легочной гипертензии вторичной по отношению к сердечной недостаточности, радиации и хемотерапевтического повреждения, или других травм; при лечении сосудистых нарушений центральной нервной системы /таких как удар, мигрень и субарахноидное кровотечение/; лечении расстройств в поведении, связанных с центральной нервной системой; при лечении желудочно-кишечных заболеваний, таких как язвенный колит, болезнь Крона, повреждений слизистой желудка, язвенной и ишемической болезни пищеварительного тракта; лечении заболевания желчного пузыря или желчных протоков, таких как холангит; при лечении панкреатита; для регулирования роста клеток; при лечении доброкачественной гипертрофии простаты; рестеноза после ангиопластии или после каких-либо процедур, включающих трансплантацию; при терапии застойной сердечной недостаточности, включая ингибирование фиброза; при ингибировании дилатации левого желудочка, реконструкции и дисфункции его; и при лечении гепатотоксичности и внезапной смерти. Соединения данного изобретения могут быть полезными при лечении заболеваний серповидных эритроцитов, включающих инициирование и/или эволюцию болевых кризов при данной болезни; при лечении губительных последствий ET-продуцирующих опухолей, таких как гипертензия, являющаяся результатом гемангиоперацитомы; лечении ранних и прогрессирующих заболеваний печени и повреждений, включая сопутствующие осложнения /например, гепатотоксичность, фиброз и цирроз/; при лечении спастических болезней мочевого тракта и/или мочевого пузыря; лечении гепаторенального синдрома; при лечении иммунологических заболеваний, включая васкулит, такой как волчанка, общий склероз, смешанная криоглобулинемия; и при лечении фиброза, связанного с ренальной дисфункцией и гепатотоксичностью. Соединения данного изобретения могут быть полезны при лечении метаболических и нейрологических расстройств; при раке; при инсулинзависимом и неинсулин-зависимом сахарном диабете; при нейропатии; ретинопатии; при материнском респираторном дистресс-синдроме; при дисменорее; эпилепсии; геморрагическом и ишемическом ударе; костной реконструкции; псориазе; и при хронических воспалительных заболеваниях; таких как ревматоидный артрит, остеоартрит, саркоидоз и экзематозный дерматит /все типы дерматита/.
Соединения данного изобретения могут также преобразовываться в готовые формы препаратов в сочетании с ингибиторами эндотелин-конвертирующих ферментов /ECE/, такими как фосфорамидон; антагонистами тромбоксановых рецепторов; средствами, способствующими раскрытию калиевых каналов, ингибиторами тромбина /например, хирудином и аналогичными/; ингибиторами фактора роста, такими как модуляторы PDGF активности; антагонистами фактора активации тромбоцитов /PAF/; антагонистами рецептора ангиотензина II /AII/; ингибиторами ренина; ингибиторами ангиотензинконвертирующих ферментов /АСЕ/, такими как каптоприл, зофеноприл, фозиноприл, церанаприл, или - цеприл, эналаприл, делаприл, пентоприл, хинаприл, рамиприл, лизиноприл и соли таких соединений, ингибиторами нейтральной эндопептидазы /NEP/; Двойными NEP-ACE ингибиторами; ингибиторами НМГ СоА редуктазы, такими как правастатин и мевакор, ингибиторами сквален-синтетазы; секвестрантами желчной кислоты; такими как квестран; блокаторами кальциевых каналов; активаторами калиевых каналов; бетаадренэргическими агентами, антиаритмическими агентами; диуретиками, такими как хлоротиазид, гидрохлоротиазид, флуметиазид, гидрофлуметиазид, бендрофлуметиазид, метилхлоротиазид, трихлорметиазид, политиазид или бензотиазид, а также этакриновая кислота, трикринафен, хлорталидон, фуросемид, музолимин, буметанид, триамтерен, амилорид и спиронолактон и соли таких соединений, и тромболитическими агентами, такими как активаторы тканевого плазминогена /тРА/, рекомбинантный тРА, стрептокиназа, урокиназа, проурокиназа и комплекс активатора стрептокиназы анизоилированного плазминогена /APASAC/. Если соединения формируются в виде фиксированной дозы, такие комбинационные продукты содержат соединения данного изобретения в интервале доз, описанном ниже, и другие фармацевтически активные агенты в пределах принятого интервала доз. Соединения данного изобретения могут также формулироваться в виде готовых форм в сочетании с полезными или полезными в сочетании с ними, противогрибковыми и иммуноподавляющими агентами, такими как амфотерацин B, циклоспорины и аналогичные, для противодействия гломерулярному сокращению и вторичной нефротоксичности к таким соединениям. Соединения данного изобретения могут также использоваться в сочетании с гемодиализом.
Соединения изобретения могут назначаться орально или парентерально различным видам млекопитающих, которые известны как подверженные таким заболеваниям, например, людям, в эффективном количестве в интервале доз примерно от 0,1 до 100 мг/кг, предпочтительно примерно от 0,2 до 50 мг/кг, и более предпочтительно примерно от 0,5 до 25 мг/кг /или примерно от 1 до 2500 мг, предпочтительно примерно от 5 до 2000 кг/ в виде однократной дозы или в виде суточных доз, разделенных на 2-4 раза.
Активное вещество может использоваться в виде композиции, такой как таблетки, капсулы, растворы или суспензии, содержащей примерно от 5 до 500 мг соединения или смеси соединений формулы I на единичную дозу или в топической форме для заживления ран /0,01 - 5% по весу соединения формулы I, 1 - 5 обработок в день/. Они могут компаундироваться обычным образом с физиологически приемлемым носителем, эксципиентом, связующим, консервирующим агентом, стабилизатором, вкусовым агентом и др., или с топическим носителем, таким как Пластибаз /минеральное масло, желированное полиэтиленом/, как это принято в обычной фармацевтической практике.
Соединения изобретения могут также назначаться топически для лечения заболеваний периферических сосудов, и будучи таковыми их готовят в виде кремов или мазей.
Соединения формулы I готовят также в виде композиций, таких как стерильные растворы или суспензии для парентерального назначения. Примерно от 0,1 до 500 мг соединения формулы I смешивается с физиологически приемлемым разбавителем, носителем, эксципиентом, связующим, консервирующим агентом, стабилизатором и др. , в форме единичной дозы, принятой в обычной фармацевтической практике. Количество активного вещества в этих композициях и препаратах является таким, чтобы получилась подходящая доза в указанном интервале.
Соединения настоящего изобретения могут быть получены следующим образом (см. схему I в конце описания).
Как показано на приведенной схеме I, целевые соединения 4 могут быть получены с помощью катализируемого Pd /O/ сочетания соответствующим образом замещенного фенилсульфонамид-2-бороновокислотного промежуточного соединения 2 с 4- гетероциклическим арилгалогенидом I в присутствии подходящего основания, такого как водный карбонат калия, и растворителя, такого как смесь толуола и этанола.
Бороновая кислота (промежуточное соединение 2) может быть получено из 2-бромфенилсульфонамида 5 /получение которого описано в EP публикации N 0569193 /1993/ с помощью литиирования подходящим алкиллитием (таким как н-бутиллитий), с последующей обработкой триалкилборатом (например, триизопропилборатом/ и, наконец, добавления водной кислоты, такой как водная соляная кислота (см. схему II в конце описания).
"Prot" на схеме II представляет соответствующую защитную группу для сульфонамидной функциональной группы, также описанную в ЕР публикации N 0569193 /1993/.
Целевые соединения могут также синтезироваться с помощью альтернативного способа, показанного на схеме III в конце описания.
Как показано выше, 4 - гетероциклический арилгалогенид 6 /смотри также соединение 1/ может превращаться в бороново-кислотное промежуточное соединение 7 с помощью показанной последовательности реакций. Данное соединение при катализируемом Pd/O/ сочетании с соединением 5 может давать биарильный аналог 3, который при снятии защиты может приводить к конечному соединению 4. В некоторых случаях гетероатомы J и K или L могут требовать защиты для получения бороновой кислоты 7, и/или для облегчения реакции сочетания /присоединения/ для получения соединения 3. /Например, когда J и K или L представляют N, одна из групп может защищаться подходящей защитной группой, такой как третбутоксикарбонил и др./. В некоторых случаях также бороновая кислота может заменяться видами олова и/или галоидная группа может заменяться фрагментом - OSO2 CF3 для проведения катализируемой Pd реакции сочетания.
Что касается общих подходов или принципов при биарильном синтезе, см. публикацию Bringmann и др. Angew. Chem. Inst., англ. изд. 29 /1990/ 977 - 991.
На приведенных выше схемах выбираются конкретные группы R11 и R14, чтобы они были совместимы с показанными условиями реакции. Дополнительно, конкретные группы R11 - R14 могут превращаться в альтернативные R11 - R14 группы, или перед, или после сочетания соединения 1 с соединением 2, или соединения 5 с соединением 7, с использованием методов, известных в данной области техники.
СИНТЕЗЫ СОЕДИНЕНИЙ 1 и 6
Соединения 1 и 6 могут получаться согласно следующим схемам, 2 -арилоксазолы получаются, как показано на схеме IV, Методы A-H; 4- арилоксазолы получаются, как показано на схеме V, методы A-B; 5- арилоксазолы получаются, как изображено на схеме VI, методы A-B; тиазолы получаются, как показано на схеме VII, методы A-B; имидазолы получаются, как показаны на схеме VIII; 2- фенилалкилоксазолы получаются, как показано на схеме IX, методы A-B; пиразолы получаются, как изображено на схеме X; 3-арилизоксазолы получаются, как показано на схеме XI; 5-арилизоксазолы получаются, как показано на схеме XII; и N-арилимидазолы получаются согласно схеме XIII. На этих схемах R11 и R12 выбираются также так, чтобы быть совместимыми с показанными условиями реакции (схемы IV-XIII см. в конце описания).
А. 2-Арилоксазолы (см. схему IV, метод A).
Ациламино соединение 9 получается, как показано выше, и может циклизоваться в оксазол 10 с использованием разнообразных дегидратирующих агентов. Для информации об этом и других методах см. публикацию: Lakhan и др., Adv. Het Chem., 17 /1974/, 99.
Схема IV. Метод B (см. в конце описания).
Как показано, нагревание вместе смеси бензамида II и α- галоид-соединения 12 дает соответствующий оксазол 13. Данный метод широко используется для получения 2,4 - дизамещенных оксазолов. Для обзора см.: Lakhan и др., Ad.Het.Chem., 17, /1979/99-211.
Схема IV. Метод C (см. в конце описания).
Сложный эфир 15 может получаться или путем реакции α- галоидкетона с бензойной кислотой 14 в присутствии основания, такого как триэтиламин, или с помощью сложной этерификации соответствующим α- гидроксикетоном. Соединение 15 при обработке ацетатом аммония в уксусной кислоте дает оксазол 16.
Схема IV. Метод D (см. в конце описания).
Некоторые ацетиленовые карбинолы, такие как соединение 17, могут реагировать непосредственно с арилнитрилом 18, давая 5 - метилоксазол 19.
/см., например, Y.Yura. Японский патент 29849 /1964/.
Схема IV. Метод E (см. в конце описания).
Ацетиленовый амид 22 при нагревании циклизуется в производное оксазола 23.
Схема IV. Метод F (см. в конце описания).
4,5 - незамещенный оксазол 26 может получаться с помощью конденсации 4 - бромбензамида II с виниленкарбонатом 25 при высокой температуре в присутствии такого агента, как полифосфорная кислота. /См., например, публикацию Ferrini и др., Angew. Chem. Internat. Ed., том 2, 1963, 99/.
Схема IV. Метод G (см. в конце описания).
Циклизация N-/2,2-дихлорэтил/ амидного производного 27, полученного с помощью способов, известных в технике, в присутствии подходящего основания, такого как этилат натрия, может также давать оксазольное производное 26. /См., например, патент США N 3953465/.
Схема IV. Метод H (см. в конце описания).
Нагревание вместе смеси акрилоилхлорида 21 с оксимом 29, где R1 и R2 представляют алкил, полученным по известным в технике способам, может давать производное оксазола 10 /См., например, Bhatt, M.V. and Reddy, A.S., Tet. Lett., 21, 2359 /1980/.
Схема IV. Метод I (см. в конце описания).
Нагревание вместе смеси акрилоихлорида 21 с триазолом 25, в котором R представляет триметилсилил, полученным по способам, известным в технике, в подходящем растворителе, таком как толуол, может давать производное оксазола 26 /см., например Williams, E.L., Tet. Lett., 33, 1033-1036 /1992//.
Производное оксазола 26 можно также получить с помощью обработки акрилоилхлорида 21 триазолом /в котором R представляет водород/ в присутствии подходящего основания, такого как карбонат калия, с последующим нагреванием смеси до оптимальной температуры.
В. 4- Арилоксазолы
Схема V, Метод A (см. в конце описания).
Обработка α- бромацетофенонового производного 30 амидом при высоких температурах /обычно 130 - 150oC/ дает 4- арилоксазол 31.
Схема V. Метод B (см. в конце описания).
Некоторые α- металлированные изонитрилы 32, получаемые по методам, известным в технике, взаимодействуют с ацилгалогенидами, имидазолами или другими активированными ацильными группами, давая 2-незамещенные оксазолы 33, в которых R2 представляет алкил или арил.
C. 5-Арилоксазолы
Схема VI. Метод A (см. в конце описания).
Ацилирование α- аминоацетофенона 34 ацилхлоридом дает соединение 35. Соединение 35 после циклизации с использованием подходящего дегидратирующего агента, такого как серная кислота, дает оксазол 36. /Данный способ аналогичен способу, описанному на схеме IV, способ А/.
Схема VI. Способ B (см. в конце описания).
4-Галоидбензальдегид 37 обрабатывается тозилметилизоцианидом 38 в присутствии основания, такого как карбонат калия, в подходящем растворителе, таком как метанол, давая 5 - арилоксазольное производное 39. /См. например, А. М. Van Leusen и др., Tet. Lett., 2369 /1972//.
D. Тиазолы
Схема VII. Метод A (см. в конце описания)
4-Бромфенилбороновая кислота 41 может связываться с соответствующим образом замещенным 2-бромтиазолом 42 в присутствии Pd/O/ катализатора и подходящего основания /например, водного карбоната калия/ и растворителя, давая тиазол 40.
Схема VII. Метод B (см. в конце описания).
Конденсация п-бромбензонитрила 18 с тиокетоном дает непосредственно тиазольное производное 44.
E.Имидазолы
Схема VIII (см. в конце описания).
Конденсация производного бензальдегида 37 с глиоксалем и аммиаком дает 2-арилимидазольное производное 45. /См., например, патент США N 3682949/. Данное соединение может далее замещаться с помощью реакции его с алкилгалогенидом в присутствии подходящего основания, давая например, N-алкил-производное 46.
Относительно синтеза имидазола смотри публикацию Adv. Het. Chem., 27 /1980/, 241-323.
F. 2-фенилалкилоксазолы
Схема IX. Метод A (см. в конце описания)
2-Фенилалкилоксазолы 48, в которых p представляет 1 или 2, незамещенные в 4 и 5 положениях, могут получаться с помощью нагревания вместе фенилалкиламида 47 вместе с виниленкарбонатом 25 в присутствии агента, такого как полифосфорная кислота.
Схема IX. Метод B (см. в конце описания).
2-Арилалкил-4-замещенный-оксазол 51, в котором R1 представляет алкил, и n представляет 1 или 2, может получаться исходя из нитрила 49, как показано выше. /См., например, патент США N 4168379/.
С. Пиразолы
Схема X (см. в конце описания).
Производное пиразола 52 может быть получено с помощью нагревания арилгидразина 53 вместе с эпихлоргидрином в присутствии подходящего основания, такого как триэтиламин.
H. 3-Арилизоксазолы
Схема XI (См. в конце описания).
Обработка оксима 54, полученного по способам, известным в технике, смесью HCl/оксон, и последующая обработка основанием, таким как триэтиламин, дает арилнитрилоксид. Арилнитрилоксид обычно не выделяется, а подвергается реакции с винилацетатом, а затем смесь нагревается в кислоте /например, HCl/ в подходящем растворителе, таком как этанол, давая производное 3-арилизоксазола 55.
1. 5-Арилизоксазолы
Схема XII (см. в конце описания).
α,β-Ненасыщенный кетон 56, полученный по способам, известным в технике, при обработке гидроксиламином дает соответствующее производное оксима. Циклизация данного материала в присутствии йода и иодида калия дает производное 5 - арилизоксазола 57. R1 на данной схеме представляет алкил или арил. /См., например, J. Het. Chem., 30, 467/1993/.
J. N-Арилимидазолы
Схема XIII (см. в конце в конце описания).
N-Арилимидазольный аналог 59 может получаться с помощью стандартной реакции сочетания Улльмана, известного в технике, соединения 1,4-дибромбензола 58 с имидазолом в присутствии медной соли, такой как CuBr.
Данное изобретение далее будет описано с помощью следующих рабочих примеров, которые представляют предпочтительные воплощения изобретения. Эти примеры предназначены для иллюстрации, но не для ограничения.
Пример 1
N-(3,4-Диметил-5-изоксазолил)-4'- (2-оксазолил) [1,1'-бифенил]-2-сульфонамид
A. 2 /4-Бромфенил/оксазол
Смесь 4-бромбензолкарбоксамида /4 г, 20 ммолей/, виниленкарбоната /1,72 г, 20 ммолей/ и 10 г полифосфорной кислоты нагревалась при 170oC в течение 3 часов. После охлаждения смесь распределялась между 200 мл воды и 200 мл этилацетата. Водный слой экстрагировался двумя порциями по 150 мл этилацетата. Объединенная органическая жидкость промывалась 100 мл воды и 50 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 10:1 смеси гексан/этилацетат, давая соединение А /2.49 г, 56%/ в виде белого твердого вещества.
В. 2-Бороно-N-/3,4-диметил-5-изоксазолил/- N'-/метоксиэтоксиметил/-бензолсульфонамид
К раствору 2-бром-N-/3,4-диметил-5-изоксазолил/ N'-/метоксиэтоксиметил/ бензолсульфонамида /5.67 г, 13.52 ммолей полученного, как описано в ЕР 0563193 /1993// в 70 мл тетрагидрофурана при -78oC, н-бутиллития /2М раствора в циклогексане, 8.11 мл, 16.23 ммоля/ добавлялось на протяжении 10 минут. Получающийся раствор перемешивался при -78oC в течение 15 минут, и добавлялся триизопропилборат /1.52 г, 8.06 ммоля/.
Смесь затем подогревалась до комнатной температуры и перемешивалась в течение 2 часов. Смесь охлаждалась до 0oC, добавлялась 10% водная соляная кислота /120 мл/, и раствор перемешивался в течение 10 минут. Смесь концентрировалась до 120 мл и экстрагировалась 4 х 60 мл этилацетата. Объединенные органические экстракты промывались один раз 100 мл солевого раствора, сушились /сульфатом магния/ и концентрировались; давая соединение В /4.25 г 82%/ в виде светло-желтой смолы.
С. N-(3,4-Диметил-5-изоксазолил)-N-[(2- метоксиэтокси)метил]-4'-(2-оксазолил) [1,1'-бифенил]-2- сульфонамид
К раствору соединения В /315 мг, 0,82 ммоля/ добавлялось соединение А /456 мг, 2.05 ммоля/ и в 7,5 мл толуола и 6 мл 95% этанола в атмосфере аргона добавлялся тетракис/трифенилфосфин/ палладий /O/ /95 мг, 0.082 ммоля/ с последующим добавлением 4.5 мл 2 М водного карбоната натрия. Реакционная смесь нагревалась при 75oC в течение 4 часов, охлаждалась и разбавлялась 50 мл этилацетата. Органическая жидкость отделялась и промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 2:1 смеси гексан/этилацетат, давая соединение С /279 мг, 70%/ в виде бесцветной смолы.
D. N-(3,4-Диметил-5-изоксазолил)-4'-(2- оксазолил) [1,1'-бифенил]-2-сульфонамид
К раствору соединения С /276 мг, 0,57 ммоля/ в 10 мл 95% этанола добавлялось 10 мл 6 н. водной соляной кислоты и смесь нагревалась с обратным холодильником в течение 1 часа и 10 минут. Реакционная смесь концентрировалась, и величина pH раствора доводилась до 8 с использованием раствора бикарбоната натрия. Раствор затем подкислялся до pH 5 с помощью ледяной уксусной кислоты. Смесь экстрагировалась 3 х 40 мл этилацетата. Органическая жидкость промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием смеси 100:1 дихлорметана и метанола, давая целевое соединение /117 мг, 52%/ в виде белого твердого вещества.
Т. пл. 90-98oC /аморфное вещество/.
Анализ для C20H17N3O4S:
Вычислено: С 60,75, H 4,33, N 10,63, S 8,11.
Найдено: С 60,80, H 4,15, N 10,38, S 8,12.
Пример 2
N-(3,4-Диметил-5-изоксазолил)-4'- (2-тиазолил) [1,1'-бифенил]-2-сульфонамид
A. 2-(4-Бромфенил)тиазол
К раствору 4-бромфенилбороновой кислоты (3,01 г, 15 ммолей), 2 -бромтиазола (9,84 г, 60 ммолей) в 120 мл толуола и 96 мл 95% этанола в атмосфере аргона добавлялся тетракис (трифенилфосфин) палладий (0) (1,04 г, 0,9 ммоля), с последующим добавлением 72 мл 2 М водного карбоната натрия. Реакционная смесь нагревалась при 75oC в течение 1 часа и 15 минут, охлаждалась и разбавлялась 300 мл этилацетата. Органическая жидкость отделялась и промывалась 100 мл воды и 100 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 30: 1 гексан/этилацетатной смеси, давая соединение А /2,0 г, 56%/ в виде белого твердого вещества.
В. N-(3,4-Диметил-5-изоксазолил)-N-[(2- метоксиэтокси)метил]-4'-(2-тиазолил)[1,1'-бифенил]-2 -сульфонамид
К раствору соединения В из примера 1 (320 мг, 0,83 ммоля) и соединения А (400 мг, 1,67 ммоля) в 7,5 мл толуола и 6 мл 95% этанола в атмосфере аргона добавлялся тетракис (трифенилфосфин) палладий (0) (96 мг, 0,083 ммоля), а затем 4,5 мл 2 М водного карбоната натрия. Реакционная смесь нагревалась при 75oC в течение 3 часов, охлаждалась и разбавлялась 50 мл этилацетата. Органическая жидкость отделялась и промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 2,5:1 смеси гексана и этилацетата, давая соединение В /291 мг, 70%/ в виде бесцветной смолы.
С. N-(3,4-Диметил-5-изоксазолил)-4'-(2-тиазолил) [1,1' -бифенил]-2-сульфонамид
К раствору соединения В (290 мг, 0,58 ммоля) в 10 мл 95% этанола добавлялось 10 мл 6 н. водной соляной кислоты и смесь нагревалась с обратным холодильником в течение 1 часа. Реакционная смесь концентрировалась и величина pH раствора доводилась до 8 с использованием раствора бикарбоната натрия. Смесь затем подкислялась до pH 5 с помощью ледяной уксусной кислоты. Смесь экстрагировалась 3 раза 40-мл порциями этилацетата. Органическая жидкость промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 100: 1 смеси дихлорметана и метанола, давая целевое соединение (180 мг, 75%) в виде не совсем белого твердого вещества.
Т. пл. 87-97oC /аморфное/.
Анализ для C20H17N3O3S2• 0,34 H2O:
Вычислено: С 57,52, H 4,27, N 10,06, S 15,35.
Найдено: С 57,68, H 4,08, N 9,90, S 15,06.
Пример 3
N-(3,4-Диметил-5-изоксазолил)-4'-(4,5-диметил) 2- оксазолил) [1,1'-бифенил] 2-сульфонамид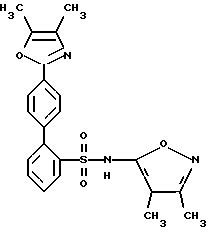
А. 4-Бромбензойная кислота, 2-оксо-1-метилпропиловый эфир
К 3-гидрокси-2-бутанону /1,32 г, 15 ммолей/ и 4-бромбензоилхлориду (3,29 г, 15 ммолей) в 15 мл дихлорметана при 0oC добавлялось по каплям 5 мл пиридина. Реакционная смесь перемешивалась при комнатной температуре в течение 5 часов, добавлялось 150 мл этилацетата, и смесь фильтровалась. Фильтрат промывался 2 х 50 мл 10% соляной кислоты, 30 мл воды и 30 мл солевого раствора, сушился и концентрировался. Остаток хроматографировался на силикагеле с использованием 10:1 смеси гексана и этилацетата, давая соединение А (3,4 г, 84%) в виде белого твердого вещества.
В. 2-(4-Бромфенил)-4,5-диметоксазол
Смесь соединения А (3,4 г, 12,54 ммоля), ацетата аммония (9,67 г, 125,4 ммолей) и 10 мл уксусной кислоты нагревалась при 100oC в течение 4 часов. После охлаждения смесь распределялась между 150 мл воды и 200 мл этилацетата. Органическая жидкость промывалась 50 мл воды и 50 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 25: 1 смеси гексана и этилацетата, давая соединение В (1,52 г, 48%) в виде белого твердого вещества.
С. N-(3,4-Диметил-5-изоксазолил)-4'-(4,5 - диметил-2-оксазолил)-N-[(2-метоксиэтокси)метил] [1,1'- бифенил]-2-сульфонамид
К раствору соединения В из примера 1 (320 мг, 0,83 ммоля) и соединения В из приведенной выше стадии (420 мг, 1,67 ммоля) в 7,5 мл толуола и 6 мл 95% этанола в атмосфере аргона добавлялся тетракис(трифенилфосфин) палладий (0) (96 мг, 0,083 ммоля), а затем 4,5 мл 2 М водного карбоната натрия. Реакционная смесь нагревалась при 75oC в течение 4 часов, охлаждалась и разбавлялась 50 мл этилацетата. Органическая жидкость отделялась и промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 2:1 смеси гексан/этанол, давая соединение С (300 мг, 70%) в виде бесцветной смолы.
D. N-(3,4-Диметил-5-изоксазолил)-4'-(4,5- диметил-2-оксазолил) [1,1'-бифенил]-2-сульфонамид.
К раствору соединения С (300 мг, 0,59 ммоля) в 10 мл 95% этанола добавлялось 10 мл 6 н. водной соляной кислоты, и смесь нагревалась с обратным холодильником в течение 1 часа. Реакционная смесь концентрировалась, и величина pH раствора доводилась до 8 с использованием раствора бикарбоната натрия. Смесь затем подкислялась до pH 5 ледяной уксусной кислотой. Смесь экстрагировалась 3x40 мл этилацетата. Органическая жидкость промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 1:1 смеси гексан/этилацетат, давая целевое соединение (178 мг, 72%) в виде белого твердого вещества.
Т. пл. 96 - 102oC /аморфное/.
Анализ для C22H21N3O4S • 0,24 H2O:
Вычислено: С 61,76, H 5,06, N 9,82, S 7,49.
Найдено: С 61,67, H 4,76, N 9,91, S 7,59.
Пример 4
N-(3,4-Диметил-5-изоксазолил)-4'- (5-оксазолил) [1,1-бифенил]-2-сульфонамид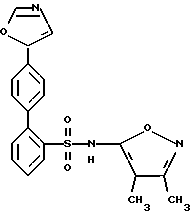
A. 5-(4-Бромфенил)оксазол
Смесь 4,74 г (25,6 ммоля) п-бромбензальдегида, 5,0 г (25,6 ммоля) тозилметилизоцианида и 4,25 г (30,7 моля) безводного карбоната калия в 150 мл метанола нагревалась с обратным холодильником в течение 3 часов. Растворитель затем выпаривался, и добавлялось к остаточному твердому веществу 150 мл воды. Рыжевато-белое твердое вещество отфильтровывалось и промывалось несколько раз водой; а затем сушилось, давая соединение А (3,65 г, 64%).
В. N-(3,4-Диметил-5-изоксазолил)-N-[(2-метоксиэтокси)метил] - 4'-(5-оксазолил) [1,1'-бифенил]-2-сульфонамид
К раствору 0,8 г (2,08 ммоля) соединения В из примера 1 и 0,12 г (0,1 ммоля) тетракис (трифенилфосфин) - палладия (0) в 25 мл толуола в атмосфере аргона добавлялось 15 мл 2 М водного карбоната натрия, а затем 0,70 г (3,12 ммоля) соединения А в 15 мл 95% этанола. Смесь нагревалась с обратным холодильником в течение 3 часов, разбавлялась 100 мл воды и экстрагировалась 3 х 75 мл этилацетата. Объединенные органические экстракты промывались один раз 100 мл солевого раствора, сушились и выпаривались. Остаток хроматографировался на 50 г силикагеля с использованием смеси гексанов и этилацетата 2:1, давая 0,49 г (49%) соединения B в виде бесцветной смолы.
С. N-(3,4-Диметил-5-изоксазолил)-4'-(5-оксазолил) [1,1-бифенил]-2-сульфонамид
К раствору 0,49 г (1,01 ммоля) соединения В в 10 мл 95% этанола добавлялось 10 мл 6 н. водной соляной кислоты, и смесь нагревалась с обратным холодильником в течение 1 часа. Смесь затем концентрировалась и разбавлялась 50 мл воды. Раствор нейтрализовался до pH 7 с использованием насыщенного водного бикарбоната натрия, а затем подкислялся до pH 4 с использованием ледяной уксусной кислоты. Полученное белое твердое вещество отфильтровывалось и сушилось (0,37 г). Кристаллизация из смеси дихлорметана /этилацетата/ гексанов давала 0,23 г (58%) целевого соединения в виде белого твердого вещества.
Т. пл. 189-191oC.
Анализ для C20H17N3O4S • 0,28 H2O:
Вычислено: С 60,00, H 4,42, N 10,49, S 8,01.
Найдено: С 60,10, H 4,17, N 10,39, S 8,04.
Пример 5
N-(3,4-Диметил-5-изоксазолил)-4'- (4-оксазолил) [1,1'-бифенил]-2-сульфонамид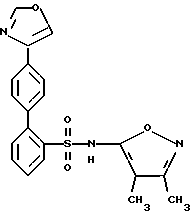
A. 4-(4-Бромфенил)оксазол
Смесь 5,0 г (18 ммолей) α,п-дибромацетофенона и 4,05 г (83,9 ммоля) формамида перемешивалась на масляной бане при 130oC в течение 3 часов. Смесь затем выливалась в 150 мл смеси льда и воды, и раствор экстрагировался 3 х 100 мл эфира. Объединенные эфирные экстракты промывались один раз водой, сушились и выпаривались. Остаток хроматографировался на 200 мл силикагеля с использованием смеси гексаны/этилацетат 3:1, давая 1,3 г (32%) соединения A в виде светло-коричневого твердого вещества.
В. N-(3,4-Диметил-5-изоксазолил)-N-(2- метоксиэтокси)метил-4'-(4-оксазолил) [1,1'-бифенил]-2- сульфонамид
К раствору 0,668 г (1,74 ммоля) соединения В из примера 1 и 0,104 г (0,09 ммоля) тетракис (три-фенилфосфин) палладия (0) в 25 мл толуола в атмосфере аргона добавлялось 15 мл 2 М водного карбоната натрия, а затем 0,52 г (2,32 ммоля) соединения А в 15 мл 95% этанола. Смесь нагревалась с обратным холодильником в течение 3 часов, разбавлялась 100 мл воды и экстрагировалась 3 х 75 мл этилацетата. Объединенные органические экстракты промывались один раз 100 мл солевого раствора, сушились и выпаривались. Остаток хроматографировался на 50 г силикагеля с использованием смеси гексанов и этилацетата 2:1, давая 0,43 г (51%) соединения B в виде бесцветной смолы.
С. N-(3,4-Диметил-5-изоксазолил)-4'-(4-оксазолил) [1,1'-бифенил]-2-сульфонамид
К раствору 0,75 мл (1,55 ммоля) соединения В в 8 мл ацетонитрила при 0oC в атмосфере аргона добавлялось 2,01 г триметилсилилхлорида и 2,73 г иодида натрия, и смесь перемешивалась при комнатной температуре в течение 1 часа. Смесь затем разбавлялась 10 мл воды и экстрагировалась 100 мл этилацетата. Органический слой промывался 10 мл насыщенного водного тиосульфата натрия, сушился и выпаривался. Данный материал очищался с помощью препаративной PHLC с обращенной фазой на 30 х 500 мм ODS S10 колонке с использованием 68% растворителя А (90% метанола, 10% воды, 0,1% трифторуксусной кислоты) и 32% растворителя В (10% метанол, 90% вода, 0,1% трифторуксусная кислота). Соответствующие фракции собирались и нейтрализовались водным бикарбонатом натрия до pH 7 и концентрировались до 10 мл. Раствор подкислялся до pH 4 с использованием ледяной уксусной кислоты, и белое твердое вещество отфильтровывалось и сушилось, давая 0,33 г (54%) целевого соединения.
Т. пл. 85-93oC (аморфное)
Анализ для C20H17N3O4S•0,21 H2O:
Вычислено: С 60,18, H 4,40, N 10,53, S 8,03.
Найдено: С 60,27, H 4,05, N 10,44, S 7,88.
Пример 6
N-(3,4-Диметил-5-изоксазолил)-4'-(2-метил-4- оксазолил) [1,1-бифенил]-2-сульфонамид
A. 4-(4-Бромфенил)-2-метилоксазол
Смесь 2,4-дибромацетофенона (2,78 г, 10 ммолей) и ацетамида (1,48 г, 25 ммолей) нагревалась при 130oC в течение 3 часов. Данная смесь выливалась на 30 г льда, и добавлялось 150 мл этилацетата. Органический слой отделялся и промывался 30 мл 1 н. гидроокиси натрия, 30 мл 1 н. соляной кислоты и 30 мл солевого раствора, сушился и концентрировался. Остаток хроматографировался на силикагеле с использованием смеси 15:1 гексан/этилацетат, давая соединение А (1,29 г, 54%) в виде белого твердого вещества.
B. N-(3,4-Диметил-5-изоксазолил)-N- [(2-метоксиэтокси)метил] - 4'-(2-метил-4-оксазолил) [1,1'-бифенил] -2-сульфонамид
К раствору соединения А (402 мг, 1,7 ммоля) и соединения В из примера 1 (259 мг, 0,68 ммоля) в 6,5 мл толуола и 5,2 мл 95% этанола в атмосфере аргона добавлялся тетракис (трифенилфосфин) палладий (0) (0,78 мг, 0,068 ммоля), а затем 3,9 мл 2 M водного карбоната натрия. Реакционная смесь нагревалась при 75oC в течение 3,5 часов, охлаждалась и разбавлялась 40 мл этилацетата. Органическая жидкость отделялась и промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 2:1 гексан/этилацетат, давая соединение В (183 мг, 54%) в виде бесцветной смолы.
С. N-(3,4-Диметил-5-изоксазолил)-4'-(2-метил-4- оксазолил) [1,1'-бифенил]-2-сульфонамид
К раствору соединения В (180 мг, 0,36 ммоля) в 6 мл 95% этанола добавлялось 6 мл 6 н. водной соляной кислоты, и смесь нагревалась в условиях дефлегмации в течение 55 минут. Реакционная смесь концентрировалась, и величина pH раствора доводилась до 8 с использованием раствора бикарбоната натрия. Раствор затем подкислялся до pH 5 ледяной уксусной кислотой. Смесь экстрагировалась 3 х 30 мл этилацетата. Органическая жидкость промывалась 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 100:1 дихлорметан/метанол, давая целевое соединение (56 мг, 38%) в виде светло-желтого твердого вещества.
Т. пл. 90 - 100oC /аморфное/.
Анализ для C21H19N3O4S:
Вычислено: С 61,60, H 4,68, N 10,26, S 7,83.
Найдено: С 61,56, H 4,33, N 9,85, S 7,94.
Пример 7
N-(3,4-Диметил-5-изоксазолил)-4'- (4-метил-2-оксазолил) [1,1'- -бифенил] -2-сульфонамид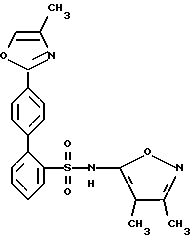
A. 2-(4-Бромфенил)-4-метилоксазол
4-Бромбензонитрил (9,1 г, 50 ммолей) и пропаргиловый спирт (2,8 г, 50 ммолей) добавлялись по каплям в 12,5 мл концентрированной серной кислоты при -15oC. Реакционная смесь перемешивалась при 0oC в течение 3 часов, подогревалась до комнатной температуры медленно и перемешивалась на протяжении ночи. Смесь выливалась в 200 мл ледяной воды, нейтрализовалась бикарбонатом натрия и экстрагировалась 3 х 200 мл этилацетата. Объединенная органическая жидкость промывалась 50 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 30: 1 смеси гексан/этилацетат, давая соединение А (1,44 г, 12%) в виде белого твердого вещества.
В. N-(3,4-Диметил-5-изоксазолил)-N-[(2-метоксиэтокси)метил] - 4'-[(4-метил-2-оксазолил)] [1,1'-бифенил]-2-сульфонамид
К раствору соединения В из примера 1 (320 мг, 0,83 ммоля) и соединения А (397 мг, 1,67 ммоля) в 7,5 мл толуола и 6 мл 95% этанола в атмосфере аргона добавлялся тетракис (трифенилфосфин) палладий (0) (96 мг, 0,083 ммоля), а затем 4,5 мл 2 М водного карбоната натрия. Реакционная смесь нагревалась при 75oC в течение 4 часов, охлаждалась и разбавлялась 50 мл этилацетата. Органическая жидкость отделялась, промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле и с использованием смеси 2:1 гексана и этилацетата, давая соединение В (300 мг, 72%) в виде бесцветной смолы.
С. N-(3,4-Диметил-5-изоксазолил)-4'-(4- метил-2-оксазолил) [1,1'-бифенил]-2-сульфонамид
К раствору соединения В (300 мг, 0,60 ммоля) в 10 мл 95% этанола добавлялось 10 мл 6 н. водной соляной кислоты, и смесь нагревалась с обратным холодильником в течение 1 часа. Реакционная смесь концентрировалась и величина pH раствора доводилась до 8 с использованием раствора бикарбоната натрия. Смесь затем подкислялась до pH 5 ледяной уксусной кислотой. Смесь экстрагировалась 3 х 40 мл этилацетата.
Органическая жидкость промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием смеси 100:1 дихлорметана и метанола, давая целевое соединение (200 мг. 81%) в виде белого твердого вещества.
Т. пл. 85 - 95oC /аморфное/.
Анализ для C21H19N3O4S • 0,25 H2O:
Вычислено: С 60,92, H 4,75, N 10,15 S 7,74.
Найдено: С 61,15, H 4,60, N 9,89, S 7,62.
Пример 8
N-(3,4-Диметил-5-изоксазолил)-4'- (5-метил-2- оксазолил) [1,1'-бифенил] -2-сульфонамид
A. 2-(4-Бромфенил)-5-метилоксазол
К 4-бромбензоилхлориду (4,39 г, 20 ммолей) в 40 мл дихлорметана при 0oC добавлялся пропаргиламин (1,10 г, 20 ммолей), а затем триэтиламин (4,05 г, 40 ммолей). Смесь перемешивалась при комнатной температуре в течение 40 минут. Добавлялось 150 мл этилацетата и смесь фильтровалась, фильтрат промывался 2 х 40 мл воды и 40 мл солевого раствора, сушился и концентрировался, давая 4-бром-N-(2-пропинил)бензамид. 4-Бром- N-(2-пропинил) бензамид добавлялся в охлажденные 47 мл концентрированной серной кислоты. Реакционная смесь перемешивалась при 5-10oC в течение 3 часов и при комнатной температуре на протяжении ночи. Смесь выливалась в 500 мл ледяной воды, нейтрализовалась карбонатом натрия до pH 8 и экстрагировалась трижды 250 мл порциями этилацетата. Объединенные органические экстракты промывались 200 мл воды и 100 мл солевого раствора, сушились и концентрировались, давая соединение А (4,5 г, 95%) в виде светло-желтого твердого вещества.
Т. пл. 61-63oC.
В. N-(3,4-Диметил-5-изоксазолил)-N-[(2-метоксиэтокси)метил]- 4'-(5-метил-2-оксазолил) [1,1'-бифенил]-2-сульфонамид
К раствору соединения В из примера 1 (320 мг, 0,83 ммоля) и соединения А (397 мг, 1,67 ммоля) в 7,5 мл толуола и 6 мл 95% этанола в атмосфере аргона добавлялся тетракис (трифенилфосфин) палладий (0) (96 мг, 0,083 ммоля) с последующим добавлением 4,5 мл 2 М водного карбоната натрия. Реакционная смесь нагревалась при 75oC в течение 3 часов, охлаждалась и разбавлялась 50 мл этилацетата. Органическая жидкость отделялась и промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 2:1 смеси гексан/этилацетат, давая соединение В (298 мг, 72%) в виде бесцветной смолы.
С. N-(3,4-Диметил-5-изоксазолил)-4'-(5-метил-2- оксазолил) [1,1-бифенил] -2-сульфонамид
К раствору соединения В (298 мг, 0,60 ммоля) в 10 мл 95% этанола добавлялось 10 мл 6 н. водной соляной кислоты, и смесь нагревалась с обратным холодильником в течение 1 часа. Реакционная смесь концентрировалась, и величина pH раствора доводилась до 8 с использованием раствора бикарбоната натрия. Раствор затем подкислялся до pH 5 ледяной уксусной кислотой. Смесь экстрагировалась 3 раза 40 мл порциями этилацетата. Органическая жидкость промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 100:1 смеси дихлорметана и метанола, давая целевое соединение (147 мг, 60%) в виде не совсем белого твердого вещества.
Т. пл. 90 - 100oC (аморфное).
Анализ для C21H19N3O4S:
Вычислено: С 61,60, H 4,68, N 10,26, S 7,83.
Найдено С 61,39, H 4,11, N 10,03, S 7,61.
Пример 9
N-(3,4-Диметил-5-изоксазолил)-4'- (1H-пиразол-1-ил) [1,1'-бифенил]-2-сульфонамид
A. 1-(4-Бромфенил)-IH-пиразол
К этилхлоргидрину (4 г, 43,23 ммоля) и 4-бромфенилгидразинхлоргидрату (19,32 г, 86,46 ммоля) в 20 мл 60% этанола добавлялся по каплям триэтиламин (8,75 г, 12,05 ммоля). Смесь медленно подогревалась, а затем нагревалась с обратным
холодильником в течение 1 часа. Растворитель выпаривался, и остаток нагревался при 170oC в течение 30 минут и при 200oC еще в течение 10 минут. Добавлялось 150 мл воды, и смесь экстрагировалась три раза 200 мл порциями этилацетата. Объединенная органическая жидкость промывалась 50 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 40:1 смеси гексана и этилацетата, давая соединение А (2,92 г, 30%), которое кристаллизовалось из гексана, давая желтые иглы.
Т. пл. 72-74oC.
В. N-(3,4-Диметил-5-изоксазолил)-N-[(2- метоксиэтокси)метил] -4'-(1H-пиразол-1-ил) [1,1'- бифенил]-2-сульфонамид
К раствору соединения В из примера 1 (320 мг, 0,83 ммоля) и соединения А (372 мг, 1,67 ммоля) в 7,5 мл толуола и 6 мл 95% этанола в атмосфере аргона добавлялся тетракис (трифенилфосфин) палладий (0) (96 мг, 0,083 ммоля) с последующим добавлением 4,5 мл 2 М водного карбоната натрия. Реакционная смесь нагревалась при 75oC в течение 2,5 часов, охлаждалась и разбавлялась 50 мл этилацетата. Органическая жидкость отделялась, промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием смеси 3,5:1 гексан/этилацетат, давая соединение В (280 мг, 70%) в виде бесцветной смолы.
С. N-(3,4-Диметил-5-изоксазолил)-4'-(1H- пиразол-1-ил) [1,1'-бифенил]-2-сульфонамид
К раствору соединения В (260 мг, 0,58 ммоля) в 10 мл 95% этанола добавлялось 10 мл 6 н. водной соляной кислоты, и смесь нагревалась с обратным холодильником в течение 1 часа. Реакционная смесь концентрировалась, и величина pH доводилась до 8 с использованием раствора бикарбоната натрия. Смесь затем подкислялась до pH 5 ледяной уксусной кислотой. Смесь экстрагировалась три раза 40 мл порциями этилацетата. Органическая жидкость промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием смеси 100:0,8 дихлорметан/метанол, давая целевое соединение (161 мг, 70%) в виде не совсем белого твердого вещества.
Т. пл. 88-98oC (аморфное).
Анализ для C20H18N4O3S • 0,12 H2O:
Вычислено: С 60,56, H 4,64, N 14,12, S 8,08.
Найдено: C 61,26, H 4,52, N 13,96, S 8,06.
Пример 10
N-(3,4-Диметил-5-изоксазолил)-4'-[1-[(2-метоксиэтокси)метил] - 1H-имидазол-2-ил] [1,1'-бифенил]-2-сульфонамид
A. 2-(4-Бромфенил)-1H-имидазол
К 4-Бромбензальдегиду (9,25 г, 50 ммолей) и глиоксалю (40 вес.%, водный раствор, 11,6 мл, 80 ммолей) в 20 мл метанола добавлялось по каплям 60 мл 30% водного гидроксида аммония. Смесь перемешивалась при комнатной температуре на протяжении ночи. Растворитель выпаривался под вакуумом. Остаток слегка подщелачивался добавлением водной гидроокиси натрия и экстрагировался тремя порциями по 300 мл этилацетата. Объединенные органические экстракты судишись и концентрировались. Остаток растворялся в 100 мл метанола и фильтровался. Фильтрат концентрировался, а остаток растирался с 20 мл этилового эфира, давая соединение А в виде коричневого твердого вещества (1,8 г, 16%).
В. 2-(4-Бромфенил)-1-[(2-метоксиэтокси)метил]-1H- имидазол
К соединению А (400 мг, 1,79 ммоля) в 18 мл тетрагидрофурана добавлялся гидрид натрия 60% в минеральном масле (86 мг, 2,15 ммолей). Смесь перемешивалась при комнатной температуре в течение 10 минут, по каплям добавлялся метоксиэтоксиметилхлорид (335 мг, 2,59 ммоля). Реакционная смесь перемешивалась при комнатной температуре в течение 2 часов и концентрировалась. Добавлялось 100 мл этилацетата, и органическая жидкость промывалась 20 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 100:400:1 смеси гексана, этилацетата и триэтиламина, давая соединение В (390 мг, 70%).
С. N-(3,4-Диметил-5-изоксазол)-N- [(2-метоксиэтокси)метил]- 4'-[1-[(2-метоксиэтокси) метил]-1H-имидазол-2-ил] [1,1'- бифенил]-2-сульфонамид
К раствору соединения В из примера 1 (722 мг, 1,88 ммоля) и соединения В, полученного выше (390 мг, 1,25 ммоля), в 11,25 мл толуола и 9 мл 95% этанола в атмосфере аргона добавлялся тетракис (трифенилфосфин) палладий (0) (145 мг, 0,125 ммоля) с последующим добавлением 6,75 мл 2 М водного карбоната натрия. Реакционная смесь нагревалась при 75oC в течение 3 часов, охлаждалась и разбавлялась 75 мл этилацетата. Органическая жидкость отделялась, промывалась 15 мл воды и 15 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 100:0,2 смеси этилацетата и триэтиламина, давая соединение С (400 мг, 56%) в виде бесцветной смолы.
Д. N-(3,4-диметил-5-изоксазолил)-4'-[1-[(2-метокси)метил] -1H- имидазол-2-ил] [1,1'-бифенил]-2-сульфонамид
К раствору соединения С (400 мг, 0,70 ммоля) в 12 мл 95% этанола добавлялось 12 мл 6 н. водной соляной кислоты, и смесь нагревалась с обратным холодильником в течение 1 часа. Реакционная смесь концентрировалась и величина pH раствора доводилась до 8 с использованием раствора бикарбоната натрия. Раствор затем подкислялся до pH 5 ледяной уксусной кислотой. Затем добавлялось 200 мл этилацетата, и органическая жидкость промывалась 20 мл воды и 20 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием смеси 100:4:0,2 дихлорметан/метанол/гидроокись аммония, давая целевое соединение (210 мг, 62%), которое кристаллизовалось из смеси этилацетата и гексана, давая белые кристаллы. Т. пл. 81-84oC.
Анализ для C24H26N4O5S • 0,24 H2О:
Вычислено: С 59,20, H 5,48, N 11,51, S 6,58.
Найдено: С 59,25, H 5,42, N 11,46, S 6,39.
Пример 11
N-(3,4-Диметил-5-изоксазолил)-4'-[1-[(2- гидроксиэтокси)метил]-1H-имидазол-2-ил] [1,1'-бифенил]-2 -сульфонамид
A. N-(3,4-Диметил-5-изоксазолил)-4'-[1-[(2- гидроксиэтокси)метил]-1H-имидазол-2-ил] [1,1'-бифенил]-2- сульфонамид
К целевому соединению примера 10 (120 мг, 0,25 ммоля) в 2,5 мл дихлорметана при 0oC по каплям добавлялся трехбромистый бор (1 М раствор в дихлорметане, 0,37 мл, 0,37 ммоля). Реакционная смесь перемешивалась при 0-3oC в течение 45 минут. Добавлялось 5 мл насыщенного водного бикарбоната натрия, и смесь перемешивалась в течение 10 минут. Смесь затем подкислялась до pH 5 ледяной уксусной кислотой и экстрагировалась тремя порциями по 40 мл смеси 100: 5 дихлорметана и метанола. Объединенные органические экстракты сушились и концентрировались. Остаток очищался с помощью препаративной HPLC на колонке 30 х 500 мм ОДS S10 с использованием 62% растворителя А (10% метанол, 90% вода, 0,1% трифторуксусная кислота) и 38% растворителя В (90% метанол, 10% вода, 0,1% тетрагидрофуран), девая целевое соединение (80 мг, 69%) в виде белого твердого вещества. Т. пл. 93 - 103oC.
Анализ для C23H24N4O5S • 0,75 H2O
Вычислено: С 57,31, H 5,33, N 11,62, S 6,65.
Найдено: С 57,61, H 5,04, N 11,33, S 6,55.
Пример 12
N-(3,4-Диметил-5-изоксазолил)-4'- (1-метил-1H- имидазол-2-ил) [1,1'-бифенил]-2-сульфонамид, литиевая соль
A. 2-(4-Бромфенил)-1-метил-1H-имидазол
К соединению А из примера 10 (700 мг, 3,14 ммоля) в 7,8 мл тетрагидрофурана и 7,8 мл диметилформамида добавлялся гидрид натрия (60% дисперсия в минеральном масле, 151 мг, 3,77 ммоля). Смесь перемешивалась при комнатной температуре в течение 10 минут. По каплям добавлялся йодметан (891 мг, 6,28 ммоля). Реакционная смесь перемешивалась при комнатной температуре в течение 1 часа и концентрировалась. Добавлялось 100 мл этилацетата, и органическая жидкость промывалась 20 мл воды и 20 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием смеси 100: 1:0,1 дихлорметан/метанол/гидроокись аммония, давая соединение А (500 мг, 67%).
В. N-(3,4-Диметил-5-изоксазолил)-N-[(2-метоксиэтокси)метил]- 4'-(1-метил-1H-имидазол-2-ил) [1,1'-бифенил]-2-сульфонамид
К раствору соединения В из примера I (320 мг, 0,83 ммоля) и соединения А (395 мг, 1,67 ммоля) в 7,5 мл толуола и 6 мл 95% этанола в атмосфере аргона добавлялся тетракис (трифенилфосфин) палладий (0) (96 мг, 0,083 ммоля), а затем 4,5 мл 2М водного карбоната натрия. Реакционная смесь нагревалась при 75oC в течение 3 часов, охлаждалась и разбавлялась 50 мл этилацетата. Органическая жидкость отделялась и промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием смеси 100:1,5:0,1 дихлорметан/метанол/бикарбонат аммония, давая соединение А (204 мг, 61%) в виде бесцветной смолы.
С. Литиевая соль N-(3,4-Диметил-5-изоксазолил)-4'- (1-метил-1H-имидазол-2-ил) [1,1'-бифенил]-2- сульфонамида
К раствору соединения В (250 мг, 0,50 ммоля) в 9 мл 95% этанола добавлялось 9 мл 6 н. водной соляной кислоты, и смесь нагревалась с обратным холодильником в течение 1 часа. Реакционная смесь концентрировалась, и величина pH раствора доводилась до 8 с использованием раствора бикарбоната натрия. Раствор затем подкислялся до pH 5 ледяной уксусной кислотой. Смесь экстрагировалась 200 мл этилацетата, и органический слой промывался 20 мл воды и 20 мл солевого раствора, сушился и концентрировался. Остаток хроматографировался на силикагеле с использованием смеси 100:0,6:0,3 дихлорметан/метанол/бикарбонат аммония, давая N-(3,4-диметил-5-изоксазолил)-4'-(1-метил-1H- имидазол-2-ил) [1,1'-бифенил]-2-сульфонамид (189 мг, 92%), который растворялся в 1 н. гидроокиси лития, добавлялся на HP-20 колонку и элюировался водой, а затем смесью 10:3 воды и метанола, давая целевое соединение в виде белого твердого вещества. Т. пл. более 200oC разл.
Анализ для C21H19N4O3SLi•2,75 H2О:
Вычислено: С 54,37, H 5,32, N 12,08, S 6,91.
Найдено: С 54,58, H 5,05, N 11,87, S 6,80.
Пример 13
Литиевая соль N-(3,4-диметил-5-изоксазолил)-4'-(1H- имидазол-2-ил) [1,1'-бифенил]-2-сульфонамида
A. 1,1-диметилэтиловый эфир 2-(4-бромфенил)-1H- имидазол-1-карбоновой кислоты
К соединению А из примера 10 (446 мг, 2 ммоля) в 20 мл ацетонитрила добавлялись ди-трет-бутилдикарбонат (524 мг, 2,4 ммоля) и 4-диметиламинопиридин (24,4 мг, 0,2 ммоля). Реакционная смесь перемешивалась при комнатной температуре на протяжении ночи и концентрировалась. Остаток хроматографировался на силикагеле с использованием 6:1 смеси гексана и этилацетата, давая соединение А (500 мг, 77%) в виде светло-желтого масла.
В. 4'-[1-[(1,1-Диметилэтокси)карбонил]-1H- имидазол-2-ил]-N-(3,4-диметил-5-изоксазолил)-N- [(2-метоксиэтокси)метил] [1,1'-бифенил]-2-сульфонамид.
К раствору соединения В из примера 1 (496 мг, 1,29 ммоля) и соединения A (500 мг, 1,55 ммоля) в 11,25 мл толуола и 9 мл 95% этанола в атмосфере аргона добавлялся тетракис (трифенилфосфин) палладий (0) (149 мг, 0,129 ммоля), а затем 6,75 мл 2 М водного карбоната натрия. Реакционная смесь нагревалась при 75oC в течение 3 часов, охлаждалась и разбавлялась 75 мл этилацетата. Органическая жидкость отделялась и промывалась 15 мл воды и 15 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием смеси 40:60:0,2 гексана, этилацетата и триэтиламина, давая соединение В (380 мг, 51%) в виде бесцветной смолы.
С. Литиевая соль N-(3,4-диметил-5-изоксазолил)-4'- (1H-имидазол-2-ил)-[1,1'-бифенил]-2-сульфонамида
К раствору соединения В (380 мг, 0,65 ммоля) в 12 мл 95% этанола добавлялось 12 мл 6 н. соляной кислоты, и смесь нагревалась с обратным холодильником в течение 1 часа и 45 минут. Реакционная смесь концентрировалась, и величина pH раствора доводилась до 8 с использованием раствора бикарбоната натрия. Раствор затем подкислялся до pH 5 ледяной уксусной кислотой, экстрагировался тремя порциями по 80 мл смеси 100:5 дихлорметана и метанола. Органические экстракты сушились и концентрировались. Остаток растворялся в 1 н. гидроокиси лития и хроматографировался на HP-20 колонке, элюируемой водой, а затем смесью 10: 2 воды и метанола, давая целевое соединение в виде белого твердого вещества (180 мг, 69%) Т.пл. выше 220oC разл.
Анализ для C20H17N4O3SLi 2.06•H2O:
Вычислено: C 54,91, H 4,87, N 12,81, S 7,33.
Найдено: C 54,99, H 4,78, N 12,73, S 6,95.
Пример 14
N-(3,4-Диметил-5-изоксазолил)-4'-(5-метил-4- оксазолил)[1,1'-бифенил]-2-сульфонамид
A. 4-(4-Бромфенил)-5-метилоксазол
К 4'-бромпропиофенону (3,52 г, 16,5 ммолей) и формамиду (10,81 г, 240 ммолей) при 50oC по каплям добавлялся бром на протяжении 10 минут. Реакционная смесь нагревалась от 50oC до 130oC на протяжении 20 минут, а затем нагревалась при 130oC в течение 4 часов. После охлаждения добавлялось 150 мл этилацетата и жидкость промывалась 2 х 20 мл водой и 20 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле, давая соединение А (1,59 г, 45%).
В. N-(3,4-Диметил-5-изоксазолил)-N-[(2-метоксиэтокси)метил] - 4'-(5-метил-4-оксазолил) [1,1'-бифенил]-2-сульфонамид
К раствору соединения В из примера 1 (384 мг, 1,0 ммоля) и соединения А (408 мг, 1,7 ммоля) в 9 мл толуола и 7,2 мл 95% этанола в атмосфере аргона добавлялся тетракис (трифенилфосфин) палладий (0) (116 мг, 0,l0 ммоля), а затем 5,4 мл 2 М водного карбоната натрия. Реакционная смесь нагревалась при 75oC в течение 3 часов, охлаждалась и разбавлялась 60 мл этилацетата. Органическая жидкость отделялась и промывалась 15 мл воды и 15 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием смеси 2,5:1 гексана и этилацетата, давая соединение В (317 мг, 64%) в виде бесцветной смолы.
С. N-(3,4-Диметил-5-изоксазолил)-4'-(5-метил-4- оксазолил) [1,1'-бифенил]-2-сульфонамид
К раствору соединения В (300 мг, 0,60 ммоля) в 10 мл 95% этанола добавлялось 10 мл 6 н. водной соляной кислоты и смесь нагревалась с обратным холодильником в течение 1 часа. Реакционная смесь концентрировалась, и величина pH доводилась до 8 с использованием раствора бикарбоната натрия. Смесь затем подкислялась до pH 5 ледяной уксусной кислотой. Смесь экстрагировалась трижды 40 мл- выми порциями этилацетата, и органические экстракты промывались 10 мл воды и 10 мл солевого раствора, сушились и концентрировались. Остаток очищался с помощью препаративной ВЭЖХ на 30 х 500 мм ОДS S10 колонке с использованием 30% растворителя А (10% метанол, 90% вода, 0,1% трифторуксусная кислота) и 70% растворителя В (90% метанол, 10% вода, 0,1% тетрагидрофуран), давая целевое соединение (150 мг, 61%) в виде белого твердого вещества.
Т. пл. 86-96oC /атмосферное вещество/.
Анализ для C21H19N3O4S•0.16 H2О:
Вычислено: С 61,17, H 4,72, N 10,19, S 7,77.
Найдено: С 61,20, H 4,35, N 10,16, S 7,58.
Пример 15
N-(3,4-Диметил-5-изоксазолил)-4'- (1H-имидазол-1-илметил) [1,1'-бифенил] -2-сульфонамид
A. N-(3,4-Диметил-5-изоксазолил)-2-бром-бензолсульфонамид
К раствору 3,0 г (11,74 ммоля) 2- бромбензолсульфонилхлорида в 10 мл пиридина добавлялось 1,32 г (11,74 ммоля) 3,4- диметил-5-изоксазоламина. Смесь перемешивалась при комнатной температуре в атмосфере аргона на протяжении ночи, добавлялась к 150 мл ледяной воды и фильтровалась. Фильтрат подкислялся до pH 2 6 н. водной соляной кислотой, и серое твердое вещество отфильтровывалось и сушилось. Твердое вещество перекристаллизовывалось из смеси метанола и воды, давая 4,0 г (более 100%) соединения А в виде рыжевато-коричневых кристаллических игл /т. пл. 125-126oC, Rf = 0,51 (10% метанол/дихлорметан)/.
В. 2-бром-N-(3,4-диметил-5-изоксазолил)-N'- (метоксиэтоксиметил)-бензолсульфонамид
К раствору 1,1 г (3,33 ммоля) соединения А в 15 мл ТГФ при комнатной температуре в атмосфере аргона добавлялось 0,19 г (4,8 ммоля) гидрида натрия (60% суспензия в минеральном масле) порциями, и раствор перемешивался при комнатной температуре в течение 10 минут. Затем добавлялся метоксиэтоксиметилхлорид (0,55 г, 4,4 ммоля), и раствор перемешивался на протяжении ночи. Смесь концентрировалась и разбавлялась 30 мл воды и экстрагировалась 40 мл этилацетата. Объединенные органические экстракты промывались 50 мл солевого раствора, сушились и выпаривались, давая 1,2 г (87%) соединения B в виде коричневой смолы.
С. N-(3,4-Диметил-5-изоксазолил)-N-[(2-метоксиэтокси)метил] - 4'-метил[1,1'-бифенил]-2-сульфонамид
К раствору соединения В, 4-метилбензолбороновой кислоты (4,76 г, 35 ммолей) в 250 мл толуола и 200 мл 95% этанола в атмосфере аргона добавлялся тетракис (трифенилфосфин) палладий (0) (2,43 г, 2,1 ммоля), а затем 150 мл 2 М водного карбоната натрия. Реакционная смесь нагревалась при 80oC в течение 2,5 часов, охлаждалась и разбавлялась 300 мл этилацетата. Органическая жидкость отделялась и промывалась 200 мл воды и 200 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием смеси 5: 1 гексана и этилацетата, давая соединение С (9,0 г, 60%) в виде бесцветной смолы Rf = 0,74, силикагель 1:1 гексан/этилацетат.
Д. 4'-(Бромметил)-N-(3,4-диметил-5-изоксазолил)- -N-[(2-метоксиэтокси)-метил]-[1,1'-бифенил]-2- сульфонамид
К соединению М (7,7 г, 17,89 ммоля) в 180 мл четыреххлористого углерода добавлялись н-бромсукцинамид (4,14 г, 23,25 ммолей) и перекись бензоила (385 мг, 1,59 ммоля). Реакционная смесь нагревалась с обратным холодильником в течение 1,5 часов. После охлаждения реакционная смесь разбавлялась 200 мл дихлорметана, промывалась 2 х 100 мл воды и 100 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле при элюировании смесью 4: 1 гексана и этилацетата, давая соединение Д (3,64 г, 40%) в виде бесцветной смолы.
Rf = 0,38, силикагель: 2:1 гексан/этилацетат.
Е. N-(3,4-Диметил-5-изоксазолил)-4'-(1H-имидазол-1- илметил)-N-[(2-метоксиэтокси)-метил] [1,1'-бифенил] -2-сульфонамид
К соединению Д (400 мг, 0,79 ммоля) и имидазолу (133 мг, 1,95 ммоля) добавлялся карбонат калия /K2CO3/ (326 мг, 2,36 ммоля). Реакционная смесь перемешивалась при комнатной температуре в течение 10 часов, а затем при 50oC в течение 1 часа. Смесь разбавлялась 50 мл этилацетата, промывалась 10 мл воды и 10 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием смеси 100:1,5 дихлорметана и метанола, давая соединение E (320 мг, 56%) в виде бесцветной смолы.
Rf = 0,52, силикагель, 10:1 трихлорметан/метанол
F. N-(3,4-Диметил-5-изоксазолил)-4'-(1H-имидазол-1- илметил) [1,1'-бифeнил]-2-сульфонамид
К раствору соединения E (220 мг, 0,44 ммоля) в 6 мл 95% этанола добавлялось 6 мл 6 н. водной соляной кислоты. Реакционная смесь нагревалась с обратным холодильником в течение 2 часов, охлаждалась и концентрировалась. Реакционная смесь нейтрализовалась насыщенным водным бикарбонатом натрия /NaHCO3/, а затем подкислялась до pH ниже 5 уксусной кислотой. Фильтрование смеси давало белое твердое вещество (91 мг, 50%), которое растворялось в 1 н. HCl и концентрировалось под вакуумом, давая хлоргидратную соль целевого соединения в виде белого твердого вещества (т.пл. 150oC разл.)
Rf = 0,27, силикагель, 10:1 дихлорметан/метанол.
Анализ для C21H20N4O3S•1.1 H2О•0,8 HCl:
Вычислено: С 55,02, H 5,28, N 12,22, S 6,99, Cl 6,19.
Найдено: С 54,67, H 4,88, N 11,97, S 6,93, Cl 6,30.
Пример 16
N-(3,4-Диметил-5-изоксазолил)-4- (3-изоксазолил) [1,1'-бифенил]-2-сульфонамид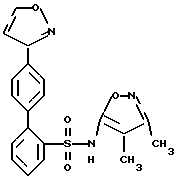
A. 4-Бром-N-гидроксибензолкарбоксимидоилбромид
К 0,5 М раствору соляной кислоты в диметилформамиде добавлялось 8,5 г (42,5 ммолей/4-бромбензальдегидоксима, и смесь охлаждалась до 5oC. Затем порциями добавлялось 13 г оксона. Смесь медленно подогревалась до комнатной температуры и перемешивалась в течение 8 часов. Реакционная смесь выливалась в 300 мл холодной воды и экстрагировалась 2 х 150 мл эфира. Объединенные органические экстракты промывались один раз 150 мл 0,5 н. водной соляной кислоты и солевым раствором (150 мл), сушились и выпаривались, давая 7,9 г (79%) соединения А.
В. 5-(Ацетилокси)-3-(4-бромфенил)-4,5-дигидроизоксазол
Смесь 4,0 г (17,06 ммоля) соединения А, 7,34 г (85,3 ммолей) винилацетата и 1,9 г (18,76 ммоля) триэтиламина в 50 мл толуола перемешивалась при 75oC в течение 2 часов. Смесь охлаждалась и добавлялась к 150 мл воды. Органический слой отделялся, а водный слой экстрагировался двумя порциями этилацетата по 50 мл. Объединенные органические экстракты промывались один раз 100 мл солевого раствора, сушились и выпаривались. Остаток кристаллизовался из смеси гексанов и этилацетата, давая 3,6 г (74%) соединения B в виде белого твердого вещества.
С. 3-(4-Бромфенил)-изоксазол
К раствору 3,0 г (10,56 ммоля) соединения В в 100 мл абсолютного этанола добавлялось 5 мл 6 н. водной соляной кислоты, и раствор нагревался с обратным холодильником в течение 3 часов. Смесь концентрировалась примерно до 10 мл, и раствор нейтрализовался с использованием водного бикарбоната натрия. Получающаяся в результате смесь экстрагировалась двумя порциями по 50 мл эфира. Объединенные органические экстракты промывались один раз 100 мл солевого раствора, сушились и выпаривались. Остаток хроматографировался на 100 г силикагеля с использованием смеси гексанов и этилацетата 9:1, давая 1,6 г (68%) соединения C в виде белого твердого вещества.
Д. N-(3,4-Диметил-5-изоксазолил)-N-[(2-метоксиэтокси)метил] - 4'-(3-изоксазолил) [1,1'- бифенил]-2-сульфонамид
К раствору 0,45 г (1,17 ммоля) соединения В из примера 1 и 0,058 г (0,05 ммоля) тетракис (трифенилфосфин) палладия (0) в 20 мл толуола в атмосфере аргона добавлялось 12 мл 2 М водного карбоната натрия, а затем 0,315 г (1,4 ммоля) соединения С в 12 мл 95% этанола. Смесь нагревалась с обратным холодильником в течение 2 часов, разбавлялась 100 мл воды и экстрагировалась 3 х 50 мл этилацетата. Объединенные органические экстракты промывались один раз 100 мл солевого раствора, сушились и выпаривались. Остаток хроматографировался на 50 г силикагеля с использованием смеси гексанов и этилацетата 2:1, давая 0,27 г (56%) соединения Д в виде бесцветной смолы.
Е. N-(3,4-Диметил-5-изоксазолил)-4'-(3-изоксазолил) [1,1'- бифенил]-2-сульфонамид
К раствору 0,26 г (0,54 ммоля) соединения Д в 10 мл 95% этанола добавлялось 10 мл 6 н. водной соляной кислоты, и смесь нагревалась с обратным холодильником в течение 1 часа. Смесь затем концентрировалась, разбавлялась 50 мл воды и экстрагировалась трижды 25 мл-выми порциями этилацетата. Объединенные органические экстракты промывались один раз водой, сушились и выпаривались (0,21 г). Данное вещество очищалось с помощью препаративной ВЭЖХ с обращенной фазой на 30 х 500 мм ОДS S10 колонке с использованием 67% растворителя В (90% метанол, 10% вода, 0,1% трифторуксусная кислота) и 33% растворителя А (10% метанол, 90% вода, 0,1% трифторуксусная кислота). Соответствующие фракции собирались, нейтрализовались водным бикарбонатом натрия до pH 7 и концентрировались до 10 мл. Раствор затем подкислялся до pH 4 с использованием ледяной уксусной кислоты, и белое твердое вещество отфильтровывалось и сушилось, давая 0,13 г (61%) целевого соединения. Т. пл. 85- 90oC.
Анализ для C20H17N3O4S•0,26 H2O:
Вычислено: С 60,04, H 4,41, N 10,50, S 8,01.
Найдено: С 60,04, H 4,30, N 10,50, S 8,15.
Пример 17
N-(3,4-Диметил-5-изоксазолил)-4'- (2-оксазолилметил) [1,1'-бифенил]-2-сульфонамид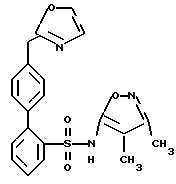
А. 4-Бромбензолацетамид
К раствору 6 г (27,9 ммоля) 4-бромфенилуксусной кислоты в 200 мл дихлорметана в атмосфере аргона добавлялось 14 мл 2 М оксалилхлорида в дихлорметане. Затем добавлялось 4 капли диметилформамида, и смесь перемешивалась при комнатной температуре в течение 1 часа. Раствор выпаривался и сушился в вакууме. Остаток растворялся в 150 мл метанола, и к смеси добавлялось 30 мл 28% водной гидроокиси аммония. Раствор перемешивался при комнатной температуре на протяжении ночи, а затем разбавлялся 150 мл воды. Получающееся белое твердое вещество отфильтровывалось, промывалось водой и сушилось, давая 5,1 г (85%) соединения А.
В. 2-[(4-Бромфенил)метил]оксазол
Смесь соединения А (2 г, 9,34 ммоля) и виниленкарбоната (0,9 г, 10,45 ммоля) в 6 г полифосфорной кислоты нагревалась при 170oC в течение 3 часов. Остаток добавлялся к 100 мл воды и экстрагировался два раза 100 мл-выми порциями этилацетата. Объединенные органические экстракты промывались один раз водой, сушились и выпаривались. Остаток хроматографировался на 200 мл силикагеля и с использованием смеси гексаны/этилацетат 2:1, давая 1,12 г (50%) соединения C в виде белого твердого вещества.
С. N-(3,4-Диметил-5-изоксазолил)-N-[(2-метоксиэтокси)метил]- 4-(2-оксазолилметил) [1,1'-бифенил]-2-сульфонамид
К раствору 0,6 г (1,56 ммоля) соединения B из примера 1 и 0,092 г (0,08 ммоля) тетракис (трифенилфосфин) палладия (0) в 30 мл толуола в атмосфере аргона добавлялось 15 мл 2М водного карбоната натрия, а затем 0,45 г (1,87 ммоля) соединения В, полученного выше, в 15 мл 95% этанола. Смесь нагревалась с обратным холодильником в течение 2 часов, разбавлялась 100 мл воды и экстрагировалась тремя 50-мл порциями этилацетата. Объединенные органические экстракты промывались один раз 100 мл солевого раствора, сушились и выпаривались. Остаток хроматографировался на 200 мл силикагеля с использованием смеси гексанов и этилацетата 2:1, давая 0,7 г (93%) соединения C в виде бесцветной смолы.
Д. N-(3,4-Диметил-5-изоксазолил)-4'-(2-оксазолилметил) [1,1'- бифенил] -2-сульфонамид
К раствору 0,7 г (1,41 ммоля) соединения С в 15 мл 95% этанола добавлялось 15 мл 6 н. водной соляной кислоты, и раствор нагревался с обратным холодильником в течение 1 часа. Смесь затем концентрировалась, разбавлялась 250 мл воды и экстрагировалась тремя 50-мл порциями этилацетата. Объединенные органические экстракты промывались один раз водой, сушились и выпаривались, давая 0,41 г бесцветной смолы. Остаток очищался с помощью препаративной ВЭЖХ в обращенной фазе на 30 х 500 мм ОДS S10 колонке с использованием 67% растворителя В (30% метанол, 10% вода, 0,1% трифторуксусная кислота) и 23% растворителя А (10% метанол, 90% вода, 0,1% трифторуксусная кислота). Соответствующие фракции собирались и нейтрализовались водным бикарбонатом натрия до pH 7 и контролировались до 10 мл. Раствор затем подкислялся до pH 4 с использованием разбавленной соляной кислоты, и получающееся белое твердое вещество отфильтровывалось и сушилось, давая 0,098 г (17%) целевого соединения.
Т. пл. 65-70oC.
1H ЯМР (CDCl3): δ 1,80 (с., 3H), 2,11 (с., 3H), 4,16 (с., 2H), 7,04 (с., 1H), 7,27 - 8,02 (м., 10H).
13C ЯМР (CDCl3): δ 6,99, 11,20, 34,67, 108,10, 127,54, 128,32, 128,92, 129,47, 130,82, 133,15, 133,44, 135,95, 137,91, 138,51, 139,37, 141,25, 154,69, 162,27, 183,42.
Пример 18
N-(3,4-Диметил-5-изоксазолил)-4'- (5-изоксазолил) [1,1'-бифенил]-2-сульфонамид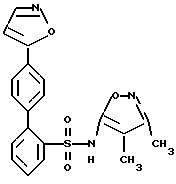
A. 1-(4-Бромфенил)-3-(диметиламино)-2-пропен-1-он
Раствор 7,0 г (35,2 ммоля) 4-бромацетофенона в 7 мл N,N- диметилформамиддиэтилацеталя нагревался с обратным холодильником в течение 20 часов. Раствор затем разбавлялся 100 мл эфира и охлаждался до 0oC. Желтое кристаллическое твердое вещество отфильтровывалось и сушилось, давая соединение А (6,85 г, 77%).
В. 5-(4-Бромфенил)изоксазол
К раствору 6,2 г (24,4 ммоля) соединения А в 70 мл метанола при 0oC добавлялся раствор 3,31 г (29,27 ммоля) гидроксиламин-0-сульфоновой кислоты в 20 мл метанола на протяжении периода 3 минут. После перемешивания при комнатной температуре в течение 1 часа реакционная смесь выливалась в смесь холодного насыщенного раствора бикарбоната натрия (200 мл) и ледяной воды (200 мл). Получающаяся в результате смесь давала в осадке 5,1 г светло-желтого твердого вещества. Перекристаллизация данного вещества в смеси гексана и этилацетата затем давала 3,12 г (57%) соединения B в виде не совсем белого твердого вещества.
С. N-(3,4-Диметил-5-изоксазолил)-N-[(2- метоксиэтокси)метил]-4'-(5-изоксазолил) [1,1'-бифенил]- 2-сульфонамид
К раствору 0,56 г (1,46 ммоля) соединения 1 из примера 1 и 0,081 г (0,07 ммоля) тетракис (трифенилфосфин) палладия (0) в 25 мл толуола в атмосфере аргона добавлялось 15 мл 2 М водного карбоната натрия, а затем 0,49 г (2,18 ммоля) соединения В в 15 мл 95% этанола. Смесь нагревалась с обратным холодильником в течение 2 часов, разбавлялась 100 мл воды и экстрагировалась тремя 50-мл порциями этилацетата. Объединенные органические экстракты промывались один раз 100 мл солевого раствора, сушились и выпаривались. Остаток хроматографировался на 50 г силикагеля с использованием смеси гексаны/этилацетат 2:1, давая 0,26 г /37%/ соединения С в виде бесцветной смолы.
Д. N-(3,4-диметил-5-изоксазолил)-4'-(5- изоксазолил) [1,1'-бифенил]-2-сульфонамид
К раствору 0,25 г /0,52 ммоля/ соединения С в 10 мл 95% этанола добавлялось 10 мл 6 н. соляной кислоты, и смесь нагревалась с обратным холодильником в течение 1 часа. Смесь затем концентрировалась, разбавлялась 100 мл воды и экстрагировалась тремя порциями по 50 мл этилацетата. Объединенные органические экстракты промывались один раз водой, сушились и выпаривались /0,21 г/. Данное вещество очищалось с помощью препаративной ВЭЖХ в обращенной фазе на колонке 30 х 500 мм ОДS S10 с использованием 63% растворителя В (90% метанол, 10% вода, 0,1% трифторуксусная кислота) и 31% растворителя А (10% метанол, 90% вода, 0,1% трифторуксусная кислота). Соответствующие фракции собирались и нейтрализовались водным бикарбонатом натрия, до pH 7 и концентрировались до 10 мл. Раствор подкислялся до pH 4 с использованием ледяной уксусной кислоты, и белое твердое вещество отфильтровывалось и сушилось, давая 0,11 г /53%/ целевого соединения.
Т. пл. 85-90oC.
Анализ для C20H17N3O4S • 0,27 H2O:
Вычислено: С 60,02, H 4,42, N 10,50, S 8,01.
Найдено: С 60,16, H 4,24, N 10,36, S 8,17.
Пример 19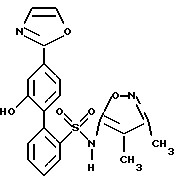
N-(3,4-Диметил-5-изоксазолил)-2'-гидрокси- 4'-(2-оксазолил) [1,1'-бифенил]-2-сульфонамид
A. 4-Бром-3-гидроксибензойная кислота
Бром /58 г, 19 мл, 0,36 моля/ в уксусной кислоте /50 мл/ медленно на протяжении 2 часов добавлялся к раствору 3- гидроксибензойной кислоты /50 г, 0,36 моля/ в уксусной кислоте /145 мл/ при перемешивании при 15oC. После перемешивания при 15oC в течение дополнительного часа, а затем при температуре окружающей среды в течение 17 часов образовавшееся твердое вещество отфильтровывалось и прополаскивалось уксусной кислотой /20 мл/. Сушка путем пропускания воздуха через осадок на фильтре в течение 4 часов давала 23,5 г /30%/ соединения А.
В. Метиловый эфир 4-бром-3-гидроксибензойной кислоты
Серная кислота /концентрированная, 9,4 мл/ добавлялась к раствору соединения А /23,5 г, 0,11 моля/ в метаноле /350 мл/. После нагревания с обратным холодильником в течение 19 часов реакционная смесь оставлялась охлаждаться до комнатной температуры, и величина pH доводилась примерно до 4 насыщенным бикарбонатом натрия. После выпаривания метанола оставшийся раствор переносился в делительную воронку. Экстрагирование эфиром /2 х 200 мл/, промывка объединенных органических слоев солевым раствором /50 мл/ и сушка над сульфатом магния давала 25 г сырого или неочищенного продукта после выпаривания растворителя. Перекристаллизация из смеси эфира и гексана давала 13,3 г /53%/ соединения В.
С. Метиловый эфир 4-бром-3-метоксибензойной кислоты
Диметилсульфат /6,4 мл, 67 ммолей/ и карбонат калия /10 г/ добавлялись к раствору соединения В (13,3 r, 57 ммолей) в ацетоне /86 мл/.
После нагревания с обратным холодильником в течение 13 часов реакционная смесь охлаждалась, осадок отфильтровывался, и фильтрат выпаривался в вакууме, давая 14,7 г сырого продукта. Флэш-хроматография /двуокись кремния, 50 мм диаметр, 10% этилацетат /гексан/ давала 13,9 г соединения С /100%/.
Д. 4-Бром-3-метоксибензойная кислота
Гидроокись калия /2 н., 120 мл, 240 ммолей/ добавлялась к раствору соединения С /19 г, 79 ммолей/ в метаноле /670 мл/. После перемешивания при температуре окружающей среды в течение 5,5 часов добавлялась вода (100 мл) и метанол удалялся в вакууме. Оставшийся раствор экстрагировался метиленхлоридом, а затем подкислялся 6 н. соляной кислотой до pH 1,5. Экстрагирование метиленхлоридом /1 х 500 мл и 2 х 200 мл/ давало 17 г /93%/ соединения Д после выпаривания растворителя.
E. 4-Бром-3-метоксибензамид
Раствор соединения Д /17 г, 73 ммоля/ и диметилформамида /0,3 мл/ в тионилхлориде /18 мл, 3,5 моля/ нагревался при 60oC в течение 2 ч. После выпаривания реакционной смеси и в вакууме и азеотропной отгонки с толуолом /дважды/ остаток растворялся в тетрагидрофуране /30 мл/ и медленно добавлялся к энергично перемешиваемому концентрированному раствору гидроокиси аммония /95 мл/. Выпавшее в осадок вещество отфильтровывалось, промывалось водой и сушилось в вакуумном десикаторе на протяжении ночи, давая 17 г /100%/ соединения E.
Г. 2-(4-Бром-3-метоксифенил)оксазол
Полифосфорная кислота /18 г/ добавлялась к соединению E /8,5 г, 37 ммолей/, и смесь нагревалась и перемешивалась до тех пор, пока она не стала гомогенной. Добавлялся виниленкарбонат /3,2 г, 2,4 мл, 37 ммолей/, и реакционная смесь перемешивалась при 160oC в точение 2 часов, в течение которых реакционная смесь выделяла газ и становилась черной и смолообразной. После охлаждения добавлялись вода и эфир, все смешивалось и декантировалось /три раза/. Декантированные слои фильтровались через Целит, и фильтрат переносился на делительную воронку. Органический слой промывался водой /10 мл/ и 1 н. гидроокисью натрия /30 мл/ и сушился над сульфатом магния, давая сырой продукт после выпаривания растворителя. Любое оставшееся в реакционном сосуде твердое вещество и Целитный фильтр прополаскивались дихлорметаном /3 х 10 мл/, который затем промывался 1 н. гидроокисью натрия /30 мл/ и сушился над сульфатом магния. Две порции сырого продукта составляли всего 3,6 г. Флэш-хроматография /двуокись кремния, 50 мм диаметр, 30% этилацетат /гексан/ давала 2,3 г (24%) соединения F.
Т. пл. 68,5-70,5oC.
G. N-(3,4-Диметил-5-изоксазолил)-2'-метокси-N- (2-метоксиэтоксиметил)-4'-(2-оксазолил) [1,1-бифенил]-2 -сульфонамид
Раствор соединения В из примера 1 /2,3 г, 2,9 ммоля/ в этаноле /продуваемый аргоном 20 минут, 16 мл/ добавлялся к раствору соединения F /1,1 г, 4,4 ммоля/ в толуоле /продуваемом аргоном 20 минут, 32 мл/.
К данному раствору добавлялся раствор карбоната натрия /1,0 г/ в воде /продуваемый аргоном 20 минут, 16 мл/, а затем тетракис/трифенилфосфин/палладий/0/ /0,28 г, 0,24 ммоля/.
После нагревания с обратным холодильником в атмосфере аргона в течение 2 часов раствор охлаждался и выливался в солевой раствор /40 мл/. Экстрагирование этилацетатом /2 х 150 мл/ и сушка объединенных органических слоев над сульфатом магния давали 4,1 г сырого продукта после выпаривания растворителя. Флэш-хроматография /двуокись кремния, 50 мм диаметр, 40% этилацетат/ гексан/ давала 0,50 г /34%/ соединения G.
H. N-(3,4-Диметил-5-изоксазолил)-2'-метокси-4'- (2-оксазолил) [1,1-бифенил]-2-сульфонамид
Раствор соединения G /0,45 г, 0,88 ммоля/ в этаноле /13,4 мл/ и 6 н. соляной кислоты /13,4 мл/ перемешивался при 90oC. Через 3,5 часа этанол выпаривался в вакууме, и остаток переносился в делительную воронку со смесью дихлорметана и воды. Экстрагирование дихлорметаном /2 х 50 мл/ и сушка над сульфатом магния давала 0,37 г (100%) соединения H после выпаривания растворителя.
1. N-(3,4-Диметил-5-изоксазолил)-2'-гидрокси- 4'-(2-оксазолил) [1,1'-бифенил]-2-сульфонамид
Треххромистый бор /1 М в дихлорметане, 6,2 мл, 6,2 ммоля/ добавлялся к раствору соединения H /0,33 г, 0,77 ммоля/ и в метиленхлориде /27 мл/ при перемешивании при -78oC. После перемешивания при -78oC в течение 30 минут холодная баня удалялась. После перемешивания всего в течение 2,5 часов реакционная смесь переносилась в делительную воронку с дихлорметаном и водой. Величина pH доводилась до 3,5 насыщенным бикарбонатом натрия.
Экстрагирование дихлорметаном /2 х 70 мл/ и сушка над сульфатом магния давали 0,68 г сырого продукта после выпаривания растворителя. Две процедуры флэш-хроматографии /двуокись кремния, 25 мм диаметр, 6% метанол: дихлорметан, и двуокись кремния, 15 мм диаметр, 50% этилацетат /дихлорметан/ давали 60 мг /19%/ целевого соединения. Т. пл. 111.0-115.0oC.
Анализ для C20H17N3O5S•0,15С4Н8О2•0.40 H2O:
Вычислено: С 57,29, H 4,43, N 9,73, S 7,42.
Найдено: С 57,30, H 58, N 9,37, S 7,18.
Пример 20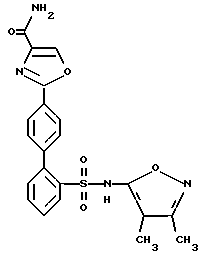
2-[2'-[[(3,4-Диметил-5-изоксазолил) амино]-сульфонил] [1,1'-бифенил]-4- ил]-4- оксазолкарбоксамид
А. 2-(4-Бромфенил)-4-оксазолкарбоксальдегид
Смесь соединения А из примера 7 /810 мг, 3,40 ммоля/, двуокиси селена /1,89 г, 17 ммолей/ и 6,8 мл диоксана нагревалась с обратным холодильником в течение 24 часов. После охлаждения смесь фильтровалась, и фильтрат концентрировался. Остаток хроматографировался на силикагеле с использованием 60: 1 смеси дихлорметана и этилацетата, давая соединение А /406 мг, 47%/ в виде светло-желтого твердого вещества.
В. N-(3,4-Диметил-5-изоксазоил)-4'-(4-формил-2- оксазолил)-N-[(2-метоксиэтокси)метил][1,1'-бифенил]- 2-сульфонамид
К раствору соединения В из примера 1 /772 мг, 2,0 ммоля/, соединения А /390 мг. 1,55 ммоля/ в 15 мл толуола и 12 мл 95% этанола в атмосфере аргона добавлялся тетракис/трифенилфосфин/палладий /0/ /116 мг, 0,1 ммоля/ с последующим добавлением 9 мл 2 М водного бикарбоната натрия. Реакционная смесь нагревалась при 75oC в течение 1 часа, охлаждалась и разбавлялась 80 мл этилацетата. Органическая жидкость отделялась, промывалась 15 мл воды и 15 мл солевого раствора, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 3:2 смеси гексан/этилацетат, давая соединение В /290 кг, 37%/ в виде бесцветной смолы.
C. 2-[2'-[[(3,4-Диметил-5-изоксазолил) [(2- метоксиэтокси)метил]амино-сульфонил] [1,1'-бифенил]-4- ил]-4-оксазолкарбоксамид
К соединению B /285 мг, 0,56 ммоля/, полученному выше, и сульфаминовой кислоте /108 мг, 1,11 ммоля/ в 5,6 мл тетрагидрофурана при 0oC добавлялся охлажденный льдом раствор хлорида натрия /101 мг, 1,11 ммоля/ в 5,6 мл воды. Смесь перемешивалась при 0oC в течение 3 минут. Добавлялось 50 мл дихлорметана, и органическая жидкость промывалась 10 мл солевого раствора, сушилась и концентрировалась, давая 2-[2'-[[(3,4-диметил-5- изоксазолил) [(2-метоксиэтокси)метил] - амино]сульфонил] [1,1'-бифенил]-4-ил]-4- оксазолкарбоновую кислоту.
К 2-[2'-[[(3,4-диметил-5-изоксазолил) [(2-метоксиэтокси)метил] -амино] сульфонил] [1,1'-бифенил]-4- ил-4-оксазолкарбоновой кислоте и 0,014 мл диметилформамида в 5,6 мл дихлорметана добавлялся оксалилхлорид /2 M в дихлорметане, 0,56 мл, 1.11 ммоля/, смесь перемешивалась в течение 0,5 часа и концентрировалась. К данной смеси добавлялись 10 мл тетрагидрофурана и 2 мл концентрированной гидроокиси аммония. Реакционная смесь перемешивалась при комнатной температуре в течение 50 минут и концентрировалась. Органическая жидкость промывалась 15 мл воды и 15 мл солевого раствора, сушилась и выпаривалась. Остаток хроматографировался на силикагеле с использованием 1:4 смеси гексана и этилацетата, давая соединение C /245 мг, 84% в три стадии/ в виде бесцветной смолы.
Д. 2-[2'-[[(3,4-Диметил-5-изоксазолил)амино] сульфонил][1,1'-бифенил]-4-ил]-4-оксазолкарбоксамид
К раствору соединения С /240 мг, 0,46 ммоля/ в 4,6 мл ацетонитрила при 0oC добавлялся триметилкремнийхлорид /297 мг, 2,74 ммоля/, а затем иодид натрия /410 мг, 2,74 ммоля/. Смесь перемешивалась при комнатной температуре в течение 1 часа. Добавлялось 6 мл воды, и смесь экстрагировалась 50 мл этилацетата. Органическая жидкость промывалась 5 мл насыщенного водного тиосульфата натрия и 5 мл солевого раствора, сушилась и концентрировалась. Остаток очищался с помощью препаративной ВЭЖХ на 30 х 500 мм ОДS S10 колонке с использованием 37% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/ и 63% растворителя В /90% метанол, 10% вода, 0,1% тетрагидрофуран/, давая целевое соединение /122 мг, 61%/ в виде белого твердого вещества.
Т. пл. 195oC разл.
Анализ для C21H18N4O5S • 0,23 H2O:
Вычислено: С 57,00; H 4,20; N 12,66; S 7,24.
Найдено: С 57,01; H 4,10; N 12,85; S 7,18.
Пример 21
N-(3,4-Диметил-5-изоксазолил)-2'- [(формиламино) метил] -4'-(2-оксазолил)-[1,1'-бифенил]-2- сульфонамид
A. 4-Бром-3-метилбензамид
К раствору 10 г /46,5 ммолей/ 4-бром-3-метилбензойной кислоты в 200 мл дихлорметана в атмосфере аргона добавлялось 30 мл 2 М раствора оксалилхлорида в дихлорметане. Затем добавлялось 4 капли диметилформамида, и смесь перемешивалась при комнатной температуре в течение 1 часа. Раствор выпаривался и сушился в вакууме. Остаток растворялся в 10 мл метанола, и к смеси добавлялось 25 мл 28% водной гидроокиси аммония. Раствор перемешивался при комнатной температуре в течение 3 часов, а затем разбавлялся 500 мл воды. Получающееся белое твердое вещество отфильтровывалось, промывалось водой и сушилось, давая 8,9 г /89%/ соединения А.
В. 2-(4-Бром-3-метилфенил)оксазол
Смесь соединения А /12 г, 56 ммолей/ и виниленкарбоната /6,5 г, 75,5 ммолей/ в 25 г полифосфорной кислоты нагревалась при 170oC в течение 3 часов. Остаток затем добавлялся к 700 мл воды и экстрагировался 3 х 250 мл этилацетата. Объединенные органические экстракты промывались один раз водой, сушились и выпаривались. Остаток хроматографировался на 200 г силикагеля с использованием дихлорметана, давая 6,7 г /50%/ соединения В в виде белого твердого вещества.
С. 2-[4-Бром-3-(бромметил)фенил]оксазол
Смесь соединения В /6,5 г, 27,3 ммоля/, N-бромсукцинимида /9,72 г, 54,6 ммолей/ и бензоилпероксида /250 мг/ в 250 мл четыреххлористого углерода нагревалась с обратным холодильником в течение 8 часов при освещении раствора лампой солнечного света. Смесь затем охлаждалась и фильтровалась. Фильтрат концентрировался, давая 10 г светло-желтого твердого вещества, которое использовалось на следующей стадии без дальнейшей очистки.
Д. 2-Бром-5-(2 оксазолил)бензальдегид
К раствору 7 г сырого соединения С в 15 мл безводного диметилсульфоксида в атмосфере аргона добавлялось 5,5 г безводного триметиламин-N-оксида (полученного, как описано в работе Soderquist и др. Tet. Letters., 27, 3961, /1986/), и смесь перемешивалась при 55oC в течение 6 часов. Смесь затем охлаждалась, добавлялась к 150 мл смеси льда и воды и экстрагировалась тремя порциями по 100 мл этилацетата. Объединенные органические экстракты промывались один раз 100 мл солевого раствора, сушились и выпаривались. Остаток хроматографировался на 300 мл силикагеля с использованием смеси гексаны/этилацетат 8: 1, давая 2,2 г /46% в две стадии/ соединения в виде белого твердого вещества.
E. N-(3,4-Диметил-5-изоксазолил)-2'- формил-N [(2-метоксиэтокси)метил] -4'-(2-оксазолил)[1,1'- бифенил]-2-сульфонамид
К раствору 2,3 г /6 ммолей/ соединения В из примера 1 и 0,3 г /0,2/ 0,26 ммоля/ тетракис/трифенилфосфин/палладия /0/ в 40 мл толуола в атмосфера аргона добавлялось 20 мл 2 М водного карбоната натрия, а затем 1,0 г /6,28 ммоля/ соединения Д в 20 мл 95% этанола. Смесь нагревалась с обратным холодильником в течение 2 часов, разбавлялась 100 мл воды и экстрагировалась 3 х 50 мл этилацетата. Объединенные органические экстракты промывались один раз 100 мл солевого раствора, сушились и выпаривались. Остаток хроматографировался на 200 мл силикагеля с использованием смеси гексаны /этилацетат 1:1, давая 1,69 г /55%/ соединения E в виде бесцветной смолы.
F. N-(3,4-Диметил-5-изоксазолил)-2'-формил-4'- (2-оксазолил) [1,1'-бифенил]-2-сульфонамид
К раствору 1,68 г /3,28 ммоля/ соединения E в 30 мл 95% этанола добавлялось 30 мл 6 н. водной соляной кислоты и смесь нагревалась с обратным холодильником в течение 1 часа. Смесь затем концентрировалась и разбавлялась 250 мл воды и экстрагировалась тремя порциями этилацетата по 150 мл. Объединенные органические экстракты затем промывались один раз водой, сушились и выпаривались, давая 1,46 г /90%/ соединения F в виде бесцветной смолы.
G. 2'-(Аминометил)-N-(3,4-диметил-5-изоксазолил) -4'-(2-оксазолил)-[1,1'-бифенил]-2-сульфонамид
К раствору 0,28 г /0,66 ммоля/ соединения F в 25 мл метанола добавлялось 5 г ацетата аммония и 1 г 3A молекулярных сит, и смесь перемешивалась при комнатной температуре в течение 1 часа. Добавлялся триацетоксиборгидрид натрия /0,42 г, 1,98 ммоля/, и смесь перемешивалась в течение дополнительных 45 минут. Раствор фильтровался, концентрировался до 10 мл, разбавлялся 25 мл воды и экстрагировался тремя порциями по 25 мл этилацетата. Объединенные органические экстракты затем промывались один раз водой, сушились и выпаривались. Остаток хроматографировался на 15 г силикагеля с использованием 5% метанола в дихлорметане, давая 0,1 г /36%/ соединения С в виде белого твердого вещества
H. N-(3,4-Диметил-5-изоксазолил)-2'-[(формиламино) метил]-4'-(2-оксазолил) [1,1'-бифенил]-2-сульфонамид
К раствору 0,06 г /0,14 ммоля/ соединения G в 10 мл дихлорметана при 0oC добавлялось 0,02 г уксусномуравьиного ангидрида и 0,02 г триэтиламина. Смесь медленно подогревалась до комнатной температуры и перемешивалась в течение 1 часа. Смесь разбавлялась 10 мл дихлорметана, промывалась 20 мл 0,1 н. водной соляной кислоты, а затем 20 мл воды. Органический слой сушился и выпаривался. Остаток очищался с помощью препаративной ВЭЖХ с обращенной фазой на 30 х 500 мм ОДS S10 колонке с использованием 56% растворителя В /90% метанол, 10% вода, 0,1% триуксусная кислота/ и 44% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/.
Соответствующие фракции собирались, нейтрализовались водным бикарбонатом натрия до pH 7 и концентрировались до 10 мл. Раствор затем подкислялся до pH 4 с использованием разбавленной соляной кислоты, и белое твердое вещество отфильтровывалось и сушилось, давая 0,013 г /21%/ целевого соединения.
Т. пл. 105-109oC.
1H ЯМР /CDCl3/: δ 1,87 /c.,3H/, 2,12 /с.,3H/, 3,89 /AB кв., J = 4,1, 15,8 Гц, 1H/, 4,50 /AB кв., J = 7,6, 15,8 Гц, 1H/, 6,63 / шир., с., 1H/, 7,03-7,93 /м., 10H/, 8,14 /с., 1H/.
13C ЯМР: /CDCl3/; δ 6,83, 10,90, 39,80, 108,68, 124,26, 124,95, 127,29, 128,18, 128,79, 129,77, 130,26, 130,26, 130,52, 132,19, 133,58, 137,44, 137,61, 138,42, 138,88, 139,58, 154,57, 161,53, 162,25.
Пример 22
N-(3,4-диметил-5-изоксазолил)-2'- [[(метоксикарбонил) амино]метил]-4'-(2-оксазолил) [1,1'-бифенил]-2-сульфонамид
A. N-(3,4-Диметил-5-изоксазолил)-2'-[[(метоксикарбонил) амино]метил]-4-(2-оксазолил) [1,1'-бифенил]-2-сульфонамид
К соединению G из примера 21 /75 мг, 0,18 ммоля/ в 3,5 мл тетрагидрофурана добавлялся триэтиламин /35 мг, 0,35 ммоля/ с последующим добавлением метилхлорформиата /17 мг, 0,18 ммоля/. Реакционная смесь перемешивалась при комнатной температуре в течение 1 часа. Добавлялись дополнительно триэтиламин /18 мг, 0,18 ммоля/ и метилхлорформиат /17 мг, 0,18 ммоля/, и реакционная смесь перемешивалась при 40oC еще в течение 1,5 часов. Реакционная смесь концентрировалась и остаток очищался с помощью препаративной ВЭЖХ на 30 х 500 мм ОДS S10 колонке с использованием 42% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/ и 58% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/, давая целевое соединение /30 мг, 35%/ в виде белого твердого вещества. Т.пл. 110-120oC /аморфное/.
Анализ для C23H22N4O6S • 0,41 H2O:
Вычислено: С 56,39, H 4,69, N 11,44, S 6,54.
Найдено: С 56,11, H 4,48, N 11,19, S 6,49.
Пример 23
N-[[2'-[(3,4-Диметил-5-изоксазолил) амино]сульфонил]- 4-(2-оксазолил)-[1,1'-бифенил]-2-ил -метил-N'-метилмочевина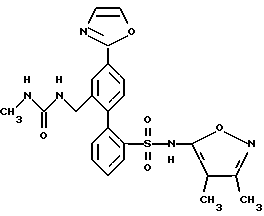
A. N-[[2'-[(3,4-Диметил-5-изоксазолил) амино] сульфонил]-4-(2-оксазолил)-[1,1'-бифенил]-2- ил]метил]-метилмочевина
К соединению G из примера 21 /75 мг, 0,18 ммоля/ в 7,1 мл тетрагидрофурана добавлялся метилизоцианат /71 мг, 1,24 ммоля/. Реакционная смесь перемешивалась при комнатной температуре на протяжении ночи и концентрировалась. Остаток очищался с помощью препаративной ВЭЖХ на 30 х 500 мм OДS S10 колонке с использованием 46% растворителя А/ 10% метанол, 90% вода, 0,1% трифторуксусная кислота/ и 54% растворителя В (90% метанол, 10% вода, 0,1% трифторуксусная кислота), давая целевое соединение /36 мг, 45%/ в виде белого твердого вещества. Т. пл. выше 150oC, разлож.
Анализ для C23H23N5O5S• 0,45 H2O•0,2 CH2Cl2:
Вычислено: С 55,00, H 4,83, N 13,82, S 6,33.
Найдено: С 54,57, H 4,58, N 13,61, S 5,95.
Пример 24
N-(3,4-Диметил-5-изоксазолил)-2'- [[(метилсульфонил)амино] метил]-4'-(2-оксазолил)-[1,1'-бифенил]-2-сульфонамид
A. N-(3,4-Диметил-5-изоксазолил)-2'-[[(метилсульфонил)амино] метил]-4'-(2-оксазолил)-[1,1'-бифенил]-2-сульфонамид
К соединению G из примера 21 /75 мг, 0,18 ммоля/ и триэтиламину /54 мг, 0,53 ммоля/ в 7,1 мл тетрагидрофурана добавлялся метансульфонилхлорид /57 мг, 0,5 ммоля/. Реакционная смесь перемешивалась при 45oC в течение 2 часов. Реакционная смесь концентрировалась, и величина pH раствора доводилась до 8 с использованием раствора бикарбоната натрия.
Раствор подкислялся до pH 5 ледяной уксусной кислотой. Смесь экстрагировалась дихлорметаном. Органическая жидкость концентрировалась, и остаток очищался с помощью препаративной ВЭЖХ на 30 х 500 мм ОДS S10 колонке с использованием 47% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/ и 53% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/, давая целевое соединение /27 мг, 30%/ в виде белого твердого вещества.
Т. пл. 110-120oC /аморфное/.
Анализ для C22H22N4O6S•0,1% CH3COOH:
Вычислено: С 52,37, H 4,45, N 10,96, S 12,56.
Найдено: С 52,43, H 4,37, N 10,76, S 12,11.
Пример 25
N-[[2'-[[(3,4-Диметил-5-изоксазолил)амино] сульфонил]-4-(2- оксазолил)-[1,1'-бифенил]-2-ил]-метил]-ацетамид
A. N-[[2'-[[(3,4-Диметил-5-изоксазолил)амино] сульфонил] -4- (2-оксазолил)[1,1'-бифенил]-2-ил]метил]ацетамид
К раствору 0,075 г /0,177 ммоля/ соединения G из примера 21 и в 10 мл дихлорметана при 0oC добавлялось 0,019 г /0,19 ммоля/ уксусного ангидрида и 0,019 г триэтиламина. Смесь затем медленно подогревалась до комнатной температуры и перемешивалась в течение 1 часа. Смесь разбавлялась 10 мл дихлорметана и промывалась 20 мл воды. Органический слой сушился и выпаривался. Остаток очищался с помощью препаративной ВЭЖХ с обращенной фазой на 30 х 500 мм OДS S10 колонке с использованием 58% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/ и 42% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/. Соответствующие фракции собирались и нейтрализовались водным бикарбонатом натрия до pH 7 и концентрировались до 10 мл. Раствор подкислялся до pH 4 с использованием разбавленной соляной кислоты, и белое твердое вещество отфильтровывалось и сушилось, давая 0,041 г /50%/ целевого соединения. Т. пл. 105-107oC.
Анализ для С23H22N4O5S• 0.42 H2O:
Вычислено: С 58,27, H 4,86, N 11,82, S 6,76.
Найдено: С 58,38, H 4,71, N 11,71, S 6,93.
Пример 26
N-[[2-[[3,4-Диметил-5-изоксазолил] амино] сульфонил]-4-[2-оксазолил[-[1,1-бифенил]-2- ил]метил]-N-фенилмочевина
A. N-[[2'-[(3,4-Диметил-5-изоксазолил)амино] сульфонил]-4-(2-оксазолил) [1,1'-бифенил]-2-ил] метил-] N'-фенилмочевина
К соединению G из примера 21 /25 мг, 0,059 ммоля/ в 3 мл тетрагидрофурана добавлялся фенилизоцианат /56 мг, 0,47 ммоля/. Реакционная смесь перемешивалась при комнатной температуре на протяжении ночи и концентрировалась. Остаток очищался с помощью препаративной ВЭЖХ хроматографии на 30 х 500 мм ОДS S10 колонке с использованием растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/ и 67% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/, давая целевое соединение /18 мг, 56%/ в виде белого твердого вещества.
1H ЯМР /CDCl3/: δ 1,82 /с., 3H/, 2,16 /с., 3H/, 3,99-4,38 /м., 2H/, 6,06 /с., шир., 1H/, 6,91 - 8,03 /м.,15H/.
13C ЯМР /CDCl3/: δ 7,60, 11,81, 42,65, 109,39, 119,92, 123,29, 124,13, 127,10, 128,26, 129,61, 130,68, 130,79, 132,96, 134,80, 157,72, 139,56, 140,00, 140,25, 140,43, 155,63, 156,58.
Пример 27
N-[[2'-[(3,4-Диметил-5-изоксазолил) амино]сульфонил]-4- (2-оксазолил)-[1,1'-бифенил]-2-ил]метил]-N'- пропилмочевина
A. N-[[2'-[(3,4-Диметил-5-изоксазолил)амино] сульфонил]-4-(2-оксазолил) [1,1'-бифенил]-2-ил] метил]-N'-пропилмочевина
К соединению из примера 21 /20 мг, 0,047 ммоля/ в 3 мл тетрагидрофурана добавлялся пропилизоцианат /36 мг, 0,424 ммоля/. Реакционная смесь перемешивалась при комнатной температуре на протяжении ночи и концентрировалась. Остаток хроматографировался на силикагеле с использованием смеси 100:4,5 дихлорметана и метанола, давая целевое соединение /16 мг, 67%/ в виде светло-желтого твердого вещества.
1H ЯМР /CD3OD/: δ 0,89 /т., J= 7 Гц, 3H/, 1.46 /м., 2H/, 1,70 /с., 3H/, 2,10 /с., 3H/, 3.06 /т., J= 7 Гц, 2H/; 4,08 /с., 2H/, 7,10 - 8,12 /м., 9H/.
13С ЯМР /CD3OD/: δ 6,57, 10,58, 11,62, 24,37, 42,91, 124,83, 125,06, 127,97, 129,10, 129,62, 130,34, 131,67, 133,11, 133,74, 139,83, 140,44, 140,87, 141,24, 141,96, 160,91, 162,99, 163,42.
Пример 28
N-[[2'-[[(3,4-Диметил-5-изоксазолил)амино] - сульфонил] -4-(2-оксазолил)-[1,1'-бифенил]-2-ил] метил]-N-метилацетамид
A. N-[[2'-[[(3,4-Диметил-5-изоксазолил)амино] сульфонил]-4-(2-оксазолил)[1,1'-бифенил]-2-ил] метил]-N-метилацетамид
К раствору 0,15 г /0,35 ммоля/ соединения F из примера 21 в 15 мл дихлорметана добавлялись метиламин /33% раствор в абсолютном этаноле, 0,13 мл, 1.06 ммоля/, ледяная уксусная кислота /0,12 г, 2 ммоля/ и 1 г 3A молекулярных сит. Смесь перемешивалась при комнатной температуре в течение 1 часа. Добавлялся триацетоксиборгидрид натрия /0,22 г, 1,06 ммоля/, и смесь перемешивалась на протяжении ночи. Раствор затем фильтровался, промывался один раз водой, сушился и выпаривался. Остаток, полученный таким образом, растворялся в 10 мл дихлорметана, и добавлялось 0,072 г /0,70 ммоля/ уксусного ангидрида и 0,071 г /0,70 ммоля/ триэтиламина. Смесь перемешивалась при комнатной температуре в течение 16 часов и выпаривалась. Остаток очищался с помощью препаративной ВЭЖХ с обращенной фазой на 30 х 500 мм OДS S10 колонке с использованием 58% растворителя В /90% метанол, 10% вода и 0,1% трифторуксусная кислота/ и 42% растворителя А (10% метанол, 90% вода, 0,1% трифторуксусная кислота). Соответствующие фракции собирались, нейтрализовались водным дикарбонатом натрия до pH 7 и концентрировались до 10 мл. Раствор подкислялся до pH 4 с использованием ледяной уксусной кислоты, и белое твердое вещество отфильтровывалось и сушилось, давая 0,069 г /41%/ целевого соединения в виде светло-желтого твердого вещества. Т. пл. 105-115oC.
Пример 29
N-[[2'-[[(3,4-Диметил-5-изоксазолил) амино] сульфонил] -4- (2-оксазолил)-[1,1'-бифенил]-2-ил]метил]бензамид
A. N-[[2'-[[(3,4-Диметил-5-изоксазолил) амино]сульфонил]-4-(2-оксазолил) [1,1'-бифенил]-2-ил- метил]бензамид
К соединению G из примера 21 /70 мг, 0,17 ммоля/ и бензоилхлориду /23 мг, 0,17 ммоля/ в 3,3 мл дихлорметана добавлялся триэтиламин /37 мг, 0,36 ммоля/. Реакционная смесь перемешивалась при комнатной температуре в течение 1,5 часов и концентрировалась. Остаток очищался с помощью препаративной ВЭЖХ на 30 х 500 мм ОДS S10 колонке с использованием 33% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/ и 67% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/, давая целевое соединение /30 мг, 34%/ в виде белого твердого вещества.
Т. пл. 128-135oC /аморфное/.
1H ЯМР /CDCl3/: δ 1,91 /с., 3H/, 2,18 /с., 3H/, 4,16-4,76 /м., 2H/, 7,13-8,13 /м., 14H/.
Пример 30
N-[[2'-[[(3,4-Диметил-5-изоксазолил) амино] сульфонил]-4-(2-оксазолил)- [1,1'-бифенил]-2- ил]метил]-2,2-диметилпропанамид
A. N-[[2'-[[(3,4-Диметил-5-изоксазолил)амино] сульфонил]-4-(2-оксазолил) [1,1'-бифенил]-2-ил] метил]-2,2-диметилпропанамид
К соединению G из примера 21 /105 мг, 0,25 ммоля/ и триметилацетилхлориду /30 мг, 0,25 ммоля/ в 4,9 мл дихлорметана добавлялся триэтиламин /55 мг, 0,54 ммоля/. Реакционная смесь перемешивалась при комнатной температуре на протяжении ночи и концентрировалась. Остаток очищался с помощью препаративной ВЭЖХ на 30 х 500 мм ОДS S10 колонке с использованием 33% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/ и 67% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/, давая целевое соединение /52 мг, 34%/ в виде белого твердого вещества.
Т. пл. 122-128oC.
1H ЯМР /CDCl3/: δ 1,18 /с., 9H/, 1,93 /с., 3H/, 2,18 /с.,3H/, 3,96-4,46 /м., 2H/, 7,24-8,05 /м., 9H/.
Пример 31
Метиловый эфир 2'-[[(3,4-диметил-5- изоксазолил)амино] сульфонил]-4-(2-оксазолил) [1,1'- бифенил]-2-карбоновой кислоты
A. 2'-[[(3,4-Диметил-5-изоксазолил)амино] сульфонил]-4-(2-оксазолил)-[1,1'-бифенил]-2- карбоновая кислота.
К соединению F из примера 21 /2,20 г, 5,20 ммоля/ и сульфаминовой кислоте /1,01 г, 10,39 ммолей/ в 52 мл ТГФ при 0oC добавлялся охлажденный льдом раствор хлорида натрия /940 мг, 10,39 ммолей/ в 52 мл воды. Смесь перемешивалась при 0oC в течение 2 минут, а затем разбавлялась 150 мл дихлорметана. Органическая жидкость отделялась и промывалась солевым раствором, сушилась и концентрировалась. Остаток очищался с помощью препаративной ВЭЖХ на ОДS S10 колонке с использованием 43% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/ и 57% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/, давая соединение А /503 мг, 22%/ в виде белого твердого вещества.
В. Метиловый эфир 2'-[[(3,4-диметил-5-изоксазолил) амино]сульфонил]-4-(2-оксазолил) [1,1'-бифенил]-2- карбоновой кислоты
К соединению А /258 мг, 0,59 ммоля/ в 5,9 мл ТГФ при 0oC добавлялся 1,1'-карбонилдиимидазол /209 мг, 1,29 ммоля/. После перемешивания при комнатной температуре в течение 1 часа добавлялся 1 мл метанола, и реакционная смесь перемешивалась при комнатной температуре на протяжении ночи. Добавлялось дополнительно 3 мл метанола, и смесь нагревалась при 50oC в течение дополнительного часа. После охлаждения до комнатной температуры добавлялось 10 мл 0,5 н. водной HCl, и смесь перемешивалась в течение 10 минут. Добавлялось 60 мл этилацетата, и органическая жидкость отделялась и промывалась солевым раствором, сушилась и концентрировалась. Остаток очищался с помощью препаративной ВЭЖХ на ОДS S10 колонке с использованием 34% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/ и 66% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/, давая целевое соединение /98 мг, 37%/ в виде белого твердого вещества.
Т. пл. 106-112oC /аморфное/. Rf = 0,54, силикагель, 20:1 дихлорметан/метанол.
1H ЯМР /CDCl3/: δ 1,84 /с., 3H/, 2,17 /с., 3H/, 3,73 /с., 3H/, 7,27-8,62 /м., 10H/.
Пример 32
N-(3,4-диметил-5-изоксазолил)-2'- (1-гидрокси-1-метилэтил)-4'- (2-оксазолил) [1,1-бифенил]-2-сульфонамид
A. N-(3,4-Диметил-5-изоксазолил)-2'-(1- гидрокси-1-метилэтил)-4'-(2-оксазолил) [1,1'- бифенил]-2-сульфонамид
К целевому соединению примера 31 /87 мг, 0,19 ммоля/ в 1,9 мл ТГФ при 0oC добавлялся метилмагнийбромид /1,4 М в смеси толуол /ТГФ 75:25, 0,43 мл, 0,60 ммоля/. Реакционная смесь перемешивалась при 0oC в течение 10 минут и при комнатной температуре в течение 3 часов. Добавлялся дополнительно метилмагнийбромид /1,4 М в смеси толуол /ТГФ 75:25, 0,069 мл, 0,096 ммоля/, и смесь перемешивалась в течение дополнительных 10 минут. Реакция гасилась смесью льда и воды и уксусной кислотой /45 мг, 0,77 ммоля/ и перемешивалась в течение 10 минут. Смесь экстрагировалась этилацетатом, и органический экстракт промывался солевым раствором, сушился и концентрировался. Остаток очищался с помощью препаративной ВЭЖХ на ОДS S10 колонке с использованием 37% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/ и 63% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/, давая целевое соединение /40 мг, 46%/ в виде белого твердого вещества.
Т. пл. 112-118oC /аморфное/. Rf = 0,27, силикагель, 20:1 дихлорметан/метанол.
1H ЯМР /CDCl3/: δ 1,46 /с., 3H/, 1,76 /с., 3H/, 1,91 /с., 3H/, 2,19 /с., 3H/, 7,11-8,08 /м., 10H/.
Пример 33
N-[[2-[[(3,4-Диметил-5-изоксазолил) амино] сульфонил] -4-(2-оксазолил)-[1,1'-бифенил]-2-ил]-метил]-2-метилпропанамид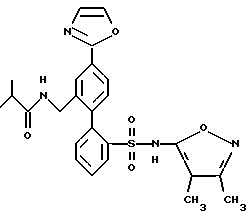
A. N-[[2'-[[(3,4-Диметил-5-изоксазолил) амино]-сульфонил]-4-(2-оксазолил) [1,1'-бифенил]-2- ил]метил]-2-метилпропанамид
К соединению G из примера 21 /70 мг, 0,17 ммоля/ и изобутирилхлориду /18 мг, 0,17 ммоля/ в 3,3 мл дихлорметана добавлялся триэтиламин /37 мг, 0,36 ммоля/. Реакционная смесь перемешивалась при комнатной температуре в течение 2 часов и концентрировалась. Остаток очищался с помощью препаративной ВЭЖХ на 30 х 500 мм ОДS S10 колонке с использованием 38% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/ и 62% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/, давая целевое соединение /36 мг, 44%/ в виде белого твердого вещества.
Т. пл. 112-120oC /аморфное/. Rf = 0,31, силикагель, 20:1 дихлорметан/метанол.
1H ЯМР /CDCl3/: δ 1,13 /м., 6H/, 1,93 /с., 3H/, 2,19 /с., 3H/; 2,42 / м. , 1H/; 4,04-4,43 / м., 2H/; 6,56-8,40 /м., 11H/.
Пример 34
N-[[2'-[[(3,4-Диметил-5-изоксазолил) амино] сульфонил] -4-(2- оксазолил)-[1,1'-бифенил]-2-ил]метил]-2,2,2-трифторацетамид
A. N-[[2'-[[(3,4-Диметил-5-изоксазолил)амино] сульфонил]-4-(2-оксазолил) [1,1'-бифенил]-2-ил]- метил]-2,2,2-трифторацетамид
К соединению G из примера 21 /40 мг, 0,094 ммоля/ в 1,9 мл дихлорметана добавлялся триэтиламин /19 мг, 0,19 ммоля/, а затем трифторуксусный ангидрид /20 мг, 0,094 ммоля/. Реакционная смесь перемешивалась при комнатной температуре в течение 2 часов и концентрировалась. Остаток очищался с помощью препаративной ВЭЖХ на 30 х 500 мм ОДS S10 колонке с использованием 37% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/ и 63% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/, давая целевое соединение /20 мг, 41%/ в виде белого твердого вещества. Т. пл. 112-120oC /аморфное/. Rf = 0,31, силикагель, 20:1 дихлорметан/метанол.
1H ЯМР /CDCl3/: δ 1,94 /с., 3H/, 2,19 /с., 3H/, 4,03-4,56 /м., 2H/, 7,06-8,06 /м.,10H/.
Пример 35
N-(3,4-Диметил-5-изоксазолил)-2'- [(метиламино) карбонил] -4'-(2-оксазолил) [1,1'-бифенил]-2-сульфонамид
A. N-(3,4-Диметил-5-изоксазолил)-2'-[(метиламино) карбонил] -4'-(2-оксазолил) [1,1'-бифенил]-2-сульфонамид.
К соединению А из примера 31 /124 мг, 0,28 ммоля/ в 2,8 мл ТГФ при 0oC добавлялся 1,1'-карбонилдиимидазол /101 мг, 0,62 ммоля/. После перемешивания при комнатной температуре в течение 2 часов добавлялся 1 мл метиламина /40% в воде/, и реакционная смесь перемешивалась при комнатной температуре в течение 3 часов. Добавлялось 10 мл 1 н. HCl и смесь перемешивалась в течение 3 минут. Смесь экстрагировалась 50 мл этилацетата, и органический экстракт промывался водой и солевым раствором, сушился и концентрировался. Остаток растворялся в 3 мл насыщенного водного раствора бикарбоната натрия и фильтровался. Фильтрат подкислялся до pH менее 5 бисульфатом натрия, и смесь фильтровалась затем, давая целевое соединение в виде белого твердого вещества /80 мг, 63%/.
Т. пл. 122-131oC.
Rf = 0,11, силькагель, 20:1 дихлорметан/метанол.
1H ЯМР /CDCl3/: δ 1,89 /с., 3H/, 2,20 /с., 3H/, 3,73 /с., 3H/, 2,76 /д., f = 3,5 Гц, 3H/, 6,53-8,16 /м., 11H/.
Пример 36
N-(3,4-Диметил-5-изоксазолил)-2', 4'-бис(2- оксазолил)[1,1'-бифенил]-2-сульфонамид
А. 2'-[[(3,4-Диметил-5-изоксазолил) [(2- метилэтокси)метил] амино] -сульфонил]-4-(2- оксазолил) [1,1'-бифенил]-2 карбоновая кислота.
К соединению E из примера 21 /525 мг, 1,03 ммоля/ и сульфаминовой кислоте /199 мг, 2,05 ммоля/ в 14,7 мл ТГФ при 0oC добавлялся охлажденный льдом раствор хлорида натрия /186 мг, 2,05 ммоля/ в 14,7 мл воды. Смесь перемешивалась при 0oC в течение 2 минут, а затем разбавлялась 100 мл дихлорметана. Органическая жидкость отделялась и промывалась солевым раствором, сушилась и концентрировалась, давая соединение А в виде смолы, которая использовалась без дальнейшей очистки.
В. 2'-[[(3,4-Диметил-5-изоксазолил) [(2-метилэтокси) метил]амино]-сульфонил]-4-(2-оксазолил) [1,1'-бифенил] -2-карбонилхлорид
К соединению А и 0,026 мл ДМФ в дихлорметане добавлялся оксалилхлорид /2 М в дихлорметане, 1,3 мл, 2,6 ммоля/. Реакционная смесь перемешивалась при комнатной температуре в течение 1 часа и концентрировалась, давая соединение В.
С. N-(3,4-Диметил-5-изоксазолил)-N-[(2- метилэтокси)метил] -2', 4'-бис(2-оксазолил) [1,1'- бифенил]-2-сульфонамид
Смесь соединения В, 1H-1,2,3-триазола /71 мг, 1,03 ммоля/ и карбоната калия /936 мг, 6,8 ммоля/ в 4,1 мл сульфолана нагревалась при 140oC в течение 3 часов. Смесь разбавлялась 100 мл этилацетата, промывалась водой и солевым раствором, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 50:70:0,1 смеси гексана, этилацетата и триэтиламина, давая соединение С.
Д. N-(3,4-Диметил-5-изоксазолил)-2', 4'-бис(2- оксазолил) [1,1'-бифенил] -2-сульфонамид
К соединению С в 10 мл 95% этанола добавлялось 10 мл 6 н. HCl. Смесь нагревалась с обратным холодильником в течение 1 часа и концентрировалась. Остаток нейтрализовался до pH 5 бикарбонатом натрия и экстрагировался этилацетатом. Органические экстракты промывались солевым раствором, сушились и концентрировались. Остаток очищался с помощью препаративной ВЭЖХ на ОДS S10 колонке с использованием 35% растворителя А /10%метанол, 90% вода, 0,1% трифторуксусная кислота/ и 65% растворителя B /90% метанол, 10% вода, 0,1% трифторуксусная кислота/, давая целевое соединение /56 мг, 12% в четыре стадии/ в виде белого твердого вещества. Т. пл. 108-113oC /аморфное/. Rf = 0,30, силикагель, 20:1 дихлорметан/метанол.
1H ЯМР /CDCl3/ δ 1,90 /с., 3H/, 2,19 /с., 3H/, 7,02-9,61 /м., 12H/.
Примеры 37 и 38
(Z)-N-(3,4 -Диметил-5-изоксазолил)-4'-(2-оксазолил)-2'-(2- фенилэтенил)-[1,1'-бифенил]- 2-сульфонамид
(E)-N-(3,4-Диметил-5-изоксазолил)-4'-(2- оксазолил)-2'-(2-фенилэтенил)-[1,1'-бифенил]-2- сульфонамид
A. (Z)-N-(3,4-Диметил-5-изоксазолил)-N-[(2- метилэтокси)метил]-4'-(2-оксазолил)-2'-(2-фенилэтенил) [1,1'- бифенил]-2-сульфонамид
и
В. (E)-N-(3,4-Диметил-5-изоксазолил)-N-[(2- метилэтокси)метил]-4'-(2-оксазолил)-2'-(2-фенилэтенил) [1,1'- бифенил]-2-сульфонамид
К бензилтрифенилфосфонилхлориду /300 мг, 0,77 ммоля/ в 7,7 мл ТГФ при -78oC добавлялся н-бутиллитий /2 М в пентане, 0,39 мл, 0,78 ммоля/. Холодная баня удалялась, и смесь перемешивалась при комнатной температуре в течение 45 минут перед охлаждением снова до -78oC. Соединение E из примера 21 /304 мг, 0,59 ммоля/ добавлялось при -78oC, и реакционная смесь затем перемешивалась при комнатной температуре в течение 2,5 часов. Добавлялось 10 мл воды и 40 мл этилацетата. Органическая жидкость отделялась и промывалась насыщенным водным хлористым аммонием и солевым раствором, сушилась и концентрировалась. Остаток хроматографировался на силикагеле с использованием 2:1 смеси гексан/этилацетат, давая смесь соединений А и В.
С. (Z)-N-(3,4-Диметил-5-изоксазолил)-4'-(2- оксазолил)-2'-(2-фенилэтенил) [1,1'-бифенил]-2- сульфонамид
и
Д. (E)-N-(3,4-Диметил-5-изоксазолил)-4'-(2- оксазолил)-2'-(2-фенилэтенил)-[1,1'-бифенил]-2- сульфонамид
К раствору соединений А и В в 6 мл 95% этанола добавлялось 6 мл 6 н. водной соляной кислоты, и смесь нагревалась с обратным холодильником в течение 1 часа. Реакционная смесь концентрировалась, и добавлялось 80 мл этилацетата. Органическая жидкость отделялась и промывалась солевым рассолом, сушилась и концентрировалась. Остаток очищался с помощью препаративной ВЭЖХ на ОДS S10 колонке с использованием 22% растворителя
A /10% метанол, 90% вода, 0,1% трифторуксусная кислота/ и 78% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/, давая соединение С, целевое соединение примера 37 /73 мг, 19% для двух стадий/ в виде белого твердого вещества.
Т. пл. 102-109oC /аморфное/, Rf = 0,32 /силикагель, 20:1 дихлорметан/метанол/.
ВЭЖХ колонка элюировалась теми же растворителями дополнительно, давая смесь, которая хлороматографировалась на силикагеле с использованием смеси 100:2 дихлорметан/метанол, давая соединение Д, целевое соединение примера 38 /27 мг, 7% для двух стадий/ в виде светло-желтого твердого вещества.
Т. пл. 109 -116oC /аморфное/, Rf = 0,32 /силикагель, 20:1 дихлорметан /метанол/.
1H ЯМР /CDCl3/ целевого соединения примера 37:
1,86 /с., 3H/, 2,16 /с., 3H/, 6,38-6,51 /м., J= 12,3 Гц, 2H/, 6,60-7,98 /м., 15H/.
1H ЯМР /CDCl3/ целевого соединения примера 38: δ 1,74 /с., 3H/, 2,01 /с. , 3H/, 6,72-7,10 /м., J= 16,4 Гц, 2H/, 7,17-7,98 /м., 15H/.
Пример 39
4-Хлор-N-[[(3,4-Диметил-5-изоксазолил)амино] сульфонил]-4-(2-оксазолил) [1,1'-бифенил]-2-ил]метил] фенилацетамид
A. 4-Хлор-N-[[2-[[(3,4-диметил-5-изоксазолил) амино] сульфонил]-4-(2-оксазолил)-[1,1'-бифенил]- 2-ил]метил]фенилацетамид
К раствору 0,20 г /0,47 ммоля/ соединения С из примера 21 в 15 мл дихлорметана добавлялось 0,082 г /0,47 ммоля/ 4- хлорбензоилхлорида и 0,104 г /1,03 ммоля / триэтиламина. Смесь затем перемешивалась при комнатной температуре в течение 16 часов и выпаривалась. Остаток очищался с помощью препаративной ВЭЖХ с обращенной фазой на 30 х 500 мм ОДS S10 колонке с использованием 79% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/ и 21% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/. Соответствующие фракции собирались и нейтрализовались водным бикарбонатом натрия до pH 7 и концентрировались до 10 мл. Раствор затем подкислялся до pH 4 с использованием ледяной уксусной кислоты, и белое твердое вещество отфильтровывалось и сушилось, давая 0,033 г /12,5%/ целевого соединения в виде белого твердого вещества. Т. пл. 130-134oC.
Пример 40
N-[[2'-[[(3,4-Диметил-5-изоксазолил) амино] сульфонил] -4-(2-оксазолил)-[1,1'-бифенил]-2-ил] метил]-N, 2,2-триметилпропанамид
A. N-[[2'-[[(3,4-Диметил-5-изоксазолил) амино]сульфонил]-4-(2-оксазолил) [1,1'-бифенил]-2- ил]метил] -N,2,2-триметилпропанамид
К раствору 0,25 г /0,59 ммоля/ промежуточного соединения, образовавшегося при получении соединения А из примера 28, в 10 мл дихлорметана добавлялось 0,078 г /0,65 ммоля/ пивалоилхлорида и 0,131 г /1,30 ммоля/ триэтиламина. Смесь затем перемешивалась при комнатной температуре в течение 16 часов и выпаривалась. Остаток очищался с помощью препаративной ВЭЖХ с обращенной фазой на 30 х 500 мм ОДS S10 колонке с использованием 75% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/ и 25% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/. Соответствующие фракции собирались и нейтрализовались водным бикарбонатом натрия до pH 7 и концентрировались до 10 мл. Раствор затем подкислялся до pH 4 с использованием водного бисульфата натрия, и белое твердое вещество отфильтровывалось и сушилось, давая 0,033 г /12%/ целевого соединения в виде белого твердого вещества.
Т. пл. 125-130oC.
Пример 41
N-[[2'-[[(3,4-Диметил-5-изоксазолил) амино] сульфонил] -4-(2- оксазолил)-[1,1'-бифенил]-2-ил]метил]-N-метилбензамид
A. N-[[2'-[[(3,4-Диметил-5-изоксазолил)амино] сульфонил]-4-(2-оксазолил) [1,1'-бифенил]-2-ил]метил]-N- метилбензамид
К раствору 0,25 г /0,59 г, ммоля/ промежуточного соединения, образовавшегося при получении соединения А из примера 28, в 10 мл дихлорметана добавлялось 0,10 г /0,71 ммоля/ бензоилхлорида и 0,13 г /1,3 ммоля/ триэтиламина. Смесь затем перемешивалась при комнатной температуре в течение 16 часов и выпаривалась. Остаток очищался с помощью препаративной ВЭЖХ с обращенной фазой на 30 x 500 мм ОДS S10 колонке с использованием 68% растворителя В /90% метанол, 10% вода, 0,1% трифторуксусная кислота/ и 32% растворителя А /10% метанол, 90% вода, 0,1% трифторуксусная кислота/. Соответствующие фракции собирались и нейтрализовались водным бикарбонатом натрия до pH 7 и концентрировались до 10 мл. Раствор затем подкислялся до pH 4 с использованием водного бисульфата натрия, и белое твердое вещество отфильтровывалось и сушилось, давая 0,075 г /23%/ целевого соединения в виде белого твердого вещества.
Т. пл. 132-140oC.
Пример 42
N-(3,4-Диметил-5-изоксазолил)-2'- оксазолил-5- ил-4'-оксазол-2-ил-[1,1'-бифенил]-2- сульфонамид
A. N-(3,4-Диметил-5-изоксазолил)-N-[(2-метоксиэтокси)метил] - 2'-оксазолил-5-ил-4'-оксазол-2-ил-[1,1'-бифенил]-2-сульфонамид
Раствор соединения F из примера 21 /300 мг, 0,57 ммоля/, тозилметилизоцианида /112 мг, 0,57 ммоля/ и карбоната калия /95 мг, 0,69 ммоля/ в 4 мл метанола нагревался с обратным холодильником в течение двух часов, после охлаждения до комнатной температуры реакционная смесь предварительно абсорбировалась на целите, и получающихся в результате порошок помещался на 2,5 х 20 см силикагельную колонку. Элюирование проводилось ступенчатым градиентом 200 мл смеси этилацетат: гексан 50:5, до этилацетата с 10% интервалами. Чистые фракции концентрировались, давая 96 мг /30%/ соединения А в виде светло-желтого масла.
В. N-(3,4-Диметил-5-изоксазолил)-2'-оксазолил-5 -ил-4'-оксазол-2-ил [1,1'-бифенил]-2-сульфонамид
Смесь соединения А /90 мг, 0,16 ммоля/, 6 н. HCl /1,6 мл/ и этанола /1,6 мл/ нагревалась с обратным холодильником в течение 2,5 часов. После охлаждения до комнатной температуры растворитель удалялся в вакууме, и остаток распределялся между этилацетатом /75 мл/ и насыщенным раствором хлористого аммония /50 мл/. Органический слои промывался водой /50 мл/ и солевым раствором /50 мл/. Сушка (сульфатом магния) и концентрирование давали розовое твердое вещество, попытки растворить данное твердое вещество в насыщенном бикарбонате натрия были безуспешными и получающаяся в результате суспензия фильтровалась и промывалась тщательно водой. Сушка под глубоким вакуумом давала 30 мг /41%/ целевого соединения в виде светло-розового твердого вещества.
Т. пл. 212-218oC /разл./.
1H ЯМР /DMCO-d6/: δ 1,56 /с., 3Н/, 2,06 /с., 3H/, 5,82 /с., 1H/, 7,21 /д., J= 8 Гц, 1H/, 7,36 /м., 1H/, 7,47 /с., 1H/, 7,79 /м., 2H/, 7,92 /д., J= 8 Гц, 1H/, 8,13 /м., 1H/, 8,32 /с., 2H/, 8,34 /с., 1H/.
Другие соединения, охватываемые настоящим изобретением, включают следующие соединения:
1. N-[[2'-[[(3,4-Диметил-5-изоксазолил)амино] сульфонил]-4-(2-оксазолил) [1,1'-бифенил]-2-ил] метил]-N-метилциклопропанамид,
2. N-[[2'-[[(3,4-Диметил-5-изоксазолил)амино] сульфонил]-4-(2-оксазолил) [1,1'-бифенил]-2-ил] метил]-2,2-диметил-N-(1-метилэтил)пропанамид,
3. N-Циклопропил-N-[[2'-[[(3,4-диметил-5- изоксазолил)амино]сульфонил] -4- (2-оксазолил), [1,1'- бифенил]-2-ил]метил]-2,2- диметилпропанамид,
4. N-[[2'-[[(3,4-Диметил-5-изоксазолил)амино] сульфонил]-4-(2-оксазолил) [1,1'-бифенил]-2-ил] метил]-2,2-диметил-N-(2,2,2-трифторэтил)-пропанамид,
5. N-(3,4-Диметил-5-изоксазолил)-2'-[2-(1 -метилэтил)-5-оксазолил]-4'-(2-оксазолил) [1,1'-бифенил] -2-сульфонамид,
6. N-(3,4-Диметил-5-изоксазолил)-2'-(4-оксазолил)-4'-(2- оксазолил)-[1,1'-бифенил]-2-сульфонамид,
7. N-(3,4-Диметил-5-изоксазолил)-2'-[2-(1-метилэтил)-4- оксазолил]-4'-(2-оксазолил) [1,1'-бифенил]-2-сульфонамид,
8. N-(3,4-Диметил-5-изоксазолил)-4'-(2-оксазолил)-2'-(2- оксазолил - метил)-[1,1'-бифенил]-2-сульфонамид,
9. N-(3,4-Диметил-5-изоксазолил)-4'-(2-оксазолил)-2'- [[5-(1-метилэтил)-2-оксазолил]метил] [1,1'- бифенил]-2-сульфонамид,
10. N-(3,4-Диметил-5-изоксазолил)-4'-(2-оксазолил)-2'- [[4-(1-метилэтил)-2-оксазолил]метил] [1,1'-бифенил]-2-сульфонамид,
11. (E)-N-(3,4-Диметил-5-изоксазолил)-2'-(4-метил-2-пентенил)-4'-(2- оксазолил) [1,1'-бифенил]-2-сульфонамид,
12. (Z)-N-(3,4-Диметил-5-изоксазолил)-2'-(4-метил-2- пентенил)-4'-(2-оксазолил) [1,1'-бифенил]-2-сульфонамид,
13. N-(3,4-Диметил-5-изоксазолил)-2'-(4- метилпентил)-4'-(2-оксазолил) [1,1'-бифенил]-2-сульфонамид,
14. транс-N-(3,4-Диметил-5-изоксазолил)-2'-[[2-(1-метилэтил) циклопропил]метил]-4'-(2-оксазолил) [1,1'- бифенил]-2-сульфонамид,
15. цис-N-(3,4-Диметил-5-изоксазолил)-2'-[[2-(1- метилэтил)циклопропил] метил]-4'-(2-оксазолил) [1,1'-бифенил]-2- сульфонамид,
16. N-(3,4-Диметил-5-изоксазолил)-4'-(2-оксазолил) [1,1':2',1''-терфенил]-2- сульфонамид,
17. N-(3,4-Диметил-5-изоксазолил)-3''-(1-метилэтил)-4'- (2-оксазолил) [1,1':2',1''-терфенил]-2-сульфонамид,
18. N-(3,4-Диметил-5-изоксазолил)-4''-(1-метилэтил)-4'-(2- оксазолил)-[1,1':2',1'']-терфенил]-2- сульфонамид,
19. N-(3,4-Диметил-5-изоксазолил)-2'-[(2-метилпропокси) метил]-4'-(2-оксазолил) [1,1'-бифенил]-2- сульфонамид,
20. N-(3,4-Диметил-5-изоксазолил)-2'-[2-(1-метилэтокси)этил] - 4'-(2-оксазолил) [1,1'-бифенил]-2-сульфонамид и
21. N-(3,4-Диметил-5-изоксазолил)-2'-[2-[(1-метилэтил)сульфонил]- этил] -4-(2-оксазолил) [1,1'-бифенил]-2-сульфонамид.
Приведенные выше соединения соответствуют (по номерам) структурам 1-21 (см. в конце описания).
Пример 43. Испытание соединений на биологическую активность.
Методика, использованная для получения этих данных, описана в статье Stein et al. Discovery and Structure - Activity Relationships of Sulfonamide ETA - Selective Antagonists (J. Med. Chem. vol 38, N 8, 1995, 1344-1354). Результаты испытаний:
Пример N - ETA Ki (нм)
1 - 1,4
5 - 0,5
19 - 1,1
22 - 0,2
23 - 0,15
25 - 0,2
26 - 0,2
27 - 0,1
28 - 0,2
29 - 0,4
31 - 3,3
32 - 1,2
35 - 3,7
36 - 22
38 - 2,5
42 - 32-

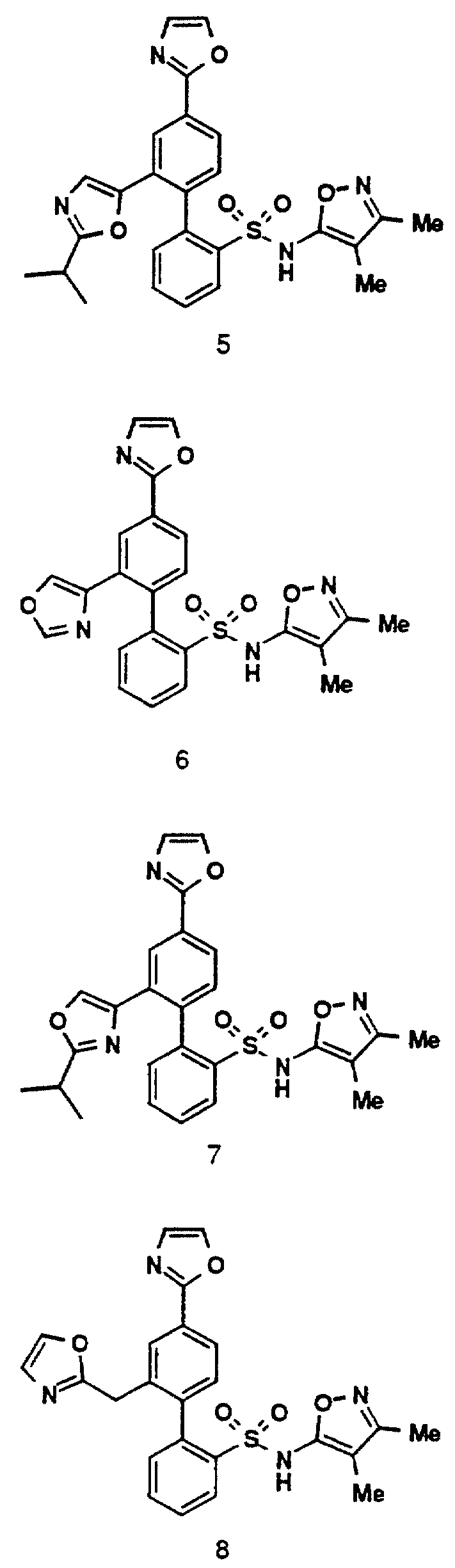


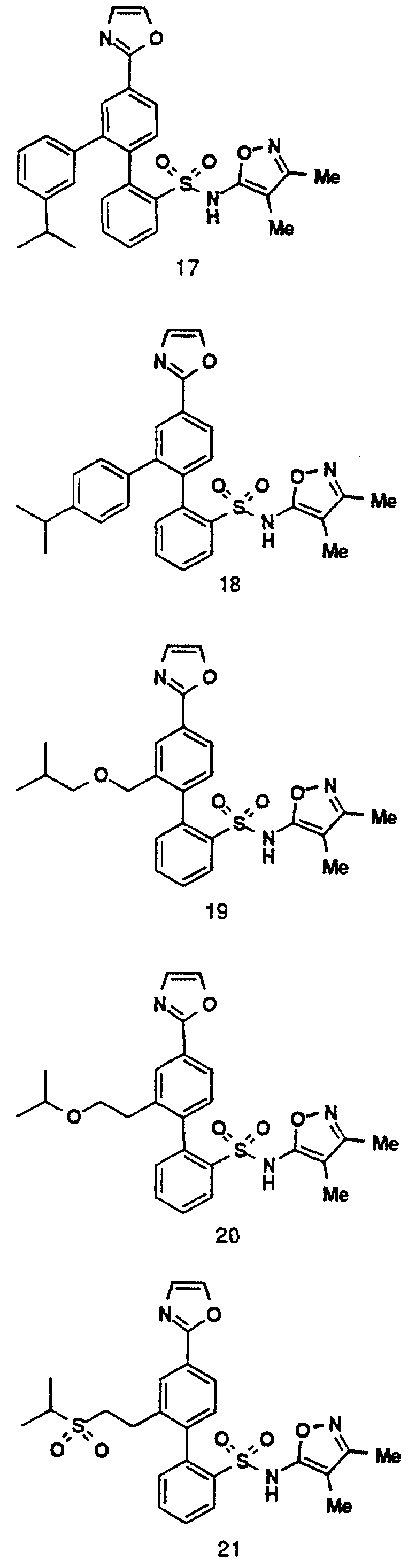
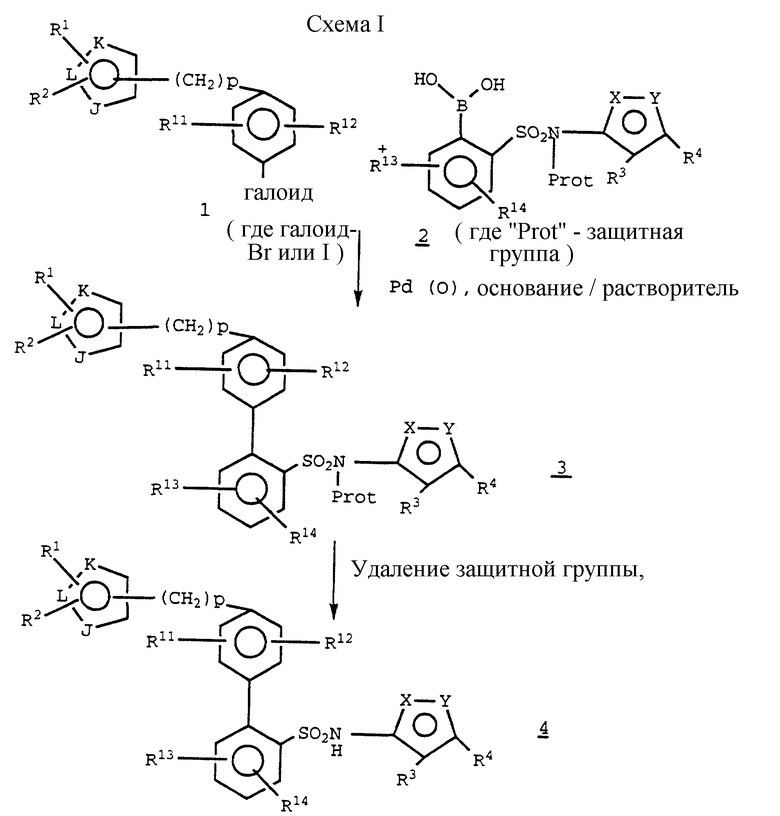


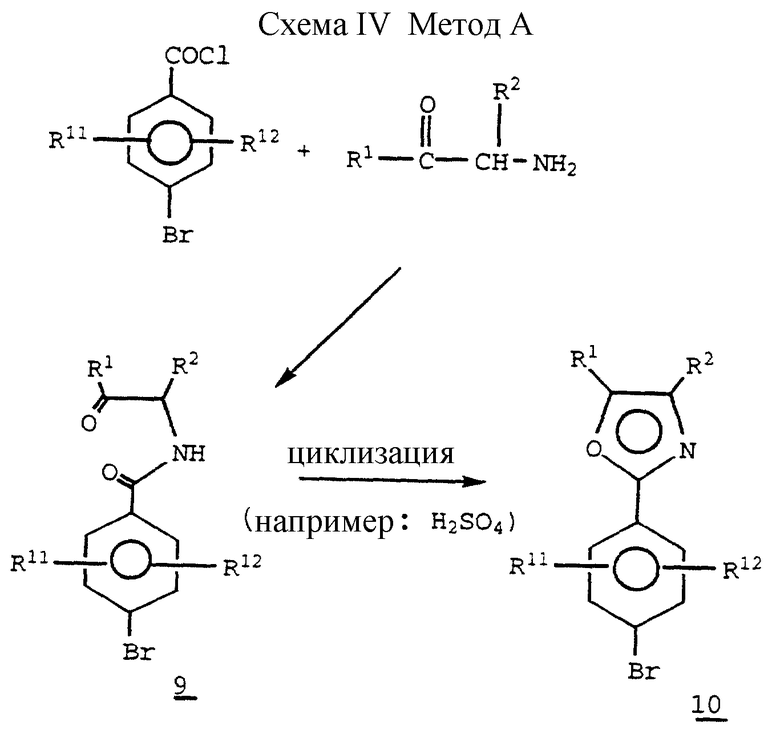


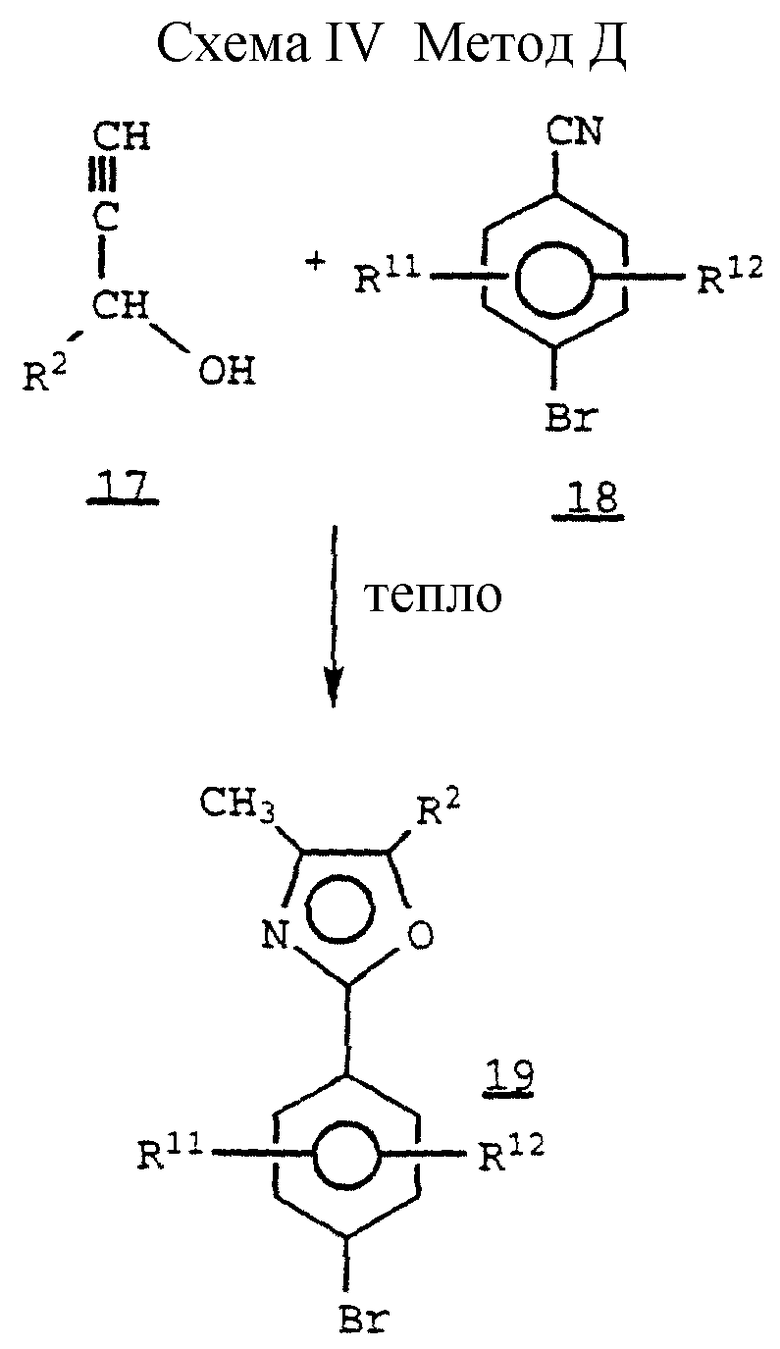

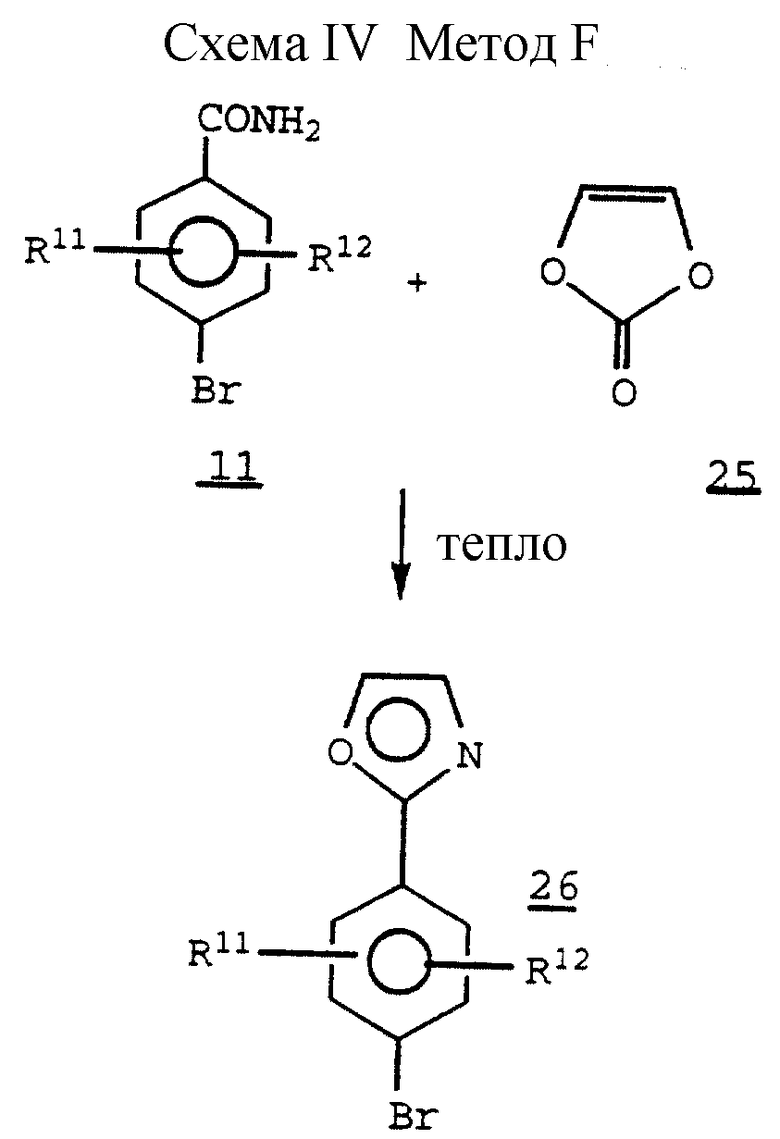
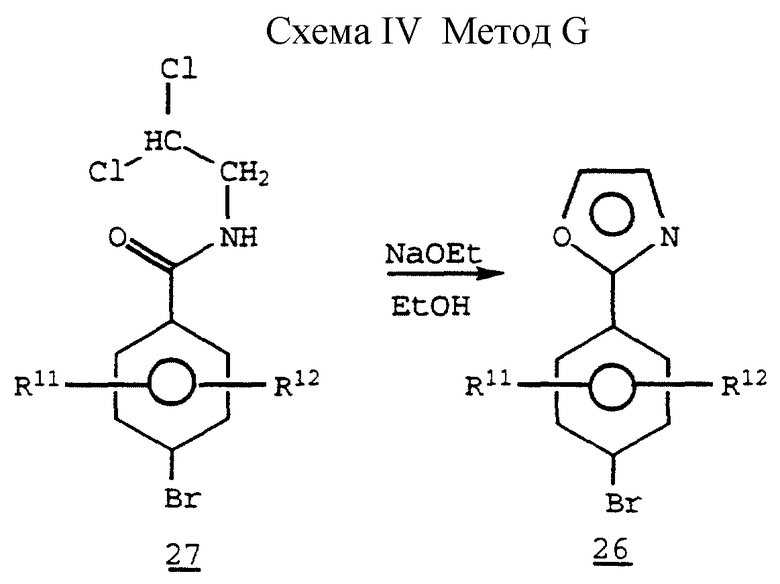
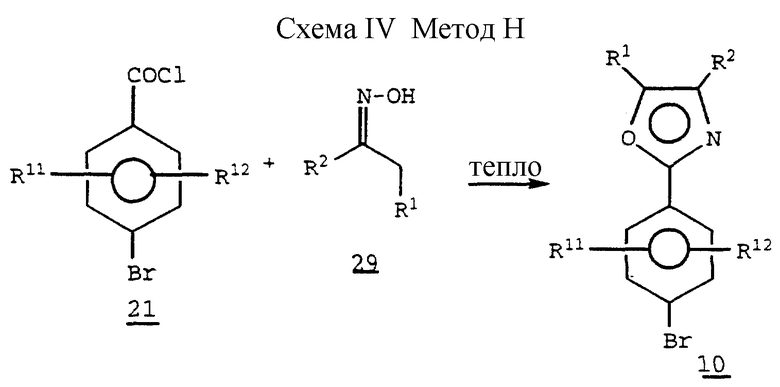





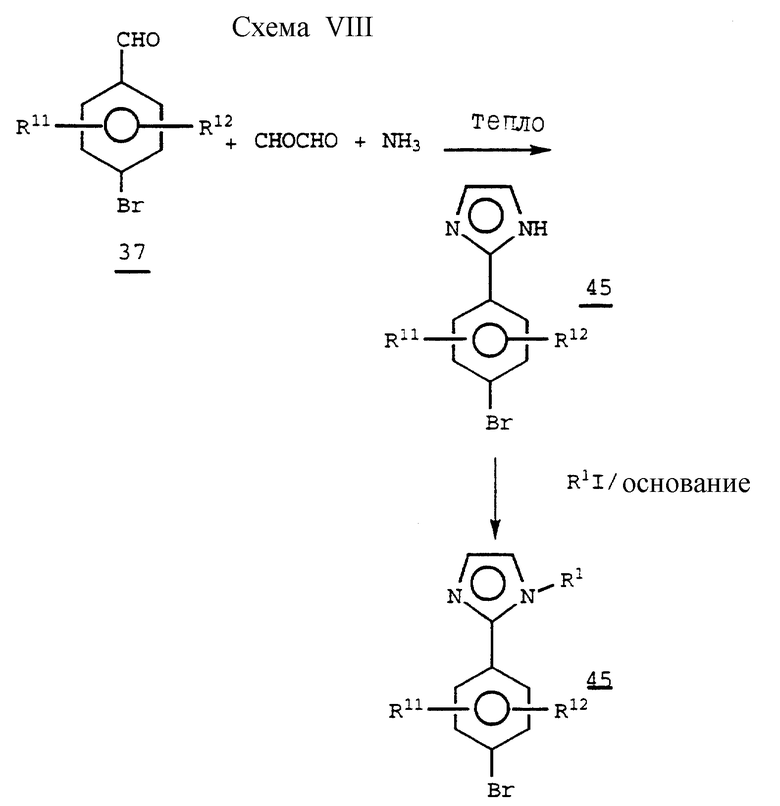
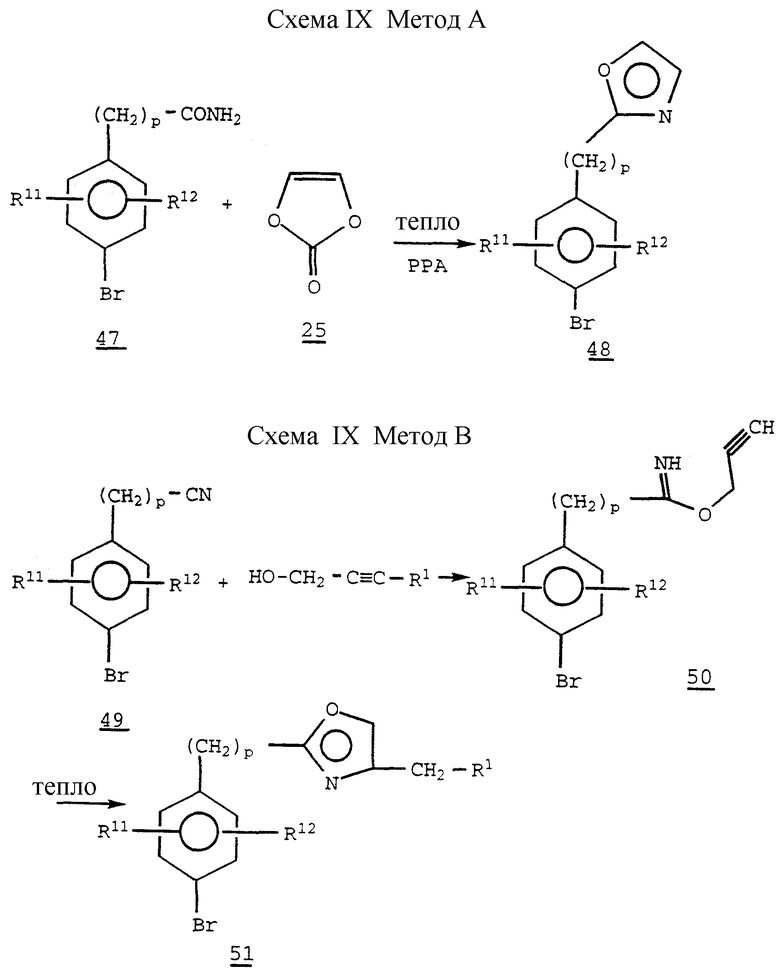



Описываются новые соединения формулы (I) или их фармацевтически приемлемые соли, где Х - О; Y - N; J - О, S, N - R15; K и L - C или N при условии, что один из них С; р = 0, 1; R - водород, низший алкил, группа Z4-NR6R7, где Z4 представляет группу Z9COZ10 и Z4, Z9, Z10 каждый означает одинарную связь; R6 - водород, алкил; R7 - водород, R2 - водород или низший алкил; R3 и R4 каждый - низший алкил; R12, R13, R14 каждый - водород; R15 - водород, алкил, гидроксиэтоксиметил, метоксиэтоксиметил; R11 - водород, гидроксил, CO2R5, где R5 - алкил, оксазолил, алкенил, замещенный фенилом; Z4-NR6R7, где Z4 представляет Z9COZ10, где Z9 и Z10 каждый представляет одинарную связь; R6 и R7 определены выше; алкил, замещенный группой Z2, где Z2 - гидроксил, группа
где Z4 - связь, Z5 - группа Z9COZ10, Z9COOZ10, Z9S(O)nZ10, где Z9, Z10 - каждый одинарная связь, Z11 - водород, алкил, Z6 - водород, алкил, фенил, фенил, замещенный одним атомом галогена, алкил, замещенный тремя атомами галогена, n = 2 или Z2 представляет группу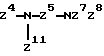
где Z4 - одинарная связь; Z5 - группа Z9COZ10, где Z9 и Z10 - одинарная связь, Z9 - водород, Z8 - алкил, фeнил; Z11 - водород, алкил. Соединения являются антагонистами эндотеллина. 14 з.п. ф-лы.


или их фармацевтически приемлемые соли,
где Х представляет О;
Y - N;
J - О, S, N, N-R15,
К и L - С или N, при условии, что один из них C;
p = 0, 1;
R1 - водород, низший алкил, группа Z4 - NR6R7, где Z4 представляет группу Z9COZ10 и Z4, Z9, Z10 - каждый означает одинарную связь, R6 - водород, алкил, R7 - водород;
R2 - водород или низший алкил;
R3 и R4 каждый - низший алкил;
R12, R13, R14 - каждый водород;
R15 - водород, алкил, гидроксиэтоксиметил, метоксиэтоксиметил;
R11 представляет 1) водород, 2) гидроксил, 3) CO2R5, где R5 - алкил, оксазолил, алкенил, замещенный фенилом, 4) Z4 - NR6R7, где Z4 - Z9COZ10, где Z9 и Z10 каждый представляет одинарную связь, R6 и R7 определены выше, 5) алкил, замещенный группой Z2, где Z2 - гидроксил, группа
где Z4 - связь;
Z5 представляет группу Z9COZ10, Z9C(O)OZ10, Z9S(O)nZ10, Z9, Z10 каждый - одинарная связь;
Z11 - водород, алкил;
Z6 - водород, алкил, фенил, фенил, замещенный одним атомом галогена, алкил, замещенный тремя атомами галогена;
n = 2;
или Z2 представляет группу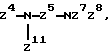
где Z4 - одинарная связь;
Z5 представляет группу Z9COZ10, где Z9 и Z10 представляют одинарную связь;
Z7 - вoдopoд;
Z8 - алкил, фенил;
Z11 - водород или алкил.
метиловый эфир 2'-[[(3,4-диметил-5-изоксазолил)амино]сульфонил]-4-(2-оксазолил)[1,1'-бифенил]-2-карбоновой кислоты;
N-(3,4-диметил-5-изоксазолил)-2'-(1-гидрокси-1-метилэтил)-4'-(2-оксазолил)[1,1-бифенил]-2-сульфонамид;
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]-метил]-2-метилпропанамид;
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метил]-2,2,2-трифторацетамид;
N-(3,4-диметил-5-изоксазолил)-2'-[(метиламино)карбонил] -4'-(2-оксазолил)[1,1'-бифенил]-2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-2', 4'-бис(2-оксазолил)[1,1'-бифенил] -2-сульфонамид;
(Z)-N-(3,4-димeтил-5-изoкcaзoлил)-4'-(2-оксазолил)-2'-(2-фенилэтенил)[1,1'-бифенил]-2-сульфонамид;
(E)-N-(3,4-диметил-5-изоаксазолил)-4'-(2-оксазолил)-2'-(2-фeнилэтeнил)[1,1'-бифенил]-2-сульфонамид;
4-хлор-N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил]-4-2-оксазолил)-[1,1'-бифенил]-2-ил]метил]фенилацетамид;
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метил]-N,2,2-триметилпропанамид;
N[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метил]-N-метилбензамид;
N-(3,4-диметил-5-изоксазолил)-2'-оксазолил-5-ил-4'-оксазол-2-ил-[1,1'-бифенил]-2-сульфонамид.
N-(3,4-диметил-5-изоксазолил)-4'-(2-оксазолил)[1,1'-бифенил]-2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-(2-тиазолил)[1,1'-бифенил] -2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-(4,5-диметил-2-оксазолил)[1,1'-бифенил] -2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-2-(5-оксазолил)[1,1'-бифенил]-2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-(4-оксазолил)[1,1-бифенил] -2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-(2-метил-4-оксазолил)[1,1'-бифенил] -2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-(4-метил-2-оксазолил)[1,1'-бифенил] -2-сульфонамид;
N-(3,4-диметил-5-изoкcaзoлил)-4'-(5-метил-2-оксазолил)[1,1'-бифенил] -2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-(1Н-пиразол-1-ил)[1,1'-бифенил]-2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-[1-[(2-метоксиэтокси)метил]-1Н-имидазол-2-ил][1,1'-бифенил]-2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-[1-[(2-гидроксиэтокси)метил] -1Н-имидазол-2-ил][1,1'-бифенил]-2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-(1-метил-1Н-имидазол-2-ил)[1,1'-бифенил]-2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-(1Н-имилазол-2-ил)[1,1'-бифенил] -2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-(5-метил-4-оксазолил)[1,1'-бифенил] -2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-(1Н-имидазол-1-ил-метил)[1,1'-бифенил] -2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-(3-изоксазолил)[1,1'-бифенил] -2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-(2-оксазолилметил)[1,1'-бифенил] -2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-4'-(5-изоксазолил)[1,1'-бифенил] -2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-2'-гидрокси-4'-(2-оксазолил)[1,1'-бифенил] -2-сульфонамид;
2-[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил][1,1'-бифенил]-4-ил] -4-оксазол-карбоксамид;
N-(3,4-димeтил-5-изoкcaзoлил)-2'-[(формиламино)метил] -4'-(2-оксазолил)[1,1'-бифенил]-2-сульфонамид;
N-(3,4-диметил-5-изоксазолил-2'-[[(метоксикарбонил)амино] метил]-4'-(2-оксазолил)[1,1'-бифенил]-2-сульфонамид;
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)-[1,1'-бифенил]-2-ил]метил]-N-метилмочевина;
N-(3,4-диметил-5-изоксазолил)-2'-[[(метилсульфонил)амино]метил]-4'-(2-оксазолил)[1,1'-бифенил]-2-сульфонамид;
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метил]ацетамид;
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)-[1,1'-бифенил]-2-ил]-мeтил-N'-фeнилмoчeвинa;
N-[[2'-[[(3,4-диметил-5-изоксазолил)-амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метил]-N'-пропилмочевина;
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метил]-N-метилацетамид;
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метилбензамид и
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил)-2-ил]метил]-2,2-диметилпропанамид.
N-(3,4-диметил-5-изоксазолил)-4'-(2-оксазолил)[1,1'-бифенил] -2-сульфонамид,
N-(3,4-диметил-5-изоксазолил)-4'-(2-тиазолил)[1,1'-бифенил]-2-сульфонамид,
N-(3,4-диметил-5-изоксазолил)-4'-(1Н-пиразол-1-ил)[1,1'-бифенил]-2-сульфонамид,
N-(3,4-диметил-5-изоксазолил)-4'-(1-метил-1Н-имидазол-2-ил)[1,1'-бифенил]-2-сульфонамид,
N-(3,4-диметил-5-изоксазолил)-2'-гидрокси-4-(2-оксазолил)[1,1'-бифенил] -2-сульфонамид,
2-[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил][1,1'-бифенил]-4-ил] -4-оксазолкарбоксамид,
N-(3,4-диметил-5-изоксазолил)-2'-[(формиламино)метил] -4'-(2-оксазолил)[1,1'-бифенил]-2-сульфонамид,
N-(3,4-диметил-5-изоксазолил)-2'-[[(метоксикарбонил)амино] метил] -4'-(2-оксазолил)[1,1'-бифенил]-2-сульфонамид,
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)-[1,1'-бифенил]-2-ил]метил]N'-метилмочевина,
N-(3,4-диметил-5-изоксазолил)-2'-[[(метилсульфонил)амино]метил]-4'-(2-оксазолил)[1,1'-бифенил]-2-сульфонамид,
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)-[1,1'-бифенил]-2-ил]метил]ацетамид,
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)-[1,1'-бифенил]-2-ил]метил]-N'-фенилмочевина,
N-[[2'-[[(3,4-диметил-5-изоксаэолил)амино] сульфонил] -4-(2-оксазолил)-[1,1'-бифенил]-2-ил]метил]-N'-пропилмочевина,
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метил]-N-метилацетамид,
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метил]бензамид, и
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метил]-2, 2-диметилпропанамид.
метиловый эфир 2'-[[(3,4-диметил-5-изоксазолил)амино]сульфонил]-4-(2-оксазолил)[1,1'-бифенил]-2-карбоновой кислоты;
N-(3,4-диметил-5-изоксазолил)-2'-(1-гидрокси-1-метилэтил)-4'-(2-оксазолил)[1,1'-бифенил]-2-сульфонамид;
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метил]-2-метилпропанамид;
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метил]-2,2,2-трифторацетамид;
N-(3,4-диметил-5-изоксазолил)-2'-[(метиламино)-карбонил] -4'-(2-оксазолил)[1,1'-бифенил]-2-сульфонамид;
N-(3,4-диметил-5-изоксазолил)-2', 4'-бис(2-оксазолил)[1,1'-бифенил] -2-сульфонамид;
(Z)-N-(3,4-диметил-5-изоксазолил)-4'-(2-оксазолил)-2'-(2-фенилэтенил)[1,1'-бифенил]2-сульфонамид;
(Е)-N-(3,4-диметил-5-изоксазолил)-4'-(2-оксазолил)-2'-(2-фенилэтенил)[1,1'-бифенил[2-сульфонамид;
4-хлор-N-[[2'-[[(3,4/диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1-бифенил]-2-ил]метил]фенилацетамид;
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метил]-N,2,2-триметилпропанамид;
N-[[2'-[[(3,4-диметил-5-изоксазолил)амино] сульфонил] -4-(2-оксазолил)[1,1'-бифенил]-2-ил]метил]-N-метилбензамид и
N-[[2'-[[(3,4-диметил-5-изоксазолил)-2'-оксазолил-5-ил-4'-оксазол-2-ил[1,1'-бифенил]-2-сульфонамид.
Приоритет по пунктам и признакам:
26.08.1994 по п.1 (кроме соединений, у которых R'' - оксазолил, алкенил, замещенный фенилом, Z6 - фенил, замещенный одним галогеном, алкил, замещенный тремя галогенами), пп.2 - 5 и 6 (кроме значений R'' - оксазолил, алкенил, замещенный фенилом), пп.7 - 11, 13 и 14;
04.01.1995 по пп.13 и 14;
25.08.1995 по пп.12, 15.
| EP 569163 A1, 10.11.1993 | |||
| Электронные часы, корректируемые радиосигналами точного времени | 1975 |
|
SU558258A1 |
| US 3660383 А1, 02.05.1972 | |||
| СУЛЬФОНАМИДНОЕ ПРОИЗВОДНОЕ ИЗОКСАЗОЛА ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ | 1993 |
|
RU2116301C1 |
Авторы
Даты
2001-10-20—Публикация
1995-08-25—Подача