Настоящее изобретение касается способа полимеризации олефинов, а именно, способа полимеризации в присутствии каталитической системы, включающей твердое каталитическое комплексное соединение на основе соединений магния, переходного металла и галогена и металлоорганическое соединение (сокатализатор).
В английском патенте GB 1464909 раскрываются каталитические системы, включающие твердое вещество на основе соединений магния, переходного металла и галогена и сокатализатор.
В примере 1 этого патента осуществляется полимеризация этилена в присутствии триизобутилалюминия (сокатализатор) и каталитически твердого вещества, полученного при смешивании этилата магния с тетрабензилтитаном и при введении в эту смесь дихлорида этилалюминия до получения твердого осадка.
Полученный в присутствии этого известного каталитического твердого вещества полиэтилен имеет высокое содержание олигомеров (полимеров с малой молекулярной массой, содержащих максимально 15 мономерных единиц), которые вызывают появление дыма при последующем использовании полиэтилена, например, процессе выдувания флаконов. Кроме того, олигомеры разрушают механические и реологические свойства полиолефинов.
Согласно изобретению с целью устранения этих недостатков, предлагается новый способ получения полиолефинов, в частности, с малым содержанием олигомеров и с улучшенными механическими и реологическими свойствами.
Таким образом, изобретение касается способа полимеризации олефинов, по которому по крайней мере один олефин вводят в контакт с каталитической системой, включающей:
а) твердый каталитический комплекс на основе соединений магния, переходного металла и галогена, причем указанный каталитический комплекс получают, на первом этапе, путем реакции по крайней мере одного соединения магния, выбранного из органических кислородсодержащих соединений и галогенсодержащих соединений магния, с по крайней мере одним соединением переходного металла группы IVB или VB Периодической таблицы, выбранным из органических кислородсодержащих соединений и галогенсодержащих соединений переходного металла, до получения жидкого комплекса, и, на втором этапе, осаждают это жидкое комплексное соединение с помощью галогенсодержащего алюминийорганического соединения общей формулы Al Rn X3-n, где R - радикал углеводорода, X - галоген, а n - меньше 3, для образования твердого каталитического комплекса; и
б) металлоорганическое соединение металла групп IA, IIA, IIB, IIIA и IVA Периодической таблицы;
кроме того, по изобретению твердая каталитическая система включает:
с) по крайней мере один донор электронов, который применяют после первого этапа получения твердого каталитического комплекса, на котором получают жидкий комплекс.
Одним из основных признаков изобретения состоит в использовании донора электронов после первого этапа получения твердого каталитического комплекса, на котором получают жидкое комплексное соединение. Заявитель констатирует, что применение донора электронов на первом этапе получения жидкого комплекса приводит к получению катализаторов полимеров с малым кажущимся удельным весом, что выражается в малом выходе. Донор электронов может, таким образом, использоваться либо во время получения твердого каталитического комплекса (одновременно с последующим этапом или на дополнительном этапе), либо на стадии полимеризации одновременно с твердым каталитическим комплексом и металлоорганическим соединением.
Твердый каталитический комплекс, используемый в способе изобретения, предпочтительно предварительно не полимеризуют.
В первом варианте способа по изобретению донор электронов используется во время получения твердого каталитического комплекса непосредственно после первого этапа, т.е. после образования жидкого комплекса, и до этапа осаждения. Обработка с помощью донора электронов может быть осуществлена любым известным адекватным способом. Донор электронов может вводиться в жидкий комплекс в чистом виде или в виде раствора в растворителе, таком как жидкие алифатические, циклоалифатические и ароматические углеводороды. Предпочтительными растворителями являются углеводороды, содержащие до 20 атомов углерода и, в частности, линейные алканы (такие как н-бутан, н-гексан и н-гептан) или разветвленные алканы (такие как изобутан, изопентан, изооктан) или циклоалканы (такие как циклопентан и циклогексан). При использовании линейных алканов получают хорошие результаты. Предпочтителен гексан.
По первому варианту, температура обработки донором электронов, как правило, ниже температуры разложения донора электронов и жидкого комплекса. В частности, она по крайний мере составляет -20oC, точнее по крайней мере 0oC, причем чаще применяются температуры по крайней мере 20oC. Обычно температура составляет самое большее 150oC, в частности, самое большее 120oC, причем рекомендуются температуры, самое большее 100oC, например самое большее 70oC.
Продолжительность обработки донором электронов по первому варианту обычно составляет от 0,5 минуты до 5 часов, предпочтительно от 1 минуты до 2 часов, например от 5 минут до 1 часа. Давление, при котором осуществляется обработка, не является критическим, предпочтительно работают при атмосферном давлении.
Обычно, по первому варианту используют по крайней мере 0,01 моля донора электронов на моль переходного металла, а именно, по крайней мере 0,02 моля, причем предпочтительны значения по крайней мере 0,05 моля. Используемое количество донора электронов не превышает, как правило, 50 молей на моль переходного металла, предпочтительно не превышает 30 молей, причем рекомендуются значения самое большее 20 молей. Наиболее подходящие количества от 0,2 до 12 молей.
Первый вариант позволяет не только сократить содержание олигомеров в полученных полиолефинах, но также и повысить полимеризационную активность твердого каталитического комплекса и заметно увеличить удельный вес полученных полиолефинов. Кроме того, полученный по первому варианту твердый каталитический комплекс более чувствителен к регуляторам молекулярной массы полиолефинов, таким образом требуется меньшее количество регулятора молекулярной массы (например водорода) для получения заданной молекулярной массы. Первый вариант позволяет также модулировать морфологию твердого каталитического комплекса и, таким образом, морфологию полиолефинов, полученных из этого твердого каталитического комплекса. В частности, он позволяет уменьшить ширину гранулометрического распределения твердого каталитического комплекса.
Во втором варианте способа получения, в соответствии с изобретением, донор электронов используется при получении твердого каталитического комплекса после этапа осаждения из жидкого комплекса и предпочтительно после возможных промежуточных этапов созревания и промывки осадка (которые описаны ниже), но до контакта твердого каталитического комплекса с олефином для его полимеризации. Для этого, донор электронов может быть введен в чистом виде или в форме раствора в растворителе, таком как описано выше, в суспензию твердого каталитического комплекса в инертном разбавителе. Этот инертный разбавитель может быть выбран, например, из алифатических или циклоалифатических углеводородов. Подходят также и линейные или разветвленные алканы или циклоалканы, содержащие до 20 атомов углерода. Особенно гексан.
Температура, давление, используемое количество донора электронов и продолжительность обработки донором электронов по второму варианту соответствуют описанному выше первому варианту.
Второй вариант позволяет не только сократить содержание олигомеров в полученных полиолефинах, но и модулировать влияние на твердый каталитический комплекс регуляторов молекулярной массы полиолефинов (например водород) путем изменения количества используемого донора электронов. Так, было отмечено, что чем больше количество используемого донора электронов, тем ярче выражено влияние на твердый каталитический комплекс регулятора. Из этого следует, что может быть получена очень широкая гамма полиолефинов с сильно разнящимися молекулярными массами, и, следовательно, совершенно разными показателями текучести.
Третий вариант способа по изобретению состоит в использовании донора электронов при полимеризации, а не при получении твердого каталитического комплекса. Он дает лучшие результаты при осуществлении полимеризации в газовой фазе. По третьему варианту донор электронов может вводиться отдельно в полимеризационную среду в любой момент, предпочтительно в начале полимеризации. Наиболее интересна та форма осуществления третьего варианта, при которой донор электронов вводят в предварительно приготовленную смесь полимеризационной среды с металлоорганическим соединением. Эта смесь может быть получена простым контактом донора электронов с металлоорганическим соединением или при введении донора электронов, предпочтительно постепенно в раствор металлоорганического соединения, или же вводя в раствор донора электронов в раствор металлоорганического соединения. Предпочтительно введение донора электронов в чистом виде в раствор металлоорганического соединения в растворителе, таком как определено выше для двух других вариантов.
В третьем варианте обычно используют такое количество донора электронов, чтобы молярное соотношение используемого количества металлоорганического соединения и используемого количества донора электронов равнялось бы по крайней мере 0,01, а именно по крайней мере 0,05, наиболее интересны значения по крайней мере 0,2. Чаще всего отношение этих количеств не превышает 100, предпочтительно не превышает 80, рекомендуются значения самое большее 60.
Преимуществом третьего варианта является не только снижение содержания олигомеров в полученных полиолефинах, но и повышение полимеризационной активности твердого каталитического комплекса. Его преимущества выявляются особенно при способе полимеризации в газовой фазе, который характеризуется, главным образом, ограниченной способностью к теплопередаче, т.к. кинетический профиль твердого каталитического комплекса имеет ярко выраженный индуктивный период.
В рамках настоящего изобретения под донором электронов понимаются органические соединения, содержащие один или несколько атомов или одну или несколько групп атомов, имеющих одну или несколько пар свободных электронов, такие как, например, кислород, азот, сера или группы, содержащие один из этих элементов. Предпочтительно донор электронов выбирают из органических соединений, содержащих один или несколько атомов или одну или несколько групп атомов, имеющих одну или несколько пар свободных электронов, кроме спиртов, фенолов, силанов и полисилоксанов. Примерами использования доноров электронов в способе по изобретению являются эфиры, кетоны, альдегиды, органические кислоты, сложные эфиры органических кислот, галогениды органических кислот, амиды органических кислот, амины и нитрилы.
В качестве примера эфиров можно привести эфиры, содержащие от 2 до 20 атомов углерода, такие как изоамиловый эфир. Обычно используются кетоны, содержащие от 3 до 18 атомов углерода, такие как метилэтилкетон и ацетофенон. Обычно используются альдегиды, содержащие от 2 до 15 атомов углерода, такие как октилальдегид и бензальдегид. Примером органических кислот являются органические кислоты, содержащие до 24 атомов углерода, такие как бутановая кислота и анисовая кислота. В качестве сложных эфиров органических кислот можно использовать, например, эфиры, содержащие от 2 до 30 атомов углерода, такие как метилацетат, этилпропионат, метилбутират, пропилметакрилат, этилбензоат, фенилбензоат, о-этил-метоксибензоат, п-метилтолуат, метилсалицилат, этилнафтоат, фталат и этил- или бутил-анизат. Особенно подходят этилбензоат, 3,5-бис(1,1-диметилэтил)-4-гидрокси-октадецилбензолпропионат или дибутилфталат. В качестве примера галогенидов органических кислот можно привести галогениды, содержащие от 2 до 15 атомов углерода, такие как ацетилхлорид и толуилхлорид. В качестве амидов кислот можно привести, например, ацетамид, бензамид и толуамид. Обычно используются амины, такие как например диэтиламин, пиперидин, трибензиламин, анилин и пиридин. В качестве нитрилов можно использовать, например, ацетонитрил и бензонитрил. Особенно подходят простые и сложные эфиры органических кислот. Предпочтительны сложные эфиры органических кислот, в частности этилбензоат и дибутилфталат, и особенно этилбензоат.
Используемый в способе полимеризации по изобретению твердый каталитический комплекс получают в результате по крайней мере двух последовательных этапов, а именно первого этапа образования жидкого комплекса и последующего этапа осаждения, известных из литературы.
Первый этап получения твердого каталитического комплекса состоит в получении жидкого комплекса путем реакции соединения магния с соединением переходного металла. Естественно, можно использовать одновременно несколько различных соединений магния. Можно также использовать одновременно несколько различных соединений одного переходного металла или несколько соединений с различными переходными металлами. Реакция на первом этапе может быть осуществлена любым известным адекватным способом для получения комплекса в жидком состоянии. Если рабочие условия реакции обуславливают жидкую форму соединения магния и/или соединения переходного металла, предпочтительно осуществлять реакцию путем простого смешивания этих реактивов в отсутствии растворителя или разбавителя. Однако можно проводить реакцию в присутствии разбавителя, если количества жидкости в реакционной среде недостаточно для завершения реакции или если рабочие условия реакции обуславливают твердую форму двух реактивов. Разбавитель обычно выбирают из тех, которые могут растворять по крайней мере один из реагентов и, в частности, один из описанных выше растворителей.
Используемое количество соединения переходного металла определяется по соотношению с используемым количеством соединения магния. Оно может варьироваться в широком диапазоне. Как правило, оно составляет по крайней мере 0,01 моля переходного металла, содержащегося в соединении переходного металла, на моль магния, содержащегося в соединении магния, в частности, по крайней мере 0,02 моля, предпочтительны значения по крайней мере 0,05. Обычно используют количества, самое большее, 20 молей переходного металла, содержащегося в соединении переходного металла, на моль магния, присутствующего в соединении магния, а именно, самое большее, 10 молей, причем рекомендуются значения, самое большее, 5 молей.
Температура, при которой проводят реакцию соединения магния и соединения переходного металла при первом этапе получения твердого каталитического комплекса, зависит от природы реагентов и предпочтительно ниже температуры разложения реагентов и жидкого комплекса, полученного в результате этой реакции. Как правило, она составляет по крайней мере -20oC, в частности, по крайней мере 0oC, причем чаще используются температуры по крайней мере 20oC. Обычно применяются температуры самое большее 200oC, особенно самое большее 180oC, причем предпочтение отдается температурам, самое большее 150oC, например около 140oC.
Продолжительность первого этапа получения твердого каталитического комплекса зависит от природы реагентов и рабочих условий реакции и, предпочтительно, достаточна для завершения реакции между реагентами. Продолжительность реакции может варьироваться, как правило, от 10 минут до 20 часов, точнее от 2 до 15 часов, например от 4 до 10 часов.
Давление, при котором осуществляется реакция на "первом этапе, и скорость введения реагентов не являются критическими. Для удобства, как правило, работают при атмосферном давлении; скорость введения выбирают, как правило, таким образом, чтобы не вызвать резкого нагрева реакционной среды из-за возможного самоускорения реакции. Реакционную среду перемешивают, как правило, таким образом, чтобы обеспечить ее однородность в течение всей реакции. Реакция может осуществляться как в непрерывном, так и в периодическом режиме.
По завершении первого этапа формирования твердого каталитического комплекса, собирают жидкий комплекс соединения магния и соединения переходного металла, который можно использовать при последующем этапе или который можно, при необходимости, хранить в разбавителе, предпочтительно инертном, с целью его последующей полной рекуперации и использования в присутствии разбавителя. Разбавитель чаще всего выбирают из алифатических или циклоалифатических углеводородов, предпочтительно содержащих до 20 атомов углерода, таких как, например, алканы, изобутан, пентан, гексан, гептан или циклогексан или их смеси. Особенно подходит гексан.
Соединение магния выбирают из органических кислородсодержащих соединений и галогенсодержащих соединений магния.
Под органическим кислородсодержащим соединением магния понимают все соединения, где органический радикал связан с магнием через кислород, т.е. все соединения, содержащие по крайней мере одну последовательность связей магний-кислород-органический радикал на атом магния. Органические радикалы, связанные с магнием через кислород, как правило выбирают из радикалов, содержащих до 20 атомов углерода, и особенно из тех, которые содержат до 10 атомов углерода. Хорошие результаты получены, когда эти радикалы содержат от 2 до 6 атомов углерода. Эти радикалы могут быть насыщены и ненасыщенны, с разветвленной, прямой или циклической цепью. Их выбирают предпочтительно из углеводородных радикалов, в частности из алкилов (линейных или разветвленных), алкиленов, арилов, циклоалкилов, арилалкилов, алкиларилов, ацилов и их производных, полученных замещением.
Кроме органических радикалов, связанных с магнием через кислород, органические кислородсодержащие соединения магния могут содержать и другие радикалы. Предпочтительно ими являются радикалы -OH, (SO4)1/2, -NO3, -(PO4)1/3, -(CO3)1/2 и -ClO4. Речь также может идти об органических радикалах, углерод которых связан непосредственно с магнием.
В качестве используемых органических кислородсодержащих соединений магния можно привести алкоксиды (такие как этилат и циклогексанолат), алкилалкоксиды (такие как этилэтилат), гидроксиалкоксиды (такие как гидроксиметилат), феноксиды (такие как нафтенат), карбоксилаты, при необходимости, гидратированные (такие как ацетат и бензоат). Речь может идти также и об органических азот-кислородсодержащих соединениях, т.е. соединениях, содержащих цепи связей магний-кислород-азот-органический радикал (такие как оксиматы, в частности бутил-оксимат, соли гидроксиламинокислоты, в частности производное N-нитрозо-N,N-фенил-гидроксиламина), хелаты, т.е. органические кислородсодержащие соединения, в которых магний содержит по крайней мере один ряд обычных связей типа магний-кислород-органический радикал и по крайней мере одну координационную связь для образования гетероцикла, в который включен магний, (такие как энолаты, в частности, ацетилацетонат), силанолаты, т.е. соединения, содержащие ряды связей магний-кислород-кремний-углеводородный радикал (такие как трифенилсиланолат). Можно также привести в качестве примера органические кислородсодержащие соединения магния, содержащие несколько различных органических радикалов (такие как метоксиэтилат магния), сложные алкоксиды и феноксиды магния и другого металла (такие как Mg[Al(OR)4)2] смеси двух или нескольких органических кислородсодержащих соединений магния, определенных выше.
Под галогенсодержащим соединением магния подразумевают любое соединение, содержащее по крайней мере одну связь магний - галоген. Галогеном может быть фтор, бром или йод. Предпочтителен хлор.
В качестве галогенсодержащих соединений магния можно привести дигалогениды, предпочтительно содержащие максимально одну молекулу воды на молекулу дигалогенида, комплексные дигалогениды (такие как MgCl2•6NH3 или MgCl2•6CH3OH), соединения, содержащие кроме связи магний-галоген, органический радикал, связанный с магнием через кислород (такие как Mg(OH)Cl или Mg(O-CH3)Cl). Также речь может идти о соединениях, содержащих кроме связи магний-галоген одну связь магний-органический радикал (такие как Mg(C2H5)Cl), продукты гидролиза гидратированных галогенидов магния, если эти продукты содержат также связи магний-галоген, смешанные соединения, содержащие, галоген- и кислородсодержащие соединения магния (такие как MgCl2•MgO•H2O) или смеси двух или нескольких галогенсодержащих соединений магния, определенных выше.
Из подходящих соединений магния используют, предпочтительно те, которые содержат на атом магния только связи магний-кислород-органический радикал и/или связи магний-галоген, кроме любой другой связи. Лучшие результаты были получены при использовании органических кислородсодержащих соединений, особенно тех, которые содержат только на атом магния связи магний-кислород-органический радикал. Предпочтительны алкоксиды магния. Лучшие результаты были получены при использовании диалкоксидов магния, в частности диэтилата магния.
Соединение переходного металла выбирают из органических кислородсодержащих соединений и галогенсодержащих соединений переходного металла.
Под органическим кислородсодержащим соединением переходного металла понимают все соединения, где органический радикал связан с переходным металлом через кислород, т.е. все соединения, содержащие по крайней мере одну последовательность связей переходный металл-кислород-органический радикал на атом переходного металла. Органические радикалы соответствуют описанным выше для органических кислородсодержащих соединений магния.
Переходный металл выбирают преимущественно из титана, циркония, гафния и ванадия. Хорошо подходят титан и цирконий. Предпочтителен титан. Если переходный металл является титаном, цирконием или гафнием, предпочтительно, используют соединения переходного металла в четырехвалентном состоянии, т.к. они чаще всего находятся в жидком виде и в любом случае, как правило, лучше растворимы, чем те, где валентность переходного металла ниже 4.
Используемые органические кислородсодержащие соединения переходного металла могут также содержать связи переходный металл-кислород-переходный металл.
Органические кислородсодержащие соединения переходного металла могут быть представлены общей формулой MOx(OR')m-2x, где М - переходный металл с валентностью m, R' - органический радикал, такой как определено выше, а 0 ≤ x ≤ (m-1)/2. Предпочтительно используют соединения, где 0 ≤ x ≤ (m-2)/2.
Само собой разумеется, что органические кислородсодержащие соединения переходного металла могут содержать несколько различных органических радикалов.
Среди органических кислородсодержащих соединений переходного металла можно привести алкоксиды (такие как Ti(O-nC4H9)4), феноксиды (такие как Zr(OC6H5)4), оксиалкоксиды (такие как HO(OC2H5)2), конденсированные алкоксиды (такие как Ti2O(O-i-C3H7)6), карбоксилаты (такие как Zr(OOCCH3)4) и энолаты (такие как ацетилацетонат гафния).
Под галогенсодержащим соединением переходного металла подразумевают все соединения, содержащие по крайней мере одну связь переходной металл-галоген. Галоген соответствует галогенам, определенным выше для галогенсодержащих соединений магния. Предпочтителен хлор.
Из галогенсодержащих соединений переходного металла можно привести галогениды, в частности тетрагалогениды (такие как TiCl4), комплексные галогениды (такие как ZnCl4•6NH3), сложные галогениды переходного металла и щелочного металла (такие как Na2TiCl6), оксигалогениды (такие как HOCl2) и галогеналкоксиды (такие как Ti(OC2H5)2Cl2 или Zn(OiC3H7)Cl).
Само собой разумеется, что можно использовать одновременно несколько соединений переходного металла. Если желательно получить полиолефин с широким молекулярно-весовым распределением, могут быть предпочтительно использованы соединения различных переходных металлов, в частности соединение титана и соединение циркония.
Из всех подходящих соединений переходного металла предпочтительно используются те, которые содержат на атом переходного металла только связи переходный металл-кислород-органический радикал и/или связи переходный металл-галоген, кроме любой другой связи. Лучшие результаты получены при использовании органических кислородсодержащих соединений переходного металла, в частности тех, которые содержат только на атом переходного металла связи переходный металл-кислород-органический радикал. Наиболее приемлемы алкоксиды. Лучшие результаты были получены при использовании тетраалкоксидов титана или циркония, в частности тетрабутилат титана или циркония.
Получение твердого каталитического комплекса включает в себя последующий этап, так называемый этап осаждения, который предназначен для сокращения валентности переходного металла и, при необходимости, одновременной галогенизации соединения магния и/или соединения переходного металла, т.е. замещения галогенами алкокси-групп соединения магния и/или соединения переходного металла таким образом, чтобы полученный в результате первого этапа жидкий комплекс был осажден в твердый каталитический комплекс. Восстановление и, при необходимости, галогенизация осуществляются одновременно с помощью галогенсодержащего алюминийорганического соединения, действующего как восстановитель и галогенизирующее вещество, вызывающее выпадение в осадок твердого каталитического комплекса.
Обработка с помощью галогенсодержащего алюминийорганического соединения на этапе осаждения твердого каталитического комплекса может осуществляться любым известным адекватным способом и предпочтительно постепенным введением галогенсодержащего алюминийорганического соединения в жидкий комплекс, полученный в результате первого этапа, указанного выше.
Используемое количество галогенсодержащего алюминийорганического соединения зависит от используемых количеств соединения магния и соединения переходного металла и является достаточным для достижения желаемой степени восстановления и, при необходимости, желаемой степени галогенизации. Практически не представляет интереса использование количеств, больше максимально необходимых для завершения восстановления, и, при необходимости, галогенизации, т.к. избыточное количество приводит к повышению содержания алюминия в твердом каталитическом комплексе, что нежелательно. Как правило, это количество составляет по крайней мере 0,5 моля алюминия на используемый моль переходного металла, предпочтительно по крайней мере 1 моль; причем, как правило, используются по крайней мере 2 моля; обычно оно составляет самое большее 50 молей алюминия на моль переходного металла, в частности, самое большее, 30 молей, причем предпочтительны значения самое большее 20 молей.
Температура, при которой осуществляется этап осаждения жидкого комплекса, преимущественно ниже температуры кипения при обычном давлении галогенсодержащего алюминийорганического соединения. Обычно она составляет по крайней мере -20oC, в частности, по крайней мере 0oC, причем рекомендуются температуры по крайней мере 20oC. Как правило, температура не превышает 150oC, в частности, не превышает 100oC, причем обычно эти температуры составляют самое большее 80oC.
Продолжительность этапа осаждения жидкого комплекса предпочтительно достаточна для завершения осаждения. Она может варьироваться от 1 минуты до 10 часов, точнее от 10 минут до 8 часов, например от 0,5 часа до 5 часов.
Давление, при котором осуществляется этап осаждения жидкого комплекса, не является критическим. Для удобства, как правило, работают при атмосферном давлении. Скорость введения реактивов выбирают, как правило, таким образом, чтобы не вызвать резкого нагрева реакционной среды из-за возможного самоускорения реакции. Реакционную среду перемешивают, как правило, таким образом, чтобы обеспечить ее однородность в течение всей реакции. Реакция может осуществляться как в непрерывном, так и периодическом режиме.
Галогенсодержащее алюминийорганическое соединение отвечает предпочтительно формуле AlRnX3-n, где R - радикал углеводорода, содержащий до 20 атомов углерода и, предпочтительно, до 6 атомов углерода. Хорошие результаты получают, если R - алкил (линейный или разветвленный), циклоалкил, арилалкил, арил и алкиларил. Лучшие результаты получены, если R является линейным или разветвленным алкилом. X выбирают, как правило, из фтора, хлора, брома или йода. Особенно подходит хлор; n не превышает, предпочтительно, 1,5, в частности 1. В качестве примера галогенсодержащего алюминийорганического соединения, используемого по изобретению, можно привести трихлорид алюминия (AlCl3), дихлорид этилалюминия [Al(C2H5)Cl2], полуторный хлорид этилалюминия [Al2(C2H5)Cl3] и хлорид диэтилалюминия [Al(C2H5)2Cl]. Предпочтителен дихлорид этилалюминия или дихлорид изобутилалюминия.
Продуктом этапа осаждения жидкого комплекса с помощью галогенсодержащего алюминийорганического соединения является твердый каталитический комплекс, состоящий из гомогенного осадка (причем компоненты осаждаются одновременно из жидкого комплекса) смеси галогенида магния, галогенида переходного металла и, в случае необходимости, частично восстановленных и/или частично галогенированных соединений, а также, в случае необходимости, донора электронов. Речь идет о химически связанных комплексах, продуктах химических реакций, а не результате смешивания или адсорбции. Действительно, невозможно выделить тот или другой компонент этих комплексов, используя чисто физические методы разделения.
После этапа осаждения жидкого комплекса может, предпочтительно, следовать выдержка для созревания, целью которой является продолжение реакции осаждения и получение твердого каталитического комплекса, имеющего улучшенную прочность на растрескивание, неконтролируемую при полимеризации. Созревание осуществляют при температуре, как правило, эквивалентной или превышающей температуру, при которой осуществляется осаждение. Время его проведения не является критическим и, как правило, составляет от 5 минут до 12 часов, предпочтительно по крайней мере 0,5 часа.
После этапа осаждения жидкого комплекса может также следовать, предпочтительно после возможного этапа созревания, этап промывки для удаления избытка реагентов и возможных побочных продуктов, образующихся в процессе получения, которыми может быть пропитан твердый каталитический комплекс. Для промывки может быть использован любой инертный разбавитель и, например, алканы и циклоалканы, содержащие до 20 атомов углерода. Хорошо подходят гексан и изобутан. После промывки твердый каталитический комплекс может быть высушен, например, обдуванием потоком инертного газа, такого как азот, предпочтительно сухой.
Металлоорганическое соединение, которое служит активатором твердого каталитического комплекса и обычно называется "сокатализатором", может быть выбрано из металлоорганических соединений лития, магния, цинка, алюминия или олова. Лучшие результаты были получены при использовании алюминийорганических соединений.
В качестве металлоорганических соединений можно использовать полностью алкилированные соединения, в которых прямые или разветвленные алкильные цепи содержат до 20 атомов углерода, такие как, например, н-бутиллитий, диэтилмагний, диэтилцинк, тетраэтилолово, тетрабутилолово и триалкилалюминий. Можно также использовать гидриды алкилов металлов, в которых алкильные радикалы также содержат до 20 атомов углерода, такие как гидрид диизобутилалюминия и гидрид триметилолова. Подходят также и алкилгалогениды металлов, где алкильные радикалы содержат до 20 атомов углерода, такие как полуторный хлорид этилалюминия, хлорид диэтилалюминия и хлорид диизобутилалюминия. Можно также использовать алюминийорганические соединения, полученные путем реакции триалкилалюминиев или гидридов диалкилалюминия, радикалы которых содержат до 20 атомов углерода, и диолефинов, содержащих от 4 до 20 атомов углерода, в частности, соединения, так называемые изопренилалюминии.
Как правило, предпочтение отдается триалкилалюминиям и особенно тем, чьи алкильные цепи прямые и содержат до 18 атомов углерода, в частности, от 2 до 8 атомов углерода. Предпочтительны триэтилалюминий и триизобутилалюминий.
Общее количество органометаллического соединения, используемое в способе полимеризации по изобретению, может варьироваться в широком диапазоне. Оно, как правило, составляет от 0,02 до 50 ммолей на литр растворителя, разбавителя или объема реактора, и предпочтительно от 0,02 до 2,5 ммоля на литр.
Количество твердого каталитического комплекса, используемое в способе полимеризации по изобретению, определяется в зависимости от содержания переходного металла в этом комплексе. Как правило, оно выбирается таким образом, чтобы концентрация составляла от 0,001 до 2,5, и предпочтительно от 0,01 до 0,25 ммоля переходного металла на литр растворителя, разбавителя или объема реактора.
Молярное соотношение общего количества металла в металлоорганическом соединении и общего количества переходного металла в соединении переходного металла обычно составляет по крайней мере 1, в частности по крайней мере 5, причем наиболее интересны значения по крайней мере 10. Как правило, это соотношение составляет самое большее 100, предпочтительно самое большее 75, причем рекомендуются значения самое большее 50.
Способ полимеризации по изобретению может осуществляться любым известным методом в растворе в растворителе, которым может быть олефин даже в жидком состоянии, или в суспензии в углеводородном разбавителе, или же в газовой фазе. Хорошие результаты получают при полимеризации в суспензии. При осуществлении способа изобретения по третьему варианту, полимеризация проводится, преимущественно, в газовой фазе.
Полимеризация осуществляется при контакте олефина с каталитической системой, содержащей твердый каталитический комплекс, металлоорганическое соединение и донор электронов.
Полимеризующийся олефин может быть выбран из олефинов, содержащих от 2 до 20 атомов углерода, и предпочтительно, от 2 до 6 атомов углерода, таких как этилен, пропилен, 1-бутилен, 4-метилпентен-1 и 1-гексилен. Хорошо подходят этилен, 1-бутилен и 1-гексилен. Предпочтителен этилен. Можно, разумеется, использовать одновременно несколько различных олефинов для получения сополимеров, например смесей двух упомянутые выше олефинов или одного или нескольких этих олефинов с одним или несколькими диолефинами, содержащими от 4 до 20 атомами углерода, предпочтительно. Этими диолефинами могут быть неконъюгированные алифатические диолефины, такие как 1,4-гексадиен, моноциклические диолефины, такие как 4-винилциклогексилен, 1,3-дивинилциклогексан, циклопентадиен или 1,5-циклооктадиен, алициклические диолефины, имеющие эндоциклический мостик, такие как дициклопентадиен или норборнадиен, и конъюгированные алифатические диолефины, такие как бутадиен и изопрен.
Способ изобретения применяется с особенным успехом для получения гомополимеров этилена и сополимеров, содержащих по крайней мере 90% молярных этилена, предпочтительно 95% молярных этилена.
Полимеризация в суспензии осуществляется, как правило, в углеводородном растворителе, таком как алифатические, циклоалифатические и ароматические жидкие углеводороды при температуре, при которой растворялось бы по крайней мере 80% (предпочтительно по крайней мере 90%) образованного полимера. Предпочтительными разбавителями являются линейные алканы, такие как н-бутан, н-гексан и н-гептан, или разветвленные алканы, такие как изобутан, изопентан, изооктан и 2,2-диметилпропан, или циклоалканы, такие как циклопентан и циклогексан, или их смеси. Лучшие результаты получают при использовании гексана и изобутана. Температуру полимеризации выбирают, как правило, между 20 и 200oC, предпочтительно между 50 и 150oC, в частности между 65 и 115oC. Парциальное давление олефина выбирают, как правило, между атмосферным давлением и 5 МПа, предпочтительно, между 0,2 до 2 МПа, в частности между 0,4 и 1,5 МПа.
Полимеризация в газовой фазе происходит в результате контакта газового потока, содержащего по крайней мере один олефин, с каталитической системой, например в псевдоожиженном слое. Для этого расход газового потока должен быть достаточным для поддержания полиолефина в псевдоожиженном состоянии и зависит от скорости образования последнего и скорости потребления каталитической системы. Общее парциальное давление олефина(ов) может быть ниже или выше атмосферного давления, причем предпочтительно парциальное давление варьируется до, приблизительно, 7 МПа. Как правило, подходит давление от 0,2 до 5 МПа. Выбранная температура не является критической, как правило, она составляет от 30 до 200oC. При необходимости можно использовать газ-разбавитель, который должен быть инертен по отношению к полиолефину.
Способ полимеризации по изобретению может, при необходимости, осуществляться в присутствии регулятора молекулярной массы, такого как водород.
Способ полимеризации по изобретению может осуществляться в непрерывном или периодическом режиме только в одном реакторе или в нескольких, расположенных последовательно реакторах, причем условия полимеризации (температура, вероятное содержание сомономера, возможное содержание водорода, тип полимеризационной среды) в одном реакторе отличаются от условий полимеризации в других реакторах.
Способ полимеризации по изобретению позволяет получать полиолефины, имеющие, в частности, низкое содержание олигомеров, что делает их пригодными для последующей переработки без образования дыма при формовании деталей с великолепными механическими свойствами.
Приведенные ниже примеры иллюстрируют изобретение. Ниже объясняются значения символов в тексте этих примеров, единиц приведенных величин и методы измерения этих величин.
MI2 - показатель текучести полиолефина, определяющий расход полиолефина, расплавленного при 190oC, который продавливают через фильеру диаметром 2 мм и длиной 8 мм с помощью уравновешенного поршня массой 2,16 кг, причем этот расход выражается в г/10 мин по стандарту ASTM D 1238 (1990).
μ - динамическая вязкость полиолефина, выраженная в дПа•с и измеряемая по градиенту (перепаду) скорости 100 с при 190oC.
α - активность твердого каталитического комплекса, выраженная в кг полученного нерастворимого полиолефина на час и грамм используемого титана и на МПа давления олефина.
СП - стандартная плотность полиолефина, выраженная в кг/м3 и измеренная по стандарту ISO 1183 (1987).
СО - содержание олигомера в полиолефине, выраженное в граммах олигомера на кг полиолефина и измеренная путем экстрагирования в кипящем гексане.
Tинд. - индуктивный период твердого каталитического комплекса, выраженный в минутах и определенный как время от момента введения олефина до момента понижения давления, характерного для начала полимеризации.
Во всех примерах получали твердые каталитические комплексы, которые затем использовались для полимеризации этилена. Примеры 1, 3 и 5 иллюстрируют первый вариант осуществления изобретения; примеры 2, 4 и 6 даны для сравнения. Примеры 7 и 9 иллюстрируют второй вариант осуществления изобретения; примеры 8 и 10 даны для сравнения. Примеры 11 и 13 иллюстрируют третий вариант осуществления изобретения; пример 12 дан для сравнения.
Пример 1 (соответствует изобретению)
В этом примере проводят полимеризацию этилена в присутствии сокатализатора и твердого каталитического комплекса, полученного с использованием донора электронов после первого этапа формирования жидкого комплекса и до последующего этапа осаждения этого жидкого комплекса в соответствии с первым вариантом осуществления изобретения, описанным выше.
А. Получение твердого каталитического комплекса
A.1. Образование жидкого комплекса
В течение 5 часов при 110oC проводят реакцию диэтилата магния, приготовленного in situ путем реакции металлического магния с этанолом, с тетрабутилатом титана в таких количествах, что молярное соотношение титана и магния равняется 2.
А.2. Обработка донором электронов
В жидкий комплекс, полученный на этапе A.1. и разбавленный в гексане, вводят, перемешивая, этилбензоат в таком количестве, что молярное соотношение этилбензоата и титана равняется 1. Полученная таким образом смесь выдерживается при 35oC при перемешивании в течение 0,5 часа.
А.3. Осаждение
Полученные на этапе А.2. обработанный комплекс осаждают путем смешивания его с раствором дихлорида изобутилалюминия в гексане (в таком количестве, что молярное соотношение алюминия и титана равно 6) при перемешивании в течение 2 часов при 45oC. Полученную таким образом смесь подвергают созреванию в течение 45 минут при 60oC. Затем собирают твердый каталитический комплекс, который промывают в гексане. Полученный твердый каталитический комплекс содержит (в вес.%): Ti - 11,8, Cl - 46,3, Al - 1,6, Mg - 6,0.
Остаток состоит из элементов, входящих в состав продуктов, используемых для образования твердого каталитического комплекса, таких как углерод, водород и кислород.
Б. Полимеризация этилена
В автоклав на 3 литра, оснащенный мешалкой, вводят 1 л гексана и 2 ммоля триэтилалюминия (сокатализатор). Затем повышают температуру до 85oC и поддерживают ее постоянной в течение всей полимеризации. Затем вводят единичную дозу водорода при давлении 0,4 МПа и этилен. Затем впрыскивают 2,6 мг твердого каталитического комплекса, полученного на этапе А. Парциальное давление этилена поддерживается постоянным при 0,6 МПа в течение 2 часов. Автоклав затем дегазируют и охлаждают. Каталитический комплекс имеет активность α 198. В автоклаве собирают 74 г полиэтилена, имеющего следующие свойства:
MI2 = 5,7
СП = 965,8
СО = 6,3
μ = 6700
Пример 2 (для сравнения)
В примере осуществляют полимеризацию этилена при рабочих условиях примера 1Б (в частности, в присутствии количества водорода, используемого для примера 1Б) с введением твердого каталитического комплекса, полученного без донора электронов.
А. Получение твердого каталитического комплекса
Были повторены операции примера 1А за исключением этапа А2, который пропускают. Полученный твердый каталитический комплекс содержит (в вес.%): Ti - 19,5, Cl - 63,2, Al - 2,8, Mg - 5,4.
Остаток состоит из элементов, входящих в состав продуктов, используемых для образования твердого каталитического комплекса, таких как углерод, водород и кислород.
Б. Полимеризация этилена
Были повторены операции примера 1Б с вдуванием 4,4 мг твердого каталитического комплекса. Каталитический комплекс имеет активность α 75. В автоклаве собирают 75 г полиэтилена, имеющего следующие характеристики:
MI2 = 1,4
СП = 963,7
СО = 11,0
μ = 13900.
Сравнение результатов примера 2 (MI2 = 1,4, что соответствует большим молекулярным массам полиэтилена) с результатами примера 1 (MI2 = 5,7, что соответствует малым молекулярным массам полиэтилена) выявило преимущества применения изобретения в отношении влияния на твердый каталитический комплекс водорода и показало, в частности, что твердый каталитический комплекс примера 2 менее чувствителен к водороду, чем твердый каталитический комплекс примера 1.
Пример 3 (соответствует изобретению)
В этом примере использован твердый каталитический комплекс примера 1, полученный по первому варианту осуществления изобретения, описанному выше, для получения сополимера этилена и бутилена.
А. Получение твердого каталитического комплекса
Были повторены операции примера 1А.
Б. Сополимеризация этилена
Проводят сополимеризацию этилена с бутиленом в непрерывном режиме в кольцевом реакторе, в который непрерывно вводят гексан, этилен (в таком количестве, что концентрация этилена в гексане равна 13 г/л), водород (в таком количестве, что молярное соотношение водород/этилен равно 0,076), бутилен (в таком количестве, что молярное соотношение бутилен/этилен равно 0,057), триэтилалюминий (в таком количестве, что концентрация алюминия в гексане равна 25 ppm) и твердый каталитический комплекс, полученный в примере 1А. Температура в реакторе составляет 80oC. Непрерывный процесс характеризуется временем выдержки 3 часа и выходом 30 кг/ч. Полученный полиэтилен имеет следующие свойства:
MI2 = 1,9
СП = 952,3
СО = 2,5
μ = 13800.
Пример 4 (для сравнения)
В этом примере получают сополимер этилена и бутилена, имеющий MI2 и СП сополимера примера 3 (с использованием концентрации водорода и бутилена в способе по примеру 3Б) в присутствии твердого каталитического комплекса без донора электронов.
А. Получение твердого каталитического комплекса
Повторяют операции, примера 1А за исключением этапа А2, который пропускают. Полученный твердый каталитический комплекс содержит (в вес.%): Ti - 19,5, Cl - 63,2, Al - 2,8, Mg - 5,4.
Остаток состоит из элементов, входящих в состав продуктов, используемых для образования твердого каталитического комплекса, таких как углерод, водород и кислород.
Б. Сополимеризация этилена
Были повторены операции примера 3Б с использованием катализатора, полученного на этапе А при следующих операционных условиях:
молярное соотношение водород/этилен = 0,094
молярное соотношение бутилен/этилен = 0,051
Полученный полиэтилен имел следующие свойства:
MI2 = 1,8
СП = 953,7
СО = 4,5
μ = 13700.
Сравнение результатов примера 4 с результатами примера 3 выявило преимущества применения изобретения в части содержания олигомеров в полученных полиолефинах и показало, в частности, что использование твердого каталитического комплекса примера 4 для получения полиэтилена с заданными MI2 и СП приводит к более высокому содержанию олигомеров.
Пример 5 (соответствует изобретению)
В этом примере получают твердый каталитический комплекс, используя донор электронов после первого этапа образования жидкого комплекса и до последующего этапа осаждения, по описанному выше первому варианту осуществления изобретения. Затем определяют гранулометрию твердого каталитического комплекса.
А. Получение твердого каталитического комплекса
А.1. Образование жидкого комплекса
В течение 5 часов при 110oC проводят реакцию диэтилата магния, который получают путем реакции in situ металлического магния и этанола, с тетрабутилатом титана, взятых в таком количестве, что молярное соотношение титана и магния равняется 2.
А. 2. Обработка донором электронов
В жидкий комплекс, полученный на этапе A.I и разбавленный в гексане, вводят перемешивая этилбензоат в таком количестве, что молярное соотношение этилбензоата и титана равняется 1. Полученная таким образом смесь выдерживается при 35oC при перемешивании в течение 0,5 часа.
А.3. Осаждение
Полученный на этапе А. 2 комплекс осаждают путем смешения его с раствором дихлорида изобутилалюминия (в таком количестве, что молярное соотношение алюминия и титана равно 3,75) при перемешивании в течение 1,5 часов при 45oC. Полученную таким образом смесь подвергают созреванию в течение 45 минут при 60oC. Затем собирают твердый каталитический комплекс, который промывают в гексане. Полученный твердый каталитический комплекс содержит (в вec.%): Ti - 14,3, Cl - 32,4, Al - 0,4, Mg - 3,5.
Остаток состоит из элементов, входящих в состав продуктов, используемых для образования твердого каталитического комплекса, таких как углерод, водород и кислород.
Б. Гранулометрия
Гранулометрия полученного твердого каталитического комплекса характеризуется средним диаметром (<d>) 19 мкм и широтой гранулометрического распределения 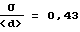 (имеет типичное отклонение).
(имеет типичное отклонение).
Пример 6 (для сравнения)
В этом примере твердый каталитический комплекс получают без донора электронов, с последующим анализом гранулометрии.
А. Получение твердого каталитического комплекса
Повторяют операции примера 5А за исключением этапа А. 2, который пропускают. Полученный твердый каталитической комплекс содержит (в вес.%): Ti - 17,7, Cl - 38,6, Al - 2,1, Mg - 4,4, и имеет гранулометрию, определенную средним диаметром (<d>) 14 мкм и широтой гранулометрического распределения 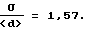
Сравнение результатов примера 6 с результатами примера 5 выявило преимущества изобретения в части ширины гранулометрического распределения твердого каталитического комплекса.
Пример 7 (соответствует изобретению)
В этом примере полимеризацию этилена проводят с использованием каталитической системы, содержащей твердый каталитический комплекс, приготовленный с использованием доноров электронов после этапа осаждения жидкого комплекса и до его введения в полимеризационную среду, в соответствии с описанным выше вторым вариантом осуществления изобретения.
А. Получение твердого каталитического комплекса
А.1. Образование жидкого комплекса
В течение 5 часов при 110oC проводят реакцию диэтилата магния, приготовленного путем реакции in situ металлического магния и этанола, с тетрабутилатом титана, взятых в таких количествах, что молярное соотношение титана и магния равняется 2.
А.2. Осаждение
Полученный на этапе А. 2 жидкий комплекс осаждают путем соединения его с раствором дихлорида изобутилалюминия (в таком количестве, что молярное соотношение алюминия и титана равно 6) при перемешивании в течение 2 часов при 45oC. Полученную таким образом смесь подвергают созреванию в течение 45 минут при 60oC. Затем собирают твердый каталитический комплекс, который промывают в гексане.
А.3. Обработка донором электронов
В суспензию в гексане полученного на этапе А.2 твердого каталитического комплекса вводят, помешивая, этилбензоат в таком количестве, что молярное соотношение этилбензоата и титана равно 10. Полученная таким образом смесь выдерживается при 30oC при перемешивании в течение 1 часа. Обработанное таким образом твердое вещество промывают в гексане. Полученный твердый каталитический комплекс содержит (в вес.%): Ti - 16,6, Cl - 59,1, Al - 2,5, Mg - 4,8.
Остаток состоит из элементов, входящих в состав продуктов, используемых для образования твердого каталитического комплекса, таких как углерод, водород и кислород.
Б. Полимеризация этилена
В автоклав на 3 литра, оснащенный мешалкой, вводят 1 л гексана и 2 ммоля триэтилалюминия. Затем повышают температуру до 85oC и поддерживают ее постоянной в течение всей полимеризации. Затем вводят единичную дозу водорода при давлении 0,4 МПа и этилен. Затем впрыскивают 10,2 мг твердого каталитического комплекса, полученного на этапе А. Парциальное давление этилена поддерживается постоянным при 0,6 МПа в течение 2 часов. Автоклав затем дегазируют и охлаждают. Каталитический комплекс имеет активность 69. В автоклаве собирают 145 г полиэтилена, имеющего следующие характеристики:
MI2 = 2,7
СП = 964,1
СО = 11,9
Пример 8 (для сравнения)
В этом примере полиэтилен, имеющий MI2 и СП полиэтилена примера 7, получают при использовании твердого каталитического комплекса без донора электронов.
А. Получение твердого каталитического комплекса
Повторены операции примера 7А за исключением этапа А.3, который пропускают. Полученный твердый каталитический комплекс содержит (в вес.%): Ti - 17,0, Cl - 61,2, Al - 2,7, Mg - 4,6.
Остаток состоит из элементов, входящих в состав продуктов, используемых для образования твердого каталитического комплекса, таких как углерод, водород и кислород.
Б. Полимеризация этилена
Были повторены операции примера 7Б с впрыскиванием 7,9 мг твердого каталитического комплекса. Каталитический комплекс имеет активность α 79. В автоклаве собирают 128 г полиэтилена, который имеет следующие свойства:
MI2 = 2,9
СП = 964,2
СО = 18,2
Сравнение результатов примера 8 с результатами примера 7 выявило преимущества применения изобретения в части содержания олигомеров в полученных полиолефинах и показало, в частности, что использование твердого каталитического комплекса примера 8 для получения полиэтилена с заданными MI2 и СП приводит к более высокому содержанию олигомеров.
Пример 9 (соответствует изобретению)
В этом примере осуществляют полимеризацию этилена с использованием твердого каталитического комплекса, содержащего два различных переходных металла и полученного в соответствии с описанным выше вторым вариантом осуществления изобретения.
А. Получение твердого каталитического комплекса
А.1. Образование жидкого комплекса
В течение 7 часов при 140oC проводят реакцию диэтилата магния с тетрабутилатом титана и тетрабутилатом циркония, взятых в таких количествах, что молярное соотношение титана и магния равно 0,6, а молярное соотношение циркония и титана равно 2.
А.2. Осаждение
Полученный на этапе А.I жидкий комплекс осаждают путем соединения его с раствором дихлорида изобутилалюминия (в таком количестве, что молярное соотношение алюминия и общего количества титана и циркония равно 7,8) при перемешивании в течение 120 минут при 45oC. Полученную таким образом смесь подвергают созреванию в течение 90 минут при 60oC. Затем собирают твердый каталитический комплекс, который промывают в гексане.
А.3. Обработка донором электронов
В суспензию в гексане полученного на этапе А.2 твердого каталитического комплекса вводят при перемешивании этилбензоат в таком количестве, что молярное соотношение этилбензоата и общего количества титана и циркония равно 4,2. Полученная таким образом смесь выдерживается при 35oC при перемешивании в течение 1 часа. Обработанное таким образом твердое вещество промывают в гексане. Полученный твердый каталитический комплекс содержит (в вec.%): Ti - 3, Zr - 8,1, Cl - 25,5, Al -0,5, Mg - 2,5.
Остаток состоит из элементов, входящих в состав продуктов, используемых для образования твердого каталитического комплекса, таких как углерод, водород и кислород.
Б. Полимеризация этилена
В автоклав на 3 литра, оснащенный мешалкой, вводят 1 л гексана и 2 ммоля триизобутилалюминия. Затем повышают температуру до 85oC и поддерживают ее постоянной в течение всей полимеризации. Затем вводят порцию водорода при давлении 0,9 МПа и этилен. Затем впрыскивают 45 мг твердого каталитического комплекса, полученного на этапе А. Парциальное давление этилена поддерживается постоянным при 0,6 МПа в течение 2 часов. Автоклав затем дегазируют и охлаждают. Каталитический комплекс имеет активность α 144. В автоклаве собирают 234 г полиэтилена, имеющего следующие характеристики:
MI2 = 22
СП = 967,4
СО = 32.
Пример 10 (для сравнения)
В этом примере осуществляют полимеризацию этилена при рабочих условиях примера 9.Б с введением твердого каталитического комплекса, содержащего два различных переходных металла и полученного без донора электронов.
А. Получение твердого каталитического комплекса
Повторяют операции примера 9.А за исключением этапа А.3, который пропускают. Полученный твердый каталитический комплекс содержит (в вес.%): Ti - 5,3, Zr - 8,1, Cl - 51,3, Al - 1,7, Mg - 4,1.
Остаток состоит из элементов, входящих в состав продуктов, используемых для образования твердого каталитического комплекса, таких как углерод, водород и кислород.
Б. Полимеризация этилена
Повторяют операции примера 9.Б с вдуванием 51 мг твердого каталитического комплекса. Каталитический комплекс имеет активность 113. В автоклаве собирают 365 мг полиэтилена, имеющего следующие свойства:
MI2 = 0,1
СП = 960,2
СО = 33.
Сравнение результатов примера 10 (MI2 = 0,1, что соответствует большим молекулярным массам полиэтилена) с результатами примера 9 (MI2 = 22, что соответствует малым молекулярным массам полиэтилена) выявило преимущества изобретения в части реакции твердых каталитических комплексов на водород и показало, в частности, что твердый каталитический комплекс примера 10 заметно менее чувствителен к водороду, чем твердый каталитический комплекс примера 9.
Пример 11 (соответствует изобретению)
В этом примере осуществляют полимеризацию этилена в присутствии твердого каталитического комплекса без донора электронов и смеси донора электронов с металлоорганическим соединением, в соответствии с наиболее интересным вариантом осуществления изобретения по описанному выше третьему варианту.
А. Получение твердого комплекса
А.1. Образование жидкого комплекса
В течение 5 часов при 110oC проводят реакцию диэтилата магния, приготовленного путем взаимодействия in situ металлического магния и этанола, с тетрабутилатом титана в таких количествах, что молярное соотношение титана и магния равняется 2.
А.2. Осаждение
Полученный на этапе А.1 жидкий комплекс осаждают путем смешения его с раствором дихлорида изобутилалюминия (в таком количестве, что молярное соотношение алюминия и титана равно 6) при перемешивании в течение 2 часов при 45oC. Полученную таким образом смесь выдерживают в течение 45 минут при 60oC. Затем собирают твердый каталитический комплекс, который промывают несколько раз в гексане. Полученный твердый каталитический комплекс содержит (в вес.%): Ti - 19,5, Cl - 63,2, Al - 2,8, Mg - 5,4.
Остаток состоит из элементов, входящих в состав продуктов, используемых для образования твердого каталитического комплекса, таких как углерод, водород и кислород.
Б. Смесь донора электронов и металлоорганического соединения
При комнатной температуре в течение нескольких минут смешивают раствор триэтилалюминия в гексане и этилбензоат в молярном соотношении бензоат/триэтилалюминий 0,25.
C. Полимеризация этилена
В автоклав на 3 литра, оснащенный мешалкой, вводят 1 л гексана и смесь, полученную на этапе Б, содержащую 2 ммоля триэтилалюминия. Затем повышают температуру до 85oC и поддерживают ее постоянной в течение всей полимеризации. Затем вводят единичную дозу водорода при давлении 0,4 МПа и этилена. Затем впрыскивают 7,1 мг твердого каталитического комплекса, полученного на этапе А. Парциальное давление этилена поддерживается постоянным при 0,6 МПа в течение 2 часов. Автоклав затем дегазируют и охлаждают. Каталитический комплекс имеет активность α 124. В автоклаве собирают 208 г полиэтилена, имеющего следующие свойства:
MI2 = 3,4
СП = 962,8
СО = 16,9
μ = 8500.
Пример 12 (для сравнения)
В этом примере осуществляют полимеризацию этилена в условиях примера 11Б в присутствии твердого каталитического комплекса и сокатализатора и в отсутствии донора электронов.
А. Получение твердого каталитического комплекса
Повторяют операции примера 11А.
Б. Полимеризация этилена
Повторяют операции примера 11C с введением 2 ммолей триэтилалюминия в автоклав вместо смеси бензоат-триэтилалюминий и в присутствии 6,0 мг твердого каталитического комплекса.
Каталитический комплекс имеет активность α 64 и индуктивный период 0 минут. В автоклаве собирают 90 г полиэтилена, который имеет следующие свойства:
MI2 = 1,9
СП = 964,1
СО = 18,9
μ = 11500
Сравнение результатов примера 12 с результатами примера 11 выявило преимущества изобретения в части каталитической активности твердых каталитических комплексов.
Пример 13 (соответствует изобретению)
В этом примере осуществляют полимеризацию этилена в присутствии твердого каталитического комплекса без донора электронов и смеси донора электронов с металлоорганическим соединением в соответствии с наиболее интересной формой осуществления изобретения по описанному выше третьему варианту.
А. Получение твердого комплекса
Повторяют операции примера 11.А.
Б. Смесь донора электронов и металлоорганического соединения
При комнатной температуре в течение нескольких минут смешивают раствор триэтилалюминия в гексане и этилбензоат в молярном соотношении бензоат/триэтилалюминий 0,294.
C. Полимеризация этилена
В автоклав на 3 литра, оснащенный мешалкой, вводят 1 л гексана и смесь, полученную на этапе Б, содержащую 2 ммоля триэтилалюминия. Затем повышают температуру до 85oC и поддерживают ее постоянной в течение всей полимеризации. Затем вводят порцию водорода при давлении 0,4 МПа и этилен. Затем впрыскивают 4,9 мг твердого каталитического комплекса, полученного на этапе А. Парциальное давление этилена поддерживается постоянным при 0,6 МПа в течение 4 часов. Автоклав затем дегазируют и охлаждают. Каталитический комплекс имеет активность α 23 и индуктивный период Tинд - 120 минут. В автоклаве собирают 76 г полиэтилена, имеющего следующие свойства:
MI2 = 0,95
СП = 961,6
СО = 1,2
μ = 15900.
Сравнение результатов примера 13 и результатов примера 12 выявило изменение индуктивного периода твердого каталитического комплекса в результате применения изобретения.
Пример 14 (соответствует изобретению)
В этом примере полимеризацию этилена проводят в присутствии сокатализатора и твердого каталитического комплекса, полученного с использованием донора электронов после первого этапа образования жидкого комплекса и перед последующим этапом осаждения этого жидкого комплекса в соответствии с описанным выше первым вариантом осуществления изобретения.
А. Получение твердого каталитического комплекса
А.1. Образование жидкого комплекса
В течение 5 часов при 110oC проводят реакцию диэтилата магния, приготовленного путем реакции in situ металлического магния и этанола, с тетрабутилатом титана, взятых в количествах таких, что молярное соотношение титана к магнию равняется 1.
А.2. Обработка донором электронов
В жидкий комплекс, полученный на этапе А.1 и разбавленный гексаном, вводят помешивая этилбензоат в таком количестве, что молярное соотношение этилбензоата и магния в конечном твердом каталитическом комплексе равно 0,1. Полученная таким образом смесь выдерживается при 35oC при перемешивании в течение 0,5 часа.
А.3. Осаждение
Полученный на этапе А.2 комплекс осаждают путем соединения его с раствором дихлорида изобутилалюминия в гексане (в таком количестве, что молярное соотношение алюминия и титана равно 7) при перемешивании в течение 1,5 часов при 45oC. Полученную таким образом смесь выдерживают в течение 45 минут при 60oC. Затем собирают твердый каталитический комплекс, который промывают в гексане. Полученный твердый комплекс содержит (в вес.%): Ti - 12,4, Cl - 53,7, Al - 3,8, Mg - 7,7.
Остаток состоит из элементов, входящих в состав продуктов, используемых для образования твердого каталитического комплекса, таких как углерод, водород и кислород. Гранулометрия твердого каталитического комплекса характеризуется средним диаметром (<d>) 9 мкм.
Б. Полимеризация этилена
В автоклав на 3 литра, оснащенный мешалкой, вводят 1 л гексана и 2 ммоля триэтилалюминия (сокатализатор). Затем повышают температуру до 85oC и поддерживают ее постоянной в течение всей полимеризации. Затем вводят порцию водорода при давлении 0,2 МПа и этилен. Затем впрыскивают 7,8 мг твердого каталитического комплекса, полученного на этапе А. Парциальное давление этилена поддерживается постоянным при 0,6 МПа в течение 2 часов. Автоклав затем дегазируют и охлаждают. В автоклаве собирают 263 г полиэтилена, имеющего следующие характеристики:
MI2 = 0,47
СП = 959,0
нас.уд.вес = 318
μ = 23000.
Пример 15 (для сравнения)
В этом примере осуществляют полимеризацию этилена при рабочих условиях примера 14Б с введением твердого каталитического комплекса, полученного с использованием донора электронов на первом этапе образования жидкого комплекса.
А. Получение твердого каталитического комплекса
А.1. Образование жидкого комплекса
В течение 4 часов при 140oC проводят реакцию диэтилата магния с тетрабутилатом титана, взятых в таком количестве, что молярное соотношение титана и магния равняется 1, и с этилбензоатом, взятым в таком количестве, что молярное соотношение этилбензоата и магния в конечном твердом каталитическом комплексе равно 0,1.
А.2. Осаждение
Полученный на этапе А.1 комплекс осаждают путем смешения его с раствором дихлорида изобутилалюминия в гексане (в таком количестве, что молярное соотношение алюминия и титана равно 7) при перемешивании в течение 1,5 часов при 45oC. Полученную таким образом смесь выдерживают в течение 45 минут при 60oC.
Затем, собирают твердый каталитический комплекс, который промывают в гексане. Полученный твердый каталитический комплекс содержит (в вес.%): Ti - 12,0, Cl - 55,8, Al - 3,4, Mg - 3,8.
Остаток состоит из элементов, входящих в состав продуктов, используемых для образования твердого каталитического комплекса, таких как углерод, водород и кислород. Гранулометрия твердого каталитического комплекса характеризуется средним диаметром (<d>) 38 мкм.
Б. Полимеризация этилена
Повторяют операции примера 14Б за исключением используемого количества твердого каталитического комплекса, которое составляет 4,2 мг. В автоклаве собирают 168 г полиэтилена, имеющего следующие характеристики:
MI2 = 0,57
СП = 959,3
нас.уд.вес = 222
μ = 21400.
Сравнение результатов примера 15 с результатами примера 14 выявило преимущества применения изобретения в части объемного удельного веса полученных полимеров.
Способ применим при полимеризации в присутствии каталитической системы. Согласно предложенному способу вводят в контакт по крайней мере один олефин с каталитической системой, содержащей: а) твердый каталитический комплекс на основе магния, переходного металла и галогена, причем указанный твердый каталитический комплекс получают путем реакции, на первом этапе по крайней мере одного соединения магния, выбранного из органических кислородсодержащих соединений и галогенсодержащих соединений магния с по крайней мере одним соединением переходного металла группы IVВ или VВ Периодической таблицы, выбранным из органических кислородсодержащих соединений и галогенсодержащих соединений переходного металла, с получением жидкого комплекса, и на втором этапе осаждают указанный жидкий комплекс с помощью галогенсодержащего алюминийорганического соединения общей формулы AlR4X3-n, где R - радикал углеводорода, Х - галоген, a n - меньше 3, для образования твердого каталитического комплекса, и б) металлоорганическое соединение металла групп IА, IIА, IIВ, IIА и IVА Периодической таблицы; с) по крайней мере один донор электронов, который применяют после первого этапа получения твердого каталитического комплекса, продуктом которого является жидкий комплекс. Достигается улучшение механических и реологических свойств полиголефинов за счет снижения содержания олигомеров. 15 з.п.ф-лы.
| Орудие для щелевания склонов | 1987 |
|
SU1464909A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИОЛЕФИНОВ | 0 |
|
SU376947A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИОЛЕФИНОВ | 1971 |
|
SU428610A3 |
| Способ получения твердого каталитического компонента и способ получения катализатора для полимеризации пропилена | 1987 |
|
SU1614750A3 |
| ВСЕСОЮЗНАЯ rSiS? y"-"!;.'] Vi'WfVf'r ~f.',". 5 2fAi?.fiifsb~j:.nh;. M-. Ai'ii; | 0 |
|
SU389173A1 |
| US 5326838 A, 05.07.94 | |||
| JP 57165407 A, 12.10.82 | |||
| УГОЛЬНАЯ МАССА ДЛЯ АНОДОВ АЛЮМИНИЕВЫХ ЭЛЕКТРОЛИЗЕРОВ | 0 |
|
SU398698A1 |
| УСТРОЙСТВО ДЛЯ МАГНИТНОЙ ЗАПИСИ | 1972 |
|
SU435557A1 |
| EP 0604401 A2, 29.06.94. | |||
Авторы
Даты
1999-12-27—Публикация
1995-09-21—Подача