Изобретение относится к гидрометаллургической переработке рудных концентратов, а более конкретно к переработке лопаритового концентрата.
Лопаритовый концентрат является сложным комплексным сырьем, содержащим оксиды большого количества химических элементов. Используемый для переработки лопаритовый концентрат марки КЛ-1 с содержанием лопарита в нем не менее 95% в соответствии с действующими техническими условиями содержит, вес.%: оксид тантала (Ta2O5) - 0,57; оксид ниобия (Nb2O5) - 8,14; оксид титана (TiO2) - 38,1; оксиды редкоземельных металлов цериевой группы, в основном оксид лантана (La2O3), оксид церия (Ce2O3), оксид празеодима (Pr2O3), оксид неодима (Nd2O3) - 32; оксид натрия (Na2O) - 7,9-9,06; оксид кальция (CaO) - 4,2-5,7; оксид стронция (SrO) - 2,3-3,0; оксид железа (Fe2O3) - 2,0-2,5; оксид кремния (SiO2) - 1,95-2,5; оксид алюминия (Al2O3) - 0,6-0,7; оксид калия (K2O) - 0,26-0,75; оксид фосфора (P2O5) - 0,15-0,22 и источник альфа-излучения - оксид тория (ThO2) - 0,54.
Из лопаритового концентрата извлекают наиболее ценные оксиды тантала, ниобия, титана, а также менее ценные оксиды редкоземельных металлов. Настоящая заявка касается извлечения оксидов тугоплавких металлов тантала, ниобия и титана.
До настоящего времени были известны и применялись два способа переработки лопаритового концентрата, обеспечивающие получение оксидов тугоплавких металлов, именуемые специалистами хлорной и сернокислотной технологиями.
Получение оксидов тугоплавких металлов путем переработки лопаритового концентрата способом хлорирования является более простым с технологической точки зрения (см. А.Н.Зеликман и др. "Металлургия редких металлов", М., Металлургия, 1991, с.95-100). Его сущность состоит в том, что лопаритовый концентрат предварительно подвергают сухому помолу и шихтовке с коксом. Шихту подвергают воздействию 100% осушенным газообразным хлором при 950-1050oC. Различия в летучести образующихся хлоридов компонентов лопаритового концентрата позволяют разделить его на основные ценные составляющие.
Хлорная технология переработки лопарита обеспечивает извлечение 93-94% ниобия и 86-88% тантала в технические оксиды, 96,5-97% титана в технический тетрахлорид.
Однако, хлорная технология очень опасна и вредна для обслуживающего персонала, а также окружающей среды из-за применяемого в больших количествах хлора, и поэтому на сегодняшний день она совершенно не приемлема для использования с точки зрения экологической безопасности.
Более безопасным и наиболее близким аналогом заявляемого изобретения является способ получения оксидов тугоплавких металлов путем переработки лопаритового концентрата с использованием концентрированной серной кислоты для вскрытия лопарита (см. А.Н.Зеликман и др. "Металлургия редких металлов", М., Металлургия, 1991, с.101, 103-105).
Этот способ основан на разложении лопаритового концентрата серной кислотой и разделении ценных составляющих с использованием различий в растворимости двойных сульфатов титана, ниобия и тантала, редкоземельных элементов с сульфатами щелочных металлов или аммония. Исходный концентрат лопарита измельчают до крупности не менее 0,075 мм и подвергают классификации. Вскрытие концентрата осуществляют с помощью 95% серной кислоты, расходуемой из расчета 2,78 т на 1 т измельченного концентрата. Для предотвращения спекания реагирующей массы и повышения извлечения в раствор ниобия и тантала, к серной кислоте добавляют сульфат аммония (0,2 т на 1 т концентрата). В результате вскрытия, протекающего при температуре, достигающей 270-280oC, ниобий и тантал в присутствии больших количеств титана входят в состав двойных сульфатов титана в виде изоморфной примеси. Редкоземельные элементы входят в состав двойных сульфатов РЗЭ R2(SO4)3•(NH4)2SO4. Продукт сульфатизации - сульфатный спек подвергают водному выщелачиванию. В результате этого в твердой фазе остаются двойные сульфаты РЗЭ, а в жидкой фазе остается сернокислый раствор титана, ниобия и тантала. При этом активность, обусловленная наличием в лопарите источника альфа-излучения тория Th и мезотория MsTh, разделяется между твердой и жидкой фазами по 50%. Извлечение окислов тугоплавких металлов из их сернокислого раствора начинается с отделения титана от ниобия и тантала. Для отделения титана от ниобия и тантала используют осаждение сульфатом аммония малорастворимой титановой соли (NH4)2TiO(SO4)2•H2O. В осадок выделяется 70-80% титана от его содержания в растворе. Двойной сульфат титана используют как эффективный дубитель в кожевенной промышленности. Термическим его разложением получают технический диоксид титана. Остающийся после выделения титановой соли раствор, именуемый сернокислый маточник, содержит тантал, ниобий и остатки титана. Этот раствор подвергают фторированию 40% плавиковой кислотой HF. После этого осуществляют фильтрацию раствора для отделения осадка фторидов с активностью (торий Th и мезоторий MsTh). Затем для извлечения тантала и ниобия осуществляют процесс разделительной экстракции на 100% трибутилфосфате ТБФ. При этом в растворе концентрация фтора F 32-35 г/л, а серной кислоты H2SO4 250-300 г/л. После экстракции трибутилфосфат с танталом и ниобием направляют на поочередную реэкстракцию, т.е. смыв с трибутилфосфата с помощью своих реэкстрагирующих растворов. Полученные регенераты тантала и ниобия обрабатывают аммиаком, в результате чего получают гидроокиси тантала и ниобия Ta(OH)5 и Ni(OH)5. Гидроокиси подвергают последовательной отмывке, сушке и прокалке, в результате чего получают готовый продукт - пятиокиси тантала и ниобия Ta2O5 и Ni2O5. Для обеспечения возможности последующего извлечения редкоземельных металлов осуществляют дополнительный самостоятельный технологический цикл конверсии двойных сульфатов РЗЭ в карбонаты, который не является предметом настоящей заявки и, поэтому, в данной заявке не рассматривается. Оставшийся после извлечения окислов тугоплавких металлов рафинат подвергают переработке для обезвреживания и утилизации. Рафинат содержит серную кислоту, фтор с концентрацией F 20-25 г/л и титан с концентрацией TiO2 ~ 10 г/л. Серную кислоту нейтрализуют до pH 4-6. Затем осуществляют связывание и осаждение фтора с помощью известкового молока с концентрацией CaO 200 г/л в виде нерастворимого осадка CaF2. Нейтрализованный рафинат подвергают фильтрации, в результате чего отделяют кек, содержащий Ti(OH)4, CaF2, CaO. Кек подвергают захоронению на шламохранилище. Фильтрат с концентрацией (NH4)2SO4 300 г/л упаривают и утилизируют в виде малоценного сульфата аммония, применяемого в качестве азотного удобрения.
В данном способе получения окислов тугоплавких металлов из лопаритового концентрата для вскрытия концентрата используется более безопасный для окружающей среды химический реагент по сравнению с хлорной технологией. Однако, данный способ обладает рядом существенных недостатков. Основным из них является значительные потери окислов тугоплавких металлов в процессе их извлечения. Это объясняется тем, что сразу же на первом этапе - вскрытии концентрата - происходит вскрытие и высвобождение этих наиболее ценных, которые переходят в сернокислый раствор и распределяются среди менее ценных компонентов, находящихся в твердой фазе. В результате этого приходится отделять от наиболее ценных компонентов менее ценные двойные сульфаты РЗЭ, с которыми уходит в различных формах до 25-30% тантала и ниобия. Для возвращения тантала и ниобия приходится осуществлять дополнительную переработку отвального кека, остающегося после переработки двойных сульфатов РЗЭ. Кроме того происходят безвозвратные потери тантала и ниобия с кристаллами титановой соли при ее высаливании из сернокислого раствора тантала, ниобия и титана. Выделение титана из сульфатных растворов в виде двойной титановой соли приводит к большим потерям титана ввиду значительной растворимости титановой соли в этих условиях. В связи с этим сквозное извлечение титана в готовую продукцию составляет не более 72%. Извлекаемые этим способом окислы тугоплавких металлов имеют повышенную активность вследствие перехода в их сернокислый раствор порядка 50% исходной активности. Кроме всего этого дефицитная и дорогостоящая плавиковая кислота, используемая для сульфатно-фторидной экстракции тантала и ниобия, в данном способе не утилизируется, т.к. концентрация фтора в рафинате после экстракции составляет всего 25-30 г/л, что делает утилизацию экономически не целесообразной. При реализации способа имеется большой расход серной кислоты, т.к. кислота из рафинатов не извлекается, а только утилизируется в виде малоценного сульфата аммония. Все это делает способ сложным, малоэффективным и экономически не выгодным.
В основу настоящего изобретения была положена задача разработать способ получения окислов тугоплавких металлов из лопаритового концентрата, в котором их извлечение и переработка рафинатов осуществлялись бы при таких условиях, чтобы исключались потери извлекаемых ценных компонентов, обеспечивался возврат в технологию плавиковой и серной кислот, обеспечивалось получение радиоактивно чистых готовых продуктов, благодаря чему обеспечивается упрощение способа, повышение его эффективности и экономичности.
Поставленная задача решается тем, что в способе получения окислов тугоплавких металлов из лопаритового концентрата, включающем измельчение концентрата до крупности частиц по меньшей мере 0,075 мм с классификацией, вскрытие лопаритового концентрата концентрированной неорганической кислотой при атмосферном давлении и температуре свыше 100oC, а также последующее образование из продуктов вскрытия концентрата фторидных соединений тантала и ниобия под воздействием плавиковой кислоты и их экстракцию с помощью трибутилфосфата, а также извлечение диоксида титана, новым является то, что образование фторидных соединений тантала и ниобия обеспечивают растворением плавиковой кислотой с концентрацией по меньшей мере 40%, гидратного кека окислов тугоплавких металлов, образующегося в результате вскрытия лопаритового концентрата концентрированной азотной кислотой, с одновременным образованием в результате этого фтор-титановой кислоты, после извлечения окислов тантала и ниобия осуществляют упарку рафината в 1,5-2,0 раза при 105-108oC, затем извлечение из него плавиковой кислоты путем ее отгонки с помощью концентрированной серной кислоты и возврат плавиковой кислоты на растворение гидратного кека, из оставшегося кубового остатка выкристаллизовывают сульфат титанила моногидрат, из которого получают готовый продукт в виде диоксида титана, а остающийся маточник, содержащий концентрированную серную кислоту, возвращают в оборот для извлечения плавиковой кислоты из упаренного рафината.
Благодаря такому решению гидратный кек, в котором полностью на 100% сосредоточены извлекаемые окислы тугоплавких металлов, подвергается растворению в плавиковой кислоте. Последующая экстракция тантала и ниобия трибутилфосфатом с помощью образовавшейся фтор-титановой кислоты обеспечивает полное без потерь их извлечение в готовый продукт. Переработка рафината с высокой концентрацией фтора позволяет выделить из него и вернуть в оборот (на растворение гидратного кека ОТМ) порядка 90% дорогостоящей и дефицитной плавиковой кислоты HF, а в кубовом остатке сосредоточить весь диоксид титана и остальные 10% от исходного HF. Выделение из кубового остатка титана в виде кристаллов сульфата титанила моногидрата с последующей его переработкой в готовый продукт, а также возврат серной кислоты в маточнике с остаточным титаном на отгонку фтора позволяют полностью выделить диоксид титана, вернуть в оборот большую часть серной кислоты и остатки фтора. Благодаря всему этому и обеспечивается упрощение способа, повышение его эффективности и экономичности.
Новым является также то, что выкристаллизовывание сульфата титанила моногидрата осуществляют путем нагревания кубового остатка острым паром до 140-150oC при его перемещении в непрерывном потоке в течение 5,5-6,0 ч.
Благодаря такому решению обеспечивается дополнительная очистка кристаллов сульфата титанила моногидрата от примесей, а сами образующиеся кристаллы обладают хорошей фильтруемостью и отстаиваемостью.
Заявляемый способ получения окислов тугоплавких металлов из лопаритового концентрата осуществляется следующим образом. Исходный концентрат лопарита измельчается до крупности по меньшей мере 95% частиц не более 0,075 мм мокрым помолом с классификацией частиц и сгущением пульпы лопаритового концентрата. Затем осуществляют азотнокислотное вскрытие пульпы лопарита при атмосферном давлении азотной кислотой HNO3 с концентрацией C 650-700 г/л при 115-118oC. Поскольку процесс азотнокислотного вскрытия пульпы подробно рассмотрен в ранее поданной заявке этого же заявителя, в данной заявке он раскрывается в обобщенном виде. После азотнокислотного вскрытия получают пульпу вскрытия - азотнокислая пульпа гидратного кека окислов тугоплавких металлов (ОТМ). В результате вскрытия в раствор перешли все окислы редкоземельных металлов, превратившись в растворимую форму нитратов редкоземельных элементов R(NO3)3. Одновременно в процессе вскрытия под воздействием азотной кислоты в раствор перешли в форме нитратов и все примеси лопарита, включая источник альфа-активности оксид тория и мезоторий. Наиболее ценные из выделяемых компонентов лопарита - оксиды тантала, ниобия и титана практически не растворяются азотной кислотой и поэтому полностью, на 100% остаются в твердой части пульпы, превратившись в гидратированные окислы тугоплавких металлов - гидратный кек окислов тугоплавких металлов. При этом в кеке эти компоненты находятся в смеси, аналогично тому, как они находились в лопарите. Таким образом в результате вскрытия лопаритового концентрата азотной кислотой происходит полное однократное отделение наиболее ценных компонентов (тантала, ниобия), остающихся в гидратном кеке без каких-либо потерь, от менее ценных компонентов, перешедших в раствор. При этом гидратный кек практически свободен от радиоактивности, т.к. ~ 95% оксида тория и мезотория находится в азотнокислом растворе нитратов РЗЭ и примесей и, поэтому, при дальнейшей переработке не требуется специального процесса дезактивации кека ОТМ. Затем азотнокислую пульпу гидратного кека разбавляют водой в 1,5-2,0 раза и охлаждают. После охлаждения осуществляют фильтрацию раствора азотнокислой пульпы гидратного кека и последующую его отмывку от азотнокислых растворов нитратов редкоземельных элементов и примесей. В результате отмывки получают чистый гидратный кек ОТМ в виде пульпы с концентрацией нитратов NO3 ~ 2 г/л и концентрацией твердого Cтв 150-200 г/л. Чистый гидратный кек является исходным продуктом для последующего получения из него оксидов тугоплавких металлов, которые полностью остались в нем.
Извлечение окислов тугоплавких металлов из чистого гидратного кека осуществляют его растворением в плавиковой кислоте с концентрацией по меньшей мере 40% или более no HF. Растворение идет с большим выделением тепла. Для снижения температуры отвод тепла из реакционной емкости осуществляют водой, пропускаемой через змеевик. После растворения фторидную пульпу подвергают отстаиванию и фильтрации для удаления из фторидного раствора тантала, ниобия и титана нерастворенной части кека ОТМ, состоящей в основном из фторидов РЗЭ, кальция и кремния. Количество осадка не превышает 10% от исходной массы гидратного кека. Осадок отдувают на фильтре от влаги воздухом. Осадок распульповывают известковым молоком, в результате чего фтор переходит в нерастворимый осадок, и откачивают на шламонакопитель. Чистый фторидный раствор тантала, ниобия и титана направляют на экстракцию тантала и ниобия с помощью 100% трибутилфосфата. Экстракция протекает аналогично экстракции, осуществляемой после сернокислотного вскрытия. При этом в заявляемом способе фтор-титановая кислота H2TiF6, образовавшаяся из титана под воздействием плавиковой кислоты, способствует переходу фторидных соединений тантала и ниобия в трибутилфосфат. В данном случае фтор-титановая кислота играет роль серной кислоты при экстракции после сернокислотного вскрытия. Трибутилфосфат со смытым им танталом и ниобием затем направляют на поочередную реэкстракцию (смыв с трибутилфосфата) ниобия и тантала с помощью своих реэкстрагирующих растворов. Получаемые в результате реэкстракции регенераты тантала и ниобия подвергают обработке 25% аммиаком NH4OH. В результате осаждения получают гидроокиси тантала и ниобия Ta(OH)5 и Ni(OH)5. Гидроокиси подвергают последовательной отмывке, сушке и прокалке, в результате чего получают оксиды (пятиокиси) тантала и ниобия Ta2O5 и Ni2O5, являющиеся готовым продуктом, получаемым в результате реализации заявляемого способа. При этом процент извлечения оксидов тантала и ниобия из лопаритового концентрата достигает по меньшей мере 93% и они практически полностью лишены радиоактивности, т.к. не содержат тория Th и мезотория MsTh. Это объясняется тем, что порядка 5% радиоактивности, переходящие в гидратный кек при вскрытии лопаритового концентрата азотной кислотой, остаются связанными в осадке, остающемся от кека после его растворения плавиковой кислотой. Такой готовый продукт является особо ценным исходным продуктом для металлургии, электроники и технологии полупроводников. После извлечения тантала и ниобия рафинат подвергают переработке с целью извлечения оставшейся двуокиси титана, а также извлечения и повторного использования (утилизации) плавиковой кислоты HF. Практически весь титан присутствует в рафинате в виде фтор-титановой кислоты H2TiF6 и в очень малом количестве в виде соединения (NH4)2TiF6. В небольшом количестве также присутствуют NH4F и Na2SiF6. Перед переработкой рафинат упаривают в 1,5-2,0 раза при 105-108oC для повышения концентрации извлекаемых из рафината компонентов и уменьшения расхода применяемых при этом химических реагентов. В результате упарки концентрация фтора C возрастает с 200 до 300 г/л, а концентрация TiO2 возрастает с 300 до 450 г/л. Переработку рафината начинают с отгонки плавиковой кислоты. Для этого используют концентрированную 92% серную кислоту H2SO4. Кислоту вводят в упаренный рафинат до достижения концентрации C=1000-1100 г/л. Температуру поддерживают в пределах 110-120oC. При таких условиях происходит бурное выделение парогазовой смеси паров (HF+H2O). Парогазовую смесь подвергают охлаждению для конденсации паров воды и абсорбции паров фтористого водорода чистой водой с получением в результате этого 40% плавиковой кислоты HF. В результате отгонки из рафината выделяют порядка 90% плавиковой кислоты, которая вновь направляется на растворение гидратного кека ОТМ. Возвращаемая плавиковая кислота называется оборотной и составляет 90% от общего количества плавиковой кислоты, применяемой для растворения гидратного кека ОТМ. Совершенно очевидно, что процесс извлечения тантала и ниобия из гидратного кека путем его растворения плавиковой кислотой без ее последующей регенерации и возвращения в оборот сделал бы его экономически нецелесообразным. Остающийся кубовый остаток содержит порядка 10% исходной HF и весь TiO2. Из кубового остатка выкристаллизовывают сульфат титанила моногидрат СТМ (TiOSO4•H2O). Выкристаллизовывание сульфат титанила моногидрата осуществляют путем нагрева кубового остатка острым паром до 140-150oC и выдержки при перемещении его в непрерывном потоке в течение 5,5-6,0 ч. Под воздействием пара кроме нагрева происходит разбавление пульпы кубового остатка на 25-30% по сравнению с исходным. Образующиеся при этих условиях кристаллы СТМ имеют высокую чистоту, т.к. все примеси, в частности железо, остаются в растворе, а сами кристаллы обладают хорошей фильтруемостью и отстаиваемостью. Кристаллы СТМ отделяют для дальнейшей переработки. При переработке кристаллы сульфат титанила моногидрата растворяют в воде и нейтрализуют аммиаком NH4OH. В результате этого в осадок выпадает гидроокись титана Ti(OH)4. Затем осуществляют фильтрацию, отмывку и отдувку осадка гидроокиси титана. После этого осуществляют сушку гидроокиси титана и прокалку при температуре t=900-950oC. В результате получают диоксид титана TiO2 в рутильной форме, которая является готовым продуктом и применяется в качестве пигмента в лакокрасочной промышленности и в качестве катализатора для очистки газовых выбросов ТЭЦ. Остающийся маточник содержит концентрированную серную кислоту с концентрацией C=1200-1300 г/л и указанный выше остаток HF. Серную кислоту возвращают для обработки упаренного рафината при отгонке HF. Возвращаемая серная кислота называется оборотной и составляет порядка 76% (38000 т/г) от общего количества используемой серной кислоты (50500 т/г). Пополняемый со склада объем серной кислоты составляет порядка 24% (12500 т/г). Благодаря выделению титана в виде сульфата титанила моногидрата с оборотом серной кислоты, достигается высокая степень выделения титана в готовую продукцию. При этом сквозное извлечение титана составляет не менее 95%.
Нижезаявляемый способ иллюстрируется конкретным примером его осуществления.
Переработали способом азотнокислого вскрытия 1000 кг лопаритового концентрата марки КЛ-1 указанного выше состава.
Вскрытие концентрата осуществляли при следующих условиях.
1. После исходного мокрого помола концентрата > 95% частиц имеют крупность не более 0,074 мм.
2. Содержание твердого в пульпе вскрытия - 600 г/л.
3. Исходная концентрация азотной кислоты - 700 г/л.
4. Температура вскрытия - 115-118oC.
5. Время вскрытия - 40 ч.
6. Интенсивное перемешивание механической мешалкой (число оборотов n= 200-220 об/мин).
На вскрытие лопаритового концентрата было израсходовано:
1. Азотная кислота 70% - 1440 кг.
2. Техническая вода - 400 кг.
3. Греющий пар (глухой) - 550 кг.
4. Вода на отмывку гидратного кека ОТМ - 3000 кг.
В результате азотнокислой переработки достигнуто вскрытие лопаритового концентрата (по сумме редкоземельных элементов) - 95%.
Получено отмытого гидратного кека ОТМ - 575 кг (по сухому) следующего состава, %: Ta2O5 - 0,99%; Nb2O5 - 14,5; TiO2 - 66,2; сумма оксидов РЗЭ - 2,78; ThO2 - 0,05; CaO - 0,4; Na2O - 0,75; Fe2O3 - 0,35; SiO2 - 3,5; NO3 - 0,1.
Дезактивированные нитратные растворы РЗЭ перерабатывались по традиционной экстракционной технологии.
Отмытый гидратный кек в виде пульпы с содержанием по твердому ~ 800 г/л перерабатывали по фторидной технологии, т.е. растворяли 40% плавиковой кислотой. Затем осветленный фторидный раствор подавали на экстракционный передел с получением пятиокисей тантала и ниобия. Остающиеся рафинаты перерабатывались с получением диоксида титана и сульфата аммония.
В результате переработки 575 кг гидратного кека по фторидной технологии было получено:
- гидрооксид тантала - 5,3 кг; сквозное извлечение - 93,0% по Ta2O5;
- пятиокись ниобия - 75,3 кг; сквозное извлечение - 93,5% по Nb2O5;
- диоксид титана - 362 кг; сквозное извлечение - 95,0% по TiO2.
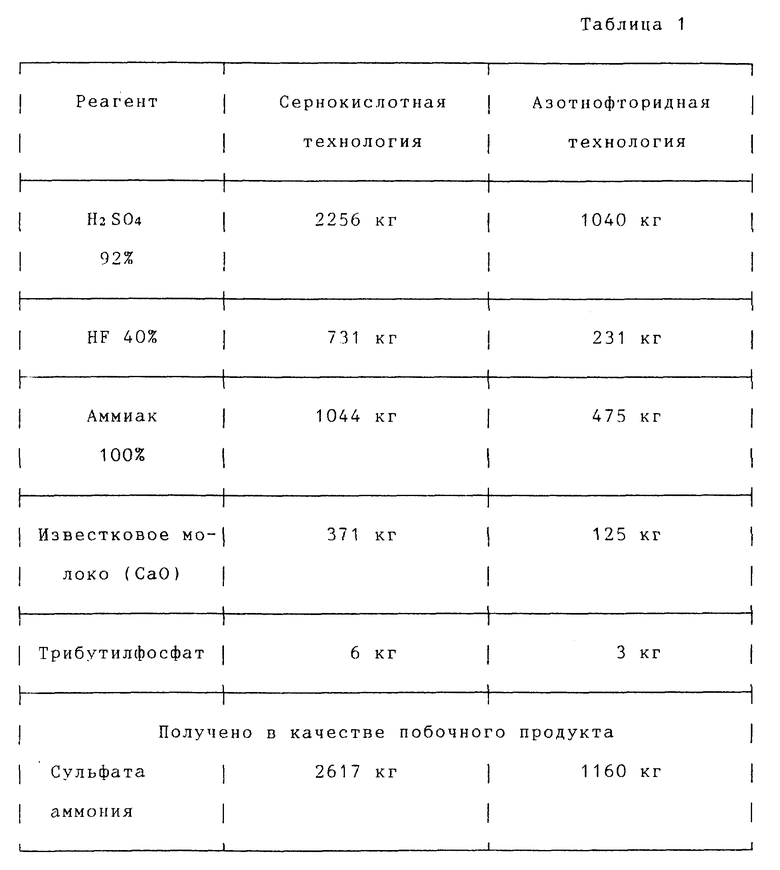
Расход реагентов на получение данной продукции в соответствии с заявляемым способом по сравнению с сернокислотной технологией представлен в табл. 1.
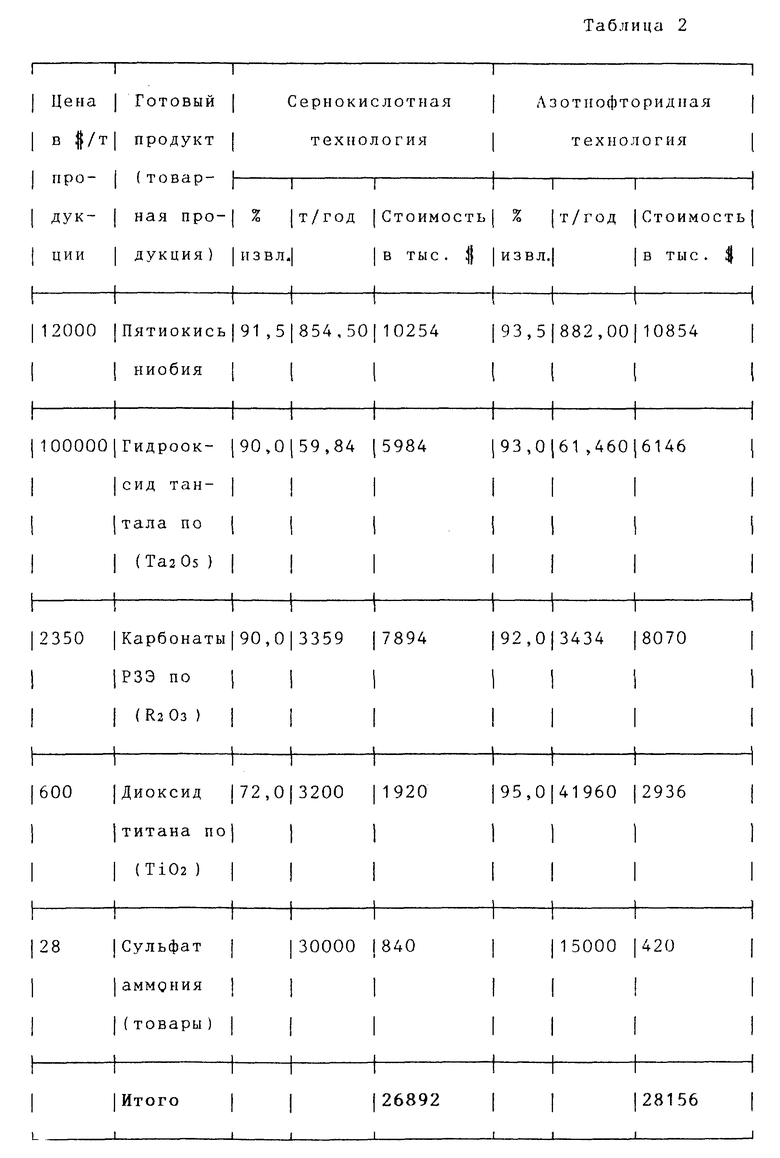
Преимущества заявляемого способа получения окислов тугоплавких металлов из лопаритового концентрата по сравнению с сернокислотным способом видны из приводимых в табл. 2 данных на примере цеха ГАО "Силмет" (Эстония) по переработке 12 тыс. т исходного сырья в год.
Из приведенных примеров и данных табл. 1 и 2 видно, что преимущества заявляемого способа по сравнению со способом-прототипом заключаются не только в более высоком сквозном извлечении ценных компонентов в готовую продукцию, но и в значительно меньших расходах основных реагентов на переработку гидратного кека. Это не только снижает прямые затраты на переработку лопаритового концентрата и уменьшает себестоимость готовой продукции, но также уменьшает затраты на переработку и утилизацию отходов и выбросов вредных веществ в окружающую среду.
Из приведенных конкретных примеров осуществления заявляемого изобретения для любого специалиста в данной области совершенно очевидна возможность его реализации с одновременным решением поставленной задачи. При этом также очевидно, что при реализации изобретения могут быть сделаны незначительные изменения, которые однако не будут выходить за пределы изобретения, определяемые приводимой ниже формулой изобретения.
Заявляемый способ получения окислов тугоплавких металлов из лопаритового концентрата обеспечивает полное однократное отделение наиболее ценных компонентов тантала, ниобия и титана от менее ценных компонентов и примесей. При этом наиболее ценные компоненты извлекаются практически без потерь и абсолютно чистыми от радиоактивности. Способ имеет высокую экономическую эффективность, т.к. особо ценная и дорогостоящая плавиковая кислота практически полностью регенерируется после использования и возвращается в оборот, а концентрированная серная кислота, расход которой очень велик, регенерируется и возвращается в оборот в объеме порядка 76% от общего объема. Способ значительно проще в аппаратурном оформлении по сравнению со способом прототипом, т.к. имеет значительно меньшие объемы участвующих в процессе ингредиентов и легко поддается полной автоматизации ввиду практической непрерывности процесса. Способ создает более щадящие (менее коррозионные) условия для работы оборудования ввиду более низких температур и замены сульфатно-фторидных сред на фторидные среды. Уменьшает затраты и трудоемкость на поддержание оборудования в рабочем состоянии, а также количество обслуживающего персонала.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ОКИСЛОВ ТУГОПЛАВКИХ МЕТАЛЛОВ ИЗ ЛОПАРИТОВОГО КОНЦЕНТРАТА | 1999 |
|
RU2149912C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКИСЛОВ ТУГОПЛАВКИХ МЕТАЛЛОВ ИЗ ЛОПАРИТОВОГО КОНЦЕНТРАТА | 2000 |
|
RU2160787C1 |
| СПОСОБ ПЕРЕРАБОТКИ ЛОПАРИТОВОГО КОНЦЕНТРАТА | 2000 |
|
RU2168556C1 |
| СПОСОБ ПЕРЕРАБОТКИ ЛОПАРИТОВОГО КОНЦЕНТРАТА | 1999 |
|
RU2145980C1 |
| СПОСОБ ПЕРЕРАБОТКИ ЛОПАРИТОВОГО КОНЦЕНТРАТА | 2000 |
|
RU2171303C1 |
| СПОСОБ ПЕРЕРАБОТКИ ЛОПАРИТОВОГО КОНЦЕНТРАТА | 2001 |
|
RU2211871C1 |
| СПОСОБ ПЕРЕРАБОТКИ ЛОПАРИТОВОГО КОНЦЕНТРАТА | 2001 |
|
RU2211870C1 |
| СПОСОБ ПЕРЕРАБОТКИ КОЛУМБИТОВОГО КОНЦЕНТРАТА | 2014 |
|
RU2576562C1 |
| СПОСОБ ПЕРЕРАБОТКИ ЛОПАРИТОВОГО КОНЦЕНТРАТА | 2000 |
|
RU2182887C2 |
| СПОСОБ ПЕРЕРАБОТКИ ЛОПАРИТОВОГО КОНЦЕНТРАТА | 2013 |
|
RU2513327C1 |
Изобретение относится к гидрометаллургической переработке рудных концентратов, а более конкретно к переработке лопаритового концентрата. Способ получения окислов тугоплавких металлов из лопаритового концентрата включает измельчение концентрата до крупности частиц по меньшей мере 0,075 мм с классификацией, вскрытие лопаритового концентрата концентрированной азотной кислотой при атмосферном давлении и температуре свыше 100°С, образование из продуктов вскрытия концентрата фторидных соединений тантала и ниобия под воздействием плавиковой кислоты и их экстракцию с помощью трибутилфосфата. Образование фторидных соединений тантала и ниобия обеспечивают растворением плавиковой кислотой с концентрацией по меньшей мере 40% гидратного кека окислов тугоплавких металлов, образующегося в результате вскрытия лопаритового концентрата концентрированной азотной кислотой, с одновременным образованием в результате этого фтор-титановой кислоты. После извлечения тантала и ниобия экстракцией осуществляют упарку рафината в 1,5-2,0 раза при 105-108°С, затем извлечение из него плавиковой кислоты путем ее отгонки с помощью концентрированной серной кислоты и возврат плавиковой кислоты на растворение гидратного кека. Из оставшегося кубового остатка выкристаллизовывают сульфат титанила моногидрат, из которого получают готовый продукт в виде диоксида титана, а оставшийся маточник, содержащий концентрированную серную кислоту, возвращают в оборот для извлечения плавиковой кислоты из упаренного рафината. Способ позволяет упростить технологию, повысить ее эффективность и экономичность. 1 з.п. ф-лы, 2 табл.
| Зеликман А.Н | |||
| и др | |||
| Металлургия редких металлов | |||
| - М.: Металлургия, 1991, с.101 - 105 | |||
| Способ переработки лопаритовых руд или концентратов | 1936 |
|
SU50965A1 |
| СПОСОБ ВСКРЫТИЯ ЛОПАРИТОВЫХ КОНЦЕНТРАТОВ | 0 |
|
SU198654A1 |
| СПОСОБ ВЫЩЕЛАЧИВАНИЯ ТАНТАЛА И НИОБИЯ ИЗ ПРОДУКТОВ РАЗЛОЖЕНИЯ ТАНТАЛО-НИОБИЕВОГОСЫРЬЯ | 0 |
|
SU165308A1 |
| Станок для намотки статора электрической машины | 1978 |
|
SU765941A1 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| Экономайзер | 0 |
|
SU94A1 |
Авторы
Даты
2000-04-20—Публикация
1999-09-07—Подача