Изобретение относится к пероральным твердым фармацевтическим композициям, содержащим гемфиброзил, и к способу их получения. В частности, настоящее изобретение относится к пероральным гемфиброзил-содержащим композициям, изготовленным, предпочтительно, в форме таблеток, таблеток с пленочным покрытием и капсул.
Гемфиброзил - 5-(2,5-диметилфенокси)-2,2-диметилпентаноевая кислота - представляет собой хорошо известное антигиперлипопротеиннемическое средство, используемое в высоких суточных дозах, составляющих от 900 мг до 1500 мг. Этот активный агент плохо растворим в воде и обладает гидрофобными свойствами. Поэтому получение гемфиброзил-содержащих фармацевтических композиций с адекватным растворением и адекватной адсорбцией активного ингредиента представляет серьезные трудности.
В целях увеличения растворимости активного ингредиента, в композициях, выпускаемых промышленностью, используются различные поверхностно-активные вещества (ПАВ). Так, например, 300-миллиграммовые капсулы и 600-миллиграммовые таблетки, выпускаемые в США (производитель: Parke Davis), содержат в качестве поверхностно-активного вещества полисорбат 80 [производное поли(окси-1,2-этандиил)-сорбитанмоно-9-октадеканоата] и лаурилсульфат натрия, соответственно (Physicians Desk Reference, 45th Edition, (1991), издатель: E. P. Barnhert, Oradell, N.Y., USA, стр. 1668. 450-мг таблетки, содержащие гемфиброзил и выпускаемые в Германии фирмой Parke Davis, также содержат полисорбат 80 в качестве ПАВ (Rote Liste, 1992, Bundesverband der Pharm. Ind. Frankfurt, par. 57020).
Гемфиброзил-содержащие фармацевтические композиции с быстрым и пролонгированным высвобождением активного ингредиента раскрываются в HU-PS N 204192. В этой работе, при изготовлении гранул, в качестве поверхностно-активного вещества (ПАВ) используется 0,7-0,8% полисорбата 80 (Твин 80).
В HU-PS N 204194 раскрываются гемфиброзил-содержащие композиции с быстрым высвобождением активного ингредиента, и композиции, активный ингредиент которых доставляется в кишечник. Указанные гранулы с быстрым высвобождением получают с использованием 0,5% лаурилсульфата натрия.
В HU-PS N 204193 раскрываются диспергируемые в виде композиции гемфиброзила. Эти композиции с непродолжительным высвобождением изготавливают путем покрытия тонкодисперсных частиц гемфиброзила смесью микрокристаллического воска и гидрофильного вещества (например, жирными спиртами, сложными эфирами жирных кислот, полиолами, производными целлюлозы, виниловыми производными) с последующим покрытием полученных частиц 0,5-2,0% ПАВ. Для этих целей в качестве ПАВ предлагается использовать лаурилсульфат натрия.
В соответствии с оценкой в ранее опубликованной заявке на Европатент N 462067, выпускаемые промышленностью гемфиброзильные капсулы содержат около 0,2% лаурилсульфата натрия, а выпускаемые промышленностью таблетки содержат около 0,7% лаурилсульфата натрия. Однако указанного содержания ПАВ не достаточно для обеспечения нужной растворимости активного ингредиента. Как указывается в заявке на Европатент N 462067, гемфиброзил-содержащие таблетки могут быть получены с использованием большего количества (а именно, 1-4%), по отношению к количеству гемфиброзила, ПАВ, имеющего гидрофильно-липофильный баланс (ГЛБ) от 10 до 50. В указанной заявке на Европатент раскрываются следующие поверхностно-активные вещества (ПАВ): полисорбаты, добавки типа Плюрона (сополимеры полиоксиэтилена и полиоксипропилена), щелочные соли сульфатов жирных кислот (в частности, лаурилсульфат натрия), соли жирных кислот (например, олеат натрия) и триэтаноламиноолеат. В вышеупомянутой заявке на Европатент N 462067 особо подчеркивается, что указанные поверхностно-активные вещества должны быть использованы в количестве 1-4 мас.% . по отношению к количеству гемфиброзила в данной композиции.
Согласно опубликованной заявке на Европатент N 475894, быстрорастворимые таблетки гемфиброзила могут быть получены с использованием в качестве носителя буферных солей сильных оснований и слабых кислот (например, карбонаты и цитраты), имеющих значение pH в водной среде около 5. Однако, как видно из вышеуказанной заявки, для достижения необходимого быстрого растворения активного ингредиента данные композиции должны содержать, по меньшей мере, 1% лаурилсульфата натрия.
Поверхностно-активные вещества, используемые в фармацевтических композициях для перорального введения, не могут рассматриваться как абсолютно инертные добавки. Эти добавки не только стимулируют растворение и адсорбцию активного ингредиента, они могут также способствовать растворению и адсорбции в желудочно-кишечном тракте некоторых других частично токсичных веществ. Исходя из этого, желательно избегать использования слишком большого количества ПАВ. Это особенно относится к фармацевтическим композициям, содержащим активные ингредиенты, которые вводятся пациентам в больших дозах и в течение длительного периода времени, поскольку в этом случае в организм может быть введено большее количество ПАВ.
Учитывая, что гемфиброзил принадлежит к активным ингредиентам, которые должны вводиться в больших дозах и концентрируются в течение длительного периода времени, существует строгое требование для гемфиброзил-содержащих фармацевтических композиций, которое обеспечит быстрое растворение и адсорбцию активной составляющей путем использования относительно небольшого количества ПАВ.
Поэтому целью настоящего изобретения является получение гемфиброзил-содержащих фармацевтических композиций, которые не имеют недостатков известных композиций и содержат относительно небольшое количество поверхностно-активного вещества.
Другой целью настоящего изобретения является предотвращение замедления растворения активного ингредиента, которое, в частности, имеет место после хранения при высоких температурах.
Еще одной целью настоящего изобретения является получение гемфиброзил-содержащих твердых фармацевтических композиций, имеющих малое среднеквадратичное отклонение в скорости растворения отдельных капсул и таблеток в пределах одной партии и среди нескольких партий.
Вышеуказанные цели могут быть с успехом достигнуты благодаря использованию настоящего изобретения.
Настоящее изобретение относится к пероральной твердой фармацевтической композиции, содержащей гемфиброзил в качестве активного ингредиента, и стандартные фармацевтические добавки, включающие в себя в качестве ПАВ бис(2-этил-гексил)-натрий-сульфосукцинат в количестве 0,05-0,5 мас. % по отношению к содержанию гемфиброзила в данной композиции.
Было неожиданно обнаружено, что относительно небольшое количество (0,05-0,5% по отношению к содержанию гемфиброзила в композиции) бис-(2-этил-гексил)-натрий-сульфосукцината (именуемого "Диотилан") обеспечивает очень быстрое и однородное растворение активного ингредиента, высвобождаемого из таблеток или капсул. При этом среднеквадратичное отклонение в скорости растворения в пределах данной партии и среди различных партий очень мало. Другое преимущество фармацевтической композиции заключается в том, что благодаря добавлению Диотилана в вышеуказанном количестве можно с успехом предотвратить снижение скорости растворения, которое, в частности, имеет место после длительного хранения при высокой температуре.
В другом варианте своего осуществления настоящее изобретение относится к способу получения пероральных твердых фармацевтических композиций, содержащих гемфиброзил в качестве активного ингредиента и стандартные фармацевтическое добавки, где в качестве ПАВ используется бис-(2-этил-гексил)-натрий-сульфосукцинат в количестве 0,05-0,5 мас.% по отношению к содержанию гемфиброзила в композиции.
Как указывалось выше, преимущественный эффект, получаемый при использовании Диотилана в относительно небольших концентрациях, является неожиданным и не может быть предсказан исходя из материала, изложенного в предшествующих работах. Согласно заявке на Европатент N 462067, быстрое растворение гемфиброзила может быть достигнуто лишь с использованием более чем 1% гидрофильного ПАВ, имеющего гидрофильнолипофильный баланс (ГЛБ) в пределах 10 - 50. Диотилан также принадлежит к группе ПАВ, обладающих гидрофильными свойствами. Однако в заявке на Европатент N 462067 полностью отсутствуют какие-либо упоминания относительно использования Диотиолана. Поэтому указанная заявка на Европатент создает предубеждение против настоящего изобретения при отсутствии повода.
Гемфиброзильные композиции настоящего изобретения содержат Диотилан в сочетании со стандартными добавками, обычно используемыми при изготовлении таблеток и капсул. Так, например, могут быть использованы следующие предпочтительные добавки:
- наполнители, например микрокристаллическая целлюлоза, лактоза, маннит, крахмал, целлюлоза или фосфат кальция и т.п.;
- связующие вещества, предпочтительно, желатин, поливинилпирролидон, гидроксипропилметилцеллюлоза, поливиниловый спирт, поливинилбутираль и т.п.;
- дезинтегрирующие агенты, предпочтительно, крахмал, карбоксиметиловый крахмал, карбоксиметилцеллюлоза, структурированный поливинилпирролидон и т. п.;
- замасливатели, предпочтительно стеарат магния, стеарат кальция, стеариновая кислота, гидрогенизированное касторовое масло, тальк и т.п.;
- агенты, увеличивающие скольжение, предпочтительно, коллоидальная кремниевая кислота, тальк и т.п.
Фармацевтические композиции настоящего изобретения изготавливают предпочтительно в форме таблеток, таблеток с пленочным покрытием, и капсул.
Для получения гемфиброзил-содержащих капсул, таблеток или таблеток с пленочным покрытием настоящего изобретения, активный ингредиент в сухом виде гомогенизируют с наполнителем (например, целлюлозой, лактозой, маннитом, крахмалом, микрокристаллической целлюлозой, фосфатом кальция или т.п.), взятым в количестве 0-40 мас.% по отношению к содержимому капсулы или сердцевины непокрытой таблетки. По желанию, сухой гомогенизат может быть гранулирован известными способами. Гранулирование может быть осуществлено с использованием процедур как "мокрой", так и "сухой" грануляции. В случае "сухой" грануляции, гомогенизат смешивают со связующим веществом, обычно используемым для изготовления капсул и таблеток (таким, как поливинилпирролидон, гидроксипропилцеллюлоза, поливинилбутираль, гидроксипропилметилцеллюлоза, желатин и т.п.) и взятым в количестве не более чем 5 мас.%, и с Диотиланом, взятым в количестве 0,05-0,5 мас.% по отношению к количеству гемфиброзила; после чего полученную смесь прессуют в брикеты или таблетки, измельчают и просеивают для получения частиц с нужным размером (например, 0,1-1,0 мм). "Мокрую" грануляцию осуществляют путем размешивания гомогенизата с раствором, содержащим не более чем 5 мас.% связующего вещества (такого, как поливинилпирролидон, гидроксипропилметилцеллюлоза, желатин, поливиниловый спирт, и т.п.) и 0,05-0,5 мас.% Диотилана (по отношению к количеству гемфиброзила) и полученным с использованием воды, или C1-3-алканола, или смеси воды и алканола. Процедура гранулирования может быть также осуществлена путем опрыскивания смеси в виде порошка, флюидизированного в грануляторе с псевдоожижением, раствором связующего вещества и Диотилана. Полученные таким образом гранулы осушают и просеивают с получением частиц нужного размера (обычно ниже 1,0 мм). Затем гомогенизат или полученные из него гранулы смешивают с замасливателем (например, таким, как стеарат магния, стеарат кальция, стеариновая кислота, гидрогенизированное касторовое масло или тальк) и/или с добавкой, понижающей трение (например, такой, как коллоидальная кремниевая кислота или тальк), после чего полученную смесь инкапсулируют или прессуют в таблетки, причем, если необходимо, эти таблетки могут быть покрыты пленкой с использованием водорастворимых полимеров (например, таких, как гидроксипропилметилцеллюлоза, полиэтиленгликоль и т.п.).
Качество композиции может быть охарактеризовано однородностью растворения активного ингредиента и равномерностью скорости растворения. Растворение гемфиброзила, содержащегося в композиции, оценивали методом "лопастного" перемешивания, описанного в USP XXII, осуществляемого при 37oC, с использованием в качестве растворяющей среды 900 мл фосфатного буфера (pH 7,4). Количество высвобождаемого гемфиброзила определяют с помощью ВЭЖХ.
Количество гемфиброзила, высвобождаемого из композиции, определяли сразу, вначале теста на растворение и через 5, 15, 30 и 45 минут после начала теста на растворение, соответственно. Для каждой партии использовали 6 дубликатов (капсулы, таблетки с пленочным покрытием, таблетки) и строили графики для среднего количества (%) растворенного гемфиброзила, высвобожденного из каждой таблетки, или для среднего количества (%) гемфиброзила, высвобожденного и растворенного из 6 композиций.
Однородность растворения оценивали путем определения для данного момента времени относительно среднеквадратичного отклонения (rsd) в процентных содержаниях растворенного гемфиброзила в пределах одной партии; среднего показателя растворения для 6 таблеток; и среднеквадратичного отклонения для средних показателей среди различных партий (RSD). Эти величины показаны на диаграммах в сравнении с данными растворения, и с rsd- и RSD-величинами для гемфиброзил-содержащих твердых фармацевтических композиций, выпускаемых промышленностью.
Величины rsd и RSD вычисляли по следующим формулам:
Среднее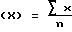
Отклонение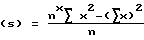
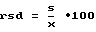
Отклонение средних величин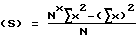
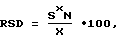
где x - измеренные показатели растворения (%); n - число параллельных измерений (6 дубликатов для каждой партии); X - средний показатель растворения (на партию); N - число испытуемых партий; s - среднеквадратичное отклонение в показателях растворения (внутри одной партии); S - среднеквадратичное отклонение в показателях растворения (среди различных партий); rsd - среднеквадратичное отклонение в % (внутри одной партии); RSD - среднеквадратичное отклонение в % (среди различных партий).
В дальнейшем изобретение поясняется описанием конкретных, но не ограничивающих, примеров осуществления изобретения и прилагаемыми чертежами, на которых:
фиг. 1 - высвобождение активного ингредиента из капсул;
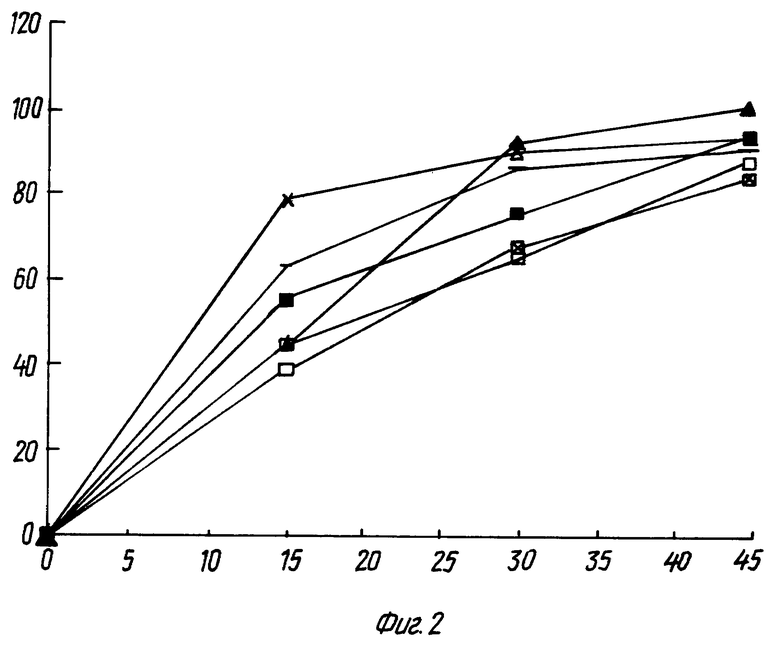
фиг. 2 - высвобождение активного ингредиента из капсул; выпускаемых промышленностью;
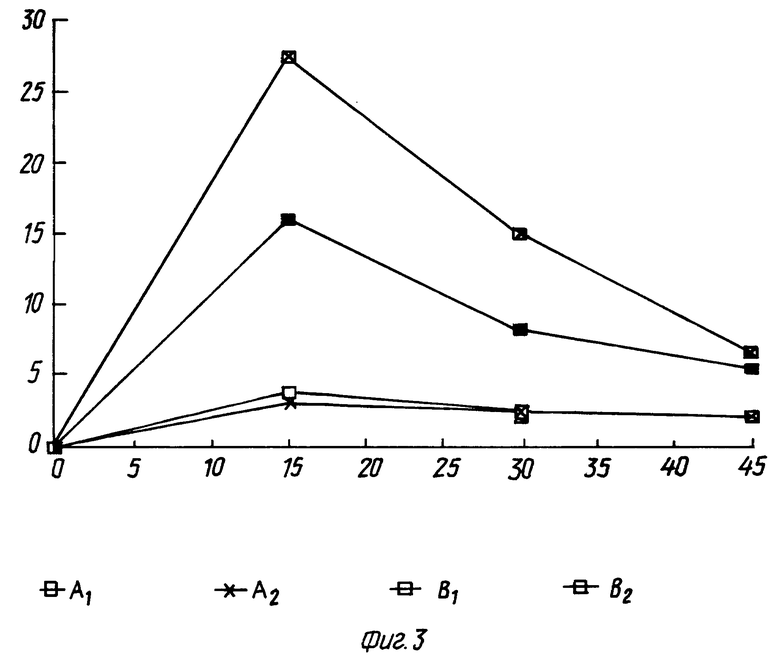
фиг. 3 - среднеквадратичное отклонение в скоростях высвобождения из капсул;
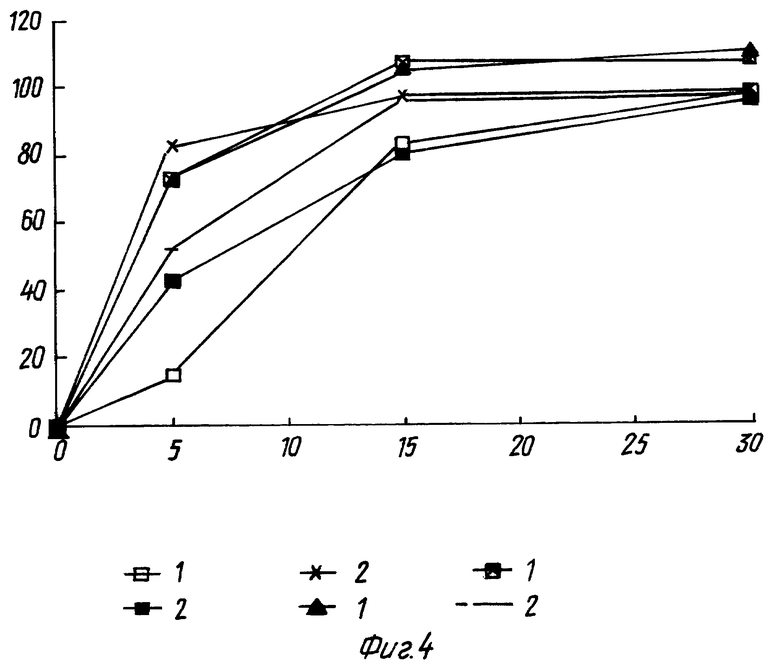
фиг. 4 - высвобождение активного ингредиента из таблеток;
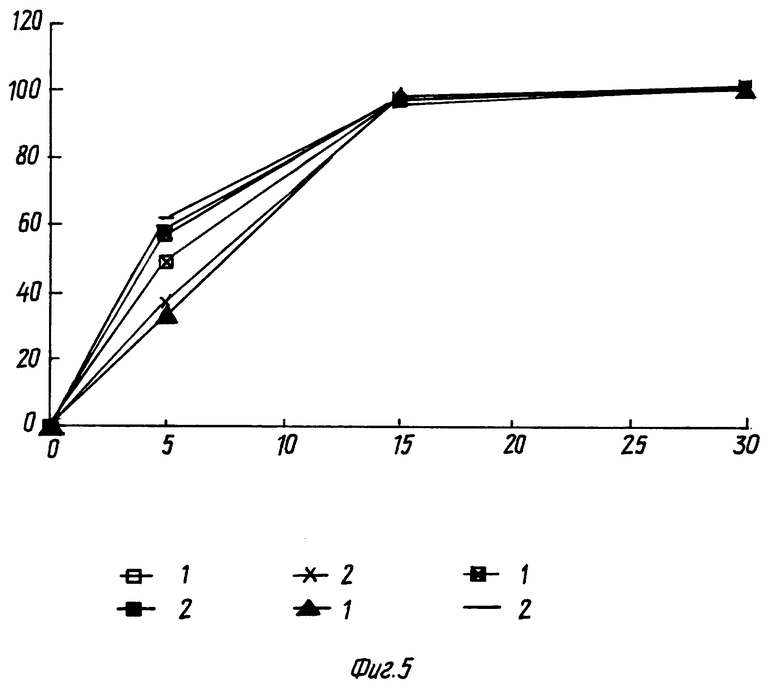
фиг. 5 - высвобождение активного ингредиента из таблеток; выпускаемых промышленностью;
фиг. 6 - относительное среднеквадратичное отклонение в величинах растворения.
Пример 1
Гемфиброзил-содержащая капсула
Получали гемфиброзил-содержащие капсулы, имеющие следующий состав:
Компонент - Количество, мг/капсула
Гемфиброзил - 300
Кукурузный крахмал - 63
Гидроксипропилметилцеллюлоза - 16
Стеарат магния - 6
Натрий-содержащий карбоксиметиллированный крахмал - 12
Коллоидальная кремниевая кислота - 2,4
Диотилан - 0,4
Гемфиброзил и кукурузный крахмал гомогенизировали в смесителе Lodige, а затем гранулировали с водным раствором Диотилана и гидроксипропилметилцеллюлозы. Полученные гранулы осушали, просеивали через сито в 0,8 мм и возвращали в смеситель Lodige, после чего добавляли компоненты внешнего слоя (стеарат магния, натрий-содержащий карбоксиметиловый крахмал, коллоидальную кремниевую кислоту) и полученную смесь гомогенизировали. Затем этой гомогенизированной смесью заполняли жесткие желатиновые капсулы (размер "0").
Высвобождение активного ингредиента (растворение) оценивали методом "лопастного размешивания", описанным в USP XXII и проводимым при 37oC с использованием в качестве растворяющей среды 900 мл фосфатного буфера (pH 94). Количество высвобожденного гемфиброзила определяли с помощью ВЭЖХ.
Данные растворения для капсул, полученных в соответствии с настоящим изобретением, приводятся на фиг. 1, а данные растворения для капсул, выпускаемых промышленностью (США), приводятся, в целях сравнения, на фиг. 2.
Среднеквадратичное отклонение для каждой партии (для теста использовали 6 капсул) вычисляли исходя из экспериментальных данных. На фиг. 3 представлен график зависимости rsd-величин от времени.
Как видно из вышеприведенных данных, растворение активного ингредиента внутри одной партии в случае капсул настоящего изобретения является более однородным (меньшее значение среднеквадратичного отклонения), чем в случае капсул, выпускаемых промышленностью (стандартных капсул).
Пример 2
Гемфиброзил-содержащие таблетки с пленочным покрытием
Получали гемфиброзил-содержащие таблетки с пленочным покрытием, имеющие следующий состав:
Компонент - Количество, мг/таблетка
Гемфиброзил - 600,0
Микрокристаллическая целлюлоза - 120,0
Желатин - 40,0
Диотилан - 2,0
Стеарат кальция - 16,0
Натрий-содержащий карбоксиметиллированный крахмал - 54,0
Тальк - 24,0
Коллоидальная кремниевая кислота - 8,0
Пленочное покрытие
Компонент - Количество, мг
Гидроксипропилметилцеллюлоза - 9,5
Полиэтиленгликоль - 4,0
Симетикон - 0,5
Диоксид титана - 2,0
Полная масса: 800,0 мг
Гемфиброзил и микрокристаллическую целлюлозу гомогенизировали в вихревом смесителе Lodige и гомогенизат гранулировали со смесью водного раствора желатина (pH 3-4) и этанолового раствора Диотилана. Полученные гранулы осушали, просеивали через сито 0,8 мм и возвращали в смеситель Lodige, после чего смесь гомогенизировали с компонентами внешнего слоя (стеаратом кальция, натрий-содержащим карбоксиметиллированным крахмалом, тальком, коллоидальной кремниевой кислотой). Гомогенизированную смесь прессовали в овальные двояковыпуклые таблетки, весом 864 мг. Эти таблетки покрывали (в сосуде для изготовления драже) водорастворимой пленкой путем опрыскивания таблеток водной дисперсией, содержащей вышеуказанные компоненты.
Растворение активного ингредиента оценивали методом, описанным в USP XXII ("лопастный" метод) и осуществляемым при 37oC с использованием 900 мл фосфатного буфера (pH 7,4) в качестве растворяющей среды. Количество высвобождаемого гемфиброзила определяли с помощью ВЭЖХ.
Оценку растворения для таблеток с пленочным покрытием, полученных в соответствии с настоящим изобретением, и для таблеток, выпускаемых промышленностью (США), проводили сразу после изготовления или закупки, соответственно, а также после хранения при 40oC в течение 3 месяцев. Как в случае таблеток настоящего изобретения, так и в случае закупленных таблеток с пленочным покрытием, для каждого теста использовали 3 партии, и каждая партия состояла из 6 таблеток с пленочным покрытием.
На фиг. 4 представлен график данных, полученных для 3 партий, каждая из которых состояла из 6 таблеток настоящего изобретения. На фигуре приводятся средние данные, полученные сразу после изготовления таблеток и через 3 месяца после хранения при 40oC, соответственно. На фиг. 5 представлен график соответствующих данных, полученных для готовых композиций, выпускаемых промышленностью.
Как видно из представленных графиков, скорость растворения для выпускаемых промышленностью таблеток с пленочным покрытием значительно снижается после их хранения. Более того, в случае промышленных образцов, средние показатели растворения, измеренные для различных партий, обнаруживали значительно более высокое среднеквадратичное отклонение, чем средние показатели, полученные для композиций настоящего изобретения.
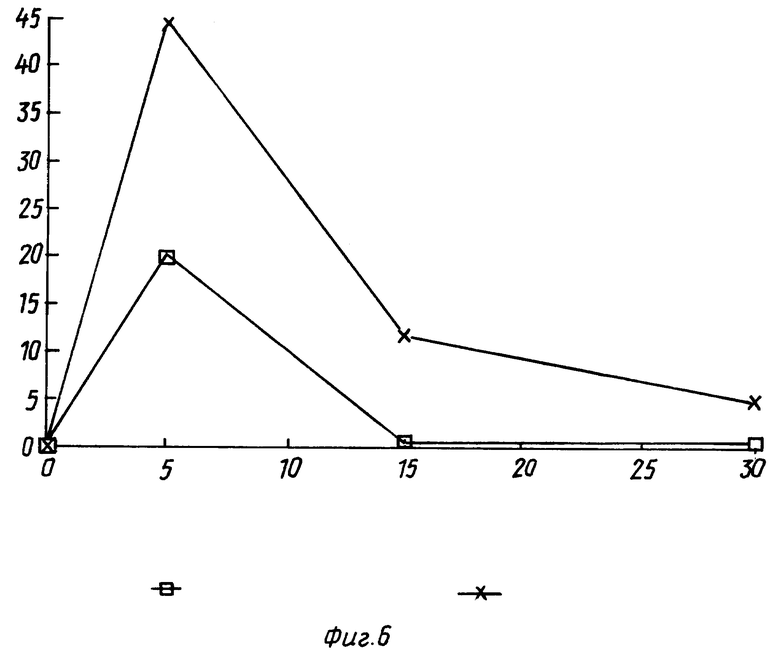
Для более точной оценки однородности растворения были вычислены относительные среднеквадратичные отклонения (RSD) в средних величинах для отдельных партий в случае таблеток настоящего изобретения и таблеток, выпускаемых промышленностью, после чего были построены диаграммы зависимости полученных данных от времени (см. фиг. 6).
Как можно видеть из фиг. 6, в случае продукта настоящего изобретения, среднеквадратичное отклонение в показателях растворения среди отдельных партий значительно ниже, чем в случае промышленного продукта.
Пример 3
Сравнительный тест
В этом эксперименте определяли и сравнивали скорости растворения Диотилан-содержащих таблеток настоящего изобретения; таблеток, содержащих идентичное количество лаурилсульфата натрия; и таблеток, не содержащих ПАВ.
Таблетки получали в соответствии с процедурой, описанной в Примере 2 (Эксперимент 3A). Согласно Эксперименту 3B, Диотилан заменяли идентичным количеством лаурилсульфата натрия. А согласно Эксперименту 3C, в грануляционный раствор не добавляли никакого ПАВ. В Экспериментах 3A и 3B масса таблеток составляла до 864 мг, а в Эксперименте 3C масса таблеток составляла до 862 мг.
Растворение таблеток оценивали методом, описанным в примере 2 за исключением того, что в данном случае не использовали пленочного покрытия.
Результаты измерений представлены в таблице.
Полученные данные со всей очевидностью продемонстрировали, что при отсутствии ПАВ скорость растворения очень мала. Добавление 0,33 мас.% лаурилсульфата натрия способствует увеличению скорости растворения, но наилучший результат дает использование Диотилана в соответствии с настоящим изобретением. Неожиданным также оказался тот факт, что такому быстрому высвобождению и растворению гемфиброзила (активного ингредиента) способствует использование Диотилана в низких концентрациях.
Надписи к фигурам
Фиг. 1.
Высвобождение активного ингредиента из капсул настоящего изобретения (6 капсул)
Высвобожденный гемфиброзил (%)
Время растворения (минуты)
Фиг. 2
Высвобождение активного ингредиента из капсул, выпускаемых промышленностью (6 капсул)
Высвобожденный гемфиброзил (%)
Время растворения (минуты)
Фиг. 3
Среднеквадратичное отклонение в скоростях высвобождения из капсул (2 партии по 6 капсул в каждой)
Процент среднеквадратичного отклонения
Время растворения (минуты)
A1 и A2 = капсулы настоящего изобретения
B1 и B2 = капсулы, выпускаемые промышленностью
Фиг. 4
Высвобождение активного ингредиента из таблеток настоящего изобретения (3 партии, среднее для 2•6 таблеток в каждой)
Высвобожденный гемфиброзил (%)
Время растворения (минуты)
1 = измеряли после получения
2 = измеряли после хранения
Фиг. 5
Высвобождение активного ингредиента и таблеток, выпускаемых промышленностью (3 партии, среднее для 2•6 таблеток в каждой)
Высвобожденный гемфиброзил (%)
Время растворения (минуты)
1 = измеряли после закупки
2 = измеряли после хранения
Фиг. 6
Относительно среднеквадратичное отклонение в величинах растворения (3-3 партии, отклонение в 2•6 средних величинах)
Процент отклонения
Время растворения (минуты)
Таблетки настоящего изобретения
Промышленные таблетки.

Сущность изобретения: пероральная твердая фармацевтическая композиция содержит в качестве активного ингредиента гемфиброзил, а также стандартные фармацевтические добавки. В качестве поверхностно-активного вещества композиция включает бис-(2-этил-гексил)-натрийсульфосукцинат в количестве 0,05-0,5 мас. % по отношению к содержанию гемфиброзила в данной композиции. Фармацевтические композиции изобретения обеспечивают однородное растворение указанного активного ингредиента с равномерной скоростью, малое среднеквадратичное отклонение скоростей растворения. 2 с. и 8 з.п. ф-лы, 6 ил., 1 табл.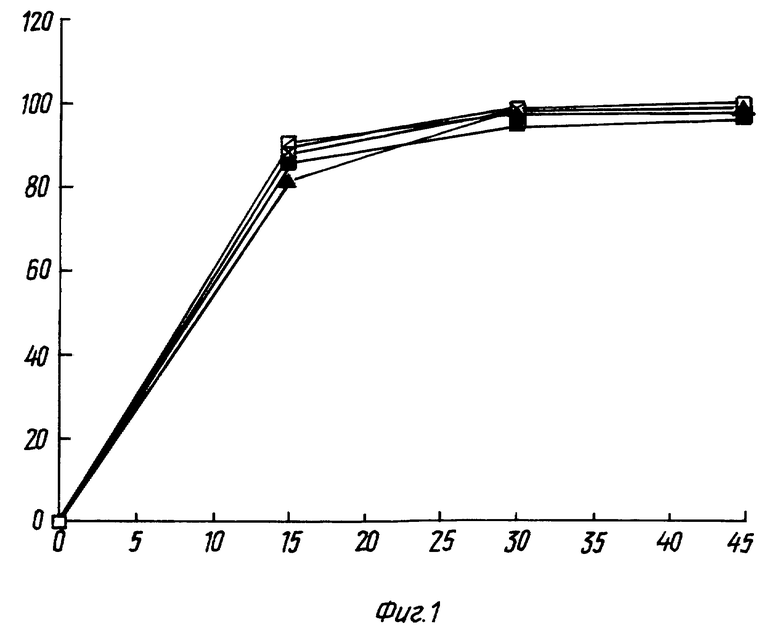
| Способ измерения линейных размеров | 1973 |
|
SU462067A1 |
| EP 0475894 А1, 18.03.92 | |||
| VIDAL | |||
| Справочник | |||
| Лекарственные препараты в России | |||
| Астра ФармСервис, 1995, с | |||
| Саморазгружающаяся железнодорожная платформа | 1921 |
|
SU366A1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2121835C1 |
| Технология лекарственных форм./Под ред | |||
| Л.А | |||
| Ивановой | |||
| - М.: Медицина, 1991, т.2, с | |||
| Способ обделки поверхностей приборов отопления с целью увеличения теплоотдачи | 1919 |
|
SU135A1 |
Авторы
Даты
2000-07-10—Публикация
1995-04-27—Подача