Изобретение относится к области физико-химических методов анализа, в частности к устройствам для определения активности ионов тяжелых металлов в растворах, а именно к электродам с твердой мембраной, и может найти применение как при анализе промышленных сточных вод, так и при экологическом мониторинге водных экосистем.
Известны ионоселективные электроды с гомогенными и гетерогенными твердыми мембранами, закрепленными в корпусе (Никольский Б.П., Матерова Е.А. Ионоселективные электроды. - Л: Химия, 1980, с. 206), которые подразделяют на следующие группы.
1. Кристаллические мембранные электроды - ионоселективные электроды, в которых мембрана - это кристаллический материал, изготовленный из единственного вещества или гомогенизированной смеси. Например, сульфид-серебряный электрод, выпускаемый фирмой "Орион", включает спрессованную поликристаллическую мембрану Ag2S, а выпускаемый фирмой "Crytur" - монокристалл Ag2S. Мембраны для медного, свинцового и кадмиевого поликристаллических электродов получают, как правило, из смесей сульфида серебра и сульфида (халькогенида) соответствующего металла (Никольский Б.П., Матерова Е.А. Ионоселективные электроды. - Л.: Химия, 1980, с. 97-115).
2. Стеклянные электроды, в которых чувствительной мембраной является тонкая пленка стекла. Наиболее распространенными мембранами такого типа, чувствительными к ионам тяжелых металлов, являются стекла, в состав которых входят халькогениды соответствующих металлов. Примером такого электрода может служить ионоселективный электрод, описанный в патенте РФ N 2034289, кл. G 01 N 27/333, опубл. 10.05.89, Власов Ю.Г., Бычков Е.А., Легин А.В. "Состав халькогенидной стеклянной мембраны электрода для определения ионов свинца, где мембрану получают сплавлением сульфида свинца, иодида серебра и дисульфида германия, смешанных в определенных пропорциях, при давлении 102 Па и температуре 1300 К в течение 24 часов. Плав разрезают на плоскопараллельные диски толщиной 1 - 5 мм, полируют до зеркального блеска на пасте ГОИ и вклеивают эпоксидным компаундом в поливинилхлоридный корпус электрода.
3. Гетерогенные мембраны, в которых активные вещества или смеси активных веществ смешивают с инертной матрицей, такой как силиконовый каучук или поливинилхлорид, или внедряют в гидрофобинизированный графит, образуя чувствительную мембрану. Например, предложена мембрана свинецселективного электрода, включающая нейтральный переносчик в качестве электродоактивного компонента, пластификатор и поливинилхлоридную матрицу, которая дополнительно содержит липофильную добавку (Патент РФ N 2054666, кл. - G 01 N 27/333 от 23.09.93, Пятова Е.Н., Копытин А.В. и др. Мембрана свинецселективного электрода).
Наиболее близкими заявляемому являются электроды, выпускаемые фирмой "Орион", в которых спрессованная поликристаллическая мембрана, состоящая из смеси сульфидов соответствующих металлов и серебра, помещена в корпус из эпоксидного реактопласта (Справочное руководство по применению ионоселективных электродов. М.: Мир, 1986, 231 с.).
Недостатками вышеперечисленных электродов с твердыми мембранами являются сложность изготовления, невозможность восстановления мембраны после отравления, а также использование солей драгоценных металлов. Кроме того, в РФ не налажен промышленный выпуск ионоселективных электродов для определения тяжелых металлов, используются только электроды зарубежного производства
Задачей изобретения является расширение арсенала простых в изготовлении, регенерируемых ионоселективных электродов с твердой мембраной для определения ионов тяжелых металлов.
Поставленная задача решается созданием ионоселективного электрода для определения ионов тяжелых металлов, включающего корпус и мембрану на основе сульфида металла. Причем мембрана выполнена в виде нанесенной на корпус пленки сульфида определяемого металла толщиной 50-500 нм.
Предлагаемые электроды изготавливают достаточно простым и доступным способом химического осаждения из щелочных растворов тиомочевины в присутствии солей свинца и модифицируют ионами соответствующих металлов. Для этого рабочую часть корпуса электрода опускают на 1 час в щелочной раствор тиомочевины в присутствии солей свинца (J.E. Reynolds, J.Chem.Soc., London, 45, 162 (1884)). В результате разложения тиомочевинного комплекса свинца на границе раздела фаз выделяется сульфид свинца в виде тонкой пленки с металлическим зеркальным блеском, которая выполняет функцию мембраны, обратимую к ионам свинца. Путем последующей модификации поверхности пленки в растворах солей тяжелых металлов с pKs больших, чем у сульфида свинца, можно получить мембраны, активные к ионам Cu(II), Ag(I), Cd(II), Hg(II), Fe(III). Мембраны, чувствительные к ионам цинка, кадмия и таллия могут быть получены альтернативным способом химического осаждения из растворов по методикам, описанным в литературе (Mokili В., Charreire Y., Cortes R., Lincot D. // Thin Solid Films. - 1996. - 288. N 1-2. - P. 21-28: Бетенеков Н.Д., Медведев В.П. , Китаев Г.А. // Радиохимия, N 3, 1978, с. 431-438; Юсупов P.А. Исследование кинетики и механизма реакций образования сульфидов свинца и таллия в щелочных растворах тиомочевины и тиосемикарбазида. Дисс.канд. хим. наук. КГУ, Казань, 1981).
Пленки сульфида свинца, используемые в качестве ионоселективной мембраны, имеют толщину, которая задается временем контактирования реакционного раствора с поверхностью электрода. При толщине пленок менее 50 нм снижается интервал определяемых концентраций, а при более 500 нм происходит механическое отслоение пленки сульфида свинца.
Пример 1. Изготовление ионоселективного электрода для определения ионов свинца. Платиновый электрод марки ЭВП-1 обезжиривался насыщенным раствором Na2CO3, выдерживался в течение 20 минут в 1М растворе NaOH и промывался дистиллированной водой. В химический стакан емкостью 250 мл наливали 187,5 мл дистиллированной воды, опускали подготовленный платиновый электрод на глубину не более 2 см, вливали 12,5 мл 0,2 М раствора азотнокислого свинца, 25 мл свежеприготовленного 1 М раствора КОН и 25 мл 0,2 М раствора тиомочевины. Раствор перемешивали при комнатной температуре. По истечении 60 минут электроды, покрытые в результате химической реакции поликристаллической пленкой сульфида свинца толщиной 150 нм, вынимали из раствора, споласкивали дистиллированной водой и обтирали фильтровальной бумагой.
Пример 2. Электрод изготовлен аналогично примеру 1, но время контактирования с реакционным раствором составляет 15 минут. В результате химической реакции получили поликристаллическую пленку сульфида свинца толщиной 30 нм.
Пример 3. Изготовление ионоселективного электрода для определения ионов свинца. На поверхность стеклянного электрода с pH-функцией марки ЭСЛ-63-07 наносили пленку сульфида свинца по методике, приведенной в примере 1.
Пример 4. Изготовление ионоселективного электрода для определения ионов свинца. Стеклянный электрод с pNa-функцией марки ЭСЛ-51-07 покрывали пленкой сульфида свинца с внутренней и внешней поверхности. Для этого измерительную часть электрода отделяли и проводили осаждение сульфида свинца, как это описано в примере 1. Далее внутрь измерительной части электрода заливали 0,1 М раствор нитрата свинца и соединяли ее с верхней частью электрода с помощью уплотняющего резинового кольца.
Пример 5. Изготовление ионоселективного электрода для определения ионов свинца. Пластинку из нержавеющей стали размером 20х20х1 мм3, имеющую контакт для подсоединения к pH-метру, покрывали пленкой сульфида свинца по методике, описанной в примере 1.
Пример 6. Изготовление ионоселективного электрода для определения ионов серебра. Электрод, полученный по методике, описанной в примере 1, помещают на сутки в 10-2 М раствор AgNO3 объемом 50 мл для протекания реакции ионного обмена Pb(II) - Ag(I). При этом степень замещения ионов свинца в пленке сульфида на ионы серебра составляет 85%.
Аналогично примеру 6 могут быть получены электроды, селективные по отношению к ионам Cu(II), Cd(II), Hg(II), Fe(III).
Методика потенциометрических измерений с использованием ионоселективных электродов.
Для измерения электродных характеристик применяли следующую электрохимическую ячейку:
где MS - пленка сульфида определяемого металла.
В работе использовали pH-метр - милливольтметр pH-673М, в качестве электрода сравнения - насыщенный хлор-серебряный электрод марки ЭВЛ-1МЗ. 0,1М растворы определяемых металлов готовили на бидистиллате по навеске из препаратов марки "хч", точную концентрацию устанавливали известными титриметрическими методами.
Градуировочные растворы в области от 10-2 до 10-7 моль/л готовили непосредственно перед измерением путем разбавления исходного раствора. Для предотвращения попадания ионов хлора из электрода сравнения в анализируемый раствор насыщенный хлор-серебряный электрод помещали в промежуточный сосуд, содержащий 1M раствор KNO3. Для поддержания постоянной ионной силы в 50 мл раствора добавляли 10 мл 5-10-2 М раствора NaClO4. PH среды поддерживали с помощью ацетатного буферного раствора с pH 5. Электролитический контакт между электродами осуществляли с помощью солевого мостика, содержащего 1%-ный раствор агар-агара в присутствии 1M раствора KNO3.
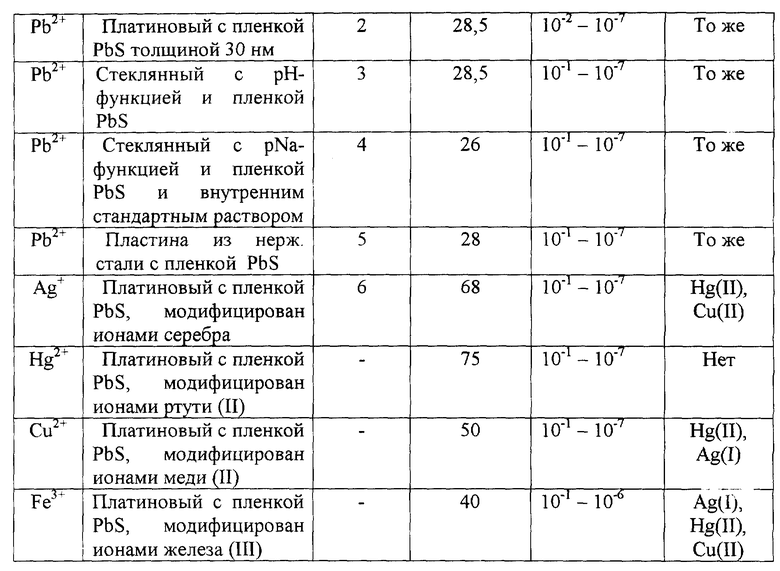
Аналитические характеристики электродов, изготовленных по описанным выше методикам, приведены в таблице 1.
Предлагаемые электроды устойчивы к механическим воздействиям и сохраняют химический состав как на воздухе, так и в растворах с pH от 4 до 7, время отклика электрода в зависимости от концентрации ионов составляет от 30 до 120 с.
Введение в определяемый раствор ионов калия, натрия, аммония, никеля, кобальта, цинка и кадмия не оказывает влияния на потенциал электродов, приведенных в таблице 1.
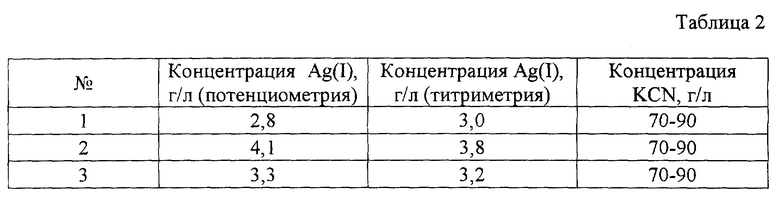
В качестве иллюстрации возможности использования предлагаемых электродов приведем пример определения содержания Ag(I) в электролитах серебрения. При потенциометрических измерениях использовали стеклянный электрод с pNa-функцией, внешняя поверхность которого покрыта пленкой сульфида свинца и модифицирована ионами серебра в 0,1 М растворе AgNO3. Содержание Ag(I) параллельно контролировалось химическим титрованием роданидом калия с использованием железоаммонийных квасцов в качестве индикатора. Данные анализа представлены в таблице 2.
Сопоставление результатов анализов показывает удовлетворительную сходимость, относительное отклонение не превышает 8%.
По эксплуатационным характеристикам предлагаемые электроды не уступают ионоселективным электродам, выпускаемым фирмой "Орион", но значительно доступнее и проще в изготовлении. Так, установлено (Hirata Н., Higashiyama К - Ibid. , 1971, v. 54, p. 415), что наилучшими условиями для прессования мембраны из PbS и Ag2S оказалось давление 1 кПа (10 т/см2) при 350-500oC в течение 3 часов. Изготовление предлагаемого электрода не требует применения специальной аппаратуры, использования высоких температур и давления. Кроме того, достоинствами этого электрода являются: 1) отсутствие солей драгоценных металлов, что значительно удешевляет электрод, 2) возможность регенерации мембраны в лабораторных условиях после отравления ее мешающими ионами путем растворения в кислотах и последующего химического осаждения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Кадмий-селективный электрод | 2019 |
|
RU2712920C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ СОРБЕНТА С МЕТАЛЛОСУЛЬФИДНЫМ ПОГЛОЩАЮЩИМ СЛОЕМ | 1999 |
|
RU2153395C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ СЕРЕБРА ИЗ СТОЧНЫХ ВОД И ОТРАБОТАННЫХ ТЕХНОЛОГИЧЕСКИХ РАСТВОРОВ | 1999 |
|
RU2154031C1 |
| МЕМБРАНА СВИНЕЦСЕЛЕКТИВНОГО ЭЛЕКТРОДА | 1993 |
|
RU2054666C1 |
| ПОЛУПРОВОДНИКОВЫЙ СЕНСОРНЫЙ ЭЛЕМЕНТ ДЛЯ ОПРЕДЕЛЕНИЯ ИОНОВ СВИНЦА В ВОДНЫХ РАСТВОРАХ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2015 |
|
RU2612358C2 |
| Состав мембраны ионоселективного электрода для определения хлорид-ионов | 1989 |
|
SU1622812A1 |
| Состав халькогенидной стеклянной мембраны электрода для определения ионов свинца | 1988 |
|
SU1583820A1 |
| СОСТАВ МЕМБРАНЫ ИОНОСЕЛЕКТИВНОГО ЭЛЕКТРОДА ДЛЯ ОПРЕДЕЛЕНИЯ ИОНОВ СВИНЦА | 2006 |
|
RU2315988C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ СЕРЕБРА ИЗ СТОЧНЫХ ВОД И ОТРАБОТАННЫХ ТЕХНОЛОГИЧЕСКИХ РАСТВОРОВ | 2001 |
|
RU2209184C2 |
| Состав мембраны ионоселективного электрода для определения тиомочевины в растворах | 1987 |
|
SU1492262A1 |

Изобретение относится к области физико-химических методов анализа, в частности к устройствам для определения активности ионов тяжелых металлов в растворах, а именно к электродам с твердой мембраной, и может найти применение как при анализе промышленных сточных вод, так и при экологическом мониторинге водных экосистем. Ионоселективный электрод для определения ионов тяжелых металлов включает корпус и мембрану на основе сульфида металла, причем мембрана выполнена в виде нанесенной на корпус пленки сульфида определяемого металла толщиной 50-500 нм. Достигается упрощение изготовления мембранных моноселективных электродов при большей их доступности. 2 табл.
Ионоселективный электрод для определения ионов тяжелых металлов, включающий корпус и мембрану на основе сульфида металла, отличающийся тем, что мембрана выполнена в виде нанесенной на корпус пленки сульфида определяемого металла толщиной 50 - 500 нм.
| Справочное руководство по применению ионоселективных электродов | |||
| - М.: Мир, 1986, 231 с | |||
| Состав мембраны халькогенидного стеклянного электрода для определения ионов свинца | 1987 |
|
SU1497554A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ЭТИЛОВОГО СПИРТА В СЛОЖНЫХ ВОДНО-СПИРТОВЫХ РАСТВОРАХ | 1992 |
|
RU2065162C1 |
| Твердотельный ионоселективный электрод для определения свинца (II) | 1988 |
|
SU1608554A1 |
| Состав мембраны ионоселективного электрода для определения активности ионов свинца | 1990 |
|
SU1733994A1 |
| СОСТАВ ХАЛЬКОГЕНИДНОЙ СТЕКЛЯННОЙ МЕМБРАНЫ ЭЛЕКТРОДА ДЛЯ ОПРЕДЕЛЕНИЯ ИОНОВ СВИНЦА | 1989 |
|
RU2034289C1 |
| US 4995960 A, 26.02.1991 | |||
| DE 4208957 A1, 17.02.1994 | |||
| Автоматический огнетушитель | 0 |
|
SU92A1 |
Авторы
Даты
2000-07-10—Публикация
1999-09-15—Подача