Это изобретение относится к изоляции и очистке липидных компонентов клеточной оболочки, происходящих от бактерий, принадлежащих к родам Mycobacterium, Corynebacterium, Nocardia или Rhodococcus, из которых наиболее распространенным и наиболее важным с точки зрения человеческого здоровья является род Mycobacterium.
Род Mycobacterium включает большое число как сапрофитных, так и патогенных видов. Наиболее известные члены рода, М.tuberculosis и M.leprae, являются соответственно возбудителями туберкулеза и проказы, которые входят в число наиболее серьезных заболеваний, наблюдаемых у человека.
Туберкулез: Современное положение
Туберкулез рассматривается как наиболее распространенная передающаяся контактным путем болезнь в большей части мира. Несмотря на большие успехи медицинской науки и ряд эффективных лекарств, что иногда создает впечатление, будто болезнь побеждена, и несмотря на организованные международные усилия, туберкулез остается проблемой мирового здравоохранения ошеломляющего масштаба: примерно одна треть населения инфицирована М.tuberculosis (Fauci, 1995), было сообщено о более 8 миллионах новых случаев в мире и о более чем 3 миллионах смертей только в 1990 г (Snider, 1994). Прогноз, сделанный Всемирной Организацией Здравоохранения, показывает, что к 2000 году ежегодные цифры возрастут до 10,2 миллионов новых случаев и 3,5 миллионов смертей, причем Азия и Африка южнее Сахары будут наиболее пораженными континентами (De Cock et al., 1992; Dolin, Raviglione, Snider and Kochi, 1994; Raviglione, and Kochi, 1995; Wilkinson and de Cock, 1996). В соответствии с недавно опубликованным "Докладом ВОЗ о эпидемии туберкулеза, 1995" цифры, прогнозируемые на следующее десятилетие, еще более тревожны: 300 миллионов новых случаев и 30 миллионов смертей (Holler, 1995). В действительности, в 1993 г ВОЗ объявила туберкулез глобальной угрозой общественному здоровью (Bloomfield, 1995; Wilkinson and de Cock, 1996).
Главные причины этого драматического возвращения и неослабевающего распространения туберкулеза могут быть определены как:
1) Недостаточная защита, предлагаемая всемирной программой вакцинирования, основанной на использовании БЦЖ (BCG, Bacillus of Calmette and Guerin: штамм M.Bovis, ослабленный по Calmette и Guerin пропусканием его 231 раз за период 13 лет через среду, содержащую глицерин и бычью желчь).
2) Проблемы, связанные с выявлением туберкулеза.
3) Проблемы, связанные с лечением туберкулеза и появлением устойчивых к многим лекарствам штаммов М.tuberculosis.
4) Взаимодействие с ВИЧ-инфекцией.
5) Социально-экономические аспекты.
1. Недостаточная защита, предлагаемая всемирной программой вакцинирования, основанной на БЦЖ.
Попытки предотвратить распространение туберкулеза, вызывая сопротивление инфекции М.tuberculosis, были предприняты в начале этого века с использованием вакцинации БЦЖ. На основании многих контролируемых опытов было установлено, что защитная эффективность, получаемая при вакцинации БЦЖ, варьируется от 0 до 80% (Snider, 1994; Hershfield, 1995), и на основе анализа публикаций было найдено, что эффективность БЦЖ вакцинации примерно 50% (Colditz et al., 1994; O'Brien, 1995).
Был предложен ряд гипотез/объяснений этого неудовлетворительного положения (Fine, 1994). Наиболее значимыми являются:
i) Вариации вакцин БЦЖ, которые могут быть вызваны вариацией штаммов или различием процессов получения;
ii) различия в патогенезе М.tuberculosis;
iii) различия в воздействии окружающих микобактерий - окружающие микобактерии могут взаимодействовать антагонистически или синергически с БЦЖ;
iv) генетические различия между группами населения, подвергаемыми вакцинации БЦЖ;
v) различия в питании и пребывании на солнце между различными группами населения;
vi) различия между схемами разных опытов;
vii) неадекватность критерия, используемого для оценки защитного действия вакцинации БЦЖ.
2. Проблемы, связанные с выявлением туберкулеза.
Точное и своевременное выявление туберкулеза и родственных микобактериальных заболеваний является одним из важных требований для разработки более успешной глобальной стратегии борьбы с этими болезнями.
Главными недостатками традиционных лабораторных методов обнаружения являются или неспособность различить живые и мертвые бациллы (быстрое и простое окрашивание по ZiehI-Neelsen) или то, что если эти методы подтверждают присутствие живых бацилл (прямое культивирование), требуется несколько недель для завершения лабораторных тестов. Это, в свою очередь, может отсрочить назначение лечения и может привести к дальнейшему развитию болезни.
Хотя недавно разработанные молекулярные подходы к диагностированию туберкулеза (Godfrey-Faussett, 1994; Richeldi, Barnini and Saltini, 1995; Bloomfield, 1995; Vlaspolder, Singer and Roggeveen, 1995) привели к использованию этих быстрых и чувствительных инструментов обнаружения передовыми лабораториями в развитых странах, они дороги и требуют специально подготовленного персонала. По этим причинам они не подходят для скрининга - выявления туберкулеза в бедных ресурсами и эндемических по ТБЦ регионах, уже отягощенных затратами на контроль болезни (O'Brien, 1995; Voelker, 1995).
Подобное положение существует и в области быстрого тестирования чувствительности к лекарствам (Schaberg et al., 1995; Pretorius et al., 1996) и быстрого культивирования Mycobacterium (Bloomfield, 1995). Значительные успехи в этих областях не могут быть использованы по финансовым причинам в странах, наиболее пораженных туберкулезной пандемией.
3. Проблемы, связанные с лечением туберкулеза и появлением устойчивых к многим лекарствам штаммов М.tuberculosis.
Разработка эффективной химиотерапии туберкулеза сделала возможным лечение инфицированных людей, предотвращая тем самым полное развитие болезни. Хотя антитуберкулезные препараты с доказанным бактерицидным действием (рифампицин, изониазид и пиразинамид), также как и препараты с бактериостатическим или повышающими сопротивление организма и профилактическими свойствами (стрептомицин сульфат, этамбутол и тиацетазон) являются доступными (Weil, 1994), всемирный успех в борьбе с болезнью не был до сих пор достигнут из-за двух главных факторов: невыполнения пациентами предписанного режима и финансовых ограничений, существующих в развивающихся странах.
Сомнительно, чтобы превентивная терапия изониазидом оказалась эффективной для контроля над туберкулезом в развивающихся странах. Этот подход, хотя и широко применяемый в Северной Америке, имеет два главных недостатка. Во-первых, эту терапию, возможно, потребуется применять в течение всей жизни больного ТБЦ, и, во-вторых, ее стоимость, а именно 18 долларов США на пациента на шестимесячный курс, может оказаться непомерно высокой, особенно для наиболее пораженных регионов, где для всего здравоохранения доступно лишь 4 доллара США на пациента в год (O'Brien, 1995).
Прерванное и/или незавершенное лечение, кроме вредных эффектов для пациента, приводит к появлению и распространению устойчивых к мультипрепаратам штаммов М. tuberculosis, что еще более осложняет общую ситуацию (Beyers et al. , 1996). Недавняя оценка ВОЗ показала, что 50 миллионов человек во всем мире могут быть уже носителями штаммов M.tuberculosis, устойчивых к одному или более из наиболее употребительных антитуберкулезных препаратов. Уже в 1991 г было установлено, что одна треть от всех туберкулезных больных в Нью-Йорке была устойчива, по крайней мере, к одному препарату, и почти 20% были устойчивы к комбинации рифампицина и изониазида (Неnderson, 1995).
4. Взаимодействие с ВИЧ-инфекцией.
Документированная тесная связь между туберкулезом и ВИЧ-инфекцией, а также часто встречающееся сопутствующее протекание обеих болезней усиливают тяжесть ситуации (Torres et al., 1990; De Cock, 1994; Cantwell and Binkin, 1994; Murray, 1994; Antonucci et al., 1995; Mofeson et al., 1995; Davies, Wilkinson and Colvin, 1996; Wilkinson and Moore, 1996). Согласно Public Health Reports (1995) ожидается, что число людей, которые болеют туберкулезом в Азии из-за параллельного инфицирования ВИЧ, увеличится в семь раз за это десятилетие.
Появление устойчивости к мультипрепаратам среди штаммов М. tuberculosis и других атипичных микобактерий придало дополнительную важность этой проблеме (Blumberg, Miller and Koornhof, 1994; Morse, 1994; Yew and Chau, 1995).
5. Социально-экономические аспекты.
Другие причины, обуславливающие дальнейшее распространение болезни, такие как безработица, перенаселение, общее ухудшение экономических условий, алкоголизм и эрозия инфраструктуры общественного здравоохранения были недавно рассмотрены Darbyshire (1995), Fauci (1995), Law et al. (1995) и Mangtani et al. (1995).
Возрастающий поток иммигрантов из эндемичных областей в страны, где туберкулез был под достаточно хорошим контролем, например, в США, создает дополнительные проблемы для сдерживания распространения туберкулеза (Huebner and Castro, 1995). Сообщается, что число случаев туберкулеза среди иммигрантов в США в 12 раз выше, чем наблюдаемое среди местного населения (Ballew and Becker, 1995).
Тенденции, обсужденные выше, оказывают огромное влияние на улучшение существующих подходов к лечению ТБЦ- больных как в эндемичных областях, так и в развивающихся странах, и на разработку новых препаратов, способных предотвратить и/или побороть туберкулез (Cole, 1995; Voelker, 1995). Хотя у исследователей, работающих в обоих направлениях, можно наблюдать осторожный оптимизм (Mwinga, 1995; Grosset, 1995), существующие в настоящее время экономические ограничения, даже в развитых странах, налагают серьезные ограничения на финансирование, необходимое для разработки новых антитуберкулезных препаратов, стоимость которой определена в 150 миллионов долларов США на каждое новое соединение (Grosset, 1995).
Иммунологические перспективы профилактики и лечения
Ввиду серьезности перечисленных выше проблем, ограниченных возможностей существующих методов борьбы с туберкулезом и высокой стоимости разработки новых форм для химиопрофилактики и химиотерапии, иммунологические подходы могли бы представлять релевантную и реалистичную альтернативу при поиске эффективного и экономически приемлемого решения для контроля и лечения туберкулеза и сопутствующих состояний.
Результаты, полученные в ряде испытаний, использующих лечение убитыми клетками M.vaccae (Stanford and Grange, 1994) убеждают, что этот сапрофитный микроорганизм может найти применение в иммунотерапии туберкулеза или как единственный агент (Barh et al., 1990a; Barh et al., 1990b; Stanford et al., 1990a) или в сочетании с химиотерапией (Stanford et al., 1990b; Prior et al. , 1995; Onybebujoh et al., 1995).
Модуляция воспалительных процессов, вызываемая использованием талидомида, была недавно применена при борьбе с туберкулезом. Благоприятный эффект талидомида на клинические проявления туберкулеза, сообщенный Cole (1995), дает основания обратить внимание на иммуномодуляторные свойства этого препарата при лечении болезни. Эти эффекты талидомида связываются с его сильным ингибирующим действием на некротический опухолевый фактор, цитокин, участвующий в воспалительном процессе, сопутствующем туберкулезу.
Достоинства этих двух подходов могут быть использованы и при лечении резистентных к лекарствам форм туберкулеза. Сообщались обнадеживающие данные ряда испытаний в этом направлении, проведенных в Иране (Etemadi, Farid and Stanford, 1992) и в Кувейте, Румынии, Вьетнаме и Индии (Stanford and Grange, 1993).
Иммунологические мишени
Попытки идентифицировать иммунологически активные компоненты М.tuberculosis в течение последних десятилетий фокусировались, главным образом, на протеинах (Daniel, 1984; Chaparas, 1984; Yanez et al., 1986; Deshpande et al., 1994; Torres et al., 1994), полисахаридах (Daniel, 1984; Misaki, Azurna and Yamamura, 1987), пептидогликолипидах и фосфолипидах (Brennan, 1984), липополисахаридах (Hunter, Gaylord and Brennan, 1986), гликолипидах (Brennan, 1984; Mс Neil et al., 1989) и липоарабиноманнане (Arya, 1993; Sieling et al., 1995).
Хотя липидные компоненты клеточных оболочек были ассоциированы с вирулентностью М.tuberculosis (Collins, 1994), считалось, что эти соединения липидной природы, т.е. бета-гидрокси жирные кислоты, не обладают иммуногенными свойствами. Возможность того, что миколиновые кислоты могут играть важную роль в сложном процессе иммунологического отклика человеческого организма на инфекцию M. tuberculosis, стала очевидной только недавно.
Гуморальная реакция на конъюгат миколиновые кислоты-BSA (альбумин бычьей сыворотки) впервые наблюдалась в 1994 (Патентная заявка Южной Африки N 95/3077 и публикация заявки PCT N WO 95/28642). Примерно в то же время измеримая клеточная иммунная реакция на миколиновые кислоты была продемонстрирована Beckman et al. (1994). Авторы обнаружили, что эти соединения стимулируют пролиферацию редкой субпопуляции человеческих двуотрицательных Т-клеток и описали новый путь антиген-представления молекулами CD1, существующими на профессиональных антиген-представляющих клетках, подобных макрофагам и дендритным клеткам (Beckman et al., 1994; Beckman et al., 1995; Rosat et al. , 1995). Подобным образом было найдено, что пренилпирофосфат также представлен молекулами CD1 на антиген-представляющих клетках (Morita et al., 1995).
Липидные компоненты оболочек клеток микобактерий
Считается, что микобактериальные клеточные оболочки являются высокодифференцированной и сложной структурой, характеризуемой весьма высоким содержанием липидов, которые составляют около 60% от массы клеточной оболочки (Grange, 1988). Диаграмма, представляющая микробактериальную клеточную оболочку дана на фиг. 1.
Считается, что миколиновые кислоты, основные липиды оболочки клеток Mycobacteria (Petit and Lederer, 1984) являются главным компонентом внешнего проницаемого барьера (Wheeler et al., 1994) и ответственны за "жирно-кислотность" этой группы микроорганизмов (Grange, 1988). Присутствие большого количества миколиновых кислот, связанных с различными типами свободных липидов, составляет основу целостности микобактериальной оболочки (Besra et al., 1993).
Миколиновые кислоты встречаются в природе как смеси различных типов. Они часто образуют эфиры с карбогидратами, например с арабинозой, образуя главный частокол клеточной оболочки, и с трегалозой, образуя димиколилтрегалозу, так называемый "корд-фактор", который ассоциируется с вирулентностью М.tuberculosis. Миколиновые кислоты обнаружены в бактериальных видах, отличных от Mycobacterium, т.е. в Coryne-bacterium и в Nocardia (Goren, 1972). Следовательно, различают три основные группы миколиновых кислот (The Merck Index 1989), а именно:
i) кориномиколиновые кислоты (с длиной ацильной цепи C28-C40),
ii) нокардомиколиновые кислоты (с длиной ацильной цепи C40-C60),
iii) микобактериальные миколиновые кислоты (с длиной ацильной цепи C60-C90).
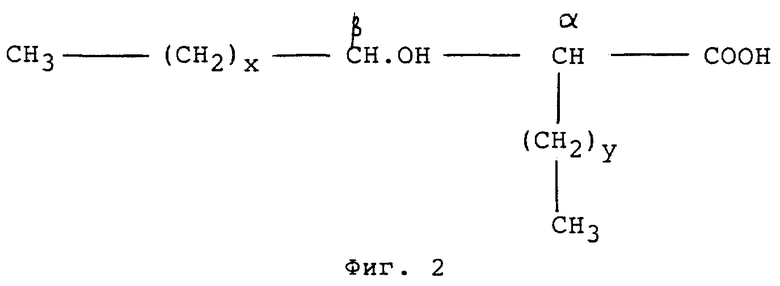
Миколиновые кислоты являются бета-гидрокси жирными кислотами с большой молекулярной массой, которые имеют умеренно длинные алифатические цепи в альфа-положении. Общая формула миколиновых кислот показана на фиг. 2.
Все известные миколиновые кислоты имеют базовую структуру R2CH(OH)CHR1COOH, где R1 - линейный алкан C20-C24 и R2 является более сложной структурой, имеющей от 30 до 60 атомов углерода, которая может содержать различное число двойных связей углерод-углерод и/или циклопропановые кольца, метильные ветви или кислородные функциональные группы, такие как C= O, CH3OCH= , COOH (The Merck Index, 1989). Хотя миколиновые кислоты очень разнообразны, альфа-цепь, за исключением длины, является существенным инвариантом - постоянным признаком любой группы миколиновых кислот (Goren, 1972).
Миколиновые кислоты растворимы в очень ограниченном круге растворителей, что усложняет их очистку (Brennan and Nikaido, 1995) и приводит к утомительной и дорогостоящей процедуре. Beckmann et al. (1994), например, добились очистки миколиновых кислот от М.tuberculosis только после дериватизации пара-бромофенацилбромидом, разделения ЖХВР с обращенной фазой, сбора фракции кластера пиков миколиновых кислот, реомыления и экстракции.
Учитывая потенциальную роль, которую липидные компоненты клеточных оболочек и, в частности миколиновые кислоты, могут играть в иммунотерапии и иммунопрофилактике туберкулеза и/или его побочных эффектов, в настоящем изобретении предложен новый более эффективный метод очистки больших количеств этих соединений.
Сущность изобретения
Предметом изобретения является способ выделения и очистки специфического компонента микробной клеточной оболочки липидной или сахарной природы или его производного, или его аналога из экстрагированной смеси компонента клеточной оболочки или его производного, или его аналога и примесей или из синтетической смеси компонента клеточной оболочки, или его аналога и примесей, включающий стадии:
растворения экстрагированной смеси или синтетической смеси в двухфазном растворителе для получения раствора;
разделения раствора на верхнюю фазу и нижнюю фазу;
обработки фаз противоточной распределительной (ПТР) сепарацией, включающей число циклов, необходимое для того, чтобы выделить компонент микробной клеточной оболочки или его аналог, или его производное в верхнюю фазу или в нижнюю фазу;
удаления выделенного компонента микробной клеточной оболочки или его аналога или его производного из верхней фазы или из нижней фазы.
Специфический компонент клеточной оболочки или его производное, или его аналог может являться липидом или сахаром.
Специфический компонент клеточной оболочки или его производное, или его аналог, предпочтительно, является липидом.
Более предпочтительно, липид является жирной кислотой.
Более предпочтительно, липид является миколиновой кислотой.
Еще более предпочтительно, компонент клеточной оболочки является группой компонентов или их аналогов, или их производных и группа является смесью миколиновых кислот или их производных, или их аналогов.
Компонент микробной клеточной оболочки может быть извлечен из бактерий, грибов или дрожжей.
Компонент микробной клеточной оболочки, предпочтительно, извлечен из бактерий, которые могут быть выбраны из Mycobac-teria, Corynebacteria, Nocardia, Rhodococci, Amycolata и других подобных бактериальных видов.
Когда бактерии выбраны из Mycobacteria, они могут быть выбраны из штаммов М.tuberculosis, M.avium и M.vaccae.
Двухфазная система растворителей, предпочтительно, включает хлороформ, метанол и воду.
Двухфазная система растворителей, предпочтительно, включает верхнюю жидкую фазу и нижнюю жидкую фазу.
Способ, предпочтительно, включает также стадии перемешивания и доведения до равновесия верхней и нижней фаз системы растворителей.
Предпочтительно, состав верхней фазы 12-18% хлороформа, 45-55% метанола и 25-40% воды. Более предпочтительно, состав верхней фазы 15% хлороформа, 52% метанола и 33% воды.
Предпочтительно, состав нижней фазы 50-80% хлороформа, 15-40% метанола и 2-8% воды. Более предпочтительно, состав нижней фазы 68% хлороформа, 27% метанола и 5% воды.
Жидкостно-жидкостная экстракция может быть противоточной экстракцией или многократной экстракцией одной из фаз.
Очищенный компонент клеточной оболочки или его аналог, или его производные могут быть подвергнуты экстракции ацетоном для удаления примесей.
Предпочтительно, компонент клеточной оболочки или его аналог, или его производное не нуждается в химической дериватизации для его отделения от любых загрязнений, которые могут появиться при росте микробов в среде для роста микробов или в синтетической смеси.
Очищенный компонент клеточной оболочки или его производное, или его аналог может быть омылен, чтобы устранить любую его этерификацию метилом.
Краткое описание рисунков
Изобретение будет теперь описано более подробно только путем примеров со ссылками на прилагаемые рисунки, где на
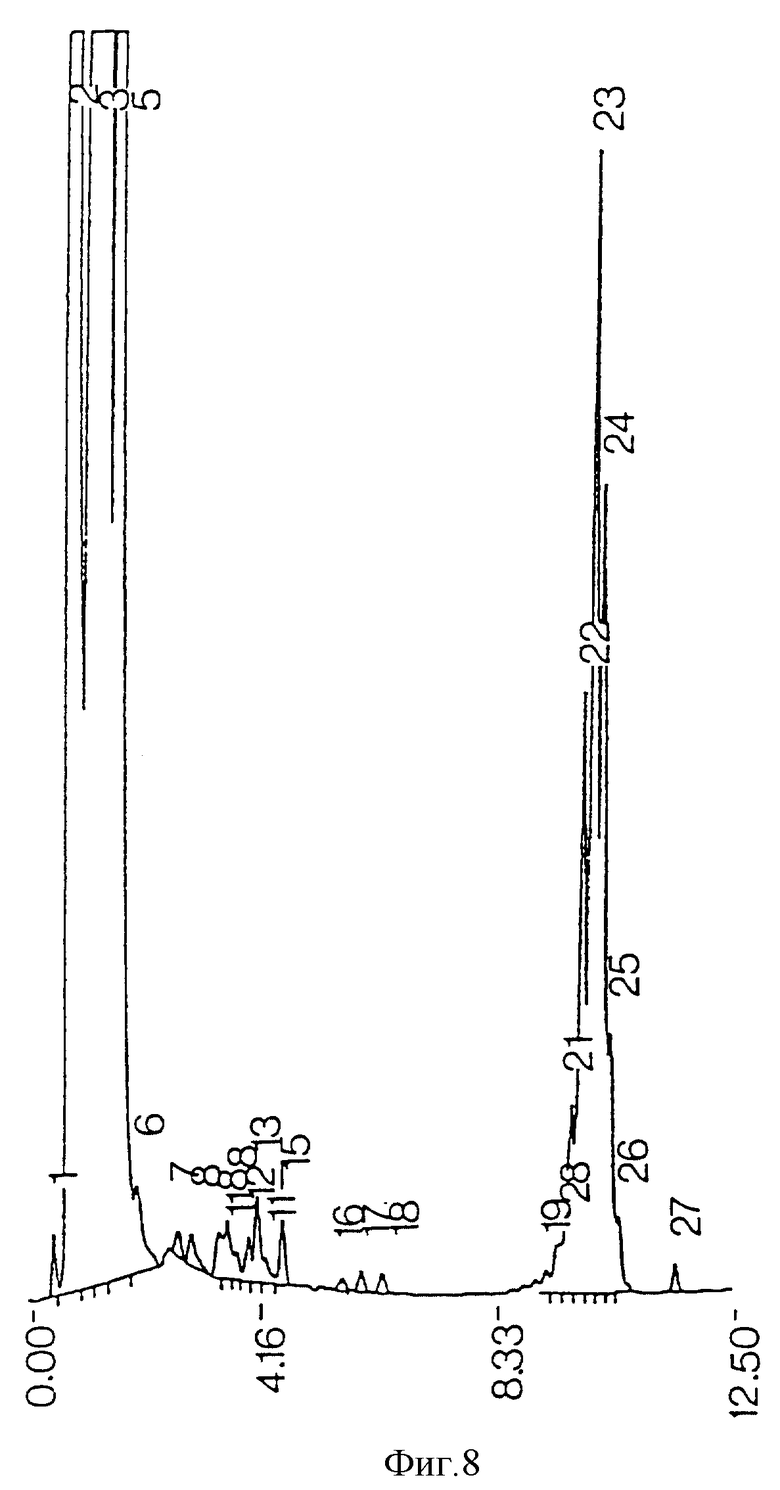
фиг. 8 - ЖХВР сырого экстракта М.tuberculosis;
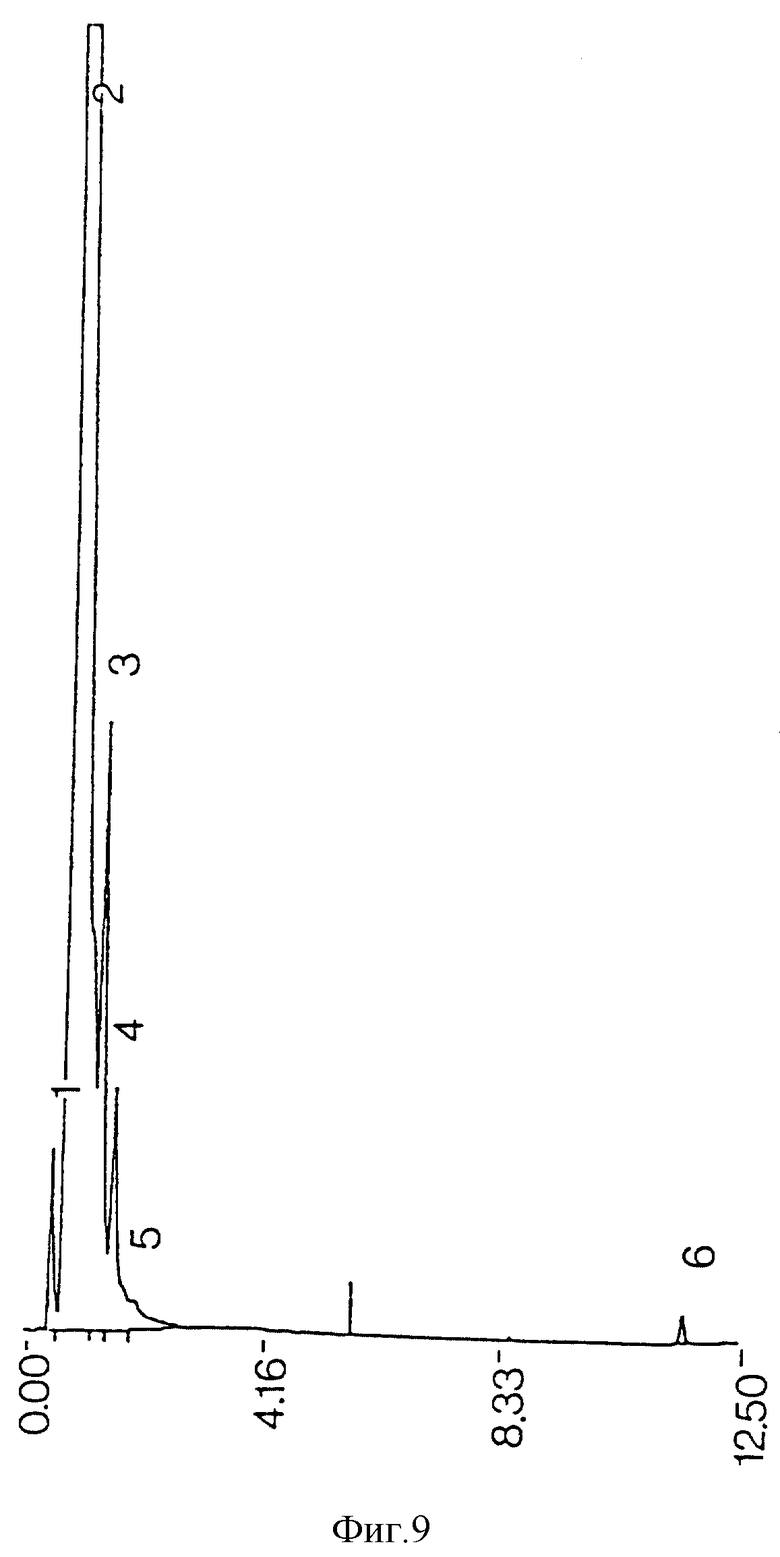
фиг. 9 - ЖХВР сырого экстракта реактивов;
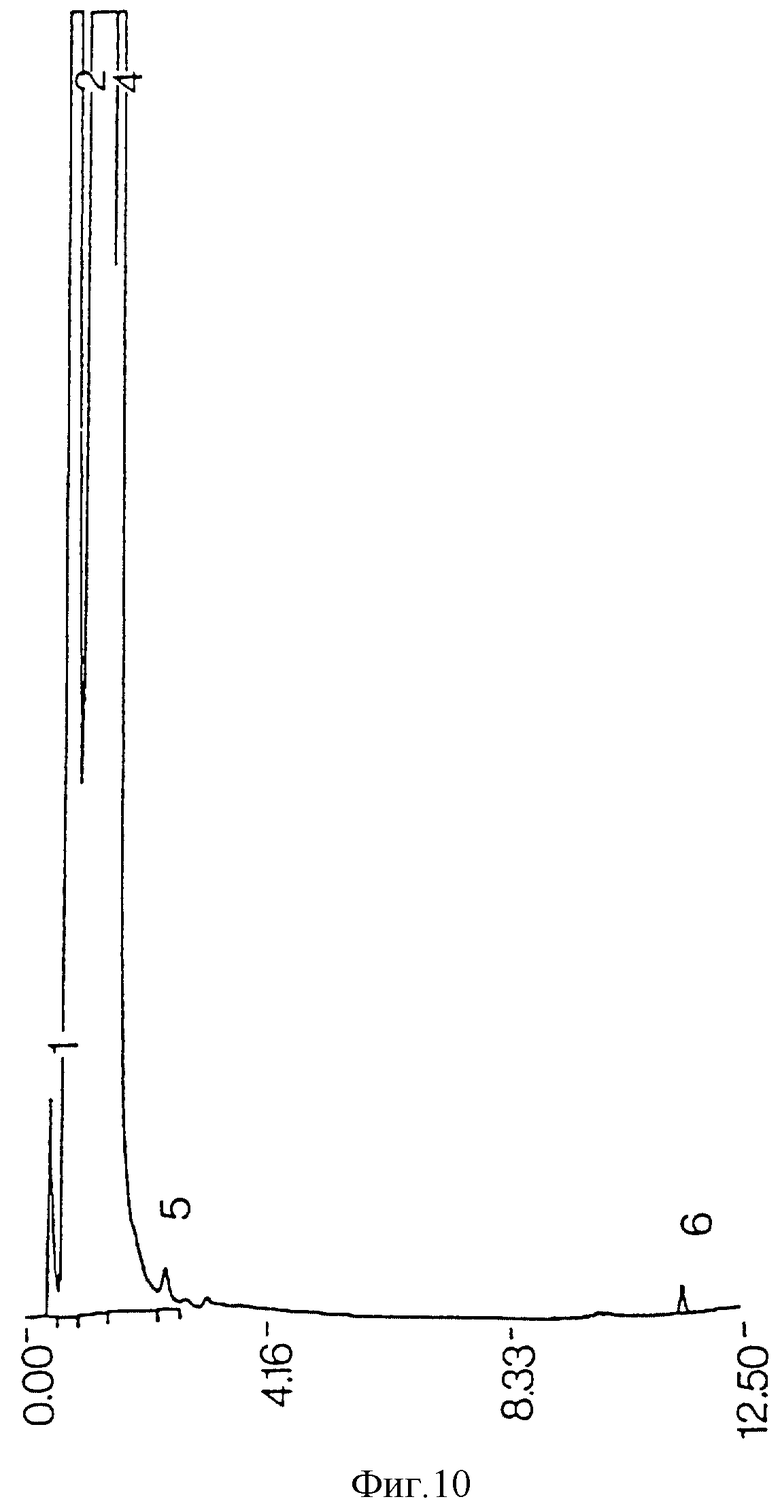
фиг. 10 - ЖХВР сырого экстракта среды;
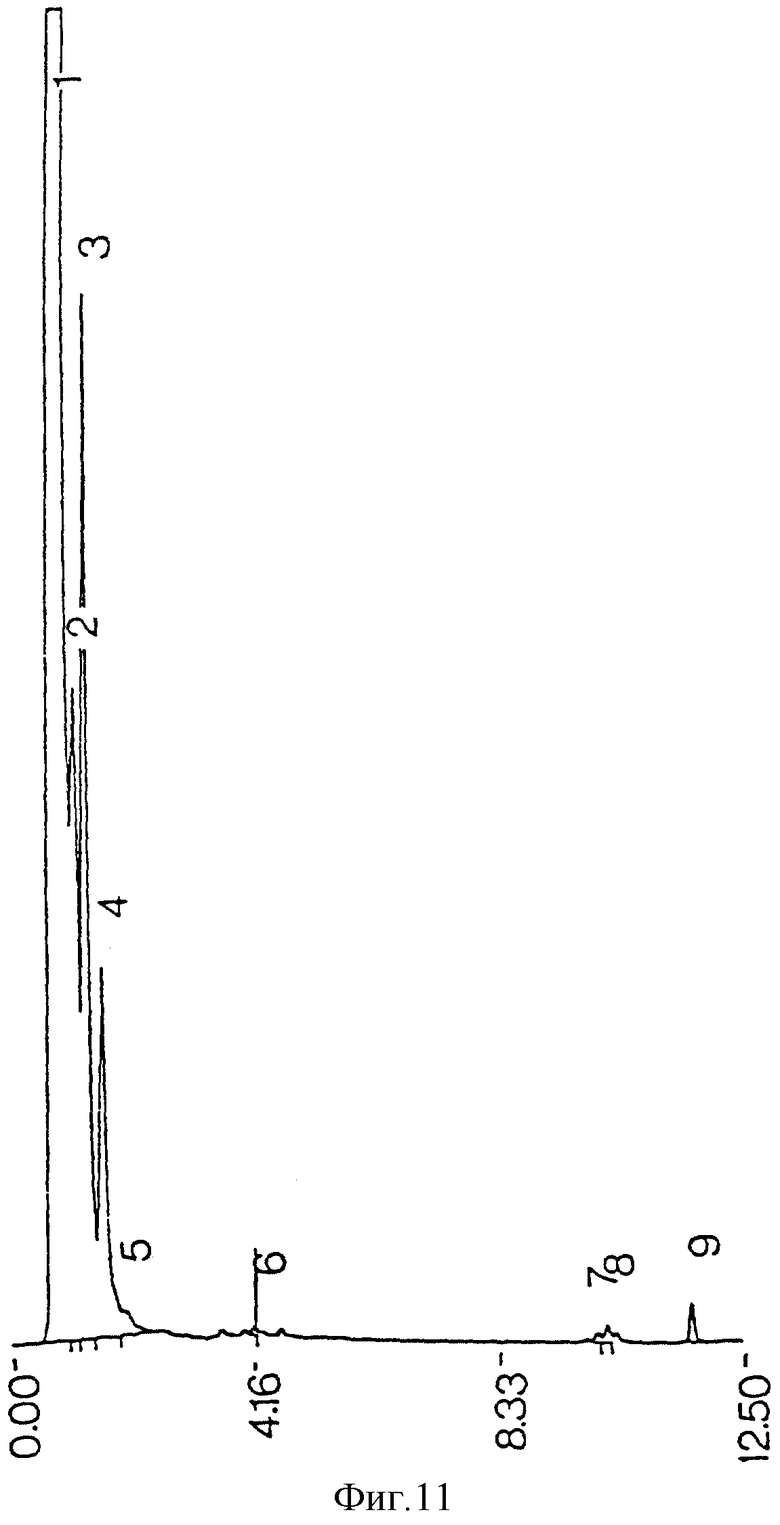
фиг. 11 - ЖХВР супернатанта сырого экстракта М. tuberculosis, экстрагированного ацетоном;
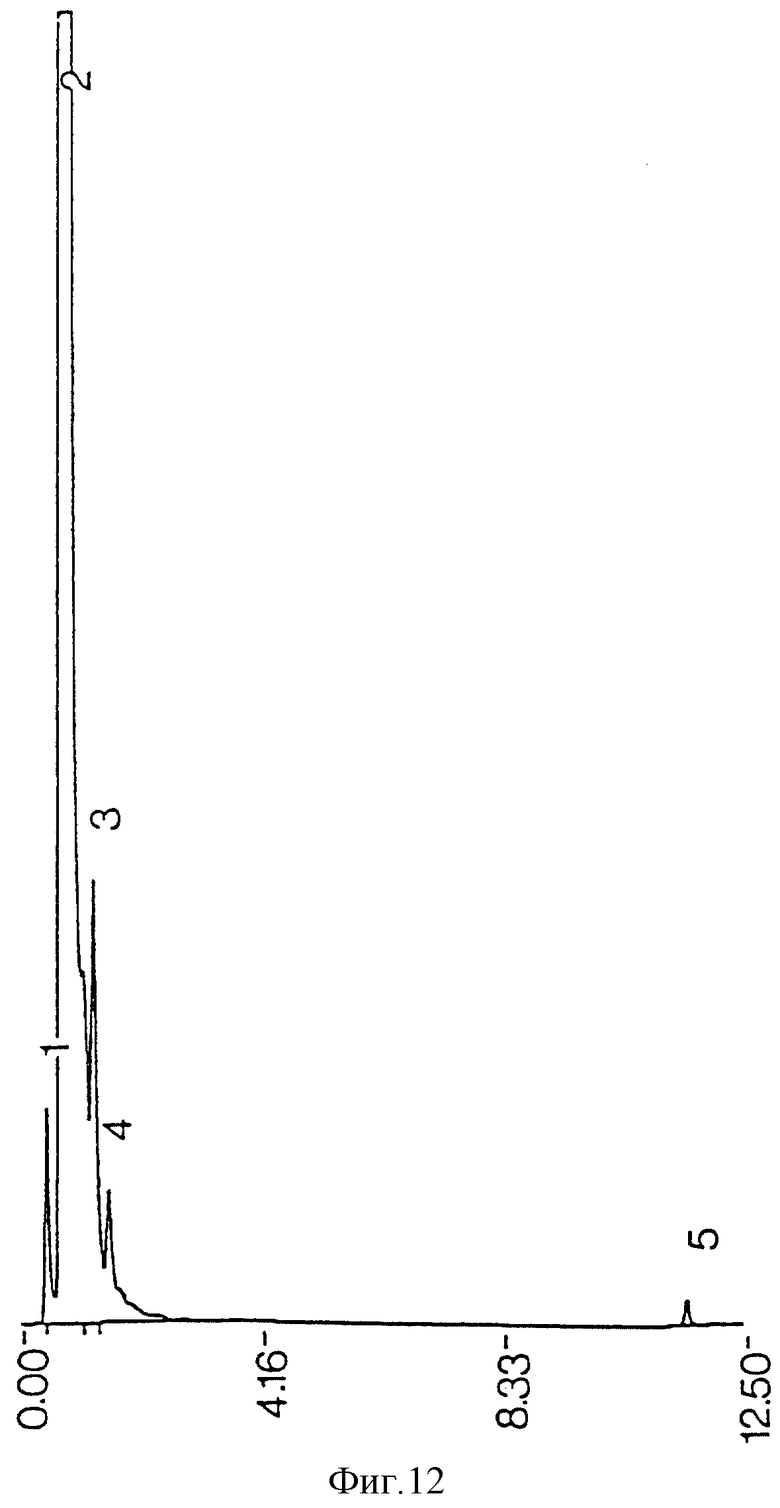
фиг. 12 - ЖХВР супернатанта сырого экстракта реактивов, экстрагированного ацетоном;
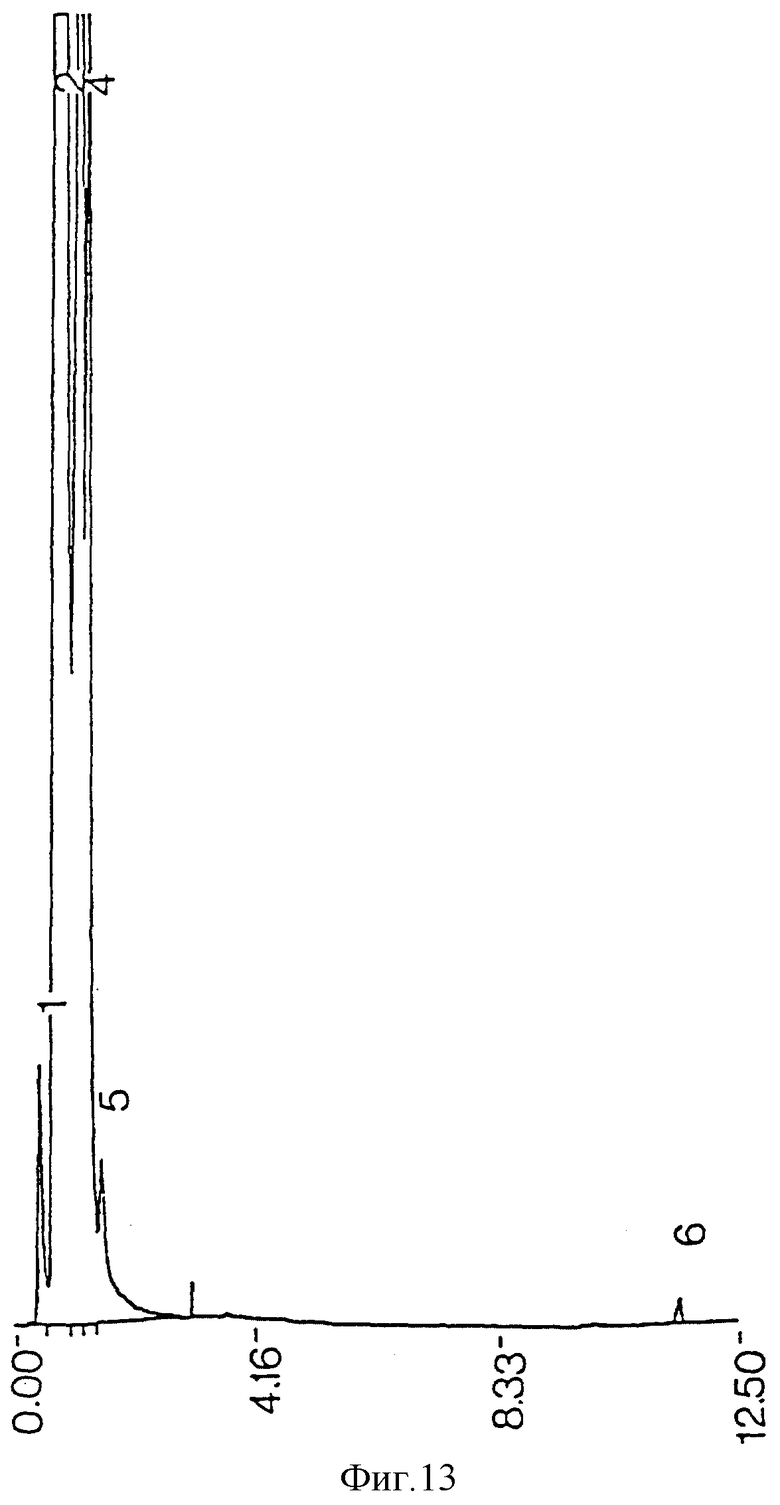
фиг. 13 - ЖХВР супернатанта сырого экстракта среды, экстрагированного ацетоном;
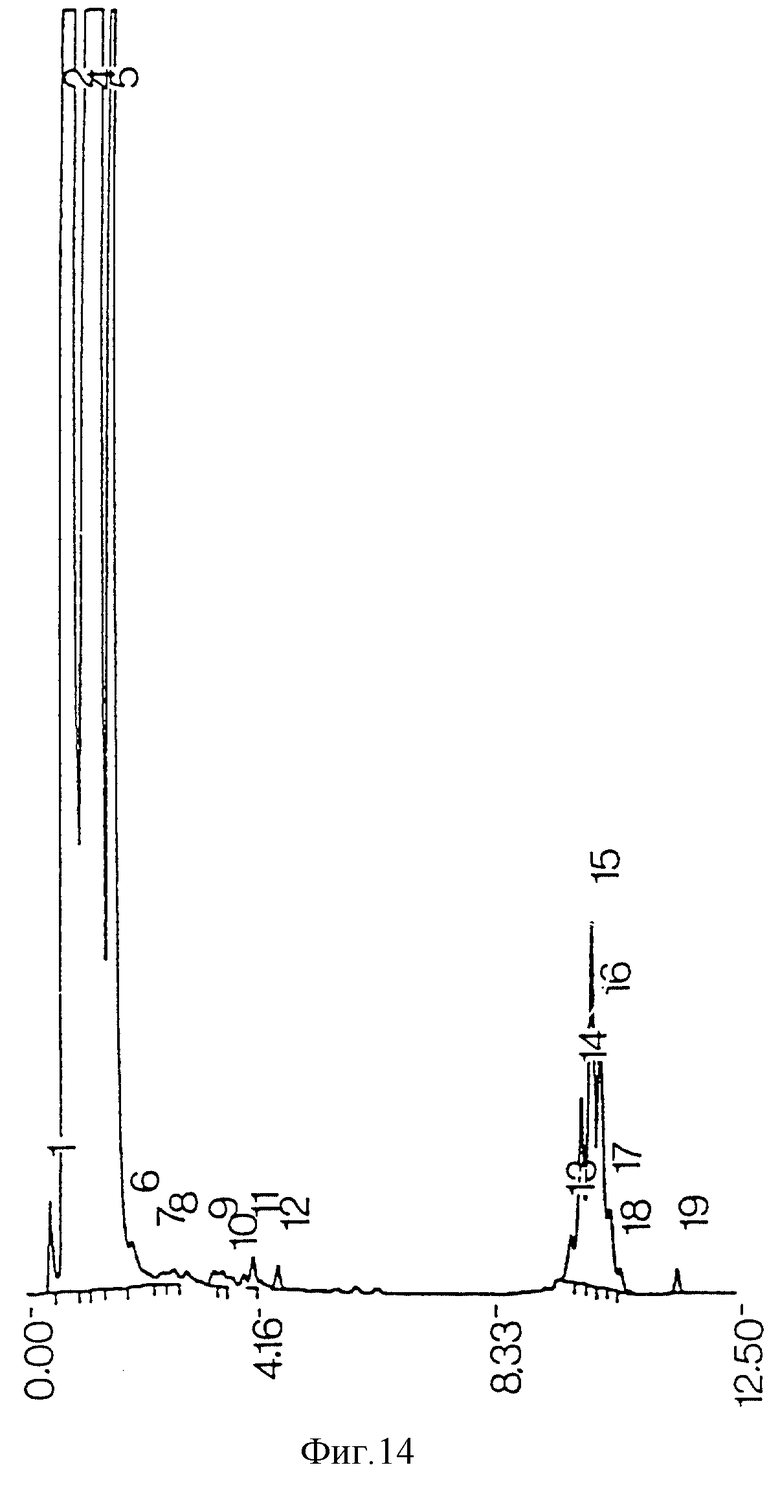
фиг. 14 - ЖХВР экстрагированного ацетоном сырого экстракта М. tuberculosis;
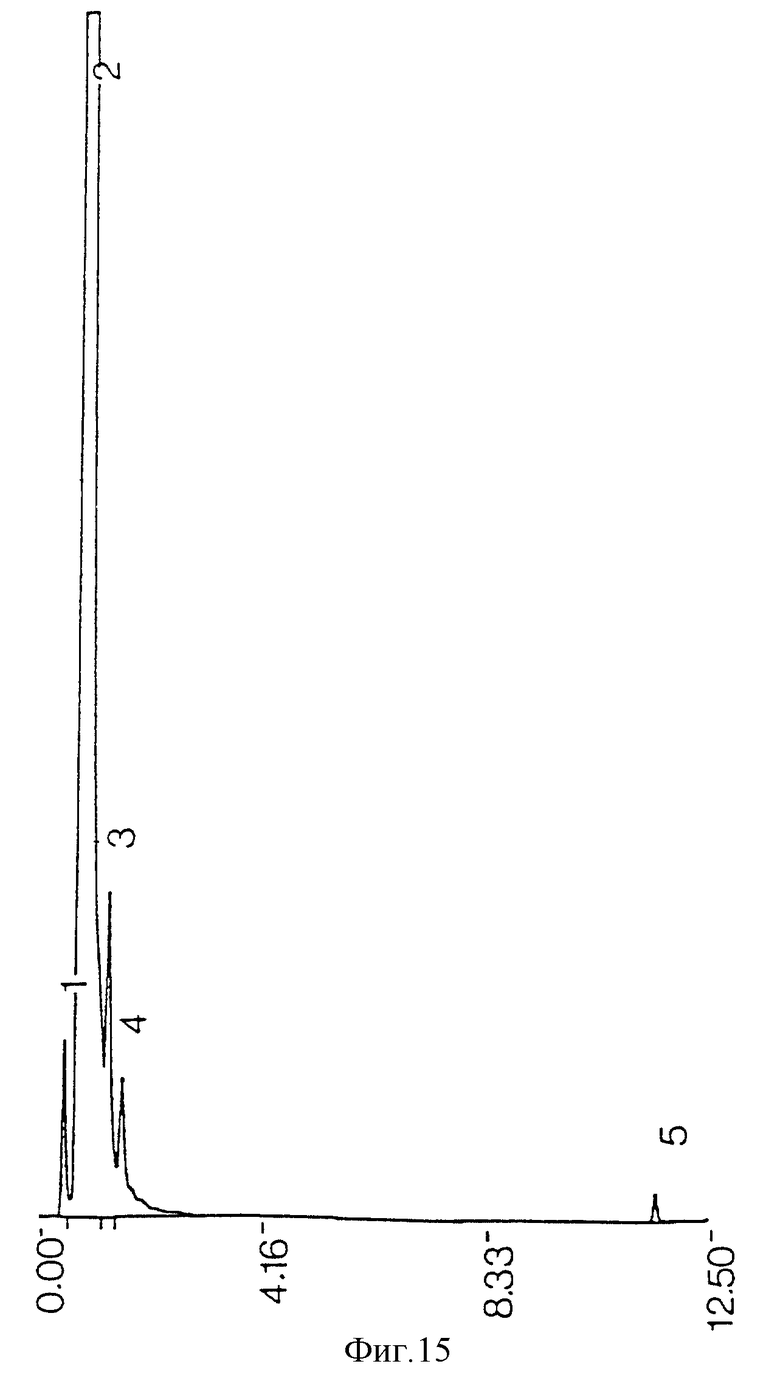
фиг. 15 - ЖХВР экстрагированного ацетоном сырого экстракта реактивов;
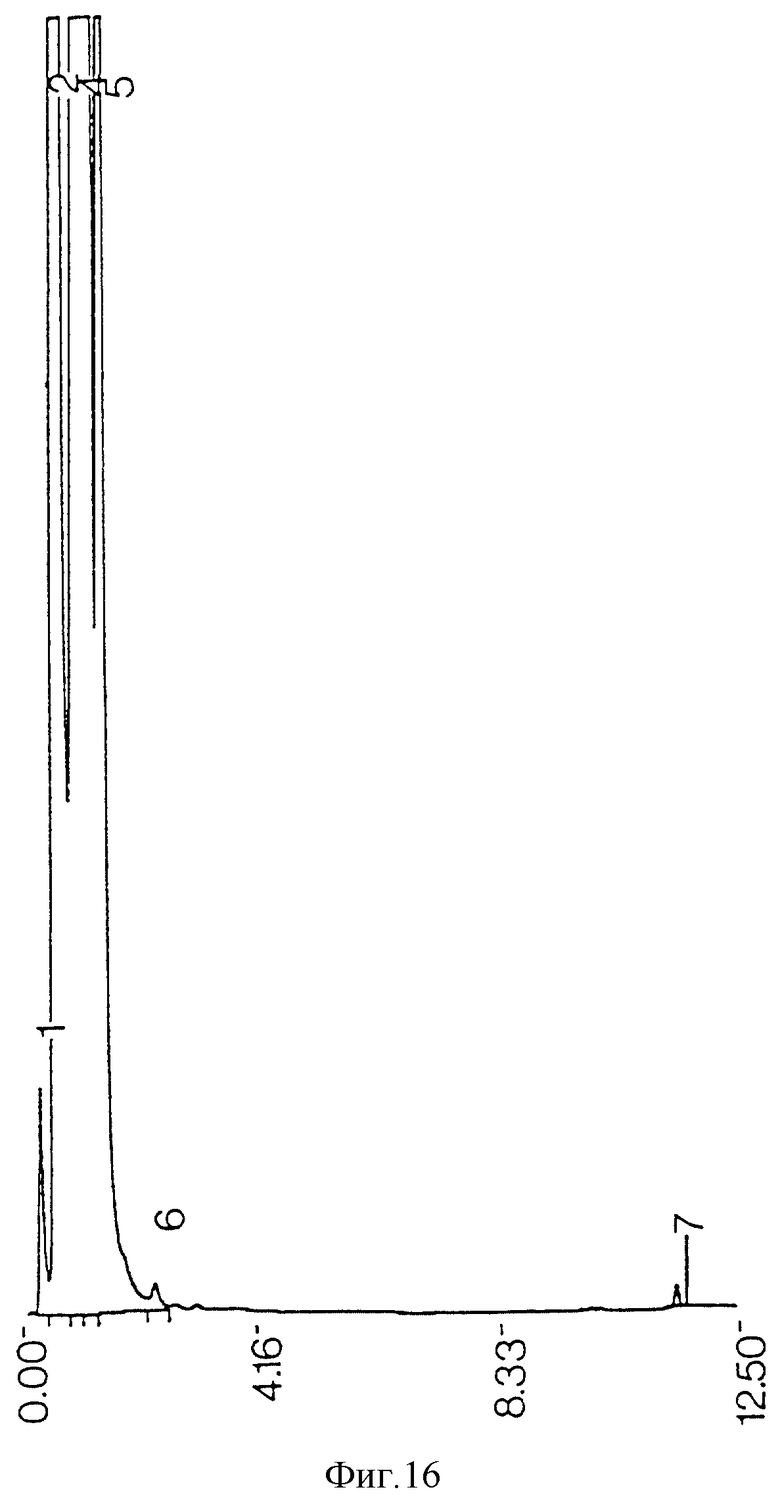
фиг. 16 - ЖХВР экстрагированного ацетоном сырого экстракта среды;
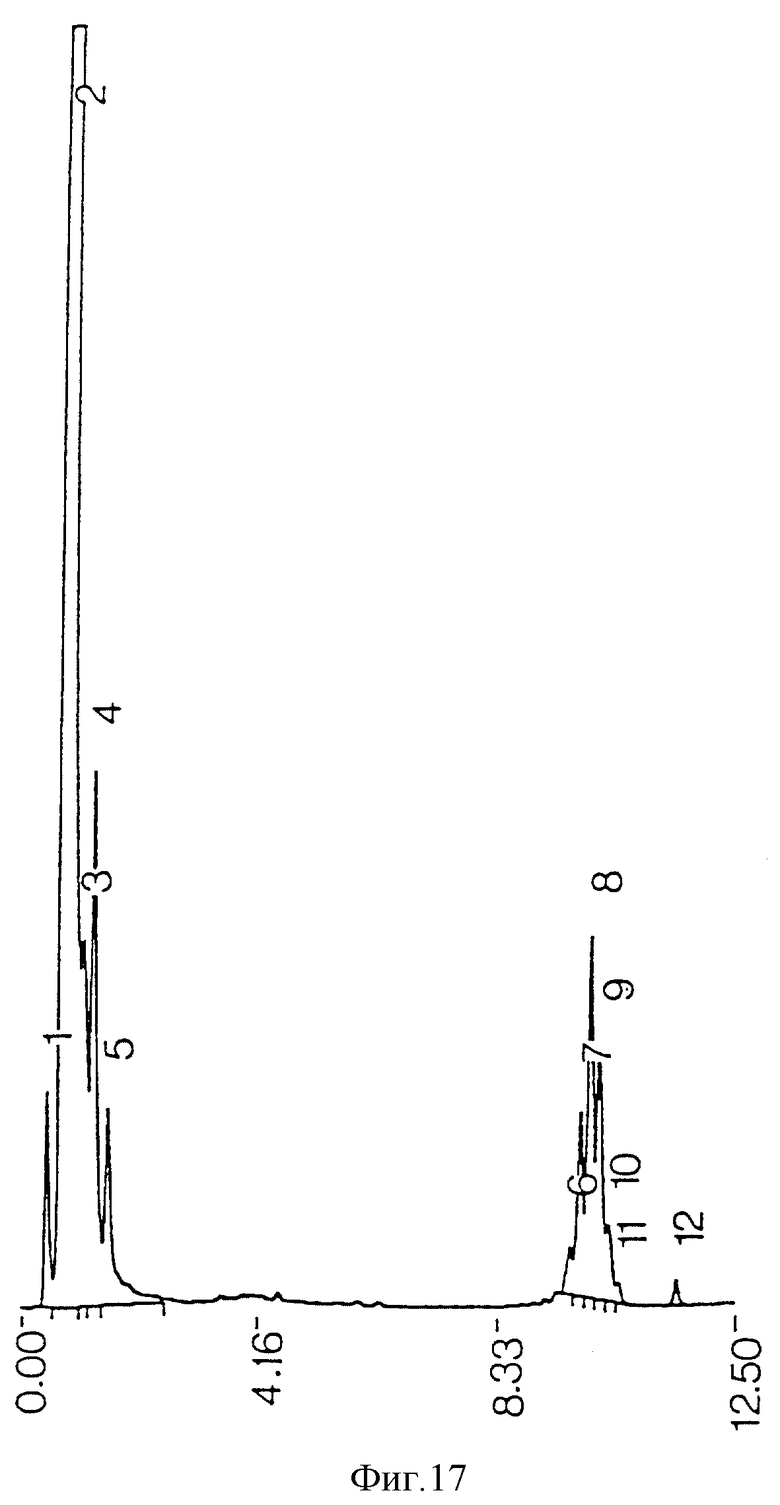
фиг. 17 - ЖХВР очищенных противотоком миколиновых кислот М.tuberculosis из экстрагированного ацетоном сырого экстракта
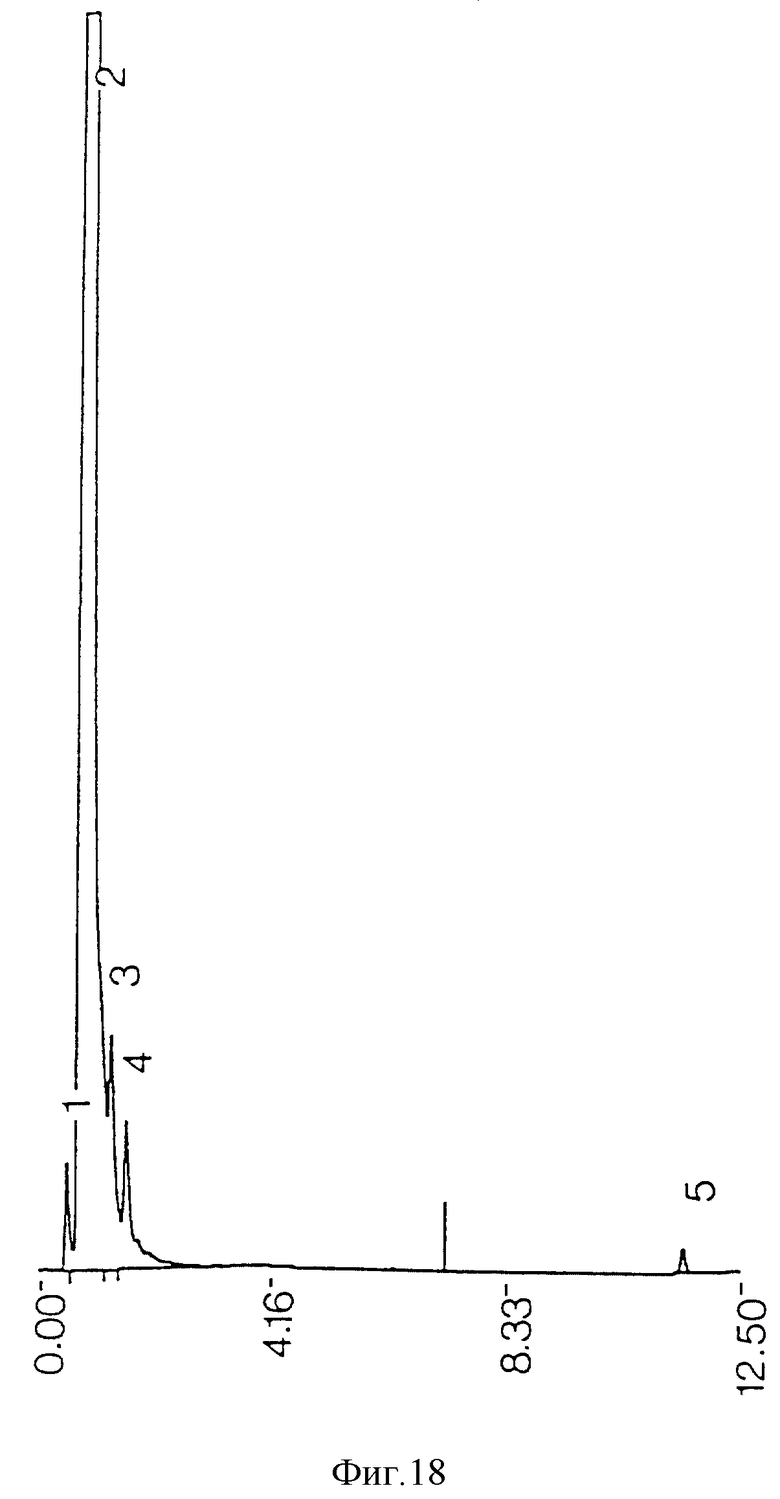
фиг. 18 - ЖХВР очищенных противотоком реактивов из экстрагированного ацетоном сырого экстракта;
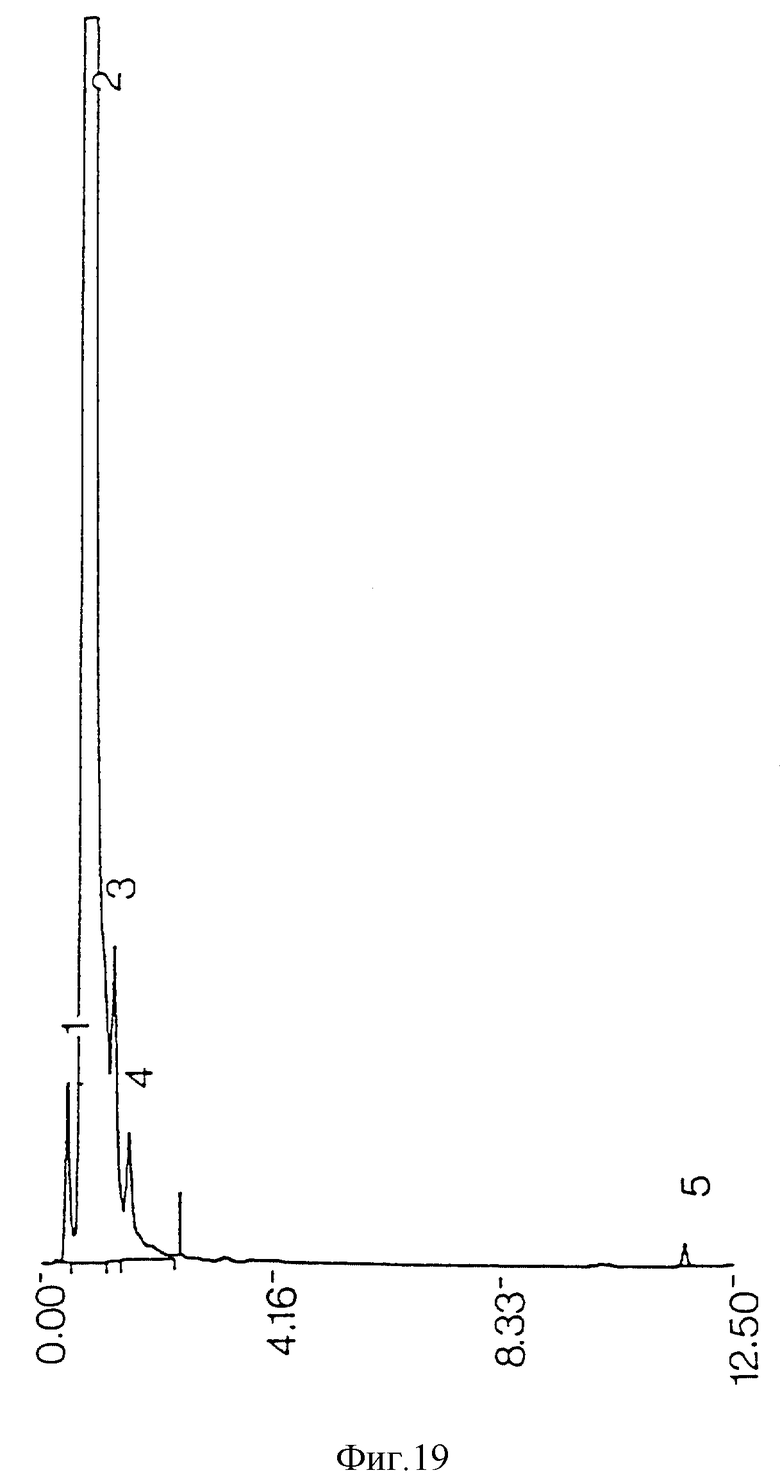
фиг. 19 - ЖХВР очищенной противотоком среды из экстрагированного ацетоном сырого экстракта;
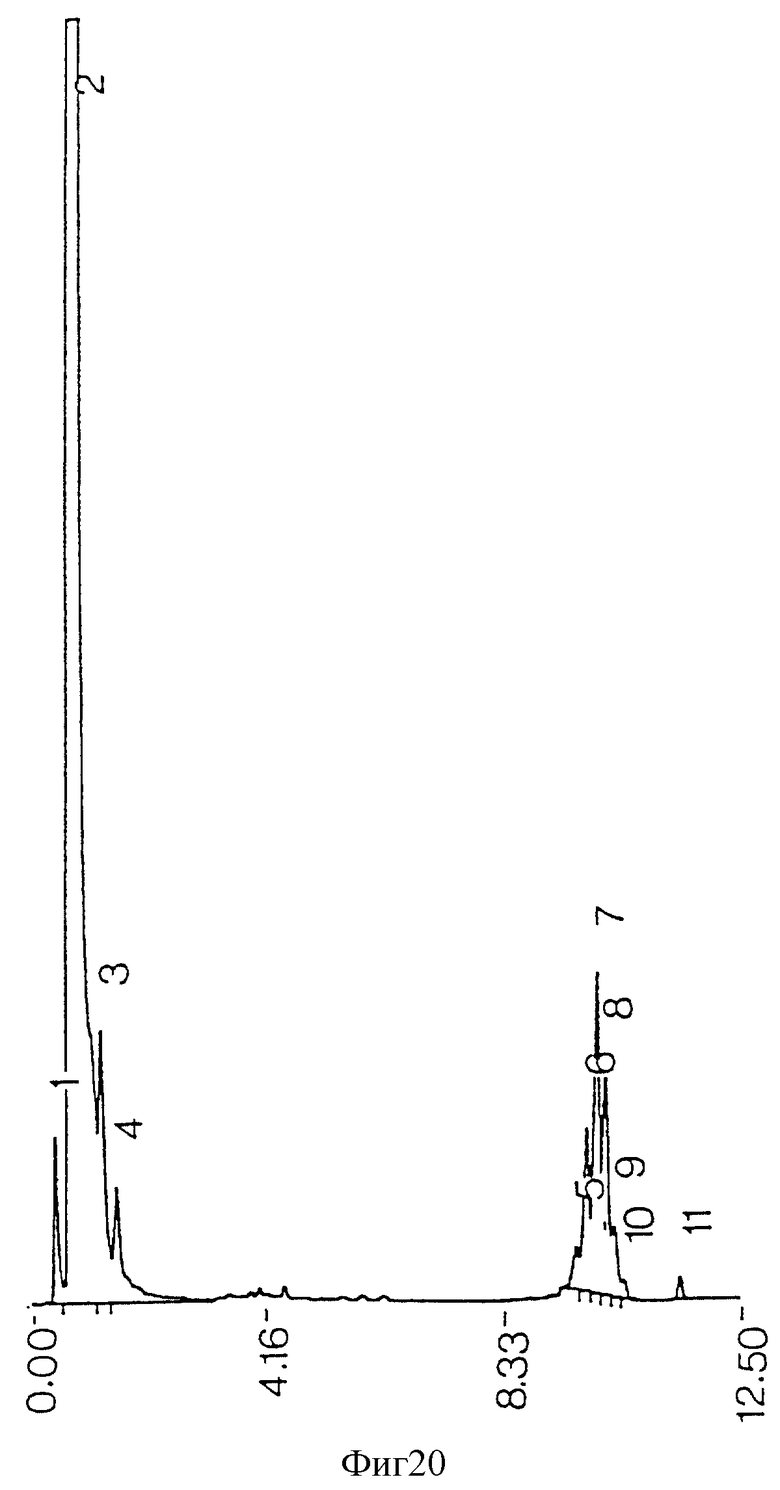
фиг. 20 - ЖХВР очищенных противотоком миколиновых кислот из сырого экстракта М.tuberculosis, не экстрагированного ацетоном;
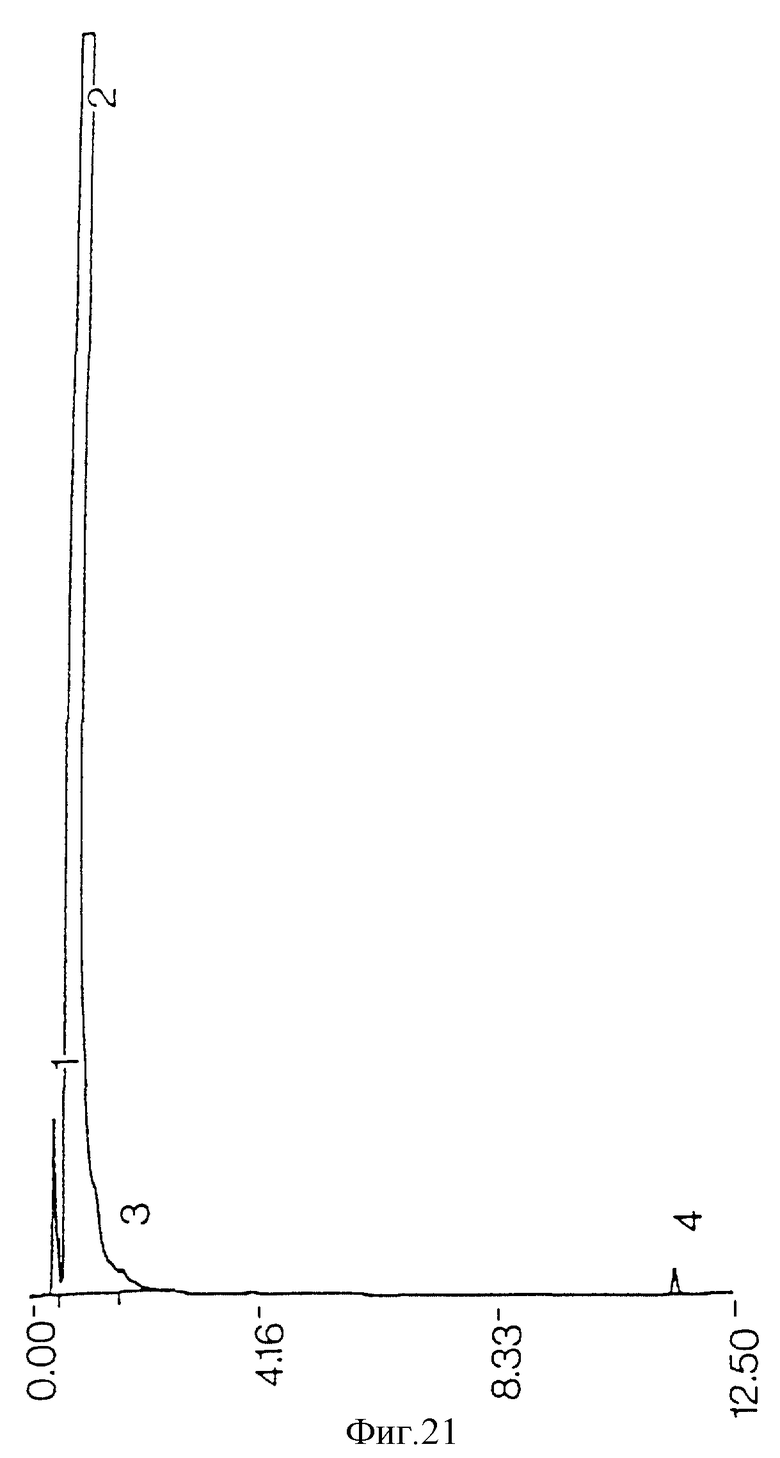
фиг. 21 - ЖХВР очищенных противотоком реактивов из сырого экстракта реактивов, не экстрагированного ацетоном;
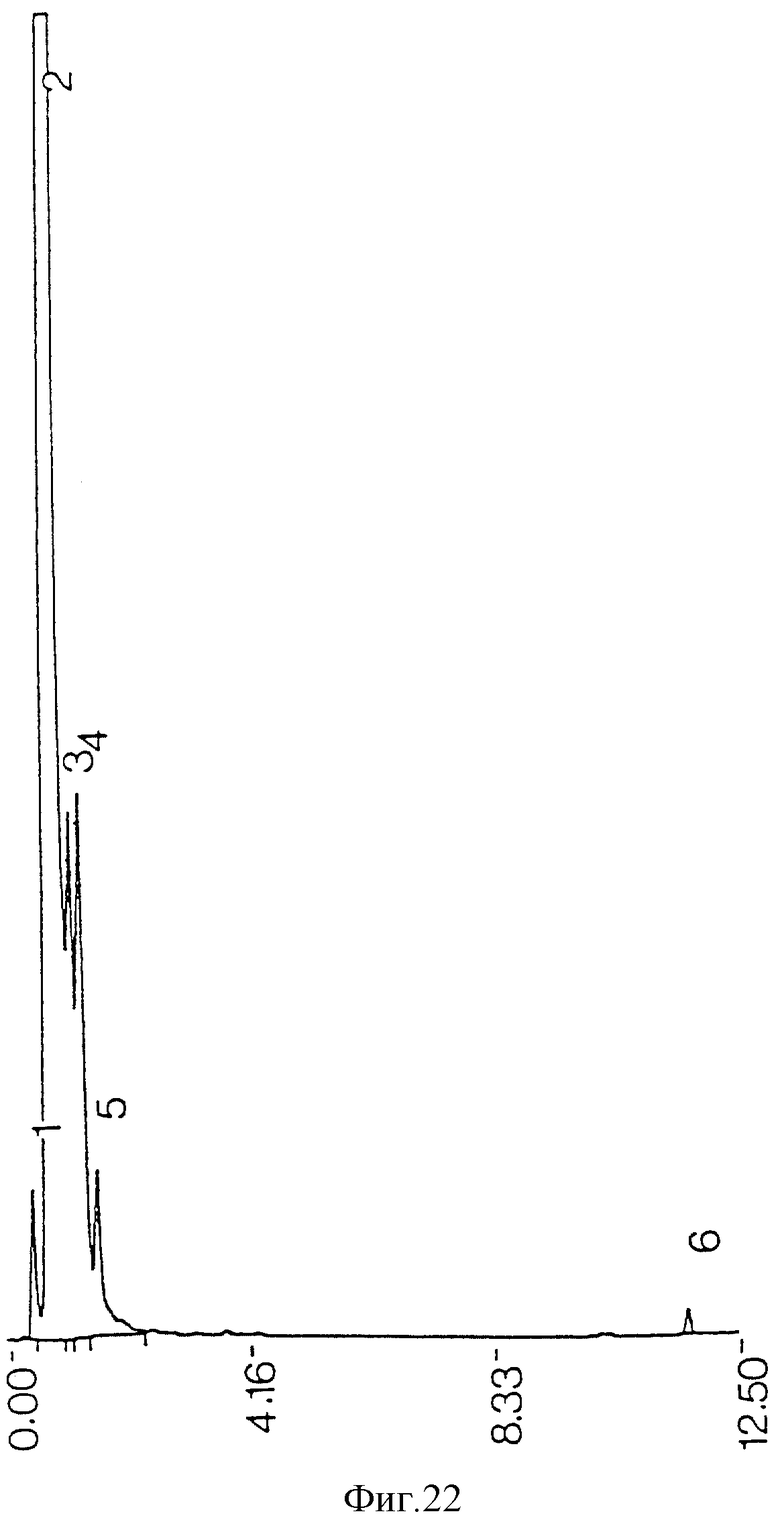
фиг. 22 - ЖХВР очищенной противотоком среды из сырого экстракта среды, не экстрагированного ацетоном;
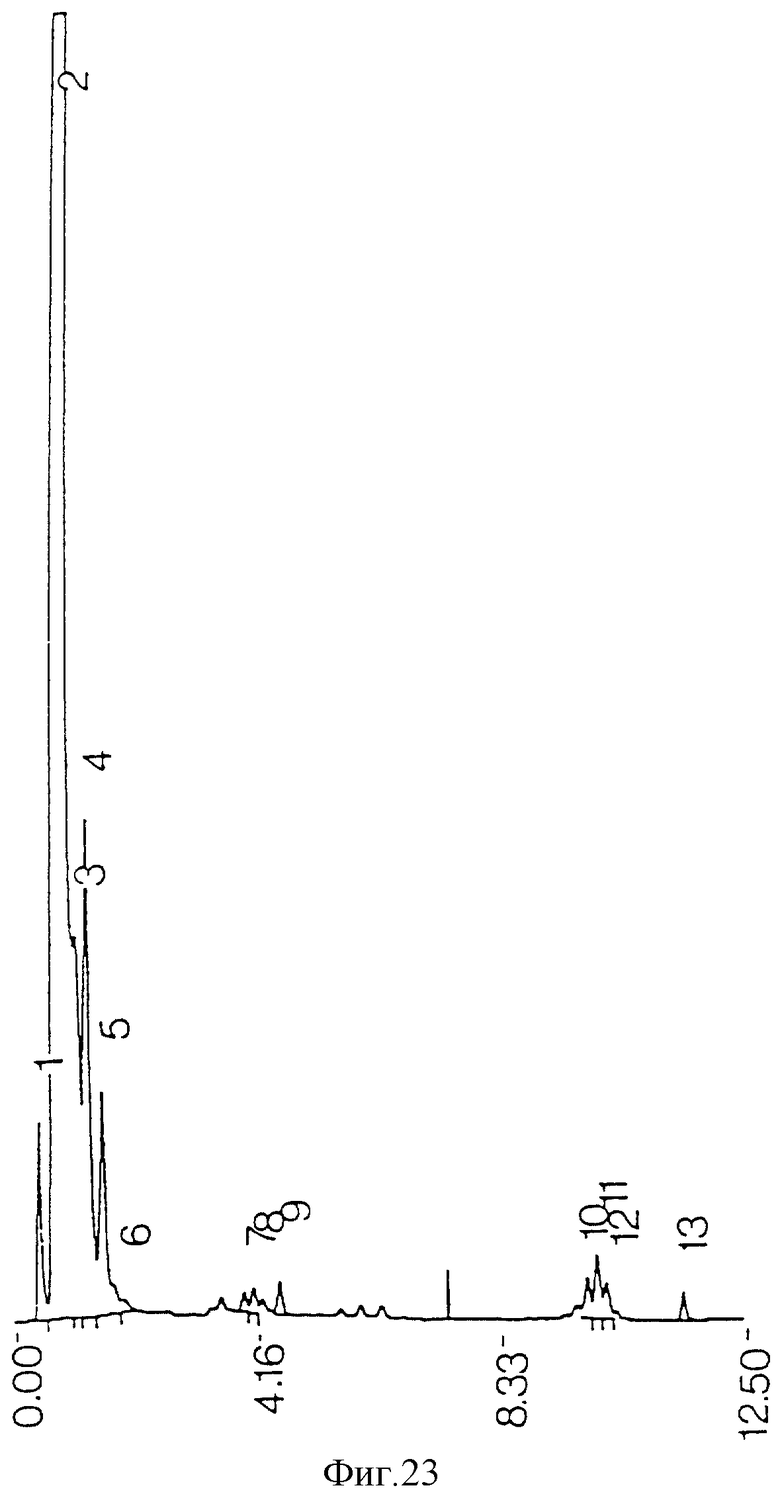
фиг. 23 - ЖХВР ацетонового супернатанта миколиновых кислот из М.tuberculosis, экстрагированного ацетоном после противоточной очистки;
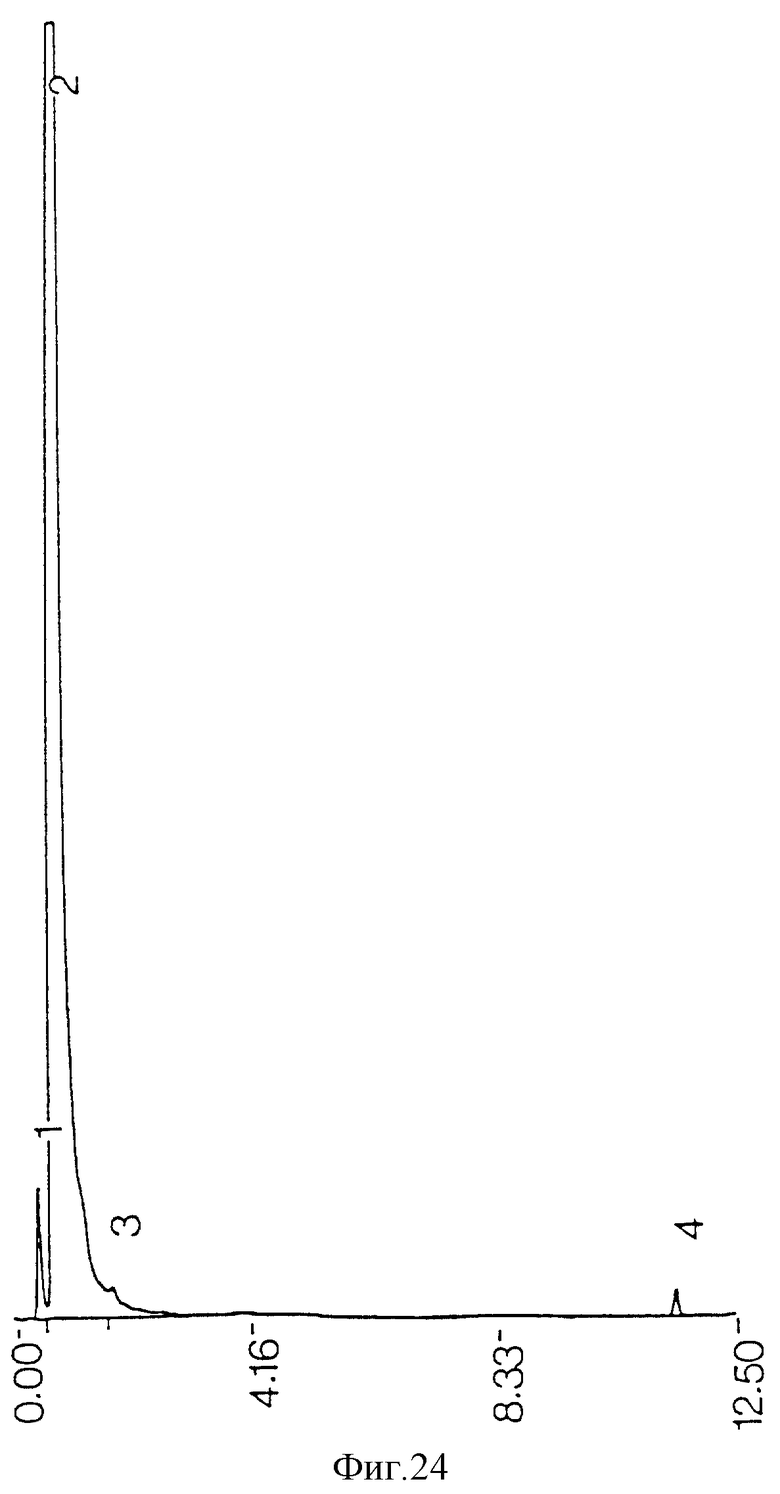
фиг. 24 - ЖХВР ацетонового супернатанта реактивов, экстрагированного ацетоном после противоточной очистки;
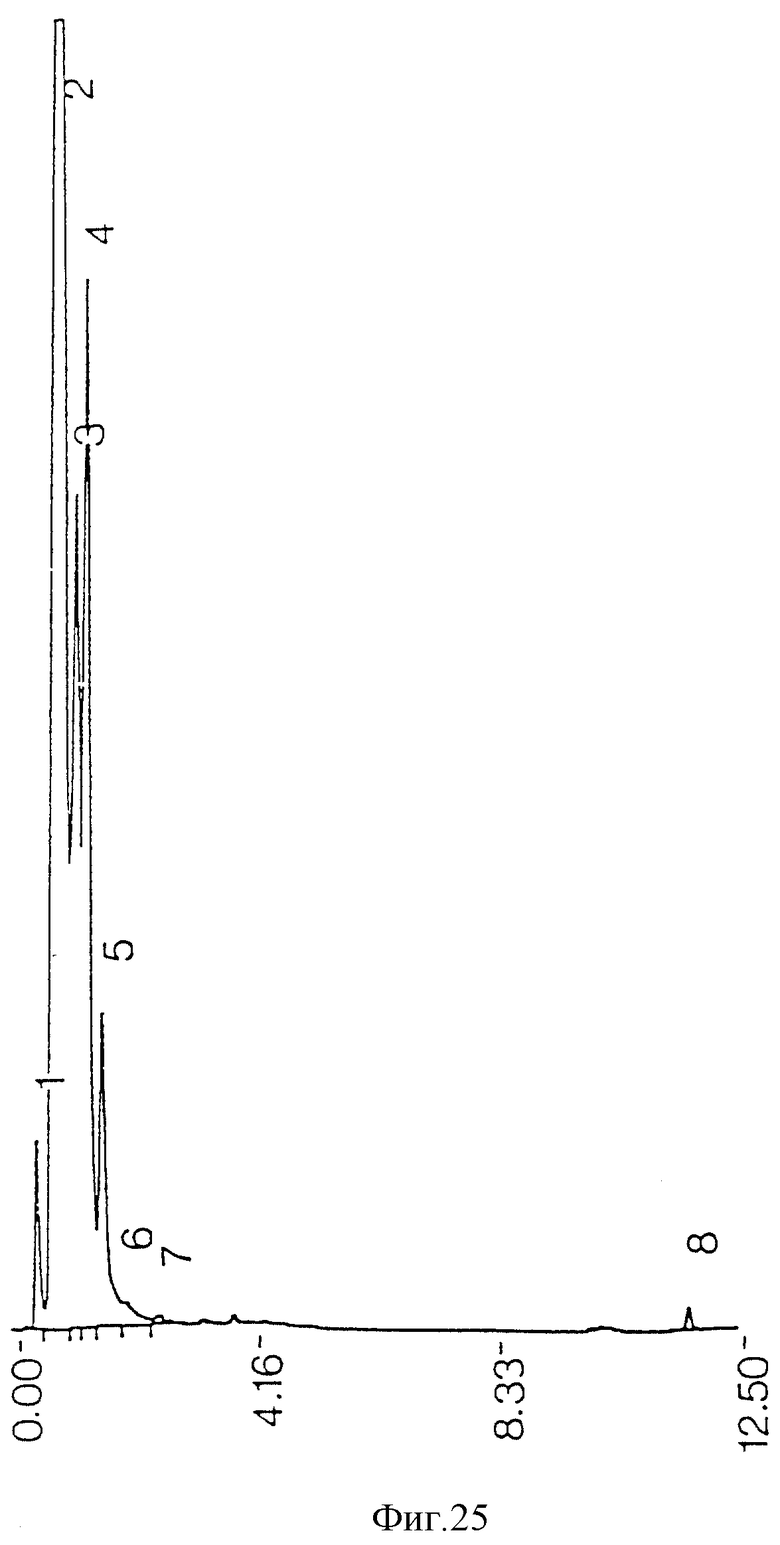
фиг. 25 - ЖХВР ацетонового супернатанта среды, экстрагированного ацетоном после противоточной очистки;
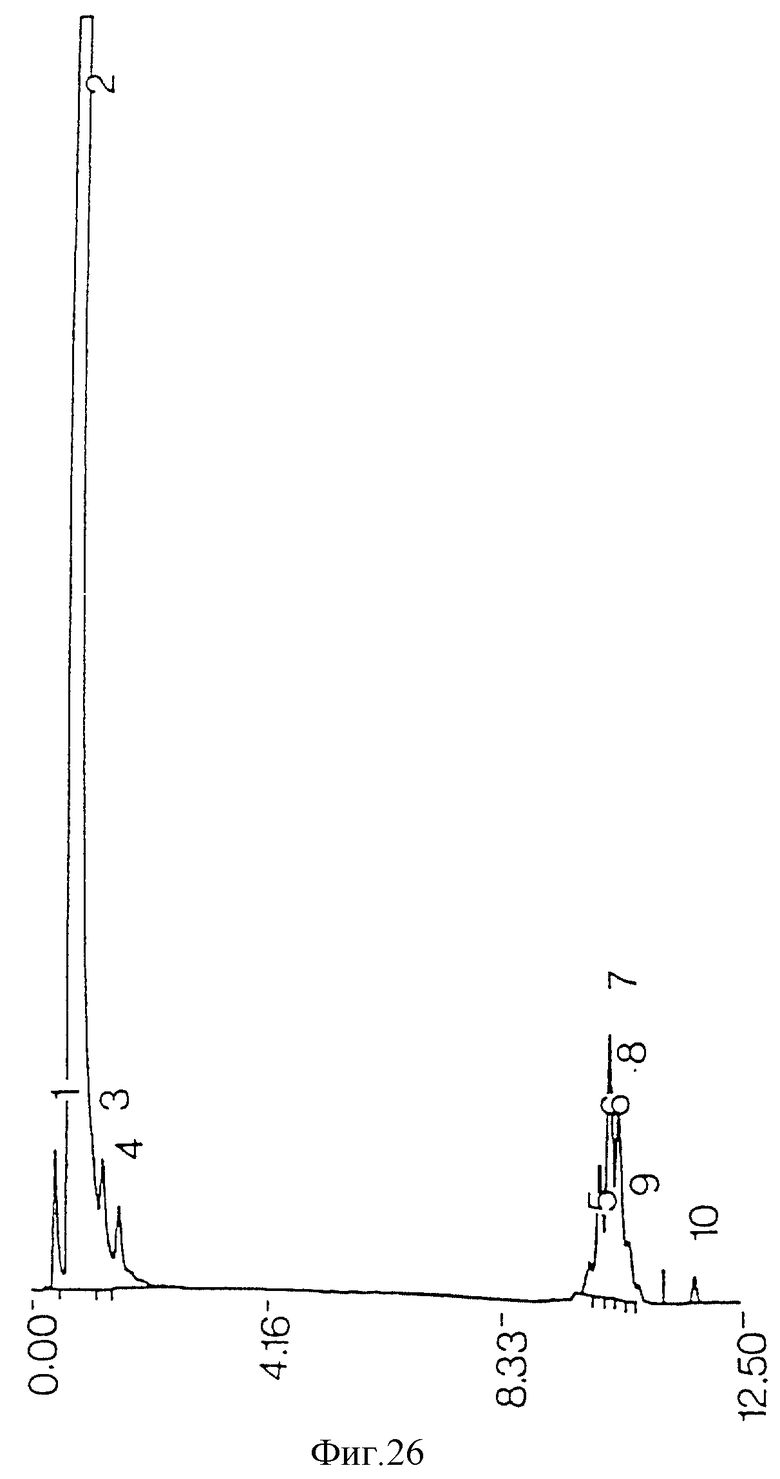
фиг. 26 - ЖХВР очищенных миколиновых кислот из М.tuberculosis, экстрагированных ацетоном после противоточной очистки;
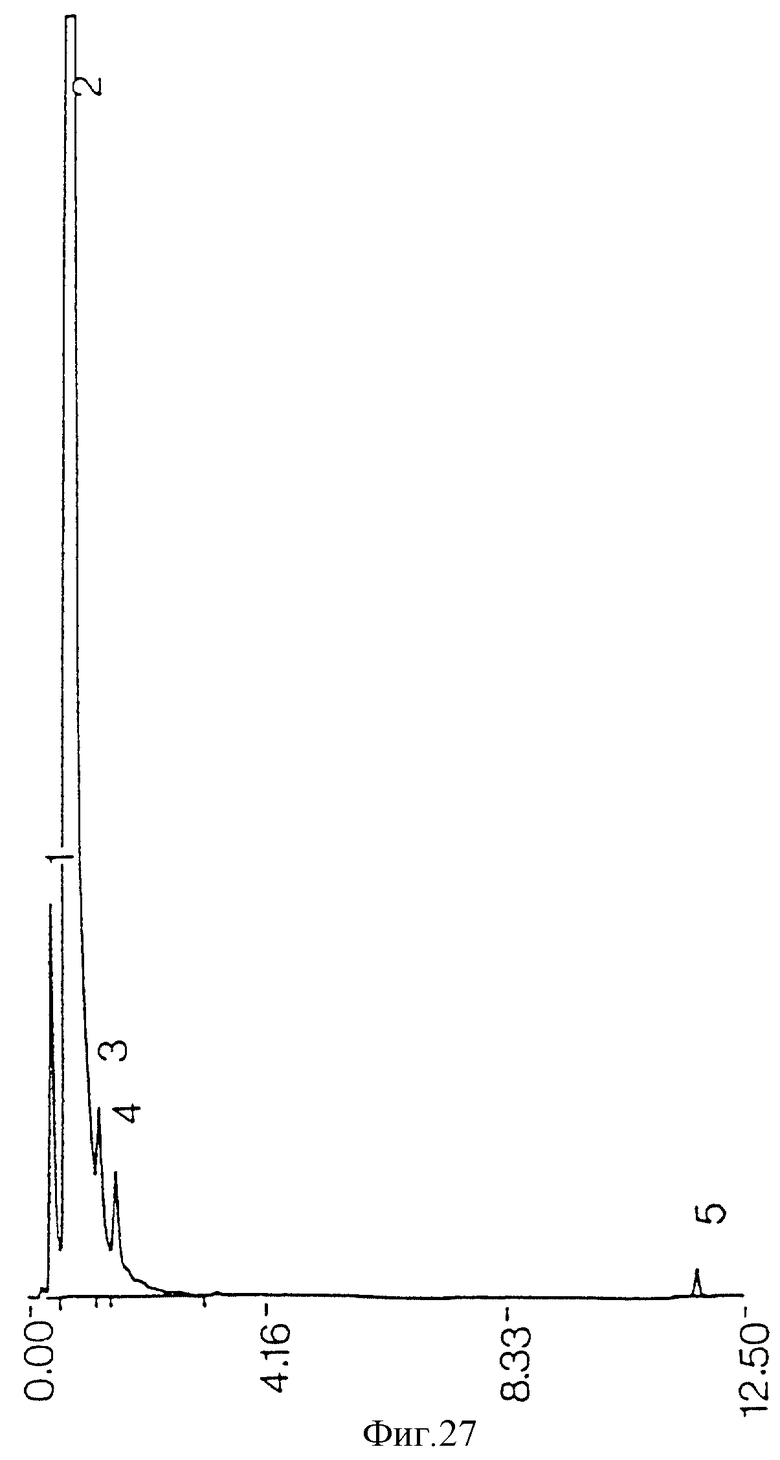
фиг. 27 - ЖХВР очищенных реактивов, экстрагированных ацетоном после противоточной очистки;
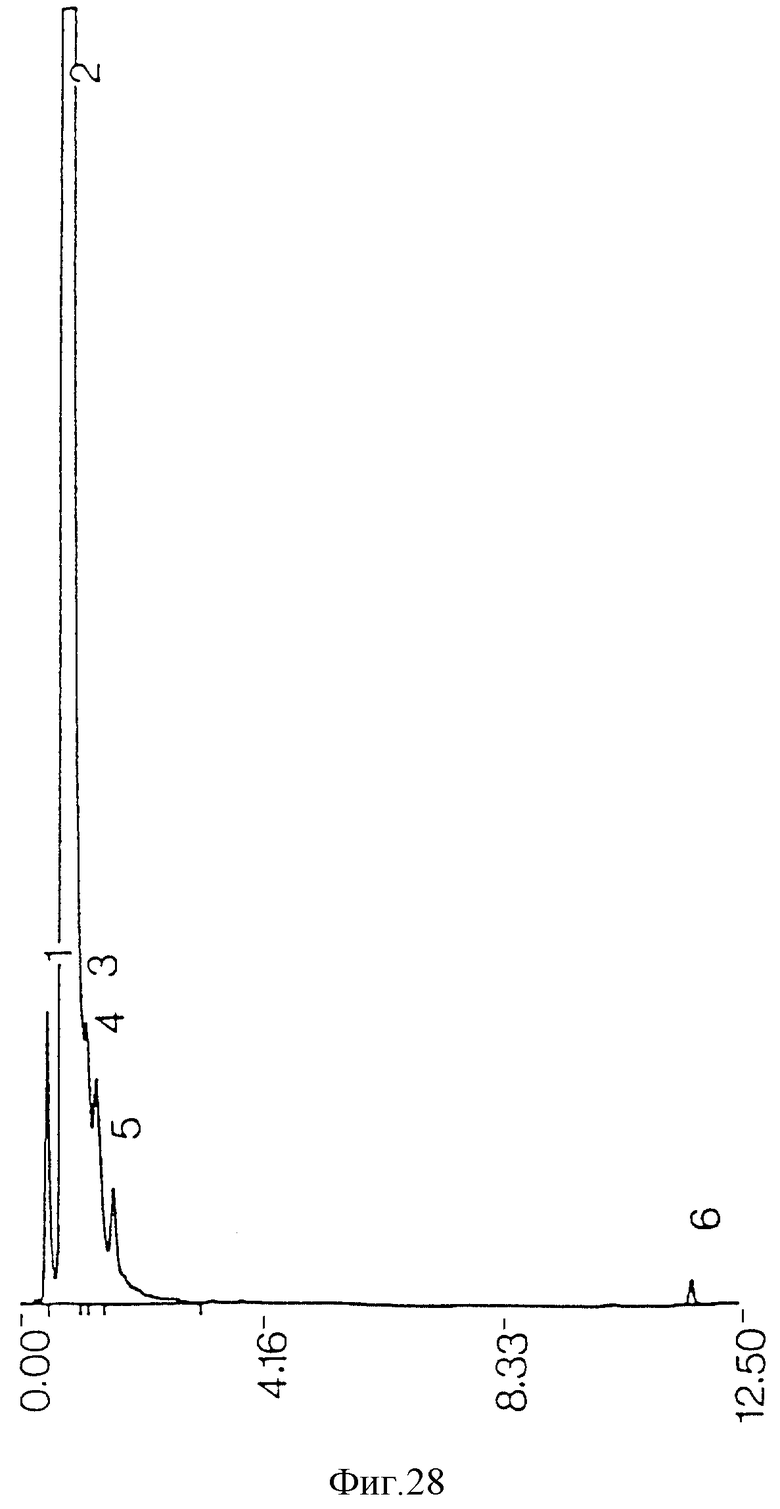
фиг. 28 - ЖХВР очищенной среды, экстрагированной ацетоном после противоточной очистки;
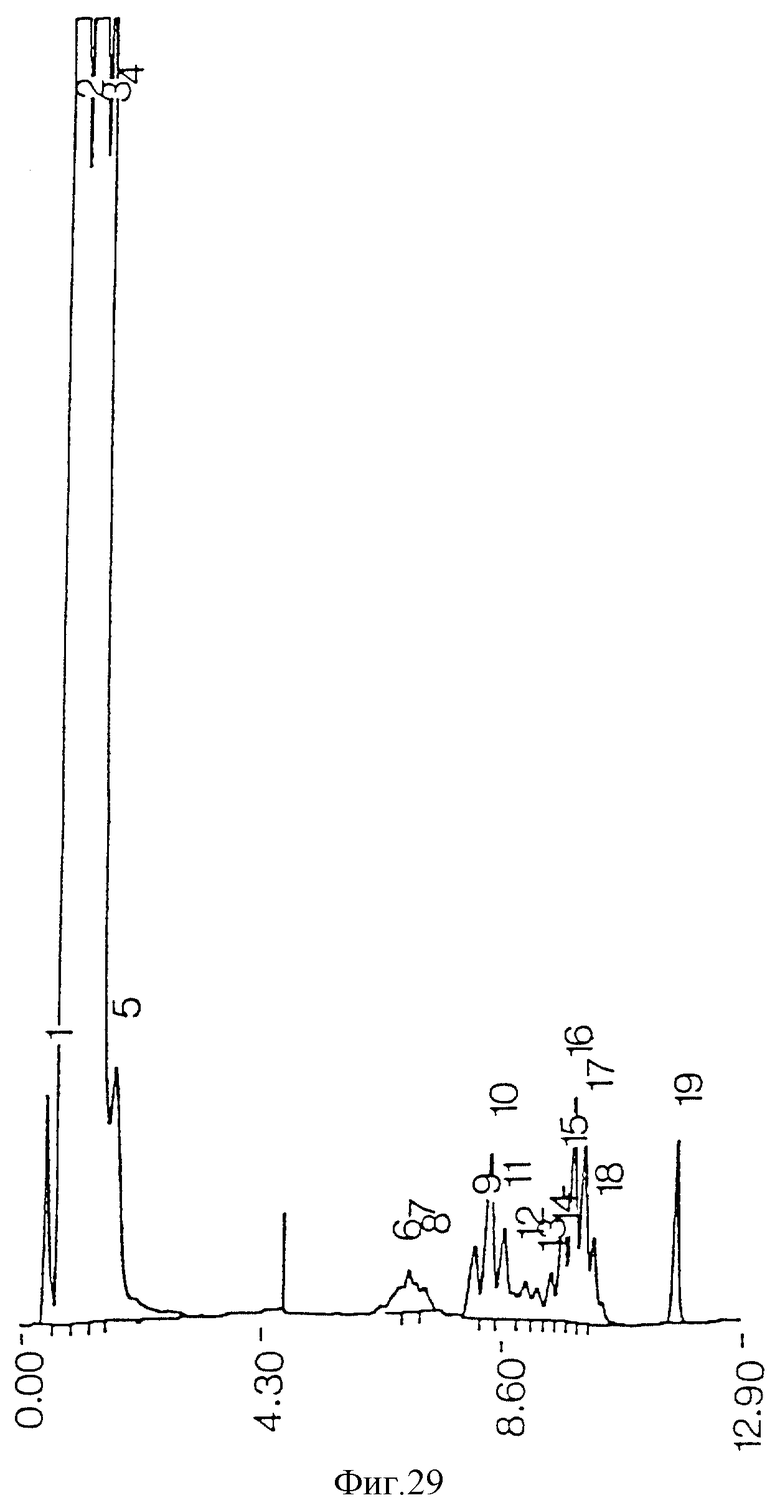
фиг. 29 - ЖХВР сырого экстракта из M. vaccae, реомыленного;
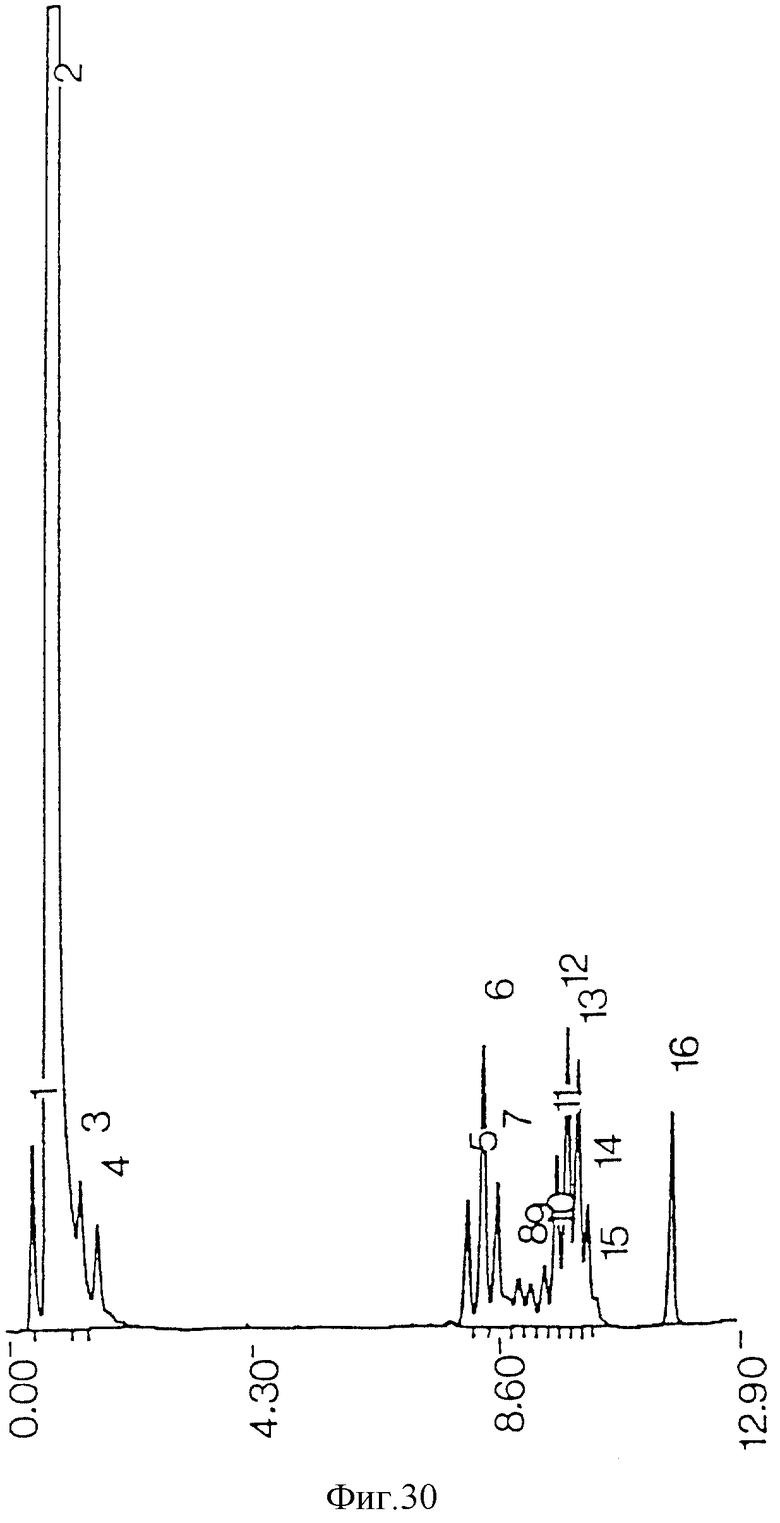
фиг. 30 - ЖХВР миколиновых кислот из M. vaccae, промытых ацетоном, после противоточной очистки.
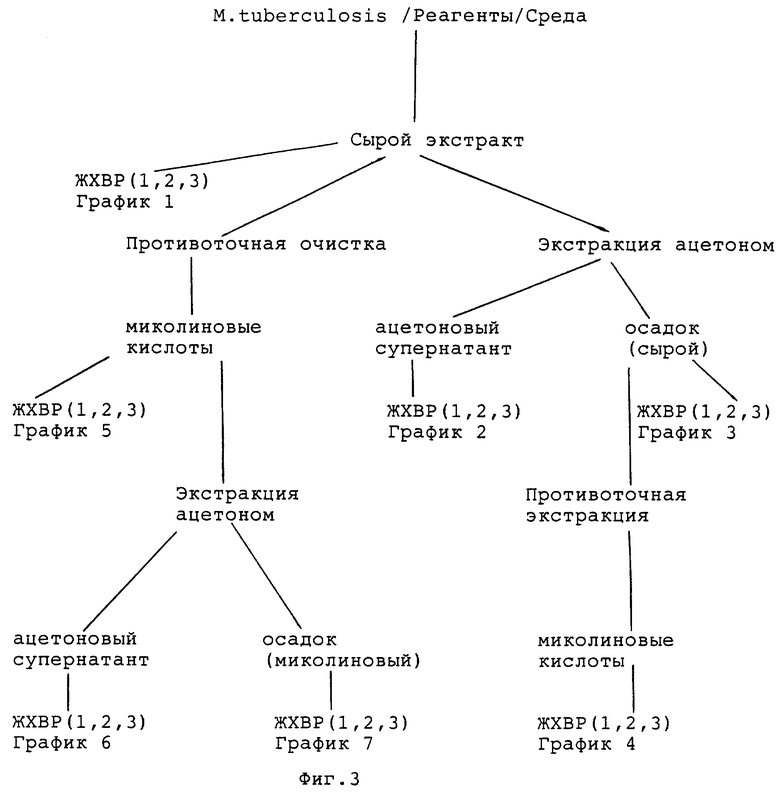
Схематическое представление различных процедур очистки, выполненных на сырых экстрактах компонентов бактериальных клеточных оболочек, и различных стадий, на которых проводился анализ ЖХВР, в виде диаграммы очистки миколиновых кислот из сырого экстракта липидных клеточных оболочек, принадлежащих M.tuberculosis, приведено на фиг. 3.
Описание изобретения
Цель изобретения
Целью настоящего изобретения является выделение и очистка липидных компонентов микробной клеточной оболочки, их производных и их аналогов, в особенности миколиновых кислот, происходящих от различных микробных штаммов, для следующих областей использования:
1. Разработка антитуберкулезных и других антимикобактериальных иммунологических препаратов, таких как вакцины для человека и животных. Такие препараты могут быть получены на основе миколиновых кислот с сопутствующим присутствием других микобактериальных клеточных компонентов или без их присутствия и могут требовать или не требовать использования присадок различного типа, включая интерлейкины. Разработка таких препаратов будет включать любые манипуляции, необходимые для того, чтобы сделать миколиновые кислоты или другие липидные компоненты клеточных оболочек иммуногенными (например, приготовление иммуногенных конъюгатов - субъединиц вакцин).
2. Разработка и производство диагностических тест-систем для подтверждения присутствия микобактериальных клеток в образцах, таких как слюна, спинномозговая жидкость, кровь, моча, стул и т.д.
3. Получение и выпуск в продажу индивидуальных очищенных компонентов клеточных оболочек для исследовательских и других целей (например, для использования в качестве стандарта или при разработке диагностических тестов).
4. Иммунотерапия болезней микобактериального и другого происхождения, включающая аутоиммунные побочные эффекты.
5. Иммунотерапия устойчивых к мультипрепаратам микобактериальных инфекций.
6. Разработка тестов (in vitro или in vivo) для определения реакции гуморальной или клеточной иммунной системы (степени стимуляции гуморальной или клеточной иммунной системы) на процесс иммунизации или на инфекционный процесс.
7. Разработка новых антитуберкулезных лекарств, нацеленных на ингибирование синтеза клеточных оболочек.
8. Иммунный контроль опухолевых нарушений.
Высокая степень чистоты миколиновых кислот является важной для разработки иммунопрофилактических препаратов, таких как вакцины, иммунотерапии и/или методов выявления, и более конкретно, для:
i) определения системы растворителей, в которой проводится приготовление конъюгатов;
ii) приготовления конъюгатов, необходимых для иммунизации экспериментальных животных;
iii) определения эффективности сочетания миколиновых кислот с молекулами носителя, т.е. для мониторинга процесса конъюгации;
iv) приготовления других конъюгатов, необходимых для мониторинга процесса иммунизации и для разработки иммуноиспытаний типа ELISA;
v) определения специфичности производимых антител и их характеристики;
vi) разработки новых антитуберкулезных лекарств, нацеленных на ингибирование бактериального синтеза клеточных оболочек.
Настоящее изобретение предлагает способ, использующий двухфазную систему растворителей, для одновременной очистки и разделения различных классов соединений, которыми могут быть компоненты клеточных оболочек или их производные, или их аналоги, которые могут быть экстрагированы из культуры релевантных клеток или которые могут быть синтезированы. В предпочтительном варианте осуществления изобретения липидные компоненты клеточных оболочек микробного происхождения могут быть отделены от загрязняющего материала и отделены как группа от загрязнений. Очищенные липидные компоненты клеточных оболочек, например миколиновые кислоты, также как другие липидные компоненты клеточных оболочек, полученные из оболочек бактериальных клеток таких микроорганизмов, как Mycobacteria, Corynebacteria, Nocardia и Rhodococci, могут быть выделены как группа этим способом. Хотя способ применим для всех штаммов Mycobacteria, Corynebacteria, Nocardia и Rhodococcus, примеры представляют детали экспериментов, относящиеся к двум штаммам Mycobacteria.
По существу способ предполагает подвергнуть сырой экстракт компонентов микробных клеточных оболочек, растворенный в специальной двухфазной системе растворителей, противоточному разделению жидкость/жидкость для очистки определенного компонента клеточных оболочек в большом масштабе. В случае миколиновых кислот способ дает выход порядка от 3 до 12% от сухой массы сырого клеточного экстракта очищенной миколиновой кислоты. Способ предполагает сбор культуры бактериальных, например микобактериальных клеток, за которым следует омыление и экстракция липидных компонентов клеточных оболочек. Стадия омыления необходима для того, чтобы освободить липидный компонент от остального скелета клетки, или для того, чтобы отделить свободную соль жирной кислоты от любых ее эфиров, а стадия экстракции необходима для удаления омыляющих агентов из смеси компонента клеточной оболочки с реактивом.
Сырой клеточный экстракт, полученный крупномасштабным процессом экстракции, растворяют в нижней фазе двухфазной системы растворителей и добавляют некоторое количество верхней фазы двухфазной системы растворителей. Этот раствор затем подвергают противоточному распределению в серии из приблизительно 25 циклов, каждый цикл включает смешение верхней и нижней фаз, разделение фаз и перенос разделенных фаз к чистым верхней и нижней фазам.
Метиловая этерификация очищенных липидных компонентов клеточной оболочки происходит в результате их длительного пребывания в содержащих метанол растворителях. Она легко обращается омылением, т.е. добавлением Реактива A при комнатной температуре и повторной экстракцией, как описано в Методике.
Различные группы жирных кислот из клеточных оболочек могут быть идентифицированы в различных пробирках по картине их эмульгирования в нижней и верхней фазе. Фракция миколиновых кислот, например, легко распознавалась по картине эмульгирования преимущественно в нижней фазе в нескольких первых пробирках. Материал, выделенный противотоком, затем извлекается из пробирок. Фракция миколиновых кислот, даже после очистки противоточным распределением, еще содержит загрязняющий материал. Было найдено, что добавление некоторого количества ацетона к очищенному образцу экстрагирует эти загрязнения. (Было найдено, что если ацетон добавляется к сырому экстракту, экстрагируется только часть примесей, происходящих из ингредиентов среды бактериальной культуры, но не все примеси). Очищенные миколиновые кислоты подвергались анализу ЖХВР для определения их чистоты, профиля и выхода.
Способ по изобретению был применен для очистки миколиновых кислот из М. tuberculosis, M. avium и M.vaccae и была подтверждена его эффективность для всех этих штаммов микобактерий. Таким образом, используя способ по изобретению, стало впервые возможно выделить относительно большое количество миколиновых кислот или других специфических липидных компонентов клеточных оболочек и очистить их для последующего использования, такого как любое из перечисленных выше применений.
Примеры
Материалы
Культуры
Mycobacterium teberculosis H37Rv ATCC 27294 - вирулентный штамм, первоначально выделенный из легких больного человека, использовался в экспериментах.
Mycobacterium vaccae ATCC 15483 - штамм, первоначально выделенный из коровьего молока.
Культуры были приобретены в лиофилизированной форме у American Type Culture Collection (ATCC), Maryland, USA.
Среды
Для выращивания М. tuberculosis и M.vaccae были использованы следующие среды:
Жидкая среда - бульон Dubos.
Твердые среды - среда Lowenstein-Jensen (LJ); среда Middledrook 7H-10.
Среды были подготовлены так, как рекомендовано Kent and Kubica (1985) в Guide for the Level III Laboratory, Public Health U.S. Department of Health and Human Services, Atlanta.
Реактивы
Для очистки экстрагированных миколиновых кислот использовались следующие реактивы:
Хлороформ (Saarchem, аналитической чистоты).
Метанол (Merck, химически чистый).
Ацетон (BDH, аналитической чистоты).
Для приготовления реактивов, использованных для экстракции, дериватизации и для анализа миколиновых кислот методом жидкостной хроматографии высокого разрешения (ЖХВР), использовались метанол для ЖХВР и дважды дистиллированная деионизированная вода.
Реактив A: 25% гидроокись калия (аналитической чистоты), растворенная в смеси метанол-вода (1:1); 62,5 г гидроокиси калия растворялось в 125 мл воды и добавлялось 125 мл метанола (BDH, для ЖХВР).
Реактив B: концентрированная соляная кислота (BDH, аналитической чистоты), разбавленная водой (1:1).
Реактив C: 2% бикарбонат калия (BDH, аналитической чистоты), растворенный в смеси метанол-вода (1:1); 10 г бикарбоната калия растворялись в 250 мл воды и добавлялось 250 мл метанола.
Реактив D: пара-бромофенацилбромид в краун-эфире (Pierce Chemical Co, Cat. N 48891) распределяли в количествах по 500 мкл в маленькие сосуды янтарного цвета с завинчивающейся крышкой с покрытой тефлоном перегородкой. Крышки закрывали и сосуды заворачивали в пленку Parafilm. Реактив D хранили при 4oC.
Реактив Е: реактив E готовили смешением реагента B с метанолом в соотношении 1:1.
Стандарт для ЖХВР
High Molecular Weight Internal Standard (C - 100) от Ribi Immuno Chem Research Company, Cat. No R-50. Стандарт в количестве 1 мг суспендировали в 2,0 мл метиленхлорида (BDH, для ЖХВР), аликвоты по 350 мкл распределялись по маленьким сосудам с завинчивающейся крышкой с покрытыми тефлоном перегородками. Сосуды заворачивали в пленку Parafilm и хранили при 4oC.
Хлороформ (Associated Chemical Enterprises, химически чистый).
Метиленхлорид (BDH, для ЖХВР).
Реактивы A, B, C и E готовили непосредственно перед экспериментами, соблюдая все необходимые предосторожности.
Аппаратура для противоточного распределения
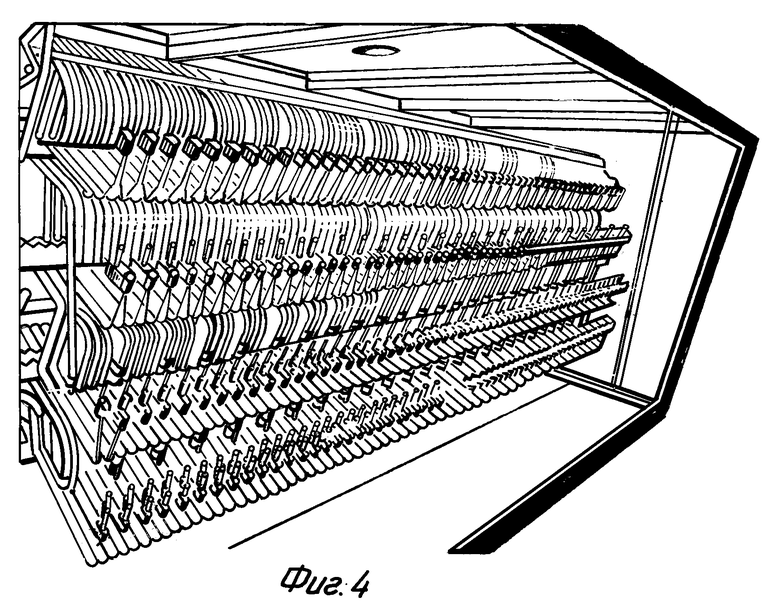
При исследованиях использовалась противоточная установка, произведенная H О POST, Instrument Company Inc., Middle Village, New York. Фотография установки в Department of Biochemistry в University of Pretoria показана на фиг. 4. "Поезда" (ряды-системы) в этой модели состоят из 2 х 250 взаимосвязанных пробирок.
Конечно, может использоваться любая другая химико-технологическая система противоточного распределения.
Инфракрасный спектрометр
ИК-спектральный анализ очищенных противотоком миколиновых кислот проводился с использованием аппарата BOMEM Michelson 100 FTIR и плоттера Hewlett Packard.
Методики
В экспериментальной работе использовались следующие методики:
Выращивание бактериальных штаммов
Бактерии выращивались при 37oC с использованием:
бульона Dubos,
среды Lowenstein-Jensen (скошенный агар),
агаровой среды Middlebrook 7H-10 (скошенный агар).
Засев среды и манипуляция с культурами Mycobacterium проводились в соответствии с процедурами, рекомендованными Kent and Kubica (1985) в Guide for the Level III Laboratory, Public Health US. Department of Health and Human Services, Atlanta.
Приготовление липидных компонентов клеточных оболочек из бактериальных проб
Приготовление бактериальных проб включало три стадии:
сбор клеток Mycobacteria,
омыление,
экстракция жирных кислот.
Сбор клеток проводился соскребем бактериальной культуры с поверхности скосов среды. Эта культура также может быть собрана из жидких культур центрифугированием. Гомогенные бактериальные суспензии готовились в Реактиве A путем встряхивания или взбалтывания собранных клеток со стерильными стеклянными бусинами до конечной концентрации приблизительно 1 х 107 KOE/мл (КОЕ - колониеобразующие единицы).
Омыление Mycobacteria в Реактиве A проводили в автоклаве при 121oC в течение одного часа.
Омыление, экстракция и дериватизация жирных кислот проводились так, как описано у Butler, Jost and Kilburn (1991).
Экстракция липидных компонентов клеточных оболочек
Пробы охлаждались и 1,5 мл Реактива B добавляли к каждой пробе. После взбалтывания проверяли pH каждой пробы и, если требовалось, доводили его до 1 Реактивом B.
Затем 2,0 мл хлороформа добавляли к каждой пробе и взбалтывали 30 секунд. Слои разделяли. Нижний слой удаляли пипеткой Пастера, переносили в WISP-сосуды и выпаривали до сухого остатка при 85oC в нагреваемом блочном испарителе в токе азота. Для нейтрализации следов удаленной кислоты 100 мкл Реактива C добавляли к каждой пробе и жидкость упаривали до сухого остатка при 85oC в нагреваемом блочном испарителе в токе азота. Пробы хранили в темноте под слоем ацетона при 4oC до использования или анализа методом ЖХВР.
Дериватизация жирных кислот для анализа ЖХВР
Экстрагированные и очищенные жирные кислоты (миколиновые кислоты) дериватизировали следующим образом:
Ацетон удаляли из проб выпариванием в нагреваемом блочном испарителе при 85oC в токе азота. К каждой охлажденной пробе добавляли 2,0 мл Реактива A. Пробы взбалтывали 30 секунд, вводили Реактив В (1,5 мл), пробы опять перемешивали и, если требовалось, доводили pH до 1,0. Затем вводили хлороформ (2,0 мл), после чего добавляли 100 мкл Реактива C. Закупоренные пробы взбалтывали 30 секунд, нагревали в течение 5 минут при 85oC в нагреваемом блочном испарителе и высушивали в токе азота.
Дериватизацию проводили введением 1,0 мл хлороформа и 100-150 мкл Реактива D, пробы взбалтывались в течение 30 секунд, сосуды, содержащие пробы, герметизировались и помещались в нагреваемый блочный испаритель на 20 минут при 85oC. После охлаждения проб добавляли Реактив E (1,0 мл). Пробы опять взбалтывались в течение 30 секунд, после чего разделялись на слои. Нижний слой удаляли пипеткой Пастера и переносили в WISP-сосуды. Сосуды помещались в нагреваемый испаритель и их содержимое упаривалось до сухого остатка при 85oC в токе азота.
Остатки ресуспендировали в 0,212 г (что соответствует 160 мкл) метиленхлорида, закупоривали и взбалтывали. Каждую преобразованную пробу, в которую вводили 5 мкл внутреннего стандарта ЖХВР, фильтровали через мембранный фильтр 0,45 мкм в янтарного цвета WISP-сосуд. Вновь закупоренные сосуды хранили при 4oC до анализа методом ЖХВР.
Анализ ЖХВР и количественное определение миколиновых кислот
При ЖХВР-анализе анализировали по 25 мкл из каждой пробы (державшейся на льду во время манипуляций). Контрольные образцы, т.е. 25 мкл фильтрованного метиленхлорида, прогонялись перед анализом каждого набора проб. Если анализировалось большое количество проб, то для подтверждения надежности аппарата ЖХВР контрольные образцы прогонялись после каждых трех или четырех испытуемых проб.
Анализы ЖХВР с обращенной фазой проводились с использованием аппарата жидкостной хроматографии высокого разрешения Waters System (Milford, MA), состоящего из:
системного контроллера (Waters 600 Е);
детектора (Waters 486 Tunalde);
автоотборника проб (Waters 712 WISP);
модуля данных (Microsep М 741);
колонки Waters (Nova-Pak C18 60A, 4 мкм, 3,9 x 150 мм) и
концевого соединительного устройства для картриджа стальных колонок.
Колонка (Guard-Pak/Nova-Pak C18).
Условия опытов были следующими:
Подвижная фаза:
Растворитель A: метанол для ЖХВР,
Растворитель B: метиленхлорид для ЖХВР.
Скорость потока 2,5 мл/мин.
Температура колонки 30oC.
Детектор был установлен на 260 нм.
Градиент ЖХВР первоначально составлял 98% (об/об) метанола (Растворитель A) и 2% (об/об) метиленхлорида (Растворитель B). Градиент увеличивали линейно до 80% A и 20% B за одну минуту, до 35% A и 65% В за десять минут, выдерживали постоянным 5 секунд и затем снижали за 10 секунд до прежнего 98% A и 2% B. Это соотношение выдерживалось 6 минут, чтобы обеспечить стабилизацию системы перед вводом следующей пробы.
Математический расчет количественного содержания миколиновых кислот проводили сравнением суммарной площади пиков испытуемых образцов с площадью пика введенного количества внутреннего высокомолекулярного стандарта ЖХВР.
Очистка миколиновых кислот и групповое выделение других жирных кислот
В эксперименте использовали систему противоточного распределения, включающую 25 пробирок, пронумерованных от 0 до 24. В буферный резервуар вводили примерно 900 мл верхней фазы.
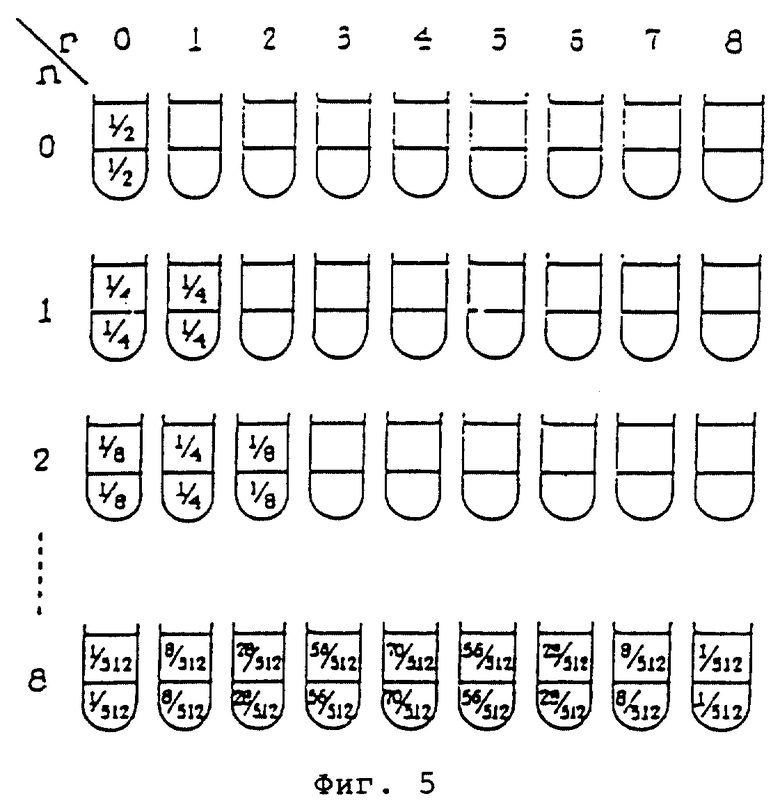
В пробирку номер 0 вводили пробу сырого клеточного экстракта М.tuberculosis (30-150 мг), полученного крупномасштабной экстракцией, растворенную в 10 мл нижней фазы и в 10 мл верхней фазы. В остальные 24 пробирки вводили аликвоты из 10 мл нижней фазы. Верхняя фаза в количествах 10 мл на цикл автоматически распределялась в пробирку номер 0 с повторением в течение 25 циклов, что давало в результате приблизительно 16 часов операции. Таким образом, проводилось 25 циклов и каждый цикл состоял из 20 минут качания и 40 минут на разделение фаз.
Процесс представлен графически на фиг. 5.
На каждом переносе любое растворенное вещество, полученное из пробы и присутствующее в верхней фазе, переносилось в последующую пробирку. После завершения 25 переносов выделенные фракции растворенного вещества должны быть распределены по системе из 25 пробирок.
Для доказательства распределения жирных кислот по двадцати пяти пробиркам наблюдали картину эмульгирования в верхней и нижней фазах по системе пробирок и соответственно определяли фракции.
Выделенный противотоком материал затем удаляли из пробирок, используя 50-миллилитровый стеклянный шприц с прикрепленным тефлоновым тюбингом. Материал объединялся в семь фракций, которые высушивали порознь под вакуумом в испарителе Buchi при 70oC, высушенный материал снова растворялся в хлороформе, метаноле или воде (приблизительно в 5 мл), переносился в янтарные WISP-сосуды и хранился при 4oC до использования.
Экстракция ацетоном
Для того, чтобы удалить любые остаточные загрязнения, еще присутствующие в очищенном противотоком материале, дополнительная экстракция ацетоном проводилась следующим образом. К пробе очищенных миколиновых кислот (приблизительно 5,0 мг), помещенной в WISP-сосуд, добавлялась аликвота ацетона (3,0 мл) и проба перемешивалась взбалтыванием. После осаждения ацетон удалялся аспирацией и процесс повторялся два раза. Окончательно очищенные и проэкстрагированные пробы хранились под слоем ацетона.
Выход миколиновых кислот, очищенных противоточным разделением
Для того, чтобы подсчитать приблизительный выход после очистки/разделения, весовое количество миколиновых кислот, присутствующих в пробах, полученных после противоточного разделения/очистки, сравнивали с количеством этих соединений, присутствующих в сыром клеточном экстракте, поданном в противоточный аппарат, рассчитанным по отношению площадей пиков кластера пиков миколиновых кислот и площади пика стандарта на ЖХВР-хроматограмме сырого клеточного экстракта.
Альтернативно площадь пика кластера пиков миколиновых кислот на ЖХВР-хроматограмме очищенных миколиновых кислот сравнивали с хроматограммой, полученной для сырого экстракта, чтобы определить выход и чистоту продукта.
Инфракрасный спектральный анализ очищенных миколиновых кислот
Проводился ИК-спектральный анализ очищенных противотоком образцов (1 мг), экстрагированных из М.tuberculosis. Миколиновые кислоты растворяли в 1 мл хлороформа для ЖХВР и вводили в жидкостный сосуд. В качестве эталона использовали хлороформ для ЖХВР. Поглощение эталона затем вычиталось из профиля пробы.
Результаты
Очистка миколиновых кислот из М. tuberculosis
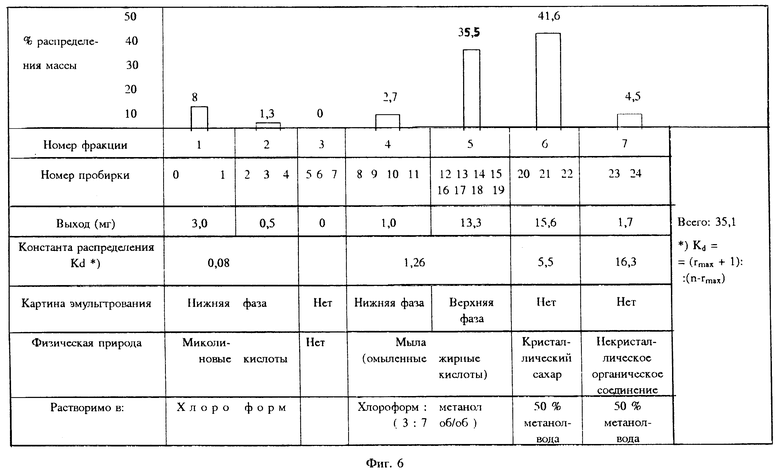
Было найдено, что материал (37,5 мг), извлеченный из М.tuberculosis H37Rv (ATCC 27294) по методу, предложенному Butler, Jost and Kilburn (1991) для извлечения миколиновых кислот, содержит менее чем 10% миколиновых кислот после 25 циклов противоточной экстракции (фиг. 6). Миколиновые кислоты были идентифицированы методом ЖХВР только во фракциях 1 и 2, которые вместе содержали 9,3% от сухой массы сырого экстракта, загруженного в противоточный аппарат. Наблюдаемый коэффициент распределения миколиновых кислот был только 0,08, когда величина коэффициента, позволяющая полностью отделить их от более коротких омыленных кислот, около 1,26 (фиг. 6). Фракция миколиновых кислот легко обнаруживалась по картине ее эмульгирования в системе противоточных пробирок в первых нескольких пробирках системы пробирок, за которыми следовали 3 пробирки, не содержащие сколько-нибудь значительное количество материала. Омыленные жирные кислоты с короткой цепью могли быть идентифицированы в 4 пробирках, содержащих эмульсию в нижней фазе, за которыми непосредственно следовали 8 пробирок с эмульсией в верхней фазе, указывающих на равновесие между диссоциированными (эмульсия в верхней фазе) и протонными (эмульсия в нижней фазе)жирными кислотами в процессе разделения. Остающиеся фракции 6 и 7 не могли быть проанализированы методом ЖХВР, т.к. они были нерастворимы в хлороформе, и что также исключало возможность содержания в них любых миколиновых кислот.
Профили ЖХВР (хроматограммы) сырого экстракта, полученного из М.tuberculosis, использованных реактивов и бактериальной среды представлены на фиг. 8, 9, 10 соответственно.
Миколиновые кислоты, очищенные противоточным распределением, еще содержали некоторый загрязняющий материал, что можно было определить из ЖХВР по времени удерживания, измеряемого в 4-6 минут (фиг.20). Диаграмма, показывающая, как ацетон был применен для извлечения этих загрязнений, приведена на фиг. 3. Диаграмма представляет систематическое исследование одной большой партии сырого экстракта, полученного из М. tuberculosis, что позволяет провести прямое сравнение профилей ЖХВР и рассчитать относительные выходы.
Загрязняющие пики не возникают из реактивов, использованных при процедурах экстракции и очистки (фиг. 21), но могут происходить из ингредиентов среды бактериальной культуры (фиг. 22). Когда экстракция ацетоном проводилась на сыром экстракте до противоточной очистки, наблюдалась некоторая степень извлечения примесей из проб бактериальной среды (фиг. 11) и среды культуры (фиг. 13), но она была недостаточной для удаления всех примесей из конечного очищенного противотоком продукта (фиг. 17). Когда ацетоном экстрагировались высушенные очищенные противотоком миколиновые кислоты, было обнаружено, что загрязнения растворяются в ацетоне (фиг. 23 и 25). ЖХВР-анализ промытой ацетоном фракции миколиновых кислот показал, что эта фракция свободна от любых загрязнений (фиг. 26), отличных от тех, которые обусловлены реактивами дериватизации и могут быть обнаружены при анализе экстрактов от очистки реагентов (фиг. 27) и среды культуры (фиг. 28).
На основании этих результатов утверждается, что сырой экстракт из Mycobacteria, полученный по методу Butler, Jost and Kilburn (1991) и очищенный, как описано выше, противоточным разделением с последующей экстракцией ацетоном, дает миколиновые кислоты, свободные от любых обнаруживаемых ЖХВР примесей (фиг. 26).
Чистота миколиновых кислот была также определена сравнением массы очищенного противотоком материала с выходом миколиновых кислот, рассчитанным на основе поверхности пиков поглощения на хроматограмме ЖХВР. Очищенные противотоком миколиновые кислоты перед ацетоновой промывкой (фиг. 20; 0,3 мг) анализировали методом ЖХВР после дериватизации, как описано выше. Когда поверхность пика поглощения внутреннего стандарта (представляющую 5,01 мкг) сравнили с поверхностью пиков миколиновых кислот, был подсчитан выход 0,27 мг миколиновых кислот, что составило 90% от взвешенного материала. Учитывая, что часть материала была потеряна при переносе фаз по сосудам при процессах дериватизации и экстракции и часть загрязнений удалена при ацетоновой экстракции, можно считать, что чистота фракции миколиновых кислот, представленная профилем ЖХВР на фиг. 26, приближается к 100%.
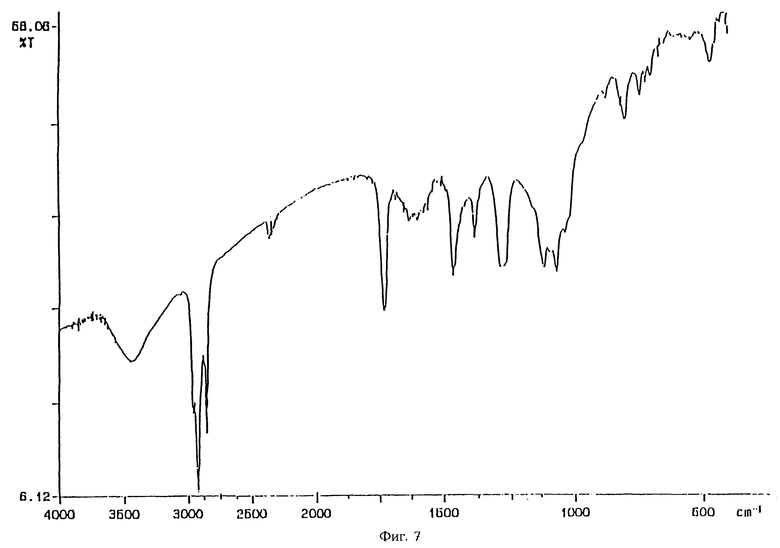
Противоточная очистка дает миколиновые кислоты в виде производных метилового эфира. Это очевидно из инфракрасного спектра очищенных противотоком миколиновых кислот перед ацетоновой экстракцией (фиг. 7) и из ЖХВР-анализа, если реомыление в Реактиве A после очистки не проводилось (результаты не приведены). Добавление Реактива A восстанавливает свободную кислоту и является необходимым для дериватизации пара-бромофенацилбромидом.
Очистка миколиновых кислот из M.vaccae
Культуру M.vaccae экстрагировали и очищали тем же способом, как культуру М. tuberculosis. ЖХВР-анализ сырого экстракта (фиг. 29) показал три кластера пиков с временами удерживания более 5 минут и широкий кластер пиков реактивов/жирных кислот с короткой цепью с временем удерживания менее 2 минут. После противоточной очистки и промывки ацетоном остались два кластера пиков с временем удерживания в колонке ЖХВР более 5 минут (фиг. 30). Кроме того, кластер пиков реактивов/ жирных кислот с короткой цепью стал значительно уже, не оставляя следов детектируемых загрязнений. Исходя из массы миколиновые кислоты были очищены с выходом приблизительно 5%, тогда как выход 4,3% был рассчитан из сравнения площадей кластеров пиков миколиновых кислот на ЖХВР-хроматограммах экстрактов сырых и очищенных миколиновых кислот.
Подобные результаты были получены для очищенных противотоком миколиновых кислот, извлеченных из M.avium (ATCC 25291). Кроме несколько более низкого выхода, эти результаты подобны полученным при очистке миколиновых кислот из М. tuberculosis, демонстрируя, таким образом, широкую применимость способа противоточной очистки миколиновых кислот для видов Мусоbacteria.
Ссылки
Antonucci, G., H., Girardi, M.C., Raviglione and G. Ippolio. 1995. Risk factors for tuberculosis in HIV-infected persons: a prospective cohort study. JAMA, The Journal of the American Medical Association, 274, 143-148.
Arya, S. C. 1993. Serologic diagnosis of tuberculosis through assays of lipoarabinomannan antigen or antibody or lysozyme level. J. Clin. Microbiol. , 31,2836-2837.
Ballew, К. A. and D.M., Becker. 1995. Tuberculosis screening in adults who have received bacille Calmette-Guerin vaccine. Southern Med. J., 88, 1025-1030.
Bahr, G.M., J.L. Stanford, T.D. Chugh et al. 1990a. An investigation of patients with pulmonary tuberculosis in Kuwait in preparation for studies of immunotherapy with Mycobacterium vaccae. Tubercle, 71, 77-86.
Bahr, G. M. , M.A. Shaaban, M. Gabriel et al., 1990b. Improved immunotherapy for pulmonary tuberculosis with Mycobacterium vaccae. Tubercle, 71,259-266.
Beckman, E.M., S.A. Porcelli, C.T. Morita et al. 1994. Recognition of a lipid antigen by GD1-restricted αβ+ T cells. Nature, 372, 691-694.
Beckman, E.M., S.A. Porcelli, C.T. Morita, S. Furlong and M.B. Brenner. 1995. DC1 molecules: a third pathway of antigen presentation. In : Proceedings of the IX-th International Congress of Immunology. San Francisco, 23-29 July, 4190.
Berger, F. M., Bona, C., Lechevalier, M.P. 1995. Immunological adjuvant and process for preparing the same. United States Patent No 4 877 612.
Besra, G. S., D. E. Minnikin, M. J. Simpson, M. S. Baird, P. R. Wheeler and C. Ratledge. 1993. The synthesis of methyl 4-(2- octadecylcyclopropen-1-yl)butanoate: a possible inhibitor in mycolic acid biosynthesis. Chemistry and Physics of Lipids, 66,35-40.
Beyers, A.D., P.R. Donald, P.D. van Helden et al. 1996. Tuberculosis research - the way forward. SAMJ. South African Medical Journal, 86, 30-33.
Bloomfield, G. 1995. Diagnosis of tuberculosis. In: Tuberculosis: Trends and Opportunities, PJB Publications Ltd, Chpt. 4, pp 59-84.
Blumberg, L., B. Miller and H.J. Koornhof. 1994. Multiple drug resistant Mycobacterium tuberculosis. Book of Abstracts: Tuberculosis - Towards 2000. A scientific conference and workshops on the short-term future of tuberculosis in the developing world, with particular emphasis on Africa. Pretoria, South. Africa, 13-17 March, 1994.
Brennan, P. J. 1984. Antigenic peptidoglycolipids, phospholipids and glycolipids. In:The Mycobacteria - A sourcebook, chpt 18, pp 467-489. Publ. Marcel Dekker, Inc., New York and Basel.
Brennan, P.J. and H. Nikaido, 1995. The envelope of Mycobacteria. Annu. Rev. Biochem. 64,29-63.
Butler, W. R. , K. C. Jost and J. 0. Kilburn. 1991. Identification of Mycobacteria by High-Performance Liquid Chromatography. J. Clin. Microbiol, 29, (11), 2468-2472.
Cantwell, M. C. and N. J. Binkin. 1994. Tuberculosis and HIV in sub-Saharan Africa: Can a good tuberculosis control program make a difference? Book of Abstracts: Tuberculosis - Towards 2000. A scientific conference and workshops on the shon-term future of tuberculosis in the developing world, with particular emphasis on Africa. Pretoria, South Africa, 13-17 March 1994.
Chaparas, S. D. 1984. Immunologically based diagnostic tests with tuberculin and other mycobacterial antigens. In: The Mycobacteria - A sourcebook, chpt 9, pp 195-220. Publ. Marcel Dekker. Inc., New York and Basel.
Colditz, G.A., T.F. Brewer, C.S. Berkey et al. 1994. Efficacy of BCG vaccine in the prevention of tuberculosis: meta analysis of the published literature. JAMA, The Journal of the American Medical Association, 271, 698-702.
Cole, S. 1995. The Challenge of Tuberculosis: Statements on Global Control and Prevention. Basic science. (Lancet Conference). The Lancet, 346, 816-817.
Collins, F. M. 1994. The immune response to mycobacterial infection-development of new vaccines. Veterinary Microbiology, 40, 95-110.
Daniel, T.M. 1984. Soluble mycobacterial antigens. In: The Mycobacteria - A sourcebook, chpt 17, pp 417-465. Publ. Marcel Dekker, Inc., New York and Basel.
Darbyshire, J.H. 1995. Tuberculosis: old reasons for a new increase? Br. Med. J., 310.954-955.
Davies, G. R. , D. Wilkinson and M. Colvin. 1996. HIV and tuberculosis. SAMJ. South African Medical Journal. 86, 91.
De Cock, K. M. 1994. Impact of Interaction with HIV. In: Tuberculosis Back to the Future, London School of Hygiene & Tropical Medicine, Third Annual Public Health Forum; Editors: J.D.H. Роrter and K.P.J. McAdam. Publ. John Wiley & Sons, Chichester, New York, Brisbane, Toronto, Singapore, Chpt 2, pp 35- 52.
De Cock, K.M., B. Soro, I.M. Coulibaly and S.B. Lucas. 1992. Tuberculosis and HIV infection in sub-Saharan Africa. JAMA. The Journal of the American Medical Association, 268, 1581-1587.
Deshpande, R.H., M.B. Khan, D.A. Bhat and R.G. Navalkar. 1994. Purification and partial characterisation of a novel 66-kDa seroreactive protein of Mycobacterium tuberculosis. H37Rv. J. Med. Microbiol., 41, 173-178.
Dolin, P. J., M. C. Raviglione and A. Kochi. 1994. Global tuberculosis incidence and mortality during 1990-2000. Bulletin of the World Health Organisation, 72, (2), 213-230.
Etemadi, A. , R. Farid and J.L. Stanford. 1992. Immunotherapy for drug resistant tuberculosis. The Lancet, 340, 1360-1361.
Fauci, A. S. 1995. New science aimed at an ancient killer. JAMA. The Journal of the American Medical Association, 274, 786.
Fine, P. E. M. 1994. Immunities in and to tuberculosis: implications for pathogenesis and vaccination. In: Tuberculosis Back to the Future, London School of Hygiene & Tropical Medicine, Third Annual Public Health Forum; Editors: J.D.H. Porter and K.P.J. McAdam. Publ. John Wiley & Sons, Chichester, New York, Brisbane, Toronto, Singapore, Chpt 1, pp 13-33.
Godfrey-Faussett, P. 1994. Of molecules and men: the detection of tuberculosis, past, present and future. In: Tuberculosis Back to the Future, London School of Hygiene & Tropical Medicine, Third Annual Public Health Forum; Editors: J. D. H. Porter and K.P.J. McAdam. Publ. John Wiley &. Sons, Chichester, New York, Brisbane, Toronto, Singapore, Chpt 4, pp 79-96.
Goren, M. B. 1972. Mycobacterial Lipids: Selected Topics. Bacteriological Reviews, 36,33-64.
Grange, J. M. 1988. Chapter 2: The genus Mycobacterium. In: Mycobacieria and Human Disease. Edward Arnold (Publishers) Ltd, London, UK; Victoria, Australia; Baltimore, Maryland, USA, pp 8-17.
Grosset, J. 1995. The Challenge of Tuberculosis: Statements on Global Control and Prevention. Treatment in developed countries. (Lancet Conference). The Lancet, 346, 810-812.
Henderson C. W. 1995. WHO Reports 1,000 New ТВ Cases Every Hour. AIDS Weekly, May 15, 1995.
Hershfield, E. S. 1995. The Challenge of Tuberculosis: Statements on Global Control and Prevention. Prevention in the developed countries. (Lancet Conference). The Lancet, 346, 813-814.
Holler, A. 1995. ID Vaccine and Pasteur Merieux - Connaught Complete Licensing and Collaboration Agreement on Tuberculosis Vaccine. Business Wire, 2, October 1995, Vancouver, Canada.
Huebner, R.E. and K.G. Castro. 1995. The changing face of tuberculosis. Annu. Rev. Med. 46, 47-55.
Hunter, S. W., H. Gaylord and P.J. Brennan. 1986. Structure and antigenicity of the phosphorylated lipopolysaccharide antigens from the leprosy and tubercule bacilli. J. Biol. Chem. 261, 12345-12351.
Kent, P.T. and G.P. Kubica. 1985. Public Health Mycobacteriology - a Guide for the Level III Laboratory, Public Health U.S. Department of Health and Human Services, Public Health Service, Centers for Disease Control, Laboratory Program Office, Atlanta, Georgia.
Law, M. R. , J. K. Morris, N. Bhatii, R. Halliday and J. Moore-Gillon. 1995. Reasons for increased incidence of tuberculosis. British Med. J. 311, 688.
Mangtani, P., D.J. Jolley, J.M. Watson and L.C. Rodrigues. 1995. Socioeconomic deprivation and notification rates for tuberculosis in London during 1982-1991. Br. Med. J. 310, 963-966.
Mc Neil, M., D. Chatterjee, S.Wu Hunter and P.J. Brennan. 1989. Mycobacterial glycolipids: isolation, structure, antigenicity and synthesis of neoantigens. In: Methods in Enzymology, 179, pp 215-242.
Misaki, A. , I. Azuma and Y. Yamamura. 1987. Structural and immunochemical studies on D-arabino-D-mannans and D-manans of Mycobacterium tuberculosis and other Mycobacterium species. J. Biochem. 82, 1759-1770.
Mofenson, L. M. , E M. Rodriguez, R. Hershow et al. 1995. Mycobacterium tuberculosis infection in pregnant and nonpregnant women infected with HIV in the Women and Infant Transmission study. Arch. Intern. Mod. 155, 1066-1072.
Morita, C. T., E. Beckman, J.F. Bukowski et al. 1995. Direct presentation of nonpeptide prenyl pyrophosphate antigens to human τδ T cells. In: Proceedings of the IX-th International Congress of Immunology, San Francisco, 23-29 July. 1495.
Morse, D. L. 1994. Multidrug resistance; The New York experience. In: Tuberculosis Back to the Future, London School of Hygiene & Tropical Medicine, Third Annual Public Health Forum; Editors: J.D.H. Porter and K.P.J. McAdam. Publ. JohnWiley & Sons, Chichesrer. New York, Brisbane, Toronto, Singapore. Chpt 11, pp 225-237.
Murray, C. J. L. 1994. Resource allocation priorities: value for money in tuberculosis. In: Tuberculosis Back to the Future, London School of Hygiene & Tropical Medicine, Third Annual Public Health Forum; Editors: J.D.H. Porter and K. P. J. McAdam. Publ. John Wiley & Sons, Chichester, New York, Brisbane, Toronto. Singapore, Chpt 9, pp 193-211.
Mwinga, A. 1995. The Challenge of Tuberculosis: Statements on Global Control and Prevention. Treatment in developing countries. (Lancet Conference). The Lancet, 346. 812-813.
O'Brien, R. 1995. The Challenge of Tuberculosis: Scatements on Global Control and Prevention. Prevention in developing countries. (Lancet Conference). The Lancet. 346, 814-816.
Onybebujoh, P. V. C., T. Abdulmumini, S. Robinson, G.A.W. Rook and J.L. Stanford. 1995. Immunotherapy with Mycobacterium vaccae as an addition to chemotherapy for the treatment of pulmonary tuberculosis under difficult conditions in Africa. Respir. Med., 89, 199-207.
Petit, J-F and E. Lederer. 1984. The structure of the mycobacterial cell wall. In: The Mycobacteria. A Sourcebook. Editors: G.P. Kubica and L.G. Wayne, Marcel Dekker, Inc, New York and Basel, Part A, Chpt. 12, 301-339.
Pretorius, G.S., F.A. Sirgel, H.S. Schaaf, P.D. van Helden and T.C. Victor. 1996. Rifampicin resistance in Mycobacterium tuberculosis - rapid detection and implications in chemotherapy. SAMJ. South African Medical Journal, 86,50-55.
Prior, J.G., A.A. Khan, K.A.V. Cartwright, P.A. Jankins and J.L. Stanford. 1995. Immunotherapy with Mycobacterium vaccae combined with second line chemotherapy in drug-resistant abdominal tuberculosis. K. Infect. 31,59-61.
Public Health Reports, 1995. 110, 108-109.
Raviglione, M.C., D.E Snider and A. Kochi. 1995. Global epidemiology of tuberculosis - morbidity and mortality of a worldwide epidemic. JAMA. The Journal of the American Medical Association, 273, 220-226.
Richeldi, L. , S. Barnini and C. Saltini. 1995. Molecular diagnosis of tuberculosis. Eur. Respir. J. Supplement 8/20, 689-700.
Rosat, J. P. , E. M. Beckman, S. Рогсеlli and M.B. Brenner. 1995. CD-1 restricted τδ T cell response to mycobacterial antigens. In: Proceedings of the IX-th International Congress of Immunology. San Francisco, 23-29 July, 1488.
Schaberg, Т., В. Reichert, T. Schulin, H. Lode and H. Mauch. 1995. Rapid drug susceptibility testing of Mycobacterium tuberculosis using conventional solid media. Eur. Respir. J., 8, 1688-1693.
Sieling, P., D. Chatterjee, T. Pirgozy et al. 1995. GD1 presentation of non-peptide ligands from microbial pathogens to αβ TCR T-cells. In: Proceedings of the IX-th International Congress of Immunology. San Francisco, 23-29 July, 2726.
Snider, D. E. 1994. Tuberculosis: the world situation. History of the disease and efforts to combat it. In: Tuberculosis, Back to the Future. London School of Hygiene & Tropical Medicine, Third Annual Public Health Forum. Editors: J. D. H. Porter and K.P.J. McAdam. John Wiley & Sons (Publishers), Chichester, UK, Chpt. 1, pp 13-33.
South African Provisional Patent Application N 94/25/75: "A method for detecting the presence of a Mycobacterium species and a kit and antibodies for used therein".
South African Patent Application N 95/30/77: "A method for detecting the presence of a Mycobacterium species and a kit and antibodies for used therein".
Stanford, J.L., G.A.W. Rook, G.M. Bahr et al., 1990a. Mycobacterium vaccae in immunoprophylaxis and immunocherapy of leprosy and tuberculosis. (Review). Vaccine, 8,525-530.
Stanford, J.L., G.M. Bahr, G.A.W. Rook et al., 1990b. Immunocherapy with Mycobacterium vaccae as an adjunct to chemotherapy in the treatment of pulmonary tuberculosis. Tubercle. 71, 87-93.
Stanford, J. L. and J.M. Grange. 1993. New concepts for the control of tuberculosis in the twenty first century. J. R. Coll. Physicians Lond., 27, 218-223.
Stanford, J. L. and J.M. Grange. 1994. The promise of immunotherapy for tuberculosis. Respir. Med. 88, 3-7.
The Merck Index, 1989. Editors: S. Budavari. M.J. O'Neil, A. Smith and P.E. Heckelman, Eleventh Edition, p 6236.
Torres, R.A., S. Mani, J. Altholz and P. W. Brickner. 1990. Human Immunodeficiency Virus Infection Among Homeless Men in a New York City Shelter. Arch. Intern. Med., 150, 2030-2036.
Torres, M. , P. Mendez-Sampeiro, L. Jimenez-Zamudio et al. 1994. Comparison of the immune response against Mycobacterium tuberculosis antigens between a group of patients with active pulmonary tuberculosis and healthy household contacts. Clin. Exp. Immunol., 96, 75-78.
Vlaspolder, F., P. Singer and C. Roggeveen. 1995. Diagnostic value of an amplification method (Gen-Probe) compared with that of culture for diagnosis of tuberculosis. J. Clin. Microbiol., 33, 2699-2703.
Voelker, R. 1995. New initiative for global TB control. JAMA. The Journal of the American Medical Association, 274, 1255-1257.
Walter, H. and G. Johansson. 1986. Partitioning in Aqueous Two-Phase Systems: An Overview. Analytical Biochemistry, 155, 215- 242.
Weil, D. E. C. 1994. Drug supply: meeting a global need. In: Tuberculosis, Back to the Future. London School of Hygiene & Tropical Medicine, Third Annual Public Health Forum. Editors: J.D.H. Porter and K.P.J. McAdam. John Wiley & Sons (Publishers), Chichesrer, UK. Chpt 6, pp 123-143.
Wheeler, P. R. , G. S. Besra, P.J. Brennan and D. E. Minnikin. 1994. Mycolic acids biosynthesis - the early stages. Book of Abstracts: Tuberculosis - Towards 2000. A scientific conference and workshops on the short-term future of tuberculosis in the developing world, with particular emphasis on Africa. Pretoria, South Africa. 13-17 March, 1994.
WHO Report on the Tuberculosis Epidemic, World Health Organisation, WHO/TB/1995/183.
Wilkinson, D. and K.M. de Cock. 1996. Tuberculosis control in South Africa-time for a new paradigm? SAMJ, South African Medical Journal, 86, 33-35.
Wilkinson, D. and A.J. Moore. 1996. HIV-related tuberculosis in South Africa - clinical features and outcome. SAMJ, South African Medical Journal, 86,64-67.
Yanez, M. A. , M. P. Coppola, D.A. Russo et al. 1986. Detemunacion of mycobacterial antigens in sputum by enzyme immunoassay. J. Clin. Microbiol, 23,822-825.
Yew, W.W. and C.H. Chau. 1995. Drug-resistant tuberculosis in the 1990s. (Review). Eur. Respir. J., 8, 1184-1192.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВИДОВОЙ ИДЕНТИФИКАЦИИ МИКОБАКТЕРИЙ КОМПЛЕКСА MAIS (MYCOBACTERIUM AVIUM, M.INTRACELLULARE, M.SCROFULACEUM) И M.TUBERCULOSIS | 2004 |
|
RU2319748C2 |
| СПОСОБ ВЫЯВЛЕНИЯ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА ГЕНОТИПА BEIJING | 2008 |
|
RU2405836C2 |
| ПРОТИВОТУБЕРКУЛЕЗНАЯ ВАКЦИНА С УЛУЧШЕННОЙ ЭФФЕКТИВНОСТЬЮ | 2004 |
|
RU2342400C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ДЛЯ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА И ДРУГИХ ВНУТРИКЛЕТОЧНЫХ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ И ВАКЦИНА, ПОЛУЧЕННАЯ ПО НАЗВАННОМУ СПОСОБУ | 2001 |
|
RU2262950C2 |
| Мультиэпитопный полипептид для иммунизации против Mycobacterium tuberculosis | 2023 |
|
RU2824195C1 |
| Группа антигенов и тест-система для диагностики инфекции М.tuberculosis complex | 2022 |
|
RU2802789C1 |
| СПОСОБ ВЫЯВЛЕНИЯ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА ГЕНОТИПА ВЕIJING В РЕЖИМЕ РЕАЛЬНОГО ВРЕМЕНИ | 2011 |
|
RU2528866C2 |
| СПОСОБ ГЕНОТИПИРОВАНИЯ ШТАММОВ Mycobacterium tuberculosis | 2013 |
|
RU2547598C1 |
| РЕКОМБИНАНТНАЯ BCG, СВЕРХЭКСПРЕССИРУЮЩАЯ PhoP-PhoR | 2017 |
|
RU2760580C2 |
| СПОСОБ ДИАГНОСТИКИ ЧУВСТВИТЕЛЬНОСТИ ШТАММОВ Mycobacterium tuberculosis К ФТОРХИНОЛОНАМ ПО ГЕНУ gyr B | 2010 |
|
RU2439162C1 |












Способ использует многофазную систему растворителей для одновременных очистки и разделения различных классов соединений. Соединения могут быть компонентами клеточных оболочек или их производными, или аналогами и могут быть экстрагированы из культуры релевантных клеток или могут быть синтезированы. Компоненты клеточных оболочек могут быть липидными компонентами клеточных оболочек микробного происхождения, которые могут быть отделены как группа от загрязняющего материала. Использование изобретения позволяет упростить диагностику туберкулеза. 20 з.п.ф-лы, 30 ил.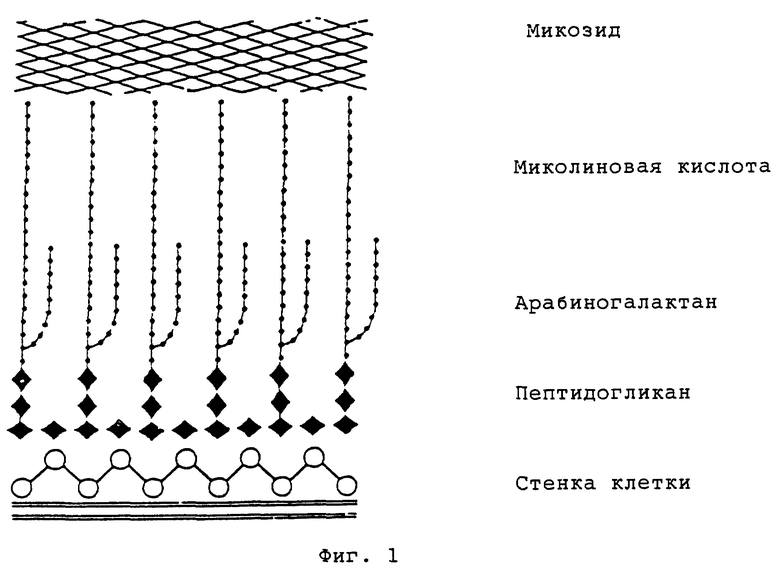
| Beckman E.M | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Nature, 372, pp.691 - 694 | |||
| ПНЕВМОВИБРАЦИОННАЯ УСТАНОВКА ДЛЯ ТРАНСПОРТИРОВАНИЯ И РД:СТАРИВАНИЯ СЫПУЧИХМАТЕРИАЛОВ | 0 |
|
SU261248A1 |
| Способ выделения и очистки липидов тканей | 1984 |
|
SU1193157A1 |
Авторы
Даты
2000-08-27—Публикация
1996-02-22—Подача