Область техники, к которой относится настоящее изобретение
Настоящее изобретение относится к вакцинам против туберкулеза (ТБ). В частности, в настоящем изобретении представлена рекомбинантная BCG, которая сверхэкспрессирует двух компонентную регуляторную систему phoP-phoR и обеспечивает улучшенную защиту от туберкулеза.
Предшествующий уровень техники настоящего изобретения
Туберкулез (ТБ), вызванный Mycobacterium tuberculosis (М. tb), наряду с ВИЧ/СПИД является основной причиной смертности от инфекционных заболеваний во всем мире. В 2014 году ТБ привел к 1,5 миллионам смертельных исходов и 9,6 миллионам новых случаев инфекции. Нехватка защитных вакцин, появление устойчивых к лекарственным средствам штаммов М. tb и высокий процент коинфицирования М. fb/ВИЧ продолжают способствовать эпидемии ТБ. Бацилла Кальмета-Герена (BCG) является единственной лицензированной вакциной против ТБ, и хотя она эффективна против распространенных форм ТБ у детей1,2, BCG характеризуется ограниченной защитой от ТБ легких у взрослых, наиболее распространенной и контагиозной формы заболевания. В клинических исследованиях были показаны изменчивые показатели эффективности в диапазоне от 0 до 80%3-5.
Одна из гипотез, объясняющих изменчивую эффективность BCG, заключается в гетерогенности штаммов BCG6. BCG была получена из вирулентного штамма Mycobacterium bovis путем пассирования in vitro в 1908-1921 гг. Последующее распространение по всему миру и непрерывное пассирование вплоть до 1960-х годов привело к появлению ряда подштаммов BCG. Были детально задокументированы генетические различия между штаммами BCG, включая делеции и дупликации геномных областей, а также однонуклеотидные полиморфизмы (SNP)7-12. Влияние этих различий на эффективность BCG против ТБ является предметом дискуссии6,13 и в настоящее время нет достаточного количества данных, чтобы рекомендовать какой-либо конкретный штамм, так как было проведено недостаточно клинических испытаний, в которых бы сравнивалось сразу несколько штаммов BCG14.
Современные стратегии по улучшению вакцин против ТБ включают разработку субъединичных и живых аттенуированных вакцин15,16. Однако, на животных моделях ни одна субъединичная вакцина не оказалась эффективнее BCG. Недостаточная защитная эффективность MVA85A, наиболее перспективной субъединичной вакцины, у детей грудного возраста, вакцинированных BCG, в недавнем клиническом испытании17 еще больше подчеркивает важность исследования живых вакцин18. Было разработано несколько подходов для создания живых вакцин, включая получение рекомбинантных BCG и аттенуированных штаммов М. tb. Из них лишь для некоторых была доказана эффективность на животных моделях по сравнению с BCG, включая три живых вакцины (rBCG30, VPM1002 и MTBVAC), которые вошли в клинические испытания. rBCG30 является рекомбинантным штаммом BCG-Tice, который сверхэкспрессирует антиген Ag85B. Вакцинация морских свинок штаммом rBCG30 с последующим заражением М. tb обеспечила в результате снижение бактериальной нагрузки на 0,5-1,0 log10 и продление их выживания по сравнению с животными, иммунизированными родительским штаммом BCG19,20. Однако этот эффект был специфичен для BCG-Tice, поскольку сверхэкспрессия Ag85B в BCG-Connaught не обеспечила улучшение защитных свойств20. VPM1002 представляет собой рекомбинантную BCG, которая экспрессирует листериолизин из Listeria monocytogenes. Целесообразность получения этой вакцины была обусловлена представлением о том, что листериолизин может способствовать фагосомальному проникновению BCG в цитозоль макрофагов, тем самым увеличивая презентацию антигена21. Мыши BALB/c, вакцинированные VPM1002, характеризовались снижением нагрузки М. tb на 0,5-1,0 log10 по сравнению со снижением в случае родительского штамма21,22; однако такого улучшения в отношении защиты не наблюдалось на модели морской свинки23. Мутант М. tb с делецией в phoP оценивали в качестве претендента на вакцину исходя из того, что аттенуированная М. tb может иметь больше общих антигенов с клиническими штаммами М. tb, чем BCG24. М. tb ΔphoP обеспечивала такую же защиту у мышей, как и BCG, при этом демонстрируя лучшую защиту у морских свинок при заражении М. tb24,25. С целью обеспечения безопасности fadD26 удаляли для большей аттенуации штамма (MTBVAC), что в результате обусловило профиль безопасности, сопоставимый с BCG-Pasteur или BCG-Danish у мышей SCID26.
Краткое раскрытие настоящего изобретения
Настоящее изобретение относится к вакцинам против туберкулеза, включающим рекомбинантный штамм микобактерии, которая сверхэкспрессирует двухкомпонентную регуляторную систему phoP-phoR. Иммуногенность существующих штаммов BCG в качестве вакцины недостаточна для обеспечения оптимальной защиты хозяина от туберкулеза. В то же время полученный с помощью методов генной инженерии штамм BCG по настоящему изобретению, который сверхэкспрессирует phoP-phoR, является более иммуногенным и обеспечивает лучшую защиту от туберкулеза. Любая полученная с помощью методов генной инженерии микробактерия, которая сверхпродуцирует phoP-phoR на уровне, достаточном для того, чтобы вызвать 2-х (или более) кратную индукцию экспрессии PhoP-PhoR-регулируемых генов или белков, может быть успешно использована при применении настоящего изобретения на практике. В случае, когда рекомбинантную микробактерию по настоящему изобретению вводят млекопитающему-хозяину, у хозяина повышается выработка ИФ-γ CD4+ Т-клетками, и эта рекомбинантная микробактерия обеспечивает защиту от туберкулеза.
Было проведено более десятка исследований по сравнению иммунного ответа, индуцированного различными штаммами BCG у людей14,27. Однако в большинство этих исследований было включено всего лишь два или три штамма BCG. Различия в дизайне исследований, такие как выбранные штаммы BCG, возраст при иммунизации и размер популяции, привели к неоднозначным результатам14. Тем не менее, крупнейшее из этих исследований, которое было проведено под руководством ВОЗ в 1970-х годах, позволило сравнить 11 штаммов BCG у детей28. Было обнаружено, что BCG-Prague существенно выделяется, что проявляется в более слабой реакции на туберкулин по сравнению с другими штаммами BCG, включая BCG-Danish, BCG-Pasteur, BCG-Glaxo, BCG-Japan, BCG-Russia и BCG-Moreau28,29. Обеспокоенность по поводу низкой иммуногенности указанного штамма привела к его замене на BCG-Russia в Чехословакии в 1981 году, спустя почти 30 лет использования30. Причины слабой реакции на туберкулин BCG-Prague остаются неизвестными. Однако было обнаружено, что phoP в BCG-Prague является псевдогеном, содержащим вставку размером 1 п. н., которая нарушает С-концевой ДНК-связывающий домен9. Эта мутация специфична для BCG-Prague, так как все другие штаммы BCG содержат phoP дикого типа (WT). PhoP является регулятором ответа двухкомпонентной системы PhoP-PhoR и активирует более 40 генов в М. tb, включая два Т-клеточных антигена (Ag85A, РРЕ18), которые были использованы для конструирования субъединичных вакцин16,31. Таким образом, была сформулирована гипотеза, состоящая в том, что низкая иммуногенность BCG-Prague является результатом мутации в phoP9, а сверхэкспрессия phoP у BCG может предоставить эффективное средство для повышения иммуногенности и, следовательно, защитной эффективности. Соответственно, в WO 2011/130878А1 было показано, что комплементация BCG-Prague с phoP WT или сверхэкспрессия phoP у BCG-Japan обеспечивали увеличение выработки ИФ-γ.
Настоящее изобретение основывается на обнаружении того, что сверхэкспрессия phoP-phoR в штамме BCG, таком как BCG-Japan, усиливает его иммуногенность и защитную эффективность, из чего можно сделать вывод, что это может быть общеприменимым подходом для улучшения BCG. В настоящем изобретении было показано, что вакцинация мышей C57BL/6 рекомбинантным штаммом rBCG-Japan/PhoPR индуцировала выработку ИФ-γ CD4+ Т-клетками на более высоких уровнях, чем вакцинация родительской BCG. Морские свинки, вакцинированные rBCG-Japan/PhoPR, были лучше защищены при заражении Mycobacterium tuberculosis, при этом у них наблюдали существенно более продолжительное выживание, меньшую бактериальную нагрузку и менее тяжелую патологию по сравнению с животными, иммунизированными родительской BCG. В целом было подтверждено, что рекомбинантная BCG по настоящему изобретению, которая сверхэкспрессирует phoP-phoR, обеспечивает более эффективную защиту от туберкулеза, чем применяемые на сегодняшний день BCG.
Иллюстративная аминокислотная последовательность PhoP представлена на фиг. 1А [SEQ ID NO: 1], а кодирующая ее иллюстративная нуклеотидная последовательность представлена на фиг. 1B [SEQ ID NO: 2]. Иллюстративная аминокислотная последовательность PhoR представлена на фиг. 1С [SEQ ID NO: 3], а кодирующая ее иллюстративная нуклеотидная последовательность представлена на фиг. 1D [SEQ ID NO: 4]. Эти последовательности представляют собой PhoP и PhoR из BCG-Pasteur, как это показано в геномной последовательности, доступной на веб-сайте Института Пастера (http://genodb.pasteur.fr/cgi-bin/WebObjects/GenoList).
Настоящее изобретение относится к рекомбинантной Mycobacterium bovis-BCG, которая сверхэкспрессирует ДНК, кодирующую PhoP [SEQ ID NO: 1; SEQ ID NO 2] и PhoR [SEQ ID NO: 3; SEQ ID NO: 4].
Настоящее изобретение относится к рекомбинантной Mycobacterium bovis-BCG, содержащей нуклеиновую кислоту, способную к сверхэкспрессии, причем указанная нуклеиновая кислота кодирует PhoP [SEQ ID NO: 1; SEQ ID NO: 2] и PhoR [SEQ ID NO: 3; SEQ ID NO: 4].
В одном варианте осуществления рекомбинантный штамм Mycobacterium bovis-BCG выбран из группы, состоящей из Mycobacterium bovis-BCG-Russia, Mycobacterium bovis-BCG-Moreau, Mycobacterium bovis-BCG-Japan, Mycobacterium bovis-BCG-Sweden, Mycobacterium bovis-BCG-Birkhaug, Mycobacterium bovis-BCG-Prague, Mycobacterium bovis-BCG-Glaxo, Mycobacterium bivis-BCG-Denmark, Mycobacterium bovis-BCG-Tice, Mycobacterium bovis-BCG-Frappier, Mycobacterium fcovw-BCG-Connaught, Mycobacterium bovis-BCG-Phipps, Mycobacterium bovis-BCG-Pasteur и Mycobacterium bovis-BCG-China.
Кроме того, рекомбинантные микобактерии по настоящему изобретению не обязательно должны ограничиваться штаммами BCG. Специалистам в данной области техники будет понятно, что можно также использовать и другие штаммы Mycobacterium, включая аттенуированные штаммы М. tb.
В еще одном варианте осуществления вакцина по настоящему изобретению может представлять собой субъединичную вакцину или ДНК-вакцину. В некоторых вариантах осуществления вакцина будет доставляться посредством патогенов легких. Например, последовательности ДНК, кодирующие PhoP и PhoR, могут быть встроены в хромосому или находиться в виде внехромосомной нуклеиновой кислоты патогена легкого, такого как аттенуированный Pseudomonas aeruginosa, или других известных аттенуированных грибов или вирусов. В качестве альтернативы, нуклеиновая кислота, кодирующая регулон PhoP и PhoR, может быть доставлена другими способами, известными специалистам в данной области техники, например, с помощью липосом, аденовирусных векторов и т.п.
Другим аспектом настоящего изобретения является фармацевтическая композиция, содержащая живой рекомбинантный штамм Mycobacterium bovis-BCG, содержащий нуклеиновую кислоту, способную к сверхэкспрессии, причем указанная нуклеиновая кислота кодирует PhoP [SEQ ID NO: 1; SEQ ID NO: 2] и PhoR [SEQ ID NO: 3; SEQ ID NO: 4].
Согласно дополнительному аспекту настоящего изобретения предложена вакцина или иммуногенная композиция для лечения или профилактики заражения микробактериями у млекопитающего, содержащая живой рекомбинантный штамм Mycobacterium bovis-BCG, содержащий нуклеиновую кислоту, способную к сверхэкспрессии, причем указанная нуклеиновая кислота кодирует PhoP [SEQ ID NO: 1; SEQ ID NO: 2] и PhoR [SEQ ID NO: 3; SEQ ID NO: 4].
Другой аспект настоящего изобретения относится к способу лечения или профилактики заражения Mycobacterium tuberculosis или Mycobacterium bovis у млекопитающего, предусматривающему введение млекопитающему вакцины или иммуногенной композиции по настоящему изобретению. В одном варианте осуществления млекопитающее представляет собой корову. В другом варианте осуществления млекопитающее представляет собой человека. В еще одном варианте осуществления вакцину или иммуногенную композицию вводят в присутствии адъюванта.
Дополнительным аспектом настоящего изобретения является способ лечения или профилактики рака у млекопитающего, предусматривающий введение млекопитающему вакцины или иммуногенной композиции по настоящему изобретению. В одном варианте осуществления рак представляет собой рак мочевого пузыря. В другом варианте осуществления вакцину или иммуногенную композицию вводят в присутствии адъюванта.
Краткое описание чертежей
На фиг. 1 приведены последовательности PhoP-PhoR. (а) Аминокислотная последовательность PhoP BCG-Pasteur; (b) ДНК-последовательность phoP BCG-Pasteur. (с) Аминокислотная последовательность PhoR BCG-Pasteur; (d) ДНК-последовательность phoR BCG-Pasteur.
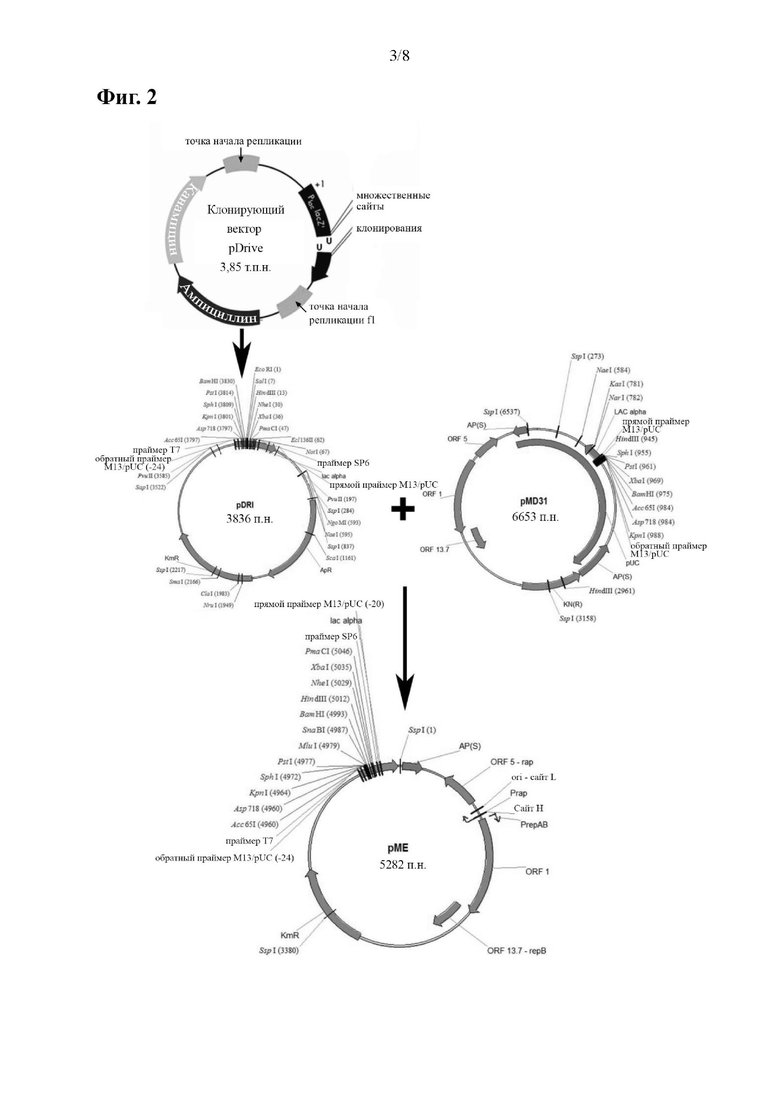
На фиг. 2 приведен клонирующий вектор рМЕ.
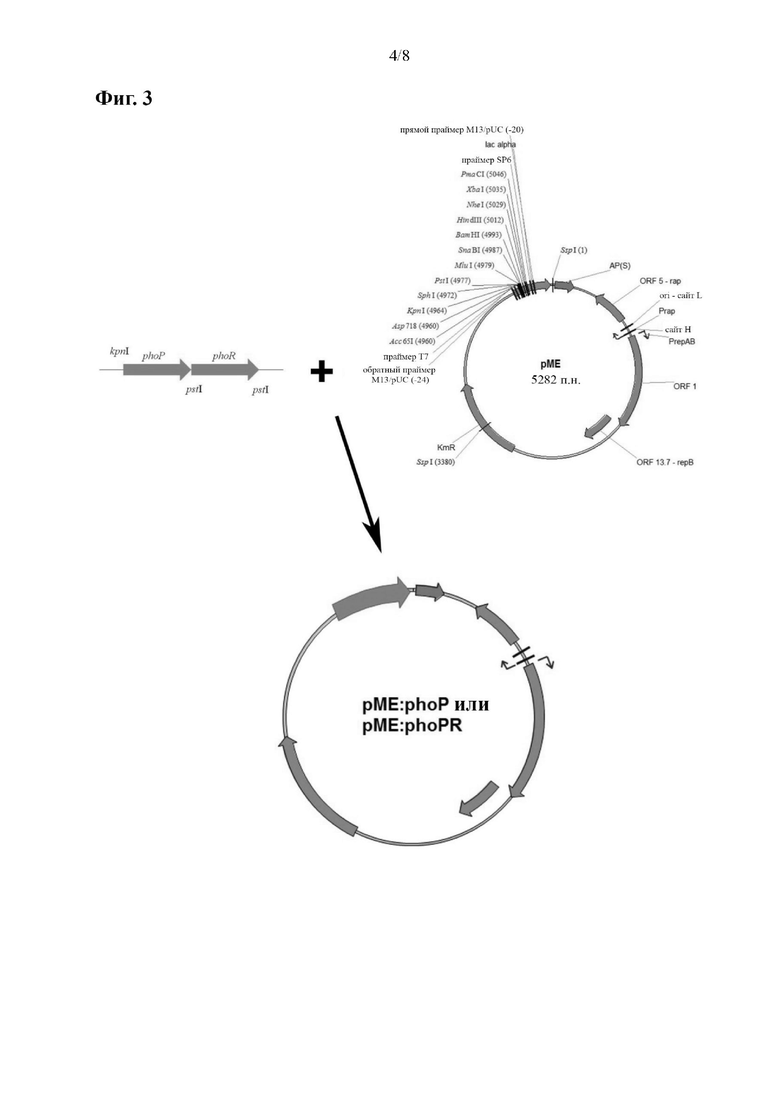
На фиг. 3 приведены сконструированные векторы экспрессии для phoP и phoP-phoR.
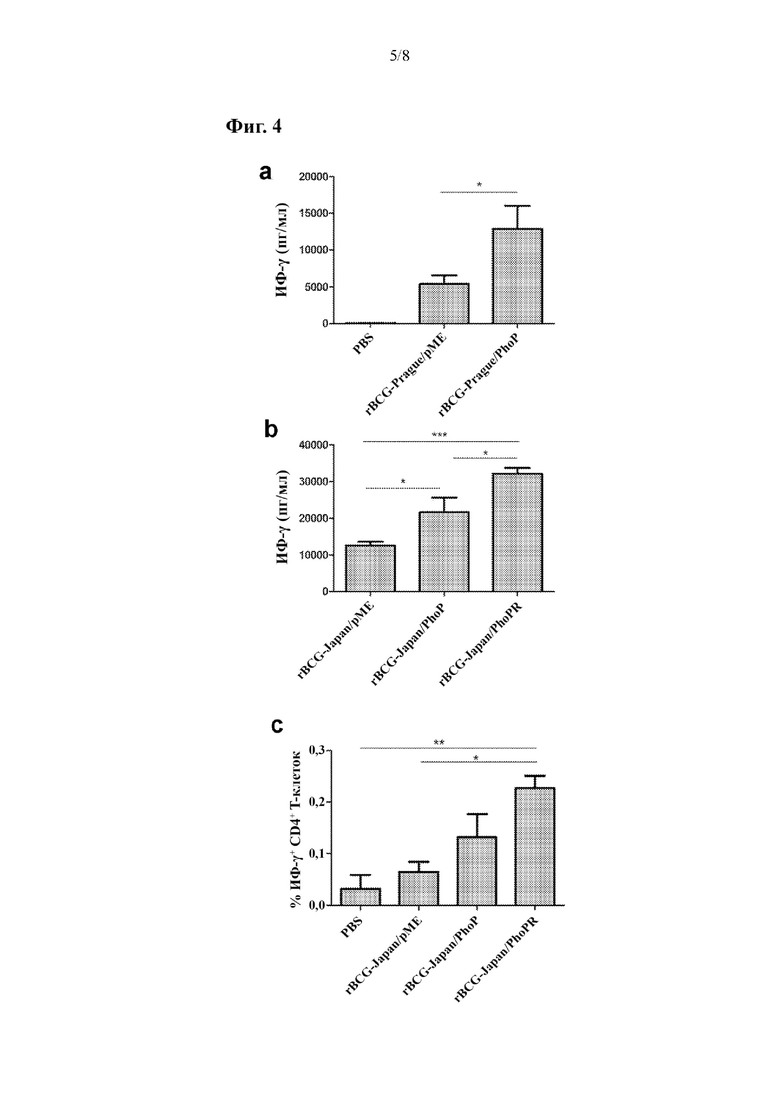
На фиг. 4 показано, что rBCG-Japan/PhoPR в большей степени индуцирует выработку ИФ-γ CD4+ Т-клетками, чем родительская BCG.
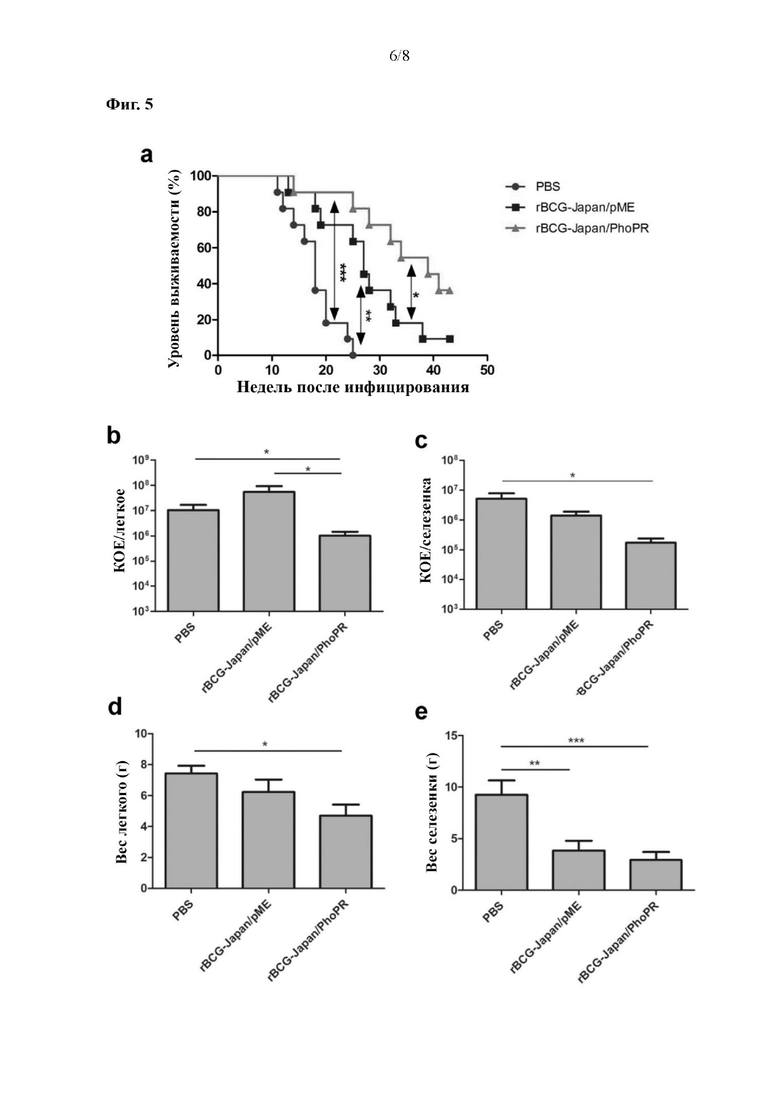
На фиг. 5 показано, что rBCG-Japan/PhoPR обеспечивает продление выживания морских свинок, инфицированных М. tb.
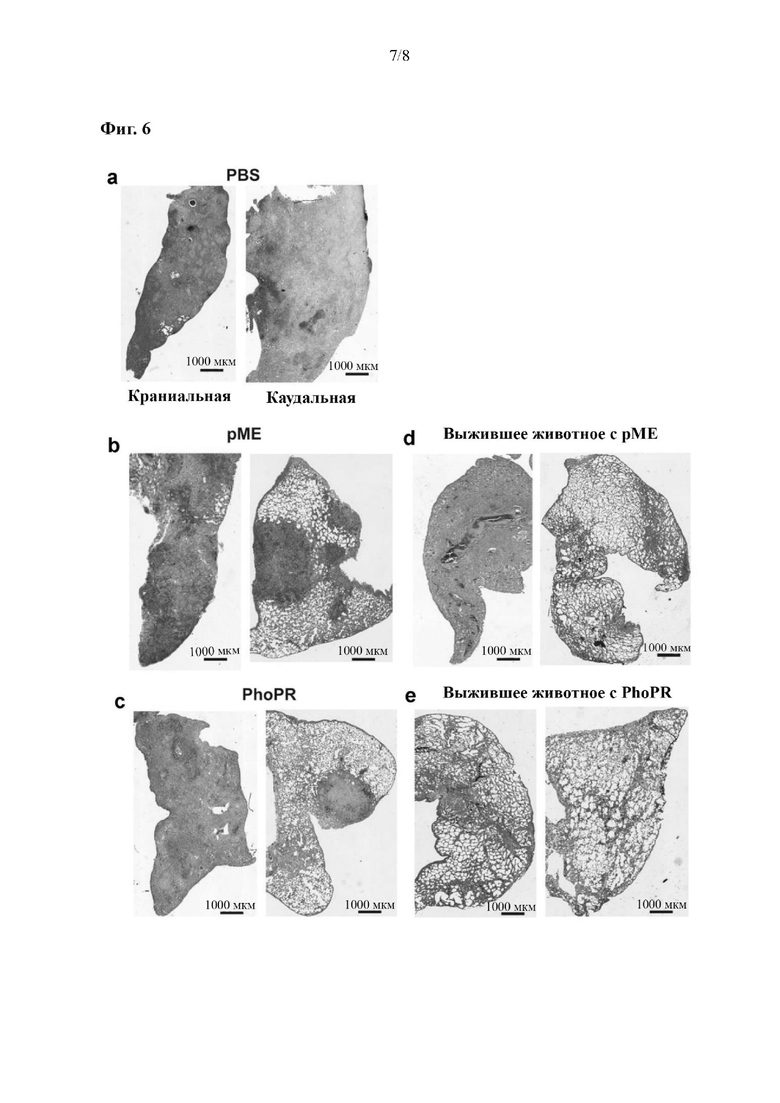
На фиг. 6 показано, что rBCG-Japan/PhoPR обеспечивает уменьшение патологии легкого у морских свинок, инфицированных М. tb.
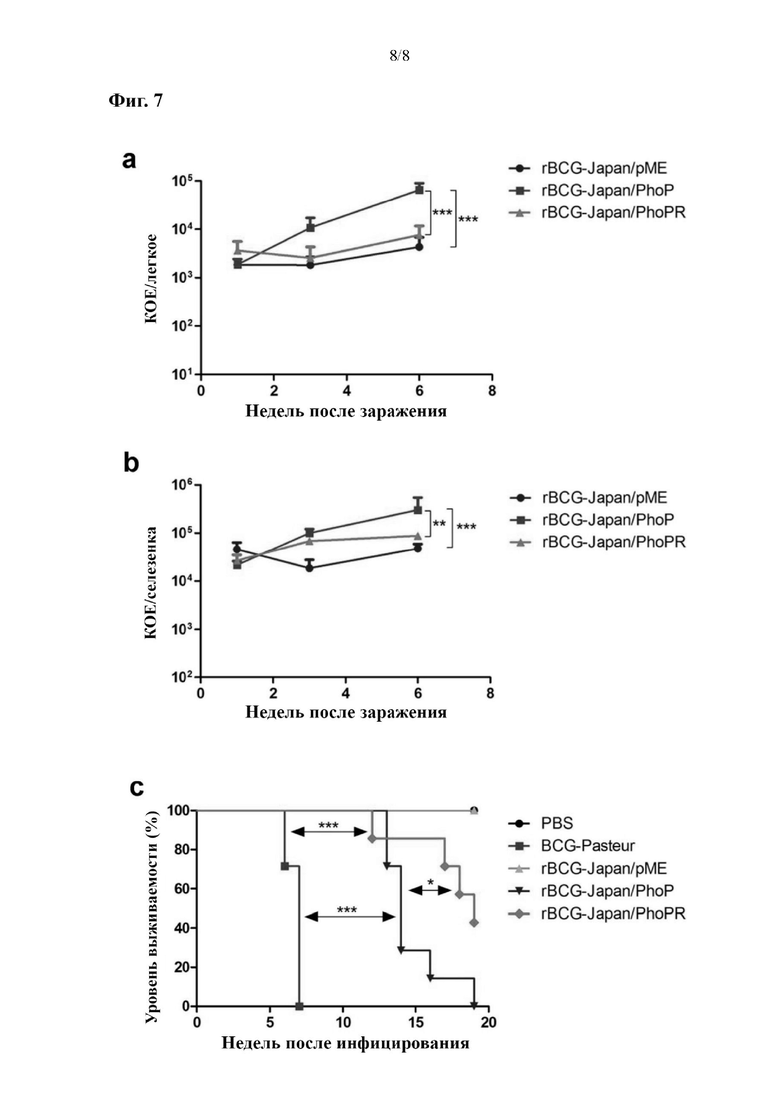
На фиг. 7 показано, что rBCG-Japan/PhoPR безопасна для мышей SCID.
Подробное раскрытие настоящего изобретения
Для защиты от ТБ требуется вовлечение клеточно-опосредованного иммунного ответа, который включает несколько составляющих, в том числе CD4+ и CD8+ Т-клетки, но все же остается до конца не изученным16,32,33. BCG индуцирует ответ Т-хелперов 1 типа (Th1), в основном посредством выработки ИФ-γ CD4+ Т-клетками34. Как правило, иммуногенность BCG определяют путем оценки чувствительности к туберкулину (PPD, очищеный белковый дериват из М. tb), индуцируемой вакциной у детей, являющихся туберкулин-отрицательными до вакцинации30. Хотя в последние годы использование туберкулина в качестве вспомогательной меры защиты поставлено под сомнение35,36, реакция на туберкулин продолжает использоваться в качестве анализа in vivo клеточно-опосредованного иммунного ответа и в качестве маркера иммуногенности19,37. В подтверждение этого существует тесная связь между реакцией на туберкулин и уровнями PPD-специфичной выработки ИФ-γ у детей грудного возраста, вакцинированных BCG38. Кроме того, было обнаружено, что усиление выработки ИФ-γ при реакции на туберкулин не оказывает существенного влияния в качестве дополнительной меры защитной иммунной системы от туберкулеза у молодых людей39. В исследованиях, проведенных в 1970-х годах, было обнаружено, что BCG-Prague постоянно демонстрирует значимо более слабую реакцию на туберкулин у детей и морских свинок, чем другие 10 протестированных штаммов BCG28,29. Обеспокоенность по поводу низкой иммуногенности указанного штамма привела к его замене на BCG-Russia в Чехословакии в 1981 году, спустя почти 30 лет использования30.
Причины слабой реакции на туберкулин в случае BCG-Prague остаются неизвестными. Была выдвинута гипотеза, что мутация в гене phoP у BCG-Prague, обнаруженная в более ранних исследованиях9, обуславливает снижение ее иммуногенности.
Чтобы проверить данную гипотезу, сначала комплементировали BCG-Prague с интактным геном phoP и определили влияние указанного штамма на иммуногенность. Ген phoP WT из BCG-Pasteur клонировали в составе бифункционального мультикопийного вектора рМЕ и вводили в BCG-Prague (rBCG-Prague/PhoP). Мышей C57BL/6 вакцинировали рекомбинантными штаммами BCG-Prague и измеряли уровни PPD-специфичной выработки ИФ-γ с помощью ELISA. Соответственно, rBCG-Prague/PhoP индуцировала более высокие уровни PDD-специфичного высвобождения ИФ-γ у мышей C57BL/6, которые были примерно в 2,4 раза выше, чем у мышей, иммунизированных родительским штаммом (фиг. 4а, р<0,05).
Чтобы проверить, может ли сверхэкспрессия phoP использоваться в качестве общеприменяемого способа для повышения иммуногенности BCG, была сконструирована рекомбинантная BCG, сверхэкспрессирующая phoP в еще одном штамме BCG, BCG-Japan, и полученная на ее основе rBCG-Japan/PhoP. PhoR представляет собой гистидинкиназу, которая распознает неизвестный внеклеточный сигнал и фосфорилирует PhoP31. Поскольку BCG-Japan имеет интактную phoP-phoR, которая транскрибируется в ее геноме, также была создана rBCG-Japan/PhoPR, сверхэкспрессирующая как phoP, так и phoR для поддержания функционального соотношения этой двухкомпонентной системы.
В соответствии с результатами, полученными при использовании BCG-Prague, как rBCG-Japan/PhoP, так и rBCG-Japan/PhoPR индуцировали значимо более высокие уровни PPD-специфичной выработки ИФ-γ у мышей C57BL/6 по сравнению с родительским штаммом (фиг. 4b). Интересно, что среди трех штаммов, именно rBCG-Japan/PhoPR индуцировал наиболее высокий уровень выработки ИФ-γ.
Чтобы определить источник, вырабатываемый индуцированный рекомбинантными штаммами BCG ИФ-γ, также проводили окрашивание на наличие внутриклеточных цитокинов и FACS-анализы. Было обнаружено, что за более интенсивное высвобождение ИФ-γ, вероятно, ответственны CD4+ Т-клетки (фиг. 4 с). Количество вырабатывающих ИФ-γ CD4+ Т-клеток у мышей, вакцинированных rBCG-Japan/PhoPR, было в ~ 3,5 раза выше, чем у мышей, вакцинированных родительским штаммом, что согласуется с разницей в кратности (~ 2,6 раза) выработки общего ИФ-γ между этими двумя группами (фиг. 4b, с).
В тоже время, ни один рекомбинантный штамм BCG-Japan не индуцировал устойчивый ответ CD8+ Т-клеток при сравнении с контролем с использованием имитационной иммунизации. Не было обнаружено значимой выработки других цитокинов (ИЛ-2, ФНО, ИЛ-12, ИЛ-4, ИЛ-5 и ИЛ-10) рекомбинантными штаммами BCG-Japan.
В целом, эти результаты свидетельствуют о том, что мутация phoP частично ответственна за низкую иммуногенность BCG-Prague. Более того, сверхэкспрессия phoP-phoR в BCG-Japan дополнительно стимулировала выработку ИФ-γ CD4+ Т-клетками, что указывает на то, что это может быть использовано в качестве общеприменимого подхода для повышения защитной эффективности BCG.
Чтобы проверить, улучшает ли сверхэкспрессия phoP-phoR опосредованную BCG защиту от инфицирования М. tb, проводили долгосрочный (10 месяцев) эксперимент по выживаемости морских свинок. Морских свинок (11 животных на группу) вакцинировали rBCG-Japan/PhoPR, родительским штаммом или PBS и подвергали заражению респираторным путем с дозой 1000 КОЕМ, tb H37Rv/легкое через 8 недель после вакцинации. При наличии показателей к умерщвлению из соображений гуманности морских свинок подвергали эвтаназии, и строили графики кривых выживаемости с использованием метода Каплана-Мейера.
Среднее время выживания для групп с введением PBS, родительского штамма и rBCG-Japan/PhoPR составляло 18, 27 и 39 недель соответственно (фиг. 5а). С помощью логрангового критерия было показано, что выживание в группе с введением rBCG-Japan/PhoPR было значимо более продолжительным, чем в группе с введением родительской BCG (р<0,05) и группе с введением PBS (р<0,0001). Выживание в группе с введением родительского штамма также было значимо более продолжительным, чем в группе с введением PBS (р<0,01).
По сравнению с невакцинированными животными, родительская BCG обеспечивала продление выживания морских свинок на 9 недель, тогда как rBCG-Japan/PhoPR обеспечивала продление выживания морских свинок на 21 неделю (улучшение на 133% по сравнению с группой, которой вводили родительский штамм). К 43 неделе после заражения, когда эксперимент был завершен, в группе с введением родительского штамма выжила только одна морская свинка, по сравнению с четырьмя животными, которые выжили в группе с введением rBCG-Japan/PhoPR. В группе с введением PBS все животные умерли от инфекции к 25 неделе.
Легкие и селезенку морских свинок дополнительно анализировали после того, как животных подвергали эвтаназии при наличии показателей к умерщвлению из соображений гуманности или в экспериментальной конечной точке. Как и в предыдущем наблюдении, в группе с введением rBCG-Japan/PhoPR в легких было на приблизительно 1,7 log10 меньше М. tb, чем в группе с введением родительского штамма BCG (фиг. 5b, р<0,05). Нагрузка М. tb в селезенке морских свинок из группы с введением rBCG-Japan/PhoPR также была на приблизительно 1,0 log10 ниже, чем в группе с введением родительского штамма BCG, и эта разница приближается к значимой (р=0,066). Соответственно, у животных из группы с введением rBCG-Japan/PhoPR наблюдали наименьшие показатели веса легкого и селезенки по сравнению с животными из двух других групп (фиг. 5d, е).
Легкие пяти животных анализировали гистологическими методами. В данную выборку было включено по одному животному из каждой группы, у которых достигались показатели к умерщвлению из соображений гуманности, единственное выжившее животное в группе с введением родительского штамма, и одно животное из четырех выживших к 43 неделе в группе с введением rBCG-Japan/PhoPR. Интересно, что смертность морских свинок, по-видимому, связана со степенью повреждения тканей в каудальной доле легкого. У трех животных, которые подвергались эвтаназии до завершения эксперимента, было обширное (фиг. 6а) или частичное уплотнение тканей (фиг. 6b, с) в каудальных долях легких, а также обширное уплотнение в краниальных долях легких. В свою очередь, у двух выживших животных наблюдались здоровые ткани в каудальной доле, несмотря на то, что у одного животного из группы с введением родительского штамма также было обширное повреждение ткани в краниальной доле (фиг. 6d). Удивительно, но у выжившего животного из группы с введением rBCG-Japan/PhoPR были нормальные легкие без видимого уплотнения тканей в обеих долях (фиг. 6е).
Отчасти PhoP считается фактором вирулентности М. tb24 из-за того, что он активирует секрецию EsxA, важного эффектора вирулентности М. tb40. В связи с этим, возможно, сверхэкспрессия phoP-phoR в BCG может привести к повышению вирулентности и негативно отразиться на безопасности. С другой стороны, поскольку esxA является частью области различий гена 1 (RD1), которая отсутствует в геномах всех штаммов BCG12, степень влияния сверхэкспрессии phoP-phoR на вирулентность BCG остается неясной.
Чтобы решить эту проблему, мышей SCID сначала инфицировали рекомбинантными штаммами BCG-Japan и наблюдали за ростом бактерий в органах-мишенях в течение периода до 6 недель. Интересно, что в ходе эксперимента не было выявлено значимой разницы между ростом rBCG-Japan/PhoPR и родительской BCG в легких или селезенке (фиг. 7а, b). Однако сверхэкспрессия одного только phoP приводила к повышению скорости деления BCG-Japan у мышей SCro по сравнению как с родительским штаммом, так и с rBCG-Japan/PhoPR.
Затем был проведен долгосрочный эксперимент по выживаемости мышей SCID. BCG-Pasteur, который является одним из самых вирулентных штаммов BCG41, также был включен в этот эксперимент для сравнения. Среднее время выживания мышей SCID, инфицированных BCG-Pasteur, rBCG-Japan/PhoP и rBCG-Japan/PhoPR, составляло 7, 14 и 19 недель соответственно (фиг. 7 с). Все мыши SCID, инфицированные родительским штаммом или PBS, оставались живыми к моменту завершения эксперимента на 20 неделе. С помощью логрангового критерия было показано, что группа с введением rBCG-Japan/PhoP характеризовалась значимо более низкой продолжительностью выживания по сравнению с группой, которой вводили rBCG-Japan/PhoPR (р=0,02), и группой, которой вводили родительский штамм (р<0,001), что согласуется с наблюдаемыми более высокими показателями бактериальной нагрузки в этой группе при проведении краткосрочных экспериментов с инфицированием животных (фиг. 7а, b). В группе с введением rBCG-Japan/PhoPR также было показано снижение продолжительности выживания по сравнению с группой, которой вводили родительский штамм (р<0,02). Важно отметить, что у мышей SCID как rBCG-Japan/PhoPR, так и rBCG-Japan/PhoP были значимо менее вирулентными, чем BCG-Pasteur (р<0,001). В целом эти результаты свидетельствуют о том, что сверхэкспрессия phoP-phoR в BCG-Japan не приводит к повышению скорости ее деления у мышей SCID и вызывает лишь умеренное повышение вирулентности.
В целом, было продемонстрировано, что рекомбинантная BCG, сверхэкспрессирующая phoP-phoR, обеспечивает улучшенную защиту от туберкулеза. rBCG-Japan/PhoPR продемонстрировала наилучшую защиту на морских свинках, о чем свидетельствует значимое продление выживания и уменьшение патологии, что является отличительным признаком для тестирования новых вакцин на животных моделях. В качестве животной модели морские свинки являются «золотым стандартом» для тестирования эффективности вакцин против ТБ20. Патогенез заболевания, очаги патологии и ответ на вакцинацию BCG аналогичны описанным у людей.
Существует консенсус о том, что новые претенденты на вакцины против ТБ должны соответствовать определенным критериям для перехода от стадии их разработки к доклиническим испытаниям. Эти критерии включают надежную индукцию ИФ-γ, более высокую защитную эффективность, чем у BCG, а также профиль безопасности, сопоставимый с таковым у BCG на принятых животных моделях42. Штамм rBCG-Japan/PhoPR уже удовлетворяет этим критериям и, таким образом, является многообещающим претендентом для будущих клинических испытаний.
М. bovis-BCG также используют при лечении рака мочевого пузыря. В многочисленных рандомизированных контролируемых клинических испытаниях продемонстрировано, что внутри пузырное введение BCG может предотвратить или отсрочить рецидив опухоли43. Требуют уточнения детали того, каким образом BCG оказывает этот эффект. При этом для противоопухолевого ответа требуется интактный Т-клеточной ответ и вовлечение повышенного уровня экспрессии цитокинов Т-хелперами 1 типа44. По сути, штамм BCG, такой как rBCG-Japan/PhoPR, в случае которого наблюдают повышение продукции цитокина ИФ-γ клетками Th1, может обеспечивать повышенную противоопухолевую активность.
Таким образом, применяют рекомбинантные штаммы BCG, которые сверхэкспрессируют phoP-phoR, в качестве вакцин для предупреждения ТБ и других микобактериальных инфекций. Эти вакцины в виде рекомбинантных BCG обуславливают более эффективную иммунную защиту от туберкулеза.
В полученной с помощью методов генной инженерии (то есть рекомбинантной) микобактерии по настоящему изобретению сверхэкспрессируются белки PhoP и PhoR, т.е. эти два белка экспрессируются на уровне, который превышает уровень экспрессии в соответствующем контрольном организме, таком как та же микобактерия, которая не была получена с помощью методов генной инженерии для сверхэкспрессии PhoP и PhoR. Специалисты в данной области техники хорошо знакомы со сравнительными методами измерений активности белков, и в том числе с использованием подходящих стандартов и контролей для подобных измерений.
Сверхэкспрессия белков PhoP и PhoR в микобактерии может быть осуществлена любым подходящим способом, известным в данной области техники. Как правило, способ будет включать соединение последовательностей нуклеиновых кислот, кодирующих белки PhoP и PhoR, с последовательностями контроля экспрессии, которые в естественных условиях не связаны с генами phoP и phoR. Специалистам в данной области техники будет понятно, что многие такие последовательности контроля экспрессии известны и будут подходящими для использования по настоящему изобретению. Например, если требуется конститутивная экспрессия генов phoP и phoR, последовательности контроля экспрессии (например, промоторы и ассоциированные последовательности) включают без ограничения: оптимальный промотор микобактерий hsp65, асе или msp 12, промотор Т7 и т.п. В качестве альтернативы, сверхэкспрессия phoP и phoR может быть индуцируемой, например, находиться под контролем промоторов, индуцируемых тетрациклином.
Белки, полипептиды или пептиды, кодируемые в соответствии с настоящим изобретением, включают встречающиеся в природе белки, полипептиды или пептиды, или их гомологи, которые выполняют ту же функцию, что и встречающиеся в природе белки, полипептиды или пептиды. Такие гомологи включают белки, полипептиды или пептиды, характеризующиеся по меньшей мере 60%, предпочтительно приблизительно 70% или более, 80% или более и наиболее предпочтительно 90% или более, например, 95%, 96%, 97%, 98 или 99% гомологией с аминокислотными последовательностями встречающихся в природе белков, полипептидов или пептидов, например с аминокислотными последовательностями, представленными в SEQ ID NO: 1 и SEQ ID NO: 3. Такие гомологи включают белки, полипептиды или пептиды с заменой, добавлением и удалением одного или нескольких (например 1-50, 1-20, 1-10, 1-5) аминокислотных остатков в аминокислотных последовательностях встречающихся в природе белков, полипептидов или пептидов (например, в аминокислотных последовательностях, представленных в SEQ ID NO: 1 и SEQ ID NO: 3). Такие гомологи включают, в частности, белки, полипептиды или пептиды с консервативной(консервативными) аминокислотной(аминокислотными) заменой(заменами).
Термины «PhoP» и «PhoR» в контексте настоящего документа относятся к двухкомпонентной регуляторной системе PhoP-PhoR. PhoP представляет собой регулятор ответа, a PhoR представляет собой гистидинкиназу. PhoP или PhoR, кодируемые в соответствии с настоящим изобретением, включают встречающиеся в природе функциональные PhoP и PhoR, например, из рода Mycobacterium, предпочтительно из Mycobacterium tuberculosis или Mycobacterium bovis, или их гомологи, как описано выше. Иллюстративные аминокислотные последовательности PhoP и PhoR представлены на фиг. 1а SEQ ID NO: 1 и на фиг. 1c SEQ ID NO: 3.
Термин «сверхэкспрессировать», «сверхэкспрессирующий» или «сверхэкспрессия» в контексте настоящего документа относится к уровню экспрессии белка целевым геном, экспрессируемым в рекомбинантной бактерии, превышающему уровень экспрессии того же белка, экспрессируемого в исходной бактерии, не являющейся рекомбинантной. Например, представляющий интерес белок экспрессируется в рекомбинантной бактерии на уровне, в 1,1, 1,5, 2, 4, 10, 20, 50, 100, 500, 1000 или более раз превышающем таковой у нерекомбинантной бактерии. Сверхэкспрессия может быть осуществлена посредством методов генной инженерии, например, с использованием мультикопийных плазмид и/или сильных промоторов.
Вариации молекул нуклеиновых кислот
Модификации
Многие модификации можно производить в последовательностях нуклеиновых кислот молекул ДНК, раскрытых в настоящей заявке, и они будут понятны специалисту в данной области техники. Настоящее изобретение включает модификации нуклеотидных последовательностей (или их фрагментов), раскрытых в настоящей заявке, которые кодируют белки или пептиды в клетках бактерий или млекопитающих, которые выполняют ту же функцию, что и белки или пептиды, раскрытые в настоящей заявке. Модификации включают замену, вставку или удаление одного или нескольких (например, 1-50, 1-20, 1-10, 1-5) нуклеотидов, или изменение относительных положений или порядка одного или нескольких (например, 1-50, 1-20, 1-10, 1-5) нуклеотидов.
Молекулы нуклеиновой кислоты могут кодировать консервативные изменения аминокислоты в белках PhoP и PhoR. Настоящее изобретение включает функционально эквивалентные молекулы нуклеиновой кислоты, которые кодируют консервативные изменения аминокислоты и обуславливают молчащие аминокислотные изменения в белках PhoP и PhoR. Способы эмпирического определения консервативных групп аминокислотных замен хорошо известны в данной области техники (см., например, Wu, Thomas D. "Discovering Emperically Conserved Amino Acid Substitution Groups in Databases of Protein Families "
(http://www.ncbi.nlm.nih.gov:80/entrez/query.fcgi?cmd=Retrieve&db=PubMed&list_uids=887752 3&dopt=Abstract).
Молекулы нуклеиновой кислоты могут кодировать неконсервативные аминокислотные замены, вставки или удаления в гене phoP и/или phoR. Настоящее изобретение включает функционально эквивалентные молекулы нуклеиновой кислоты, которые позволяют вносить неконсервативные аминокислотные замены в аминокислотные последовательности белков PhoP и PhoR. Функционально эквивалентные молекулы нуклеиновой кислоты включают ДНК и РНК, которые кодируют пептиды, пептиды и белки, имеющие неконсервативные аминокислотные замены (предпочтительно замена химически сходной аминокислоты), вставки или удаления, но которые также сохраняют ту же или сходную функцию с белками PhoP и PhoR или пептидами, раскрытыми в настоящей заявке. Настоящее изобретение включает ДНК или РНК, кодирующие фрагменты или варианты белка PhoP и PhoR.
Фрагменты пригодны в качестве иммуногенов и в составе иммуногенных композиций. PhoP- и PhoR-подобную активность таких фрагментов и вариантов определяют с помощью анализов, как описано ниже.
Идентичность последовательностей
Молекулы нуклеиновой кислоты по настоящему изобретению также включают молекулы нуклеиновой кислоты (или их фрагменты), характеризующиеся по меньшей мере приблизительно: 60% идентичностью, по меньшей мере 70% идентичностью, по меньшей мере 80% идентичностью, по меньшей мере 90% идентичностью, по меньшей мере 95% идентичностью, по меньшей мере 96% идентичностью, по меньшей мере 97% идентичностью, по меньшей мере 98% идентичностью или, наиболее предпочтительно, по меньшей мере 99% или 99,5% идентичностью с молекулой нуклеиновой кислоты по настоящему изобретению, и причем молекулы нуклеиновой кислоты способны к экспрессии в клетках бактерий или млекопитающих. Под идентичностью понимается сходство двух нуклеотидных последовательностей, которые выровнены с получением совпадения наивысшего порядка. Идентичность рассчитывают в соответствии со способами, известными в данной области техники. Например, если нуклеотидная последовательность (называемая «последовательность А») характеризуется 90% идентичностью с частью SEQ ID NO: 2, тогда последовательность А будет идентична указанной части SEQ ID NO: 2, за исключением того, что последовательность А может содержать до 10 точечных мутаций (таких как замены другими нуклеотидами) на каждые 100 нуклеотидов указанной части SEQ ID NO: 2.
Идентичность последовательностей (каждая конструкция предпочтительно не имеет вставку молекулы кодирующей нуклеиновой кислоты) предпочтительно характеризуется по меньшей мере приблизительно: 70% идентичностью, по меньшей мере 80% идентичностью, по меньшей мере 90% идентичностью, по меньшей мере 95% идентичностью, по меньшей мере 96% идентичностью, по меньшей мере 97% идентичностью, по меньшей мере 98% идентичностью или, наиболее предпочтительно, по меньшей мере 99% или 99,5% идентичностью с последовательностями, представленными в SEQ ID NO: 2 или комплементарными им последовательностями. Идентичность последовательностей предпочтительно будет рассчитана с помощью программного обеспечения GCG, предоставляемого на платформе Bioinformatics (Университет Висконсина). Также доступно и другое программное обеспечение для расчета идентичности последовательностей, такое как программное обеспечение Clustal W (предпочтительно с использованием параметров по умолчанию; Thompson, JD et al., Nucleic Acid Res. 22: 4673-4680), BLAST P, алгоритмы BLAST X, BLASTN для Mycobacterium avium Института геномных исследований (http: tigrblast.tigr.org/), BLASTN для Mycobacterium bovis, M. Bovis-BCG (Pastuer), M. marinum, M. leprae, M. tuberculosis института Сенгера (http://www.sanger.ac.uk/Proiects/Microbes/), методы поиска BLAST для М. tuberculosis Института Пастера (Tuberculist) (http://genolist.pasteur.fr/TubercuList/). методы поиска BLAST для М. leprae Института Пастера (Leproma) (http://genolist.pasteur.fr/Leproma/), BLASTN для М. Paratuberculosis в рамках Проекта Микробного Генома, Университет Миннесоты
(http://www. cbc.umn. edu/ResearchProj ects/Ptb/ и http://www.cbc.umn. edu/ResearchProj ects/AG A C/Mptb/Mptbhome.html), различные поиски BLAST Национального центра биотехнологической информации - США (http://www.ncbi.nlm.nih.gov/BLAST/) и различные поиски BLAST в рамках проекта GenomeNet (Центр биоинформатики Институт химических исследований) (http://blast.genome.ad.jp/).
Поскольку генетический код является вырожденным, последовательности нуклеиновых кислот в SEQ ID NO: 2 и SEQ ID NO: 4 не являются единственными последовательностями, которые могут кодировать полипептид, обладающий активностями PhoP и PhoR. Настоящее изобретение включает молекулы нуклеиновой кислоты, которые несут ту же основную генетическую информацию, что и молекулы нуклеиновой кислоты, представленные в SEQ ID NO: 2 и SEQ ID NO: 4. Молекулы нуклеиновой кислоты (включая РНК), имеющие одно или несколько изменений по сравнению с последовательностями, описанными в настоящей заявке, и которые опосредуют образование полипептидов, представленных в SEQ ID NO: 1 и SEQ ID NO: 3, входят в объем настоящего изобретения.
Другие эквивалентные функциональные формы нуклеиновых кислот, кодирующих белки PhoP и PhoR, могут также быть выделены с использованием обычных методов гибридизации ДНК-ДНК или ДНК-РНК.
Гибридизация
Настоящее изобретение включает ДНК, которая имеет последовательность с достаточной идентичностью с молекулой нуклеиновой кислоты, описанной в настоящей заявке, для гибридизации в жестких условиях (методы гибридизации хорошо известны из уровня техники). Настоящее изобретение также включает молекулы нуклеиновой кислоты, которые гибридизируются с одной или несколькими последовательностями в SEQ ID NO: 2 и SEQ ID NO: 4 или комплементарными им последовательностями. Такие молекулы нуклеиновой кислоты предпочтительно гибридизируются в условиях высокой жесткости (см. Sambrook et al. Molecular Cloning: A Laboratory Manual, Most Recent Edition, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y.). Условия высокой жесткости включают отмывки растворами с пониженным содержанием соли (предпочтительно приблизительно 0,2% SSC) и проводятся при температуре приблизительно 50-65°С.
Вакцины
Специалисту в данной области техники известны способы получения живых рекомбинантных вакцин. Как правило, такие вакцины получают в инъекционной форме, в виде либо жидких растворов, либо суспензий; также могут быть получены твердые формы, подходящие для растворения или суспендирования в жидкости перед инъекцией. Препарат также может быть эмульгирован или покрыт белковой оболочкой в липосомах. Живые иммуногенные ингредиенты часто смешивают с наполнителями, которые являются фармацевтически приемлемыми и совместимыми с активным ингредиентом. Подходящими наполнителями являются, например, вода, физиологический раствор, декстроза, глицерин, этанол и т.д. и их комбинации. Кроме того, при необходимости, вакцина может содержать незначительные количества вспомогательных веществ, таких как смачивающие или эмульгирующие средства, средства, поддерживающие рН в определенном диапазоне, и/или адъюванты, которые повышают эффективность вакцины. Примеры адъювантов, которые могут быть эффективными, включают без ограничения: гидроксид алюминия, N-ацетилмурамил-L-треонил-D)-изоглутамин (thr-MDP), N-ацетил-нормурамил-L-аланил-D-изоглутамин (CGP 11637, называемый nor-MDP), N-ацетилмурамил-L-аланил-D-изоглутаминил-L-аланин-2-(1'-2'-дипальмитоил-sn-глицеро-3-гидроксифосфорилокси)-этиламин (CGP 19835А, называемый МТР-РЕ) и RIBI, который содержит три экстрагированных из бактерий компонента, монофосфориллипид А, димиколят трегалозы и каркас клеточной стенки туберкулезной палочки (MPL+TDM+CWS) в виде эмульсии на основе 2% сквален/Tween 80™.
Эффективность адъюванта может быть определена путем измерения количества антител, направленных против иммуногенного полипептида, содержащего антигенную последовательность Mycobacterium tuberculosis, полученную в результате введения живых рекомбинантных вакцин Mycobacterium bovis-BCG, которые также содержат различные адъюванты.
Вакцины обычно вводят парентерально путем инъекции, например, подкожно или внутримышечно. Дополнительные составы, которые подходят для других способов введения, включают в себя суппозитории и, в некоторых случаях, пероральные составы. Для суппозиториев общепринятые связующие вещества и носители могут включать, например, полиалкиленгликоли или триглицериды; такие суппозитории могут быть составлены из смесей, содержащих активный ингредиент в количестве от 0,5% до 10%, предпочтительно от 1% до 2%. Пероральные составы включают такие обычно используемые наполнители, как, например, маннит, лактоза, крахмал, стеарат магния, сахарин натрия, целлюлоза, карбонат магния и т.д., имеющие фармацевтическую степень чистоты. Такие композиции находятся в форме растворов, суспензий, таблеток, пилюль, капсул, составов с замедленным высвобождением вещества или порошков и содержат от 10% до 95% активного ингредиента, предпочтительно от 25% до 70%.
Вакцины вводят способом, совместимым с лекарственной формой, и в таком количестве, которое будет профилактически и/или терапевтически эффективным.
Вакцина может вводиться по схеме введения однократной дозы или, предпочтительно, по схеме введения многократных доз. Схема введения многократных доз представляет собой схему, при которой первичный курс вакцинации может состоять из 1-10 отдельных доз, за которыми следуют другие дозы, вводимые через последовательные интервалы времени, необходимые для поддержания и/или усиления иммунного ответа, например, с введением второй дозы через 1-4 месяца, и, если необходимо, введением последующей(последующих) дозы(доз) через несколько месяцев. Режим дозирования также будет, по меньшей мере частично, определяться потребностями индивидуума и зависеть от мнения практикующего врача.
Кроме того, живую рекомбинантную вакцину Mycobacterium bovis-BCG вводят в сочетании с другими иммунорегуляторными средствами, например, иммуноглобулинами.
Предметом настоящего изобретения является также состав на основе поливалентной вакцины в виде готовой смеси или таковой, которую необходимо смешать перед использованием, включающий живую рекомбинантную вакцину Mycobacterium bovis-BCG, как определено выше, с другой вакциной, и, в частности, другой живой рекомбинантной вакциной Mycobacterium bovis-BCG, как определено выше, причем эти вакцины содержат последовательности с различными вставками.
Фармацевтические композиции
Фармацевтические композиции по настоящему изобретению используют для лечения или профилактики заражения Mycobacterium tuberculosis или Mycobacterium bovis у млекопитающего. Фармацевтические композиции по настоящему изобретению также используют для лечения пациентов с дегенеративными заболеваниями, нарушениями или аномальными физическими состояниями, такими как рак.
Фармацевтические композиции можно вводить людям или животным различными способами, как, например, в виде таблеток, путем аэрозольного введения, интратрахеального вливания и внутривенной инъекции.
Примеры
Пример 1. Клонирующий вектор рМЕ.
Устойчивый к канамицину бифункциональный вектор, который содержит промотор Т7, получали следующим образом. Для получения pDRI клонирующий вектор pDrive (полученный от Qiagen) разрезали с помощью EcoRI, и вектор подвергался самолигированию. pDRI расщепляли с помощью Sspl и выделяли фрагмент размером 1903 п. н. Бифункциональный вектор pMD31 (Wu et al., 1993, Molecular Microbiology, 7, 407-417) расщепляли с помощью Sspl и выделяли фрагмент размером 3379 п. н. Два фрагмента, полученных при помощи Sspl, лигировали для получения рМЕ (5282 п. н.), который содержал исходный промотор Т7 из pDRIVE. Клонирующий вектор рМЕ показан на фиг. 2.
Пример 2. Конструирование векторов экспрессии для phoPu phoP-phoR.
Продукт длиной 1028 п. н., содержащий phoP, а также участок длинной 257 п. н., расположенный выше сайта инициации трансляции phoP, амплифицировали с помощью ПЦР с использованием прямого праймера phoP-F (5'-AAAAAGGTACCGCTTGTTTGGCCATGTCAAC-3') и обратного праймера phoP-R (5'-AAAAACTGCAGGCTGCCGATCCGATTAACTAC-3'), которые содержат сайты рестрикции KpnI и PstI (подчеркнуты), соответственно. Используя эти сайты рестрикции, продукт ПЦР лигировали с бифункциональным вектором рМЕ (pME-PhoP). Точно так же вектор, который экспрессирует оперон phoP-phoR (pME-PhoPR), был сконструирован путем клонирования продукта ПЦР размером 2501 п. н., содержащего phoP и phoR (а также внутренний участок между двумя генами, 177 п. н., расположенных выше старт-кодона phoP, и 78 п. н., расположенных ниже стоп-кодона phoR), в рМЕ. Этот продукт был амплифицирован с помощью ПЦР из геномной ДНК BCG-Pasteur с использованием прямого праймера phoPR-F (5'-AAAAAGGTACCGGTCGCAATACCCACGAG-3') и обратного праймера phoPR-R (5'-AAAAACTGCAGCCTCAGTGATTTCGGCTTTG-3'), которые содержат сайты рестрикции KpnI и PstI (подчеркнуты), соответственно. Конструкции были подтверждены методом секвенирования ДНК.
Конструкции, а также пустой вектор рМЕ, были независимо введены в BCG-Prague и BCG-Japan путем электропорации. Получение рекомбинантных BCG осуществляли следующим образом: М. bovis BCG-Japan (АТСС №35737) и М. bovis BCG-Prague (АТСС №35742) трансформировали плазмидой pME-PhoP или pME-PhoPR путем электропорации, и электропорированные клетки высевали на чашки Петри со средой 7Н11, дополненной 10% OADC (Difco) и 25 мкг/мл канамицина. После 4 недель инкубации при 37°С отбирали отдельные колонии и наращивали их в жидкой среде 7Н9, дополненной 10% ADC (Difco) и 25 мкг/мл канамицина. После культивирования в течение 3 недель в этой среде, из отобранных клонов выделяли плазмидную ДНК и подтверждали ее методом секвенирования ДНК. Затем готовили стоковые растворы рекомбинантных штаммов BCG для замораживания путем смешивания 1 мл культуры с 1 мл 50% стерильного раствора глицерина, и помещали на хранение при -80°С.
Сконструированные векторы экспрессии для phoP и phoP-phoR показаны на фиг. 3.
Пример 3. rBCG-Japan/PhoPR в большей степени индуцирует выработку ИФ-γ CD4+ Т-клетками, чем родительский штамм BCG.
Самки мышей C57BL/6 были приобретены у Charles River Laboratories и находились в соответствующей возрастной группе (6 недель) в каждом эксперименте. Четырех мышей на группу заражали путем подкожного введения в заднюю область шеи примерно 5×104 КОЕ штамма BCG в 0,2 мл PBS/0,01% Tween 80. Контрольным мышам вводили 0,2 мл PBS/0,01% Tween 80. Через 8 недель мышей подвергали эвтаназии, выделяли спленоциты. Количественные показатели выработки ИФ-γ определяли с применением ферментного иммуносорбентного анализа (ELISA) с использованием набора OptEIA Mouse IFN-γ ELISA (BD Biosciences). Образцы, используемые для ELISA, представляли собой супернатанты из спленоцитов, стимулированных PPD (10 мкг/мл) в течение 72 часов. Вкратце, образцы добавляли в трех повторах в 96-луночные планшеты с лунками с плоским дном (Nunc MaxiSorp), предварительно покрытые иммобилизованными антителами и проводили измерения в соответствии с протоколом производителя. Абсорбцию считывали при 450 нм на считывающем устройстве для микропланшетов (TECAN infinite М200). Уровни ИФ-γ рассчитывали исходя из калибровочной кривой, которую строили с использованием стандартных растворов ИФ-γ. Результаты показаны на фигурах 4а и 4b. Данные представлены в виде среднего±SEM после вычета показаний образцов, не подвергавшихся стимуляции PPD. На фиг. 4а показаны данные, анализируемые с помощью двустороннего t-критерия Стьюдента; на фиг. 4b показаны данные, обработанные с помощью одно факторного дисперсионного анализа (ANOVA) с поправкой Бонферрони для множественных сравнений. *р<0,05, **р<0,01, ***р<0,001.
Чтобы определить источник, вырабатываемый индуцированный рекомбинантными штаммами BCG ИФ-γ, также проводили окрашивание на наличие внутриклеточных цитокинов и FACS-анализы. Вкратце, спленоциты высевали в посевной дозе 2×106 клеток/лунку в 100 мкл среды с тремя повторами и стимулировали 2,5 мкг/лунку очищенного белкового деривата (PPD) (Statens Serum Institute, Дания), или в качестве контроля добавляли полную среду RPMI (cRPMI; RPMI/10% FBS/1% L-глутамин/1% пенициллин/стрептомицин) и инкубировали при 37°С и 5% СО2. После 19 часов стимуляции к клеткам добавляли GolgiPlug (BD Biosciences) в конечном разведении 1:1000 и инкубировали в течение дополнительных 5 часов. Спустя в общей сложности 24 часа стимуляции планшеты центрифугировали при 1400 об/мин в течение 5 минут при 4°С. Супернатант удаляли, а клеточный осадок промывали 200 мкл буфера для FACS (0,5% BSA/PBS) и ресуспендировали в FcBlock (eBiosciences), разведенном в буфере для FACS (1:400), и инкубировали смесь в течение 15 минут в темноте на льду. В планшеты добавляли еще 150 мкл буфера для FACS, перемешивали и центрифугировали при 1400 об/мин в течение 5 минут при 4°С. Супернатант удаляли и окрашивали клетки на наличие внеклеточных поверхностных маркеров Т-клеток: CD3-PE, CD4-FITC и CD8a-PercyPCy5.5 (BD Biosciences) разводили в буфере для FACS и инкубировали смесь в течение 30 минут в темноте на льду. После окрашивания на внеклеточные поверхностные маркеры клетки промывали 150 мкл буфера для FACS, и пермеабилизовали и фиксировали с помощью 1х раствора CytoFix/CytoPerm (BD Biosciences) в течение 20 минут. Затем клетки промывали 1х раствором PermWash (BD Biosciences) и инкубировали с ИФ-γ-АРС (BD Biosciences) в течение 30 минут для окрашивания на внутриклеточный ИФ-γ. Клетки центрифугировали, как описано выше, ресуспендировали в 200 мкл буфера для FACS и анализировали на проточном цитометре BD FACSCalibur™ (BD Biosciences). В общей сложности в лимфоцитарном гейте было получено 300000 событий на образец, и их анализировали с использованием Flow Jo V7.6. Гейты для анализа были установлены на основе изотипических контролей. Данные представлены в виде среднего±SEM после вычета показаний образцов, не подвергавшихся стимуляции PPD. Результаты показаны на фиг. 4с, и с целью статистического анализа они были обработаны с помощью одно факторного дисперсионного анализа (ANOVA) с поправкой Бонферрони для множественных сравнений. *р<0,05, **р<0,01, ***р<0,001.
Пример 4. rBCG-Japan/PhoPR обеспечивает продление выживания морских свинок, инфицированных М. tb.
Группы из 11 самок морских свинок Hartely (200-250 г) были приобретены у Charles River Laboratories, и их вакцинировали путем подкожного введения 5×104 КОЕ BCG-Japan, содержащих рМЕ (rBCG-Japan/pME), pME-PhoPR (rBCG-Japan/PhoPR), в 0,2 мл PBS/0,01% Tween 80 или только PBS/0,01% Tween80 в качестве контроля. Через восемь недель после вакцинации морских свинок заражали 1000 КОЕМ, tb H37Rv путем аэрозольного введения с использованием ингалятора GlasCol. При наличии показателей к умерщвлению из соображений гуманности морских свинок подвергали эвтаназии, и строили графики кривых выживаемости с использованием способа Каплана-Мейера. Результат показан на фиг. 5а. Была проведена проверка по логранговому критерию для сравнения каждой пары кривых выживаемости. *р<0,05, **р<0,01, p***<0,0001.
Легкие и селезенку морских свинок забирали после того, как их подвергали эвтаназии при наличии показателей к умерщвлению из соображений гуманности. Селезенку и все правое легкое гомогенизировали раздельно и высевали на агар 7Н11 для количественного определения нагрузки М. tb в каждом органе. Колонии подсчитывали после инкубации при 37°С в течение трех недель. Результаты показаны на фигурах 5b и 5с. Измеряли показатели веса органов для всех животных в каждой группе, и результаты показаны на фигурах 5d и 5е. Данные на фигурах 5b-5е представлены в виде среднего±SEM, и они были обработаны с помощью однофакторного дисперсионного анализа (ANOVA) с поправкой Бонферрони для множественных сравнений. *р<0,05, **р<0,01, ***р<0,001.
Пример 5. rBCG-Japan/PhoPR обеспечивает уменьшение патологии легкого у морских свинок, инфицированных М. tb.
Шесть морских свинок из эксперимента, описанного на фиг. 4, было выбрано для гистологического анализа. К ним относятся по одной морской свинке из каждой группы, у которых достигались показатели к умерщвлению из соображений гуманности к 25, 27 и 39 неделе соответственно (фигуры 6а-6с). Морские свинки, которым вводили вакцину с рМЕ (фиг. 6b) и PhoPR (фиг. 6b) представлены шестью животными, которых подвергли эвтаназии, из каждой группы (медиана). Было включено единственное выжившее животное из группы, которой вводили вакцину с рМЕ (фиг. 6d), и одно случайно выбранное выжившее животное из группы, которой вводили вакцину с PhoPR (фиг. 6e). У каждой морской свинки анализировали срезы каудальной и краниальной долей левого легкого с помощью окрашивания гематоксилином-эозином. Вкратце, фиксированные формалином ткани погружали в парафиновые блоки. Готовили серию срезов (толщиной 5 мкм), и подвергали их процессу депарафинирования с тремя заменами ксилола (по 3 минуты в каждом случае) с последующей регидратацией с помощью четырех промывок спиртом (100%, 100%, 95%, 70%, 3 минуты в каждом случае). Срезы окрашивали гематоксилином и эозином (EMD Chemicals) и исследовали с использованием Cytation™ 5 (BioTek).
Пример 6. rBCG-Japan/PhoPR является безопасной для мышей SCID.
Краткосрочный анализ бактериальной нагрузки: самки мышей Fox Chase СВ17 SCID (Charles River Laboratories) находились в соответствующей возрастной группе (в возрасте 7 недель). Группы из 12 мышей инфицировали путем внутривенного введения в боковую хвостовую вену 105 КОЕ rBCG-Japan/pME, rBCG-Japan/PhoP или rBCG-Japan/PhoPR в 0,2 мл PBS/0,01% Tween 80 или только PBS/0,01% Tween 80 в качестве контроля. К 1, 3 и 6 неделе после инфицирования мышей (n=4 на каждый момент времени) подвергали эвтаназии и забирали легкие и селезенку, гомогенизировали их в PBS и высевали на агар 7Н11 для определения бактериальной нагрузки в легких (фиг. 7а) и селезенке (фиг. 7b). Данные показаны в виде среднего±SD. Данные обрабатывали с помощью о дно фактор но го дисперсионного анализа (ANOVA) с поправкой Бонферрони для множественных сравнений. *р<0,05, **р<0,01, ***р<0,001.
Долгосрочный анализ выживаемости: группы из десяти самок мышей SCTD от Charles River Laboratories, находящихся в соответствующей возрастной группе (в возрасте 7 недель), инфицировали путем внутривенного введения в боковую хвостовую вену 107 КОЕ BCG-Pasteur, трех вышеупомянутых рекомбинантных штаммов BCG-Japan или PBS/0,01% Tween 80, как описано выше. Трех мышей из каждой группы подвергали эвтаназии в день 1 после инфицирования (для оценки инфицирующей дозы), тогда как за оставшимися мышами наблюдали еженедельно до момента, когда у них достигались показатели к умерщвлению из соображений гуманности (снижение веса тела максимум на 20%). Графики кривых выживаемости строили с использованием способа Каплана-Мейера. Результаты показаны на фиг. 7с. Была проведена проверка по логранговому критерию для сравнения каждой пары кривых выживаемости. *р<0,05, ***р<0,001.
Список литературы
1. Colditz, G.A., et al. The efficacy of bacillus Calmette-Guerin vaccination of newborns and infants in the prevention of tuberculosis: meta-analyses of the published literature. Pediatrics 96, 29-35 (1995).
2. Trunz, B.B., Fine, P. & Dye, C. Effect of BCG vaccination on childhood tuberculous meningitis and miliary tuberculosis worldwide: a meta-analysis and assessment of cost-effectiveness. Lancet 367, 1173-1180 (2006).
3. Brewer, T.F. Preventing tuberculosis with bacillus Calmette-Guerin vaccine: a metaanalysis of the literature. Clin Infect Dis 31 Suppl 3, S64-67 (2000).
4. Colditz, G.A., et al. Efficacy of BCG vaccine in the prevention of tuberculosis. Metaanalysis of the published literature. JAMA 271, 698-702 (1994).
5. Fine, P.E. Variation in protection by BCG: implications of and for heterologous immunity. Lancet 346, 1339-1345 (1995).
6. Behr, M.A. BCG--different strains, different vaccines? Lancet Infect Dis 2, 86-92 (2002).
7. Behr, M.A. & Small, P.M. A historical and molecular phylogeny of BCG strains. Vaccine 17, 915-922 (1999).
8. Brosch, R., et al. Genome plasticity of BCG and impact on vaccine efficacy. Proc Natl Acad Sci USA 104, 5596-5601 (2007).
9. Leung, A.S., et al. Novel genome polymorphisms in BCG vaccine strains and impact on efficacy. BMC Genomics 9, 413 (2008).
10. Garcia Pelayo, M.C., et al. A comprehensive survey of single nucleotide polymorphisms (SNPs) across Mycobacterium bovis strains and M. bovis BCG vaccine strains refines the genealogy and defines a minimal set of SNPs that separate virulent M. bovis strains and M. bovis BCG strains. InfectImmun 77, 2230-2238 (2009).
11. Mahairas, G.G., Sabo, P.J., Hickey, M.J., Singh, D.C. & Stover, C.K. Molecular analysis of genetic differences between Mycobacterium bovis BCG and virulent M. bovis. J Bacteriol 178, 1274-1282 (1996).
12. Behr, M.A., et al. Comparative genomics of BCG vaccines by whole-genome DNA microarray. Science 284, 1520-1523 (1999).
13. Horwitz, M.A., Harth, G., Dillon, B.J. & Maslesa-Galic, S. Commonly administered BCG strains including an evolutionarily early strain and evolutionarily late strains of disparate genealogy induce comparable protective immunity against tuberculosis. Vaccine 27, 441-445 (2009).
14. Ritz, N, Hanekom, W.A., Robins-Browne, R., Britton, W.J. & Curtis, N. Influence of BCG vaccine strain on the immune response and protection against tuberculosis. FEMS Microbiol Rev 32, 821-841 (2008).
15. Skeiky, Y.A. & Sadoff, J.C. Advances in tuberculosis vaccine strategies. Nat Rev Microbiol 4, 469-476 (2006).
16. Andersen, P. & Kaufmann, S.H. Novel vaccination strategies against tuberculosis. Cold Spring Harb Perspect Med 4(2014).
17. Tameris, M.D., et al. Safety and efficacy of MVA85A, a new tuberculosis vaccine, in infants previously vaccinated with BCG: a randomised, placebo-controlled phase 2b trial. Lancet (2013).
18. Developing whole mycobacteria cell vaccines for tuberculosis: Workshop proceedings, Max Planck Institute for Infection Biology, Berlin, Germany, July 9, 2014. Vaccine 33, 3047-3055 (2015).
19. Horwitz, M.A., Harth, G., Dillon, B.J. & Maslesa-Galic, S. Recombinant bacillus calmette-guerin (BCG) vaccines expressing the Mycobacterium tuberculosis 30-kDa major secretory protein induce greater protective immunity against tuberculosis than conventional BCG vaccines in a highly susceptible animal model. Proc Natl Acad Sci USA 97, 13853-13858 (2000).
20. Horwitz, M.A. & Harth, G. A new vaccine against tuberculosis affords greater survival after challenge than the current vaccine in the guinea pig model of pulmonary tuberculosis. Infect Immun 71, 1672-1679 (2003).
21. Grode, L., et al. Increased vaccine efficacy against tuberculosis of recombinant Mycobacterium bovis bacille Calmette-Guerin mutants that secrete listeriolysin. J Clin Invest 115, 2472-2479 (2005).
22. Desel, C., et al. Recombinant BCG DeltaureC hly+induces superior protection over parental BCG by stimulating a balanced combination of type 1 and type 17 cytokine responses. J Infect Dis 204, 1573-1584 (2011).
23. Williams, A., et al. Evaluation of vaccines in the EU TB Vaccine Cluster using a guinea pig aerosol infection model of tuberculosis. Tuberculosis (Edinb) 85, 29-38 (2005).
24. Martin, С., al. The live Mycobacterium tuberculosis phoP mutant strain is more attenuated than BCG and confers protective immunity against tuberculosis in mice and guinea pigs. Vaccine 14, 3408-3419 (2006).
25. Aguilar, D., et al. Immunological responses and protective immunity against tuberculosis conferred by vaccination of Balb/C mice with the attenuated Mycobacterium tuberculosis (phoP) S02 strain. Clin Exp Immunol 147, 330-338 (2007).
26. Arbues, A., et al. Construction, characterization and preclinical evaluation of MTBVAC, the first live-attenuated M. tuberculosis-based vaccine to enter clinical trials. Vaccine 31, 4867-4873 (2013).
27. Ritz, N., et al. The influence of bacille Calmette-Guerin vaccine strain on the immune response against tuberculosis: a randomized trial. Am J Respir Crit Care Med 185, 213-222 (2012).
28. Vallishayee, R.S., Shashidhara, A.N., Bunch-Christensen, K. & Guld, J. Tuberculin sensitivity and skin lesions in children after vaccination with 11 different BCG strains. Bull World Health Organ 51, 489-494 (1974).
29. Ladefoged, A., Bunch-Christensen, K. & Guld, J. Tuberculin sensitivity in guinea-pigs after vaccination with varying doses of BCG of 12 different strains. Bull World Health Organ 53, 435-443 (1976).
30. Milstien, J.B. & Gibson, J.J. Quality control of BCG vaccine by WHO: a review of factors that may influence vaccine effectiveness and safety. Bull World Health Organ 68, 93-108 (1990).
31. Walters, S.B., et al. The Mycobacterium tuberculosis PhoPR two-component system regulates genes essential for virulence and complex lipid biosynthesis. Mol Microbiol 60, 312-330 (2006).
32. Cooper, A.M. Cell-mediated immune responses in tuberculosis. Annu Rev Immunol 27, 393-422 (2009).
33. North, R.J. & Jung, Y.J. Immunity to tuberculosis. Annu Rev Immunol 22, 599-623 (2004).
34. Black, G.F., et al. BCG-induced increase in interferon-gamma response to mycobacterial antigens and efficacy of BCG vaccination in Malawi and the UK: two randomised controlled studies. Lancet 359, 1393-1401 (2002).
35. Comstock, G.W. Identification of an effective vaccine against tuberculosis. Am Rev RespirDis 138, 479-480 (1988).
36. Fine, P.E., Sterne, J.A., Ponnighaus, J.M. & Rees, R.J. Delayed-type hypersensitivity, mycobacterial vaccines and protective immunity. Lancet 344, 1245-1249 (1994).
37. Castillo-Rodal, A.I., et al. Mycobacterium bovis BCG substrains confer different levels of protection against Mycobacterium tuberculosis infection in a BALB/c model of progressive pulmonary tuberculosis. InfectImmun 74, 1718-1724 (2006).
38. Lalor, M.K., et al. Population differences in immune responses to Bacille Calmette-Guerin vaccination in infancy. J InfectDis 199, 795-800 (2009).
39. Gallant, C.J., et al. Tuberculin skin test and in vitro assays provide complementary measures of antimycobacterial immunity in children and adolescents. Chest 137, 1071-1077 (2010).
40. Frigui, W., et al. Control of M. tuberculosis ESAT-6 secretion and specific T cell recognition by PhoP. PLoS Pathog 4, e33 (2008).
41. Zhang, L., et al. Variable Virulence and Efficacy of BCG Vaccine Strains in Mice and Correlation With Genome Polymorphisms. Mol Ther 24, 398-405 (2016).
42. Barker, L., Hessel, L. & Walker, B. Rational approach to selection and clinical development of TB vaccine candidates. Tuberculosis (Edinb) 92 Suppl 1, S25-29 (2012).
43. Lamm, D.L. Efficacy and safety of bacille Calmette-Guerin immunotherapy in superficial bladder cancer. Clin Infect Dis 31 Suppl 3, S86-90 (2000).
44. Prescott, S., Jackson, A.M., Hawkyard, S.J., Alexandroff, A.B. & James, K. Mechanisms of action of intravesical bacille Calmette-Guerin: local immune mechanisms. Clin Infect Dis 31 Suppl 3, S91-93 (2000).
--->
a. SEQ ID NO:1
10 20 30 40 50 60
MRKGVDLVTA GTPGENTTPE ARVLVVDDEA NIVELLSVSL KFQGFEVYTA TNGAQALDRA
70 80 90 100 110 120
RETRPDAVIL DVMMPGMDGF GVLRRLRADG IDAPALFLTA RDSLQDKIAG LTLGGDDYVT
130 140 150 160 170 180
KPFSLEEVVA RLRVILRRAG KGNKEPRNVR LTFADIELDE ETHEVWKAGQ PVSLSPTEFT
190 200 210 220 230 240
LLRYFVINAG TVLSKPKILD HVWRYDFGGD VNVVESYVSY LRRKIDTGEK RLLHTLRGVG
YVLREPR
b. SEQ ID NO:2
1 - atg cgg aaa ggg gtt gat ctc gtg acg gcg
31 - gga acc cca ggc gaa aac acc aca ccg gag
61 - gct cgt gtc ctc gtg gtc gat gat gag gcc
91 - aac atc gtt gaa ctg ctg tcg gtg agc ctc
121 - aag ttc cag ggc ttt gaa gtc tac acc gcg
151 - acc aac ggg gca cag gcg ctg gat cgg gcc
181 - cgg gaa acc cgg ccg gac gcg gtg atc ctc
211 - gat gtg atg atg ccc ggg atg gac ggc ttt
241 - ggg gtg ctg cgc cgg ctg cgc gcc gac ggc
271 - atc gat gcc ccg gcg ttg ttc ctg acg gcc
301 - cgt gac tcg cta cag gac aag atc gcg ggt
331 - ctg acc ctg ggt ggt gac gac tat gtg aca
361 - aag ccc ttc agt ttg gag gag gtc gtg gcc
391 - agg ctg cgg gtc atc ctg cga cgc gcg ggc
421 - aag ggc aac aag gaa cca cgt aat gtt cga
451 - ctg acg ttc gcc gat atc gag ctc gac gag
481 - gag acc cac gaa gtg tgg aag gcg ggc caa
511 - ccg gtg tcg ctg tcg ccc acc gaa ttc acc
541 - ctg ctg cgc tat ttc gtg atc aac gcg ggc
571 - acc gtg ctg agc aag cct aag att ctc gac
601 - cac gtt tgg cgc tac gac ttc ggt ggt gat
631 - gtc aac gtc gtc gag tcc tac gtg tcg tat
661 - ctg cgc cgc aag atc gac act ggg gag aag
691 - cgg ctg ctg cac acg ctg cgc ggg gtg ggc
721 - tac gta ctg cgg gag cct cga tga
c. SEQ ID NO:3
10 20 30 40 50 60
MARHLRGRLP LRVRLVAATL ILVATGLVAS GIAVTSMLQH RLTSRIDRVL LEEAQIWAQI
70 80 90 100 110 120
TLPLAPDPYP IHNPDRPPSR FYVRVISPDG QSYTALNDNT AIPAVPANND VGRHPTTLPS
130 140 150 160 170 180
IGGSKTLWRA VSVRASDGYL TTVAIDLADV RSTVRSLVLL QVGIGSAVLV VLGVAGYAVV
190 200 210 220 230 240
RRSLRPLAEF EQTAAAIGAG QLDRRVPQWH PRTEVGRLSL ALNGMLAQIQ RAVASAESSA
250 260 270 280 290 300
EKARDSEDRM RQFITDASHE LRTPLTTIRG FAELYRQGAA RDVGMLLSRI ESEASRMGLL
310 320 330 340 350 360
VDDLLLLARL DAHRPLELCR VDLLALASDA AHDARAMDPK RRITLEVLDG PGTPEVLGDE
370 380 390 400 410 420
SRLRQVLRNL VANAIQHTPE SADVTVRVGT EGDDAILEVA DDGPGMSQED ALRVFERFYR
430 440 450 460 470 480
ADSSRARASG GTGLGLSIVD SLVAAHGGAV TVTTALGEGC CFRVSLPRVS DVDQLSLTPV
VPGPP
d. SEQ ID NO:4
1 - atg gcc aga cac ctt cga gga agg ctg ccc
31 - cta cgg gta cgc ctg gtc gca gcc acg ctg
61 - atc ctg gtg gcc act gga ctt gtg gcc tcg
91 - ggg atc gcg gtc acc tcg atg ttg cag cac
121 - cgg ctg acc agc cgg atc gat cgg gtg ttg
151 - ctc gag gaa gcc caa atc tgg gcg cag atc
181 - acg ctg ccc ttg gcg ccg gac ccc tac cct
211 - att cat aac ccc gat cgg ccg ccg tcg agg
241 - ttc tac gtt cgg gtg atc agc ccc gac ggc
271 - cag agc tat acg gca ctc aac gac aac act
301 - gcc ata ccg gcg gtg ccc gcc aac aat gat
331 - gtc ggc cgg cac ccg acg acg ctg cca tcg
361 - atc ggc gga tcc aag act tta tgg cgc gcg
391 - gtc tcg gtg cgc gcg tcg gat ggc tac ttg
421 - acc acc gtc gcc att gat ctg gcc gac gtc
451 - cgg agc acc gtg cgg tca ctg gtg ctg ttg
481 - cag gtc ggc ata ggc agt gcg gtg ctg gtt
511 - gtc ctc ggg gtg gcg ggc tac gct gtg gtt
541 - cgc cgc agc ctg cgg ccg ctg gca gaa ttc
571 - gag cag acg gcc gcg gcg atc ggc gcg ggg
601 - cag ctg gat cgc cgg gtc ccg cag tgg cat
631 - ccg cga act gag gtc ggc cgg ctt tcg ttg
661 - gcg ctc aac gga atg ctg gca caa att cag
691 - cgg gcg gtg gcg tcc gcg gaa tct tcc gcc
721 - gaa aag gcc cgg gat tca gag gac cgg atg
751 - cga cag ttc atc acc gac gcc agc cat gaa
781 - ctg cgt acc ccg ttg acc act atc cgc ggc
811 - ttc gcg gag ctg tac cga caa gga gcc gcc
841 - cgc gac gtg ggc atg ctg ctg tcg cgg att
871 - gag agc gaa gcg agc cgg atg ggg ctg ctg
901 - gtg gac gat ttg ctg ctg ctt gcc cgg cta
931 - gat gcg cac cgg ccg ttg gaa ctg tgc cgg
961 - gtg gac ctg ctg gcg ctg gcc agt gat gcc
991 - gcg cac gac gcg cgg gcg atg gac ccc aaa
1021 - cgc agg atc acc ctg gag gtc ctt gac ggc
1051 - ccc ggc acc ccg gag gtc ctc ggc gac gaa
1081 - tcg cgg ctt cgg cag gtg ctg cgc aat ctc
1111 - gtt gca aat gcc ata cag cac acc ccg gaa
1141 - agc gcc gac gtc acc gtg cga gtc ggc acc
1171 - gag ggc gac gac gcc atc ctc gag gtc gcc
1201 - gat gac ggt ccg ggc atg agt cag gag gat
1231 - gcg ctg cgg gtg ttc gag cgg ttc tat cgc
1261 - gcc gac tcg tcg cgg gcg cgc gcc agc ggc
1291 - ggg acc gga ctg ggg ttg tcg atc gtc gac
1321 - tct ttg gtg gcg gcc cat ggc gga gcg gtc
1351 - acc gtg acg acc gcg ctc ggg gag ggt tgc
1381 - tgc ttt cgt gtc tcg ctg ccg cgc gtc agt
1411 - gac gtg gac cag ctg agc ctc acg cca gtt
1441 - gtg cca ggg ccg ccc tga
<---


Группа изобретений относится к живому рекомбинантному штамму Mycobacterium bovis-BCG для защиты от туберкулеза и его использованию. Предложен живой рекомбинантный штамм Mycobacterium bovis-BCG для защиты от туберкулеза, который сверхэкспрессирует нуклеиновые кислоты, кодирующие белки PhoP и PhoR, при этом сверхэкспрессия осуществляется методами генной инженерии. Указанный штамм используют в составе фармацевтической композиции и вакцины, предназначенных для лечения или профилактики заражения микобактериями Mycobacterium tuberculosis у млекопитающего. Указанный штамм используют в способе лечения или профилактики заражения Mycobacterium tuberculosis у млекопитающего, а также в способе лечения или профилактики рака мочевого пузыря у млекопитающего. Группа изобретений позволяет получить штамм с усиленной иммуногенностью и защитной эффективностью, а также с умеренной вирулентностью. 5 н. и 11 з.п. ф-лы, 7 ил., 6 пр.
1. Живой рекомбинантный штамм Mycobacterium bovis-BCG для защиты от туберкулеза, который сверхэкспрессирует нуклеиновые кислоты, кодирующие белки PhoP и PhoR, и сверхэкспрессия осуществляется методами генной инженерии.
2. Живой рекомбинантный штамм Mycobacterium bovis-BCG по п. 1, где белки PhoP и PhoR происходят из Mycobacterium tuberculosis или Mycobacterium bovis.
3. Живой рекомбинантный штамм Mycobacterium bovis-BCG по п. 1, где нуклеиновые кислоты кодируют
(i) аминокислотную последовательность, представленную в SEQ ID NO:1; и
(ii) аминокислотную последовательность, представленную в SEQ ID NO:3.
4. Живой рекомбинантный штамм Mycobacterium bovis-BCG по п. 1, где нуклеиновые кислоты предусматривают
(i) нуклеотидную последовательность, представленную в SEQ ID NO:2; или
(ii) последовательность, которая гибридизируется с нуклеотидной последовательностью (i) в жестких условиях гибридизации; и
(iii) нуклеотидную последовательность, представленную в SEQ ID NO:4; или
(iv) последовательность, которая гибридизируется с нуклеотидной последовательностью (iv) в жестких условиях гибридизации.
5. Живой рекомбинантный штамм Mycobacterium bovis-BCG по любому из пп. 1-4, где штамм Mycobacterium bovis-BCG выбран из существующих штаммов BCG, включая без ограничения: Mycobacterium bovis-BCG-Russia (ATCC №35740), Mycobacterium bovis-BCG-Moreau (ATCC №35736), Mycobacterium bovis-BCG-Japan (ATCC №35737), Mycobacterium bovis-BCG-Sweden (ATCC №35732), Mycobacterium bovis-BCG-Birkhaug (ATCC №35731), Mycobacterium bovis-BCG-Prague (ATCC №35742), Mycobacterium bovis-BCG-Glaxo (ATCC №35741), Mycobacterium bovis-BCG-Denmark (ATCC №35733), Mycobacterium bovis-BCG-Tice (ATCC №35743, №27289), Mycobacterium bovis-BCG-Frappier (ATCC №35746, SM-R; ATCC №35747, INH-R), Mycobacterium bovis-BCG-Connaught (ATCC №35745), Mycobacterium bovis-BCG-Phipps (ATCC №35744), Mycobacterium bovis-BCG-Pasteur (ATCC №35734), BCG-Mexican (ATCC №35738) и Mycobacterium bovis-BCG-China (Шанхайский институт биологических продуктов (Shanghai Institute of Biological Product)).
6. Фармацевтическая композиция для лечения или профилактики заражения микобактериями Mycobacterium tuberculosis у млекопитающего, содержащая фармацевтически эффективное количество живого рекомбинантного штамма Mycobacterium bovis-BCG по любому из пп. 1-5.
7. Вакцина для лечения или профилактики заражения микобактериями Mycobacterium tuberculosis у млекопитающего, содержащая фармацевтически приемлемое количество живого рекомбинантного штамма Mycobacterium bovis-BCG по любому из пп. 1-5.
8. Вакцина по п. 7, дополнительно содержащая фармацевтически приемлемый носитель.
9. Вакцина по п. 7 или 8, дополнительно содержащая адъювант.
10. Вакцина по любому из пп. 7-9, дополнительно содержащая иммуногенный материал от одного или нескольких других патогенов.
11. Способ лечения или профилактики заражения Mycobacterium tuberculosis у млекопитающего, предусматривающий введение млекопитающему живого рекомбинантного штамма Mycobacterium bovis-BCG по любому из пп. 1-5.
12. Способ по п. 11, в котором млекопитающее представляет собой корову.
13. Способ по п. 11, в котором млекопитающее представляет собой человека.
14. Способ по п. 11, в котором живой рекомбинантный штамм Mycobacterium bovis-BCG вводят в присутствии адъюванта.
15. Способ лечения или профилактики рака мочевого пузыря у млекопитающего, предусматривающий введение млекопитающему живого рекомбинантного штамма Mycobacterium bovis-BCG по любому из пп. 1-5.
16. Способ по п. 15, в котором живой рекомбинантный штамм Mycobacterium bovis-BCG вводят в присутствии адъюванта.
| WO 2011130878 A1, 27.10.2011 | |||
| CIMINO M | |||
| ET AL | |||
| Identification of DNA binding motifs of the Mycobacterium tuberculosis PhoP/PhoR two-component signal transduction system | |||
| PLoS One | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| ANIL KUMAR V | |||
| ET AL | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| J Biol | |||
Авторы
Даты
2021-11-29—Публикация
2017-04-07—Подача