Предлагаемое изобретение относится к способам получения новых алюминийорганических соединений, конкретно к способу совместного получения 1-(алкокси)-2-фенилалюмациклопропана и 1-(алкокси)-2,4-дифенилалюмациклопентана общей формулы (1) и (2)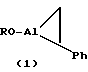
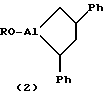
R = н-C6H13, н-C12H21, CH2Ph.
Предлагаемый способ может найти применение в тонком органическом, а также в металлорганическом синтезе.
Известен способ /У. М. Джемилев, А.Г. Ибрагимов, А.П. Золотарев, Р.Р. Муслухов, Г.А. Толстиков. Изв. АН СССР. Сер. хим. N 12, 1990, с. 2831-2841/ получения циклического кислородсодержащего алюминийорганического соединения, а именно 1-этил-3-(6-метоксигекс-4-ен-1-ил)алюмациклопентана общей формулы (3)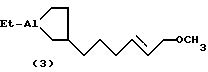
реакцией триэтилалюминия (Et3Al) с 1-метокси-2E, 7-октадиеном в присутствии катализатора Cp2ZrCl2 при температуре 25oC за 6 часов с выходом 81% по схеме: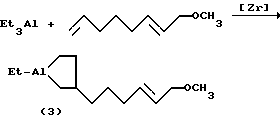
Известный способ не позволяет синтезировать 1-алкокси-2-фенилалюмациклопропаны (1) и 1-алкокси-2,4-дифенилалюмациклопентаны (2).
Известен способ /U.M. Dzhemilev, A.G. Ibragimov, A.B. Morozow. Mendeleev Commun, 1992, N 1. P. 26-28/ получения циклических кислородсодержащих алюминийорганических соединений, а именно 1-этокси-транс-3,4-диалкилзамещенных алюмациклопентанов общей формулы (4):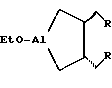
где R = н-C3H7, н-C5H11, н-C8H17,
реакцией α-олефинов (1-октен, 1-гексен, 1-ундецен) с этоксидихлораланом (EtO - AlCl2) в присутствии металлического магния (порошок) и катализатора Cp2ZrCl2 (5 мол.%) при температуре 20oC за 8 часов в ТГФ с выходом ≈ 75% по схеме: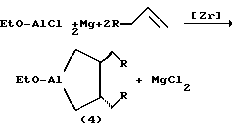
R = н-C3H7, н-C5H11, н-C8H17.
Известным способом не могут быть получены 1-(алкокси)-2-фенилалюмациклопропаны (1) и 1-(алкокси)-2,4-дифенилалюмациклопентаны (2).
Таким образом, в литературе совершенно отсутствуют сведения по региоселективному синтезу 1-(алкокси)-2-фенилалюмациклопропанов (1) и 1-(алкокси)-2,4-дифенилалюмациклопентанов (2).
Предлагается способ региоселективного синтеза новых типов алюминийорганических соединений, а именно 1-(алкокси)-2-фенилалюмациклопропана (1) и 1-алкокси-2,4-дифенилалюмациклопентана (2).
Поставленная цель достигается взаимодействием стирола с алкоксидихлораланами общей формулы RO - AlCl2, где R = н-C3H7, н-C5H11, н-C8H17, и металлическим магнием (порошок), взятых в мольном соотношении 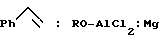 = 10: (10-14): (10-14), преимущественно 10:12:12, в присутствии катализатора четыреххлористого циркония (ZrCl4) в количестве 3-5 мол. % по отношению к стиролу, предпочтительно 4 мол.%, а атмосфере аргона при комнатной температуре (22-23oC) и нормальном давлении в ТГФ. Время реакции 6-10 часов. Общий выход целевых продуктов (1) и (2) составляет 64-86%. Соотношение (1) и (2) зависит от исходных алкоксидихлораланов (RO-AlCl2) и составляет в среднем ≈ 2:1. Реакция протекает по схеме:
= 10: (10-14): (10-14), преимущественно 10:12:12, в присутствии катализатора четыреххлористого циркония (ZrCl4) в количестве 3-5 мол. % по отношению к стиролу, предпочтительно 4 мол.%, а атмосфере аргона при комнатной температуре (22-23oC) и нормальном давлении в ТГФ. Время реакции 6-10 часов. Общий выход целевых продуктов (1) и (2) составляет 64-86%. Соотношение (1) и (2) зависит от исходных алкоксидихлораланов (RO-AlCl2) и составляет в среднем ≈ 2:1. Реакция протекает по схеме:
R = н-C6H13, н-C10H21, CH2Ph.
1-алкокси-2-фенилалюмациклопропан (1) и 1-(алкокси)-2,4-дифенилалюмациклопентан (2) образуются только лишь с участием алкоксидов алюминия (RO-AlCl2) под действием катализатора ZrCl4. В присутствии других соединений алюминия (например, i-Bu2AlH, i-Bu3Al; i-Bu2AlCl, AlEt2Cl, AlEt3) или другого катализатора (например, Zr(acac)4, Zr(OBu)4) целевые продукты (1) и (2) не образуются.
Проведение указанной реакции в присутствии ZrCl4 больше 5 мол.% не приводит к существенному увеличению выхода целевых продуктов. Использование катализатора менее 3 мол.% снижает выход 1-алкокси-2-фенилалюмациклопропана (1) и 1-(алкокси)-2,4-дифенилалюмациклопентана (2), что связано, по-видимому, со снижением каталитически активных центров в реакционной массе. Опыты проводили при комнатной температуре (22-23oC). При более высокой температуре (например, 60oC) увеличивается содержание продуктов уплотнения, а при меньшей температуре (например, 0oC) снижается скорость реакции.
Изменение соотношения исходных реагентов в сторону увеличения содержания алкоксидихлоранов (RO-AlCl2) или Mg по отношению к стиролу (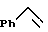 ) не приводит к существенному повышению выхода целевых продуктов (1) и (2).
) не приводит к существенному повышению выхода целевых продуктов (1) и (2).
Существенные отличия предлагаемого способа.
1. В предлагаемом способе используется катализатор ZrCl4 и в качестве исходного реагента стирол с системой сопряженных двойных связей, что и обуславливает формирование замещенных алюмациклопропанов (1) и 2,4-дизамещенных алюмациклопентанов (2). В известном способе применяются катализатор Cp2ZrCl2 и  олефины, содержащие изолированную концевую двойную связь, что обуславливает формирование исключительно транс-3,4-дизамещенных алюмациклопентанов (4).
олефины, содержащие изолированную концевую двойную связь, что обуславливает формирование исключительно транс-3,4-дизамещенных алюмациклопентанов (4).
Предлагаемый способ обладает следующими преимуществами.
1. Способ позволяет получать с высокой региоселективностью 1-(алкокси)-2-дифенилалюмациклопропаны (1) и 1-(алкокси)-2,4-дифенилалюмациклопентаны (2), синтез которых в литературе не описан.
Способ поясняется следующими примерами.
Пример 1. В стеклянный реактор объемом 50 мл, установленный на магнитной мешалке, в атмосфере аргона помещают 10 мл ТГФ, 10 ммоль стирола, 12 ммоль магния (порошок), 12 ммоль гексаноксидихлоралана и 0,4 ммоль ZrCl4, перемешивают 8 часов. Получают индивидуальные 1-(гексан-окси)-2-фенилалюмациклопропан (1) и 1-(гексан-окси)-2,4-дифенилалюмациклопентан (2) в соотношении ≈ 2: 1 с общим выходом 79%. Выход целевых продуктов определяли по продуктам гидролиза. При гидролизе 1-(гексан-окси)-2-дифенилалюмациклопропана (1) и 1-(гексан-окси)-2,4-дифенилалюмациклопентана (2) образуются соответственно этилбензол (5) и 1,3-дифенилбутан (6), при дейтеролизе целевых продуктов (1) и (2) получены соответственно 1,2-дидейтероэтилбензол (7) и 1,4-дидейтеро-1,3-дифенилбутан (8) по следующей схеме: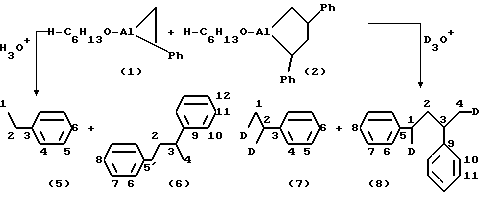
Спектр ЯМР 13C ( δ, м.д.) этилбензола (5): 15,6к (C1), 28,9 (C2), 144,2с (C3), 127,9 д (C4), 128,4 д (C5), 125,6 д (C6).
Спектр ЯМР 13C ( δ, м.д.) 1,3-дифенилбутана (6): 33,9 т (C1), 40,0 т (C2), 39,5 д (C3), 22,5 к (C4), 142,5 с (C5), 128,2 д (C6), 128,3 д (C7), 125,6 д (C8), 147,2 с( C9), 127,1 д (C10), 128.3 д (C11), 125,9 д (C12).
Спектр ЯМР 13C ( δ, м.д.) 1,2-дидейтероэтилбензола (7): 15,4 т (J13C-D = 22 Гц, C1), 28,6 т (J13C-D = 22 Гц, C2), 144,2 с (C3), 127,9 д (C4), 128,4 д (C5), 125,6 д (C6).
Спектр ЯМР 13C ( δ, м.д.) 1,4-дидейтеро-1,3-дифенилбутана (8): 33,5 т (J13C-D = 19,5 Гц, C1), 39,8 т (C2), 39,4 д (C3), 22,1 т (J13C-D = 19,5 Гц, C4), 142,4 с (C5), 128,2 д (C6), 128,3 д (C7), 125,6 д (C8), 147,2 с (C9), 127,0 д (C10), 128,3 д (C11), 125,9 д (C12).
Другие примеры, подтверждающие способ, приведены в таблице.
Реакции проводили при комнатной температуре (22-23oC) в ТГФ. Повышение температуры не целесообразно, т.к. не наблюдается существенного увеличения выхода целевых продуктов. При более низкой температуре снижается скорость реакции. Соотношение целевых продуктов зависит от исходных диалкоксидихлораланов и приближается к значению (1):(2) ≈ 2:1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-(ДИАЛКИЛАМИНО)-2-ФЕНИЛАЛЮМАЦИКЛОПРОПАНА И 1-(ДИАЛКИЛАМИНО)-2,4-ДИФЕНИЛАЛЮМАЦИКЛОПЕНТАНА | 1996 |
|
RU2156771C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(АЛКОКСИ)-2-ФЕНИЛ(АЛКИЛ)-АЛЮМАЦИКЛОПРОПАНОВ | 1996 |
|
RU2156769C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(ДИАЛКИЛАМИНО)-2-ФЕНИЛ(АЛКИЛ)АЛЮМАЦИКЛОПРОПАНОВ | 1996 |
|
RU2156770C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(АЛКОКСИ)-2-(2'-ФЕНИЛЭТИЛЕН)-3-ФЕНИЛАЛЮМАЦИКЛОПРОПАНОВ | 1997 |
|
RU2145327C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АЛКОКСИ (ИЛИ ДИАЛКИЛАМИНО)-2,3-ДИФЕНИЛ(АЛКИЛ)-АЛЮМАЦИКЛОПРОПЕНОВ | 1996 |
|
RU2151772C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-ЭТИЛ-2-ФЕНИЛАЛЮМАЦИКЛОПРОПАНА И 1-ЭТИЛ-2,4-ДИФЕНИЛАЛЮМАЦИКЛОПЕНТАНА | 1996 |
|
RU2153499C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АЛКОКСИ-3-АЛКИЛАЛЮМАЦИКЛОПЕНТАНОВ | 1998 |
|
RU2139877C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(ДИАЛКИЛАМИН)-2(2'-ФЕНИЛЭТИЛЕН)-3- ФЕНИЛАЛЮМАЦИКЛОПРОПАНОВ | 1997 |
|
RU2145328C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-ЭТИЛ-2,4-ДИАЛКИЛ(АРИЛ)АЛЮМАЦИКЛОПЕНТАДИЕНОВ И 1-ЭТИЛ-2-АЛКИЛ(АРИЛ)АЛЮМАЦИКЛОПРОПЕНОВ | 1997 |
|
RU2130026C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(ДИАЛКИЛАМИН)-3-АЛКИЛАЛЮМАЦИКЛОПЕНТАНОВ | 1998 |
|
RU2139876C1 |

Изобретение относится к способу совместного получения 1-(алкокси)-2-фенилалюмациклопропана формулы (1) и 1-(алкокси)-2,4-дифенилалюмациклопентана формулы (2), где R - н-С6Н13, н-С10Н21, CH2Ph, который заключается во взаимодействии стирола с алкоксидихлораланами общей формулы RO - AlCl2 и металлическим магнием, взятыми в мольном соотношении 10 : 10-14 : 10-14 соответственно в присутствии катализатора четыреххлористого циркония в атмосфере аргона в среде тетрагидрофурана при нормальных условиях в течение 6-10 ч. Предлагаемый способ может найти применение в тонком органическом, а также металлоорганическом синтезе и позволяет получать совместно 1-(алкокси)-2-фенилалюмациклопропан и 1-(алкокси)-2,4-дифенилалюмациклопентан с высокой степенью региоселективностью. 1 табл.
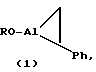
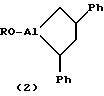
Способ совместного получения 1-(алкокси)-2-фенилалюмациклопропана формулы 1 и 1-(алкокси)-2,4-дифенилалюмациклопентана формулы 2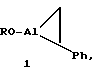

где R - н-C6H13, н-C10H21, CH2Ph,
отличающийся тем, что стирол  подвергают взаимодействию с алкоксидихлораланами общей формулы
подвергают взаимодействию с алкоксидихлораланами общей формулы
RO-AlCl2,
где R описан выше,
и металлическим магнием, взятыми в мольном соотношении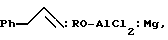
равном 10:10-14:10-14, в присутствии катализатора четыреххлористого циркония ZrCl4 в количестве 3-5 мол.% по отношению к стиролу, в атмосфере аргона при нормальных условиях в среде тетрагидрофурана в течение 6-10 ч.
| DZHEMILEV U.M | |||
| et al., Mendeleev Commun., 1992, N 1, с | |||
| Прибор для получения стереоскопических впечатлений от двух изображений различного масштаба | 1917 |
|
SU26A1 |
| ДЖЕМИЛЕВ У.М | |||
| и др | |||
| Ретоселективный синтез β-замещенных алюмоциклопентанов циклометаллированием α-олефинов с помощью EtAl в присутствии CpZrCl | |||
| Известия АН СССР | |||
| Серия химическая | |||
| Способ приготовления консистентных мазей | 1919 |
|
SU1990A1 |
| СЛОЖНАЯ СТОЙКА ДЛЯ КРЕПЛЕНИЯ ГОРНЫХ ВЫРАБОТОК | 1921 |
|
SU2831A1 |
| Способ получения 1-хлор-(транс-3,4-диалкил)алюмоциклопентанов | 1990 |
|
SU1792940A1 |
| EP 342444 A2, 28.11.1990. | |||
Авторы
Даты
2000-09-27—Публикация
1996-05-30—Подача