Изобретение относится к молекулярной биологии и биотехнологии, а точнее к способу иммобилизации олигонуклеотидов в органических полимерных гелях, получаемых сополимеризацией непредельных мономеров, где в качестве одного из мономеров служат олигонуклеотиды, модифицированные непредельными фрагментами. Изобретение может найти применение при секвенировании и картировании ДНК, в генетическом анализе, детектировании мутаций, в медицине и для других приложений.
Известный способ иммобилизации олигонуклеотидов в органических гелях [Rehman F.N., Audeh М., Abrams E.S., Hammond P.W., Boles T.C., Nucleic Acids Res., 27 (1999) 649-655] состоит в сополимеризации модифицированных непредельными группами олигонуклеотидов с акриламидом и N,N'- метиленбисакриламидом. Синтез соответствующих олигонуклеотидов осуществляется с использованием фосфорамидита AcryditeTM, производимого фирмой "Mosaic Technologies". Этот продукт позволяет вводить по 5'- положению олигонуклеотида акриламидный фрагмент.
В соответствии с этим способом иммобилизация олигонуклеотидов, модифицированных с помощью фосфорамидита AcryditeTM, в полиакриламидном геле проводится путем сополимеризации акриламида, N,N'-метиленбисакриламида и модифицированного олигонуклеотида под действием катализаторов - персульфата аммония и тетраметилэтилендиамина.
Недостатками этого способа иммобилизации являются следующие.
Стабильность акриламидных производных олигонуклеотидов, определяемая стабильностью акриламидного фрагмента, невысока. В то же время для изготовления олигонуклеотидных микрочипов необходимо содержать библиотеку модифицированных олигонуклеотидов и часто ее использовать. Это означает проведение многочисленных циклов заморозки - разморозки растворов олигонуклеотидов и заметное время их выдерживания при комнатной температуре. Известно, что растворы акриламида в буферных растворах легко подвергаются самопроизвольной полимеризации при комнатной температуре. Таким образом, наличие реакционноспособного и малостабильного акриламидного фрагмента в составе олигонуклеотидов заметно сужает область возможных применений данного метода иммобилизации.
Другим недостатком известного способа является ограничение в положении модификации олигонуклеотидов. Введение акриламидного звена с помощью реагента AcryditeTM возможно лишь по 5'-концевому положению, тогда как в большом числе случаев требуется провести модификацию этого положения какой либо другой группой, например, флуоресцентным красителем.
В основу предлагаемого изобретения положена задача повышения устойчивости олигонуклеотидов, модифицированных непредельными группами, способными к сополимеризации с акриламидом и N,N'-метиленбисакриламидом, и реализация возможности введения таких реакционноспособных групп в любое заранее заданное положение олигонуклеотидной цепи.
Поставленная задача решена тем, что в заявляемом способе иммобилизации олигонуклеотидов в органических полимерных гелях методом сополимеризации модифицированных непредельными фрагментами олигонуклеотидов с ненасыщенными мономерами в качестве непредельных фрагментов используют группы общей формулы R1R2C= CR3R4, где R1 и R4 - H или алкил C1-С3; R2 - (CH2)n-O-Х и R3 - (CH2)n-O-Y, n= 1-6; X и Y - фосфодиэфирные группы, связывающие непредельные фрагменты с соседними нуклеотидными звеньями или соседними непредельными фрагментами, или одна из групп X или Y представляет собой атом водорода, которые вводят в синтетический олигонуклеотид в ходе стандартного фосфорамидитного метода с использованием фосфорамидитов общей формулы R5R6C=CR7R8, где R5 - R8 - H или алкил C1-C3; R6 - (CH2)n-O-Р(OCH2CH2CN)(N(C3H7)2)2,
n=1-6; R7 - -(CH2)n-O-DMT, n=1-6 (DMT = 4,4'-диметокситритил).
Указанные фосфорамидиты можно использовать как "строительные блоки" на любой стадии олигонуклеотидного синтеза, т.е. вводить непредельные фрагменты в любое заранее заданное положение олигонуклеотидной цепи. Эти "блоки" получают из непредельных соединений, содержащих гидроксильную группу, реакцией с 2-цианэтил-N, N,N',N'- тетраизопропилфосфорамидитом в ацетонитриле в присутствии 1H- тетразола.
Для предотвращения в ходе олигонуклеотидного синтеза нежелательных реакций по двойной связи непредельного фрагмента стандартный раствор окислителя заменяют на 0,1 М раствор трет-бутилгидропероксида в тетрагидрофуране.
Целесообразно в качестве одного из мономеров при сополимеризации использовать акриламид.
Способ иммобилизации олигонуклеотидов может быть реализован в двух вариантах:
1) путем фотоинициируемой сополимеризации, при которой смесь непредельных мономеров, включая модифицированный олигонуклеотид, содержащую все необходимые добавки, такие как TEMED, глицерин и другие компоненты, подвергают воздействию УФ или видимого света, в результате чего происходит полимеризация.
При использовании данного способа иммобилизации, например, для изготовления олигонуклеотидных матриц, фотоинициируемая сополимеризация проводится между двумя стеклами, одно из которых служит маской. Маска может быть изготовлена из обычного или кварцевого стекла. Формирование гелевой ячейки с иммобилизованным олигонуклеотидом происходит лишь в зонах, соответствующих прозрачным окошкам в маске. При этом топология микроматрицы соответствует расположению окошек на маске. Иммобилизация индивидуального олигонуклеотида в каждой отдельной ячейке достигается либо путем физического разделения зон полимеризации, либо путем последовательного проведения циклов сополимеризации отдельных олигонуклеотидов;
2) путем химически индуцируемой сополимеризации смеси непредельных мономеров под действием системы персульфат аммония - TEMED.
Изготовление микроматриц с помощью химически индуцируемой сополимеризации проводится следующим образом. Смеси непредельных мономеров, содержащих индивидуальные олигонуклеотиды и другие необходимые компоненты, кроме одного (например TEMED), распределяются в виде микрокапель по поверхности стекла или другой поверхности с помощью какого либо наносящего устройства. Таким устройством может являться микропипетка, пиновый наноситель, струйный принтер или другое устройство. После формирования матрицы растворов мономеров стекло погружается в раствор органического растворителя, содержащий компонент, необходимый для инициирования полимеризации (TEMED). Органический растворитель не смешивается с растворами мономеров, препятствуя таким образом возможному перемешиванию растворов с различными олигонуклеотидами.
Заявляемый способ иммобилизации пригоден для использования в изготовлении полиакриламидных олигонуклеотидных микроматриц с размерами ячеек от 5 микрон.
Предлагаемое изобретение поясняется следующими фигурами и примерами, где
на фиг. 1 представлена схема синтеза одного из фосфорамидитов, используемого в качестве "строительного блока" для синтеза модифицированных непредельными группами олигонуклеотидов,
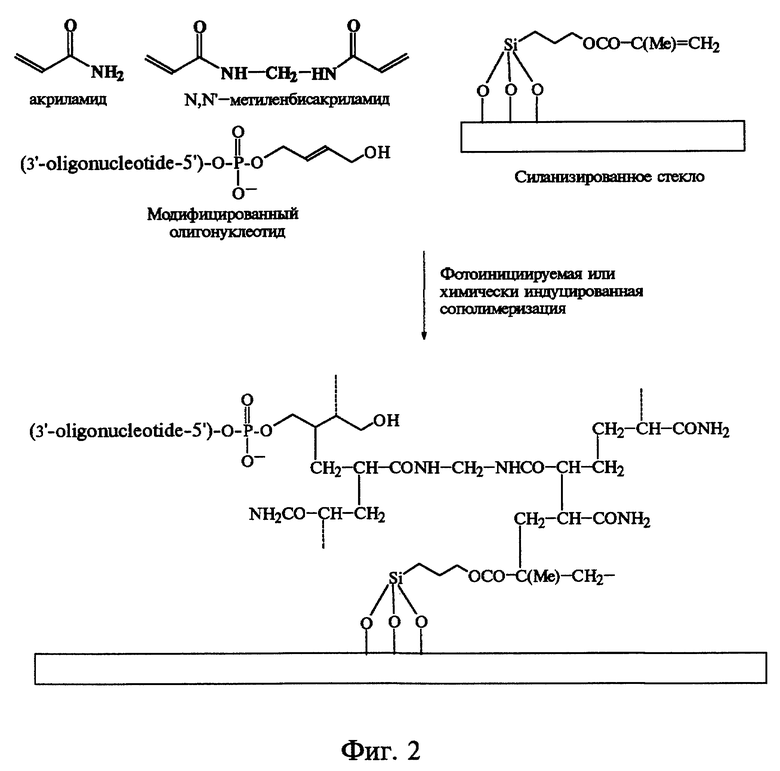
на фиг. 2 - схема фотоинициируемой или химически индуцируемой иммобилизации олигонуклеотидов,
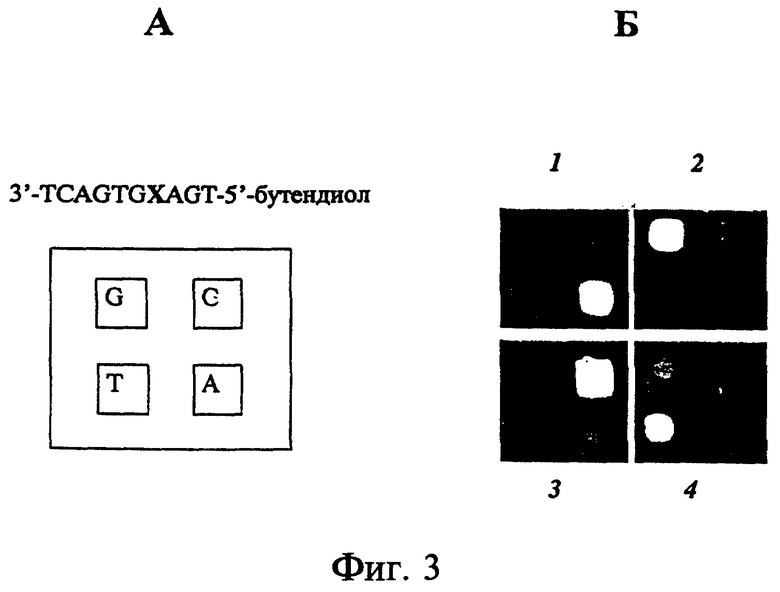
на фиг. 3 - использование иммобилизованных с помощью фотоинициируемой сополимеризации олигонуклеотидов для гибридизации,
на фиг. 4 - использование иммобилизованного с помощью химически индуцируемой сополимеризации олигонуклеотида для гибридизации.
Пример 1. Синтез фосфорамидита О-диметокситритилбут-2-ен-1,4-диола.
К раствору 5 ммолей бут-2-ен-1,4-диола в 50 мл пиридина добавляют 1 ммоль 4,4'-диметокситритилхлорида при перемешивании. Ход реакции контролируют с помощью ТСХ в системе хлороформ- метанол-гексан (9:1:10). По завершении реакции пиридин упаривают, к остатку добавляют толуол и упаривают снова. Вязкую массу растворяют в хлороформе и промывают водой. Хлороформенный раствор сушат сульфатом натрия и упаривают. Остаток очищают хроматографией на силикагеле. Выход продукта после очистки составляет 80%. Монозащищенный диол (0.5 ммоля) растворяют в 2 мл безводного ацетонитрила и добавляют 1 экв. 1H-тетразола и 1.1 экв. 2-цианэтил-N,N,N'N'-тетраизопропилфосфорамидита. Ход реакции контролируют с помощью ТСХ в системе хлороформ-метанол-гексан (9: 1:10). По завершении реакции реакционную смесь разбавляют этилацетатом до 100 мл и последовательно промывают водным раствором бикарбоната натрия и водой. Органический слой сушат сульфатом натрия и упаривают. Выход целевого продукта составляет 90%. Схема синтеза показана на фиг. 1.
Пример 2. Фотоинициируемая сополимеризация модифицированных олигонуклеотидов.
Раствор мономеров для сополимеризации содержит 5% смеси акриламид-N, N'-метиленбисакриламид (19:1), 40% глицерина, 0,1 М натрий-фосфатный буфер, pH 7.0, 1.2% TEMED, 0.002% метиленового синего и 0.3 мМ раствор олигонуклеотида, модифицированного непредельной группой (0.2 мкл). Полимеризацию проводят в УФ-печи (Stratalinker 1800-UV) при облучении светом 254 нм (фиг. 2).
Сополимеризацию используют для изготовления микроматрицы с размером ячеек 500 микрон. После каждого цикла сополимеризации стекло с приполимеризованными ячейками промывают водой в течение 5 мин. Затем меняют маску и раствор олигонуклеотида и повторяют полимеризационный цикл. Маска имеет только одно квадратное окно в разных положениях по отношению к матрице. Контроль иммобилизации осуществляют, наблюдая связывание комплементарных флуоресцентно меченных олигонуклеотидов (фиг. 3).
Пример 3. Химически индуцируемая сополимеризация модифицированных олигонуклеотидов.
Капли раствора, содержащего 5% смеси акриламид-N,N'- метиленбисакриламид (19: 1), 0.1 М натрий-фосфатный буфер, pH 7.0, 40% глицерина, 0.05% персульфата аммония и 0.3 мМ олигонуклеотида, модифицированного непредельными фрагментами (0.2 мкл), наносят микродозатором на поверхность стекла. Стекло предварительно обрабатывают 13-(триэтоксисилил)пропил]метакрилатом. Сформированную матрицу растворов погружают в 80 мл 0.5% раствора TEMED в гексане. Полимеризация обычно занимает 1 час при комнатной температуре. После этого микроматрицу отмывают водой в течение 1 часа при 60oC и высушивают (фиг. 2). Контроль иммобилизации осуществляют, наблюдая связывание комплементарного флуоресцентно меченного олигонуклеотида (фиг. 4).

Изобретение относится к молекулярной биологии и биотехнологии, а точнее к способу иммобилизации олигонуклеотидов в органических полимерных гелях. Изобретение может найти применение при секвенировании и картировании ДНК, в генетическом анализе, детектировании мутаций, в медицине и для других приложений. Описывается способ иммобилизации олигонуклеотидов в органических полимерных гелях методом сополимеризации модифицированных непредельными фрагментами олигонуклеотидов с ненасыщенными мономерами, причем в качестве непредельного фрагмента олигонуклеотида используется одна или несколько групп общей формулы R1R2C=СR3R4, где R1 и R4 - H или алкил C1-C3; R2 - (CH2)n-O-X и R3 - (CH2)n-O-Y, n = 1 - 6; X и Y - фосфодиэфирные группы, связывающие непредельные фрагменты с соседними нуклеотидными звеньями или соседними непредельными фрагментами, или одна из групп X или Y представляет собой атом водорода, которые вводят в олигонуклеотид в ходе стандартного фосфорамидитного олигонуклеотидного синтеза с использованием фосфорамидитов общей формулы R5R6C = CR7R8, где R5 и R8 - H или алкил C1-C3; R6 - (CH2)n-O-P(OCH2CH2CN)(N(C3H7)2)2, n = 1 - 6; R7 - -(CH2)n-O-DMT, n = 1 - 6 (DMT = 4,4'-диметокситритил). Технический результат - повышение устойчивости олигонуклеотидов, модифицированных непредельными группами, способными к сополимеризации с акриламидом и N,N'-метиленбисакриламидом, и реализация возможности введения таких реакционноспособных групп в любое заранее заданное положение олигонуклеотидной цепи. 3 з.п. ф-лы, 4 ил.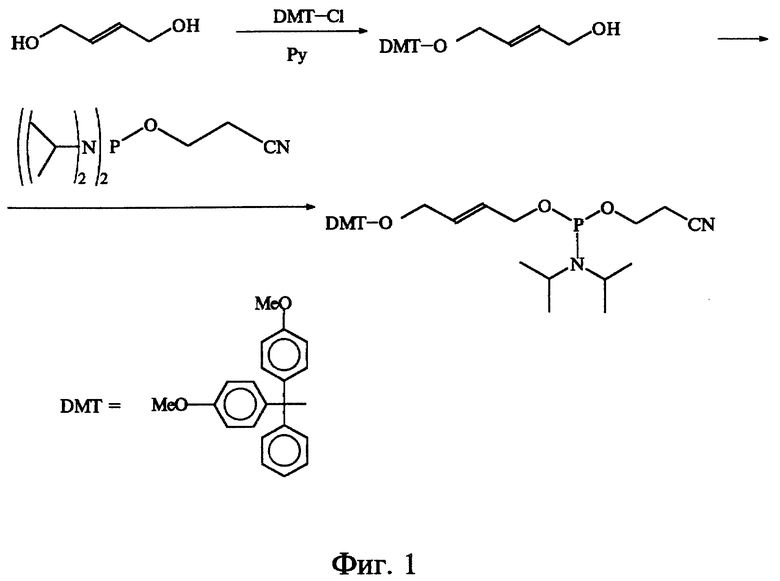
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| US 5981734 А, 09.11.1999 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| US 5412087 А, 02.05.1995 | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| ВАСИЛИСКОВ В.А | |||
| и др | |||
| Метод получения микрочипов с помощью сополимеризации с акриламидом | |||
| Молекулярная биология | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| US 5837860 А, 17.11.1998. | |||
Авторы
Даты
2000-10-10—Публикация
1999-07-19—Подача