Область техники, к которой относится данное изобретение
Настоящее изобретение относится к генам агглютинации дрожжей, а также к дрожжам, которые их содержат.
Предпосылки создания изобретения
В ферментационной промышленности агглютинация дрожжей представляет собой весьма важное явление, и в этой связи дрожжи, способные к агглютинации, достаточно интенсивно изучались с целью выявления причины, вызывающей агглютинацию. Известно, что агглютинация дрожжей контролируется множеством генов, среди которых относительно хорошо изученные принадлежат к гену агглютинации FL01, который картирован на правой ветви дрожжевой хромосомы 1.
Структура гена агглютинации FL01, полученного из дрожжей Sacharomyces cerevisiae, была абсолютно неизвестной, но в 1989 году ген был клонирован впервые авторами настоящего изобретения с соавторами, при этом была получена рестрикционная карта гена (Watari et al., Agricultural and Biological Chemistry, Vol. 53, N 3, p. 901-903, 1989). (Тем не менее, последовательность нуклеотидных оснований оставалась неизвестной).
Мы, авторы настоящего изобретения, сообщали о возможности превращать промышленные дрожжи, не обладающие способностью к агглютинации, в дрожжи, обладающие способностью к агглютинации, для их практического использования путем введения гена агглютинации FL01 в различные промышленные дрожжи (Watari et al. , Agricultural and Biological Chemistry, Vol. 55, N 6, p. 1547-1552, 1991); однако, не всегда было возможно придать сильные и стабильные агглютинирующие свойства всем промышленным дрожжам.
Мы, авторы настоящего изобретения, продолжали далее интенсивно изучать FL01 ген и обнаружили при этом, что данный ген, который мы, авторы настоящего изобретения с соавторами, рассматривали как ген FL01 (Watari et al., Agricultural and Biological Chemistry, Vol. 53, N 3, p. 901-903, 1989), не был интактным FL01 геном, присутствующим на хромосоме 1 дрожжей Sacharomyces cerevisiae, штамм ABXL-ID, но представлял собой FL01 ген, часть которого была делетирована в процессе поддержания плазмиды в Esherichia coli, штамм К12, содержащий интактный FL01 ген (этот ген мы дальше будем называть как FL01S).
Раскрытие изобретения
Целью настоящего изобретения является определение структуры интактного FL01 гена (этот ген мы будем далее определять как FL01L), а также разработка технологии придания более сильных и более стабильных агглютинирующих свойств различным промышленным дрожжам.
К настоящему времени мы, авторы настоящего изобретения, в результате различных исследований, связанных с FL01 геном, смогли выделить интактный FL01 ген или FL01L ген, определили полную нуклеотидную последовательность этого гена и открыли далее, чем при использовании FL01L гена возможно выращивать для промышленного использования различные дрожжи с более сильными и стабильными агглютинирующими свойствами, чем это было возможно с использованием FL01S гена, и на этом настоящее изобретение завершается.
Другими словами, настоящее изобретение относится к гену агглютинации размером 4,7±0,2 кb в дрожжах, который кодирует полипептид, обладающий агглютинирующей активностью, а более специфично оно относится к вышеупомянутому гену агглютинации, полученному из дрожжей Sacharomyces cerevisiae, характеризующемуся рестрикционной картой, представленной на фиг. 1, а более специфично оно относится к вышеупомянутому гену агглютинации, который принципиально кодирует аминокислотную последовательность, представленную в Последовательности N 1.
Настоящее изобретение относится также к гену агглютинации размером 2,6±0,2 кb в дрожжах, который кодирует полипептидную цепь, обладающую агглютинирующей активностью, и более специфично, к гену агглютинации, полученному из дрожжей Sacharomyces cerevisiaе, определенному картой рестрикционного расщепления, представленной на фиг. 2, и более специфично к гену агглютинации, кодирующему аминокислотную последовательность, представленную в Последовательности N 2.
Далее настоящее изобретение относится к дрожжам, либо содержащим вышеупомянутый ген агглютинации, либо имеющим агглютинирующие свойства.
"Ген агглютинации" в контексте настоящего описания используется для определения гена, который контролирует агглютинацию дрожжей.
Действие изобретения
Как описано выше, гены агглютинации, в соответствии с настоящим изобретением, способны придавать агглютинирующие свойства неагглютинирующим дрожжам Sacharomyces cerevisiae. Значение использования дрожжей, обладающих агглютинирующими свойствами в ферментационной промышленности, состоит в том, что:
1) клетки могут быстро быть отделены от ферментационной среды по завершении ферментации и таким образом процесс может быть упрощен так, что отпадает необходимость проведения других процедур для отделения дрожжей от ферментационной среды, включая центрифугирование и т.д.;
2) ферментируемая масса обладает достаточно высокой степенью прозрачности, при этом груз снижается во время последнего фильтрования ферментируемой массы и, таким образом, повышается эффективность процесса;
3) возможна непрерывная ферментация так же, как с иммобилизованными клетками, при этом не требуется реакторов или какого-то специального оборудования.
Кроме того, ранее предпринимались попытки выращивания дрожжей, обладающих способностью к агглютинации, с использованием метода индукции, методов получения гибридов, слияния клеток и т.д. для естественных или искусственных мутантов, но при этом очень часто сообщалось о том, что такие методы сопровождаются изменением генетических свойств исходного выращиваемого штамма и обычно нарушением желательных свойств исходного варианта. Однако, в соответствии с настоящим изобретением, возможно улучшать агглютинирующие свойства выращиваемых штаммов просто путем введения в них генов, которые не нарушают других желательных свойств исходного штамма, что является основным преимуществом предлагаемого в изобретении метода.
Краткое описание чертежей
Фиг. 1.
Карта рестрикционного расщепления FL01L гена в соответствии с настоящим изобретением. На чертеже сайты расщепления каждого рестрикционного энзима изображены как Ac для AccI, B для BglI, RV для EcoRV, K для KpnI, Pv для PvuII.
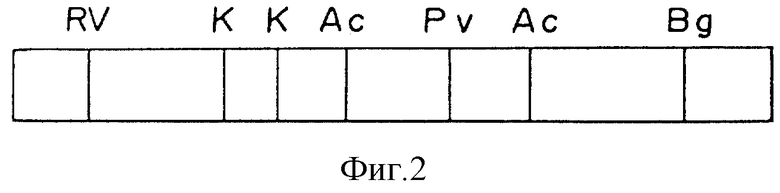
Фиг. 2.
Карта рестрикционного расщепления FL01S гена в соответствии с настоящим изобретением.
На чертеже сайты расщепления каждого рестрикционного энзима отражаются как Ac для AccI, Bg для BglII, RV для EcoRV, K для KpnI, Pv для PvuII.
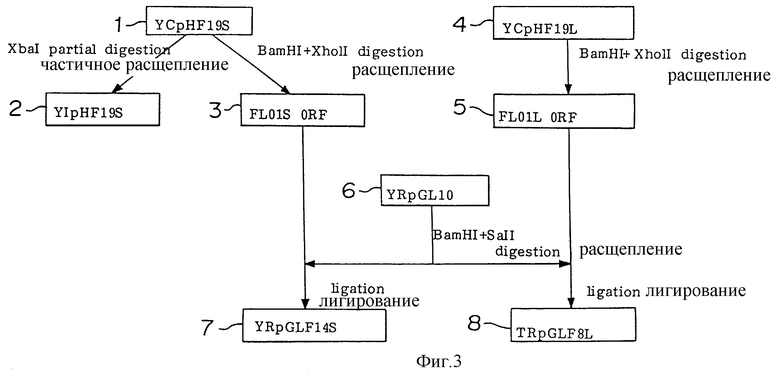
Фиг. 3
Схема получения плазмид YRpGLF14S и YRpGLF8L, содержащих гены агглютинации EL01S и FL01L, для прямой селекции дрожжей.
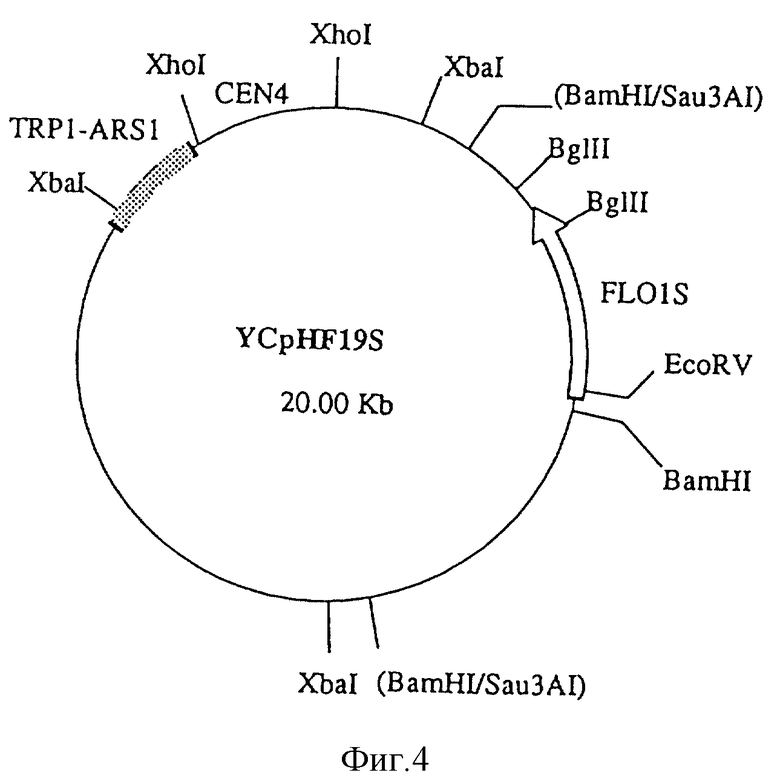
Фиг. 4
YCpHF19S (20,00 кb).
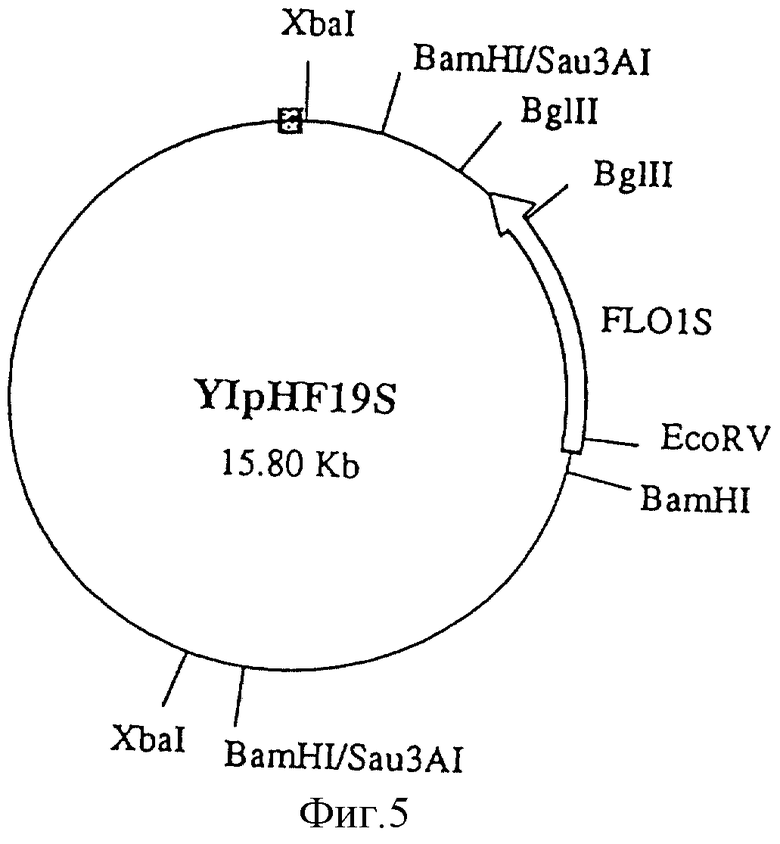
Фиг. 5.
YIpHF19S (15,80 кb).
Фиг. 6
5,8 кb BamHI - XhoI фрагмент YCpHF19S, содержащий FL01S ген.
Фиг. 7
YCpHF19L (22,10 кb)
Фиг. 8
7,9 кb BamHI-XhoI фрагмент YCpHF19L, содержащий FL01L ген.
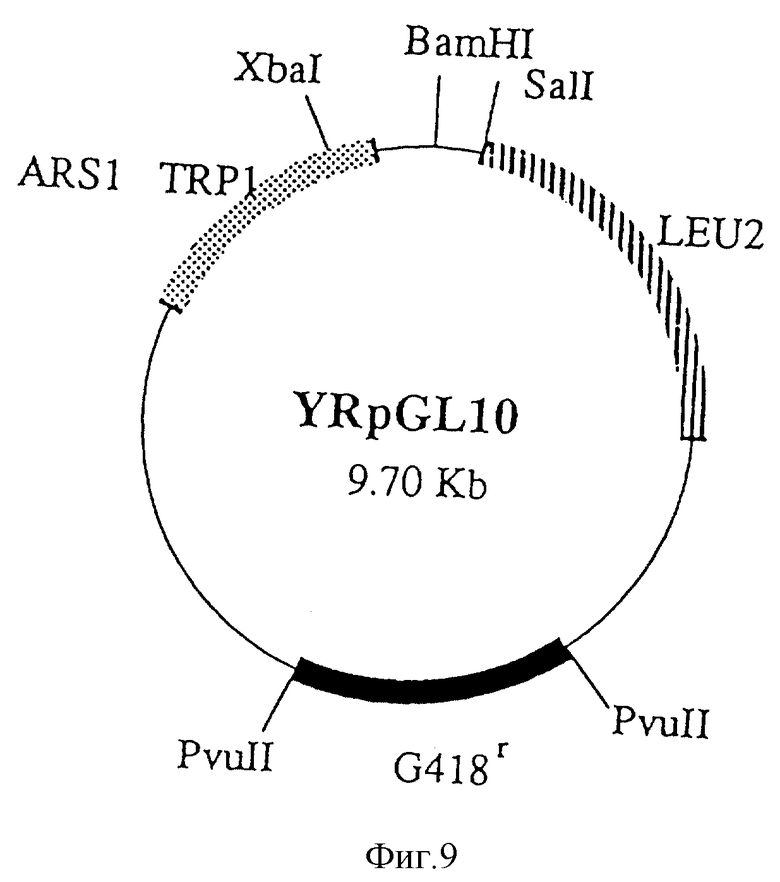
Фиг. 9
YRpGL10 (9,70 кb).
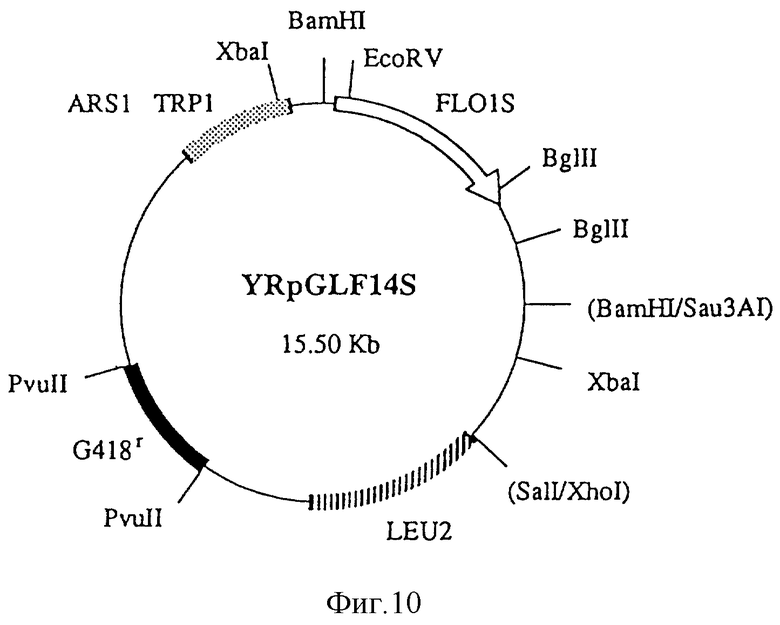
Фиг. 10.
YRpGLF14S (15,50 кb).
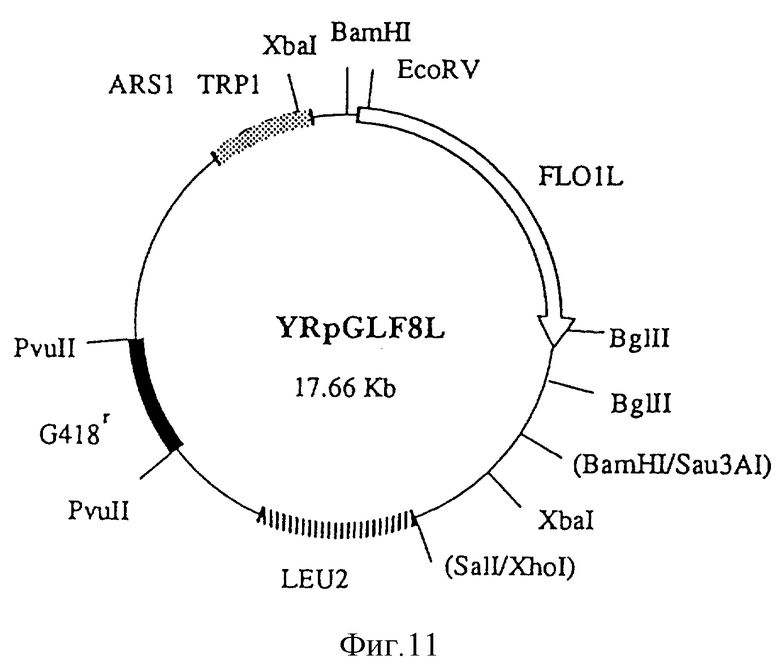
Фиг. 11
YRpGLF8L (17,66 кb).
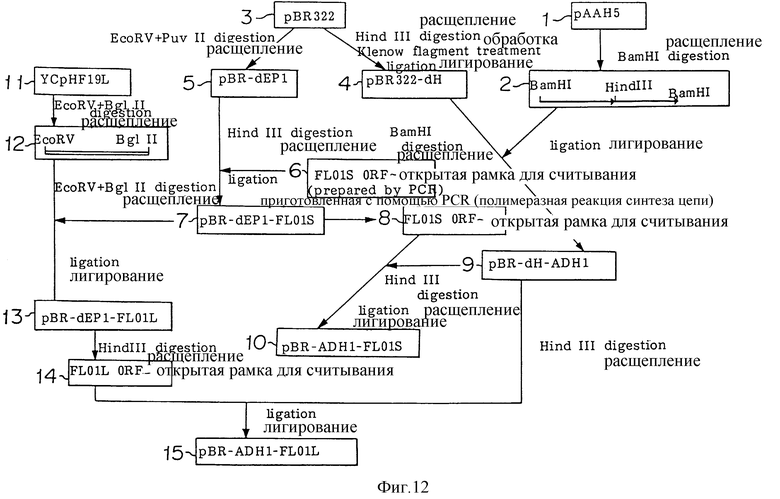
Фиг. 12
Схема получения плазмид pBR-ADHI-FL01S и pBR-ADHI-FL01L, содержащих гены агглютинации FL01S и FL01L, для включения в хромосомы дрожжей.
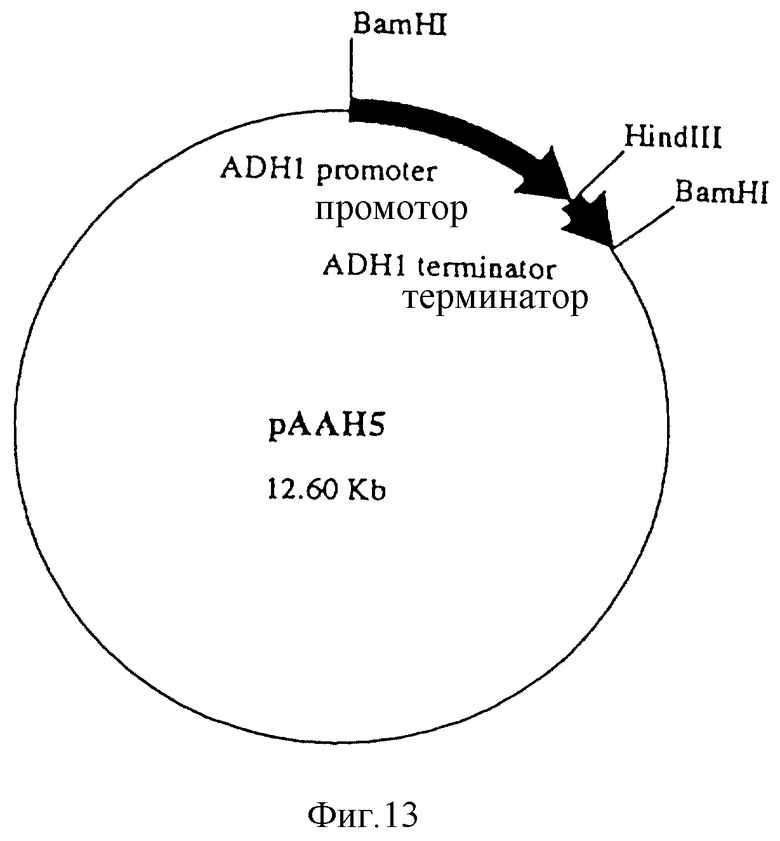
Фиг. 13
pAAH5 (12,60 кb).
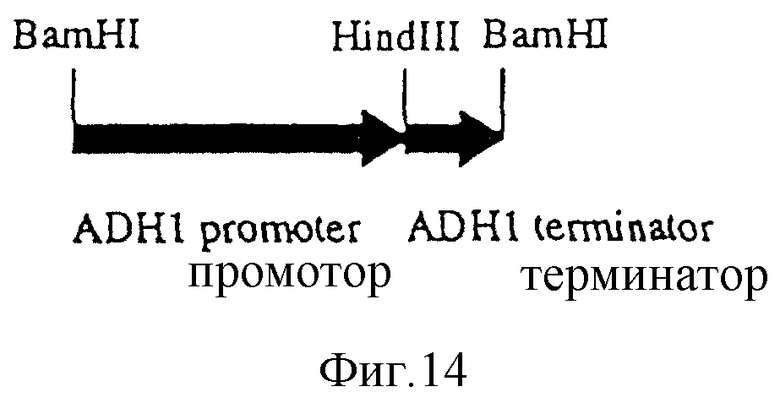
Фиг. 14
pAAH5, расщепленная BamHI (12,60 кb).
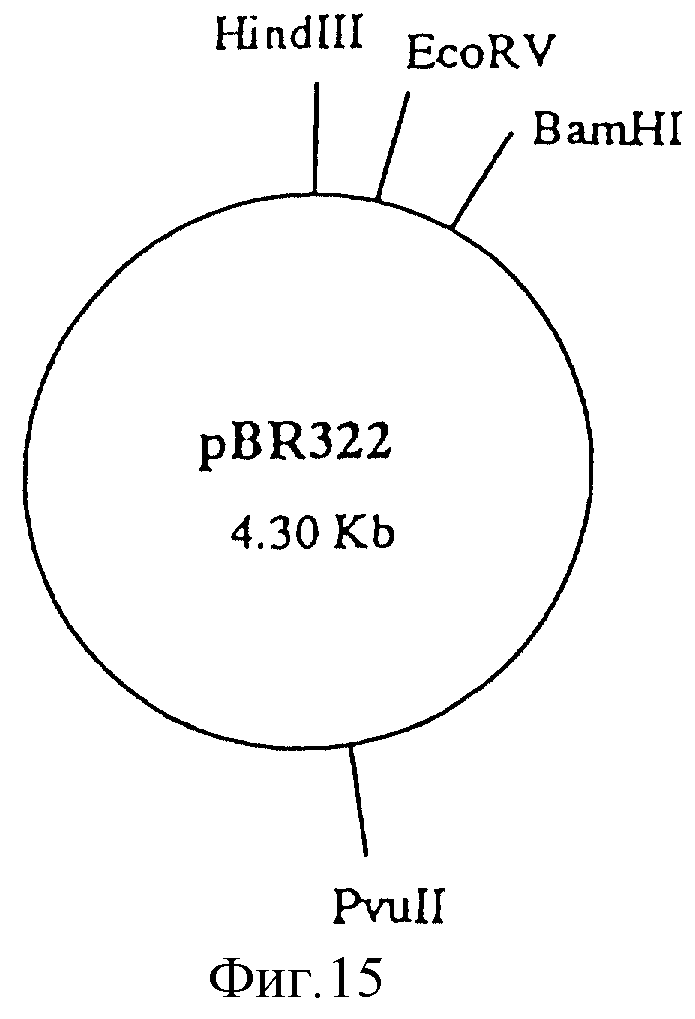
Фиг. 15
pBR322 (4,30 кb).
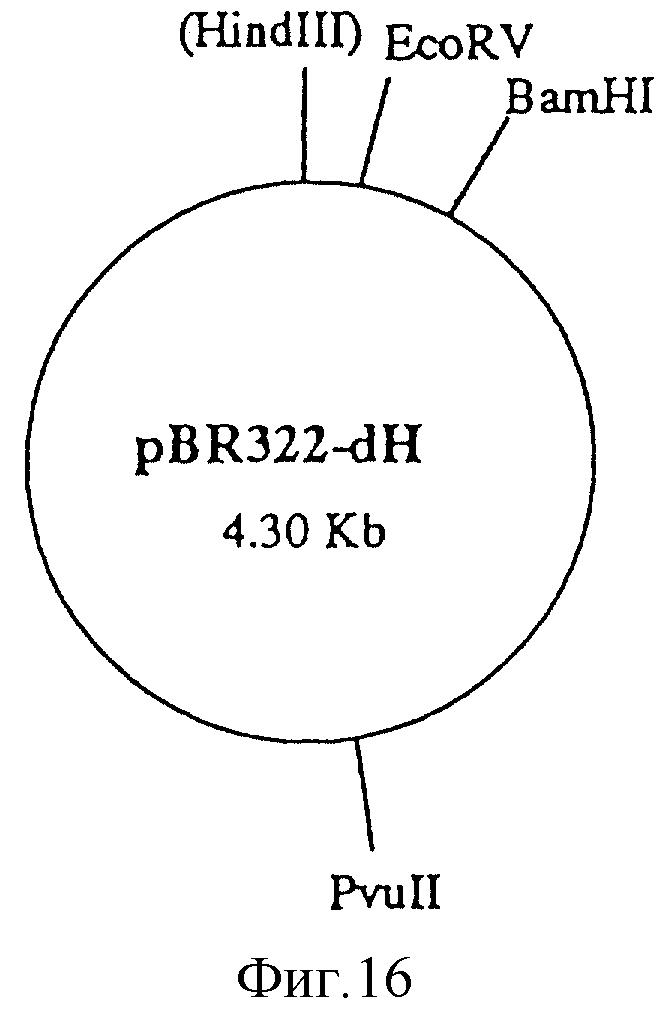
Фиг. 16
pBR322-dH (4,30 кb).
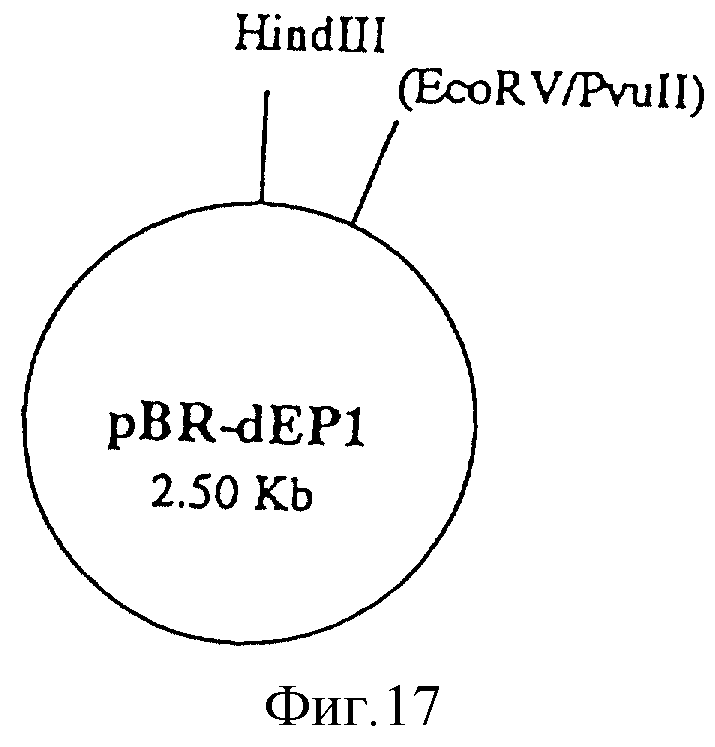
Фиг. 17
pBR-DEP1 (2,50 кb).
Фиг. 18
Открытая рамка считывания FL01S, полученная с помощью PCR.
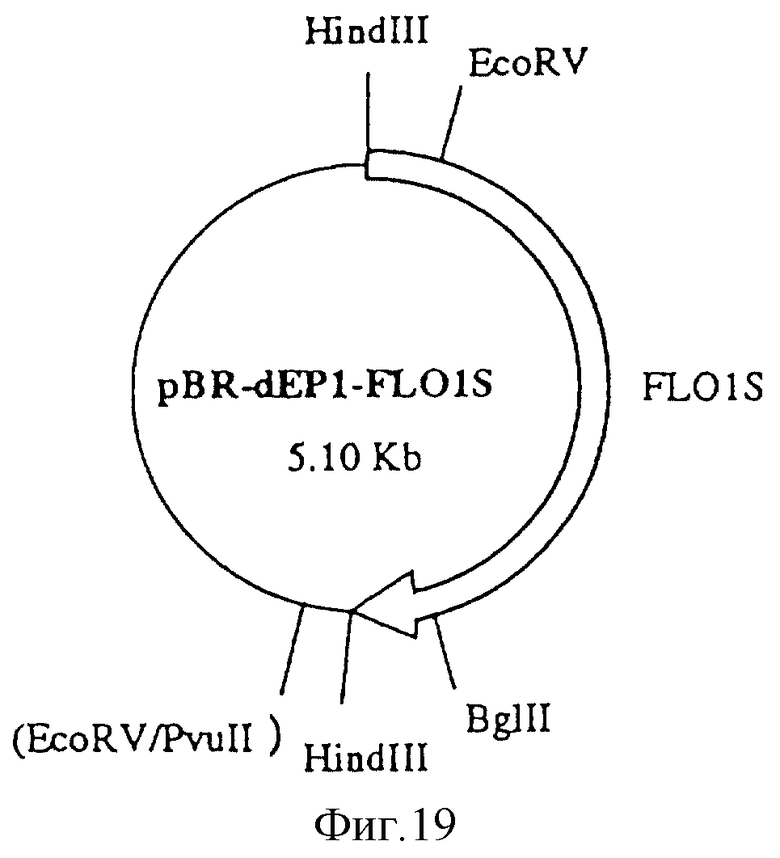
Фиг. 19
pBR-dEP1-FL01S (5,1 кb).
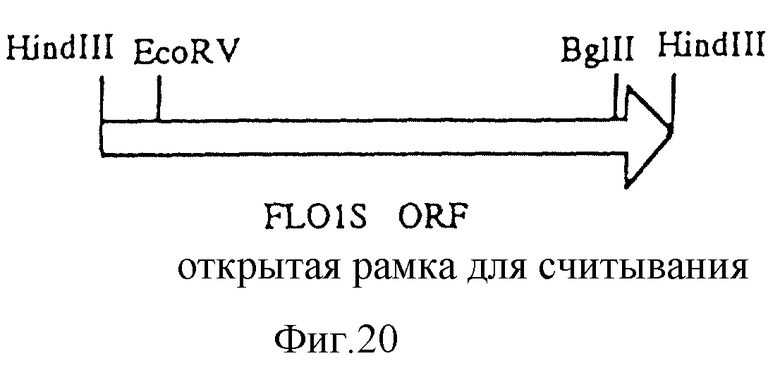
Фиг. 20
Открытая рамка считывания FL01L.
Фиг. 21
pBR-dH-ADHI (6,20 кb).
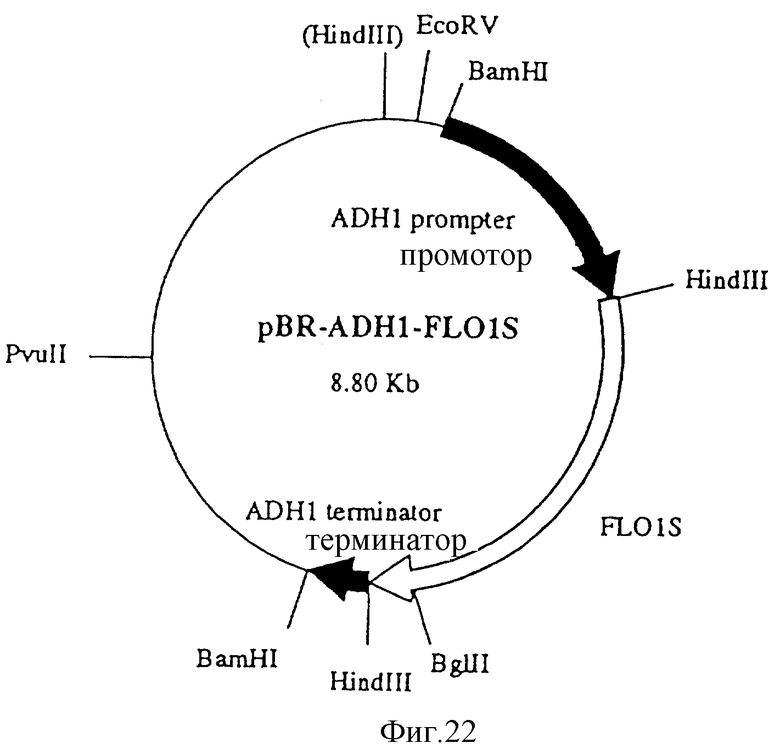
Фиг. 22
pBR-ADHI-FL01S (8,80 кb).
Фиг. 23
YCpHF19L (22,10 кb).
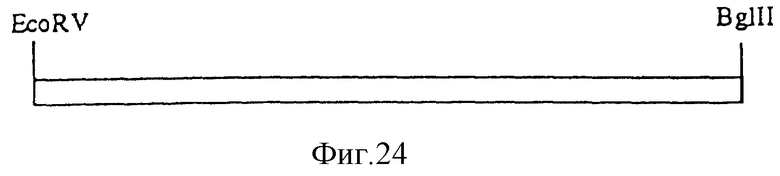
Фиг. 24
YCpHF19L, расщепленная EcoRv + BglII.
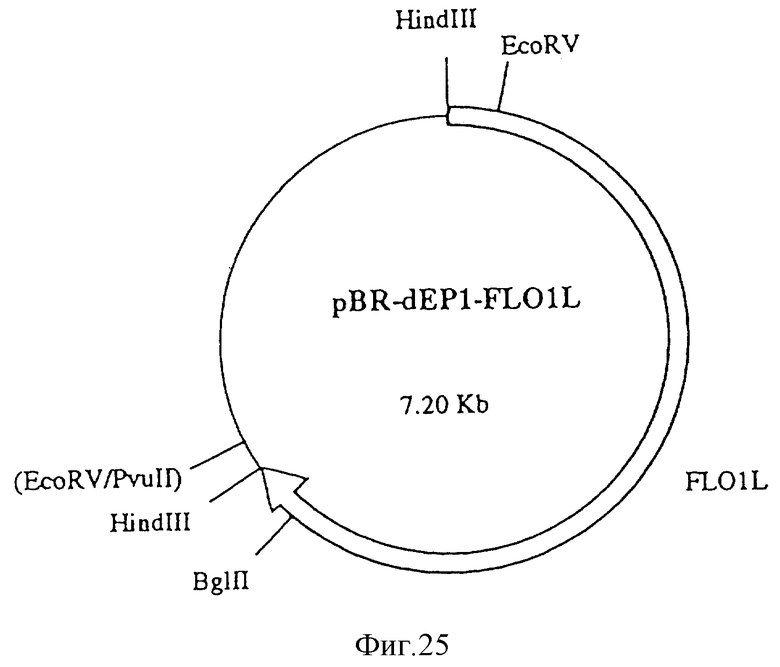
Фиг. 25
pBR-dEP1-FL01L (7,20 кb).
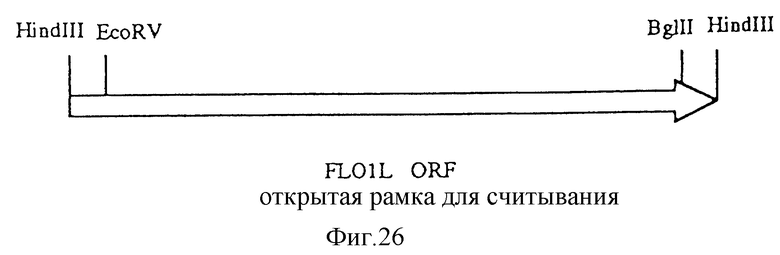
Фиг. 26
Открытая рамка считывания FL01L.
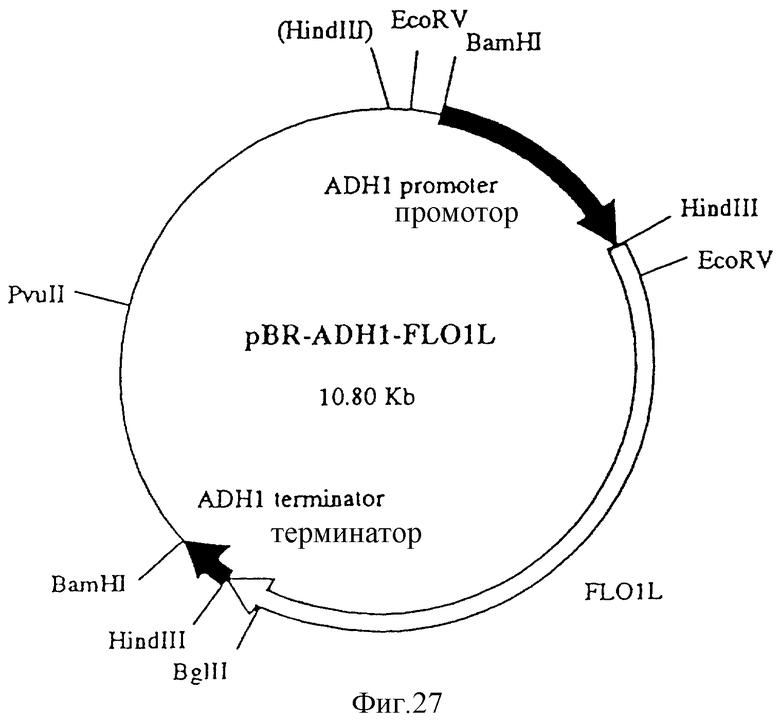
Фиг. 27
pBR-ADHI-FL01L (10,80 кb).
Предпочтительный способ реализации изобретения
Более конкретное объяснение настоящего изобретения предлагается ниже.
Ген агглютинации.
В соответствии с настоящим изобретением, гены, придающие дрожжам Sacchoromyces cerevisiae агглютинирующие свойства, включают ген дрожжей размером 4,7±0,2 кb, который кодирует полипептид, обладающий агглютинирующей активностью, а также ген агглютинации размером 2,6 ± 0,2 кb, полученный из вышеупомянутого гена агглютинации. При этом данные гены соответствуют гену FL01L (также обозначенному как FL01L) и гену FL01S (также обозначаемому как FL01S), полученным из гена агглютинации FL01 из дрожжей Saccharomyces cerevisiae, описанных выше. FL01S представляет собой FL01L ген с частью делетированной нуклеотидной последовательности. К тому же, как будет представлено позже, ген FL01 также заключает гены, которые являются искусственными или естественными производными гена FL01L и обладают агглютинирующими свойствами, хотя длина их открытой рамки для считывания может различаться. Отсюда, ген FL01L представляет собой интактный ген FL01 на хромосоме I дрожжей Saccharomyces cerevisiae, а FL01S представляет собой ген FL01L с частью делетированной открытой рамки считывания, делеция которой осуществлена без сдвига рамки связи с этим, FL01L придает относительно сильные агглютинирующие свойства хозяйской клетке дрожжей, в которую он был включен, тогда как FL01S, в сравнении с FL01L, придает более слабые агглютинирующие свойства клетке дрожжей, в которую он включается.
В соответствии с настоящим изобретением, агглютинирующие гены присутствуют в дрожжах Saccharomyces cerevisiae в форме плазмид, которые содержат гены как составляющие их части, а также в форме инсерций в геном хозяина. Кроме того, в соответствии с настоящим изобретением гены агглютинации с целью стабильной экспрессии в дрожжах, могут быть помещены под контроль соответствующего промотора и терминатора и присутствовать в такой форме в виде плазмид или инсерций внутри генома. Используемые для таких целей промотор и терминатор могут представлять собой подходящие комбинации хорошо известных промоторов и терминаторов, таких как гена алкогольдегидрогеназы (ADHI), гена фосфоглицераткиназы (PGK) и других.
Полипептиды, кодируемые генами.
В соответствии с настоящим изобретением, FL01L ген определяется по аминокислотной последовательности полипептида, который он кодирует. Этот полипептид имеет агглютинирующую активность и представляет собой полипептид, чья аминокислотная последовательность в целом отражается последовательностью N 1. Отсюда, выражение "тот объект, чья аминокислотная последовательность в основном отражается Последовательностью N 1", означает, что некоторые аминокислоты могут быть делетированы или замещены, а также, что некоторые аминокислоты могут быть добавлены, и при этом полипептид сохраняет агглютинирующую активность.
В соответствии с настоящим изобретением, типичный полипептид, обладающий агглютинирующей активностью, имеет аминокислотную последовательность, приведенную в Последовательности N 1, и состоит из 1637 аминокислот. При этом ранее его аминокислотный состав не был известен.
Выше отмечено, что в соответствии с настоящим изобретением выражение "тот объект, чья аминокислотная последовательность в основном отражается Последовательностью N 1", означает, что некоторые аминокислоты могут быть делетированы или замещены, а также, что некоторые аминокислоты могут быть добавлены, и при этом сохраняется агглютинирующая активность полипептида; примером пептида, который имеет изменения аминокислотного состава, является такой полипептид, в котором аминокислотная последовательность с 329 аминокислоты по 1003 аминокислоту (FL01L последовательность) делетирована, при этом получается последовательность FL01S (см. Последовательность N 2) и при этом данный пептид обладает агглютинирующей активностью, хотя и несколько более слабой.
Если агглютинирующие свойства дрожжей во время ферментации достаточно сильны, то число суспендируемых клеток дрожжей будет снижено, и это приведет к снижению скорости ферментации. Поэтому желательно иметь возможность выращивать дрожжи таким способом, чтобы агглютинирующие свойства соответствующей силы были присущи каждой ферментационной системе. Агглютинирующие свойства могут стать очень сильными при введении гена FL01L, и в этой связи введение гена FL01S несколько более предпочтительно. В данном контексте, несмотря на то, что в соответствии с данным изобретением, длины полипептидов в основном совпадают с последовательностью, перечисленной в Последовательности N 1, делеции, замещения, присоединения и так далее нескольких аминокислот весьма существенны для установления агглютинирующей активности желательной силы в различных дрожжах. Таким образом, подобного рода измененные полипептиды также имеют отношение к настоящему изобретению, как полипептиды, обладающие агглютинирующей активностью.
Нуклеотидная последовательность гена агглютинации.
Ген FL01L имеет нуклеотидную последовательность, представленную в Последовательности N 1 или изомера с вырожденным кодом и имеет последовательность оснований, которая соответствует аминокислотной последовательности, представленной в Последовательности N 1 или ее изомера с вырожденным кодом. Отсюда, термин "изомер с вырожденным кодом" означает цепь ДНК, которая отличается только в вырожденном кодоне, но которая сохраняет способность кодировать тот же самый полипептид.
Последовательность оснований цепи ДНК, перечисленная в Последовательности N 1, была определена для гена FL01, полученного из Saccharomyces cerevisiae штамма ABXL-ID (Генетический Центр по хранению Дрожжей, Университет Калифорнии, США) с использованием дидезокси метода.
Коллекция цепей ДНК гена агглютинации.
В настоящее время отсутствует какая-либо информация относительно продукта FL01 гена, который имел бы агглютинирующую активность (по аминокислотной последовательности полипептида, кодируемого FL01 геном) и поэтому невозможно клонировать FL01 ген с использованием обычно применяемой процедуры гибридизации, в которой применяется соответствующий зонд ДНК, синтезированный на основе известной аминокислотной последовательности. В результате этого, авторы настоящего изобретения вынуждены были создавать генную библиотеку полной ДНК Saccharomyces cerevisiae штамма ABXL-ID с использованием "челночной" векторной плазмиды дрожжей /E. coli, при этом неагглютинирующие дрожжи трансформировались для получения агглютинирующего клона, и плазмиды выделены из трансформированного штамма (см. далее примеры с описанием деталей процедуры).
Введение гена агглютинации в дрожжи.
В соответствии с настоящим изобретением, посредством введения гена агглютинации, полученного описанным выше способом, в дрожжи, которые используются в ферментационной промышленности согласно методам биоинженерии, например пивные дрожжи, винные дрожжи, дрожжи виски, дрожжи японского саке, шоку (Shochu) дрожжи, спиртовые дрожжи и т.д. (все - представители Saccharomyces cerevisiae), возможно превращать в агглютинирующие штаммы, если они ранее не обладали способностью к агглютинации, или усиливать их агглютинирующие свойства, если они были представителями штаммов, обладающих агглютинирующими свойствами.
Дрожжи.
В соответствии с настоящим изобретением, трансформируемые дрожжи представляют собой микроорганизмы, относящиеся к роду Saccharomyces cerevisiae, описанному в The Yeasts: A Taxonomic Study, 3rd Ed. (Yarrow D., ed by N.J.W. Kreger-Van Rij, Elsevier Science Publishers B.V., Amsterdam, 1984, p. 379), или их синонимы или мутанты; однако, в соответствии с целью настоящего изобретения, предпочтительны различные промышленные дрожжи, принадлежащие к роду Saccharomyces cerevisiae, например пивные дрожжи, винные дрожжи, дрожжи виски, дрожжи японского саке, шоку (Shochu) дрожжи, спиртовые дрожжи и т.д.
Конкретные примеры их включают пивные дрожжи низового брожения W164 (Мюнхенский Институт Технологии, Германия), W204 (Мюнхенский Институт Технологии, Германия), SMA-S (Берлинский Институт Технологии, Германия), Н.Н. (Берлинский Институт Технологии, Германия), а также пивные дрожжи верхового брожения Obg.160 (Берлинский Институт Технологии, Германия), винные дрожжи: IAM 4175 (Токийский Университет), дрожжи виски: AHU 3200 (Университет Хоккайдо), дрожжи японского саке: Ассоциация N 6 (Японская Ассоциация Пива), шоку (Shochu) дрожжи: IF0 0282 (Фонд Исследовательского Института по ферментации), спиртовые дрожжи: IF0 0216 (собственность Института Исследования Ферментации) и т.д. Эти промышленные дрожжи были отобраны и культивировались в виде чистых культур в течение многих лет с получением форм, подходящих для ферментационной промышленности, т.е. форм, способных к эффективной ферментации и продукции спирта с хорошим вкусом, генетические свойства которых являются стабильными и так далее.
Трансформация.
Используемые процедуры и методы получения трансформированных форм практически не отличаются от общеприменяемых в молекулярной биологии и генной инженерии и могут включать иные методы, кроме тех, что указаны ниже, в связи с их способностью увеличивать эффективность широко используемых технологий. В соответствии с настоящим изобретением, для того, чтобы ген агглютинации подвергался экспрессии в дрожжах, необходимо, во-первых, вставить ген в плазмидной вектор, который способен к стабильному существованию в дрожжах. При этом может использоваться любой из известных в настоящее время векторов, таких как YRp, YEp, YCp, YIp и другие. Эти плазмидные векторы не только хорошо известны по их описаниям в литературе, но также достаточно легки в изготовлении.
В соответствии с настоящим изобретением, в качестве маркера для селекции нужных трансформантов можно использовать любой ген устойчивости против лекарств, такой как G418 и т.д., поскольку в случае промышленных дрожжей не существует внутренних генетических маркеров, таких как потребность в аминокислотах или нуклеиновых кислотах и т. д. Однако, возможно получить трансформант, маркированный собственно агглютинацией, используя тот факт, что рассматриваемый ген агглютинации экспрессируется в виде доминантного гена.
В соответствии с настоящим изобретением, инсерция гена агглютинации в плазмиду и введение ее далее в дрожжи достаточно легко осуществляется, но с другой стороны, данный тип плазмид обычно трудно стабильно поддерживать в клетках, и они часто теряются из трансформированных клеток. В соответствии с настоящим изобретением, для того, чтобы поддерживать цепь ДНК гена агглютинации в дрожжах в более стабильном состоянии, ее следует вставить в геном дрожжей. Более предпочтительно улучшать дрожжи, используя только гены дрожжей, особенно в случае дрожжей, используемых в пищевой промышленности, таким образом, чтобы в конечном рекомбинанте не присутствовал фрагмент недрожжевой ДНК из E. coli (содержащийся в плазмидном векторе, если плазмида выращивалась в E. coli). Мы, авторы настоящего изобретения, сделали выбор в пользу введения только гена дрожжей, используя метод ко-трансформации Пентилла с соавторами и метод замещения гена (Current Genetics, Vol. 12, p. 413-420, 1987), в соответствии с которыми только дрожжевой ген включается в геномную ДНК. Кроме того, трансформация может быть осуществлена с использованием любых подходящих методов, используемых в области молекулярной биологии и генной инженерии, таких как, например, метод протопластов Хиннена (Proceedings of National Academy of Sciences of United States of America, Vol. 75, p. 1929-1933, 1978), литий-ацетатный метод Ито с соавторами (Journal of Bacteriology, Vol. 153, p. 163-168, 1983) и другие. Получаемые с помощью таких методов дрожжи имеют, кроме введенной экзогенной ДНК, точно те же самые генетические свойства, как и у исходного штамма перед интродукцией, а с использованием, кроме того, метода хромосомной интродукции, при котором вводится только цепь ДНК гена агглютинации с помощью техники ко-трансформации и генного замещения, получаются рекомбинантные дрожжи, которые не содержат необязательных последовательностей вектора, т.е. они не обладают свойствами используемого вектора. В результате положительные качества исходного штамма никоим образом не нарушаются. При этом представляется возможным выращивать промышленные дрожжи, способность которых к агглютинации определенным образом улучшена.
Производство спиртовых жидкостей.
В соответствии с настоящим изобретением для достижения описанного выше эффекта проводится ферментация ферментируемого источника с использованием трансформированных дрожжей, содержащих ген агглютинации. Само собой разумеется, что ферментируемый источник выбирается с учетом объекта ферментации, например, при производстве пива или виски используется сусло, при производстве вина - фруктовый сок, в производстве японского саке используется койи (koji), в производстве шоку - крахмал или другие углеводные источники, а в производстве спирта - меласса, крахмал или другие углеводные источники. Кроме того, условия ферментации могут соответствовать традиционно применяемым, при этом отсутствует необходимость модифицировать существующие процедуры ферментации или использовать другое оборудование при внедрении настоящего изобретения
Поскольку используемые дрожжи проявляют тенденцию к агглютинации в получаемой спиртовой жидкости, они быстро агглютинируют и оседают на дно ферментационного куба после завершения ферментации. Таким образом, клетки дрожжей легко отделяются от ферментационной среды.
Примеры
Более детальное описание настоящего изобретения предлагается ниже со ссылками на примеры.
Пример 1
(Коллекция генов, контролирующих агглютинацию дрожжей)
Для получения FL01S нега как одного из генов агглютинации, в соответствии с настоящим изобретением, проводится следующий эксперимент (Watari et al. , Agricultural and Biological Chemistry, Vol. 53, N 3, p. 901 - 903, 1989). Используется хромосомная ДНК Saccharomyccs cerevisiae штамм ABXL-ID (генный тип: MATa FL01, Центр по хранению Генетической информации Дрожжей, Университет Калифорнии, США), которая была получена по методу Крайера с соавторами (Methods of Cell Biology, Vol. 12, p. 39 - 44, 1975). Полученная хромосомная ДНК была частично расщеплена с помощью рестрикционного фермента Sau 3AI, фрагменты ДНК размером около 5 кb были выделены с помощью центрифугирования в градиенте плотности сахарозы и встроены in vitro с помощью легирования (Watari, et al., Agricultural and Biological Chemistry, Vol. 53, N 3, p. 901 - 903, 1989), в BamHI-сайт клонирующего вектора YCpH4, который содержал ген HIS4 для синтеза гистидина в качестве селективного маркера. Esherichia coli (E. coli) штамм MC1061 (генный тип: hsdR mcrB arad139 (araABC-leu) 7679^lacX74 galU glaК rspL thi) была трансформирована с помощью легирующей смеси, а плазмиды затем были экстрагированы из трансформанта для создания генной библиотеки штамма ABXL-ID. Штамм E.coli MC1061 представляет собой штамм, широко распространенный для исследования в области технологии рекомбинантных ДНК. С использованием генной библиотеки была проведена трансформация пекарских дрожжей Saccharomyces cerevisiae штамм YJW6, которые зависят от гистидина и не обладают агглютинирующей способностью (генный тип: MAT-adeI uraI his4 canI karI) (Watari et al., Agricultural and Biological Chem. , vol. 53, N 3, p. 901 - 903, 1989). Трансформация Saccharomyces cerevisiae штамм YJW6 проводилась, в основном, по литий-ацетатному методу Ито с соавторами (Journal of Bacteriology, vol. 153, p. 163 - 168, 1983). В соответствии с этим методом, 100 мл жидкой культуральной среды в YPD (1% дрожжевого экстракта, 2% бактопептона, 2% глюкозы) инокулируют одной петлей штамма YJW6, после чего клетки инкубируют в течение ночи при 30oC, отделяют на следующее утро с помощью центрифугирования, инокулируют в новую среду того же состава и далее культивируют в течение 2 часов при 30oC. Собранные клетки промывают 40 мл стерильной воды и суспендируют в 20 мл раствора TE (10 мМ Трис-HCl буферного раствора, содержащего 1 мМ ЭДТА, pH 7,5). 5 мл полученного раствора переносят в L-образную опытную пробирку (пробирка Моно), добавляют 5 мл 0,2 М раствора ацетата лития и полученную смесь перемешивают при комнатной температуре в течение одного часа со скоростью 100 об/мин. Из раствора отбирают 0,1 мл и переносят в 1,5 мл пробирку Эппендорфа, которая уже содержит 50 мкг рекомбинантной плазмиды (осажденной этанолом и затем высушенной на воздухе). Смесь хорошо перемешивают и оставляют в течение 30 мин при 30oC. Далее, продолжая хорошо перемешивать пробирку Эппендорфа, добавляют в нее 0,1 мл 70%-ного полиэтиленгликоля # 4000, смесь хорошо перемешивают и оставляют стоять в течение одного часа при 30oC. После этого смесь нагревают до 42oC в течение 5 минут (обработка тепловым шоком), охлаждают до комнатной температуры и промывают затем клетки с помощью стерильной воды. Далее клетки суспендируют в 0,5 мл стерильной воды и 0,1 мл суспензии вносят в минимальную культуральную среду, которая не содержит гистидина (0,67% Difco, содержащий азотистые основания из дрожжей без аминокислот, 2% глюкозы, 40 мкг/мл сульфата аденина, 40 мкг/мл урацила, 2% бактоагара Difco) для получения трансформанта, независимого от гистидина. Указанный эксперимент трансформации повторяли 10 раз для получения примерно 10000 клонов трансформантов, независимых от гистидина.
Далее, среди полученных трансформантов проводили скриннинг агглютинирующих клонов. Трансформанты отбирали с планшета с помощью зубочистки, инокулировали в 96-луночный микротитровальный планшет [каждая лунка которого содержала 200 мкл минимальной жидкой культуральной среды (указанная выше минимальная среда без агара)] и культивировали при 25oC в течение трех дней. Агглютинацию наблюдали при энергичном перемешивании микроплат после культивирования с использованием специального встряхивателя для микроплат (микромиксер Titech) в течение 60 секунд. При этом агглютинирующие клоны отмечаются визуально. Один клон с относительно сильными агглютинирующими свойствами был получен из примерно 6000 трансформантов, независимых от гистидина. Этот штамм культивировали в неселективной культуральной среде YPD, на которой был получен гистидин-зависимый в связи с потерей плазмиды клон. Этот клон, будучи гистидин-зависимым, теряет также свои агглютинирующие свойства. К тому же, при выделении ДНК из первоначально полученных агглютинирующих трансформантов была также выделена плазмида из E.coli штамм MC1061, и, с помощью ретрансформации штаммом YJW6, получили трансформанты, независимые от гистидина, все обладающие агглютинирующими свойствами. Эти результаты приводят к выводу о том, что агглютинирующие свойства, наблюдаемые у трансформированного штамма, связаны не с генетической мутацией клетки-хозяина, а вызваны плазмидой в трансформированном штамме. Исходя из этого, мы, авторы настоящего изобретения, назвали плазмиду, которая содержит генетическую последовательность, контролирующую агглютинацию, как YCpHF19S. Карта рестрикции данной плазмиды представлена на фиг. 4.
Естественно предположить, что подобная плазмида, содержащая ген агглютинации, может быть использована в качестве селективного маркера для селекции агглютинирующей способности дрожжей, не содержащих маркер, в скрининговом тесте с использованием микротитровального планшета для получения нужных трансформантов. В этом эксперименте трансформанты, в которые настоящая плазмида была введена, были получены из неагглютинирующих дрожжей. Иными словами, данный тип гена аггютинации может быть использован для получения трансформантов дрожжей, принадлежащих к Saccharomyces cerevisiae без какого-либо генетического маркера. Кроме того, важнейшим достоинством такой процедуры скрининга является отсутствие необходимости готовить специальную культуральную среду (минимальную среду или среду, содержащую антибиотики) для скрининга трансформантов, и возможность культивирования в нормальной культуральной среде. К настоящему времени имеется несколько генетических маркеров, полученных из дрожжей, для приготовления трансформантов дрожжей, которые оказались очень полезными в экспериментах по самоклонированию дрожжей.
Пример 2.
(Картирование и идентификация клонирования гена агглютинации)
Для того чтобы определить, является ли ген агглютинации, клонированный в примере 1, геном FL01 на хромосоме 1 дрожжей, был выполнен эксперимент физического картирования данного гена агглютинации (Watari et al., Agricultural and Biological Chemystry, vol. 53, N 3, p. 901 - 903, 1989).
В качестве зонда используют фрагмент EcoRV размером 2,6 кb, взятый из ДНК плазмиды YCpHF19S, содержащий ген, контролирующий агглютинацию, и провели физическое картирование данного генного фрагмента с помощью электрофореза хромосомной ДНК (электрофорез в пульсирующем градиенте напряжения). Электрофорез хромосомы Saccharomyces cerevisiae штамм ABXL-ID проводили по методу Карле с соавторами (Carle et al., Proceeding of the National Academy of Science of United States of America, vol. 82, p. 3756 - 3760, 1985). Для приготовления образца при этом использовали аппарат для электрофореза Biorad CHEF. По окончании электрофореза, полоса ДНК в электрофорезном геле была подвергнута саузерн-блоттингу и гибридизации по методу Маниатиса с соавторами (Maniatis et al., Mollecular Cloning, p. 382 - 389, Cold Spring Harbor Laboratory, 1982). В результате была получена гибридная молекула, содержащая вышеупомянутый EcoRV фрагмент 2,6 кb и хромосому 1 штамма ABXL-ID, указывая на то, что ген агглютинации, клонированный в настоящем эксперименте, представляет собой ген на хромосоме 1.
Далее провели генеалогическое картирование клонированного гена агглютинации (Watari et al., Agricultural and Biological Chemystry, v. 55, N 6, p. 1547 - 1552, 1991). После частичного расщепления YCpHF19S рестриктазой XbaI, были выделены центрамерный ген (GEN4) из дрожжей и дрожжевого ориджин-репликации ARSI для получения YIp дрожжевой плазмиды YIpHF19S (см. фиг. 5), подлежащей включению. После расщепления плазмиды рестриктазой BamHI с целью повышения эффективности включения клонированного гена в дрожжи Saccharomyces cerevisiae штамм YJW2A (генный тип: MATA FL01 his 4) был трансформирован описанным выше способом для получения трансформантов, независимых от гистидина. Полученный штамм был гибридизован с Saccharomyces cerevisiae штамм YJW6 (генный тип: MAT-adeI uraI his4 canI karI) с получением способного к спорообразованию диплоида, которого далее подвергали генетическому анализу (тетрадный анализ). В результате было продемонстрировано наличие генеалогического сцепления (родительский дитип: неродительский дитип: тетратип = 22: 0 : 7) между His + свойством (отсутствие потребности в гистидине) и ADEI на хромосоме 1, что четко показывает, что порция клонированного гена агглютинации плазмиды YIpHF19S была включена в хромосому 1 штамма YJW2A.
Из результатов описанных выше экспериментов по физическому и генеалогическому картированию мы, авторы настоящего изобретения, сделали вывод о том, что клонированный ген агглютинации представляет собой FL01 ген на дрожжевой хромосоме 1. Однако, исходя из этих результатов, не было возможности узнать, представляет ли FL01 ген интактный FL01 ген, присутствующий на дрожжевой хромосоме (или FL01L ген), или он является FL01S геном, лишившимся части последовательности ДНК FL01L, как описано ниже.
Пример 3
(Определение последовательности оснований FL01S)
Мы, авторы настоящего изобретения, провели эксперимент с целью определения последовательности оснований FL01 гена (фактически FL01S гена), полученного выше.
В результате субклокирования было показано, что регион гена FL01S, необходимый для экспрессии агглютинации, состоит из фрагмента ДНК размером 4,1 кb, находящегося между сайтами Bam HI-(BamHI/sau 3AI) на плазмиде YCpHF19S. В этой связи, регион, содержащий данный фрагмент ДНК, был субклонирован на векторах pUC118 и pUC119 с мультилинкерными сайтами (оба - продукты Takara Brewing Co). Далее, каждый из субклонов анализировали по методу (Henikoff et al. , Gene, vol. 28, p. 351 - 359, 1984) и по метолу (Yanisch-Porron et al., Gene, vol. 33, p. 103, 119, 1985) с обработкой включенных участков плазмиды экзонуклеазой III и нуклеазой из растений маша, что привело к получению различных клонов небольшой длины со вставленными фрагментами, часть из которых с различными пропусками, что отражается в различной длине цепи. В результате этого процесса был получен набор делеций (продукт Takara Brewing Co. ). Для анализа вставленных фрагментов у полученных клонов был применен ди-дезокси-метод Сангера с соавторами (Sanger et al., Science, vol. 214, p. 1205 - 1210, 1981), а для определения нуклеотидной последовательности вышеупомянутого фрагмента ДНК размером 4,1 кb был использован автоматизированный секвенатор ДНК фирмы Эпплайд Байосистемс, Япония (Applied Biosystems Japan, Inc. ). В результате проведенного анализа было показано наличие открытой рамки считывания размером 2586 н.п. (Последовательность N 2), способной кодировать полипептид, состоящий из 862 аминокислот, молекулярный вес которого оценивается в 89368.
Пример 4
(Эксперимент по гибридизации по методу Саузерна)
Как было описано выше, ген агглютинации, полученный в примере 1, находится точно в FL01 локусе дрожжевой хромосомы 1. Однако, для того чтобы определить, является ли он интактным FL01 геном, была проведена гибридизация по Саузерну, описанная ниже. Из дрожжей Saccharomyces cerevisiae штамм ABXL-ID, использовавшихся для клонирования гена агглютинации, была экстрагирована ДНК, которую затем полностью расщепили с помощью рестриктазы EcoRV, подвергали электрофорезу и затем геномному анализу по Саузерну с использованием в качестве пробы EcoRV фрагмента ДНК размером 2,6 кb, содержащего открытую рамку для считывания, упомянутую выше в примере 2. Саузерн-блоттинг и гибридизацию проводили по методу Маниатиса с соавторами (Maniatis et al., Molecular Cloning p.382-389, Cold Spring Harbor Laboratory, 1982).
Были получены неожиданные результаты, заключающиеся в том, что не было обнаружено гибридизационного сигнала на участке, соответствующем примерно 2,6 кb, а на участке, соответствующем примерно 4,7 кb, этот сигнал был получен. Это заставило авторов предположить, что клонированный ген агглютинации скорее всего не идентичен FL01 гену штамма ABXL-ID, но, скорее всего, это - интактный FL01 ген с частью последовательности ДНК, потерянной по различным причинам во время процесса клонирования.
Пример 5.
(PCR (полимерная цепная реакция) эксперимент)
В данном примере авторы настоящего изобретения выполнили представленный ниже эксперимент для подтверждения структуры FL01 гена ABXL-ID с помощью PCR метода (полимеразная цепная реакция). Вначале химическим путем синтезировали цепь ДНК с использованием приведенной в примере 3 последовательности нуклеотидных оснований. То есть химически с помощью ДНК-синтезатора (продукт ABI Co. ) была синтезирована последовательность ДНК, состоящая из 33 оснований, включая регион с инициирующим кодоном открытой рамки для считывания данного гена, которая использовалась в качестве PCR 5'-праймера.
+1
5'-CCCAAGCTTAAAAATGACAATGCCTCATCGCТA-3' (Sequence N.3)
HindIII
Linker site
(ATF-старт с 14 основания 5'-конца приведенной выше последовательности представляет собой 5'- конец Последовательности FL01S).
Кроме того, химически, тем же самым способом, была синтезирована последовательность ДНК из 33 оснований, включающая комплементарную нить (обратную нить) участка, содержащего терминирующий кодон открытой рамки для считывания данного гена агглютинации, которая использовалась как PCR 3'-праймер (Последовательность N 4).
(STOP)
5'-CCCAAGCTTTTAAATAATTGCCAGCAATAAGGA-3' (Sequence N 4)
HindIII
Linker site
(TTA-старт с 10 основания 5'- конца приведенной выше последовательности представляет собой 3'-конец Последовательности FL01S (обратная нить)).
Далее, с использованием указанных 5'- и 3'-праймеров был поставлен PCR эксперимент с целой ДНК из Saccharomyces cerevisiae штамм ABXL-ID в качестве матрицы.
Для проведения PCR эксперимента использовались зимореактор, модель АВ-1800 (продукт Ato Co. ) и ДНК-полимераза Pfu (Stratagene Co.) в качестве ДНК-полимеразы. Условия проведения PCR эксперимента поддерживались идентичными таковым, описанным в методе Иниса с соавторами (Inis et al., PCR Technology p.3-12, Stockton Press, ed.Henry A.Erlich, 1989). Для подтверждения амплификации ДНК в результате PCR эксперимента исследовали полосы ДНК в агарозном геле после гель-электрофореза. При этом была получена единственная полоса в области примерно 4,7 кb, и это дало основание полагать, что открытая рамка для считывания FL01 штамма ABXL-ID составляет примерно 4,7 кb. Кроме того, в контрольном эксперименте, в котором авторы изобретения использовали плазмиду YCpHF19, содержащую клонированный ген агглютинации в качестве матрицы, была показана полоса в области примерно 2,6 кb. Исходя из полученных результатов, авторы настоящего изобретения сделали вывод о том, что интактная открытая рамка для считывания FL01 гена, присутствующая в дрожжах Saccharomyces cerеvisiae штамм ABXL-ID, составляет примерно 4,7 кb, а не 2,6 кb.
Исходя из этого, мы, авторы настоящего изобретения, сделали вывод о том, что ген агглютинации, полученный нами, представляет собой FL01 ген, часть которого по каким-то причинам утеряна, наиболее вероятно в результате внутримолекулярной рекомбинации во время поддержания YCpHF19 в E.coli штамм MC1061.
Пример 6
(Коллекция FL01 генов)
В настоящем разделе авторы провели повторные исследования на основе наших предложений о том, что плазмида, содержащая интактный FL01 ген, могла быть подвергнута контаминации в растворе YCpHF19S плазмиды, полученной из E. coli в ходе клонирования FL01. При этом в начале эксперимента была взята часть раствора плазмиды, расщеплена с помощью рестриктазы EcoRV и подвергнута электрофорезу в агарозном геле, в результате которого была обнаружена чрезвычайно слабая, но четко заметная полоса в области 4,7 кb в дополнение к полосе 2,6 кb, полученной для YCpHF19S. Эти данные позволяют предположить, что плазмидный раствор представляет собой смесь двух типов плазмид. Исходя из этого, авторы настоящего изобретения использовали данный плазмидный раствор для трансформации E.coli штамм JA221 (генный тип: reAI, lacY leuB trp^ E5 thr thi hsdR hsdM), при этом в результате экстракции плазмид из полученных трансформантов и их исследования был выделен другой тип плазмиды в дополнение к YCpHF19S, который был примерно на 2,1 кb больше, чем YCpHF19S. В этой связи, первоначально клонированная плазмида была названа YCpHF19S, а плазмида, выделенная из плазмидного раствора YCpHF19S, которая была на 2,1 кb длиннее ее, была названа YCpHF19L. Далее, в результате анализа образцов после расщепления соответствующими рестрикционными ферментами YCpHI9S и YCpHF19L, было показано, что плазмиды не имеют никаких различий в других регионах ДНК, кроме региона ДНК, содержащего открытую рамку для считывания для гена агглютинации (см. фиг. 4 и фиг.7). Таким образом, открытая рамка считывания для гена агглютинации YCpHF19L на 2,1 кb длиннее, чем соответствующая рамка для YCpHF19S. Это наблюдение привело к выводу о том, что первоначальное клонирование интактного FL01 гена (т.е. FL01L) было успешным, однако, во время поддержания YCpHF10L плазмиды в E.coli штамм MC1061, часть открытой рамки для считывания FL01L гена была делетирована, что выразилось в превращении FL01L в FL01S или YCpHF19L в YCpHF19S в связи с внутримолекулярной рекомбинацией in vivo. Исходя из этого, поскольку делеция произошла внутрирамочно, следует полагать, что FL01S сохранил способность кодировать полипептид, проявляющий агглютинирующие свойства.
Следует провести различие между FL01S как геном агглютинации на YCpHF19S и FL01L как геном агглютинации на YCpHF19L.
Кроме того, частота встречаемости делеций в значительной степени определяется типом E. coli, на котором поддерживается YCpHF19L плазмида. В этой связи, авторы настоящего изобретения обнаружили, что, например, высокая скорость конверсии встречается у штамма MC1061 (генный тип: hsdR mcrB araD 1339^ (araABC-leu) 7679^ lacX74 galU galK rpsL thi) и штамма DH5- (генный тип: sup E44^lacU169(-80lacZ^M15) hsdR17-recAI end AI gyr A96 thi-I relAI), тогда как невысокая частота конверсий свойственна штамму JA221 (генный тип: recAI, lacY leuB trp^E5 thr thi hsdR hsdM). В связи с этим, в случае поддерживания плазмиды на E.coli, авторы настоящего изобретения используют преимущественно штамм JA221. Однако, до настоящего времени причина, объясняющая различия в частоте конверсии, не ясна.
Пример 7.
(Анализ последовательности оснований FL01L)
Фрагмент ДНК, содержащий FL01L, был вырезан из YCpHF19L плазмиды, полученной ранее, и с применением метода, использованного в примере 3, была определена полная последовательность оснований. В результате было подтверждено, что открытая рамка для считывания FL01L представляет собой последовательность из 4611 пар оснований, которая кодирует полипептид, состоящий из 1537 аминокислот с молекулярным весом 160692 (Последовательность N 1). Было также показано, что FL01S представляет собой FL01L с делецией ДНК-цепи без сдвига рамки, захватывающей участок от 985 до 3009 основания от инициирующего кодона открытой рамки считывания (соответствующий участку от 329 до 1003 аминокислоты аминокислотной последовательности) (см. Последовательности N 1 и N 2). Кроме того, исходя из результатов анализа аминокислотной последовательности FL01L на участке от 278 по 1087 аминокислоту, было показано наличие повторяющейся последовательности (прямой повтор) из 45 аминокислот, обычно отражаемой следующей ниже последовательностью, при этом альтернативные возможности замены аминокислот показаны через "/" в скобках. ТреТреТре(Глу/Глн)ПроТрп(Асн/Тре/Асп)(Гли/Асп/Сер)ТреФалТреСерТреСер (Тре/Ала)Глу(Мет/Лей/Вал)(Тре/Сер)Тре(Вал/Иле)ТреГлиТреАснГли (Лей/Вал/Глн)(Про/Арг)ТреАспГлуТре(Вал/Иле)ИлеВал(Иле/Вал)(Арг/Лиз) ТреПроТре(Тре/Сер)(Ала/Глу)(Тре/Гли/Сер/Иле)(Тре/Лей/Сер)(Алс/Иле/Сер) (Мет/Сер/Иле/Тре), а в FL01L присутствуют 18 копий этой повторяющейся последовательности. Кроме того, в FL01S основная часть региона данной повторяющейся последовательности делетирована (в FL01S делетированы аминокислоты с 329 по 1003 аминокислотной последовательности FL01L) и всего лишь три копии повторяющейся последовательности присутствуют. Авторы данного изобретения считают в настоящее время, что различия в агглютинирующих способностях FL01L и FL01S (первый придает более сильные агглютинирущие свойства клетке-хозяину, чем последний) связаны с числом этих прямых повторов. Мы, авторы настоящего изобретения, полагаем, что в будущем будет возможно получать желаемые агглютинирующие свойства клетки, т.е. возможно будет регулировать агглютинирующие способности по желанию за счет регуляции числа прямых повторов.
Пример 8
[Введение FL01L гена в различные штаммы дрожжей для практического использования (1: Использование плазмидных векторов)]
Полученные выше гены агглютинации FL01S и FL01L были введены в различные промышленные дрожжи (все - неагллютинирующие) для определения: действительно ли они эффективны для выращивания штаммов дрожжей, обладающих агглютинирующими свойствами с целью практического их использования. Вначале были приготовлены плазмиды, содержащие селектируемые прямым способом FL01S или FL01L гены для трансформации промышленных дрожжей (на фиг.3 представлена схема. Номера рядом с каждой плазмидой и открытой рамкой для считывания (ORF) на приведенной схеме соответствуют номерам рядом с плазмидами и открытыми рамками для считывания, показанными детально на фиг. 4-11). BamHI-XhoI фрагмент размером 5,8 кb (фиг. 6), содержащий FL01S ген YCpHF19S был встроен между BamHI-SalI сайтами на плазмиде YRpGL10 с целью использования для прямой селекции (имеет G418-устойчивый Tn 903 ген как маркерный ген для прямой селекции и ARSl-последовательность как ориджин репликции внутри дрожжей. См. фиг. 9) для получения YRpGLF14S плазмиды (фиг.10). Кроме того, BamHI-XhoI фрагмент размером 7,9 кb (фиг.8) из YCpHF19L, был встроен между BamHI-SalI сайтами YRpGL10 с целью получения YRpGLF8L как сходной плазмиды, содержащей FL01L ген (фиг.11).
Дальше будет описан метод, используемый для трансформации промышленных дрожжей с помощью плазмид. В основном, метод трансформации промышленных дрожжей идентичен таковому, применяемому при трансформации экспериментальных дрожжей, описанному в примере 1, однако авторы изобретения внесли некоторые модификации, указанные ниже (Watari, et al., Agricultural and Biological Chemistry, vol. 55, N 6, p. 1547 - 1552, 1991). То есть 100 мл жидкой культуральной среды YPD (1% дрожжевого экстракта, 2% бактопептона, 2% глюкозы) инокулировали одной петлей клеток, которые далее культивировали при 30oC в течение ночи, затем, на следующее утро отделили с помощью центрифугирования, инокулировали в новую среду того же состава и далее культивировали в течение трех часов при 30oC. Собранные клетки промыли 40 мл стерильной воды и суспендировали примерно в 20 мл TE раствора (10 мМ Трис-HCl буферного раствора, содержащего 1 мМ ЭДТА, pH 7,5). (С целью установления концентрации суспензии равной конечной концентрации клеток примерно 2 • 108 кл/мл использовался гемометр). 5 мл полученного раствора перенесли в L-образную опытную пробирку (пробирка Моно), куда добавили 5 мл 0,2 М раствора литий-ацетата, смесь перемешивали при комнатной температуре в течение одного часа со скоростью 100 об/мин. Из смеси взяли 0,1 мл и перенесли в 1,5 мл пробирку Эппендорфа, которая уже содержит 50 мкг рекомбинантной плазмиды (осажденная этанолом и затем высушенная на воздухе), при этом смесь хорошо перемешали и оставляли стоять в течение 30 минут при 30oC. В пробирку Эппендорфа при перемешивании добавили 0,1 мл 70% полиэтиленгликоля 4000, смесь перемешали и оставляли стоять в течение 1 часа при 30oC. Затем смесь нагрели до 42oC в течение 5 минут (обработка тепловым шоком), оставили охлаждаться при комнатной температуре, после чего клетки промыли стерильной водой. В итоге клетки суспендировали в 1,4 мл YPD раствора в пробирке Эппендорфа и культивировали в течение 16 - 20 часов при 30oC. 0,1 мл культурального раствора нанесли на YPD агаровую среду, содержащую 200 мкг/мл G 418, и инкубировали при 30oC в течение 2 - 3 дней для получения трансформантов.
С использованием этого метода был проведен эксперимент по трансформации различных промышленных дрожжей. Результаты представлены в таблице 1. Кроме того, использовался следующий метод оценки агглютинирующих свойств. Каждый из трансформантов инокулировали в L-образную опытную пробирку (пробирку Моно), которая содержала 10 мл YPD жидкой среды (содержащей 100 мкг/мл G418), и культивировали при перемешивании в течение 3 дней при 28oC (100 об/мин). При этом в результате агглютинации оценивалась методом визуального наблюдения. Для оценки уровня агглютинации использовалась оценочная шкала, разработанная по методу Джонсона с соавторами (Yeast Genetics: Fundamental and Applied Aspects, p. 205 - 224, Springer Verlag, ed. by J.F.T. Spencer, D.M. Spencer, A.R.W. Smith, 1983).
Эти результаты показывают, что при введении генов агглютинации FL01S и FL01L возможно конвертировать все из большого множества неагглютинирующих промышленных дрожжей в агглютинирующие дрожжи, хотя степень агглютинации может быть различной у разных штаммов. Не вызывает сомнения тот факт, что при введении векторной плазмиды YRpGL10 хозяйские клетки остаются неагглютинирующими.
Кроме того, очевидно, что введение FL01L гена приводит к появлению более сильных агглютинирующих свойств в хозяйском штамме, чем введение FL01S гена.
Пример 9
(Введение FL01L гена в различные штаммы дрожжей для практического использования (2: Введение в дрожжевые хромосомы)
В целом, при введении экзогенных генов в хозяйские клетки в виде плазмид, плазмиды теряются из клеток в результате культивирования на селективной среде. Так, было показано, что трансформанты, полученные в примере 8, теряли достаточно быстро плазмиды при культивировании без введения селективного давления с помощью G418. В этой связи, с целью стабильного поддержания FL01 звена в дрожжах, авторы настоящего изобретения попытались включить FL01 гены в дрожжевые хромосомы.
(i) Приготовление FL01 кассет экспрессии для включения (схема представлена на фиг. 12. Номера рядом с каждой плазмидой и открытой рамкой для считывания (ORF) на схеме соответствуют номерам рядом с плазмидами и открытыми рамками для считывания, представленными детально на фиг.13 - 27).
Для получения высокой частоты экспрессии FL01 гена в дрожжах промотор был включен в направлении от 5'-конца открытой рамки для считывания FL01 гена вверх, а терминатор был включен от 3'-конца вниз в участок, контролирующий транскрипцию/трансляцию в гене дрожжевой алкогольдегидрогеназы. То есть последовательность открытой рамки для считывания или FL01S или FL01L вставлялась в Hind III сайт плазмиды pBR-dH-ADHl, который содержал промоторные и терминирующие последовательности для гена дрожжевой алкогольдегидрогеназы с получением, в итоге, pBR-ADHl-FL01S (фиг.22) и pBR-ADHl-FL01L (фиг. 27), соответственно. Кассеты для данной экспрессии приготавливались во время приготовления открытой рамки для считывания FL01S с использованием PCR метода (PCR эксперимент соответствовал таковому, описанному в примере 5), при этом мы, авторы изобретения, подтвердили результаты рестрикционного анализа и секвенирования ДНК, заключающиеся в том, что последовательность FL01S гена, приготовленного описанным способом, была в точности идентична нуклеотидной последовательности, представленной на рестрикционной карте на фиг.2, полученной по результатам примера 3 и приведенной как Последовательность N 2.
(ii) Пример включения FL01 кассеты экспрессии в геном пивных дрожжей с помощью метода ко-трансформации.
Для включения FL01 кассеты экспрессии, не содержащей последовательность векторного происхождения (последовательности, происходящие из векторной плазмиды pBR322), в хромосомную ДНК дрожжей (неагглютинирующие пивные дрожжи низового брожения W204), использовали метод ко-трансформации Пентилла с соавторами (Current Genetics, Vol. 12, p. 413-420, 1987). То есть, 50 мкг либо плазмиды pBR-ADHl-FL01S, либо плазмиды pBR-ADHl-FL01L, полученных выше в (i), расщепили рестриктазой Ba H и обработали фенол/хлороформом, после чего к смеси добавили 50 мкг G418-устойчивости плазмиды YRpGL10 и затем осадили этанолом. Образец ДНК высушили на воздухе, а дрожжи трансформировали по методу, описанному выше, в примере 8. С помощью G418-устойчивости в качестве маркера провели селекцию трансформантов, а на полученных трансформантах провели скрининг с помощью микропланшетного метода исследования (см. пример 1) для получения агглютинирующего штамма. Процедура микропланшетного метода исследования представлена ниже. Полученные трансформанты взяли из планшета с помощью зубочистки, инокулировали 96-луночный микропланшет (каждая лунка которого содержит 200 мкл YPD жидкой среды) и культивировали при 25oC в течение 3-х дней. Определение агглютинации проводилось при энергичном перемешивании микропланшетов в течение 60 секунд, после культивирования, с использованием встряхивателя микропланшет (продукт Titech Co.), после чего визуально отмечалось расположение агглютинирующих клонов.
Полученные таким образом агглютинирующие штаммы культивировались в течение 10 - 20 генераций на YPD среде без селективности, после чего клетки соответствующим образом разбавили, нанесли на YPD агаровую среду и культивировали при 30oC в течение 2 - 3 дней. Накопившиеся на планшете колонии перенесли с помощью реплик на YPD агаровую среду, которая содержала 200 мкг/мл G418 и другую YPD агаровую среду, которая не содержала G418, при этом G418-устойчивость колоний оценивалась по сохранению штаммов, которые не имели ранее G418-устойчивости. Эти штаммы потеряли плазмиду YRpGL10 из своих клеток, однако предполагается, что FL01 касается экспрессии (т.е. открытая рамка для считывания FL01S или FL01L генов при контроле экспрессии с помощью ADHl-промотора и ADHl-терминатора) была включена в ADHl-локус хромосомы путем in vivo генного замещения с использованием участка гомологичной последовательности ADHl гена.
Штамм, в который была включена FL01S кассета экспрессии, был назван W204-FL01S, а штамм, в который была включена кассета экспрессии FL01L, обозначили как W204-FL01L. Культивирование таких штаммов показывает, что в течение 50 генераций они сохраняют свои агглютинирующие свойства на том же самом уровне, как и до культивирования. При анализе штаммов W204-FL01S и W204-FL01L по методу Саузерна авторы настоящего изобретения подтвердили, что все кассеты экспрессии FL01 были включены в хромосомную ДНК.
(iii) Ферментативный тест
С использованием полученных (ii) штаммов W204-FL01S и W204-FL01L был проведен небольшой тест по ферментированию пива в объеме 2 литра. Указанный метод представляет собой стандартный метод Европейского института пивоварения (Journal of the Institute of Brewing, EBC Analytica Microbiologica, Method 2.5.4. , Tubes E.B.C., Vol. 83, p. 117-118, 1977). Клетки культивировали в 50 мл сусла при 20oC в течение 3-х дней, затем все это количество добавили в 1 л сусла и культивировали эту смесь при стоянии в течение одной недели при 15oC. Выросшие клетки собрали после центрифугирования (5000 об/мин в течение 10 мин); полученные дрожжевые клетки добавили к суслу (с подведенной заранее концентрацией кислорода в 9 ppm) при 11oP (степени плато) до концентрации 0,5% (объем/объем). Стационарная ферментация проводилась далее при 10oC в течение 10 дней. В точке, когда количества агглютинации и седиминтации оказываются сравнимыми, родительский штамм W204, бывший неагглютинирующим, имел достаточно низкий уровень осажденных дрожжей, а количество восстановленных дрожжей было в грубом приближении тем же самым, как и количество первоначально прибавленных дрожжей (т.е. 100% восстановления), в то время как W204-FL01L штамм, в который была включена FL01L кассета экспрессии, проявлял сильные агглютинирующие свойства, а количество восстановленных дрожжей было вдвое или более выше количества первоначально добавленных дрожжей (т. е. 200% или больше). Тем не менее, W204-FL01S штамм, в который была включена FL01S кассета экспрессии, проявлял очень слабую агглютинирующую активность, а количество восстановленных дрожжей было не большим, чем в случае W204. Эти результаты дают основание полагать, что адекватная агглютинация клеток хозяина не может быть индуцирована в сусле при введении единичной копии FL01S (при введении множественных копий FL01S, полученных в примере 8, W204 проявлял агглютинирующую способность даже в сусле). Тем не менее, W204-FL01S штамма с единичной копией FL01S, введенный в хромосому, проявлял среднюю агглютинирующую активность в YPD культуральной среде. Однако причина, по которой эта способность к агглютинации не проявлялась в сусле, не ясна до настоящего времени.
После завершения ферментации (предварительной ферментации), описанной выше, было проведено созревание (постферментация) данного супернатанта (молодое пиво), то есть, после завершения процесса постферментации в течение 2-х недель при 5oC и в течение 1-й недели при 0oC ферментат был подвергнут фильтрации через мембранный фильтр и карбонированию при 0oC и давлении в 2 атмосферы в течение 2-х дней, после чего его подвергли химическому анализу и испробовали на вкус полученный образец. Результаты показывают, что между W204 и W204-FL01L отсутствуют какие-либо различия. Таким образом, при изготовлении пива с использованием дрожжей по методу настоящего изобретения изменяются в сторону совершенствования только агглютинирующие свойства дрожжей, при этом не отмечается какой-либо модификации качеств дрожжей, имеющих отношение ко вкусу.
Хранение
Трансформированный штамм Escherichia coli FL01L, происходящий в результате интродукции плазмиды pBR-dEPl-FL01L (фиг.25) и содержащий цепь ДНК, в соответствии с настоящим изобретением (открытая рамка для считывания FL01L гена) в E. coli штамм JA221 был депонирован в MITI National Institute of Bioscience and Human Technology с января 13, 1993 года под номером FERM BP-4136.
Перечень последовательностей
Номер последовательности: 1 (см. в конце описания)
Длина последовательности: 4614
Тип последовательности: нуклеиновая кислота
Тип нити: двойная
Топология: линейная
Молекулярный тип: геномная ДНК
Исходный источник: Saccharomyces cerevisiae ABXL-1D
Номер последовательности: 2 (см. в конце описания).
Длина последовательности: 2589
Тип последовательности: нуклеиновая кислота
Тип цепи: двойная
Топология: линейная
Молекулярный тип: геномная ДНК
Исходный источник: Saccharomyces cerevisiae, ABXL-1D
Номер последовательности: 3
Длина последовательности: 33
Тип последовательности: нуклеиновая кислота
Тип цепи: единичная
Топология: линейная
Молекулярный тип: другая нуклеиновая кислота / синтетическая ДНК
Последовательность N 3
CCCAAGCTTA 4ATGACAA TGCCTCATCG CTA
Номер последовательности: 4
Длина последовательности: 33
Тип последовательности: нуклеиновая кислота
Тип цепи: единичная
Топология: линейная
Молекулярный тип: другая нуклеиновая кислота
Последовательность N 4
CCCAAGC3T TЗATAATTG CCAGCAATAA GGAл

















Изобретение относится к генам агглютинации дрожжей, а также к дрожжам, которые их содержат. Получены гены агглютинации дрожжей: FL01L из штамма дрожжей Saccharomyces cerevisiae ABXL-1D, имеющий размер 4,7±0,2 кb, кодирующий аминокислотную последовательность, представленную как SEQ IDN1, и определяющийся картой рестрикционного расщепления, представленной на фиг. 1. Ген агглютинации дрожжей FL01S получен из штамма дрожжей Saccharomyces cerevisiae ABXL-1D, имеющий размер 2,6±0,2 кb, кодирующий аминокислотную последовательность, представленную как SEQ ID N2, и определяющийся картой рестрикционного расщепления, представленной на фиг.2. Получены и штаммы дрожжей W204-FL01L и W204-FL01S, содержащие вышеуказанные гены, обладающие агглютинирующими свойствами. Полученные гены и дрожжи обладают более сильными и стабильными агглютинирующими свойствами. 4 с.п.ф-лы, 27 ил., 1 табл.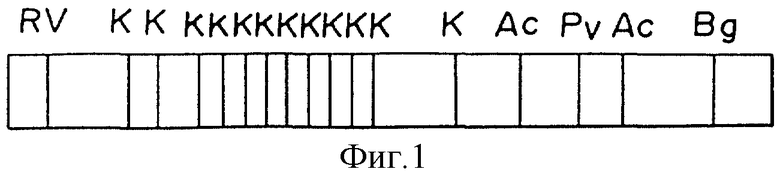
| Agricultural and Biological Chemistry, 1991, v.55, N 6, 1547-1552. |
Авторы
Даты
2000-11-27—Публикация
1994-02-24—Подача