Это изобретение относится к смеси высших первичных алифатических спиртов, содержащей спирты из порядка от 24 до 34 атомов углерода, и более конкретно, спирты с прямой цепью из 24, 26, 27, 28, 29, 30, 32 и 34 атомов углерода.
В Европейской патентной заявке 0488928 описывается смесь высших первичных алифатических спиртов из от 24 до 34 атомов углерода, которая может использоваться в качестве активной составной части фармацевтических препаратов, используемых для лечения гиперхолестеринемии, гиперлипопротеинемии типа II и стимуляции сексуального поведения у животных и людей.
В соответствии с настоящим изобретением смесь высших первичных алифатических спиртов из от 24 до 34 углеродных атомов (с этого момента называемая М. Н.Р.А.А.) в относительно узком количественном соотношении проявляет новые свойства, такие как противотромбоцитные, антитромботические и/или антиишемические, а также противодействия образованию индуцируемых лекарствами язв, и поэтому эта конкретная смесь может использоваться в качестве активного ингредиента фармацевтических препаратов, изготавливаемых для этих целей.
Задача изобретения состояла в создании М.Н.Р.А.А. из от 24 до 34 атомов углерода для фармацевтических препаратов, а также в выделении и очистке этой смеси из воска сахарного тростника, как необработанного, так и из очищенного.
Действие по снижению уровня липидов воска сахарного тростника было продемонстрировано на крысах (Fukuda, Effects of suger cane wax on serum Liver Lipids on rats; Chemical Abstracts, 106, 17, 137413 p) and mice (Sho H. et al. (1984) Effects of Okinawan sugar cane wax and fatty alcohols on serum and Liver Lipids in the rats; J. Nutri Vitaminol 30(6) 553-559).
В первую очередь были изучены эффекты воска сахарного тростника на липиды сыворотки и в печени у самцов крыс Wistar, которых кормили пищей с высоким содержанием растительных и животных жиров. Авторы обнаружили, что добавление 0,5% воска сахарного тростника в жиры рациона снижает значительно уровень сывороточных триглицеридов у крыс, которых кормят растительными или животными жирами, но только у последних значительно снижались уровни холестерина при отсутствии влияния на содержание липидов в печени. Отсюда авторы заключают, что воск сахарного тростника проявляет гиполипидемическое действие.
С другой стороны, Sho Н. et. al. (1984) изучил воздействия воска окинавского сахарного тростника на содержание липидов в сыворотке и печени крыс, которые получали диету с содержанием 0,5% этого воска, и они обнаружили значительное снижение содержания холестерина как в сыворотке, так и печени. Однако не было обнаружено значительных изменений уровня холестерина при использовании жирных спиртов из того же самого воска в диете животных. Таким образом, они отвергли то, что свойства снижения уровней липидов этим воском принадлежат этим спиртам.
Однако несколько лет спустя, Shimura S., Hagesawa T., Takano S. and Susuki T. (1987: Studies on the effect of octaconasol on the motor endurance in mice; Nutrition Reports Int. 36, 1029-1038) изучили воздействия октакозанола на мышах, понуждаемых к высокой физической активности, которые получали диету, обогащенную октакозанолом. Они обнаружили, что октакозанол, выделенный из воска сахарного тростника, значительно снижал содержание как триглицеридов, так и холестерина в печени, в то время как в сыворотке в значительной степени снижались только уровни триглицеридов. Они заключили, что октакозанол, выделенный из воска сахарного тростника, показал свойства снижения уровней липидов, что находится в противоречии с предшествующими результатами Sho Н. et al. (1984), упомянутыми выше.
Аналогично, антилипемические эффекты были далее отнесены за счет гексакозанола, другого высшего первичного алифатического спирта, хотя, как сообщалось, были необходимы очень высокие дозы для получения таких результатов (10-30 мг/кг/ в день) (Hagiwara J. 1987: Antilipaemic agents containing hexacosanol used to treat hypertension, arteriosclerosis, diabetes mellitus, heart disease and obesity; J.P.A. 62 099323).
Существуют различные коммерческие доступные липидопонижающие лекарства, которые считаются эффективными, безопасными и хорошо переносимыми, но большинство из них вызывают различные неблагоприятные побочные эффекты. Так как липидоснижающая терапия должна проводиться постоянно, этот аспект очень важен.
Например, гемфиброзил (gemfibrozil) снижает содержание триглицеридов в сыворотке, повышает ЛПВП-С (липопротеины высокой плотности-С) и вызывает легкое снижение сывороточного холестерина, но сообщалось о нескольких присущих лекарству отрицательных эффектах. Так, упоминались воздействия на желудочно-кишечный тракт, такие как эпигастральная боль, диарея, тошнота, рвота и метеоризм. Кроме того, встречались головная боль, головокружение, затуманенное зрение, импотенция, сниженное либидо и нарушения функции печени, такие как повышение трансаминаз, LDH, креатинфосфокиназы и щелочной фосфатазы, у лечившихся гемфиброзилом больных. Также он не должен применяться у больных с почечной недостаточностью.
Пробукол (probucol) является другим липидоснижающим лекарством с антиоксидантными свойствами, которое вызывает легкое снижение уровня холестерина в сыворотке и ЛПНП-С (липопротеинов низкой плотности-С). Тем не менее, недостаток его липидоснижающего действия состоит в том, что он снижает содержание фракции ЛПВП-С. Кроме того, сообщалось о нескольких отрицательных действиях, таких как желудочно-кишечные расстройства у примерно 10% лечившихся, так же как и о значительном изменении электрокардиограммы.
Другими часто используемыми липидоснижающими лекарствами являются холестирамин (cholestiramine) и холестипол (cholestipol). Эти препараты являются эффективными лекарствами первой очереди, снижающими содержание холестерина, которые сильно снижают сывороточный холестерин и ЛПНП, но имеют тенденцию повышать уровни триглицеридов. Эти лекарства вызывали несколько желудочно-кишечных симптомов, в основном, запор.
Результативность лечения обычно низка из-за неблагоприятной сиптоматики, и так как они не являются средствами, легкими для приема, и требуют дозировки от 12 до 20 г/в день для достижения желаемого эффекта. Кроме того, описаны неблагоприятные химические взаимодействия с другими лекарствами, такими как дигитоксин.
Ловастатин является первым из "статинов", лекарств, действующих как ингибиторы ГМЦКоА-редуктазы (гидроксиметилцитозин-коензим A-редуктазы) и таким образом эффективно снижающих уровень сывороточных холестерина и ЛПНП-С, он также умеренно повышает ЛПВП-С и снижает количество триглицеридов. Известно о некоторых неблагоприятных действиях этого лекарства. Так, основными отрицательными эффектами являются миопатия, легкое или умеренное повышение активности креатинфосфокиназы и постоянное повышение сывороточных трансаминаз, которое часто становится обратимым после отмены лечения.
Миопатия встречается главным образом у больных, получающих сопутствующую терапию иммуносупрессивными лекарствами, такими как гемфиброзил или ниацин (niacin). Кроме того, также сообщалось о таких неблагоприятных эффектах, как кожная сыпь, зуд, головная боль и тяжелые поражения мышц у чувствительных больных, приводящие к миолизу, у пациентов, лечившихся ловастатином. Сверх того, также сообщалось о связанных с применением лекарства тестикулярной атрофии и опухолях печени у лабораторных животных.
Аналогично, симвастатин и правастатин - это другие "статины", действующие с помощью тех же самых механизмов, что и ловастатин, и демонстрирующие примерно такое же действие по снижению холестерина. Неблагоприятные эффекты, о которых сообщают эти пациенты, сходны с теми, о которых сообщают у больных, лечившихся ловастатином, но, как утверждают, немного более низкие. У больных, лечившихся симвастатином и правастатином, показано повышение трансаминаз и креатинфосфокиназы, и пациенты сообщают о запорах, метеоризме, тошноте, головной боли, усталости, кожных высыпаниях и миопатиях.
В Европейской патентной заявке 0488928 описывается смесь высших первичных алифатических спиртов из от 24 до 34 атомов углерода с количественным соотношением спиртов, которое может использоваться для лечения гиперхолестеринемии, гиперлипопротеинемии типа II и стимуляции сексуального поведения у животных и людей. Таблица 1 показывает качественный и количественный состав смеси М.Н.Р.А.А., полученной из воска сахарного тростника в соответствии с этим изобретением.
Таблица 1: Основной качественный и количественный состав М.Н.Р.А.А., использованный в препаратах
Компоненты - Количественное отношение в смеси, %:
1-Тетракозанол - 0,5-5,0
1-Гексакозанол - 5,0-15,0
1-Гептакозанол - 0,5-5,0
1-Октакозанол - 50,0-80,0
1-Нонакозанол - 0,5-3,0
1-Триаконтанол - 6,0-20,0
1-Дотриаконтанол - 1,0-10,0
1-Тетратриаконтанол - 0,0-2,5
Специфическая смесь спиртов, предлагаемая в настоящем изобретении, показывает количественный и качественный состав ее компонентов, описанный в таблице 2.
Таблица 2: Особый качественный и количественный состав М.Н.Р.А.А., предложенный в настоящем изобретении
Компоненты - Количественное отношение в смеси, %:
1-Тетракозанол - 0,5-1,0
1-Гексакозанол - 6,0-8,0
1-Гептакозанол - 2,5-3,5
1-Октакозанол - 60,0-70,0
1-Нонакозанол - 0,5-1,0
1-Триаконтанол - 10,0-15,0
1-Дотриаконтанол - 4,5-6,0
1-Тетратриаконтанол - 0,5-2,0
Этот состав неожиданно проявляет новые эффекты, такие как антитромбоцитные, антитромботические и/или антиишемические, противодействие возникновению язв, индуцируемых лекарствами, а также защитный эффект при ишемии. Эта особая смесь демонстрирует также те же самые свойства, о которых сообщалось для смеси, описанной в Европейской патентной заявке 0488928.
М.Н.Р.А.А. согласно изобретению показывает фармакологическое взаимодействие с АСК (ацетилсалициловой кислотой) лекарством, наиболее часто используемым для лечения церебральной ишемии. Таким образом, результаты показали синергизм между антитромбоцитными, антитромботическими и антиишемическими свойствами М.Н.Р.А.А. и АСК.
М. Н. Р. А.А. согласно изобретению значительно снижает язвы желудка, вызываемые аспирином, этанолом, индометацином, веществом C4880 (Sigma) и другими медикаментами, вызывающими язву желудка у людей, получающих лечение.
Известно, что язва желудка, вызванная алкоголем, главным образом связана с повышением TхA2, как физиологического фактора, тогда как при язве, вызываемой C4880, главным образом, вовлекаются серотонергические механизмы, хотя роль TхA2 и его этиогенез нельзя исключить. С другой стороны, язва желудка, вызываемая АСК, связана с подавлением синтеза простагландинов (серия E), вызываемого АСК, так как они имеют цитопротективное действие на слизистую желудка. Было показано, что отношение TхA2 к Pg 12 в слизистой желудка играет важную роль как эндогенный механизм ее целостности.
С другой стороны, описано, что лечение некоторыми липидопонижающими лекарствами снижает склонность к гиперагрегации тромбоцитов, часто наблюдаемой у больных с гиперлипидемией, и данные экспериментов показали антиагрегаторное действие, опосредуемое этими веществами. Тем не менее, только некоторые холестеринопонижающие лекарства проявляют это свойство. Как было объяснено, атеросклероз является непостоянной комбинацией изменений интимы артерий, состоящих из местного скопления липидов, сложных углеводов, крови и продуктов крови, фиброзной ткани и отложений кальция, часто также связанных с медиальными изменениями.
Таким образом, это определение представляет атеросклероз как многофакторный процесс, включающий не только гиперлипидемию в качестве фактора риска. Таким образом, среди факторов, способствующих развитию атеросклероза, агрегация тромбоцитов имеет очень важное место. Выделяющие гранулы тромбоцитов содержат активирующую арахидоновую кислоту, которая метаболизируется в циклические эндопероксиды. Эти последние в основном трансформируются в циклические эндопероксиды и, в конце концов, превращаясь в тромбоксан A2 (TхA2), сильное сосудосуживающее и агрегирующее тромбоциты вещество.
Агрегация тромбоцитов может быть вызвана различными веществами, такими как коллаген, АДФ и эпинефрин, среди прочих. Так, в различных экспериментальных моделях "in vivo", "ex vivo" или "in vitro" для определения эффективности предполагаемых антитромбоцитных лекарств обычно использовали их действие на агрегацию тромбоцитов, вызванную этими веществами.
Эти испытания также используются для определения агрегации тромбоцитов у здоровых добровольцев и у больных с заболеваниями, часто вызывающими повышенную склонность к агрегации, такими как гиперхолестеринемия и диабет, среди прочих. Из этих тестов наиболее часто используется агрегация тромбоцитов, вызванная коллагеном. Так, например, коллаген, введенный внутривенно приводит к обратимой внутрисосудистой агрегации тромбоцитов "in vivo", и агрегаты тромбоцитов поступают в сосудистую микроциркуляцию, постепенно снижая число циркулирующих тромбоцитов и одновременно повышая концентрацию МДА (малондиальдегида) плазмы.
Кроме того, у некоторых видов эта инъекция коллагена вызывает смертность в результате тромбоза. На этих моделях антитромбоцитные лекарства обычно предотвращают снижение количества тромбоцитов и повышение концентрации МДА, так же как и гибель, вызванную коллагеном.
Некоторые лекарства, проявляющие противодействие агрегации тромбоцитов, применимы для лечения тромботических заболеваний, инфаркта миокарда и приступов стенокардии, но не все из них демонстрируют эти преимущества. С другой стороны, существуют антитромботические лекарства, которые главным образом действуют путем литических процессов, влияющие на свертываемость крови, но не на агрегацию тромбоцитов, такие как стрептокиназа и урокиназа.
Так как ишемические сердечно-сосудистые заболевания, стенокардия и патологии с закупоркой периферических сосудов являются главными последствиями атеросклероза, обычно испытывают действия отдельных лекарств на эти осложнения. Так, теоретически, лекарство, проявляющее свойства снижать холестерин, которое также может предотвращать эти осложнения путем воздействия на другие явления, включенные в эти процессы, должно быть полезным для лечения этих больных. Аналогично, снижение уровней TхA2 было связано не только с антитромбоцитным и антитромботическим действиями, но также с противоишемическими эффектами.
Фармакологический отбор антиишемических лекарств обычно включает оценку их воздействий на вызванную общую ишемию головного мозга. Так, был описан защитный эффект различных лекарств на церебральную ишемию у крыс для некоторых нестероидных противовоспалительных препаратов (НСПВП), которые подавляют реакции, катализируемые циклооксигеназой, так же как и специфические ингибиторы тромбоксансинтетазы и аналоги простациклина (Pg12) (Borzeix M.G. and Cahn J., 1988; Effects of new chemically merabolically stable prostacyclin analogues on early consequences of a transient cerebral oligemia in rats; Prostaglandins 35, 5, 653-664).
Также часто используются другие экспериментальные модели, такие как общая ишемия, экспериментально вызванная у монгольских песчанок.
Ацетилсалициловая кислота (АСК) является веществом, проявляющим антитромбоцитные, антитромботические и противоишемические свойства на экспериментальных моделях и у людей. Это лекарство наиболее широко используется для лечения острого инфаркта миокарда и ишемии, так же как и для предупреждения тромбоэмболических нарушений.
Эффекты АСК подтверждаются хорошо известным подавлением ей циклооксигеназы, ключевого фермента в метаболизме арахидоновой кислоты. Так, АСК индуцирует значительное и замечательное снижение уровней тромбоксана A2 (TхA2) в сыворотке крови вещества, которое, как признано, участвует в патофизиологии сосудистого эндотелия, и это объясняет вышеупомянутые эффекты АСК.
Тем не менее, так как подавление АСК проявляется на уровне циклооксигеназы, снижаются не только уровни TхA2, но также уровни простациклина (Pg12), вещества с фармакологическими свойствами, противоположными проявляемым TхB2. С другой стороны, принимая во внимание, что АСК подавляет синтез простагландинов (серии E), она индуцирует поражения желудка, потому что препятствует цитопротективному действию простагландинов. Это является основой главного неблагоприятного побочного действия, о котором сообщают для АСК, то есть гастрита, язвы желудка и связанных с ними нарушений.
Предпочтительный состав из специфических высших первичных алифатических спиртов, упоминаемый в настоящем изобретении, описывается в таблице 3.
Таблица 3: Более специальный качественный и количественный состав М.Н.Р. А.А., использованный в препаратах
Компоненты - Относительное количество в смеси, %:
1-Тетракозанол - 0,8+/-0,1
1-Гексакозанол - 6,7+/-0,3
1-Гептакозанол - 3,0+/-0,3
1-Октакозанол - 65,6+/-3,4
1-Нонакозанол - 0,7+/-0,1
1-Триаконтанол - 12,5+/-0,6
1-Дотриаконтанол - 5,0+/-0,4
1-Тетратриаконтанол - 0,8+/-0,1
Фармацевтические препараты с этой конкретной смесью высших первичных алифатических спиртов могут вводиться людям и животным. Суточная дозировка М. Н. Р.А.А., полученной из воска сахарного тростника, которая будет использоваться для лечения различных заболеваний, установлена в интервале между 1 и 100 мг в день, предпочтительно примерно 3-20 мг М.Н.Р.А.А., может, например, вводиться перорально или парентерально. Предпочтительным способом введения является пероральный прием покрытых пленкой таблеток, так же как и гранул или капсул.
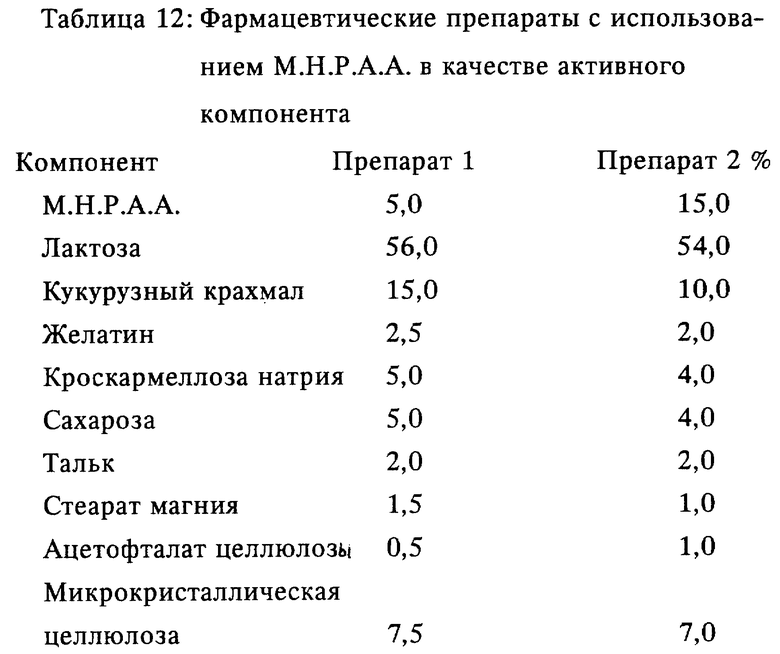
Фармацевтические препараты содержат в качестве активного ингредиента от 0,5 до 15,0 вес.% М.Н.Р.А.А. Такая дозировка получается при смешении М.Н.Р. А. А. с различными наполнителями, такими как агглютинирующие вещества, дезинтегрирующие вещества, скользящие, смазывающие вещества или только наполнители. Эти наполнители включают лактозу, кукурузный крахмал, сахарозу, стеарат магния, микрокристаллическую целлюлозу, кроскармеллозу натрия, желатин, ацетофталат целлюлозы, двуокись титана, специальный тальк для таблеток и полиэтиленгликоль.
Смесь ацетилсалициловой кислоты с М.Н.Р.А.А., объект настоящего изобретения, который будет продемонстрирован в примерах, проявляет синергизм при их фармакологическом взаимодействии, связанном с их антитромбоцитными, антитромботическими и антиишемическими свойствами, если соотношение между ними находится в пределах от 20:1 до 1:20, особенно с таким соотношением, как 10: 1 до 1:10.
Воск сахарного тростника и его природный источник, шлам, всегда представляли интерес, не только из-за их промышленной применимости, но также из-за их химического состава. Количество воска в сахарном тростнике варьирует в пределах между 0,1% и 0,3% в зависимости от его разновидности. Во время агропромышленного процесса только 40% количества воска растворяется в соке, оставшийся материал теряется с выжатым сахарным тростником.
Из этих 40%, 94% этого количества абсорбируется шламом, из которого получается неочищенный воск. Этот воск состоит из эфиров, альдегидов, кетонов, углеводов, жирных кислот и свободных спиртов, причем количество каждого зависит от разновидности и происхождения растений сахарного тростника и технологии, использованной для получения воска.
Алифатические спирты с прямой цепью, получаемые из побочных продуктов сахарного тростника, были изучены несколькими авторами, с целью выяснения из состава и главных свойств. Получение различных групп соединений из всех сортов воска, о котором сообщалось (J.A. Lamberton et al., 1959; Australian Journal of Chemistry 13, 261-268 and Horn A. and Martic J.S.; 1957; Jornal of Science Food and Agriculture, 10, 571), наводит на мысль о способе получения жирных спиртов из кутикулярного воска сахарного тростника, основанном на гомогенном омылении с помощью спиртового раствора гидроксида калия с последующей этерификацией неомыляемого материала и дальнейшей молекулярной перегонкой.
Также сообщается о другом способе выделения смеси спиртов при помощи высокоэффективной колонки с высоким вакуумом. Перегонка воска с высоким вакуумом с целью химического отделения карбонильных соединений и экстракции остающегося воска при использовании петролейного эфира. Растворитель выпаривается и оставшееся содержимое ацетилируется для его дальнейшего выделения с помощью хроматографии на окиси алюминия. В конце концов, с помощью щелочного гидролиза получаются спирты и затем перекристаллизуются из этанола, показывая температуру плавления в пределах от 80 до 82oC.
Технологический процесс для получения смеси высших алифатических первичных спиртов из воска животного и растительного происхождения основан на омылении сложных жирных эфиров с последующей экстракцией смесей спиртов с помощью жидкости в суб- и суперкритическом состоянии при температуре в интервале 25-100oC, используя соответствующие растворители, причем показано, что в зависимости от растворимости при низкой температуре и изменений давления может проводиться селективная экстракция. По этой технологии, примененной к воску сахарного тростника, можно получить 5% смеси спиртов C20-C36.
В другом проекте (Inada S., Furukawa К., Masui T., Honda К., Ogasawara J. and Tsubikamoto G.; 1986; Process for recovering primary normal aliphatic higher alcohols. J.P. 60-119514) предложен очень сходный способ экстракции, примененный к воскам, который основан на жидкостях в суб- и суперкритическом состояниях из CO2 с этиленом. Разделение органических соединений из их смесей посредством жидкостей в суб- и суперкритическом состояниях также описано. С аналитической точки зрения все эти способы являются ценными, но осуществление в большом масштабе затрудняется использованием колоночной хроматографии и молекулярной дистилляции, которые все являются неэкономичными технологиями.
Технология настоящего изобретения основывается на процессе омыления в гомогенной фазе воска сахарного тростника, предварительно расплавленного концентрированными растворами гидроксидов щелочных и щелочноземельных металлов, особенно гидроксидов металлов с низким молекулярным весом, и более конкретно, гидроксидов натрия, калия и кальция.
Концентрация растворов гидроксидов должна быть такой, что отношение по весу соответствующего гидроксида к весу воска, который подлежит переработке, должно быть свыше 5%, особенно от 8 до 25% и более конкретно от 15 до 25%. Процесс омыления протекает в течение периода в 30 минут и более конкретно в течение от 2 до 5 часов. Твердое вещество, полученное на этой стадии, отбирается в аппарат для экстракции в системе твердое тело-жидкость, где М.Н. Р. А. А. селективно экстрагируется соответствующими органическими растворителями, выбираемыми среди кетонов из от 3 до 8 атомов углерода, спиртов из от 1 до 5 атомов углерода, углеводородов из от 6 до 9 атомов углерода, галогенопроизводных, так же как и из ароматических, таких как бензол и его производные, включая их смеси.
Некоторые из растворителей, использованных в настоящем изобретении, являются следующими: ацетон, метилэтилкетон, пентанон, гексанон, гептанон, 2-метилпентанон, этанол, метанол, 2-пропанол, бутанол, тербутанол, пентан, гексан, гептан, октан, хлороформ, 1,2-дихлорэтан, дихлорметан, трихлорэтан, 1,2,3-трихлорпропан, бензол, толуол, фенол, p-метилтолуол и другие.
Экстракция проводится в течение сроков, колеблющихся в пределах от 5 до 10 часов. После чего продукт последовательно кристаллизуется с использованием вышеупомянутых растворителей или их смесей. Выход достигал порядка примерно 30%, в то время как чистота М.Н.Р.А.А. достигала порядка от 80 до 98% и, более конкретно, от 90 до 98%.
М.Н.Р.А.А., полученные таким образом, образуются спиртами, состоящими из от 22 до 38 атомов углерода. Это вещество представляет собой смесь не совсем белого цвета с температурой плавления между 76,5 и 84,5oC. Для анализа М.Н. Р. А.А. с помощью газовой хроматографии на капиллярной колонке из кварцевого стекла эти спирты превращаются в производные с помощью N-метил-N-тетраметилсилан-трифторацетамида (MSTFA).
Предложенная технология получения М.Н.Р.А.А. из воска сахарного тростника имеет некоторые преимущества по сравнению с другими, о которых сообщалось ранее. Одно из этих преимуществ связано с коротким периодом получения. Другое преимущество этого изобретения связано с практическим выходом (около 30% по весу), который может быть получен для спиртов из воска сахарного тростника, по сравнению с результатами, ранее описанными Sho et al., который сообщает о выходе ниже 5%.
Еще одно преимущество предложенной технологии связано со степенью чистоты М. Н. Р.А.А., которая может быть получена (около 98%) и значительно выше той, что сообщалась в ранее опубликованных работах. Таким образом, способ, который предложен в настоящем изобретении, является простым и подходящим для крупномасштабного производства по сравнению со способом, опубликованным Inada et al. (JP 60-119514), а также Hagiwara Y. (JP 62-87537).
И наконец, в общей картине характеристик М.Н.Р.А.А. ее очень хорошая безвредность и переносимость представляют важные преимущества в сравнении с лекарствами современного уровня развития науки. Так, результаты, полученные при изучении острого, субхронического и хронического действия, проведенном на грызунах, кроликах, собаках "бигль" и обезьянах, не выявили токсичности лекарственного препарата.
Кроме того, не показано какого-либо мутагенного действия у этого препарата или, что он обладает тератогенным действием, на крысах и кроликах. Введение М.Н.Р.А.А. на протяжении срока формирования двух поколений животных не влияло ни на развитие плода, ни на репродуктивную способность крыс. И наконец, 24-месячное изучение канцерогенности, проведенное на крысах, также показало отсутствие токсичности и канцерогенного действия у М.Н.Р.А.А.
Краткосрочные и длительные клинические испытания также подтверждают превосходную безвредность и переносимость лечения.
Объекты и цели настоящего изобретения будут описаны подробно в следующих примерах. Эти примеры не будут ограничивать объем указанного изобретения.
Пример 1
1000 г очищенного воска из сахарного тростника брали для расплавления при 100-110oC, добавляя 200 г гидроксида калия, растворенного в 150 мл воды. Этот процесс поддерживался в течение 5 ч при помешивании. М.Н.Р.А.А. экстрагировали из твердого остатка, полученного при процессе, в течение 12 ч в системе экстракции твердое тело-жидкость, используя гептан в качестве растворителя.
Полученный экстракт охлаждается при комнатной температуре, в результате чего М.Н.Р.А.А. кристаллизуется и перекристаллизовывается из метилэтилкетона. До 285 г этой смеси спиртов было получено при чистоте, доходящей до 94,70%. Температура плавления смеси находится в пределах от 80,5 до 82,5oC. Таблица 4 показывает качественный и количественный состав М.Н.Р.А.А., полученной при использовании этой методики.
Таблица 4: Качественный и количественный состав полученной М.Н.Р.А.А.
Компонент - Процентное содержание каждого спирта, %:
1-Тетракозанол - 0,81
1-Гексакозанол - 7,00
1-Гептакозанол - 2,81
1-Октакозанол - 65,09
1-Нонакозанол - 0,67
1-Триаконтанол - 12,43
1-Дотриаконтанол - 5,05
1-Тетратриаконтанол - 0,84
Неидентифицируемый компонент - 5,30
Таким же образом, в зависимости от типа используемого воска сахарного тростника смесь может содержать, %:
1-Тетракозанол - 0,5-5,0
1-Гексакозанол - 5,0-15,0
1-Гептакозанол - 0,5-5,0
1-Октакозанол - 50-80
1-Нонакозанол - 0,5-3,0
1-Триаконтанол - 6,0-20,0
1-Дотриаконтанол - 1,0-10,0
и возможно
1-Тетратриаконтанол - 0,0-2,5
суммарно 100 мас.% при чистоте 80-98%.
Такие же результаты могут быть получены и при использовании ацетона, гексана и/или диэтилэфира в качестве растворителя.
Пример 2
Берется 2 кг (два) неочищенного воска из сахарного тростника для расплавления при 85-100oC, к которым добавляется 300 г гидроксида натрия, растворенного в 200 мл воды, процесс омыления продолжался в течение 4 часов при помешивании. Экстракция М.Н.Р.А.А. выполнялась с использованием хлороформа в качестве растворителя в течение 10-часового периода в обычной системе экстракции твердое тело-жидкость, полученный экстракт охлаждается при комнатной температуре, полученный твердый остаток перекристаллизовывается из метанола и окончательно - из смеси хлороформ/метилэтилкетон. Получали М.Н.Р.А.А. (405 г) с чистотой, доходящей до 92,52%.
Температура плавления М.Н.Р.А.А. находится в пределах 79-80,5oC. Таблица 5 показывает качественный и количественный состав М.Н.Р.А.А., полученной с использованием этой методики.
Таблица 5: Качественный и количественный состав полученной М.Н.Р.А.А.
Компонент - Процентное содержание каждого спирта, %:
1-Тетракозанол - 0,87
1-Гексакозанол - 6,84
1-Гептакозанол - 3,08
1-Октакозанол - 62,92
1-Нонакозанол - 0,80
1-Триаконтанол - 12,66
1-Дотриаконтанол - 4,65
1-Тетратриаконтанол - 0,70
Неидентифицируемый компонент - 7,48
Таким же образом, в зависимости от типа используемого воска сахарного тростника смесь может содержать, %:
1-Тетракозанол - 0,5 - 1,0, особенно 0,8 ± 0,1
1-Гексакозанол - 5,5 - 8,5, особенно 6,7 ± 0,3
1-Гептакозанол - 2,0 - 3,5, особенно 3,0 ± 0,3
1-Октакозанол - 60,0 - 70,0, особенно 65,6 ± 3,4
1-Нонакозанол - 0,4 - 1,2, особенно 0,7 ± 0,1
1-Триаконтанол - 10,0 - 15,0, особенно 12,5 ± 0,6
1-Дотриаконтанол - 4,0 - 6,0, особенно 5,0 ± 0,4
1-Тетратриаконтанол - 0,4 - 2, особенно 0,8 ± 0,1
Суммарно 100 мас.% при чистоте 80-98%.
Такие же результаты могут быть получены и при использовании ацетона, гексана и/или диэтилэфира в качестве растворителя.
Пример 3
Двенадцать кг гидроксида кальция, растворенного в 7 л воды, добавляются к 50 кг очищенного воска сахарного тростника, предварительно расплавленного при 100-120oC.
Процесс омыления продолжается в течение 7,5 ч при помешивании. М.Н.Р.А. А. экстрагируется, при использовании этанола в качестве растворителя, в течение 12 часов в системе экстракции твердое тело-жидкость. Полученный экстракт оставляется для охлаждения при комнатной температуре, затем это твердое вещество перекристаллизуется из хлороформа, и получается М.Н.Р.А.А. (13,7 кг) с чистотой 93,77%.
Температура плавления смеси находится в пределах от 80,0 до 82,0oC. Таблица 6 показывает качественный и количественный состав полученной М.Н.Р. А.А. при использовании этой методики.
Таблица 6: Качественный и количественный состав полученной М.Н.Р.А.А.
Компонент - Процентное содержание каждого спирта, %:
1-тетракозанол - 0,71
1-гексакозанол - 6,88
1-гептакозанол - 3,06
1-октакозанол - 64,70
1-нонакозанол - 0,62
1-триаконтанол - 12,01
1-дотриаконтанол - 5,09
1-тетратриаконтанол - 0,90
Неидентифицируемый компонент - 6,23
Пример 4
8,6 кг гидроксида кальция, растворенного в 4,5 л воды, добавляли к 50 кг неочищенного воска сахарного тростника, предварительно расплавленного при 100-120oC. Процесс омыления производился при постоянном помешивании в течение 3 ч М.Н.Р.А.А. экстрагировался дихлорметаном в качестве растворителя в течение 12 часов в аппарате для экстракции в системе твердое тело-жидкость. Полученный продукт остается для охлаждения при комнатной температуре, и полученное твердое вещество перекристаллизуется из смеси гексана и ацетона 1:1. Смесь спиртов (6,8 кг) получалась с чистотой 92,91%.
Температура плавления М.Н.Р.А.А. составляет 78,5-80,5oC. Таблица 7 показывает количественный и качественный состав М.Н.Р.А.А., полученной этим методом.
Таблица 7: Качественный и количественный состав полученной М.Н.Р.А.А.
Компонент - Процентное содержание каждого спирта, %:
1-тетракозанол - 0,75
1-гексакозанол - 7,00
1-гептакозанол - 3,14
1-октакозанол - 63,60
1-нонакозанол - 0,62
1-триаконтанол - 12,03
1-дотриаконтанол - 4,99
1-тетратриаконтанол - 0,78
Неидентифицируемый компонент - 7,09
Пример 5
Берется двадцать (20) кг очищенного воска сахарного тростника, предварительно расплавленного при температуре 100-110oC, с добавлением 3,7 кг гидроксида калия, растворенного в 3,0 л воды. Процесс омыления продолжался 5 часов, выполняемый при постоянном помешивании. Экстракция М.Н.Р.А.А. производилась с помощью аппарата для экстракции Сокслета (Soxhlet) при использовании метилэтилкетона в качестве растворителя в течение 14 часов. Экстрагированный материал охлаждается при комнатной температуре. Далее он перекристаллизовывается из смеси гексан:хлороформ 1:1. Была получена М.Н.Р.А.А. (3,8 кг) с чистотой, составляющей 92,56%.
Температура плавления М. Н. Р. А. А. находится в пределах между 78,5 и 80,5oC. Таблица 8 показывает количественный и качественный состав М.Н.Р.А.А. , полученной с использованием этой методики.
Таблица 8: Качественный и количественный состав полученной М.Н.Р.А.А.
Компонент - Процентное содержание каждого спирта, %:
1-тетракозанол - 0,85
1-гексакозанол - 6,56
1-гептакозанол - 3,10
1-октакозанол - 63,10
1-нонакозанол - 0,72
1-триаконтанол - 12,18
1-дотриаконтанол - 5,31
1-тетратриаконтанол - 0,74
Неидентифицируемый компонент - 7,44
Пример 6
Один кг неочищенного воска сахарного тростника расплавляли предварительно при 100oC, добавляя 250 г гидроксида кальция. Процесс омыления производится при постоянном помешивании в течение 2 ч М.Н.Р.А.А. экстрагируется с использованием 2-пропанола в качестве растворителя в течение 12 часов в аппарате для экстракции в системе твердое тело-жидкость. Полученный продукт охлаждается при комнатной температуре, после чего перекристаллизуется с использованием гептана. М.Н.Р.А.А. (165 г) получался с чистотой 93,63%.
Температура плавления этой М. Н.Р.А.А. меняется в пределах от 80,0 до 81,5oC. Таблица 9 показывает качественный и количественный состав М.Н.Р.А.А. , полученной с использованием этой методики.
Таблица 9: Качественный и количественный состав полученной М.Н.Р.А.А.
Компонент - Процентное содержание каждого спирта, %:
1-тетракозанол - 0,84
1-гексакозанол - 6,52
1-гептакозанол - 3,18
1-октакозанол - 64,13
1-нонакозанол - 0,69
1-триаконтанол - 12,54
1-дотриаконтанол - 4,93
1-тетратриаконтанол - 0,80
Неидентифицируемый компонент - 6,37
Пример 7
Два (2) кг очищенного воска сахарного тростника предварительно расплавляли при 110oC, добавляя затем 400 г гидроксида натрия, растворенного в 200 мл воды. Этот процесс поддерживается в течение 3 часов при постоянном помешивании. Экстракция М.Н.Р.А.А. выполняется с использованием толуола в качестве растворителя в аппарате для экстракции в системе твердое тело-жидкость в течение 6 часов, причем она повторно перекристаллизуется с использованием метанола в качестве растворителя. М.Н.Р.А.А. (389 г) получалась с чистотой, составляющей 95,10%.
Температура плавления смеси находится в интервале между 81,0 и 83,0oC. Таблица 10 показывает качественный и количественный состав М.Н.Р.А.А., полученной с использованием этого метода.
Таблица 10: Качественный и количественный состав полученной М.Н.Р.А.А.
Компонент - Процентное содержание каждого спирта, %:
1-тетракозанол - 0,80
1-гексакозанол - 7,00
1-гептакозанол - 2,82
1-октакозанол - 64,54
1-нонакозанол - 0,72
1-триаконтанол - 13,02
1-дотриаконтанол - 5,31
1-тетратриаконтанол - 0,89
Неидентифицируемый компонент - 4,40
Пример 7а
1000 г очищенного воска сахарного тростника расплавляли при 100-110oC, добавляя затем 200 г гидроксида натрия, растворенного в 150 мл воды. Этот процесс поддерживается в течение 5 часов при постоянном помешивании. Экстракция М. Н. Р. А.А. выполняется с использованием ацетона или этанола в качестве растворителя в аппарате для экстракции в системе твердое тело-жидкость в течение 9 часов. Полученный экстракт охлаждался при комнатной температуре, причем М.Н.Р.А.А. кристаллизуется и перекристаллизуется в этиловом эфире. М.Н.Р.А.А. (305 г) получалась с чистотой, составляющей 95,60%.
Температура плавления смеси находится в интервале между 81,5 и 82,5oC.
Таблица 10а показывает качественный и количественный состав М.Н.Р.А.А., полученной с использованием этого метода.
Таблица 10a: Качественный и количественный состав полученной М.Н.Р.А.А.
Компонент - Процентное содержание каждого спирта, %:
1-тетракозанол - 0,80
1-гексакозанол - 7,00
1-гептакозанол - 2,73
1-октакозанол - 65,14
1-нонакозанол - 0,70
1-триаконтанол - 13,05
1-дотриаконтанол - 5,28
1-тетратриаконтанол - 0,90
Неидентифицируемый компонент - 4,40
Пример 7б
Два (2) кг очищенного воска сахарного тростника расплавляли при 85-100oC, добавляя затем 280 г гидроксида калия, растворенного в 200 мл воды. Процесс омыления протекает в течение 2 часов при постоянном перемешивании. Экстракция М. Н. Р.А.А. осуществляется с использованием хлороформа или диэтилового эфира в качестве растворителя в течение 10 часов в системе экстрагирования твердое тело-жидкость. После этого экстракт охлаждается при комнатной температуре, причем М. Н.Р.А.А. перекристаллизуется в этаноле и окончательно в гексане. М.Н.Р.А.А. (410 г) получалась с чистотой, составляющей 93,79%, температура плавления М.Н.Р.А.А. находится в интервале между 81 и 82oC. Таблица 10б показывает качественный и количественный состав полученной М.Н.Р.А.А.
Таблица 10б: Качественный и количественный состав полученной М.Н.Р.А.А.
Компонент - Процентное содержание каждого спирта, %:
1-тетракозанол - 0,70
1-гексакозанол - 6,84
1-гептакозанол - 3,08
1-октакозанол - 64,27
1-нонакозанол - 0,80
1-триаконтанол - 12,75
1-дотриаконтанол - 4,65
1-тетратриаконтанол - 0,7
Неидентифицируемый компонент - 6,21
Пример 8
Пять (5) кг очищенного воска сахарного тростника обрабатывали 1 кг гидроксида калия, растворенного в 500 мл воды, после расплавления его при 120oC. Этот процесс протекает в течение 4 часов при постоянном перемешивании. М.Н.Р.А.А. экстрагируется с использованием этанола в качестве растворителя в системе экстрагирования твердое тело-жидкость в течение 5 ч. После этого экстракт охлаждается при комнатной температуре, посредством чего М.Н. Р. А.А. кристаллизуется с использованием толуола в качестве растворителя. М. Н.Р.А.А. (1490 г) получалась с чистотой, составляющей 92,20%.
Температура плавления М. Н. Р. А.А. находится в интервале между 79,5 и 81,0oC. Таблица 11 показывает качественный и количественный состав М.Н.Р.А. А., полученной с использованием этого метода.
Таблица 11: Качественный и количественный состав полученной М.Н.Р.А.А.
Компонент - Процентное содержание каждого спирта, %:
1-тетракозанол - 0,76
1-гексакозанол - 6,58
1-гептакозанол - 2,84
1-октакозанол - 62,43
1-нонакозанол - 0,71
1-триаконтанол - 13,08
1-дотриаконтанол - 5,05
1-тетратриаконтанол - 0,75
Неидентифицируемый компонент - 7,80
Пример 9
Композиции двух различных разработанных фармацевтических препаратов с использованием этой М. Н.Р.А.А. в качестве активной составной части представлены в таблице 12. Эти препараты были разработаны с учетом физических, химических и физико-химических свойств активной составной части. Препараты производились с помощью процесса влажной грануляции активного компонента и фармацевтических наполнителей в контролируемых долях высушиванием, дегранулированием, добавлением скользящих веществ и их штампованием.
Пример 10
Самцов новозеландских кроликов (2-3 кг) адаптировали к лабораторным условиям в течение 15 дней и по случайной выборке распределяли на 4 экспериментальные группы: контрольную (получающую только наполнители) и 3 группы, получавшие лечение М.Н.Р.А.А. в дозе 5, 50 и 200 мг/кг, суспендированных в качестве камеди акации в воде, в качестве наполнителя, путем введения в желудок через зонд (1 мл/кг) на протяжении 4 недель.
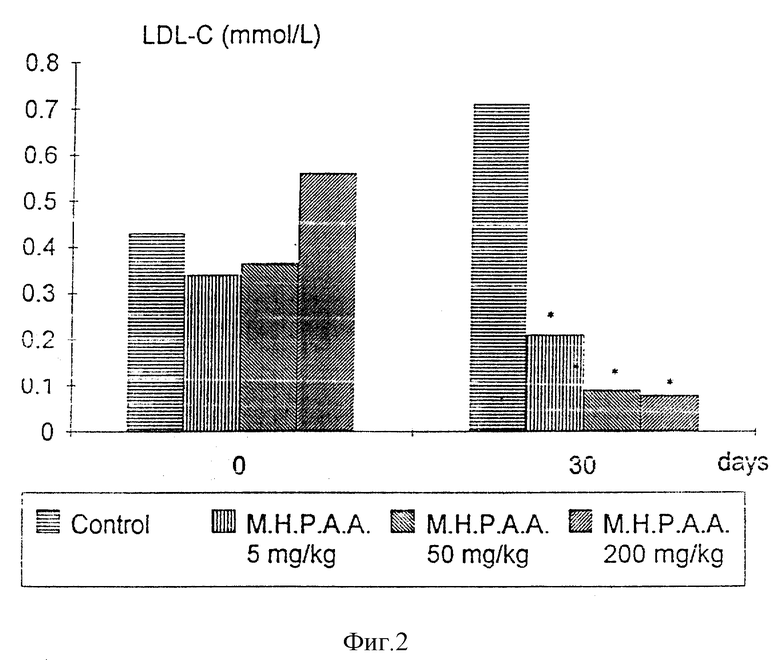
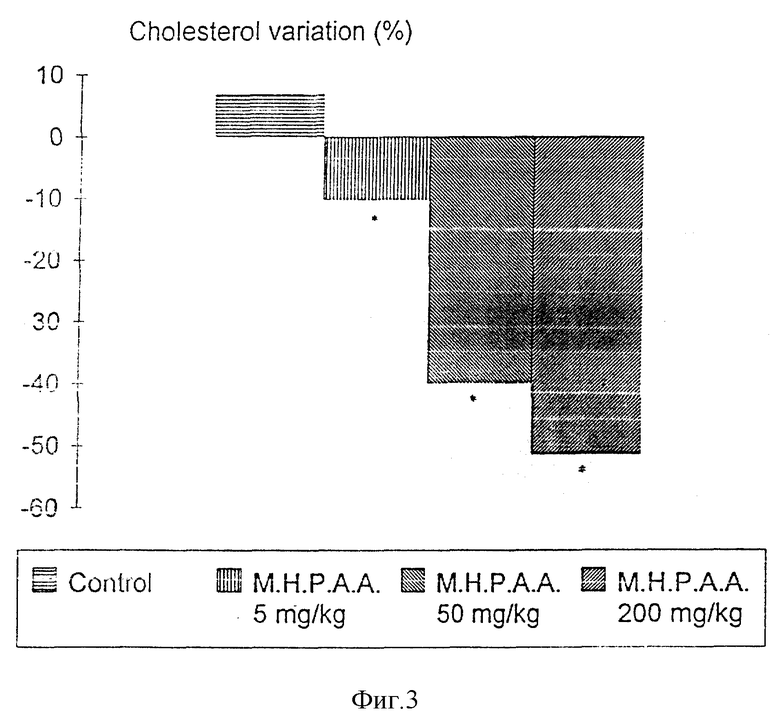
Показатели липидного профиля определяли по основным данным (за день до начала лечения и через 4 недели после). M.H.P.A.A., вводимый перорально в дозах 5, 50 и 200 мг/кг в течение 30 дней, значительно снижал (Wilcoxon, p < 0,05) в зависимости от дозы общее содержание холестерина и уровни в сыворотке ЛПНП (липопротеинов низкой плотности). Кроме того, процентные изменения в контрольной и лечившейся группах были статистически различными (Mann Whitney U, p < 0,05), смотрите фигуры 1-4.
Фиг. 1 показывает действие M.H.P.A.A. на уровни сывороточного холестерина, фиг. 2 - на уровни в сыворотке ЛПНП-С, фиг. 3 - на изменения холестерина в сыворотке и фиг. 4 - на изменения в сыворотке (%) ЛПНП-С у кроликов с нормальными уровнями холестерина в крови.
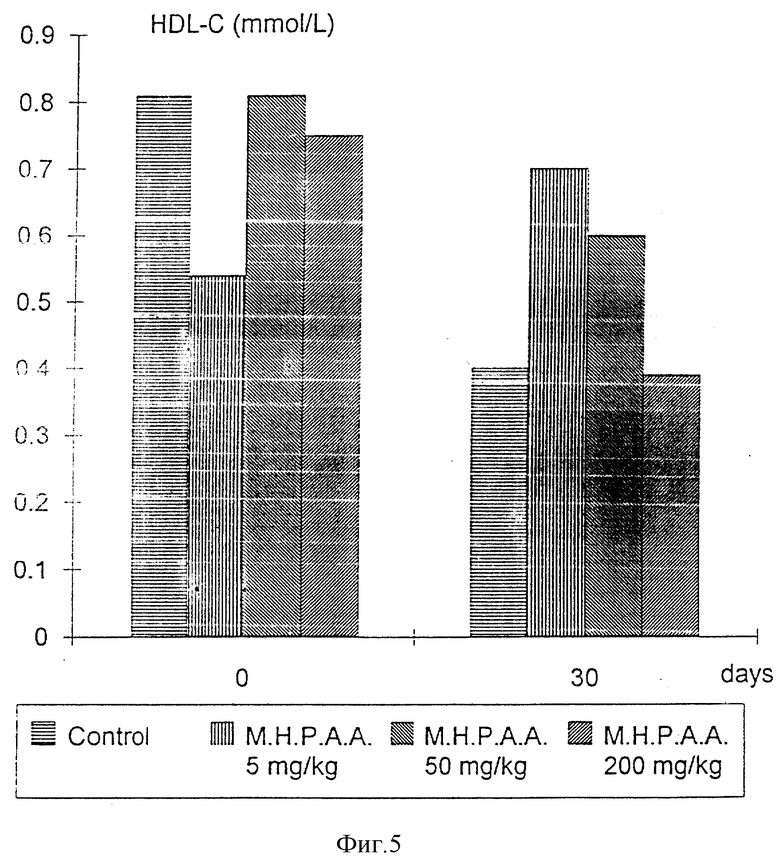
В этой серии экспериментов наивысшая вводимая доза M.H.P.A.A. (200 мг/кг) снижала сывороточный холестерин и ЛПНП-С на 51 и 78% соответственно. Фиг. 5 показывает действие M. H.P.A.A. у кроликов с нормальными уровнями холестерина в крови. Никаких значительных изменений уровней ЛПВП-С (липидов высокой плотности) не продуцировалось во всех четырех группах.
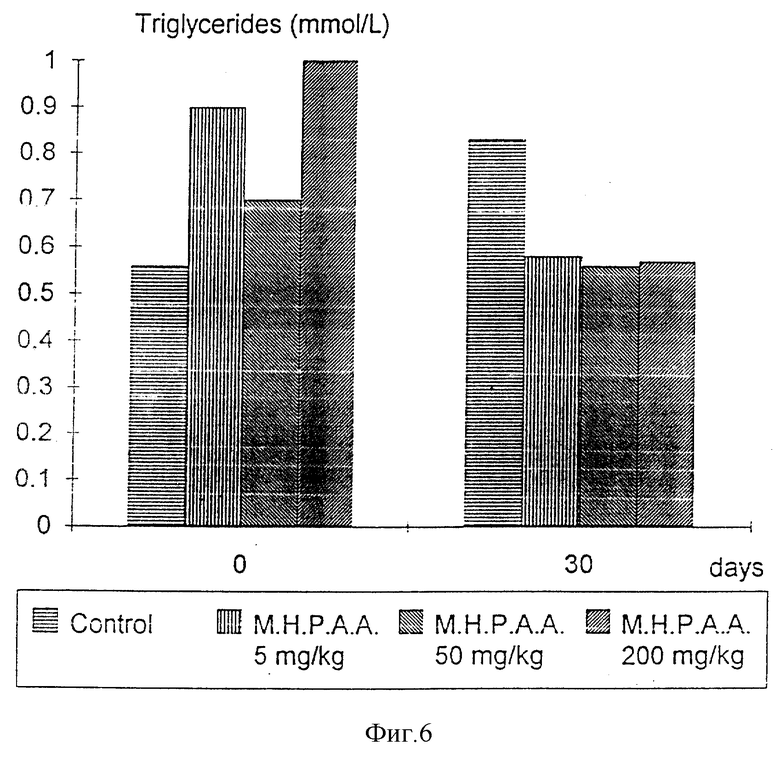
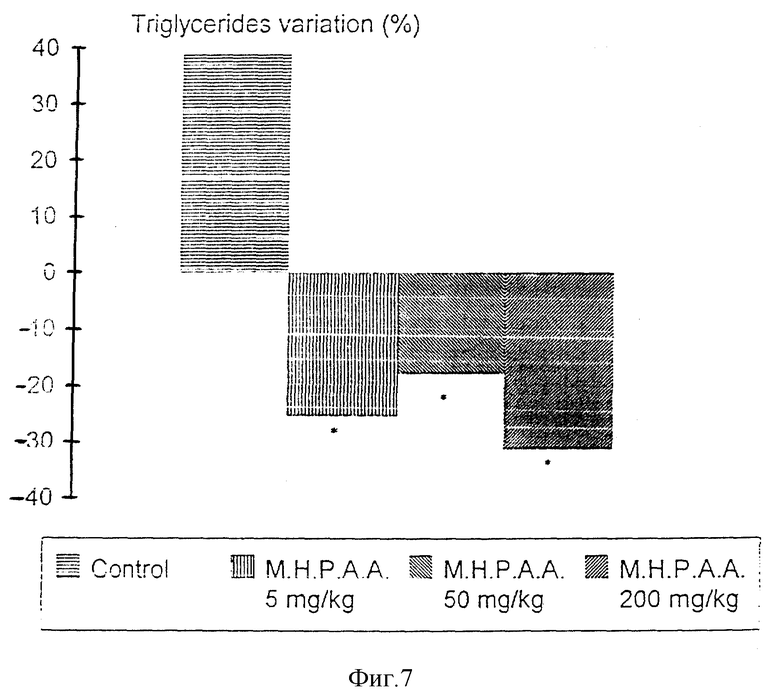
Фиг. 6 иллюстрирует действие M.H.P.A.A. на сывороточные триглицериды и фиг. 7 - на изменения сывороточных триглицеридов у кроликов с нормальным уровнем холестерина в крови. Сравнение процентных изменений триглицеридов у лечившейся и контрольной групп показало, что они были также значительны (Mann Whitney U., p < 0,05), но зависимости эффекта от дозы не наблюдалось.
Пример 11
Самцов новозеландских кроликов распределяли по случайной выборке на 4 группы: контрольную группу (получающие только наполнитель путем введения в желудок через зонд) и 3 группы, лечившиеся М.Н.Р.А.А., октакозанолом и гексакозанолом, соответственно в дозах 5 мг/кг.
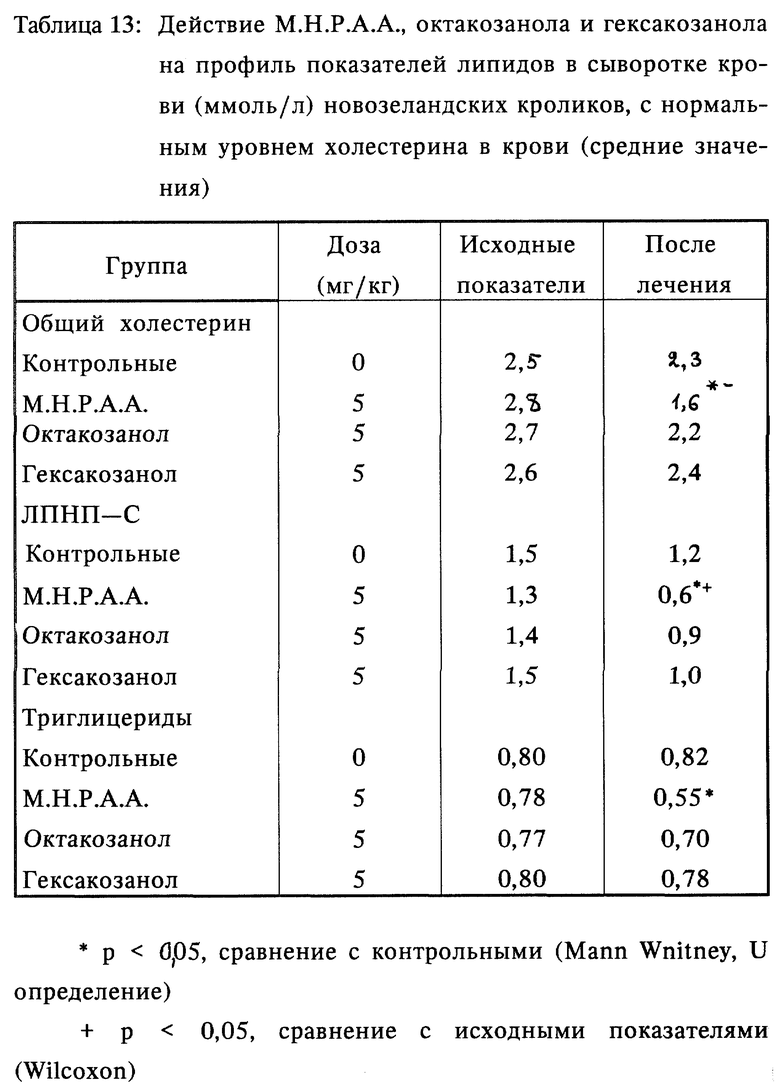
Профиль показателей липидов в сыворотке крови определяли на исходном уровне и через 30 дней лечения. М.Н.Р.А.А. значительно снижала общий уровень холестерина и ЛПНП-С.
Кроме того, уровни холестерина, ЛПНП-С и триглицеридов у кроликов, получавших М.Н.Р.А.А., были значительно ниже, чем уровни в контрольной группе.
Однако изменения профиля сывороточных липидов, наблюдаемые в группах, получавших октакозанол или гексакозанол, не достигали статистических значений различия, что показано в таблице 13.
Пример 12
После 5-недельного периода соблюдения диеты сорок пять амбулаторных больных, у которых показатели холестерина и ЛПНП-С не были достаточно отрегулированы диетой, получали таблетки, содержащие 5 мг М.Н.Р.А.А. (дважды в день, в обед и во время ужина), или плацебо в течение 6 недель.
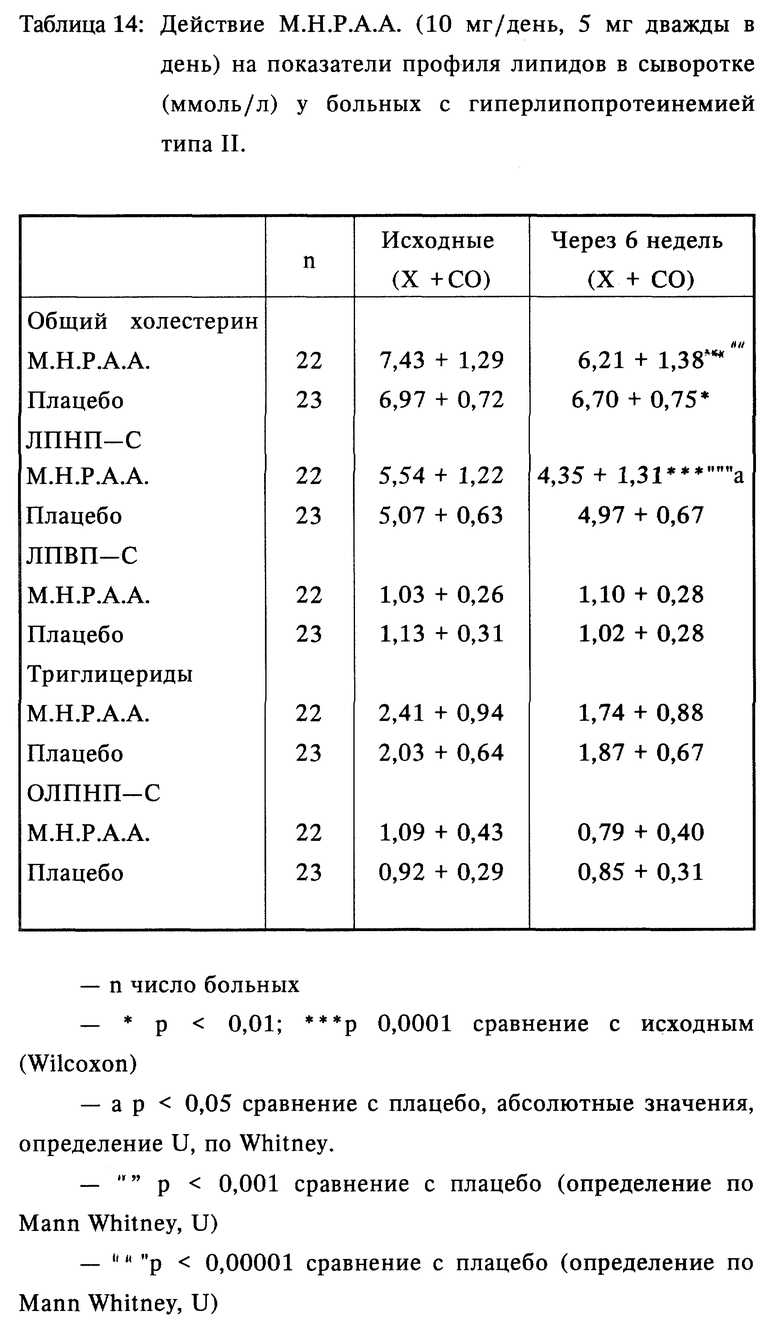
Во время этого периода активного лечения сохранялся режим диеты. Уровни показателей липидного профиля определяли в исходный момент (конец периода только соблюдения диеты), также через 4 и 6 недель после начала терапии. М. Н. Р. А. А. значительно снижала уровень общего холестерина в сыворотке на 16,23% и ЛПНП-С - на 21,33%.
Также были значительно снижены до на 17,67% и 22,28%, соответственно, отношения показателей холестерина к ЛПВП-С и ЛПНП-С к ЛПВП-С (p < 0,05 по определению Wilcoxon для парных данных).
У всех больных уровни как общего холестерина, так и ЛПНП-С через 6 недель после лечения были ниже исходных уровней. Изменения в других фракциях липидного профиля были незначительными, результаты показаны в таблицах 14 и 15.
Пример 13
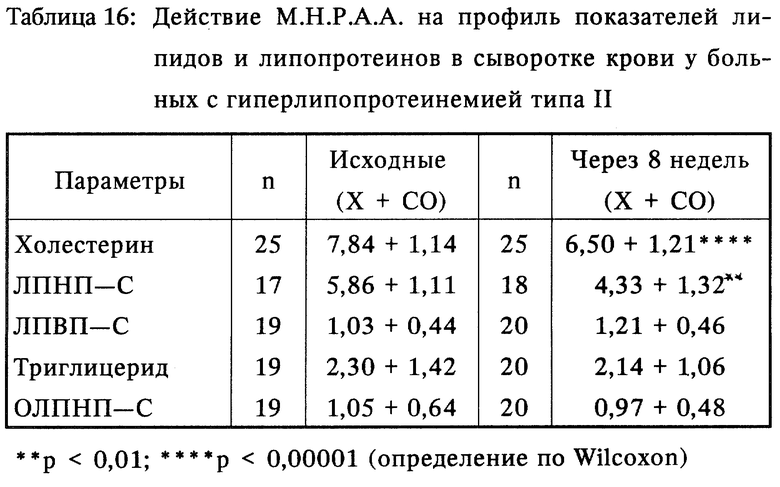
Группа больных с гиперлипопротеинемией типа II получала таблетки, содержащие 15 мг препарата после 8-недельного периода только соблюдения диеты (исходный уровень). Показатели липидного профиля определяли на исходном уровне и через 8 недель после терапии. Основные результаты суммированы в таблице 16. Препарат М.Н.Р.А.А. значительно снижал общий холестерин на 16,44% и ЛПНП-С на 23,51%.
Фиг. 8 показывает действие М.Н.Р.А.А. на профиль показателей липидов у больных с гиперлипопротеинемией типа II, причем изменения показателей холестерина, ЛПНП-С и ЛПВП-С представлены средними значениями и изменения триглицеридов в виде срединного значения. ЛПВП-С повышались на 6,40%, в то время как показатели триглицеридов и ОЛПНП-С снижались на 7,80% и 10,83%, соответственно, но эти изменения не были статистически значимыми.
В таблице 17 показаны изменения по отношениям ЛПНП-С к ЛПВП-С и холестерина к ЛПВП-С, они были значительно снижены на 29,07% и 23,72%, соответственно.
Пример 14
В первую очередь исследовалось действие M.H.P.A.A. на АДФ и индуцируемую коллагеном агрегацию тромбоцитов у крыс. Группу самцов крыс Sprague-Dawley весом 250-350 г распределяли по случайной выборке на две экспериментальные группы.
M.H.P.A.A. вводили перорально в виде суспензии в носителе из водного раствора камеди акации путем внутрижелудочного введения через зонд в течение 4 недель.
В исследование были включены следующие группы: контрольная группа (получающая только носитель) и группа, получавшая M.H.P.A.A. (25 мг/кг).
Для проведения исследования агрегации тромбоцитов крыс анестезировали парами эфира. Брюшную полость вскрывали, и кровь (5 мл) собирали из полой вены и смешивали с 3,8% цитрата натрия (1 объем цитрата на 9 крови).
Обогащенную тромбоцитами плазму (ОТП) получали путем центрифугирования крови. Бедную тромбоцитами плазму (БТП) получали с помощью центрифугирования аликвотных образцов ОТП при 330xg в течение 15 минут. Агрегацию тромбоцитов вызывали АДФ и коллагеном и измеряли с помощью агрегометра Пейтона, как описано (McGregor L., Morazain R. and Renaud S.,; 1980; Effect of dietary Linoleic acid on platelet functions in the rat; Trombosis Res. 20, 499).
Статистическое сравнение результатов, полученных в лечившейся и контрольной группах, проводилось с использованием непараметрного U определения по Mann-Whitney. У крыс, лечившихся М.Н.Р.А.А. в дозе 25 мг/кг в течение 4 недель, показано значительное подавление агрегации тромбоцитов ex vivo, при применении субмаксимальных доз АДФ и коллагена.
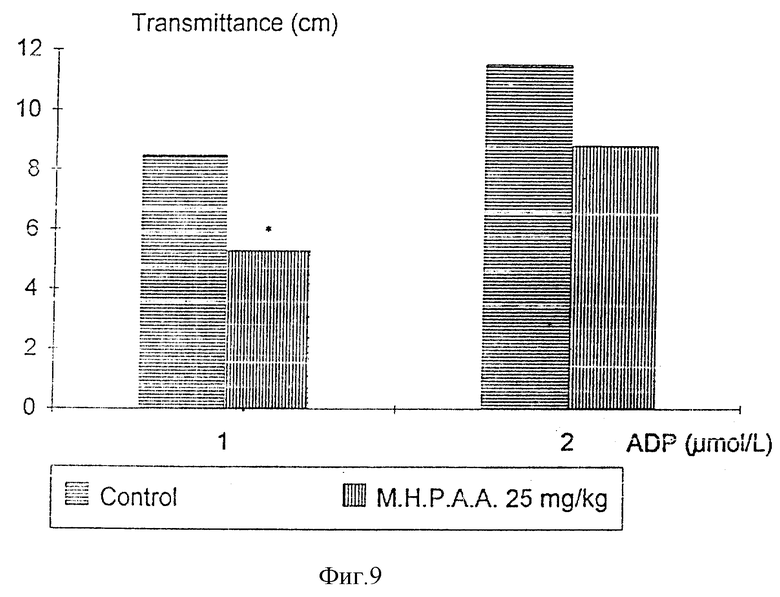
Фиг. 9 показывает агрегацию тромбоцитов у крыс, вызванную АДФ, при введении им М. Н. Р. А.А. в течение 1 месяца, и фиг. 10 - вызванную коллагеном агрегацию тромбоцитов у крыс, которым вводили М.Н.Р.А.А. в течение 1 месяца (p < < 0,05, U определение по Mann-Whitney, 15 см % пропускания).
Введения М. Н. Р. А.А. крысам перорально в течение 4 недель значительно подавляло вызываемую АДФ и коллагеном агрегацию тромбоцитов, наводя на мысль, что М.Н.Р.А.А. действует как противотромбоцитное лекарство.
Пример 15
Чтобы охарактеризовать действие М.Н.Р.А.А. на агрегацию тромбоцитов ex vivo у крыс, были проведены некоторые исследования хода его антиагрегаторного действия на тромбоциты.
С этой целью крыс Sprague-Dawley обоих полов весом 250-350 г распределяли на 4 экспериментальные группы: одна контрольная группа и 3 группы животных, получавших разовые дозы М.Н.Р.А.А. в 25, 50 и 200 мг/кг, соответственно. Кроме того, исследовалось действие на агрегацию тромбоцитов через 2, 6 и 24 часа после введения дозы 200 мг/кг.
М. Н. Р. А.А. готовили, как описано в примере 14, и вводили перорально в однократных дозах за два часа до эксперимента.
Контрольные животные получали тот же объем носителя.
Всех животных лишали пищи, но давали свободный доступ к воде в течение 20 часов перед экспериментом. Всех животных анестезировали эфиром и затем отбирали пробы крови из полой вены и смешивали с 3,8% цитрата натрия (9 объемов крови на 1 антикоагулянта). Кровь центрифугировали при 250 g в течение 10 минут для получения обогащенной тромбоцитами плазмы (ОТП).
После отделения ОТП остаток центрифугировали при 1300 g в течение 15 минут для получения бедной тромбоцитами плазмы (БТП).
Агрегацию тромбоцитов оценивали количественно с помощью турбодиметрического метода (Born G., 1962; Aggregation of blood platelets by adenosine diphosphate and its reversal; Nature (London) 194, 927-929).
Уровни агрегации тромбоцитов измеряли после калибровки прибора на 0% пропускания света для ОТП и на 100% для БТП. Кривые агрегации записывали в течение 5 мин. Фиг. 11 показывает действие М.Н.Р.А.А. на вызванную АДФ агрегацию тромбоцитов в обогащенной тромбоцитами плазме крыс, p < < 0,05 (тест U, Mann-Whitney).
Результаты выражены в процентах от максимальной агрегации (%). Группы сравнивали, используя U тест Mann-Whitney (p < < 0,05).
М. Н. Р.А.А. (50 и 200 мг/кг), вводимая за 2 часа перед отбором образцов крови, подавляла индуцируемую АДФ агрегацию тромбоцитов, тогда как более низкие дозы (25 мг/кг) не давали значительного изменения реакций на АДФ. Наивысшая доза М.Н.Р.А.А. (200 мг/кг) была выбрана для изучения протекания со временем антитромбоцитного действия.
Фиг. 12 показывает действие на индуцированную АДФ агрегацию тромбоцитов при концентрации 2 мкмоль/л, p < < 0,01. Хотя через 2 ч агрегация тромбоцитов была значительно подавлена, через 6 ч подавление имело только пограничные значения (p = 0,06), тогда как через 24 ч никаких статистических различий не получено.
Результаты показывают, что пероральное введение поликозанола крысам за два часа до отбора образцов крови подавляло в зависимости от дозы вызываемую АДФ агрегацию тромбоцитов в ОТП крыс, получивших М.Н.Р.А.А. в дозе 50 и 200 мг/кг.
Подавляющее действие М.Н.Р.А.А. на индуцируемую АДФ агрегацию обратимо, так как через 6 часов после лечения им в дозе 200 мг/кг, подавление агрегации тромбоцитов имело только пограничное значение, и через 24 часа после лечения было выявлено отсутствие эффективности, показывающее, что М.Н.Р.А.А. не вызывает постоянных изменений в клетках.
Пример 16
Изучено действие М.Н.Р.А.А. на внутрисосудистую агрегацию тромбоцитов у крыс и на вызванную коллагеном гибель мышей. Крыс-самцов Sprague-Dawley весом 250-300 г и мышей-самок 57BL6 весом 20-35 г распределяли по случайной выборке в разные экспериментальные группы.
М.Н.Р.А.А. готовили, как описано в примере 14, в то же время АСК растворяли в 5% NaHCO3. Лекарственные препараты вводили перорально через зонд в желудок за два часа перед исследованием. Животные не получали пищи в течение 16 часов перед пероральным введением лекарств. Крысам давали 1 мл/100 г веса тела, а мышам 0,5 мл/20 г веса тела, контрольные животные получали эквивалентные объемы носителя.
При изучении внутрисосудистой агрегации тромбоцитов у крыс использовали 4 группы экспериментальных животных.
1) контрольную, 2, 3 и 4, получавших 5, 10 и 20 мг/кг М.Н.Р.А.А., соответственно. Животных анестезировали внутривенным введением фенобарбитала натрия (30-40 мг/кг). В каротидную артерию вставляли канюлю для отбора образцов крови перед и через 90 секунд после внутривенной инъекции 30 мг/кг в вену пениса.
Кровь (900 мкл) отбирали в пластиковые пробирки, содержащие 100 мкл смеси из 0,7 мг/мл индометацина и 0,19 мг/мл EDTA. Аликвотный образец использовался для определения концентрации тромбоцитов в каждом образце путем подсчета при оптической микроскопии.
Затем кровь центрифугировали и определяли концентрацию в плазме малондиальдегида (МДА) с помощью метода с тиобарбитуровой кислотой (Satoh М, 1978; Serum Lipid peroxyde in cerebroyascular disorders determined by a new colorimetric method; Clin. Chim. Acta 90, 34-43).
Изменения числа тромбоцитов и концентраций МДА в плазме после инъекции коллагена выражались в виде процента от исходных значений. Различия между контрольной и получавшими лечение группами определяли, используя U тест Mann-Whitney.
Для изучения вызываемой коллагеном гибели мышей (крыс?) группы в эксперименте были следующими:
1) контрольная: животные, получающие только носитель, но при индуцировании гибели путем внутривенной инъекции коллагена,
2) животные, предварительно получавшие М.Н.Р.А.А. в дозе 360 мг/кг за 2 часа до инъекции коллагена;
3) животные, предварительно получавшие М.Н.Р.А.А. в дозе 360 мг/кг за 1, 4, 8 и 24 часа до вызова гибели и
4) животные, предварительно получавшие М.Н.Р.А.А. в дозе 180 мг/кг и АСК в дозе 50 мг/кг за 2 часа до исследования.
Растворимый в кислоте коллаген кожи телят типа III получали, как описано у (Kimura Y., Kaube Т. and Watanabe К., 1985; Effect of celostagel on platelet aggregation and experimental thrombosis; Arzneim. Forsch., Orug Research 35, 1140-1148) и использовали в конечной концентрации 2,5 мг/мл. Инъекцию 0,1 мл/20 г производили через ретро-орбитальное сплетение.
Эта доза приводила к 60-100% гибели контрольных животных. Сравнение процента смертности среди контрольных и получавших лечение животных производилось с применением точного определения вероятности Фишера.
Фиг. 13 показывает действие М.Н.Р.А.А. на внутрисосудистую агрегацию тромбоцитов у крыс, p < < 0,05; p < < 0,01 (U тест по Mann Whitney). М.Н.Р. А.А. значительно подавляла снижение числа циркулирующих тромбоцитов и одновременное повышение концентрации МДА в плазме, вызванное коллагеном.
Фиг. 14 демонстрирует действие М.Н.Р.А.А. на вызываемую коллагеном гибель мышей C57BL6, p < < 0,01 (U тест Mann-Whitney).
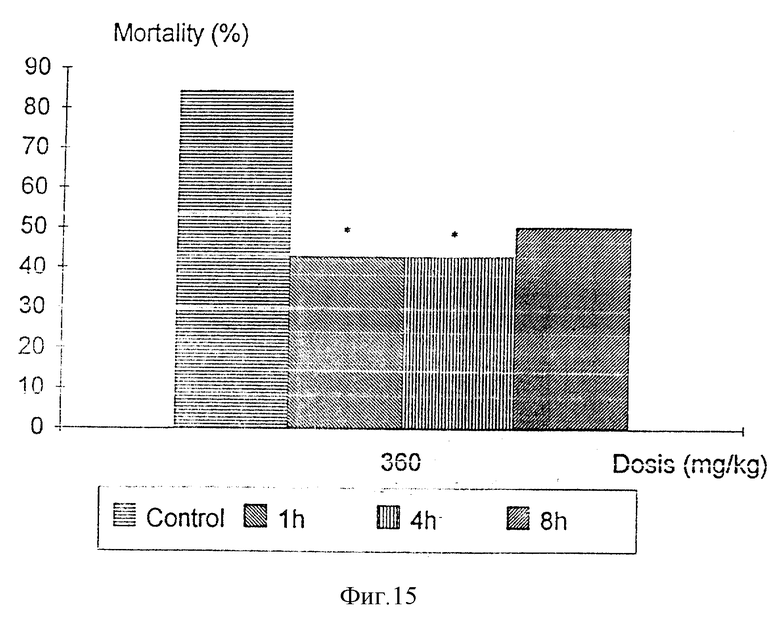
Вызываемая коллагеном гибель значительно снижалась М.Н.Р.А.А. в дозе 360 мг/кг. Это защитное действие при вызываемой коллагеном гибели наблюдалось, когда эта доза вводилась за 1 и 4 часа перед исследованием, но эти значения не получали при введении за 8 часов перед исследованием.
Фиг. 15 показывает действие М.Н.Р.А.А. на вызываемую коллагеном гибель мышей C57BL6, p < < 0,05 (U тест Mann-Whitney).
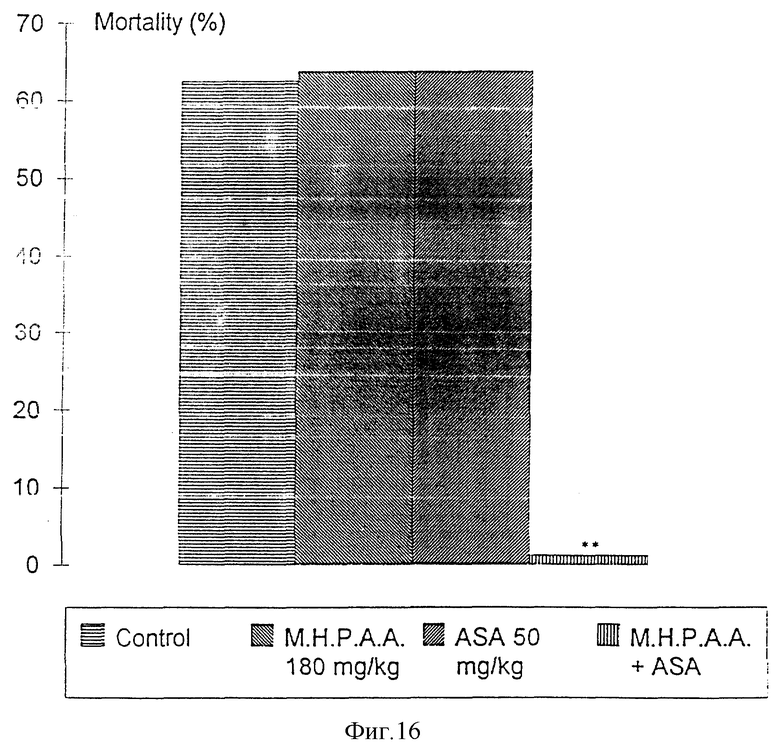
Фиг. 16 иллюстрирует действие комбинированного введения М.Н.Р.А.А. и АСК на вызываемую коллагеном гибель мышей, p < < 0,01 (точное определение вероятности Фишера). Комбинация М. Н.Р.А.А. (180 мг/кг) и АСК (50 мг/кг) также приводит к значительному статистическому снижению вызываемой коллагеном гибели, тогда как лечение обоими препаратами, вводимыми отдельно, оказывалось неэффективным.
Дозы М.Н.Р.А.А. и АСК, которые были неэффективны при введении отдельно, были явно защищающими при совместном введении, показывая таким образом синергизм антитромботического действия М.Н.Р.А.А. и АСК.
Пример 17
Для анализа действия М.Н.Р.А.А. на церебральный инфаркт у крыс, крыс-самцов Sprague-Dawley весом 290-330 г распределяли на следующие экспериментальные группы:
1) отрицательный контроль: крысы без наложения лигатуры, получающие только носитель через желудочный зонд,
2) положительный контроль: крысы с наложением лигатуры, получающие также носитель через желудочный зонд,
3) и 4) крысы с наложенной лигатурой, получающие М.Н.Р.А.А. (5 и 25 мг/кг) тем же самым путем.
Введение разных препаратов производилось ежедневно в течение 4 недель. Последние введения производились за 12 часов до наложения лигатуры, а также через 8 и 24 часа после наложения лигатуры, что обычно применяется на этой модели.
Для вызова церебральной ишемии животных осторожно анестезировали, и олигемию вызывали двусторонней лигатурой общих сонных артерий.
Затем сразу подкожно вводили нитропруссид натрия (0,8 мг/250 г), чтобы вызвать артериальную гипотензию. Перетяжки сонных артерий удаляли через 60 минут, и за животными наблюдали в течение 72 часов и затем забивали. Мозг быстро удаляли и помещали в сушильный шкаф при 80oC на 24 часа. Определяли вес как в сыром виде, так и сухой, чтобы установить содержание воды (отек) и применяли следующую формулу;
Отек = Вес в сыром виде - сухой вес / Вес в сыром виде · 100
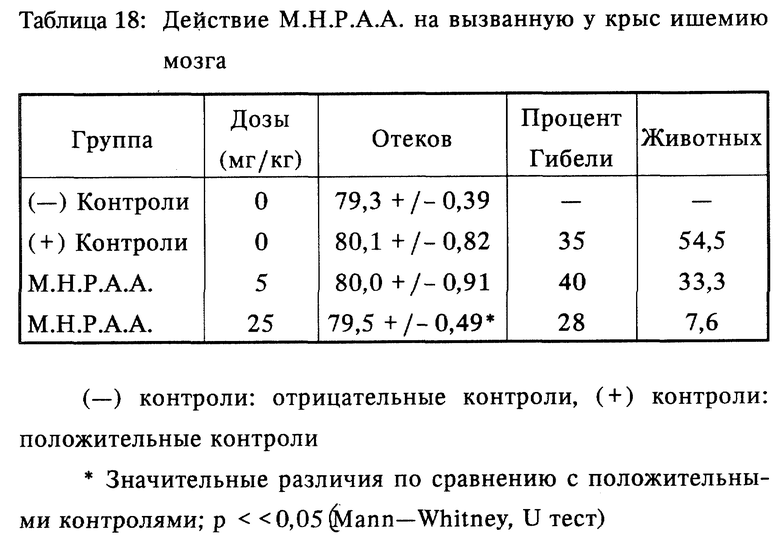
Статистический анализ результатов выполнялся с использованием непараметрного U теста по Mann-Whitney. M.H.P.A.A. в дозе 25 мг/кг значительно снижал отек мозга (p < < 0,05), когда вводился ежедневно в течение 4 недель.
Эта доза также снижала степень гибели и процент животных с отеком, хотя уменьшение этих других показателей не достигало значительных уровней.
Эти данные показывают, что M.H.P.A.A. в дозе 25 мг/кг существенно защищает от церебральной ишемии, вызванной экспериментально у крыс, так как получено существенное снижение отека мозга.
Наблюдалось также снижение процента животных, получавших лечение, у которых выявлены области отека мозга, но это снижение не достигало значительных уровней (таблица 18).
Пример 18
Для изучения синергизма между М.Н.Р.А.А. и аспирином при действии на вызванную у крыс ишемию мозга самцов крыс весом 250-300 г распределяли на 5 групп:
1) отрицательные контроли (крысы без наложения лигатуры);
2) положительные контроли (животные с наложенной лигатурой, получающие только носитель);
3) животные, получающие перорально через желудочный зонд 25 мг/кг М.Н.Р. А.А.;
4) животные, получающие перорально АСК, растворенную в 5% бикарбонате натрия, в дозе 30 мг/кг;
5) крысы, которым вводят перорально АСК (30 мг/кг) + М.Н.Р.А.А. (25 мг/кг). Лекарственные препараты вводили за два часа перед экспериментом.
Чтобы вызвать ишемию, животных осторожно анестезировали эфиром и сонные артерии препарировали и накладывали лигатуру. Гипотензию затем вызывали с помощью подкожной инъекции нитропруссида натрия (0,8 мг/250 г). Перетяжки сонных артерий удаляли через 60 минут, и за животными наблюдали в течение 24 часов. Их забивали, мозг сразу удаляли и помещали в сушильный шкаф при 80oC на 24 часа для определения содержания воды.
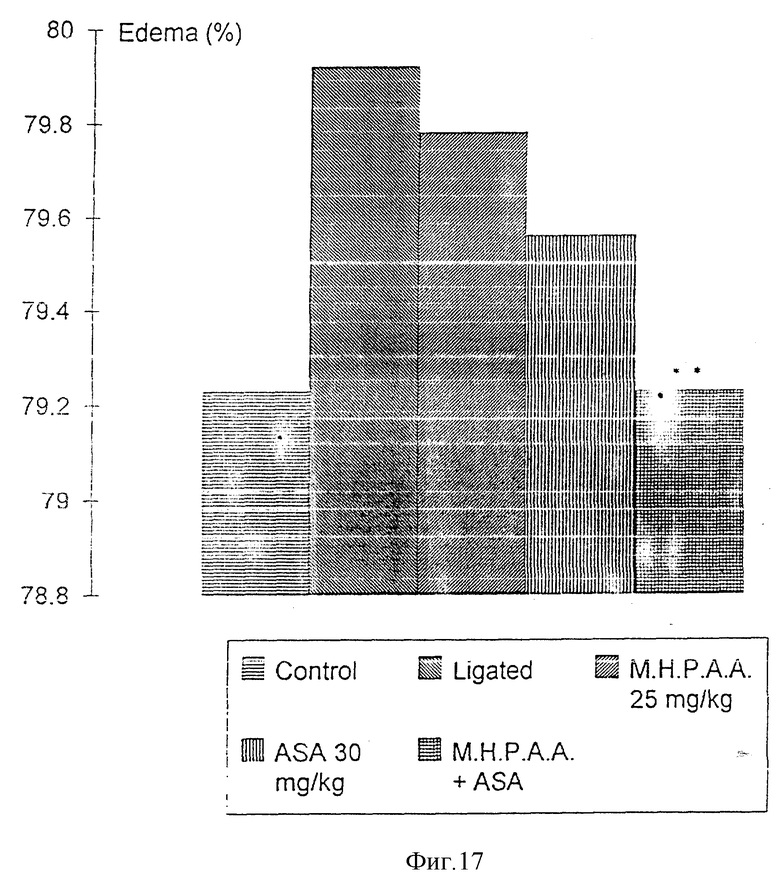
Результаты анализировали, используя непараметрный U тест Mann-Whitney. Фиг. 17 показывает синергизм между М.Н.Р.А.А. и АСК при ишемии мозга у крыс, p < < 0,01 (U тест Мann-Whitney). Ни М.Н.Р.А.А., ни аспирин не снижали значительно ишемии мозга, когда их вводили животным отдельно в вышеупомянутых дозах.
Тем не менее, при совместном введении получали значительную защиту. Эти результаты подтверждают синергизм между антиишемическим действием М.Н.Р.А.А. и АСК.
Пример 19
Использовали монгольских песчанок обоих полов (вес тела 60-80 г) и предварительно адаптировали к лабораторным условиям в течение недели. М.Н.Р.А. А. вводили через желудочный зонд суспендированным в носителе - водном растворе Твин-20.
Животных распределяли по случайной выборке на следующие группы:
(1) положительные контроли (животные с наложением лигатуры, получающие только носитель),
(2) М.Н.Р.А.А. (50 мг/кг) и
(3) М.Н.Р.А.А. (300 мг/кг).
Все препараты вводили за два часа перед индукцией ишемии мозга, Левую общую сонную артерию выделяли на шее и накладывали двойную лигатуру хирургической нитью под эфирной анестезией.
За поведением каждого животного наблюдали в течение 24 часов, отмечая клинические симптомы ишемии мозга, такие как движение по кругу, приступы вращения и захваты.
Отмечалась также гибель животных. Статистическое сравнение частоты гибели и клинических симптомов в группах проводили, используя точную оценку вероятности Фишера.
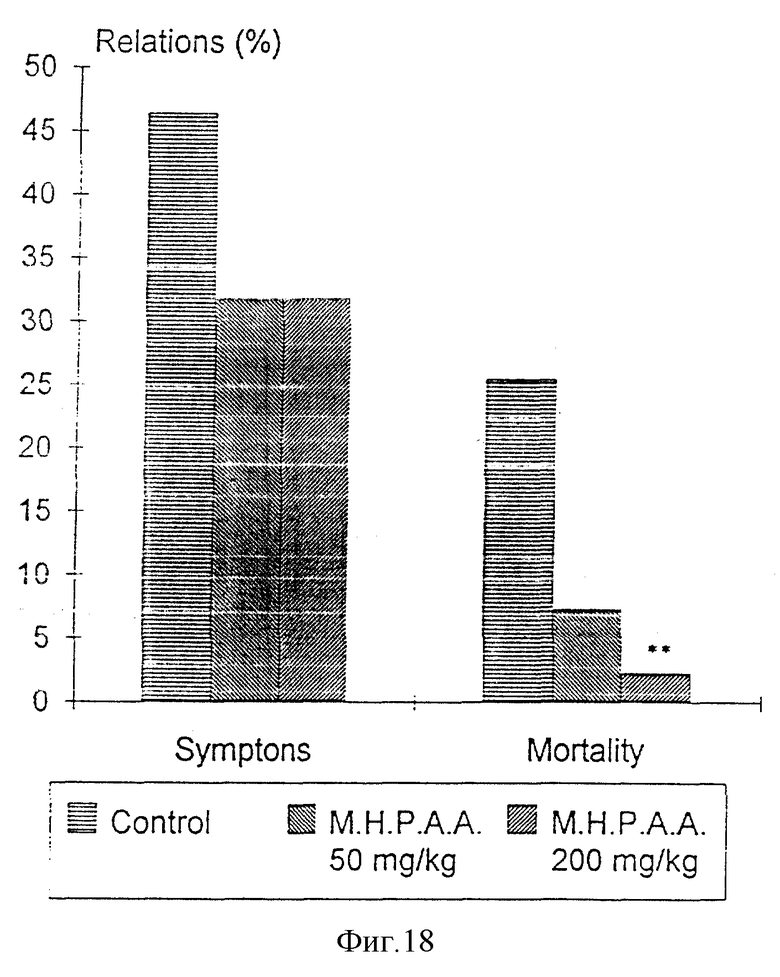
Фиг. 18 показывает действие М.Н.Р.А.А. на инфаркт мозга, вызванный у монгольских песчанок, p < < 0,05 (U тест Mann-Whitney). Результаты показывают, что лечение снижало симптомы и значительно уменьшало гибель животных.
Хорошо известно, что примерно у 60% монгольских песчанок развивается неврологическая недостаточность, такая как поведение кружения и припадки вращения после перевязки общей сонной артерии.
Эти симптомы были связаны с тем фактом, что примерно у 2/3 этих животных существует неполноценность или отсутствие соединяющих артерий между базилярной и каротидной системой.
Кроме того, почти 80% животных, у которых проявляются клинические симптомы, умирают в течение 72 часов после наложения лигатуры.
Так как тяжесть церебрального инфаркта всех областей мозга трудно оценить, в то время как гибель крыс легко подсчитать, обычно используется этот параметр для оценки предполагаемых антиишемических препаратов.
Наши результаты показывают, что М.Н.Р.А.А. (200 мг/кг) в значительной степени защищает от общей ишемии мозга, вызываемый двусторонней лигатурой общих сонных артерий у монгольских песчанок. Таким образом показана применимость М.Н.Р.А.А. для предупреждения развития общей ишемии.
Пример 20
Изучали действие М.Н.Р.А.А. на язву желудка, вызванную различными лекарствами. Использовались крысы Sprague Dawley обоих полов весом 200-220 г. Животных адаптировали к лабораторным условиям в течение недели с предоставлением им пищи и воды ad Libitum (сколько хотят).
После 24-часового голодания крыс делили по случайной выборке на две экспериментальные группы. Животным из первой группы внутрибрюшинно вводили М.Н. Р.А.А. в дозе 25 мг/кг, в виде суспензии в растворе Твин 20 в воде.
В то время как животные второй группы (контрольной) получали только тот же самый объем растворителя. В каждом случае экспериментальная процедура для индукции различных типов язв желудка, вызванных лекарством, проводилась как в контрольной, так и в группе, получающей лечение (для каждого типа язвы использовались две группы):
А) Язву желудка вызывали C 4880 (Sigma). Методика исполнения была сходна с методикой, описанной Awouter F. , Nemegeens C.J.E. and Jansken P.A.J. (1985: Apharmacological analysis of the rat mast cell 5-HT gastric Lesion test and the effect of ketanserin; Drug. Div. Res. 5, 303-312).
Для этого подкожно вводили дифенгидрамин в дозе 10 мг/кг и через 30 минут внутривенно вводили C 4880. Животных забивали через 4 часа после введения C 4880 и быстро удаляли желудки, вскрывали их по длине наибольшей кривизны и промывали дистиллированной водой.
Затем выворачивали слизистые оболочки, и пораженные области измеряли под увеличительным стеклом. Результаты выражали в процентах площади, на которой проявляется поражение.
В этой модели предварительное введение препаратов (М. Н.Р.А.А. или растворителя) производилась за 30 минут до инъекции дифенгидрамина.
В) Язва, вызванная алкоголем. Процедура выполнялась, как описано Zengil Н., Onik Е., Erean T.S. and Tarker R.K. (1987: Protective effect of ilopnost and UK 38485 against gastric mucosal damage by various stimuli; Prostaglandins Leukotrienes and Medicine 30, 61-67).
По этой причине через один час после введения дозы М.Н.Р.А.А. или растворителя крысам перорально через желудочный зонд вводили 40% этанол (1 мл/крысу). Через два часа крыс забивали, и процедура количественной оценки язвы желудка выполнялась как описано.
C) Язва желудка, вызванная АСК: Процедура выполнялась в соответствии с методикой тех же самых авторов, на которых ссылались в предыдущем абзаце.
Через один час после введения М.Н.Р.А.А. или растворителя крысам перорально вводили АСК (100 мг/кг). Через два часа крыс забивали, и процедура измерения язв желудка производилась, как описано.
Сравнение между контрольной и получавшей М.Н.Р.А.А. группами осуществлялось с применением непараметрного U теста Mann-Whitney.
Фиг. 19 показывает действие М.Н.Р.А.А. на язвы, вызванное C 4880 и алкоголем, p < < 0,05. Вводимая внутрибрюшинно М.Н.Р.А.А. (25 мг/кг) значительно подавляла появление язвы желудка, вызванной C 4880, этанолом и АСК.
Кроме того, как можно видеть в таблице 19, вводимая перорально М.Н.Р.А. А. не только снижает TхB2, но также повышает Pg12, таким образом очень значительно снижая отношение TхB2 к Pg12.
Снижение уровней TхB2 и повышение Pg12, вызванное М.Н.Р.А.А., могли объяснить защитное действие этой смеси против язвы желудка.
Таким образом, наблюдается высокозначимое снижение отношения TхB2 к Pg12, когда применяется комбинированное введение М.Н.Р.А.А. и АСК. Кроме того, этот механизм мог также обосновать действие смеси спиртов на другие язвы желудка, вызванные лекарствами.
Пример 21
Сорок пять амбулаторных больных обоих полов в возрасте от 25 до 70 лет с гиперлипопротеинемией типа II получали М.Н.Р.А.А. или плацебо в виде таблеток один раз в день в течение 6 недель (лечившиеся пациенты получали 5 мг/день М.Н.Р.А.А.) в условиях двойного слепого проведения испытаний.
Перед и после лечения определялись следующие параметры: время кровотечения, число тромбоцитов, протромбиновое время, активность прогрессивного антитромбина, время лизиса, эуглобулиновая фракция плазмы, агрегация тромбоцитов, вызванная АДФ, и концентрация малондиальдегида (МДА).
Таблица 20 суммирует данные. Они показывают, что ни один из параметров, связанных с процессом коагуляции, не был затронут, в то время как получено значительное различие между группами по агрегации тромбоцитов, вызванной АДФ. Кроме того, также наблюдалось предельно значимое снижение МДА (p = 0,058).
| название | год | авторы | номер документа |
|---|---|---|---|
| СМЕСЬ ПЕРВИЧНЫХ ЖИРНЫХ КИСЛОТ, ПОЛУЧАЕМЫХ ИЗ САХАРНО-ТРОСТНИКОВОГО ВОСКА | 1998 |
|
RU2217130C2 |
| СМЕСЬ КОМПОНЕНТОВ С ВЫСОКОЙ МОЛЕКУЛЯРНОЙ МАССОЙ, ПОЛУЧЕННЫХ ИЗ ВОСКА САХАРНОГО ТРОСТНИКА (Saccharum officinarum L.) | 2022 |
|
RU2840422C2 |
| КОМБИНАЦИЯ, ОБЛАДАЮЩАЯ АНТИАГРЕГАНТНОЙ, ЛИПИДРЕГУЛИРУЮЩЕЙ И ГАСТРОПРОТЕКТОРНОЙ АКТИВНОСТЯМИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2010 |
|
RU2453314C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ И КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ОЖИРЕНИЯ И ЕЕ ПРИМЕНЕНИЕ | 2011 |
|
RU2608928C2 |
| КОМБИНИРОВАННОЕ АНТИАГРЕГАНТНОЕ И АНТИОКСИДАНТНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2010 |
|
RU2430728C1 |
| Средство, обладающее антиагрегантной, цитопротекторной и антиоксидантной активностью | 2018 |
|
RU2694061C1 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, ОБЛАДАЮЩАЯ АНТИГИСТАМИННОЙ АКТИВНОСТЬЮ | 1992 |
|
RU2099336C1 |
| КАРДИОПРОТЕКТОРНОЕ, АНТИАРИТМИЧЕСКОЕ, ПРОТИВОИШЕМИЧЕСКОЕ СРЕДСТВО | 2007 |
|
RU2366426C2 |
| ДОНОРЫ ОКИСИ АЗОТА, СПОСОБНЫЕ СНИЖАТЬ ТОКСИЧНОСТЬ ОТ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ | 1997 |
|
RU2192247C2 |
| ПОЛИМЕРНЫЙ ВОДОРАСТВОРИМЫЙ АНАЛОГ АЦЕТИЛСАЛИЦИЛОВОЙ КИСЛОТЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2000 |
|
RU2201234C2 |












Описывается новая смесь высших первичных алифатических спиртов С24 - С34, содержащая, мас.%: 1-тетракозанол 0,5 - 1,0, 1-гексакозанол 5,5 - 8,5, 1-гептакозанол 2,0 - 3,5, 1-октакозанол 60,0 - 70,0, 1-нонакозанол 0,4 - 1,2, 1-триаконтанол 10,0 - 15,0, 1-дотриаконтанол 4,0 - 6,0, 1-тетратриаконтанол 0,4 - 2,0. Смесь может использоваться для лечения гиперхолестеринемии и осложнений атеросклероза, таких как повышенная способность тромбоцитов к аггрегации, ишемия и тромбоз, и предупреждает вызываемую лекарствами язву желудка и улучшает сексуальную активность самцов. Это является появлением новых свойств у смеси. Описывается также способ ее получения и фармацевтические композиции на ее основе. 3 с. и 11 з.п. ф-лы, 19 ил., 20 табл.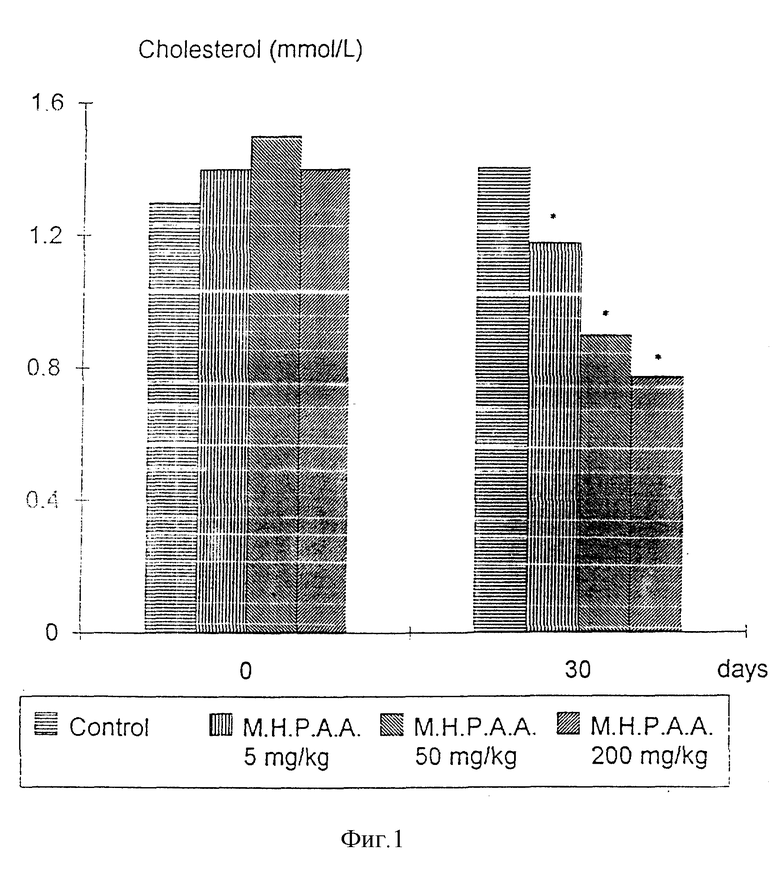
1-Тетракозанол - 0,5 - 1,0
1-Гексакозанол - 5,5 - 8,5
1-Гептакозанол - 2,0 - 3,5
1-Октакозанол - 60,0 - 70,0
1-Нонакозанол - 0,4 - 1,2
1-Триаконтанол - 10,0 - 15,0
1-Дотриаконтанол - 4,0 - 6,0
1-Тетратриаконтанол - 0,4 - 2,0
2. Смесь по п.1, отличающаяся тем, что содержит, мас.%:
1-Тетракозанол - 0,8 ± 0,1
1-Гексакозанол - 6,7 ± 0,3
1-Гептакозанол - 3,0 ± 0,3
1-Октакозанол - 65,6 ± 3,4
1-Нонакозанол - 0,7 ± 0,1
1-Триаконтанол - 12,5 ± 0,6
1-Дотриаконтанол - 5,0 ± 0,4
1-Тетратриаконтанол - 0,8 ± 0,1
3. Смесь по пп.1 и 2, проявляющая антитромбоцитную, антитромботическую и защищающую от общей ишемии мозга активность.
Лактозу - 50,0 - 65,0
Кукурузный крахмал - 10 - 20
Сахарозу - 3,0 - 6,0
Микрокристаллическую целлюлозу - 6,0 - 10,0
Желатин - 1,5 - 4,0
Кросскармеллозу натрия - 3,0 - 7,0
Тальк - 1,0 - 3,0
Стеарат магния - 0,5 - 2,5
и, возможно, другие фармацевтические эксципиенты, например 0,5 - 1,5 мас.% ацетофталата целлюлозы.
| Механизированная крепь сопряжения лавы со штреком | 1973 |
|
SU488928A1 |
| DE 1202262, 07.10.65 | |||
| 0 |
|
SU287000A1 | |
| EP 514009 A1, 19.11.92 | |||
| Пожарный двухцилиндровый насос | 0 |
|
SU90A1 |
| СПОСОБ ПРИЦЕЛИВАНИЯ ПРИ ПАРАШЮТНОМ ДЕСАНТИРОВАНИИ ГРУЗОВ | 1995 |
|
RU2105699C1 |
| УЗЕЛ ОПОРЫ БОКОВОЙ РАМЫ НА КОЛЕСНУЮ ПАРУ ТЕЛЕЖКИ ГРУЗОВОГО ВАГОНА | 2013 |
|
RU2570930C2 |
| EP 452257 A1, 26.03.91 | |||
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1993, ч.2, с.79-80 | |||
| МИРОНОВ В.А | |||
| и др | |||
| Химический состав и биологическая активность экстрактов из компонентов плодов облепихи | |||
| - Химико-фармацевтический журнал, т.23, № 11, 1989, с.1357-1364. | |||
Авторы
Даты
2001-02-20—Публикация
1993-02-25—Подача