Изобретение относится к биохимии, точнее к группе биологически активных веществ, обладающих противовирусным действием.
Известен препарат - дуплекс полирибоинозината и полирибоцитидилата, поли(И) · поли(Ц). Он обладает противовирусной и интерферон-индуцирующей активностью в организме теплокровных животных, однако при этом имеет и недостаток - высокую токсичность, причем его токсичность дополнительно усиливается в клетках и организмах, пораженных вирусной инфекцией [Field A.K., Tytell A. A. , Lampson G.P., Hilleman M.R. Inducers of interferon and host resistance. II. Multistranded synthetic polynucleotide complexes. //Proc. Natl. Acad. Sci. USA. - 1967. - V. 58, N 3. - P. 1004-1010. [1], De Clercq E. , Stewart W.E., De Somer P. Increased toxicity of double-stranded ribonucleic acid in virusinfected animals, //Infect, immunity. - 1973. - V. 7. - P. 167-172. [2]].
Известен также дуплекс полирибогуанилата и полирибоцитидилата - поли(Г)·поли(Ц). Он также обладает значительной противовирусной и интерферон-индуцирующей активностью, однако его недостаток - склонность к агрегации и гелеобразованию в водных растворах [Тимковский А.Л., Коган Э.М., Аксенов О. А. и др. Термоактивация поли(Г)·поли(Ц): описание эффекта и его предполагаемый механизм. //Вопросы вирусол. - 1982. - Т. 27. - С. 92-96. [3]].
Известен также комплекс полирибонуклеотидного дуплекса поли(Г) · поли(Ц) с цис-диамминдихлор-платиной (II) - [поли(Г) · поли(Ц)]m · [Pt(II)X2]n, где X - NH3Cl. Противовирусная и интерферон-индуцирующая активность такого комплекса выше, чем у исходного дуплекса. Однако повышение активности происходит лишь в узкой области - при малых содержаниях Pt(II)X2 (массовое отношение m: n = 1:0,02, а обратная величина n:m = rb = 0,02 - молярная степень включения Pt(II)X2), и при этом не преодолевается склонность дуплекса к агрегации. При более высоких значениях rb активность снижается, а дуплекс дестабилизируется [Brabec V., Vrana О., Platonova G.A. et al. Biophysical studies of the modification of poly(rG)·poly(rC) by cis-platin. Relation to the biological activity of the complex. //Chem.-Biol. Interact. - 1991. - V. 78. - P. 1-12. [4]].
Наиболее близким к заявляемому является полирибонуклеотидный дуплекс полирибоаденилата и полирибоуридилата - поли (А) · поли (У), также обладающий противовирусной и интерферон-индуцирующей активностью и при этом мало токсичный и не склонный к агрегации в растворе. Благодаря этим преимуществам поли(А) · поли(У) используется в глазных клиниках в качестве противовирусного лекарства, в качестве иммуномодулятора при опухолевых заболеваниях и проходит испытания против вируса иммунодефицита человека. Однако его противовирусная и интерферон-индуцирующая активность ниже, чем у других дуплексов-аналогов [1].
Вследствие того что малотоксичный полирибонуклеотидный дуплекс поли(А) · поли(У) применяется в клинической практике, желательно обеспечить его более высокую активность.
Это обеспечивается тем, что предлагается полирибонуклеотидный дуплекс на основе полирибоаденилата и полирибоуридилата, отличающийся тем, что в него дополнительно введено соединение двухвалентной платины: или цис-диамминдихлорплатина (II), или цис-дигидроксиламиндихлорплатина (II), причем комплекс полирибонуклеотидного дуплекса имеет формулу
[поли(А)·поли(У)]m · [Pt(II)X2]n,
где Pt(II)X2 - или цис-диамминдихлорплатина (II), X = NH3Cl,
или цис-дигидроксиламиндихлорплатина (II), X = NH2OCl, при этом m:n = 1: (0,02-0,20).
Необходимость введения в полирибонуклеотидный дуплекс на основе полирибоаденилата и полирибоцитидилата соединения двухвалентной платины неочевидна. Известны результаты введения двухвалентной платины в полирибонуклеотидный дуплекс на основе полирибоинозината и полирибоцитидилата - поли(И) · поли(Ц). При этом не наблюдается повышение противовирусной и интерферон-индуцирующей активности дуплекса [De Clercq Е., Hermann D., Guschlbauer W. Interferon induction by platinum(II)-poly(I)·poly(C) complexes. //Biochim. Biophys. Acta. - 1983. - V. 741. - P. 358-363. [5]], а сам дуплекс дестабилизируется [Hermann D. , Houssier C., Guschlbauer W. Dissociation of double-stranded poly(I)·poly(C) by cisdiammine-dichloro-Pt(II). //Biochim. Biophys. Acta. - 1979. - V. 564. - P. 456-472. [6]]. При введении соединения двухвалентной платины в полирибонуклеотидный дуплекс на основе полирибогуанилата и полирибоцитидилата - поли(Г) · поли(Ц) некоторое повышение противовирусной и интерферон-индуцирующей активности наблюдается, но лишь в узком интервале содержания соединения двухвалентной платины - при rb не выше 0,02. При увеличении степени включения соединения двухвалентной платины (rb > 0,02) полирибонуклеотидный дуплекс дестабилизируется [4], и его активность резко снижается [[4], Аксенов О.А., Мурина Е.А., Коган Э.М. и др. Биологическая активность комплекса поли(Г) · поли(Ц), модифицированного соединениями двухвалентной платины. //Вопросы вирусол. - 1995. - Т. 40, N 2. - С. 56-59. [7]].
Опытным путем было установлено:
1. При введении соединения двухвалентной платины в полирибонуклеотидный дуплекс на основе полирибоаденилата и полирибоуридилата наблюдается повышение противовирусной и интерферон-индуцирующей активности, причем в намного более широком диапазоне степени включения Pt(II)X2, чем для дуплекса поли(Г) · поли(Ц) - вплоть до rb = 0,2.
2. Дуплекс поли(А) · поли(У) при введении соединения двухвалентной платины стабилизируется, что доказывается повышением его температуры плавления.
3. Токсические проявления при введении соединения двухвалентной платины в дуплекс поли(А) · поли(У) вплоть до уровня rb = 0,2 отсутствуют, что делает возможным применение его с соединением двухвалентной платины в клинических условиях.
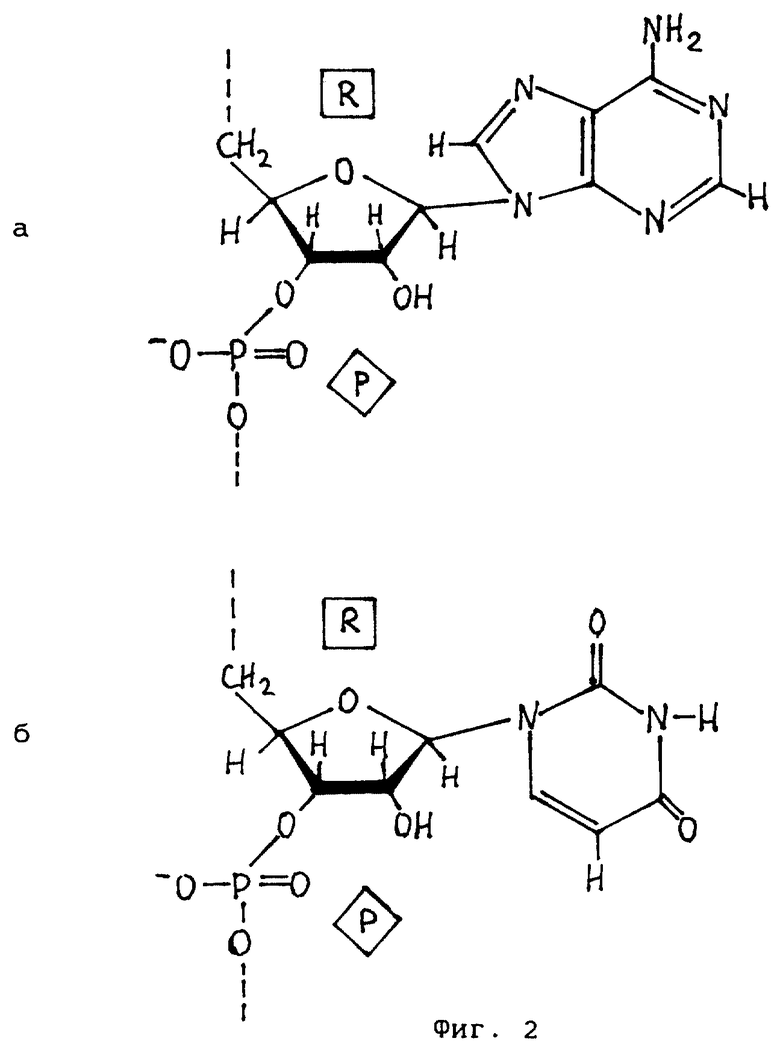
На фиг. 1 представлена структурная формула участка комплекса полирибонуклеотидного дуплекса поли(А) · поли(У) с цис-диамминдихлорплатиной (II). На фиг. 2 представлены структурные формулы звена полирибоаденилата (а) и звена полирибоуридилата (б). На фиг. 3 представлены структурные формулы цис-диамминдихлор-платины(II) (а) и цис-дигидроксиламинодихлор- платины(II) (б).
Заявляемые комплексы полирибонуклеотидного дуплекса [поли(А) · поли(У)]m · [Pt(II)X2]n получают следующим образом.
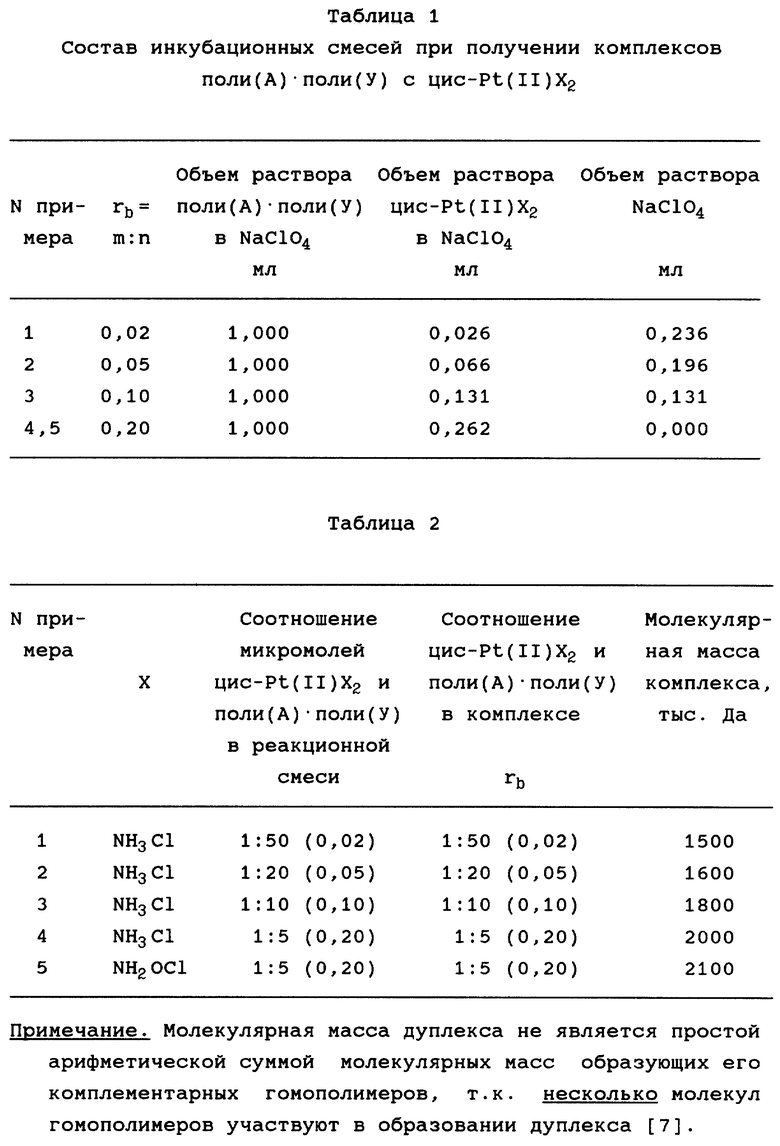
Дуплекс поли(А) · поли(У) получают из поли(А) с молекулярной массой 100-500 тыс. дальтон (Да) и поли (У) с молекулярной массой 100-500 тыс. Да смешением их эквимолярных количеств в растворе, содержащем 0,005 М натрий-фосфатный буфер, pH 7,4 и 0,1 М хлористый натрий и инкубацией смеси при 37o в течение не менее 1 часа [1]. После этого дуплекс диализуют против 0,01 М раствора этилендиамминтетраацетата Na, затем против 0,1 М NaClO4. К 1 мл 0,1 М раствора NaClO4, pH 7,0, содержащего 1,18 мкмоль поли(А) · поли(У), добавляют необходимое для получения нужного значения rb количество раствора, содержащего в 1 мл 0,923 мкмоля Pt(II)X2 и NaClO4 0,1 М, pH 7,0, и необходимый объем 0,1 М раствора NaClO4, pH 7,0, дополняющий объем реакционной смеси до 1,262 мл. Полученный раствор прогревают при температуре 37oC в течение 48 часов в темноте. Получают раствор, который содержит комплекс полирибонуклеотидного дуплекса и Pt(II)X2, при этом концентрация дуплекса - 700 мкг/мл. Таким способом получают комплексы с различным содержанием соединения Pt(II), что подтверждается примерами (таблица 1).
Характеристики комплексов поли(А) · поли(У) с цис-Pt(II)X2, где X = NH3Cl или NH2OCl, приведены в таблице 2.
Доказательства образования заявленного вещества:
а) изменение профиля элюции при гель-хроматографии по сравнению с профилем исходного дуплекса поли(А) · поли(У), молекулярная масса полученного комплекса - 1,5-2 млн Да;
б) состав комплекса охарактеризован числом ковалентно связанных атомов Pt(II) на один нуклеотидный остаток методом дифференциальной импульсной полярографии на ртутном капельном электроде [6].
Температуру плавления дуплекса поли(А) · поли(У) определяли спектрофотометрически путем регистрации изменений оптической плотности растворов при 260 нм на спектрофотометре СФ-26 при прогреве растворов в герметически закрытых кюветах, помещенных в термостатируемый кожух. Оптическую плотность, измеренную при данной температуре (At), относили к начальной оптической плотности, измеренной при 25oС (A25). За температуру плавления (Tпл) принимали значение температуры, соответствующее 50% приросту At/A25 [Michelson A. M. , Massoulie J., Guschlbauer W. Synthetic polynucleotides. //Progr. Nucl. Acids Res. Mol. Biol. - 1967. - v. 6. - P. 83-141. [8]].
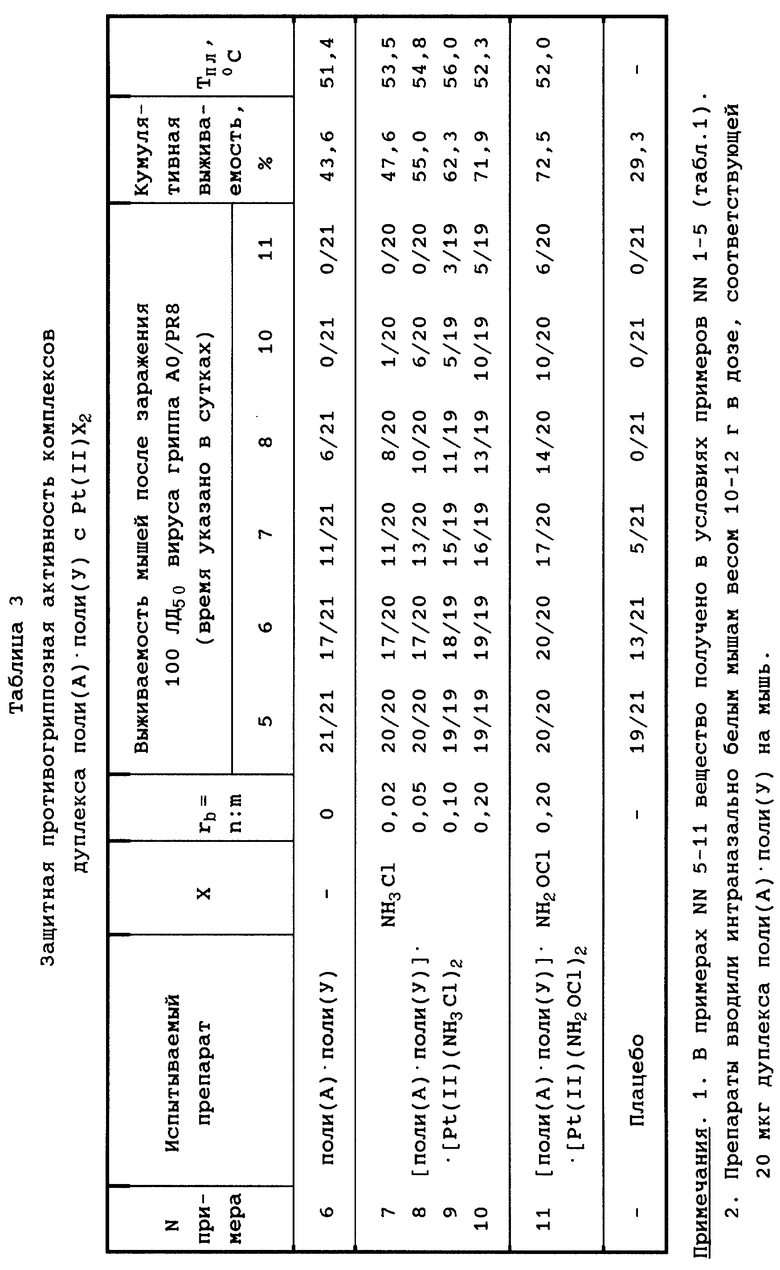
Все полученные комплексы с разным содержанием Pt(II)X2 проверены на противовирусную и интерферон-индуцирующую активность. В таблице 3 отражены данные о противовирусной (противогриппозной) активности полученных комплексов при их внутривенном введении белым мышам. Противовирусная активность комплексов монотонно возрастает с увеличением rb.
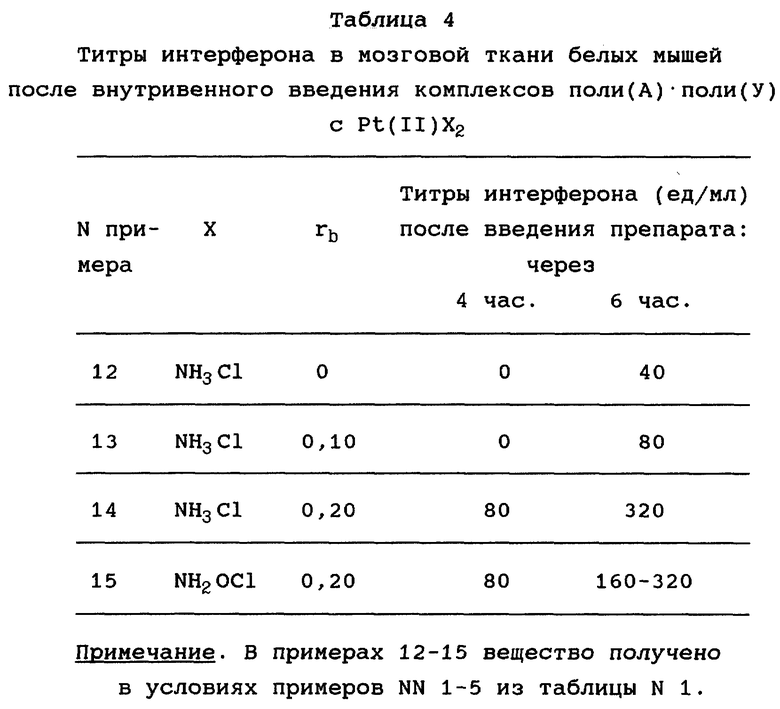
В таблице 4 отражены данные об индукции интерферона в мозгу белых мышей при внутривенном введении комплексов поли(А) · поли(У) с цис-Pt(II)X2.
С увеличением содержания неорганического соединения Pt(II)X2 в комплексе с полирибонуклеотидным дуплексом поли(А) · поли(У) уровень интерферона в мозгу животных возрастает с повышением rb, его максимальное значение наблюдается при rb = 0,20. Комплексы с более высоким rb токсичны для мышей при внутривенном введении [6, 7].
Результаты проведенных испытаний показывают, что в отличие от других полирибонуклеотидных дуплексов-аналогов, полирибонуклеотидный дуплекс на основе полирибоаденилата и полирибоуридилата после введения в него соединения двухвалентной платины приобретает более высокую противовирусную и интерферон-индуцирующую активность, повышенную стабильность и способность индуцировать образование интерферона в мозгу теплокровных животных.
Таким образом, заявляемое вещество обладает существенными преимуществами. Введение соединения двухвалентной платины в полирибонуклеотидный дуплекс поли(А) · поли(У) повышает его противовирусную и интерферон-индуцирующую активность. Активность монотонно возрастает с повышением содержания соединения Pt(II)X2 в широком диапазоне значений rb - вплоть до rb = 0,20. Добавление к дуплексу поли(А) · поли(У) соединения Pt(II)X2 увеличивает его стабильность, что отражается в повышении температуры плавления дуплекса. При введении комплекса в кровяное русло теплокровных животных значительный уровень интерферона обнаруживается в головном мозгу, что служит свидетельством преодоления гемато-энцефалического барьера и позволяет использовать заявляемое вещество в качестве противовирусного препарата против нейровирусных инфекций.
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТРОЙСТВО ДЛЯ РЕНТГЕНОФЛУОРЕСЦЕНТНОГО АНАЛИЗА | 1997 |
|
RU2158918C2 |
| Способ термоактивации двунитевых полирибонуклеотидных комплексов | 1978 |
|
SU713871A1 |
| Цис-диамминдихлороаквагидроксоплатина (1У)-сульфат и способ его получения | 1988 |
|
SU1557106A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИС-ДИХЛОРОДИАММИНПЛАТИНЫ (II) | 2013 |
|
RU2538895C2 |
| СПОСОБ ИЗМЕРЕНИЯ РАДИАЦИОННОЙ ЭЛЕКТРОПРОВОДНОСТИ ДИЭЛЕКТРИЧЕСКОГО МАТЕРИАЛА | 1999 |
|
RU2148819C1 |
| СПОСОБ РАЗДЕЛЕНИЯ ИЗОТОПОВ ВОДОРОДА | 1998 |
|
RU2148426C1 |
| КОМПОЗИЦИЯ ДЛЯ ПРИГОТОВЛЕНИЯ ПРОТИВООПУХОЛЕВОГО СРЕДСТВА И СПОСОБ ПРИГОТОВЛЕНИЯ ПРОТИВООПУХОЛЕВОГО СРЕДСТВА НА ЕЕ ОСНОВЕ | 2016 |
|
RU2667128C2 |
| СПОСОБ ИССЛЕДОВАНИЯ СТРУКТУРНО-ДИНАМИЧЕСКИХ СВОЙСТВ ВЕЩЕСТВА | 2006 |
|
RU2327975C1 |
| ТРЕХПЛАТИНОВЫЕ КОМПЛЕКСЫ PT(II), СПОСОБ ИХ ПОЛУЧЕНИЯ | 1994 |
|
RU2140422C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФУЛЛЕРЕНА C | 2001 |
|
RU2224714C2 |
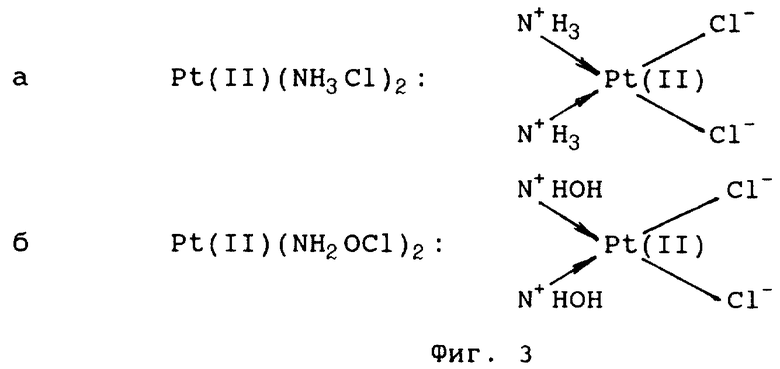
Изобретение относится к биохимии, а именно к получению биологически активных веществ, обладающих противовирусным действием. Описывается полирибонуклеотидный дуплекс на основе полирибоаденилата и полирибоуридилата, содержащий соединения двухвалентной платины в виде или цис-диамминдихлорплатины или цис-дигидроксиламиндихлорплатины (II), причем комплекс полирибонуклеотидного дуплекса имеет формулу [поли(А)·поли (Y)]m · [Pt(II)Х2]n, где Pt(II)Х2 - или цис-диамминдихлорплатина (II), X - NH3Cl, или цис-дигидроксиламиндихлорплатина (II), Х = NH2OCl, при этом m : n = 1 : (0,02 - 0,20 ). Соединение обеспечивает повышение противовирусной и интерферон-индуцирующей активности, не является токсичным, а также обладает высокой стабильностью, что делает возможным применение его в клинических условиях. 3 ил., 4 табл.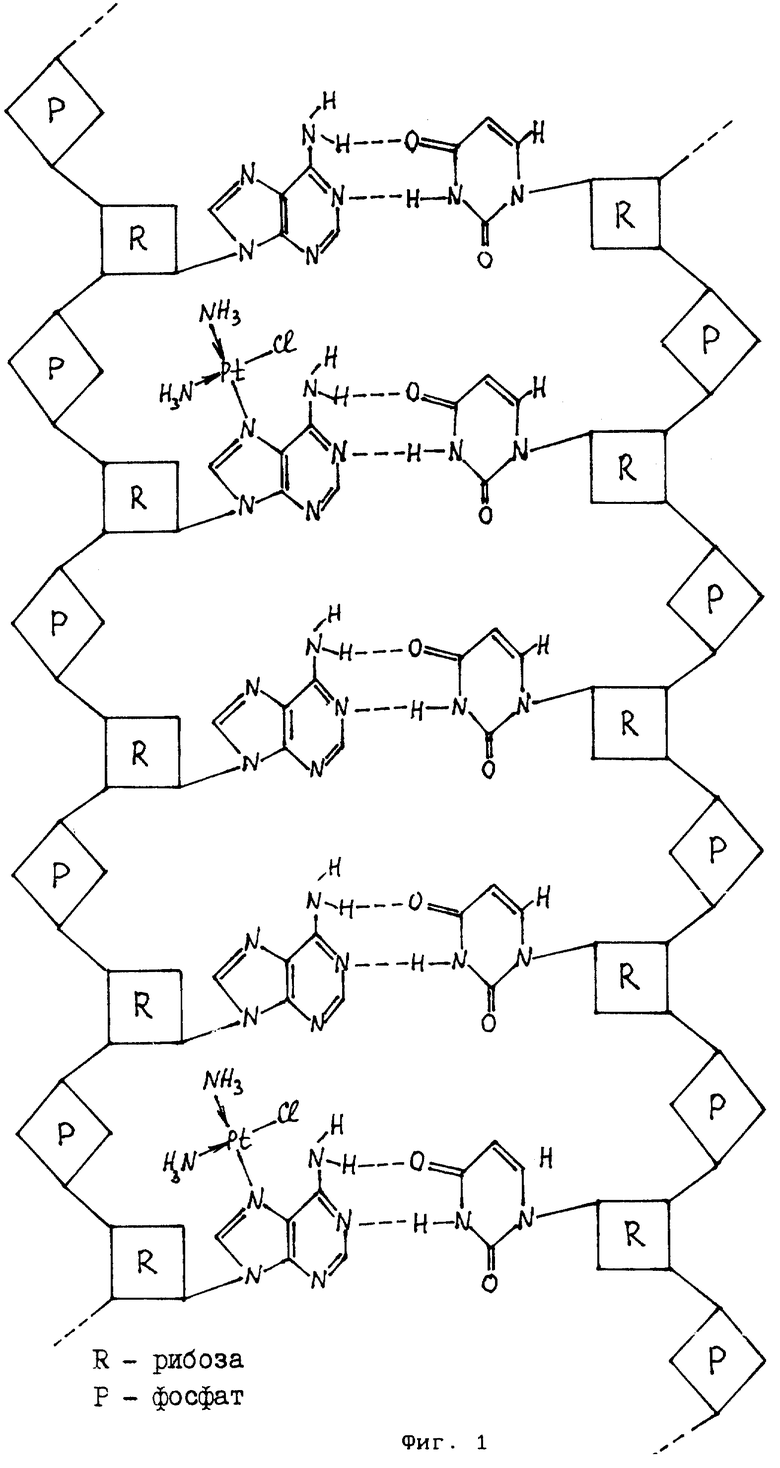
Полирибонуклеотидный дуплекс на основе полирибоаденилата и полирибоуридилата, отличающийся тем, что в него дополнительно введено соединение двухвалентной пластины в виде или цис-диамминдихлорплатины (II), или цис-дигидроксиламиндихлорплатины (II), причем комплекс полирибонуклеотидного дуплекса имеет формулу
[поли(А)·поли(У)]m·[Pt(II)Х2]n,
где Pt(II)Х2 - или цис-диамминдихлорплатина (II), Х = NН3Cl, или цис-дигидроксиламиндихлорплатина (II), Х = NН2ОСl, при этом m:n = 1:(0,02 - 0,20).
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ размножения копий рисунков, текста и т.п. | 1921 |
|
SU89A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ термоактивации двунитевых полирибонуклеотидных комплексов | 1978 |
|
SU713871A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Entrez-PubMed: PMID 444486, U1 79187869 (09.06.2000) | |||
| BARTON, J.K | |||
| et al | |||
| Cooperative binding of a platinum metallointercalation reagent to poly(A)·poly(U) | |||
| Biochemistry | |||
| Дверной замок, автоматически запирающийся на ригель, удерживаемый в крайних своих положениях помощью серии парных, симметрично расположенных цугальт | 1914 |
|
SU1979A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Entrez-PubMed: PMID 3908619, U1 86088004 (28.06.2000) | |||
| LACOUR, J | |||
| Clinical trials using polyadenylic-polyuridylic acid as an adjuvant to surgery in treating different human tumors | |||
| J | |||
| Biol | |||
| Response Mod | |||
| Приспособление для установки двигателя в топках с получающими возвратно-поступательное перемещение колосниками | 1917 |
|
SU1985A1 |
Авторы
Даты
2001-04-27—Публикация
1997-04-23—Подача