Изобретение относится к области биотехнологии и ветеринарии, а именно к созданию биопрепарата, обладающего широким спектром антибактериальной и фаголитической активности, а также способного повысить иммунный статус организма животных и птицы и восстановить их нормальную микрофлору.
Известны пробиотические препараты СБА, СТФ-1/56, предназначенные для восстановления кишечного биоценоза за счет антагонистических свойств штаммов бактерий-пробионтов (Антипов В.А., Ермакова Т.Н., Кошелева Е.К., Бадалян К. М. "Применение СБА в качестве ростимулирующего средства//Всесоюзн. Конф. "Микроорганизмы - стимуляторы и ингибиторы раст. и животных" 3 - 5 окт.1989: Тез. докл. ч.1, Ташкент, 1989, стр. 14; Мишурнова В.Н., Киржаев Ф.С., Антагонистические свойства препарата СТФ-1/56 относительно сальмонелл и кишечной палочки//Ветеринария, 1988, 10, с.34- 36).
Механизм действия пробиотиков основан на адгезивных и антагонистических свойствах бактерий-пробионтов, вытесняющих из состава кишечной популяции условно-патогенные микроорганизмы и неспецифически контролирующих избыточность их роста.
Однако известные пробиотические препараты имеют ограниченный спектр действия и обладают слабой антагонистической активностью по отношению к стафилококкам и практически не угнетают рост синегнойных бактерий (Антипов А.В. , Прозоровская К.Н., Иванина Е.К. и др.//Проблемы стафилококковых инфекций". Саратов, 1986, ч.1. с.9 - 10).
Вместе с тем известно, что кишечные дисбактериозы сопровождаются общим снижением естественной резистентности организма и зачастую осложняются инфекциями, вызванными стафилококками, псевдомонадами и энтеропатогенными бактериями (Блохина И.Н., Дорофейчук В.Г. Дисбактериозы. М., 1979; Коршунов В. М., Пинегин Б.В., Володин Н.Н. и др. - Изучение микрофлоры кишечника при формировании постлучевых и химиотерапевтических дисбактериозов. // В сб. "Теоретические и практические проблемы гнотобиологии", М., 1986, с. 190).
Избыточное присутствие в кишечном биоценозе представителей этих групп микроорганизмов затрудняет процесс профилактики и лечения желудочно-кишечных заболеваний и снижает эффективность применения пробиотиков.
Известны лечебные препараты бактериофагов, используемые для санации желудочно-кишечного тракта от стафилококков и синегнойной палочки (В кн.: Справочник практикующего врача.// Вельтищев Ю.И., Комаров Ф.И., Навашин С.М. и др. Под ред. А.И.Воробева. - 7-е изд. -М.: "Издательский дом ОНИКС", 1998; Актуальные вопросы бактериофагии и прикладной иммунологии. - Тбилиси, 1984, с. 168-266; Г.Г.Боговазова, Н.Н.Ворошилова, В.М.Бондаренко и др. - Иммунобиологические свойства и терапевтическая эффективность препаратов бактериофагов клебсиелл. // ЖМЭИ, 1992. N 3, с.31-33).
Однако известные препараты бактериофагов не обладают достаточно широким спектром литической активности. Возможность появления в популяции патогенных микроорганизмов фагорезистентных форм составляет величину порядка 10(-7) - 10(-8) и снижает эффективность фаготерапии.
Наиболее близким аналогом является биопрепарат "Стрептобифид", в состав которого входит сухая бакмасса бифидобактерий штамма Bifidobacterium globosum ВГНКИ N БФ-4/ДЕП, сухая бакмасса стрептококков штамма Streptococcus faecium ВГНКИ N 27/11-В-ДЕП, углевод, окись алюминия, гидроокись алюминия и наполнитель (RU N 2086248, A 61 K 35/74, опубл. 10.08.97).
Недостатком препарата "Стрептобифид" является невысокая эффективность по отношению к стафилококкам и синегнойным бактериям.
Задачей изобретения является создание высокоэффективного средства с широким спектром действия для лечения и профилактики дисбактериозов и кишечных дисфункций организма животных и сельскохозяйственной птицы.
Технический результат изобретения заключается в получении комплексного пробиотического и бактериофагового препарата, позволяющем сократить сроки лечения, получить более стойкий и выраженный лечебно-профилактический эффект, способного повышать иммунный статус организма животных и сельскохозяйственной птицы и устойчивого к действию ферментов желудочно-кишечного тракта.
Препарат содержит комбинацию полирецепторных вирулентных стафилококковых и псеводомонадных бактериофагов, имеющих различные рецепторы на бактерийной поверхности, снижающие частоту появления резистентных форм микроорганизмов с широким спектром литического действия, и бактерий-пробионтов, способных коррегировать кишечный биоценоз за счет антагонистических и колонизационных свойств используемых штаммов.
Сущность изобретения. Пробиотический препарат содержит сухую бакмассу бифидобактерий, сухую бакмассу стрептококков, сухую культуру стафилококковых бактериофагов штаммов ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП и ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП, углеводы, окись алюминия, гидроокись алюминия и наполнитель, при следующем соотношении компонентов, г/кг препарата:
Сухая бакмасса бифидобактерий с содержанием 10-3000 млрд. микробных клеток (м.к.) в 1 г - 2,04 - 4,0
Сухая бакмасса стрептококков с содержанием 10-3000 млрд. м.к. в 1 г - 2,0 - 4,0
Сухая культура стафилококковых бактериофагов штаммов ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП и ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП с активностью 10(-9) - 10(-12) БОЕ/г - 0,5 - 2,0
Углевод - 20-40
Окись алюминия - 30-60
Гидроокись алюминия - 100-300
Наполнитель - Остальное
Из углеводов препарат может содержать лактозу и/или сахарозу, а из наполнителей - крахмал, сухое молоко, сухую сыворотку молока, заменитель цельного молока, сахарную пудру или пищевой сахар.
Препарат может также дополнительно содержать в различных комбинациях сухую бакмассу ацидофильных бактерий с содержанием 10-3000 млрд. м.к. в 1 г и/или сухую культуру бактериофагов псевдомонадных штаммов ВГНКИ N 86/ЦМЭИ-А1-ДЕП, ВГНКИ N 87/ЦМЭИ-В2-ДЕП, ВГНКИ N 88/ЦМЭИ-С1-ДЕП с активностью каждого штамма 10(-9) - 10(-12) БОЕ/г.
В составе препарата могут быть использованы любые штаммы бифидобактерий, стрептококков и молочнокислых бактерий, характеризующиеся высокой адгезивной способностью и антагонистической активностью. В частности, могут быть использованы известные штаммы Bifidobacterium globosum ВГНКИ N БФ-4-ДЕП, Streptococcus faecium ВГНКИ N 27/11-В-ДЕП и штамм ацидофильных бактерий Lactobacillus acidophilus N A-105-ДЕП/ВГНКИ.
Входящие в состав препарата штаммы бифидобактерий и стрептококков обладают адгезивной и антагонистической активностью по отношению к условно-патогенной микрофлоре, принимают участие в процессах кишечного микробного пищеварения, вырабатывают ферменты, кислоты и другие биологически активные вещества.
Высоковирулентные полирецепиторные бактериофаги, включенные в состав препарата, являются новыми штаммами и получены из различных источников на животноводческих фермах (навоз, сточные воды, смывы с оборудования, содержимое кишечника, гнойные наружные и внутренние очаги).
Штаммы синегнойных и стафилококковых бактериофагов депонированы в коллекции микроорганизмов ВГНКИ под следующими номерами: штаммы синегнойных фагов N 86/ЦМЭИ-А1-ДЕП, N 87/ЦМЭИ-В2-ДЕП, N 88/ЦМЭИ-С1-ДЕП, штаммы стафилококковых бактериофагов под номерами N 89/ЦМЭИ-FS-1-ДЕП, N 90/ЦМЭИ-BS-2-ДЕП.
Штаммы бактериофагов имеют широкий спектр литической активности против большого круга возбудителей стафилококкозов и псевдомонозов животных. Основные методы, используемые при исследовании свойств выделенных бактериальных вирусов, описаны в монографии Адамса (Адамс М. Бактериофаги, М., Мир, 1961).
Штаммы бактериофагов синегнойной палочки ВГНКИ N 86/ЦМЭИ-А1-ДЕП, ВГНКИ N 87/ЦМЭИ-В2-ДЕП и ВГНКИ N 88/ЦМЭИ-С1-ДЕП характеризуются следующими свойствами:
Морфология и размеры фаговых частиц. Данные электронной микроскопии. Штамм фага ВГНКИ N 86/ЦМЭИ-А1-ДЕП имеет изометрическую головку диаметром 62 нм и сокращающийся хвостовой отросток (145 х 20 нм). Аппарат адсорбции фага - базальная пластинка и 6 (шесть) хвостовых фибрилл. Длина фибрилл - 50 нм.
Штамм фага состоит из удлиненной головки (92 х 58 нм) и несокращающегося хвостового отростка (170 х 12 нм). Аппарат адсорбции фага включает органеллы двух типов. Боковыми органеллами адсорбции фага закрепляются на пилях (фимбриях) синегнойной палочки. Кроме того, на конце хвостового отростка фага различимы три терминальные фибриллы (12-13 нм). С помощью этих фибрилл фаг взаимодействует с внешней мембраной P. aeruginosa после транслокации фага посредством пили к клеточной поверхности.
Штамм фага ВГНКИ N 88/ЦМЭИ-С1-ДЕП состоит из головки изометрической формы (64 нм) и короткого несокращающегося хвостового отростка длиной 10-11 нм. Какие-либо дополнительные структурные элементы у фага N 88/ЦМЭИ-С1-ДЕП не обнаружены.
Все три штамма бактериофагов содержат ДНК.
Штамм фага ВГНКИ N 86/ЦМЭИ-А1-ДЕП, штамм фага ВГНКИ N 87/ЦМЭИ-В2-ДЕП и штамм фага N 88/ЦМЭИ-С1-ДЕП - вирулентные бактериальные вирусы. Штаммы P. aeruginosa, лизогенные по этим фагам, не выявлены.
Литические свойства фагов. Для оценки литических спектров бактериальных вирусов были использованы две коллекции штаммов синегнойной палочки. Одна коллекция включала 40 изолятов синегнойной палочки, выделенных от маститных коров в различных регионах Российской Федерации. Вторая коллекция включала 28 изолятов синегнойной палочки, выделенных из почвенных и навозных образцов Челябинской области.
Штамм бактериофага ВГНКИ N 86/ЦМЭИ-А1-ДЕП лизирует 48 штаммов синегнойной палочки из 68.
Спектр хозяев фага ВГНКИ N 87/ЦМЭИ-В2-ДЕП - 47 культур P. aeruginosa.
Фаг ВГНКИ N 88/ЦМЭИ-С1-ДЕП активен по отношению к 43 штаммам из той же выборки (68 изолятов).
Комбинированный препарат из трех фагов лизирует все 68 культур синегнойной палочки.
Биологические свойства фагов представлены в табл. 1. В качестве клетки-хозяина использован штамм P. aeruginosa РАО1.
Физико-химические свойства фагов. Все три фага сохраняют литическую активность в растворах с pH от 4 до 10,5.
Инкубация суспензии фага ВГНКИ N 87/ЦМЭИ-В2-ДЕП при 60oC в течение 30 мин приводит к уменьшению титра фага на 2 lg. Фаг ВГНКИ N 86/ЦМЭИ-А1-ДЕП более устойчив к такой обработке (понижение концентрации на 1 lg). Литические свойства фага ВГНКИ N 88/ЦМЭИ-С1-ДЕН не изменяются при нагревании образца до 60oC.
Однократное замораживание-оттаивание практически не отражается на биологических свойствах фагов.
При хранении на холоду (4-8oC) препараты фагов не теряют литической активности в течение года. Штаммы стафилококковых бактериофагов ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП и ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП характеризуются следующими свойствами:
Морфология и размеры фаговых частиц. Данные электронной микроскопии. Штамм стафилококкового бактериофага ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП состоит из икосаэдрической головки диаметром 85 нм и сокращающегося хвостового отростка длиной 200 нм и шириной 15 нм. После сокращения чехол отростка имеет длину 100 нм и ширину 20 нм. Аппарат адсорбции фага - базальная пластинка с фимбриями. Базальная пластинка имеет диаметр 45-50 нм.
Штамм стафилококкового бактериофага ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП состоит из икосаэдрической головки диаметром 50 нм и длинного несокращающегося хвостового отростка длиной 240 нм.
Другие морфологические детали не исследованы. Литические свойства фагов. Для оценки литических свойств фагов была использована коллекция ВГНКИ из 117 коагулазоположительных патогенных штаммов Staphylococcus aureus, выделенных от больных маститами коров, из гнойного содержимого наружных ран, фекального содержимого в различных животноводческих хозяйствах Московской области, от домашних животных и птицы в Челябинской области, республике Удмуртия, Кировской области.
Штамм стафилококкового бактериофага ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП лизирует 102 штамма из этой коллекции.
Штамм фага ВГНКИ N 90/ЦМЭИ-В8-2-ДЕП лизирует 97 штаммов из этой коллекции.
Комбинация из двух этих фагов лизирует все 117 штаммов стафилококков.
Биологические свойства фагов. Штамм стафилококкового бактериофага ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП имеет латентный период инфекционного процесса 25-30 мин. Урожайность - 60 частиц на одну клетку.
При воспроизведении штамма стафилококкового бактериофага ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП в клетках-хозяевах латентный период составляет 40-45 минут, урожайность - 40-45 частиц на одну клетку. Физико-химические свойства фагов. Оба фага сохраняют литическую активность в растворах с pH от 4,2 до 9,7.
Инкубация суспензии штамма фага ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП при температуре 60oC в течение 30 мин приводит к уменьшению титра фага на 1 lg. Литические свойства фага ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП не изменяются при нагревании до 60oС в течение 30 мин.
Штамм ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП имеет плавучую плотность 1,47 г/мл. Содержание ГЦ-пар нуклеотидов в двухцепочной линейной ДНК составляет 32%.
Штамм стафилококкового бактериофага ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП имеет плавучую плотность 1,48 г/мл. Содержание ГЦ-пар в двухцепочечной линейной ДНК составляет 35%.
При хранении на холоду (4-10oC) фаги не теряют литической активности в течение 18 месяцев.
Изобретение иллюстрируется следующими примерами.
Пример 1. Препарат "Фагосан", содержащий культуру штамма стрептококка Streptococcus faecium ВГНКИ N 27/11-В-ДЕП (или любую другую культуру штаммов стрептококков, используемых в пробиотических препаратах), культуру штамма Bifidobacterium globosum ВГНКИ N БФ-4-ДЕП (или любую другую культуру бифидобактерий), комбинацию полирецепторных стафилококковых бактериофагов штаммов ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП, ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП готовят следующим образом:
Используемые в составе препарата штаммы микроорганизмов раздельно культивируют на жидких питательных средах, принятых для культивирования бифидобактерий и стрептококков, или на средах на основе ферментативного гидролизата казеина с добавлением дрожжевого автолизата. За время культивирования в течение (16±2) ч достигается выход биомассы каждого вида бактерий не менее 10 млрд. живых микробных клеток в 1 мл культуральной взвеси. Полученные культуры концентрируют в 10-15 раз в зависимости от плотности культуральной взвеси, отмывают от продуктов метаболизма на сепараторах или микрофильтрационных установках. Сконцентрированные бактерийные суспензии высушивают сублимационным способом по общепринятой технологии.
В полученных сухих полуфабрикатах содержится не менее 500 млрд. живых микробных клеток в одном грамме.
Отдельно получают сухие биомассы стафилококковых бактериофагов штаммов ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП и ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП. Для этого предварительно выращивают культуры клеток-хозяев в жидкой среде, инфицируют фагами и культивируют до полного лизиса микроорганизмов. Полученные фаголизаты подвергают очистке. Концентрирование фагов в лизатах определяют титрованием методом агаровых слоев (Адамс, 1961).
Технология получения фагов, номера штаммов клеток-хозяев, способ очистки являются предметом "ноу-хау".
Очищенные культуры фагов высушивают сублимационным способом с достижением активного значения фагов в 1 грамме полученного сухого полуфабриката не менее 10(-9) - 10(-12) БОЕ/г.
Активность каждого бактериофага после лиофилизации определяют согласно "Методическим рекомендациям по использованию стафилококковых бактериофагов для фаготипирования штаммов, выделенных от крупного рогатого скота", утвержденных ГУВ МСХ СССР 16.09.1976 г. на изолятах культур стафилококков, выделенных из гнойных очагов, внутренних органов и кишечного содержимого разного вида животных и на тест-штаммах.
Сухую бакмассу каждого штамма смешивают между собой в соотношении 1:1.
Сухие полуфабрикаты бактериофагов смешивают между собой в соотношении 1: 1.
Далее сухую смесь штаммов смешивают с сухими бактериофагами в соотношении 1: 1, добавляют углевод, окись и гидроокись алюминия и наполнитель (крахмал, сахарная пудра, сухое молоко, заменитель цельного молока) при следующем соотношении компонентов, г/кг:
Сухая бакмасса штамма стрептококка с содержанием 30-1000 млрд. живых микробных клеток/г - 3
Сухая бакмасса штамма бифидобактерий с содержанием 30-1000 млрд. живых микробных клеток/г - 3
Сухая культура бактериофагов стафилококковых ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП, ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП с активностью 10(-9) - 10(-12) БОЕ/г - 1
Углевод (лактоза или сахароза) - 30
Окись алюминия - 50
Гидроокись алюминия - 200
Наполнитель - До 1000
Указанный состав позволяет получать серии препарата с общим значением KOE стрептококков и бифидобактерий (при равном их количественном соотношении) от 180 млн. до 6 млрд. в одном грамме и бактерийных стафилококковых фагов с активностью от 10(-6) до 10(-9) БОЕ в одном грамме.
Пример 2. Берут штаммы бактерий Streptococcus faecium ВГНКИ N 27/11-В-ДЕП, Bifidobacterium globosum ВГНКИ N БФ/4-ДЕП, Lactobacillus acidophilus N А-105-ДЕП/ВГНКИ и штаммы стафилококковых бактериофагов ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП и ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП.
Пробиотический препарат получают путем раздельного глубинного культивирования штаммов бифидобактерий, стрептококков и ацидофильных бактерий на жидких питательных средах, принятых для культивирования этих видов микроорганизмов. Получают сухую бакмассу каждого штамма в отдельности аналогично примеру 1.
Далее сухую бакмассу каждого штамма смешивают в равных соотношениях.
Сухие полуфабрикаты бактериофагов, полученные по примеру 1, смешивают между собой в соотношении 1:1.
Далее сухую смесь штаммов смешивают с сухими бактериофагами в соотношении 1: 1, добавляют углевод, окись и гидроокись алюминия и наполнитель (например, крахмал или сахар пищевой, сахарную пудру), при следующем соотношении компонентов, г/кг:
Сухая бакмасса штамма стрептококка с содержанием 10 - 3000 млрд. живых микробных клеток в 1 г - 2
Сухая бакмасса штамма бифидобактерий с содержанием 10-3000 млрд. живых микробных клеток в 1 г - 2
Сухая бакмасса штамма ацидофильных бактерий с содержанием 30-1000 млрд. живых микробных клеток в 1 г - 2
Сухая культура бактериофагов стафилококковых штаммов ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП, ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП с активностью 10(-9) - 10(-12) БОЕ/г - 1
Углевод (лактоза или сахароза) - 30
Окись алюминия - 50
Гидроокись алюминия - 200
Наполнитель - До 1000
Указанный состав позволяет получать серии препарата с общим значением КОЕ стрептококков, бифидобактерий и ацидофильных бактерий (при равном их количественном соотношении) от 180 млн. до 6 млрд. в одном грамме, бактерийных стафилококковых фагов с активностью от 10(-6) до 10(-9) БОЕ в одном грамме.
Пример 3. Берут штаммы бактерий Streptococcus faecium ВГНКИ N 27/11-В-ДЕП, Bifidobacterium globosum ВГНКИ N БФ/4-ДЕП, Lactobacillus acidophilus N А-105-ДЕН/ВГНКИ, штаммы стафилококковых бактериофагов ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП, ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП и штаммы псевдомонадных бактериофагов ВГНКИ N 86/ЦМЭИ-А1-ДЕП, ВГНКИ N 87/ЦМЭИ-В2-ДЕН, ВГНКИ N 88/ЦМЭИ-С1-ДЕП. Сухие полуфабрикаты используемых штаммов бактерий и бактериофагов готовят аналогично примеру 1 и 2.
Активность полученных сухих полуфабрикатов стафилококковых и псевдомонадных бактериофагов составляет не менее 10(12) БОЕ в одном грамме.
Сухую смесь штаммов бифидобактерий, стрептококков, ацидофильных бактерий смешивают с сухими стафилококковыми и псевдомонадными бактериофагами в соотношении 1: 1 и добавляют углевод, окись и гидроокись алюминия и наполнитель (крахмал, сахарная пудра, сухое молоко, заменитель цельного молока) при следующем соотношении компонентов, г/кг:
Сухая бакмасса штамма стрептококка с содержанием 30-1000 млрд. живых микробных клеток/г - 3
Сухая бакмасса штамма бифидобактерий с содержанием 30-1000 млрд. живых микробных клеток/г - 3
Сухая бакмасса штамма ацидофильных бактерий с содержанием 30-1000 млрд. живых микробных клеток/г - 3
Сухая культура бактериофагов стафилококковых штаммов ВГНКИ N 89/ЦМЭИ-FS-1-ДЕП, ВГНКИ N 90/ЦМЭИ-BS-2-ДЕП с активностью 10(-9) - 10(-12) БОЕ/г - 1
Сухая культура бактериофагов псевдомонадных штаммов ВГНКИ N 86/ЦМЭИ-А1-ДЕП, ВГНКИ N 87/ЦМЭИ-В2-ДЕП, ВГНКИ N 88/ЦМЭИ-С1-ДЕП с активностью 10(-9) - 10(-12) БОЕ/г - 1
Углевод (лактоза или сахароза) - 30
Окись алюминия - 50
Гидроокись алюминия - 200
Наполнитель - До 1000
Указанный состав позволяет получать серии препарата с общим значением КОЕ стрептококков, бифидобактерий и ацидофильных бактерии (при равном их количественном соотношении) от 180 млн. до 6 млрд. в 1 г бактерийных стафилококковых и псевдомонадных фагов (при равной их активности) от 10(-6) до 10(-9) БОЕ в 1 г.
Пример 4. Препарат используют для профилактики и лечения желудочно-кишечных заболеваний смешанной этиологии.
Испытывают профилактическую эффективность серий препарата "Фагосан":
- полученного по примеру 3, с общей концентрацией бактерий в одном грамме 180 млн м.к., активностью фагов 2х10(-6) БОЕ в одном грамме;
- полученного по примеру 3, с общей концентрацией бактерий в одном грамме 600 млн м.к., концентрацией активных фагов 10(-9) БОЕ в одном грамме;
- полученного по примеру 2 с общей концентрацией бактерий в одном грамме 180 млн м.к. и активностью фагов 1•10(-6) БОЕ/г;
- полученного по примеру 1 с общей концентрацией бактерий в одном грамме 180 млн м.к. и активностью фага 1•10(-6) БОЕ/г.
В качестве биологической модели для испытания препарата "Фагосан" используют щенков 3-3,5-месячного возраста из питомника, неблагополучного по стафилококковым инфекциям. При лабораторном исследовании фекалий по общепринятой методике у щенков высевались стафилококки и бактерии группы кишечной палочки в концентрациях, превышающих принятые физиологические нормы, а также синегнойная палочка.
При визуальном осмотре щенки отстают в росте и развитии, аппетит извращенный или отсутствует, при пальпации брюшная стенка напряженная, болезненная, вздутая, дефекация частая, непроизвольная, фекалии жидкие, пузырящиеся, иногда с примесью крови.
Для проведения испытаний формируют 5 групп щенков 3-3,5-месячного возраста.
Первой группе щенков задают перорально с кормом один раз в день в течение 5 дней по 1 г препарата, приготовленного по примеру 1, с концентрацией КОЕ бактерий 180 млн., суммарной активностью бактериофагов 2•10(-6) БОЕ/г.
Второй группе щенков задают аналогично в течение 5 дней по одному грамму препарата, приготовленного по примеру 1, с суммарной концентрацией КОЕ бактерий 600 млн., суммарной активностью бактериофагов 2•10(9) БОЕ/г.
Третьей группе щенков задают аналогично в течение 5 дней по одному грамму препарата, приготовленного по примеру 2, с суммарной концентрацией КОЕ бактерий 180 млн., суммарной активностью стафилококковых бактериофагов 1•10(-6) БОЕ/г.
Четвертой группе щенков задают аналогично в течение 5 дней по 1 г препарата, приготовленного по примеру 1, с суммарной концентрацией КОЕ бактерий 180 млн., активностью стафилококковых бактериофагов 1•10(-6) БОЕ/г.
Пятую группу щенков используют в качестве контрольной и выпаивают им два раза в день по 20 мл коммерческого препарата бактериофага стафилококкового совместно с симптоматической и антибактериальной терапией.
Учитывают эффективность испытуемого препарата через 5 дней после начала лечения путем сравнения клинических результатов, полученных во всех трех группах.
У щенков первой группы начало восстановления деятельности желудочно-кишечного тракта наблюдается на второй-третий день после начала применения препарата. Акт дефекации нормализовался, фекалии без примеси слизи и без ихорозного запаха. Поведенческие реакции щенков активизировались. По окончании дачи препарата к 5 дню его применения поведенческие реакции щенков восстановились полностью, аппетит нормальный. По данным бактериологических исследований значение КОЕ лактобацилл у щенков этой группы составляет lg 6,5+0,8. 3начение КОЕ стафилококков снижается до границ физиологической нормы и составляет lg 3,2+0,2. У трех из 6 щенков в кишечном биоценозе стафилококки в разведении 10(-3) отсутствуют. Коагулазоположительные стафилококки и синегнойная палочка отсутствуют у всех щенков этой группы.
У щенков второй группы деятельность желудочно-кишечного тракта полностью восстановлена к 3-5 дню дачи препарата. По данным бактериологических исследований значение КОЕ стафилококков щенков этой группы составляет lg 2,4+0,3. Коагулазоположительные стафилококки и синегнойная палочка отсутствуют. Значение КОЕ лактобацилл в кишечном содержимом составляет lg 7,9+0,6, бактерий группы кишечной палочки lg 8,9+0,3, что соответствует границам физиологической нормы. У щенков третьей и четвертой опытных групп кишечный биоценоз восстановлен к 4-7 дню после начала дачи препаратов.
У щенков обеих опытных групп по окончании дачи испытуемого препарата в содержимом желудочно-кишечного тракта в разведении 10(-2) отсутствуют стафилококки и синегнойная палочка.
У щенков контрольной группы, получавших коммерческий препарат бактериофагов, антибактериальную и симптоматическую терапию, восстановление деятельности желудочно-кишечного тракта наблюдается через 12-14 дней после начала лечения. При этом акт дефекации полностью не восстановлен. При бактериологическом исследовании содержимого желудочно-кишечного тракта значение КОЕ лактобацилл у щенков этой группы на 14 день лечения составляет lg 5,8+0,2, что значительно ниже границ физиологической нормы. Значение КОЕ стафилококов составляет lg 4,5+0,7. У 2 из 5 щенков этой группы высеваются коагулазоположительные стафилококки и синегнойная палочка. Количество бактерий группы кишечной палочки составляет lg 9,4+0,7.
Применение препаратов способствует восстановлению кишечного биоценоза, санации кишечника от стафилококков и синегнойной палочки, от избыточной колонизации бактериями группы кишечной палочки и стимулирует рост и развитие щенков.
Пример 5. Проводят испытание эффективности препарата "Фагосан" для профилактики желудочно-кишечных заболеваний у поросят-сосунов под лактирующими свиноматками с синдромом мастит-метрит-агалактия (ММА).
Для проведения испытаний формируют 6 групп подсосных свиноматок с диагнозом ММА с примерно равным количеством поросят под лактирующей свиноматкой.
В первой группе задают препарат, приготовленный по примеру 3, с общей концентрацией бактерий 180 млн. м.к., суммарной концентрацией фагов 2•10(-6) БОЕ/г, свиноматкам перорально индивидуально один раз день в течение 5 дней по 2 г препарата, предварительно разведенного кипяченой теплой водой.
Второй группе свиноматок задают перорально индивидуально один раз в день в течение 5 дней по 2 г препарата, приготовленного по примеру 3, с общей концентрацией КОЕ бактерий-пробионтов 600 млн., суммарной активностью бактериофагов 2•10(-9) БОЕ/г, предварительно разведенного теплой кипяченой водой.
Третью группу свиноматок используют как контрольную и для профилактики желудочно-кишечных заболеваний у подсосных поросят проводят их однократную обработку антибиотиками.
В четвертой группе препарат, изготовленный по примеру 3, с общей концентрацией бактерий 180 млн. м.к., суммарной активностью фагов 2•10(-6) БОЕ/г, задают подсосным поросятам, начиная с 3-дневного возраста, индивидуально, перорально один раз в день в течение 5 дней по 0,5 г на голову, предварительно разводят препарат теплой кипяченой водой.
В пятой группе препарат, изготовленный по примеру 3, с общей концентрацией бактерий 600 млн. м.к., суммарной активностью фагов 2 • 10(-9) БОЕ/г, задают подсосным поросятам, начиная с 3-дневного возраста, в течение 5 дней индивидуально, перорально по 0,5 г на голову, предварительно разводят препарат теплой кипяченой водой.
Поросят в 6-й группе используют в качестве контроля и для профилактики желудочно-кишечных заболеваний проводят однократную обработку антибиотиками.
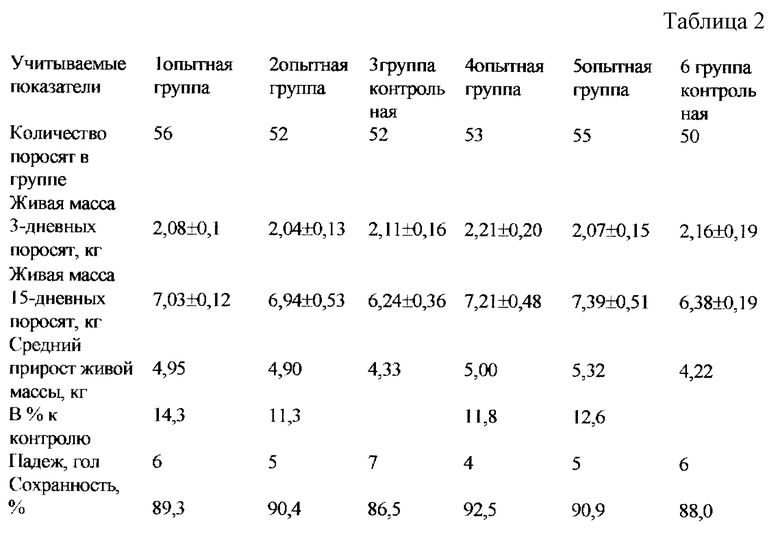
Учет показателей проводят через 12 дней после окончания дачи препаратов по общей сохранности и приросту живой массы поросят.
Полученные результаты представлены в таблице 2.
Полученные данные показывают, что применение препарата "Фагосан" супоросным свиноматкам с синдромом мастит-метрит-агалактия способствует повышению сохранности подсосных поросят. Применение препарата подсосным поросятам под лактирующими свиноматками с синдромом маститт-метрит-агалактия повышает естественную резистентность поросят и способствует увеличению их сохранности.
Таким образом, препарат обладает профилактической и лечебной эффективностью при кишечных дисбактериозах, способствует санации кишечника животных от стафилококков и синегнойной палочки, снижает количество энтеробактерий группы кишечной палочки и повышает естественную резистентность организма животных.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОБИОТИЧЕСКИЙ ПРЕПАРАТ ВЕТЕРИНАРНОГО НАЗНАЧЕНИЯ | 1999 |
|
RU2166323C2 |
| БИОПРЕПАРАТ ДЛЯ ПОВЫШЕНИЯ ПРОДУКТИВНОСТИ ПЧЕЛ | 1999 |
|
RU2166322C2 |
| ПРОБИОТИЧЕСКИЙ ПРЕПАРАТ "СТРЕПТОБИФИД" ДЛЯ ЖИВОТНЫХ | 1996 |
|
RU2086248C1 |
| ШТАММ БАКТЕРИЙ Lactobacillus casei/paracasei - ВГНКИ 10.02.62 ДЕП, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРИГОТОВЛЕНИЯ ПРОБИОТИЧЕСКОЙ ДОБАВКИ | 2010 |
|
RU2465322C2 |
| БИОПРЕПАРАТ НА ОСНОВЕ БАКТЕРИОФАГОВ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ САЛЬМОНЕЛЛЕЗА ЖИВОТНЫХ | 2002 |
|
RU2232808C1 |
| БИОПРЕПАРАТ НА ОСНОВЕ БАКТЕРИОФАГОВ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ КОЛИБАКТЕРИОЗА (ЭШЕРИХИОЗА) ЖИВОТНЫХ | 2002 |
|
RU2244747C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПИОБАКТЕРИОФАГА | 1992 |
|
RU2036232C1 |
| СРЕДСТВО АНТИБАКТЕРИАЛЬНОЕ ИЗБИРАТЕЛЬНОГО ДЕЙСТВИЯ НА ОСНОВЕ БАКТЕРИОФАГОВ | 2008 |
|
RU2366436C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИБАКТЕРИОФАГА | 2002 |
|
RU2247151C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ПАРОДОНТА БАКТЕРИОФАГАМИ | 2000 |
|
RU2165766C1 |

Изобретение предназначено для биотехнологии и ветеринарии. Препарат содержит бактерии Bifidobacterium globosum ВГНКИ БФ-4-ДЕП, штамм Streptococcus faecium ВГНКИ 27/11-В-ДЕП и комбинацию вирулентных полирецепторных стафилококковых бактериофагов. Препарат содержит также окись алюминия, гидроокись алюминия, углевод и наполнитель. Из штаммов стафилококковых бактериофагов он содержит штаммы ВГНКИ 89/ЦМЭИ-FS-1-ДЕП и ВГНКИ 90/ЦМЭИ-ВS-2-ДЕП. Из углеводов препарат может содержать лактозу и/или сахарозу, а из наполнителей - крахмал, сухое молоко, сухую сыворотку молока, заменитель цельного молока, сахарную пудру или пищевой сахар. Препарат может также дополнительно содержать в различных комбинациях сухую бакмассу ацидофильных бактерий и/или сухую культуру бактериофагов псевдомонадных штаммов ВГНКИ 86/ЦМЭИ-А1-ДЕП, ВГНКИ 87-ЦМЭИ-В2-ДЕП, ВГНКИ 88/ЦМЭИ-С1-ДЕП. Препарат обладает одновременно профилактической и лечебной эффективностью при кишечных дисбактериозах, способствует санации кишечника животных от стафилококков и синегнойной палочки, обладает широким спектром антибактериальной и фаголитической активности и повышает иммунный статус организма животных. 5 з.п. ф-лы, 2 табл.
Сухая бакмасса бифидобактерий с содержанием 10 - 3000 млрд.м.к. в 1 г - 2,0 - 4,0
Сухая бакмасса стрептококков с содержанием 10 - 3000 млрд.м.к. в 1 г - 2,0 - 4,0
Сухая культура стафилококковых бактериофагов штаммов ВГНКИ 89/ЦМЭИ-FS-1-ДЕП и ВГНКИ 90/ЦМЭИ-BS-2-ДЕП с активностью 10(-9) - 10(-12) БОЕ-г - 0,5 - 2,0
Углевод - 20 - 40
Окись алюминия - 30 - 60
Гидроокись алюминия - 100 - 300
Наполнитель - Остальное
2. Препарат по п.1, отличающийся тем, что из бифидобактерий он содержит штамм Bifidobacterium globosum ВГНКИ БФ-4/ДЕП, из стрептококков - штамм Streptococcus faecium ВГНКИ 27/11-В-ДЕП.
Авторы
Даты
2001-05-10—Публикация
1999-06-21—Подача