Изобретение относится к химическим препаратам, в частности к комплексной соли металлов, которая может быть использована в фармацевтической промышленности при изготовлении средства для лечения повышенной желудочной кислотности.
Уже известно, что ряд карбонатов алюминия магния используют как антацидные средства в терапии. В качестве примеров карбонатов алюминия магния могут быть использованы карбонаты, полученные в соответствии с Патентами США NN 3539306 и 3650704 (гидротальцит [TalcidTM (ТальцидTM)] формулы Al2Mg6(OH)16CO3 • 4H2O, Патентами США NN 4447417 и 4560545 (альмагейт [ALmaxTM (АльмаксTM) и AlmaxTM Forte (АльмаксTM форте)] формулы Al2Mg6(OH)14(CO3)2 • 4H2O и Патентом США N 4539195 (соединение формулы Al2Mg6(ОН)12(CO3)3 • H2O).
Однако существует необходимость в создании новых антацидов, которые обладали бы повышенной гастропротекторной активностью.
Данное изобретение касается нового основного карбоната алюминия магния формулы Al2Mg4(OH)12CO3 • 3H2O (1), характеризующегося ромбоэдной кристаллизацией, параметры кристаллической решетки которого составляют a=b=3,046 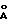 ; c = 22,79
; c = 22,79 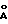 ; α = β = 90o, γ = 120o и объем ячейки = 183
; α = β = 90o, γ = 120o и объем ячейки = 183 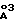 , спектр дифракции рентгеновских лучей которого имеет следующие значения d
, спектр дифракции рентгеновских лучей которого имеет следующие значения d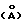 : 7,597; 3,798; 2,6202; 2,5698; 2,5322; 2,2830; 1,93545; 1,72447; 1,62930; 1,52289; 1,49318; 1,46002; 1,41351; 1,38528 и 1,31011, инфракрасный спектр которого дает характеристические полосы при 1361, 785 и 449 см-1 (фигура 1) и охарактеризованный также DSC-термограммой, полученной методом DSC (дифференциальной сканирующей калориметрии). Дифференциальная сканирующая калориметрия, проводимая при скорости нагревания 10,00oC мин-1, дает экстраполируемый пик при 239,56oC, величина пика 4,59 мВт, и пик при 237,92oC.
: 7,597; 3,798; 2,6202; 2,5698; 2,5322; 2,2830; 1,93545; 1,72447; 1,62930; 1,52289; 1,49318; 1,46002; 1,41351; 1,38528 и 1,31011, инфракрасный спектр которого дает характеристические полосы при 1361, 785 и 449 см-1 (фигура 1) и охарактеризованный также DSC-термограммой, полученной методом DSC (дифференциальной сканирующей калориметрии). Дифференциальная сканирующая калориметрия, проводимая при скорости нагревания 10,00oC мин-1, дает экстраполируемый пик при 239,56oC, величина пика 4,59 мВт, и пик при 237,92oC.
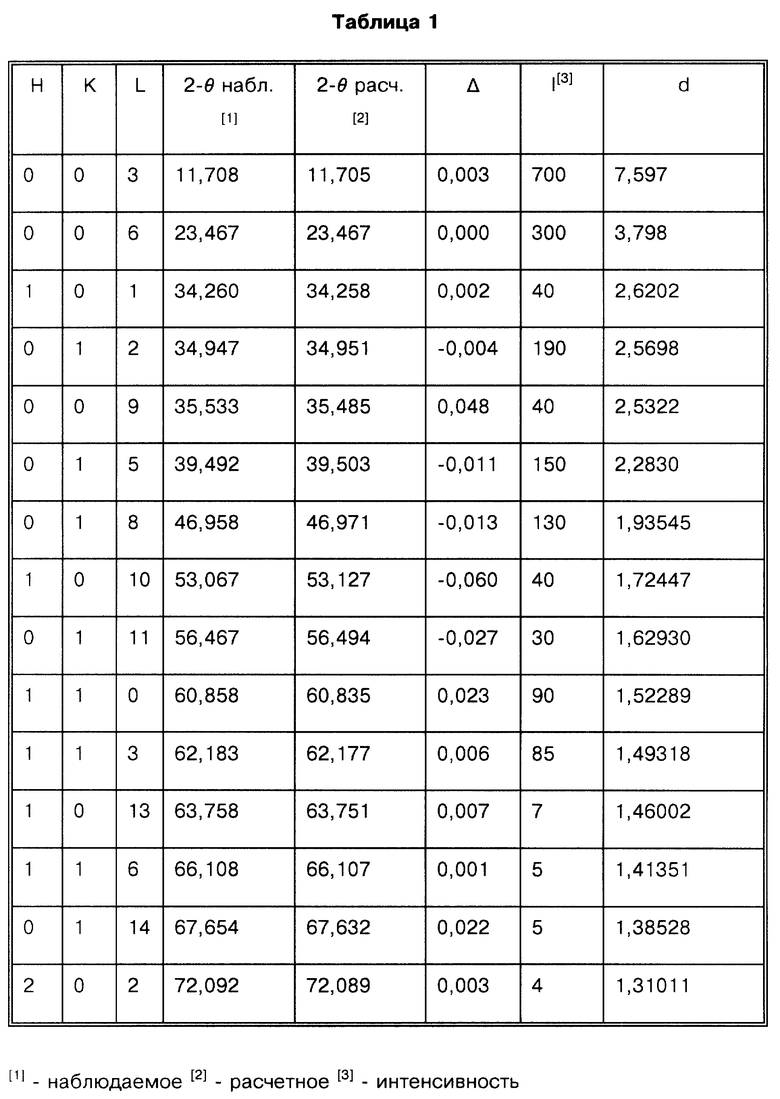
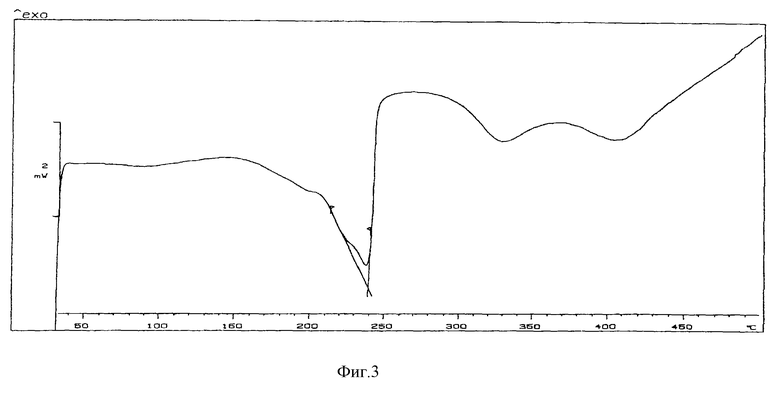
Соединение, соответствующее данному изобретению (1), отличается от соединений, описанных в вышеупомянутых патентах, и не является очевидным, несмотря на сходство их химических формул. В действительности соединение (1) имеет уникальную кристаллическую структуру, что доказано его спектром дифракции рентгеновских лучей (табл. 1). Аналогично DSC-термограмма свидетельствует о наличии уникального соединения правильной структуры (фигура 3). Соединение, соответствующее данному изобретению, обладает антацидными свойствами, а также проявляет полезную гастропротекторную активность, превосходящую активность известных соединений.
Изобретение касается также фармацевтической композиции, содержащей эффективное количество соединения, соответствующего данному изобретению, и фармацевтически приемлемый носитель.
Еще одним аспектом изобретения является способ лечения повышенной желудочной кислотности, который предусматривает введение млекопитающему эффективного количества соединения, соответствующего данному изобретению.
Соединение, соответствующее данному изобретению, получают при реакции гидроксида алюминия с гидроксидом магния и кислым карбонатом натрия в водной среде при температуре кипения смеси. Стехиометрическое соотношение гидроксида алюминия и гидроксида магния должно быть 1:2. Кислый карбонат натрия используют в молярном избытке, таким образом, что средний интервал pH находится между 9 и 11. После охлаждения системы продукт отделяют фильтрованием, промывают водой и высушивают под вакуумом при температуре между 50 и 70oC до того, как по данным взвешивания получают твердое вещество, которое снова суспендируют в воде и нагревают в колбе с обратным холодильником. Твердое вещество отфильтровывают, промывают водой и высушивают под вакуумом при температуре между 50 и 70oC и получают соединение тригидрат гидроксида карбоната алюминия магния (Al2Mg4(OH)12CO3 • 3H2O) (1) в виде ромбоэдных кристаллов. Его параметры кристаллической решетки a=b=3,046 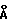 ; c=22,79
; c=22,79  ; α = β = 90o; γ = 120o. Объем кристаллической ячейки = 183
; α = β = 90o; γ = 120o. Объем кристаллической ячейки = 183 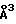 и спектр дифракции рентгеновских лучей имеет следующие значения d
и спектр дифракции рентгеновских лучей имеет следующие значения d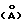 : 7,597; 3,798; 2,6202; 2,5698; 2,5322; 2,2830; 1,93545; 1,72447; 1,62930; 1,52289; 1,49318; 1,46002; 1,41351; 1,38528 и 1,31011 (табл. 1).
: 7,597; 3,798; 2,6202; 2,5698; 2,5322; 2,2830; 1,93545; 1,72447; 1,62930; 1,52289; 1,49318; 1,46002; 1,41351; 1,38528 и 1,31011 (табл. 1).
Объяснение колонок к табл. 1:
H. K.L: Параметры узлов кристаллической решетки соединения (элементарная ячейка), которая позволяет оценить триплет индексов или численные значения (H.K.L.) каждой линии дифракции.
2-θ: Изменения углов, которые показывают угловые положения, в которых линия дифракции (H. K. L.) показана на диаграмме. Если элементарная ячейка соединения и триплет (H. K.L.) известны, теоретическое положение, которое должно соответствовать наблюдаемому, может быть вычислено (obs.: наблюдаемое; cal.: расчетное).
Интенсивность: Она определяет высоту линии дифракции, которая является характеристикой атомных положений в кристаллической ячейке в противоположность угловому положению, которое является характеристикой размера кристаллической ячейки.
d: межатомное расстояние. Оно также характеризует элементарную ячейку соединения и в отличие от 2-θ не зависит от используемой для облучения длины волны.
Ромбоэдная система.
Параметры кристаллической решетки: a= b=3,046 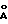 ; с=22,79
; с=22,79  ; α = β = 90o; γ = 120o. Объем кристаллической ячейки = 183
; α = β = 90o; γ = 120o. Объем кристаллической ячейки = 183  .
.
Перечень фигур чертежей и иных материалов.
На фигуре 1 представлен инфракрасный спектр только характерных для соединения полос при 1361, 785 и 449 см-1.
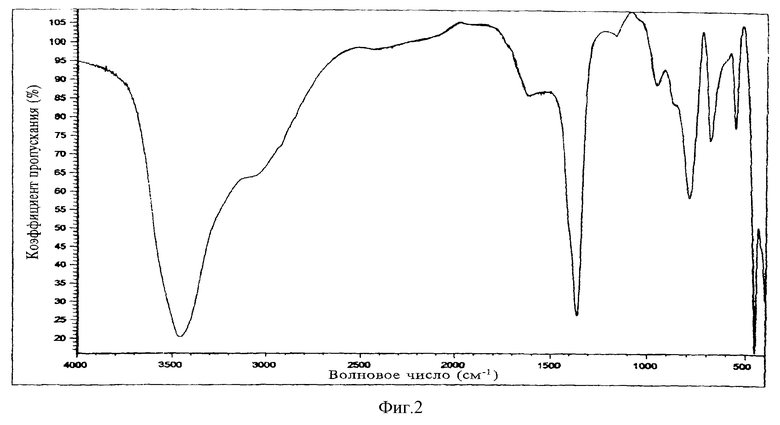
На фигуре 2 представлен полный инфракрасный спектр соединения согласно изобретению, в том числе широкой полосы при 3500-3400 см-1.
На фигуре 3 представлены результаты дифференциальной сканирующей калориметрии (DSC).
Безопасность и эффективность соединения, соответствующего данному изобретению, полученному согласно примеру 1, была продемонстрирована в тесте Ирвина (безопасность) и путем определения его антацидной и гастропротекторной активности (эффективность).
Тест Ирвина: Был использован способ, описанный R.A. Turner (Способы скрининга в фармакологии, 1965, стр. 27-34. Academic press, New York and London). В данном сравнительном тесте соединение, соответствующее примеру 1, и альмагейт перорально вводили мышам Swiss любого пола в дозах 0,3, 1 и 3 г/кг в объеме 30 мл/кг. Ни одна из протестированных доз не индуцировала изменений оцениваемых параметров (психическое состояние и депрессия, рефлексы, двигательная активность, возбуждение центральной нервной системы, мышечный тонус, зрительные симптомы, секреторно-экскреторные признаки, основные признаки, острая летальность и отсроченная летальность) ни в одной группе, и следует подчеркнуть отсутствие изменений в дефекации и летальности. Вследствие этого тест Ирвина показал безопасность соединения, соответствующего Примеру 1, и альмагейта.
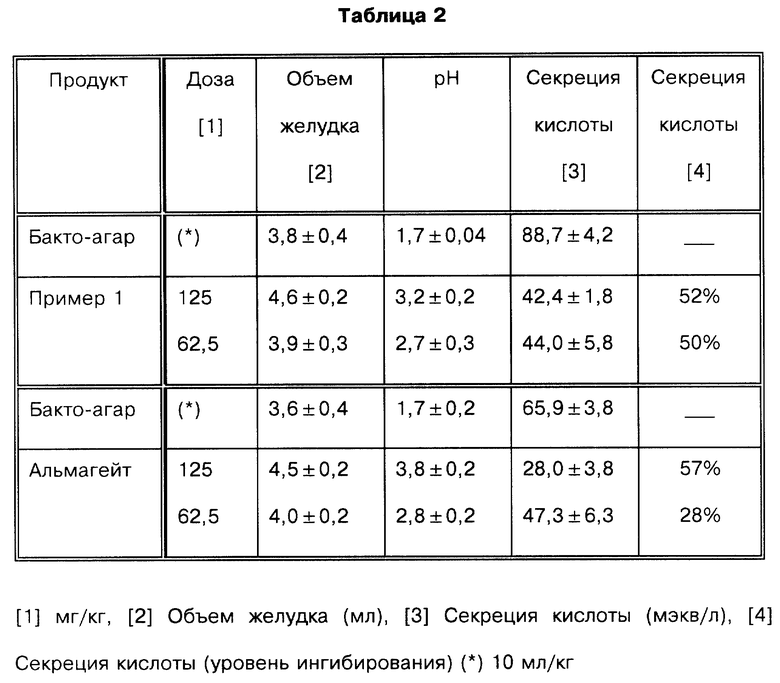
Антацидная активность: Определение антацидной активности проводили на самках крыс Wistar массой 140-160 г. Животных помещали в клетки для изучения метаболизма и не кормили от 24 час до эксперимента до 1 час до начала эксперимента, но воду давали свободно в избыточном количестве. Животным давали наркоз в виде смеси кетолара (91 мг/кг) и тиазина (3,6 мг/кг), а затем проводили лапаротомию; привратник желудка тщательно лигировали и зашивали брюшную полость, используя стерильный шовный материал (Н. Shay и соавт. Gastroenterology, 1954, т. 5, стр. 43-61). Через три часа после наложения лигатуры на привратник животным, находящимся в сознании, перорально вводили тестируемые лекарства. Одна группа из 10 животных получала соединение, соответствующее примеру 1, в 0,25% суспензии Бакто-агара в дозе 125 мг/кг, а другая группа из 10 животных - в дозе 62,5 мг/кг; была использована контрольная группа из 10 животных, получавшая дозу 10 мл/кг 0,25% Бакто-агара. Аналогично эксперимент повторяли с альмагейтом в таких же дозах и с использованием такого же числа животных; новой контрольной группе из 10 животных давали такую же дозу Бакто-агара, как в эксперименте с соединением, соответствующим примеру 1. Через 60 минут после введения животных умерщвляли, собирали содержимое желудка и определяли объем. Образцы центрифугировали при 3000 об/мин в течение 10 минут, супернатант отделяли и определяли pH и концентрацию гидрохлорной (соляной) кислоты в образцах посредством титрования (Titrolab, Radiometer). Полученные результаты представлены в табл. 2.
Из приведенных результатов можно заключить, что хотя доза 125 мг/кг соединения, соответствующего данному изобретению, вызывает нейтрализацию кислоты, близкую уровню действия альмагейта в такой же дозе, при дозе 62,5 мг/кг его активность нейтрализации кислоты превосходит активность альмагейта в такой же дозе.
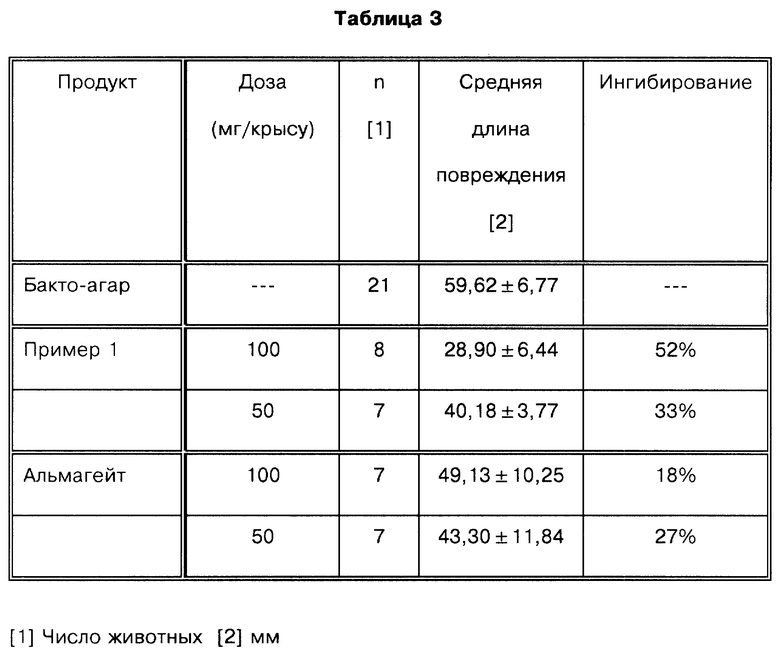
Гастропротекторная активность: Для определения гастропротекторной активности был использован экспериментальный способ индуцированного этанолом некроза желудка, описанный A. Robert и соавт. (Gastroenterology, 1979, т. 77(3), стр 433-443). Эксперимент проводили на самках крыс Spraque-Dawley массой 180-200 г, которых не кормили в течение 24 часов перед началом эксперимента. Соединение, соответствующее данному изобретению, сравнивали с альмагейтом таким же образом, как в предшествующем тесте. Соединение, соответствующее примеру 1, вводили в 0,25% суспензии Бакто-агара. Оба тестируемых продукта вводили перорально в дозах 100 и 50 мг/крысу. Одновременно контрольная группа получала 0,25% Бакто-агар. Через 30 мин животным давали абсолютный этанол в дозе 1 мл/крысу. Через шестьдесят минут после введения этанола животных умерщвляли и измеряли длину повреждений слизистой оболочки желудка. Полученные результаты приведены в табл. 3.
Полученные результаты показывают, что соединение, соответствующее данному изобретению, в качестве гастропротектора слабо превышает действие альмагейта в дозе 50 мг/крысу, но значительно превосходит альмагейт в дозе 100 мг/крысу.
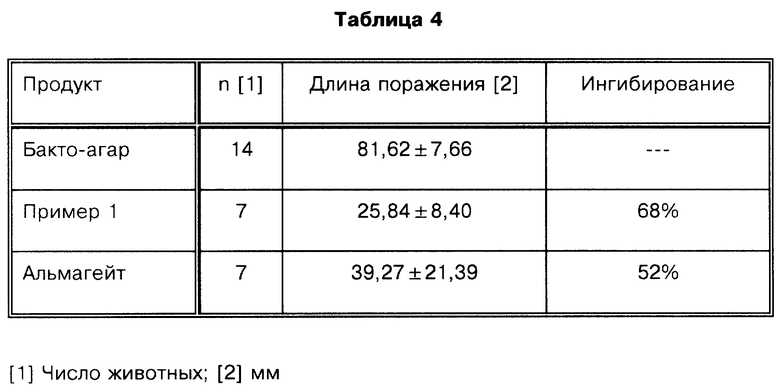
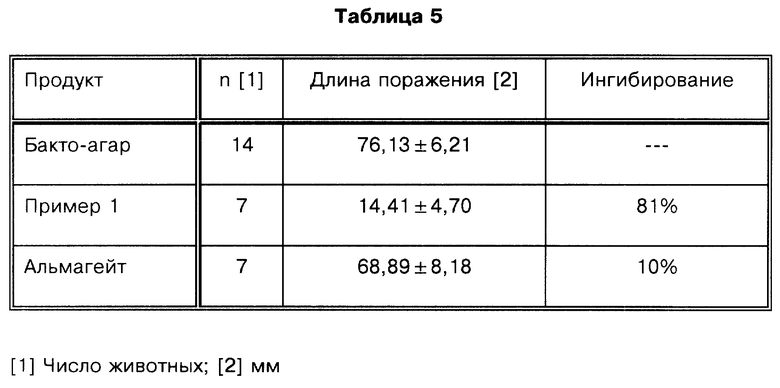
Продолжительность гастропротекторной активности: В данном эксперименте использовали самок крыс Spraque-Dawley массой 180-200 г, которых содержали в таких же условиях, как в предшествующем эксперименте. Соединение, соответствующее данному эксперименту, сравнивали с альмагейтом. Готовили суспензию соединения, соответствующего примеру 1, в 0,25% Бакто-агаре. Тестируемые продукты вводили перорально в однократной дозе 250 мг/крысу за 90 и 180 минут до введения абсолютного этанола в дозе 1 мл/крысу. Через шестьдесят минут после введения этанола животных умерщвляли и измеряли длину повреждений слизистой оболочки желудка. Полученные результаты приведены в табл. 4 (90 минут) и табл. 5 (180 минут).
Результаты показывают, что соединение, соответствующее данному изобретению, имеет полезную и неожиданно большую продолжительность гастропротекторного действия по сравнению с альмагейтом, и эта разница увеличивается за счет активности соединения, соответствующего примеру 1, в течение времени.
На основании фармакологических тестов, которые провели заявители, можно заключить, что соединение, соответствующее данному соединению, характеризуется ингибированием секреции желудочной кислоты, снижая до минимума действие агрессивных факторов на слизистую оболочку желудка и, кроме того, проявляя неожиданное гастропротекторное действие. Гастропротекция, получаемая при использовании соединения, соответствующего данному изобретению, имеет больший потенциал и продолжительность действия, чем альмагейт, что преимущественно выражается в значительно более эффективном улучшении механизмов защиты слизистой оболочки желудка. Наконец, терапевтическим применением соединения, соответствующего данному изобретению, является применение в качестве антацидного средства и гастропротектора, и оно может быть введено при лечении гиперхлогидрии, гастрита, гастродуоденита, диспепсии, эзофагита, дивертикулита, хиатальной грыжи, язвы желудка и двенадцатиперстной кишки, пациентов после операций на желудке, пациентов после ваготомии и в целом для облегчения всех нарушений и эпизодов, вызываемых повышенной желудочной кислотностью. Соединение, соответствующее изобретению, в смеси с подходящими носителями может вводиться перорально в ежедневных дозах, находящихся в интервале от 250 мг до 10 г, предпочтительно между 1 и 6 г в форме суспензий, гранул, таблеток, капсул, порошков, таблеток в оболочке и т.п.
Изобретение иллюстрируется нижеследующими примерами.
Пример 1: Тригидрат гидроксида карбоната алюминия магния (Al2Mg4(OH)12CO3 • 3H2O) (1)
В колбе с круглым дном объемом 1 литр с обратным холодильником нагревают суспензию 9,44 г гидроксида алюминия (что соответствует 5,4 г Al2O3, 53 ммол), 12,37 г Mg(OH)2 (212 ммол) и 34,4 г NaHCO3 (409 ммол) в 400 мл воды в течение 3 часов. После охлаждения нерастворимое вещество отфильтровывают, промывают водой (2 х 300 мл) и высушивают под вакуумом при 60oC в течение 20 часов. Следует использовать воду с pH 10. Полученное твердое вещество снова суспендируют в 400 мл воды, нагревают в колбе с обратным холодильником в течение 24 час, промывают водой и высушивают под вакуумом при 60oC. Выход составляет 90%. ИК- спектр (KBr): 3500-3400 (неспецифическая полоса) (фигура 2), 1361, 785 и 449 см-1 (фигура 1). DSC (дифференциальная сканирующая калориметрия): см. фигуру 3.
Кристаллографический анализ на основе дифракции рентгеновских лучей
Используют дифрактометр Siemens D5000. В ходе эксперимента используют следующие параметры:
Измеряемый интервал - 2-θ: 5-105o
Угловое увеличение - 0,02
Интервал времени - 2,5 с
Облучен λ - 1,54056 
Напряжение - 1,8 кВт
Щель приемника - 0,2o
Щель отклонения - 1o
Полученные значения d также приведены в табл. 1.
также приведены в табл. 1.
Пример 2: Приготовление суспензии тригидрата гидроксида карбоната алюминия магния
Состав на 100 мл суспензии
Тригидрат гидроксида карбоната алюминия магния - 10,00 г
Метил р-гидроксибензоат - 0,16 г
Пропил р-гидроксибензоат - 0,04 г
Метилцеллюлоза 400 cps - 1,03 г
Сорбит 70% - 24,00 г
Сахарина натриевая соль - 0,10 г
Диметикон - 0,20 г
Вкусовая ароматизирующая добавка мяты перечной - 0,05 г
Дистиллированная вода - До 100,00 мл
Данную суспензию можно вносить в контейнеры емкостью 100 мл или пакеты для разового применения емкостью 15 мл, содержащие 1,5 г активного ингредиента.
Пример 3: Приготовление диспергируемого гранулированного препарата тригидрата гидроксида карбоната алюминия магния
Состав на 5 г гранулированного препарата
Тригидрат гидроксида карбоната алюминия магния - 1,50 г
Диметилполисилоксан - 0,20 г
Сорбит, порошок - 1,00 г
Сахарина натриевая соль - 0,01 г
Поливинилпирролидон К-25 - 0,03 г
Бутилгидрокситолуол - 0,0005 г
Вкусовая ароматизирующая добавка лимона - 0,0050 г
Порошок обезжиренного молока - До 5,0000 г
Данный гранулированный препарат помещают в пакеты для разового применения для его диспергирования в воде.
Пример 4: Приготовление жевательных таблеток тригидрата гидроксида карбоната алюминия магния
Состав на таблетку, содержащую 500 мг
Тригидрат гидроксида карбоната алюминия магния - 500 мг
Микрокристаллическая целлюлоза - 120 мг
Поливинилпирролидон - 50 мг
Тальк - 20 мг
Стеарат магния - 10 мг
Вкусовая ароматизирующая добавка мяты - 5 мг
Маннит - До 1200 мг
Данные таблетки могут быть помещены в алюминиевые трубки или блистер, и их растворяют во рту или жуют.
Изобретение касается нового основного карбоната алюминия магния формулы Al2Mg4(ОН)12СО3•3Н2О (I), характеризующегося ромбоэдной кристаллизацией, параметры кристаллической решетки которого составляют a = b = 3,046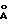 ; с = 22,79
; с = 22,79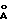 ; α = β = 90o, γ = 120o, и объем ячейки = 183
; α = β = 90o, γ = 120o, и объем ячейки = 183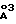 , спектр дифракции рентгеновских лучей которого имеет следующие значения d
, спектр дифракции рентгеновских лучей которого имеет следующие значения d : 7,597; 3,798; 2,6202; 2,5698; 2,5322; 2,2830; 1,93545; 1,72447; 1,62930; 1,52289; 1,49318; 1,46002; 1,41351; 1,38528 и 1,31011, в инфракрасном спектре которого присутствуют характеристические полосы при 1361 и 449 см-1 и охарактеризованный также DSC-термограммой, полученной методом DSC (дифференциальной сканирующей калориметрии), и способа его получения. Данное соединение используют в терапии как антацидное средство и гастропротектор. Изобретение расширяет ассортимент лечебных средств. 4 с. и 2 з.п. ф-лы, 3 ил., 5 табл.
: 7,597; 3,798; 2,6202; 2,5698; 2,5322; 2,2830; 1,93545; 1,72447; 1,62930; 1,52289; 1,49318; 1,46002; 1,41351; 1,38528 и 1,31011, в инфракрасном спектре которого присутствуют характеристические полосы при 1361 и 449 см-1 и охарактеризованный также DSC-термограммой, полученной методом DSC (дифференциальной сканирующей калориметрии), и способа его получения. Данное соединение используют в терапии как антацидное средство и гастропротектор. Изобретение расширяет ассортимент лечебных средств. 4 с. и 2 з.п. ф-лы, 3 ил., 5 табл.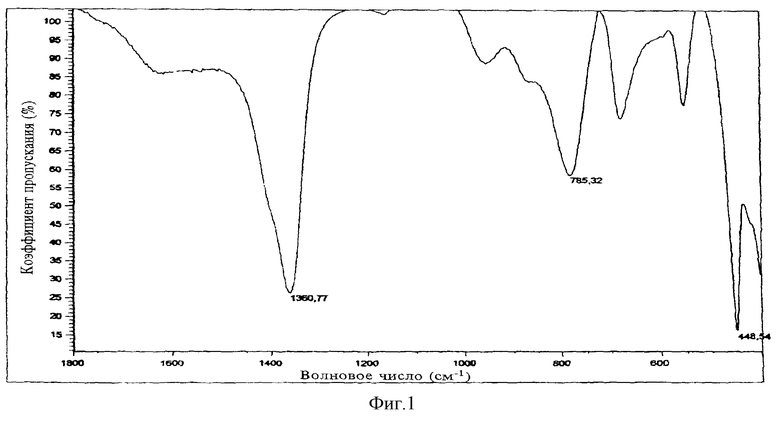
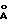 с = 22,79
с = 22,79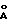 α = β = 90o, γ = 120o и объем ячейки = 183
α = β = 90o, γ = 120o и объем ячейки = 183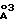 спектр дифракции рентгеновских лучей которого имеет следующие значения d
спектр дифракции рентгеновских лучей которого имеет следующие значения d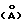 7,597; 3,798; 2,6202; 2,5698; 2,5322; 2,2830; 1,93545; 1,72447; 1,62930; 1,52289; 1,49318; 1,46002; 1,41351; 1,38528 и 1,31011, в инфракрасном спектре которого присутствуют характерные полосы при 1361, 785 и 449 см-1 и охарактеризованный также DSC-термограммой, полученной методом DSC (дифференциальной сканирующей калориметрии).
7,597; 3,798; 2,6202; 2,5698; 2,5322; 2,2830; 1,93545; 1,72447; 1,62930; 1,52289; 1,49318; 1,46002; 1,41351; 1,38528 и 1,31011, в инфракрасном спектре которого присутствуют характерные полосы при 1361, 785 и 449 см-1 и охарактеризованный также DSC-термограммой, полученной методом DSC (дифференциальной сканирующей калориметрии).
| I | |||
| PAUCH, et all ''Synthesic of disordered and Al-rich nydrotalcitelike compounds'' ''CLAYS AND CLAY MINERALS'', v.34, № 5, 1986, р.507 - 510 | |||
| Устройство для подачи смазки на стенку цилиндра | 1957 |
|
SU117289A1 |
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Способ получения алюминатов двухвалентных металлов | 1983 |
|
SU1137079A1 |
| Двойные основные соли щелочно-земельныхМЕТАллОВ и АлюМиНия и СпОСОб иХ пОлучЕНия | 1977 |
|
SU800137A1 |
Авторы
Даты
2001-06-10—Публикация
1998-12-29—Подача