Эта заявка является частично продолжением заявки США N 08/649754, поданной 29 мая 1996, которая является частично продолжающейся заявкой США N 08/463187, поданной 5 июня 1995, которые, таким образом, включены здесь в качестве ссылки.
Настоящее изобретение относится к новым прекрасителям, которые являются бесцветными и проявляют цвет при воздействии определенных длин волн электромагнитного излучения. Настоящее изобретение относится также к способам изменения обычных лейкокрасителей для образования окрашенных композиций при воздействии определенных длин волн электромагнитного излучения.
Хорошо известно, что красители в их восстановленной лейкоформе могут обеспечить основу систем, образующих цветные изображения. Лейкокрасители могут быть первоначально относительно бесцветными, но могут возвращаться в окрашенную форму при окислении, например, нитратными солями при нагреве. Примеры лейкокрасителей, используемых в системах, образующих окрашенные изображения, включают триарилметаны, ксантены, стириловые красители и азиновые красители, такие, как, например, феназины, феноксазины и фенотиазины.
Известно также, что лейкоформа данного красителя может быть нестабильной в условиях окружающей среды и может часто самопроизвольно возвращаться в окрашенную форму красителя. Эта тенденция повышается, когда для достижения интенсификации контраста добавляют фотоокислители, например, тригалогенметилсоединения, которые при экспонировании отщепляют радикалы галогена. Поэтому для композиций лейкокрасителей рекомендован ряд стабилизаторов, например, серусодержащие соединения, фенолы и другие восстановители.
Таким образом, необходим лейкокраситель, который стабилен в растворе даже в присутствии искусственного или солнечного света. Идеальный лейкокраситель можно превратить в стабильные окрашенные молекулы воздействием электромагнитного излучения, которое обычно не может присутствовать в обычном свете. Таким образом, задачей изобретения является создание стабильных лейкопроизводных красителей, которые могут быть трансформированы в стабильную окрашенную молекулу.
Одним осуществлением настоящего изобретения является способ и композиция, содержащая молекулу нового прекрасителя, который является бесцветным и стабильным к действию обычного света. Молекула прекрасителя способна образовать цвет при воздействии определенных длин волн электромагнитного излучения.
Новым прекрасителем настоящего изобретения, в частности, является краситель, который ковалентно присоединен к трансорберу излучения. Получаемая молекула прекрасителя стабильна при обычном свете, но изменчива при воздействии подходящей длины волны электромагнитного излучения. Трансорбер излучения желательно состоит из специфичного для длины волны сенсибилизатора и фотореактора. Когда прекраситель подвергают воздействию подходящей длины волны электромагнитного излучения, молекула прекрасителя изменяется и превращается в стабильную окрашенную форму красителя. В соответствии с этим настоящее изобретение заключает в себя также способ образования цвета воздействием на прекраситель подходящей длины волны ультрафиолетового излучения.
Другим осуществлением настоящего изобретения является обычный лейкокраситель, который смешивают с трансорбером излучения, предпочтительно со средством молекулярного включения. Когда смесь подвергают воздействию подходящей длины волны электромагнитного излучения, лейкокраситель превращается в его окрашенную форму.
Еще одним осуществлением настоящего изобретения является способ превращения обычного лейкокрасителя в окрашенную композицию воздействием на лейкокраситель, смешанный с трансорбером излучения, определенными длинами волн электромагнитного излучения.
Настоящее изобретение можно использовать в способах получения изображений, включая способы получения фотоизображений, системах безопасности, способах печати, способах записи и тому подобное.
Эти и другие задачи, отличительные признаки и преимущества настоящего изобретения станут очевидными после рассмотрения следующего подробного описания раскрытых осуществлений и прилагаемой формулы изобретения.
Настоящее изобретение относится в одном аспекте к прекрасителям, которые изменяются при воздействии излучения с узкой полушириной полосы с образованием окрашенных соединений. Настоящее изобретение, в частности, относится к композиции, прекрасителю, содержащему молекулу красителя, которая ковалентно присоединяется к трансорберу излучения. Когда молекула красителя ковалентно присоединяется к трансорберу излучения, композиция бесцветная. Прекраситель изменяется при воздействии излучения с конкретной узкой полушириной полосы и превращается в стабильную, окрашенную форму красителя. В соответствии с этим настоящее изобретение включает также способ образования цвета воздействием на прекраситель подходящей длины волны ультрафиолетового излучения.
В другом осуществлении настоящего изобретения композиция включает смесь обычного лейкокрасителя и трансорбера излучения. Лейкокраситель в присутствии трансорбера излучения приспособлен при воздействии на трансорбер излучения, предпочтительно ультрафиолетового излучения, превращаться в окрашенную композицию. Предпочтительный трансорбер излучения приспособлен для поглощения ультрафиолетового излучения и взаимодействия с лейкокрасителем для осуществления необратимого превращения молекулы в окрашенную композицию.
Еще одним осуществлением настоящего изобретения является способ превращения обычного лейкокрасителя в окрашенную композицию воздействием на лейкокраситель, смешанный с трансорбером излучения, определенными длинами волн электромагнитного излучения.
После определения используемых здесь различных терминов подробно описывается прекраситель по настоящему изобретению и способы проявления цвета с его использованием, а затем описание смеси лейкокраситель/трансорбер излучения и способы проявления цвета с ее использованием.
Определения
Используемый здесь термин "краситель" предназначен для включения без ограничения любого материала, который является органическим материалом, таким как органический краситель или пигмент. Желательно, чтобы краситель по существу был прозрачным, то есть существенно не взаимодействовал с ультрафиолетовым излучением, воздействию которого он подвергается. Подразумевается, что этот термин включает один материал или смесь двух или более материалов.
Термин "прекраситель" или "молекула прекрасителя", используемый здесь, означает молекулу красителя, которая ковалентно присоединена к трансорберу излучения, образуя бесцветную композицию. При обработке подходящей длиной волны электромагнитного излучения композиция способна образовать окрашенную композицию.
Термин "лейкокраситель" относится к лейкоформе красителя или бесцветной форме и представляет восстановленную форму красителя, имеющего один или два атома водорода, удаление которых вместе с дополнительным электроном в некоторых случаях приводит к образованию окрашенного красителя.
Используемый здесь термин "необратимый" означает, что краситель не будет возвращаться в его первоначальный цвет, когда он больше не подвергается воздействию ультрафиолетового излучения.
Термин "композиция" и такие варианты, как "окрашенная композиция", используют здесь для обозначения красителя и трансорбера излучения. Когда ссылка дается на бесцветную композицию, которая приспособлена для конкретного применения, термин "на основе композиции" используют в качестве модификатора для обозначения того, что материал включает краситель, трансорбер излучения и необязательно средство молекулярного включения.
Термин "средство молекулярного включения", используемый здесь, предназначен для обозначения любого вещества, имеющего химическую структуру, которая определяет по меньшей мере одну полость. То есть средство молекулярного включения является структурой, содержащей полости. Подразумевается, что используемый здесь термин "полость" включает любое отверстие или пространство с размером, достаточным для акцептирования по меньшей мере части одного из краситилей и трансорбера излучения или обоих. Средство молекулярного включения может включать также содержащую полость молекулу, к которой необязательно ковалентно присоединен трансорбер излучения. Способ получения средств молекулярного включения, ковалентно присоединенных к трансорберами излучения, и их ассоциация с красителями описываются в примерах 6-24 и находящейся в процессе одновременного рассмотрения заявке на патент N 08/461372, поданной 5 июня 1995, которая включается здесь в качестве ссылки.
Термин "функционализированное средство молекулярного включения", используют здесь для обозначения средства молекулярного включения, когда с каждой молекулой средства молекулярного включения ковалентно соединена одна или несколько молекул трансорбера ультрафиолетового излучения.
Термин "степень замещения" используют здесь для указания числа этих молекул или уходящих групп (определяются ниже), которые ковалентно соединяются с каждой молекулой средства молекулярного включения.
Термин "дериватизированное средство молекулярного включения" используют здесь для обозначения средства молекулярного включения, имеющего более двух уходящих групп, ковалентно соединенных с каждой молекулой средства молекулярного включения. Термин "уходящая группа" используют здесь для обозначения любой уходящей группы, способной принимать участие в бимолекулярной реакции нуклеофильного замещения.
Термин "ультрафиолетовое излучение" используют здесь для обозначения электромагнитного излучения, имеющего длины волн в диапазоне от около 4 до около 400 нм. Особенно желательный диапазон длин волн ультрафиолетового излучения для настоящего изобретения находится между приблизительно 100 и 375 нм. Таким образом, этот термин включает области, обычно относящиеся к УФ-области спектра и вакуумной УФ-области спектра. Диапазоны длин волн, типично относящиеся к этим двум областям, составляют от около 180 до около 400 нм и от около 100 до около 180 нм соответственно.
Термин "изменяемый" в отношении прекрасителя или смеси лейкокраситель/трансорбер излучения используют для обозначения того, что максимум абсорбции красителя способен "мутироваться" или изменяться путем воздействия излучения, предпочтительно ультрафиолетового излучения, в присутствии трансорбера излучения, так что максимум абсорбции смещается в видимую область. Обычно необходимо только, чтобы такой максимум абсорбции изменялся в максимум абсорбции, который отличается от максимума абсорбции прекрасителя до воздействия ультрафиолетового излучения, и чтобы изменение было необратимым. Другими словами, краситель должен изменяться из бесцветного в имеющий цвет.
Термин "соединение" предназначен для включения одного материала или смеси двух или более материалов. Если используют два или более материалов, необходимо, чтобы все из них абсорбировали излучение одной и той же длины волны. Как обсуждается более полно ниже, трансорбер излучения включает фотореактор и селективный для длины волны сенсибилизатор.
Термин "трансорбер радиации" используют здесь для обозначения любого материала, который приспособлен для абсорбции излучения при определенной длине волны и взаимодействия с красителем для воздействия на изменение красителя. В некоторых вариантах изобретения трансорбером излучения может быть органическое соединение. Синтез трансорбера излучения описывается в примерах 6-8 и 13 и в находящейся в процессе одновременного рассмотрения заявке на патент N 08/461372, поданной 5 июня 1995, которая включается здесь в качестве ссылки.
Молекула прекрасителя
Одним воплощением настоящего изобретения является молекула прекрасителя, которая способна изменяться под воздействием излучения с узкой полушириной полосы с образованием окрашенных соединений. Настоящее изобретение, в частности, относится к композиции, молекуле прекрасителя или "прекрасителю", содержащему молекулу красителя, которая ковалентно присоединена к трансорберу излучения. Когда молекула красителя ковалентно присоединяется к трансорберу излучения, композиция бесцветная. Прекраситель способен изменяться при воздействии излучения с определенной, узкой полушириной полосы и превращается в стабильную окрашенную форму красителя.
Настоящее изобретение включает необычные соединения, а именно трансорберы излучения, которые способны абсорбировать ультрафиолетовое излучение с узкой длиной волны. Эти соединения синтезируют смешиванием сенсибилизатора, селективного для длины волны, и фотореактора. Обычно фотореакторы не абсорбируют эффективно излучение высоких энергий. Однако, когда фотореактор смешивают с сенсибилизатором, селективным для длины волны, получаемое соединение представляет специфичное для длины волны соединение, которое эффективно абсорбирует очень узкий спектр излучения. В этом соединении специфичный для длины волны сенсибилизатор обычно абсорбирует излучение, имеющее специфичную длину волны и, следовательно, специфичное количество энергии, и передает эту энергию фотореактору. Желательно, чтобы сенсибилизатор, селективный для длины волны, был ковалентно связан с фотореактором.
В соответствии с этим трансорбер излучения, который присоединен к молекуле красителя, способен абсорбировать излучение и взаимодействовать с молекулой красителя для осуществления изменения прекрасителя с образованием окрашенного соединения. Трансорбером излучения может быть любой материал, который приспособлен для абсорбции излучения и взаимодействия с красителем для осуществления изменения красителя. Желательно, чтобы изменение прекрасителя было необратимым. В желаемом осуществлении изобретения трансорбер излучения ковалентно присоединяется к молекуле красителя, тем самым делая молекулу красителя бесцветной.
В качестве примера селективным для длины волны сенсибилизатором может быть, но не ограничивается им, фталоилглицин или 4-(4-гидроксифенил)-2-бутанон. Эти специфические для длины волны сенсибилизаторы иллюстрируются ниже.
Фталоилглицин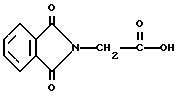
4-(4-Гидроксифенил)бутан-2-он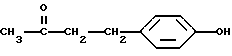
Фотореактором может быть, но не ограничивается ими, 1-(4-(2-гидроксиэтокси)фенил)-2-гидрокси-2-метилпропан-1-он (Darocur-2959) или 1-гидроксициклогексанфенилкетон (Irgacure 184). Эти фотоинициаторы, генерирующие реакционноспособные разновидности, иллюстрируются ниже.
DAROCUR-2959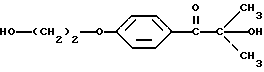
Irgacure 184 (1-гидроксициклогексанфенилкетон)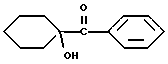
Должно быть понятно, что названные выше сенсибилизаторы и фотореакторы называют и в несвязанной форме. Например, когда фотореактор 1-гидроксициклогексанфенилкетон ковалентно связывается с сенсибилизатором через его гидроксигруппу, фотореакторная часть может быть указана как сложный эфир циклогексилфенилкетона. Когда сенсибилизатор 4-(4-гидроксифенил)-2-бутанон ковалентно связывается с фотореактором через его гидроксигруппу, сенсибилизаторная часть может быть указана как 4-(4-оксифенил)-2-бутанон. Подобным же образом, когда сенсибилизатор фталоилглицин ковалентно связывается с фотореактором через его гидроксигруппу, сенсибилизаторная часть может быть указана как фталоилглицил. Когда сенсибилизатор ковалентно связывается с фотореактором, эти сенсибилизаторы и фотореакторы могут быть для простоты указаны в их несвязанной форме.
В качестве примера трансорбером излучения может быть 2-(п-(2-метиллактоил)фенокси) этил-1,3-диоксо-2-изоиндолинацетат, имеющий формулу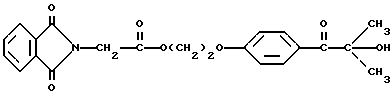
сложный эфир фталоилглицилциклогексилфенилкетона, имеющий формулу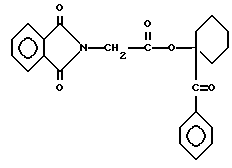
4-(4-оксифенил)-2-бутанон-1-(4-(2-оксиэтокси)фенил)-2- гидрокси-2-метилпропан-1-он (или 2-гидрокси-2-метил-4'-(2-(п- (3-оксобутил)фенокси)этокси)пропиофенон), имеющий формулу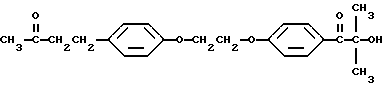
4-(4-оксифенил) 2-бутанонциклогексилфенилкетон (или 4-(п-((4- бензоилциклогексил)окси)фенил)-2-бутанон, имеющий формулу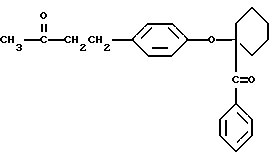
Примеры 6-8 и 13 описывают способы получения указанных выше трансорберов излучения. Должно быть понятно, что в настоящем изобретении можно использовать другие, а не конкретно перечисленные выше сенсибилизаторы, фотореакторы и трансорберы излучения.
В соответствии с этим следующая формула представляет прекраситель, где молекулой красителя является лейкоформа кристаллического фиолетового (хлорид N-(4-(бис(4-(диметиламино) фенил)метилен-2,5-циклогексадиен-1-илиден)-N-метилметанаминия), ковалентно связанная с X, где X представляет трансорбер излучения или где X представляет специфичный для длины волны сенсибилизатор, ковалентно связанный с ним, где оксиэтоксифенильная группа функционирует в качестве фотореактора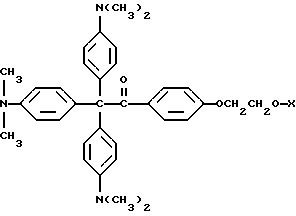
Способ получения указанного выше прекрасителя описывается в примере 25.
В качестве примера, прекрасителем могут быть, но не ограничиваются ими, соединения следующих формул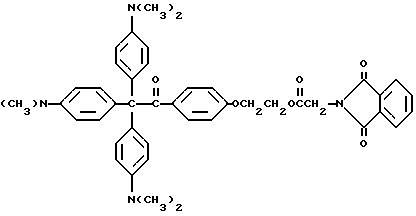
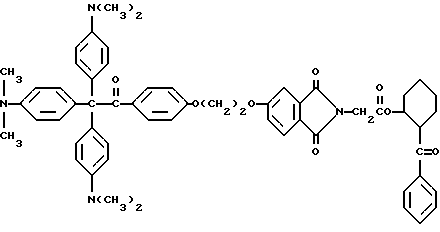
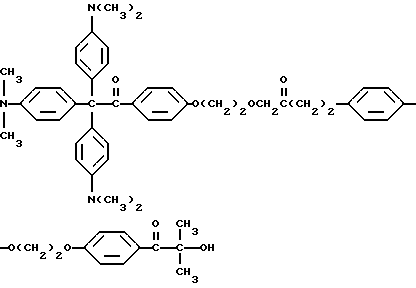
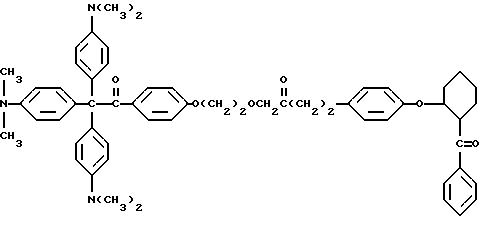
или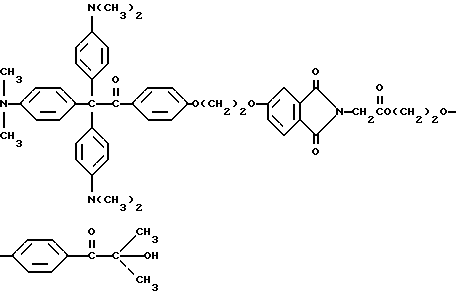
Способ получения следующего прекрасителя описывается в примере 26.
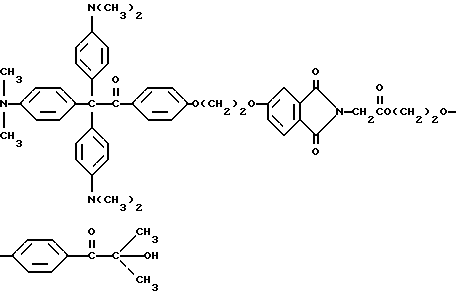
Желательный прекраситель имеет следующую формулу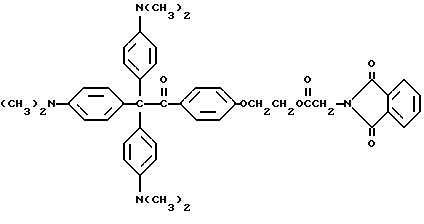
Эта определенная структура показывает трансорбер излучения, 2-(п-(2-метиллактоил)фенокси)этил-1,3-диоксо-2-изоиндолинацетат, присоединенный к кристаллическому фиолетовому (хлорид N-(4-бис(4-(диметиламино)фенил) метилен-2,5-циклогексадиен-1-илиден)-N-метилметанаминия). Примеры 1-3 описывают, как получить указанную выше молекулу прекрасителя.
Должно быть понятно, что описанные формулы являются просто примером прекрасителя, который является рассматриваемой частью настоящего изобретения, и что кристаллический фиолетовый
можно заменить на другие красителя, и что вместо указанных выше трансорберов излучения можно использовать другие трансорберы излучения.
Например, другими прекрасителями настоящего изобретения являются следующие соединения, где X представляет трансорбер излучения и где R представляет водород, метальную или этильную группу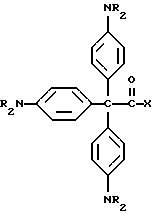
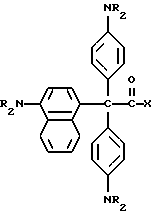
В примере 27 описывается способ получения следующего прекрасителя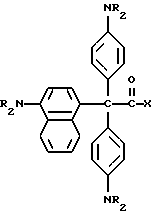
Дополнительные примеры других прекрасителей по настоящему изобретению включают следующие соединения, где R представляет алкильную или арильную группу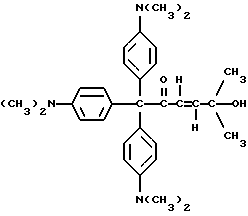
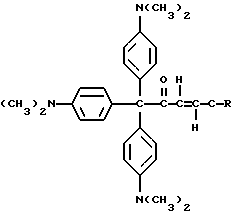
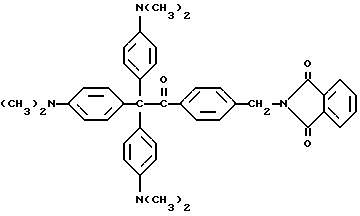
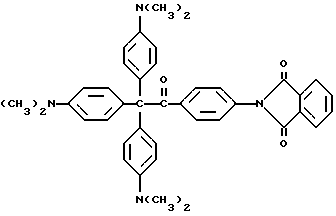
Настоящее изобретение относится также к способу образования окрашенной композиции. Этот способ заключается в облучении композиции, содержащей прекраситель. Прекраситель является молекулой, содержащей молекулу красителя, ковалентно присоединенную к трансорберу излучения. Когда молекула красителя ковалентно присоединяется к трансорберу излучения, композиция бесцветная. Способ заключается в воздействии на прекраситель ультрафиолетового излучения при уровне дозировки, достаточном для изменения красителя. Пример 4 далее иллюстрирует способ образования бесцветной композиции с использованием прекрасителя по настоящему изобретению.
Прекраситель по настоящему изобретению можно обработать излучением, имеющим длину волны от около 4 до около 1000 нм в зависимости от трансорбера излучения, который присутствует в композиции. Таким образом, излучением может быть ультрафиолетовое излучение, включая излучение в длинноволновой УФ-области и коротковолновой или вакуумной УФ-области; видимое излучение и излучение в ближней инфракрасной области. Желательно прекраситель обрабатывать излучением, имеющим длину волны от около 4 до около 700 нм. Более желательно прекраситель обрабатывать ультрафиолетовым излучением, имеющим длину волны от около 4 до около 400 нм. Более желательно, чтобы излучение имело длину волны между около 100 и 375 нм.
Настоящее изобретение относится также к субстрату, имеющему на нем изображение, которое образуется молекулой прекрасителя по настоящему изобретению.
Смесь лейкокраситель/трансорбер излучения
В другом осуществлении настоящего изобретения композиция по настоящему изобретению включает смесь обычного лейкокрасителя и трансорбера излучения. Лейкокраситель в присутствии трансорбера излучения при воздействии на трансорбер излучения, предпочтительно ультрафиолетового излучения, приспособлен для превращения в окрашенную композицию. Предпочтительный трансорбер излучения приспособлен для абсорбции ультрафиолетового излучения и взаимодействия с лейкокрасителем для осуществления необратимого превращения молекулы в окрашенную композицию.
Трансорберы излучения, которые могут быть смешаны с лейкокрасителем в настоящем изобретении, описываются выше.
Лейкокрасители, которые можно использовать в настоящем изобретении, включают, но не ограничиваются ими, аминотриарилметаны, аминоксантены, аминотиоксантены, амино-9,10-дигидроакридины, аминофеноксазины, аминофенотиазины, аминодигидрофеназины, аминодифенилметаны, лейкоиндамины, аминогидроянтарные кислоты (цианоэтаны, лейкометины), гидразины, лейкоиндигоидные красители, амино-2,3-дигидроантрахиноны, фенетиланилины, 10-ациламинодигидрофеназины, 10-ациламинофенотиазины, 10-ациламинофеноксазины и аминотриарилметаны, где водород метана замещен алкилтио-, бензилтио-, 2-фенилгидразино- или алкоксикарбонильной группой. Обычно предпочтительным классом лейкокрасителей является класс аминотриарилметанов и их производных. Аминотриарилметановые красители, а также другие классы красителей рассматриваются в работе Abrahart, E.N., Dyes and their Intermediates, Chemical Publishing Co., Inc., (1977), которая включается здесь в качестве ссылки. Аминотриарилметаны рассматриваются на с. 151 ссылки Abrahart. Желательным лейкокрасителем является аминотриарилметановый краситель.
Настоящее изобретение включает также образование окрашенной молекулы из лейкокрасителя смешиванием лейкокрасителя с трансорбером излучения и обработкой смеси определенными длинами волн электромагнитного излучения.
Композицию лейкокрасителя по настоящему изобретению можно обработать излучением, имеющим длину волны от около 4 до около 1000 нм в зависимости от трансорбера излучения, который присутствует в композиции. Таким образом, излучением может быть ультрафиолетовое излучение, включая излучение в длинноволновой УФ-области и коротковолновой или вакуумной УФ-области; видимое излучение и излучение в ближней инфракрасной области. Желательно композицию обрабатывать излучением, имеющим длину волны от около 4 до около 700 нм. Более желательно композицию по настоящему изобретению обрабатывать ультрафиолетовым излучением, имеющим длину волны от около 4 до около 400 нм. Более желательно, чтобы излучение имело длину волны между около 100 и 375 нм.
В другом осуществлении изобретения композицию прекрасителя наносят на субстрат до облучения ультрафиолетовым излучением. Настоящее изобретение относится также к субстрату, имеющему на нем изображение, которое образуется композицией лейкокрасителя по настоящему изобретению. Желательно, чтобы измененный краситель был стабильным.
Хотя лейкокраситель и трансорбер излучения были описаны как отдельные соединения, они могут быть частью той же самой молекулы, в этом случае одну молекулу обозначают прекрасителем. Например, краситель и трансорбер излучения могут быть ковалентно связаны друг с другом либо непосредственно, либо через относительно маленькую молекулу или спейсерную группу. И, наоборот, краситель и трансорбер излучения могут быть ковалентно связаны с большой молекулой, такой как олигомер или полимер. Кроме того, краситель и трансорбер излучения могут быть ассоциированы с большой молекулой, среди других способов, ван-дер-ваальсовыми силами и водородным связыванием. Другие варианты должны быть легко понятны специалистам данной области.
Прекраситель и смеси лейкокраситель/трансорбер излучения по настоящему изобретению могут необязательно содержать средство молекулярного включения, имеющее химическую структуру, которая определяет по меньшей мере одну полость. Таким образом, полостью в средстве молекулярного включения может быть туннель через средство молекулярного включения или подобное впадине пространство, или углубленное пространство в средстве молекулярного включения. Полость может быть изолированной или независимой или может быть соединена с одной или несколькими другими полостями.
Средство молекулярного включения может быть по природе неорганическим или органическим. В некоторых осуществлениях изобретения химическая структура средства молекулярного включения приспособлена для образования комплекса молекулярного включения. Средства молекулярного включения включают, но не ограничиваются ими, клатраты, цеолиты и циклодекстрины. Примеры, циклодекстринов включают, но не ограничиваются ими, α-циклодекстрин, β-циклодекстрин, γ-циклодекстрин, гидроксипропил-β-циклодекстрин, гидроксиэтил-β-циклодекстрин, сульфатированный β-циклодекстрин, гидроксиэтил-α-циклодекстрин, карбоксиметилен-α-циклодекстрин, карбоксиметил-β-циклодекстрин, карбоксиметил-γ-циклодекстрин, октилсукцинированный α-циклодекстрин, октилсукцинированный β-циклодекстрин, октилсукцинированный γ-циклодекстрин и сульфатированный β- и γ-циклодекстрин (American Maize-Products Company, Hammond, Indiana).
Желательным средством молекулярного включения является циклодекстрин. В частности, в некоторых осуществлениях изобретения желательным средством молекулярного включения является α-циклодекстрин. В других осуществлениях желательным средством молекулярного включения является β-циклодекстрин. Еще в одних осуществлениях желательным средством молекулярного включения является γ-циклодекстрин.
В тех осуществлениях изобретения, где молекулу лейкокрасителя и трансорбер излучения смешивают, каждый из лейкокрасителя и трансорбера излучения необязательно ассоциируется с одной или несколькими средствами молекулярного включения. В некоторых осуществлениях изобретения лейкокраситель по меньшей мере частично включается в полость средства молекулярного включения, и трансорбер излучения ассоциируется со средством молекулярного включения за пределами полости. В некоторых осуществлениях трансорбер излучения ковалентно связывается вне средства молекулярного включения.
Например, лейкокраситель и/или трансорбер излучения можно сохранять в непосредственной близости к средству молекулярного включения водородным связыванием, ван-дер-ваальсовыми силами или тому подобное. Термин "ассоциированный" в его самом широком смысле означает, что лейкокраситель и трансорбер излучения находятся по меньшей мере в непосредственной близости к средству молекулярного включения. Альтернативно любой или оба лейкокрасителя и трансорбера излучения могут быть ковалентно связаны со средством молекулярного включения. В некоторых осуществлениях изобретения лейкокраситель может быть ассоциирован со средством молекулярного включения при помощи водородного связывания и/или ван-дер-ваальсовых сил или тому подобное, тогда как трансорбер излучения ковалентно связывается со средством молекулярного включения. В других осуществлениях настоящего изобретения лейкокраситель по меньшей мере частично включается в полость средства молекулярного включения, и трансорбер излучения локализован вне полости средства молекулярного включения. Должно быть понятно, что один или несколько трансорберов излучения могут быть ассоциированы с одним средством молекулярного включения, один или несколько лейкокрасителей могут быть ассоциированы с одним средством молекулярного включения, или один или несколько обоих могут быть ассоциированы с одним средством молекулярного включения. Должно быть понятно также, что один или несколько пpекрасителей могут быть ассоциированы со средством молекулярного включения или один прекраситель может быть ассоциирован с более чем одним средством молекулярного включения.
В нескольких осуществлениях изобретения молекула трансорбера излучения, селективный для длины волны сенсибилизатор или фотореактор могут быть ассоциированы со средством молекулярного включения. Следует заметить, что число таких молекул может быть между приблизительно 1 и приблизительно 21 молекулами на средство молекулярного включения. Конечно, в некоторых случаях может быть более 21 молекулы на молекулу средства молекулярного включения. Желательно, чтобы было более трех таких молекул на средство молекулярного включения.
Степень замещения функционализированного средства молекулярного включения может быть в диапазоне от 1 до приблизительно 21. В качестве другого примера степень замещения может быть в диапазоне от 3 до около 10. В качестве дополнительного примера степень замещения может быть в диапазоне от около 4 до около 9.
Лейкокраситель может быть ассоциирован с функционализированным средством молекулярного включения. Термин "ассоциированный" в его наиболее широком смысле означает, что лейкокраситель сохраняется в непосредственной близости к функционализированному средству молекулярного включения. Например, лейкокраситель может сохраняться в непосредственной близости к функционализированному средству молекулярного включения путем водородного связывания, ван-дер-ваальсовых сил или тому подобное. Альтернативно лейкокраситель может быть ковалентно связан с функционализированным средством молекулярного включения, хотя это обычно ни желательно, ни необходимо. В качестве следующего примера лейкокраситель может быть по меньшей мере частично включен в полость функционализированного средства молекулярного включения.
Приведенные ниже примеры описывают способы получения и ассоциирования красителей и трансорберов ультрафиолетового излучения с β-циклодекстринами. Только для иллюстративных целей примеры 6, 7, 11 и 12 описывают один или несколько способов получения и ассоциирования красителей и трансорберов ультрафиолетового излучения с циклодекстринами.
В тех осуществлениях настоящего изобретения, в которых трансорбер ультрафиолетового излучения ковалентно связан со средством молекулярного включения, эффективен перенос энергии от трансорбера ультрафиолетового излучения к лейкокрасителю трансорбера ультрафиолетового излучения, которые присоединены к средству молекулярного включения.
В соответствии с этим настоящее изобретение относится также к композиции, которая включает лейкокраситель и функционализированное средство молекулярного включения. Только для иллюстративных целей примеры от 14 до 21 и от 23 до 24 описывают другие способы получения и ассоциирования красителей и трансорберов ультрафиолетового излучения с циклодекстринами, где более чем две молекулы трансорбера ультрафиолетового излучения ковалентно связываются с каждой молекулой средства молекулярного включения.
Настоящее изобретение предлагает также способ получения функционализированного средства молекулярного включения. Способ получения функционализированного средства молекулярного включения включает стадии обеспечения дериватизированного трансорбера ультрафиолетового излучения, имеющего нуклеофильную группу, обеспечения дериватизированного средства молекулярного включения, имеющего более двух уходящих групп на молекулу, и реакции дериватизированного трансорбера ультрафиолетового излучения с дериватизированным средством молекулярного включения в условиях, достаточных, чтобы привести к ковалентному связыванию в среднем более двух молекул трансорбера ультрафиолетового излучения с каждой молекулой средства молекулярного включения. В качестве примера дериватизированным трансорбером ультрафиолетового излучения может быть 2-[п-(2-метил- 2-меркаптометилпропионил)фенокси]этил-1,3-диоксо-2- изоиндолинацетат. В качестве другого примера дериватизированным трансорбером ультрафиолетового излучения может быть 2-меркаптометил-2- метил-4'-[2-[п-(3-оксобутил)фенокси]этокси]пропиофенон.
Обычно дериватизированный трансорбер ультрафиолетового излучения и дериватизированное средство молекулярного включения выбирают так, чтобы вызвать ковалентное связывание трансорбера ультрафиолетового излучения со средством молекулярного включения при помощи бимолекулярной реакции нуклеофильного замещения. Следовательно, выбор нуклеофильной группы и уходящих групп и получение дериватизированного трансорбера ультрафиолетового излучения и дериватизированного средства молекулярного включения соответственно могут быть легко выполнены специалистами в данной области без необходимости неуместного экспериментирования.
Нуклеофильной группой дериватизированного трансорбера ультрафиолетового излучения может быть любая нуклеофильная группа, способная принимать участие в биомолекулярной реакции нуклеофильного замещения, конечно, при условии, что реакция приводит к ковалентному связыванию более чем двух молекул трансорбера ультрафиолетового излучения со средством молекулярного включения. Нуклеофильной группой обычно будет основание Льюиса, т.е. любая группа, имеющая неподеленную пару электронов. Группа может быть нейтральной или отрицательно заряженной. Примеры нуклеофильных групп включают, с целью только иллюстрации, алифатическую гидрокси, ароматическую гидрокси, алкоксиды, карбокси, карбоксилат, амино и меркапто.
Подобным же образом уходящей группой дериватизированного средства молекулярного включения может быть любая уходящая группа, способная принимать участие в биомолекулярной реакции нуклеофильного замещения, при условии, что реакция приводит к ковалентному связыванию более чем двух молекул трансорбера ультрафиолетового излучения со средством молекулярного включения. Примеры уходящих групп включают, так же только в качестве иллюстрации, п-толуолсульфонаты (тозилаты), п-бромбензолсульфонаты (бросилаты), п-нитробензолсульфонаты (нозилаты), метансульфонаты (мезилаты), оксониевые ионы, алкилперхлораты, аммониоалкансульфонатные эфиры (бетилаты), алкилфторсульфонаты, трифторметансульфонаты (трифлаты), нонафторбутансульфонаты (нонафлаты) и 2,2,2-трифторэтансульфонаты (трезилаты).
Реакцию дериватизированного трансорбера ультрафиолетового излучения с дериватизированным средством молекулярного включения проводят в растворе. Выбор растворителя зависит от растворимостей двух дериватизированных разновидностей. Особенно пригодным растворителем является N,N-диметилформамид (ДМФ).
Условия реакции, например температура, время реакции и тому подобное, обычно выбирают основанными на природе нуклеофильных и уходящих групп. Повышенные температуры обычно не требуются. Например, температура реакции может быть в диапазоне от около 0oC до около комнатной температуры, т.е. до 20-25oC.
Получение функционализированного средства молекулярного включения, как описывается выше, обычно проводят в отсутствие красителя или лейкокрасителя. Однако лейкокраситель может быть ассоциирован с дериватизированным средством молекулярного включения до реакции дериватизированного трансорбера ультрафиолетового излучения с дериватизированным средством молекулярного включения, особенно, если желательна степень замещения выше чем около трех. При степени замещения около трех считается, что ассоциация лейкокрасителя с функционализированным средством молекулярного включения все же может позволить лейкокрасителю, по меньшей мере частично, быть включенным в полость функционализированного средства молекулярного включения. При более высоких степенях замещения, например около шести, пространственное затруднение может частично или полностью предотвратить включение лейкокрасителя, по меньшей мере частично, в полость функционализированного средства молекулярного включения. Следовательно, лейкокраситель может быть ассоциирован с дериватизированным средством молекулярного включения, которое обычно будет проявлять слабое, если вообще будет проявлять, пространственное затруднение. В этом случае лейкокраситель будет по меньшей мере частично включен в полость дериватизированного средства молекулярного включения. Затем можно проводить описанную выше бимолекулярную реакцию нуклеофильного замещения, чтобы получить композицию по настоящему изобретению, в которой лейкокраситель по меньшей мере частично включен в полость функционализированного средства молекулярного включения.
В примере 5 описывается способ получения красителя облучением лейкокрасителя, смешанного с трансорбером излучения, присоединенным к β-циклодекстрину.
Настоящее изобретение далее описывается приведенными ниже примерами.
В примерах все части приводятся в массовых частях, если не оговорено особо.
Пример 1
Получение исходного материала типа пинакола
Исходный материал для молекулы прекрасителя, который будет иметь синий цвет при облучении, получают в соответствии со следующей реакцией: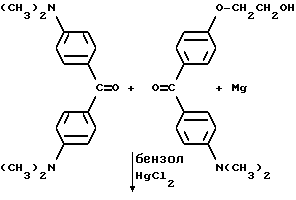
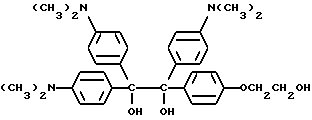
В круглодонную трехгорлую колбу на 500 мл, снабженную магнитной мешалкой, холодильником, капельной воронкой, помещают 10 г (0,037 моль) бис-диметиламинобензофенона (Aldrich Chemical Company, Inc., Milwaukee, Wisconsin), 1 г гидроксиэтоксидиметиламинобензофенона (Aldrich Chemical Company, Inc. , Milwaukee, Wisconsin) и 0,75 г магниевых стружек (Aldrich Chemical Company, Inc. , Milwaukee, Wisconsin). В реакционную смесь выливают 200 мл безводного бензола, и смесь нагревают до 50oC и медленно добавляют 0,84 г хлорида ртути в 20 мл бензола в течение 20 мин. Реакцию инициируют добавлением в колбу небольшого кристалла иода. Реакционную смесь нагревают в течение 30 мин. Органический слой отделяют, сушат, и растворитель удаляют при пониженном давлении, получая желтый твердый продукт. Этот продукт пропускают через короткую колонку с силикагелем с применением 50%-ного этилацетата в гексане в качестве растворителя.
Масс-спектр: 538 (М+-ОН), 521, 480, 252.
Пример 2
Продукт примера 1 обрабатывают в соответствии со следующей реакцией: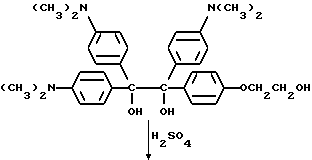
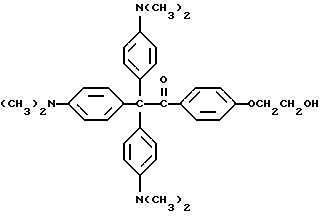
В круглодонную колбу на 250 мл добавляют 5,0 г (9 ммоль) диола из примера 1 и помещают магнитную мешалку. Добавляют 50 мл 50%-ной концентрированной серной кислоты в воде, и реакционную смесь перемешивают на водяной бане в течение 1 ч. Затем pH реакционной смеси устанавливают вплоть до около 7,0 добавлением гидроксида натрия. Осадок отделяют фильтрованием и сушат в вакууме в течение 2 ч. Выход 4,2 г (88%). Масс-спектр: 537 (М+), 520, 448, 433.
Пример 3
Продукт примера 2 подвергают следующей реакции: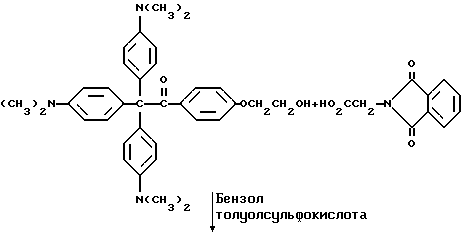
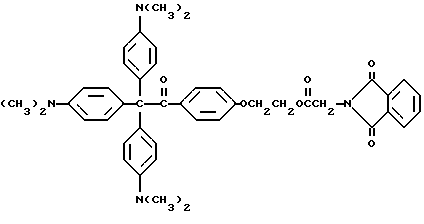
В круглодонную колбу на 250 мл, снабженную магнитной мешалкой, устройством для улавливания воды Дина и Старка и холодильником, добавляют 4,0 г (7,6 ммоль) кетона из примера 2, 1,5 г фталоилглицина (Aldrich Chemical Company, Inc. , Milwaukee, Wisconsin), 0,1 г п-толуолсульфоновой кислоты (Aldrich Chemical Company, Inc., Milwaukee, Wisconsin) и 100 мл безводного бензола (Aldrich Chemical Company, Inc., Milwaukee, Wisconsin). Реакционную смесь нагревают при кипячении с обратным холодильником в течение 8 ч, причем после этого времени в устройстве для улавливания воды собирают 0,3 мл воды. Удаление растворителя при пониженном давлении дает 5,0 г продукта.
Пример 4
0,2 г Продукта из примера 3 растворяют в 5 мл ацетонитрила (Ficher Scientific, Pittsburg, Pennsylvania). На металлическую пластину (Q-panel) помещают 3 капли смеси, и при помощи шпателя смесь распределяют по пластине. Пластину подвергают воздействию излучения возбуждением на 222 нм при движении со скоростью 12,19 м/мин (40 футов/мин) на транспортере. При действии излучения проявляется глубокий синий цвет.
Четыре капли помещают на лист белой бумаги (Neenah bond) и оставляют для распределения на нем. Влажный лист затем подвергают воздействию излучения возбуждением при 222 нм. Влажная часть площади приобретает глубокий синий цвет.
Пример 5
Лейкокраситель (лейкокраситель кристаллического фиолетового) (Aldrich Chemical Company, Inc., Milwaukee, Wisconsin) смешивают с композицией, содержащей трансорбер излучения, присоединенный к β-циклодекстрину, и представленной следующей формулой:
β-циклодекстрин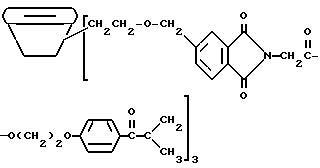
Синтез трансорбера излучения, присоединенного к β-циклодекстрину, описывается в примерах 8-11 и в находящейся в процессе одновременного рассмотрения заявке на патент США N 08/461372, поданной 5 июня 1995 и включенной здесь в качестве ссылки. 0,1 г Лейкокрасителя кристаллического фиолетового и 0,2 г трансорбера излучения, присоединенного к β-циклодестрину, смешивают в 5 мл ацетонитрила (Ficher Scientific, Pittsburg, Pennsylvania). Бесцветный раствор помещают на металлическую пластину (Q-panel) и при помощи шпателя распределяют по пластине (приблизительно 5 капель раствора). Пластину пропускают под лампой возбуждения на 222 нм (10,67 м/мин (35 фут/мин) на транспортере), после чего раствор приобретает глубокий синий цвет. Эту операцию повторяют, помещая 3 капли на бумагу (Neenach Bond) и распределяя их на бумаге шпателем. Пропускание влажной бумаги под лампой возбуждения на 222 нм с барьером диэлектрика (Haraus Noblelight AG, Hanau, Germany) проявляет синий цвет. Сам лейкокраситель не проявляет никакого цвета при обработке излучением с 222 нм.
Пример 6
Этот пример описывает получение β-циклодекстринового средства молекулярного включения, имеющего (1) трансорбер ультрафиолетового излучения, ковалентно связанный с циклодекстрином вне полости циклодекстрина, и (2) краситель, ассоциированный с циклодекстрином при помощи водородных связей и/или ван-дер-ваальсовых сил.
А. Ацилирование трансорбера по Фриделю-Крафтсу
Реакционную трехгорлую круглодонную колбу на 250 мл снабжают холодильником и уравнивающей давление капельной воронкой, снабженной трубкой для ввода азота. В колбу помещают магнитную мешалку. При промывании струей азота в колбу загружают 10 г (0,05 моль) 1-гидроксициклогексилфенилкетона (IRGACURE 184, Ciba-Geigy Corporation, Hawthorne, New York), 100 мл безводного тетрагидрофурана (Aldrich Chemical Company, Inc., Milwaukee, Wisconsin) и 5 г (0,05 моль) янтарного ангидрида (Aldrich Chemical Co., Milwaukee, WI). К непрерывно перемешиваемому содержимому колбы затем добавляют 6,7 г безводного хлорида алюминия (Aldrich Chemical Co., Milwaukee, Wisconsin). Получаемую реакционную смесь выдерживают приблизительно при 0oC на ледяной бане в течение около одного часа, после чего смеси дают нагреться до комнатной температуры в течение двух часов. Реакционную смесь затем выливают в смесь 500 мл ледяной воды и 100 мл диэтилового эфира. Эфирный слой удаляют после добавления к водной фазе небольшого количества хлорида натрия для облегчения разделения фаз. Эфирный слой сушат над безводным сульфатом магния. Эфир удаляют при пониженном давлении, оставляя 12,7 г (87%) белого кристаллического порошка. Ядерно-магнитный резонанс показал, что этот материал является 1-гидроксициклогексил-4-(2-карбоксиэтил) карбонилфенилкетоном.
Б. Получение трансорбера, ацилированного хлорангидрида
В круглодонную колбу на 250 мл, снабженную холодильником, загружают 12,0 г 1-гидроксициклогексил-4-(2- карбоксиэтил)-карбонилфенилкетона (0,04 моль), 5,95 г (0,05 моль) тионилхлорида (Aldrich Chemical Co., Milwaukee, Wisconsin) и 50 мл диэтилового эфира. Получаемую реакционную смесь перемешивают при 30oC в течение 30 мин, после чего растворитель удаляют при пониженном давлении. Остаток, белое твердое вещество, выдерживают при 0,01 мм рт.ст. в течение 30 мин для удаления остаточного растворителя и избытка тионилхлорида, получая 12,1 г (94%) 1-гидроксициклогексил-4-(2-хлорформилэтил) карбонилфенилкетона.
В. Ковалентное связывание ацилированного трансорбера с циклодекстрином
В трехгорлую круглодонную реакционную колбу на 250 мл, содержащую магнитную мешалку и снабженную термометром, холодильником и выравнивающей давление капельной воронкой, снабженной трубкой для ввода азота, загружают 10 г (9,8 ммоль) β-циклодекстрина (American Maize-Prоducts Company, Hammond, Indiana), 31,6 (98 ммоль) 1-гидроксициклогексил-4-(2-хлорформилэтил) карбонилфенилкетона и 100 мл N,N-диметилформамида при непрерывном промывании азотом. Реакционную смесь нагревают до 50oC и добавляют 0,5 мл триэтиламина. Реакционную смесь выдерживают при 50oC в течение часа и оставляют для охлаждения до комнатной температуры. Продукт реакции -β-циклодекстрин, ковалентно связанный с трансорбером ультрафиолетового излучения (называемого в дальнейшем для удобства как β-циклодекстрин-трансорбер), не выделялся.
Вышеупомянутую методику повторяют для выделения продукта реакции. В конце описываемой методики реакционную смесь концентрируют в роторном испарителе приблизительно до 10% первоначального объема. Остаток выливают в ледяную воду, в которую затем добавляют хлорид натрия для принуждения выделения продукта из раствора. Получаемый осадок отделяют фильтрованием и промывают диэтиловым эфиром. Твердый продукт сушат при пониженном давлении, получая 24,8 г белого порошка. В третьем получении остаток, оставшийся в роторном испарителе, помещают в верхнюю часть колонки длиной приблизительно 7,5 см, содержащей 15 г силикагеля. Остаток элюируют N,N-диметилформамидом, причем элюат контролируют при помощи Flexible-Backed пластин ТСХ Whatman® (Catalog N 05-713-161, Ficher Scientific, Pittsburg, Pennsylvania). Элюированный продукт выделяют выпариванием растворителя. Структуру продукта подтверждают анализом способом ядерного магнитного резонанса.
Г. Ассоциация красителя с продуктом циклодекстрин-трансорбер - Получение окрашенной композиции
К раствору 10 г (вычислено, что это составляет около 3,6 ммоль) продукта β-циклодекстрин-трансорбер в 150 мл N,N-диметилформамида в круглодонной колбе на 250 мл добавляют при комнатной температуре 1,2 г (3,6 ммоль) малахитового зеленого оксалата (Aldrich Chemical Company, Inc., Milwaukee, Wisconsin), называемого в дальнейшем для удобства красителем А. Реакционную смесь перемешивают магнитной мешалкой в течение одного часа при комнатной температуре. Большую часть растворителя затем удаляют в роторном испарителе, и остаток элюируют из колонки с силикагелем, как уже описано. Комплекс включения красителя А и продукта β-циклодекстрин-трансорбер выходит из колонки первым, чисто отделяясь как от свободного красителя А, так и продукта β-циклодекстрин-трансорбер. Элюат, содержащий комплекс, собирают, и растворитель удаляют в роторном испарителе. Остаток выдерживают при пониженном давлении 0,01 мм рт.ст. для удаления остаточного растворителя, получая сине-зеленый порошок.
Д. Изменение окрашенной композиции
Комплекс включения красителя А и продукта β-циклодекстрин-трансорбер подвергают воздействию ультрафиолетового излучения от двух разных ламп - A и B. Лампа A представляет комплект ламп возбуждения на 222 нм, состоящий из рядов четырех цилиндрических ламп, имеющих длину около 30 см. Лампы охлаждают циркулирующей водой через расположенную в центре или внутреннюю трубку лампы, и как следствие они работают при относительно низкой температуре, т. е. около 50oC. Плотность энергии у наружной поверхности ламп обычно находится в диапазоне от около 4 до около 20 Дж/м2. Однако такой диапазон в действительности отражает лишь возможность поставки потока энергии лампы возбуждения; в будущем могут быть полезными более высокие плотности энергии. Расстояние от лампы до облучаемого образца составляет 4,5 см. Лампа В представляет ртутную лампу среднего давления Hanovia на 500 Вт (Hanovia Lamp Co. , Newark, New Jersey). Расстояние от лампы В до облучаемого образца составляет около 15 см.
Несколько капель N, N-диметилформамидного раствора комплекса включения красителя A и продукта β-циклодекстрин-трансорбер помещают на пластину ТСХ и в небольшую полиэтиленовую взвешиваемую чашку. Оба образца подвергают воздействию лампы A и обесцвечивают (превращают в бесцветное состояние) за 15-20 с. Подобные результаты получают с лампой В в течение 30 с.
Первый контрольный образец, состоящий из раствора красителя A и β-циклодекстрина в N,N-диметилформамида, не обесцвечивается лампой A. Второй контрольный образец, состоящий из красителя A и 1-гидроксициклогексилфенилкетона в N,N-диметилформамиде, обесцвечивается лампой A в пределах 60 с. Однако при стоянии в пределах часа снова начинает появляться цвет.
Для оценки действия растворителя на обесцвечивание 50 мг комплекса включения красителя A и продукта β-циклодекстрин-трансорбер растворяют в 1 мл растворителя. Получаемый раствор или смесь помещают на предметное стекло микроскопа и подвергают воздействию лампы A в течение 1 мин. Скорость обесцвечивания, т. е. время придания образцу бесцветности, прямо пропорциональнa растворимости комплекса в растворителе, как суммировано в табл. 1.
Наконец, 10 мг комплекса включения красителя A и продукта β-=циклодекстрин-трансорбер помещают на предметном стекле микроскопа и измельчают пестиком. Получаемый порошок подвергают воздействию лампы A в течение 10 с. Порошок становится бесцветным. Подобные результаты получают с лампой В, но при более медленной скорости.
Пример 7
Вследствие того что при получении окрашенной композиции, описанной в следующих примерах, существует возможность для трансорбера, ацилированного хлорангидрида, по меньшей мере частично занимать полость циклодекстрина, частичного или полного исключения красителя, используют модифицированную препаративную методику. Таким образом, этот пример описывает получение β-=циклодекстринового средства молекулярного включения, имеющего (1) краситель, по меньшей мере частично включенный в полость циклодекстрина и ассоциированный с ним при помощи водородных связей и/или ван-дер-ваальсовых сил, и (2) трансорбер ультрафиолетового излучения, ковалентно связанный с циклодекстрином, по существу вне полости циклодекстрина.
А. Ассоциация красителя с циклодекстрином
К раствору 10,0 г (9,8 ммоль) β-=циклодекстрина в 150 мл N,N-диметилформамида добавляют 3,24 г (9,6 ммоль) красителя A. Получаемый раствор перемешивают при комнатной температуре в течение одного часа. Реакционный раствор концентрируют при пониженном давлении в роторном испарителе до объема одной десятой от первоначального объема. Остаток пропускают через колонку с силикагелем, как описывается в части B примера 6. Растворитель в элюате удаляют при пониженном давлении в роторном испарителе, получая 12,4 г сине-зеленого порошка, комплекса включения красителя A и β-=циклодекстрина.
Б. Ковалентное связывание ацилированного трансорбера с комплексом включения красителя и циклодекстрина - Получение окрашенной композиции
В трехгорлую круглодонную реакционную колбу на 250 мл, содержащую магнитную мешалку и снабженную термометром, холодильником и уравнивающей давление капельной воронкой, снабженной трубкой для ввода азота, загружают 10 г (9,6 ммоль) комплекса включения красителя A и β-=циклодекстрина, 31,6 г (98 ммоль) 1-гидроксициклогексил-4-(2-хлорформилэтил)карбонилфенилкетона, полученного, как описано в части Б примера 6, и 150 мл N,N-диметилформамида при непрерывном промывании азотом. Реакционную смесь нагревают до 50oC и добавляют 0,5 мл триэтиламина. Реакционную смесь выдерживают при 50oC в течение часа и дают охладиться до комнатной температуры. Реакционную смесь затем обрабатывают, как описывается выше в части A, получая 14,2 г комплекса включения красителя A и продукта β-=циклодекстрин-трансорбер, сине-зеленый порошок.
В. Превращение окрашенной композиции
Методики, описанные в части Д примера 6, повторяют с комплексом включения красителя A и продукта β-=циклодекстрин-трансорбер, полученным выше в части Б, по существу с такими же результатами.
Пример 8
Этот пример описывает способ получения трансорбера ультрафиолетового излучения, 2-[п-(2-метиллактоил)фенокси] этил-1,3-диоксо-2-изоиндолинацетата, обозначенного фталоилглицином-2959.
В трехгорлой круглодонной колбе на 250 мл, снабженной устройством для улавливания воды Дина и Старка с холодильником и двумя стеклянными пробками, смешивают следующие компоненты: 20,5 г (0,1 моль) селективного для длины волны сенсибилизатора, фталоилглицина (Aldrich Chemical Co., Milwaukee, Wisconsin); 24,6 г (0,1 моль) фотореактора, DARCUR 2959 (Ciba-Geigy, Hawthorne, New York); 100 мл бензола (Aldrich Chemical Co., Milwaukee, Wisconsin) и 0,4 г п-толуолсульфоновой кислоты (Aldrich Chemical Co., Milwaukee, Wisconsin). Смесь нагревают при кипячении с обратным холодильником в течение 3 ч, причем в течение этого времени собирают 1,8 мл воды. Растворитель удаляют при пониженном давлении, получая 43,1 г белого порошка. Порошок перекристаллизуют из 30% этилацетата в гексане (Fisher), получая 40,2 г (93%) белого кристаллического порошка, имеющего точку плавления 153-4oC. Реакцию суммируют следующим образом: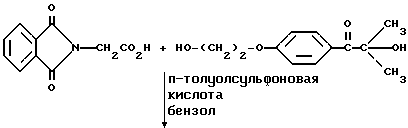
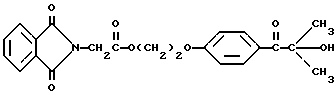
Получаемый продукт, обозначенный фталоилглицином-2959, имеет следующие физические параметры: ИК [NUJOL MULL] νmax 3440, 1760, 1740, 1680, 1600 см-1. 1H ЯМР [CDCl3] δ м.д. 1,64 [с], 4,25 [м], 4,49 [м], 6,92 [м], 7,25 [м] , 7,86 [м], 7,98 [м], 8,06 [м] м.д.
Пример 9
Этот пример описывает способ дегидратации фталоилглицина-2959, полученного в примере 8.
В круглодонной колбе на 250 мл, снабженной устройством для улавливания воды Дина и Старка с холодильником, смешивают следующие компоненты: 21,6 г (0,05 моль) фталоилглицина-2959; 100 мл безводного бензола (Aldrich Chemical Co. , Milwaukee, Wisconsin) и 0,1 г п-толуолсульфоновой кислоты (Aldrich Chemical Co., Milwaukee, Wisconsin). Смесь кипятят с обратным холодильником в течение 3 ч. После сбора в ловушке 0,7 мл воды растворитель удаляют в вакууме, получая 20,1 г (97%) белого твердого продукта. Однако анализ этого белого продукта показал, что реакция дает только от 15 до 20% целевого продукта дегидратации. Реакцию суммируют следующим образом: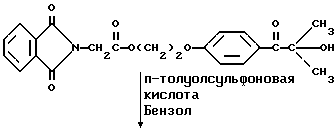
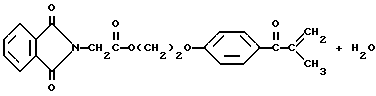
Получаемый продукт реакции имеет следующие физические параметры:
ИК [NUJOL) νmax 1617 см-1 (C=C-C=O).
Пример 10
В этом примере описывается реакция элиминирования Nohr-MacDonald, используемая для дегидратации фталоилглицина-2959, полученного в примере 8.
В круглодонную колбу на 500 мл помещают магнитную мешалку, 20,0 г (0,048 моль) фталоилглицина-2959 и 6,6 г (0,048 моль) безводного хлорида цинка (Aldrich Chemical Co. , Milwaukee, Wisconsin). Добавляют 250 мл безводного п-ксилола (Aldrich Chemical Co., Milwaukee, Wisconsin), и смесь кипятят с обратным холодильником в атмосфере аргона в течение двух часов. Реакционную смесь затем охлаждают, что приводит к образованию белого осадка, который собирают. Белый порошок затем перекристаллизуют из 20% этилацетата в гексан, получая 18,1 г (95%) белого порошка. Реакцию суммируют следующим образом: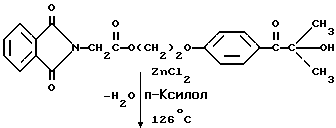
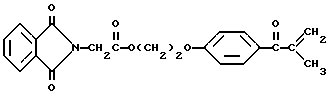
Получаемый продукт реакции имеет следующие физические параметры:
Точка плавления: от 138 до 140oC.
Масс-спектр: m/e: 393 (М+), 352, 326, 232, 160.
ИК (KBr) νmax 1758, 1708, 1677, 1600 см-1.
1H ЯМР [DMSO] δ м.д. 1,8 (с), 2,6 (с), 2,8 (д), 3,8 (д), 4,6 (м), 4,8 (м), 7,3 (м), 7,4 (м), 8,3 (м) и 8,6 (д).
13C ЯМР [DMSO] δ м.д. 65,9 (CH2=).
Пример 11
В этом примере описывается способ получения β-циклодекстрина, имеющего ковалентно связанные с ним группы дегидратированного фталоилглицина-2959 из примера 9 или 10.
В круглодонной колбе на 100 мл смешивают следующие компоненты: 5,0 г (4 ммоль) β-циклодекстрина (American Maize Product Company, Hammond, Indiana) (обозначается как β-CD в следующей реакции); 8,3 г (20 ммоль) дегидратированного фталоилглицина-2959; 50 мл безводного ДМФ; 20 мл бензола и 0,01 г п-толуолсульфонилхлорида (Aldrich Chemical Co., Milwaukee, Wisconsin). Смесь охлаждают на бане соль/лед и перемешивают в течение 24 ч. Реакционную смесь выливают в 150 мл слабого раствора бикарбоната натрия и экстрагируют три раза по 50 мл этилового эфира. Водный слой затем фильтруют, получая белый твердый продукт, содержащий β-циклодекстрин с присоединенной группой фталоилглицина-2959. Получают продукт с выходом 9,4 г. ТСХ на пластинке с обращенной фазой с использованием смеси 50:50 ДМФ/ацетонитрил показала пик нового продукта по сравнению с исходными материалами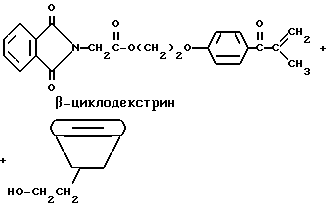
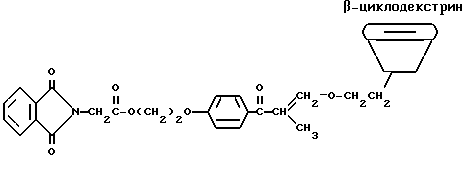
Молекула β-циклодекстрина имеет несколько первичных спиртов и вторичных спиртов, с которыми может реагировать фталоилглицин-2959. Приведенная выше реакция показывает для иллюстративных целей только одну молекулу фталоилглицина-2959.
Пример 12
В этом примере описывается способ ассоциации красителя и трансорбера ультрафиолетового излучения со средством молекулярного включения. Более особенно в этом примере описывается способ ассоциирования красителя кристаллического фиолетового со средством молекулярного включения, β-циклодекстрином, ковалентно связанным с трансорбером ультрафиолетового излучения, дегидратированным фталоилглицином-2959 примера 11.
В химический стакан на 100 мл помещают следующие компоненты: 4,0 г β-циклодекстрина, имеющего группу дегидратированного фталоилглицина-2959; и 50 мл воды. Воду нагревают до 70oC, в этой точке раствор становится прозрачным. К раствору затем добавляют 0,9 г (2,4 ммоль) кристаллического фиолетового (Aldrich Chemical Co., Milwaukee, Wisconsin), и раствор перемешивают в течение 20 мин. Затем раствор фильтруют. Осадок промывают фильтратом и затем сушат в вакуумном сушильном шкафу при 84oC. Получают фиолетово-синий порошок с выходом 4,1 г (92%). Получаемый продукт реакции имеет следующие параметры:
УФ-спектр: ДМФ νmax 610 нм (cf cv νmax 604 нм).
Пример 13
В этом примере описывается способ получения трансорбера ультрафиолетового излучения, 4-(4-гидроксифенил)бутан-2-он-2959 (хлорзамещенный).
В круглодонной колбе на 250 мл, снабженной холодильником и магнитной мешалкой, смешивают следующие компоненты: 17,6 г (0,1 моль) селективного для длины волны сенсибилизатора, 4-(4-гидроксифенил)бутан-2-она (Aldrich Chemical Company, Milwaukee, Wisconsin); 26,4 г (0,1 моль) фотореактора, хлорзамещенного DARCUR 2959 (Ciba-Geigy Corporation, Hawthorne, New York); 1,0 мл пиридина (Aldrich Chemical Company, Milwaukee, Wisconsin) и 100 мл безводного тетрагидрофурана (Aldrich Chemical Company, Milwaukee, Wisconsin). Смесь кипятят с обратным холодильником в течение 3 ч, и растворитель частично удаляют при пониженном давлении (уменьшение на 60%). Реакционную смесь затем выливают в ледяную воду и экстрагируют двумя порциями по 50 мл диэтилового эфира. После сушки над безводным сульфатом магния и удаления растворителя остается 39,1 г белого порошка. Перекристаллизация порошка из 30% этилацетата в гексане дает 36,7 г (91%) белого кристаллического порошка, имеющего точку плавления 142-3oC. Реакцию суммируют следующим образом: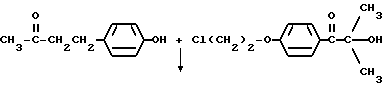
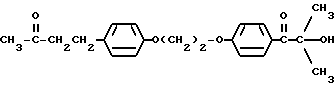
Получаемый продукт реакции имеет следующие физические параметры:
ИК [NUJOL MULL] νmax 3460, 1760, 1700, 1620, 1600 см-1
1H ЯМР [CDCl3] δ м.д. 1,62 [c], 4,2 [м], 4,5 [м], 6,9 [м] м.д.
Трансорбер ультрафиолетового излучения, полученный в этом примере, 4-(4-гидроксифенил)бутан-2-он-2959 (хлорзамещенный), можно ассоциировать с β-циклодекстрином и лейкокрасителем, таким как лейкоформа кристаллического фиолетового, с использованием способов, описанных выше, где дегидратированный фталоилглицин-2959 будет заменен на 4-(4-гидроксифенил)бутан-2-он-2959 (хлорзамещенный).
Пример 14
Получение эпоксидного промежуточного продукта дегидратированного фталоилглицина-2959
Эпоксидный промежуточный продукт дегидратированного фталоилглицина 2959 получают в соответствии со следующей реакцией: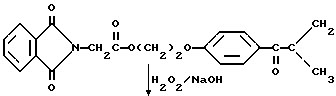
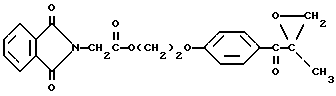
В трехгорлую круглодонную колбу на 250 мл с капельной воронкой, термометром и магнитной мешалкой помещают 30,0 г (0,076 моль) дегидратированного фталоилглицина-2959, 70 мл метанола и 20,1 мл пероксида водорода (30%-ный раствор). Реакционную смесь перемешивают и охлаждают на бане вода/лед, чтобы поддерживать температуру в диапазоне 15-20oC. В капельную воронку помещают 5,8 мл 6 н раствора NaOH, и раствор медленно добавляют в смесь, чтобы поддерживать температуру реакционной смеси 15-20oC. Эта стадия занимает около 4 мин. Смесь затем перемешивают в течение 3 ч приблизительно при 20-25oC. Реакционную смесь затем выливают в 90 мл воды и экстрагируют двумя порциями по 70 мл этилового эфира. Органические слои объединяют и промывают 100 мл воды, сушат безводным MgSO4, фильтруют, и эфир удаляют на роторном испарителе, получая белый твердый продукт (выход 20,3 г, 65%). ИК-спектроскопия показывает растяжение группы C-O-C, и этот материал используют без дальнейшей очистки.
Пример 15
Присоединение эпоксидного промежуточного продукта к тиоловому циклодекстрину
Присоединение эпоксидного промежуточного продукта дегидратированного фталоилглицина 2959 проводят в соответствии со следующей реакцией: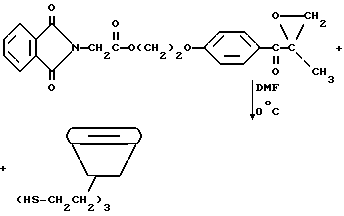
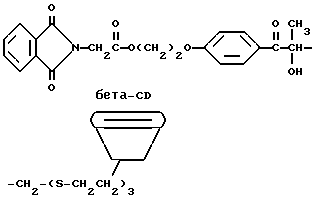
В трехгорлую круглодонную колбу на 250 мл, снабженную пробкой и двумя стеклянными пробками, причем все они скреплены медной проволокой и прикреплены к колбе каучуковыми полосками, помещают 30,0 г (0,016 моль) тиолового циклодекстрина и 100 мл безводного диметилформамида (ДМФ) (Aldrich Chemical Co., Milwaukee, Wisconsin). Реакционную смесь охлаждают на ледяной бане и добавляют 0,5 мл диизопропилэтиламина. Сероводород барботируют в колбу и положительное давление сохраняют в течение 3 ч. Во время последнего часа реакционной смеси дают нагреться до комнатной температуры.
Реакционную смесь промывают аргоном в течение 15 мин и затем выливают в 70 мл воды, к которой затем добавляют 100 мл ацетона. Происходит образование белого осадка, который отделяют фильтрованием, получая 20,2 г (84,1%) белого порошка, который используют без дальнейшей очистки.
В круглодонную колбу на 250 мл, снабженную магнитной мешалкой и помещенную на ледяную баню, помещают 12,7 г (0,031 моль), 80 мл безводного ДМФ (Aldrich Chemical Co., Milwaukee, Wisconsin) и 15,0 г (0,010 моль) тиолового CD. После охлаждения реакционной смеси добавляют 0,5 мл диизопропилэтиламина, и реакционную смесь перемешивают в течение 1 ч при температуре от 0 до 5oC и затем 2 ч при комнатной температуре. Реакционную смесь затем выливают в 200 мл ледяной воды, при этом образуется белый осадок. Этот осадок отделяют фильтрованием и промывают ацетоном. Влажный белый порошок сушат в сушильном шкафу с конвекцией при 80oC в течение 3 ч, получая белый порошок. Выход составляет 24,5 г (88%).
Пример 16
Введение Виктория чистого голубого в полость циклодекстрина
В колбу Эрленмейера на 250 мл помещают магнитную мешалку, 40,0 г (0,014 моль) соединения, полученного в примере 15, и 100 мл воды. Колбу нагревают на горячей плите до 80oC. Когда белая мутная смесь становится прозрачной, к горячему раствору добавляют 7,43 г (0,016 моль) порошка Виктория чистого голубого ВО, и смесь перемешивают в течение 10 мин, затем дают охладиться до 50oC. Твердое содержимое затем отделяют фильтрованием и промывают 20 мл холодной воды.
Осадок затем сушат в сушильном шкафу с конвекцией при 80oC в течение 2 ч, получая 27,9 г (58,1%) синего порошка.
Пример 17
Получение тозилированного циклодекстрина с присоединенным к нему дегидроксифталоилглицином 2959 проводят по следующим реакциям: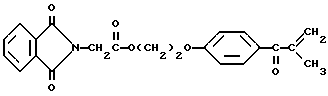
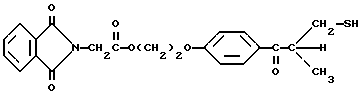
В 3-горлую круглодонную колбу на 500 мл, снабженную трубкой для барботирования, холодильником и капельной воронкой, помещают 10 г (0,025 моль) дегидратированного фталоилглицина 2959 в 150 мл безводного N,N-диэтилформамида (Aldrich Chemical Co., Milwaukee, Wisconsin), охлажденного до 0oC на ледяной бане, и перемешивают магнитной мешалкой. Синтез повторяют, за исключением того, что колбе дают нагреться вплоть до 60oC, используя теплую водяную баню, и в реакционную колбу нагнетают насосом H2S, до тех пор пока пробки не начнут двигаться (пытаясь выпустить давление). Содержимое колбы затем перемешивают в этих условиях в течение 4 ч. Насыщенный раствор выдерживают под давлением H2S. Пробки удерживаются проволочными и каучуковыми полосками. Реакционную смесь затем оставляют для нагревания в течение ночи. Раствор затем промывают аргоном в течение 30 мин, и реакционную смесь выливают на 50 г измельченного льда и экстрагируют три раза (3 х 80 мл) диэтиловым эфиром (Aldrich Chemical Co., Milwaukee, Wisconsin).
Органические слои конденсируют и промывают водой и сушат MgSO4. Удаление растворителя на роторном испарителе дает 5,2 г сырого продукта. Продукт очищают на колонке с силикагелем, используя 20%-ный этилацетат в гексане в качестве элюента. Получают 4,5 г белого твердого продукта.
Тозилированный циклодекстрин получают в соответствии со следующей реакцией: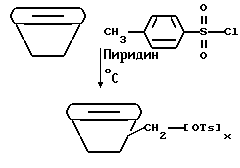
В круглодонную колбу на 100 мл помещают 6,0 г β-циклодекстрина (American Maize Product Company), 10,0 г (0,05 моль) п-толуолсульфонилхлорида (Aldrich Chemical Co. , Milwaukee, Wisconsin), 50 мл буферного раствора с pH 10 (Fisher). Получаемую смесь перемешивают при комнатной температуре в течение 8 ч, после чего ее выливают на лед (приблизительно 100 г) и экстрагируют диэтиловым эфиром. Водный слой затем выливают в 50 мл ацетона (Fisher), и получаемую мутную смесь фильтруют. Получаемый белый порошок затем пропускают через колонку с сефадексом (Aldrich Chemical Co., Milwaukee, Wisconsin) с использованием н-бутанола, этанола и воды (5:4:3, по объему) в качестве элюента, получая белый порошок. Выход его 10,9%.
Степень замещения белого порошка (тозилциклодекстрин) определяют 13C ЯМР-спектроскопией (ДМФ-d6) путем сравнения отношения гидроксизамещенных углеродов к тозилированным углеродам, оба в положении 6. Когда углерод в положении 6 имеет гидроксигруппу, пики ЯМР для каждого из шести атомов углерода даются в табл. 2.
Присутствие тозиловой группы смещает пики ЯМР атомов углерода в положении 5 и в положении 6 к 68,8 и 69,5 м.д. соответственно.
Степень замещения вычисляют интегрированием пика ЯМР для тозилированного углерода в положении 6, интегрированием пика ЯМР для гидроксизамещенного углерода в положении 6 и делением первого на последний. Интегрирования дают 23,6 и 4,1, соответственно, и степень замещения составляет 5,9. Таким образом, средняя степень замещения в этом примере около 6.
Тозилированный циклодекстрин с присоединенным к нему дегидроксифталоилглицином 2959 получают в соответствии со следующей реакцией: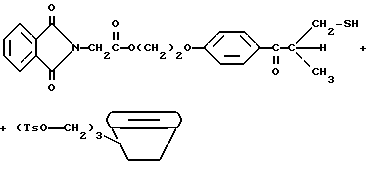
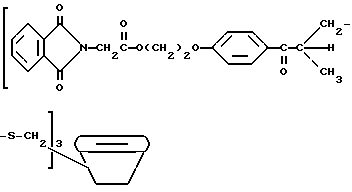
В круглодонную колбу на 250 мл добавляют 10,0 г (4,8 моль) тозилированного замещенного циклодекстрина, 20,7 г (48 ммоль) тиола (дегидратированного меркаптофталоилглицина 2959) в 100 мл ДМФ. Реакционную смесь охлаждают до 0oC на ледяной бане и перемешивают, используя магнитную мешалку. К раствору медленно прикапывают 10 мл этилдиизопропиламина (Aldrich Chemical Co., Milwaukee, Wisconsin) в 20 мл ДМФ. Реакционную смесь выдерживают при 0oC в течение 8 ч при перемешивании. Реакционную смесь экстрагируют диэтиловым эфиром. Водный слой затем обрабатывают 500 мл ацетона, и осадок отделяют фильтрованием и промывают ацетоном. Продукт затем пропускают через колонку с сефадексом с использованием н-бутанола, этанола и воды (5:4:3, по объему), получая белый порошок. Выход его 16,7 г.
Степень замещения функционализированного средства молекулярного включения определяют, как описывается выше. В этом случае присутствие дериватизированного трансорбера ультрафиолетового излучения смещает пик ЯМР атома углерода в положение 6 к 63,1. Степень замещения вычисляют интегрированием пика ЯМР для замещенного углерода в положении 6, интегрированием пика ЯМР для гидроксизамещенного углерода в положении 6 и делением первого на последний. Интегрирования дают 67,4 и 11,7 соответственно и степень замещения 5,7. Таким образом, средняя степень замещения в этом примере около 6. Приведенная выше реакция показывает, что степень замещения должна быть "n". Хотя n представляет величину замещения на одном циклодекстрине и поэтому может быть от 0 до 24, должно быть понятно, что средняя степень замещения около 6.
Пример 18
Методику примера 17 повторяют, за исключением того, что количества β-циклодекстрина и п-толуолсульфоновой кислоты (Aldrich) составляют 6,0 г и 5,0 г соответственно. Найдено, что в этом случае степень замещения циклодекстрина приблизительно 3.
Пример 19
Методику примера 17 повторяют, за исключением того, что дериватизированное средство молекулярного включения примера 18 используют вместо средства молекулярного включения примера 17. Найдено, что средняя степень замещения функционализированного средства молекулярного включения приблизительно 3.
Пример 20
В этом примере описывается получение окрашенной композиции, которая включает изменяемый краситель и функционализированное средство молекулярного включения из примера 17.
В колбу Эрленмейера на 250 мл, содержащую магнитный перемешивающий брусок, помещают 20,0 г (5,4 ммоль) функционализироанного средства молекулярного включения, полученного в примере 17, и 100 г воды. Воду нагревают до 80oC, при этой температуре получают прозрачный раствор. К раствору медленно добавляют при перемешивании 3,1 г (6,0 ммоль) Виктория чистого голубого ВО (Aldrich). Образуется осадок, который удаляют из горячего раствора фильтрованием. Осадок промывают 50 мл воды и сушат, получая 19,1 г (84%) синего порошка, окрашенной композиции, состоящей из изменяемого красителя, Виктория чистого голубого ВО, и средства молекулярного включения, имеющего ковалентно связанные с ним приблизительно шесть молекул трансорбера ультрафиолетового излучения на молекулу средства молекулярного включения.
Пример 21
Методику примера 20 повторяют, за исключением того, что функционализированное средство молекулярного включения из примера 19 используют вместо средства молекулярного включения из примера 17.
Пример 22
В этом примере описываются скорости изменения или обесцвечивания для композиций примеров 12 (где β-циклодекстрин имеет дегидратированный фталоилглицин-2959 из примера 9, ковалентно соединенный с ним), 20 и 21.
В каждом случае приблизительно 10 мг композиции помещают на стальную пластину (Q-Panel Company, Cleveland, Ohio). Наверх композиции помещают три капли (около 0,3 мл) ацетонитрила (Burdick and Jackson, Muskegon, Michigan), и два материала быстро перемешивают шпателем и распределяют на пластине в виде тонкой пленки. В пределах 5-10 с после добавления ацетонитрила каждую пластину подвергают воздействию излучения от комплекта ламп возбуждения на 222 нм. Комплект состоит из ряда четырех цилиндрических ламп, имеющих длину около 30 см. Лампы охлаждают циркулированием воды через расположенную в центре или внутреннюю трубку лампы, и вследствие этого они функционируют при относительно низкой температуре, т. е. приблизительно при 50oC. Плотность энергии у наружной поверхности ламп обычно находится в диапазоне от около 4 до около 20 Дж/м2. Однако такой диапазон в действительности отражает только возможности поставки потока энергии лампы возбуждения; в будущем могут быть выгодными более высокие плотности энергии. Расстояние от лампы до облучаемого образца составляет 4,5 см. Для каждой пленки измеряют время, когда она становится бесцветной для глаз. Результаты суммированы в табл. 3.
Несмотря на то что данные в табл. 3 демонстрируют полное превосходство окрашенных композиций по настоящему изобретению, такие данные были нанесены на график как степень замещения в зависимости от времени обесцвечивания. Этот график не только демонстрирует значительное усовершенствование окрашенных композиций по настоящему изобретению по сравнению с композициями, имеющими степень замещения меньше трех, но также показывает, что степень замещения около 6 является почти оптимальной. То есть небольшое усовершенствование, если оно вообще будет иметь место, по времени обесцвечивания будет достигнуто при степенях замещения выше чем около 6.
Пример 23
В этом примере описывается получение комплекса, состоящего из изменяемого красителя и дериватизированного средства молекулярного включения примера 17.
Методику примера 20 повторяют, за исключением того, что функционализированное средство молекулярного включения примера 17 заменяют на 10 г (4,8 ммоль) дериватизированного средства молекулярного включения примера 17 и количество Виктория чистого голубого ВО снижают до 2,5 г (4,8 ммоль). Выход промытого твердого продукта составляет 10,8 г (86%), продукт является изменяемым красителем, ассоциированным с β-циклодекстрином, имеющим в среднем шесть тозиловых групп на молекулу средства молекулярного включения.
Пример 24
В этом примере описывается получение окрашенной композиции, которая включает изменяемый краситель и функционализированное средство молекулярного включения.
Методику получения функционализированного средства молекулярного включения примера 17 повторяют, за исключением того, что тозилированный β-циклодекстрин заменяют на 10 г (3,8 ммоль) комплекса, полученного в примере 23, и количество дериватизированного трансорбера ультрафиолетового излучения, полученного в примере 17, составляет 11,6 г (27 ммоль). Количество полученной окрашенной композиции составляет 11,2 г (56%). Среднюю степень замещения определяют, как описывается выше, и было найдено, что она составляет 5,9 или приблизительно 6.
Пример 25
В этом примере описывается способ получения следующего прекрасителя по настоящему изобретению, где X представляет фотоинициатор или где X представляет специфический для длины волны сенсибилизатор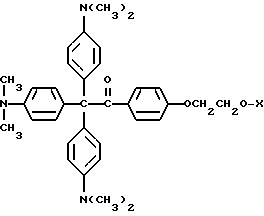
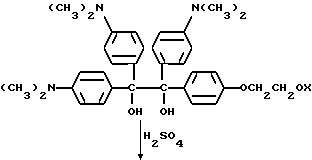
Методику примеров 1 и 2 повторяют, за исключением того, что гидроксиэтоксидиметиламинобензофенон примера 1 заменяют на X-оксиэтоксидиметиламинобензофенон. Реакцию суммируют следующим образом: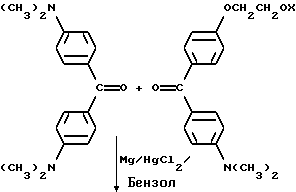
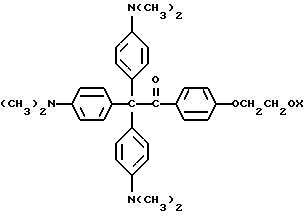
Пример 26
В этом примере описывается получение следующего прекрасителя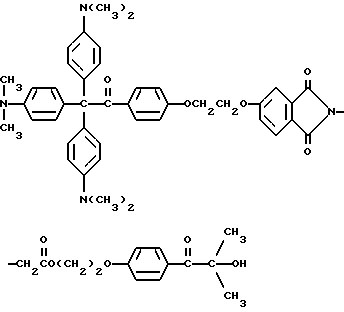
Указанный выше прекраситель получают, как суммировано ниже в стадиях A, B и C.
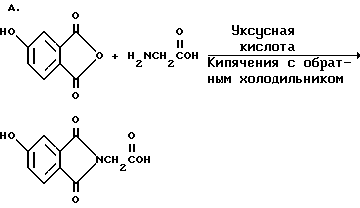
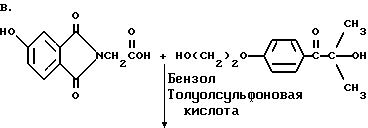
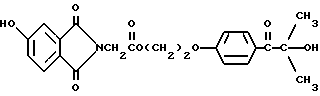
Триарилметановый продукт, полученный в примере 2, подвергают реакции с продуктом реакции стадии B, как суммировано в приведенной ниже стадии C реакции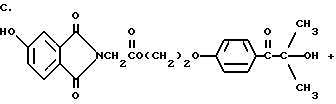
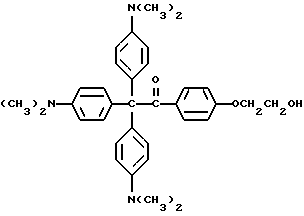
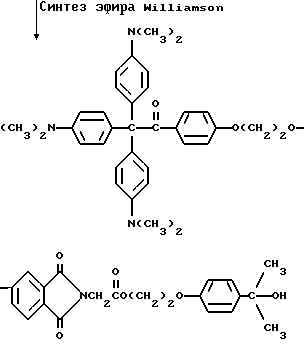
Пример 27
В этом примере описывается получение следующего прекрасителя, где X представляет трансорбер излучения и где R представляет водород, метильную или этильную группу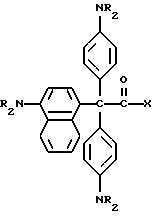
Методику примеров 1 и 2 повторяют, за исключением того, что гидроксиэтоксидиметиламинобензофенон и бис-диметиламинобензофенон примера 1 заменяют реагентами в реакции, суммированной следующим образом: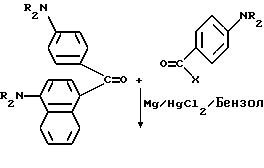
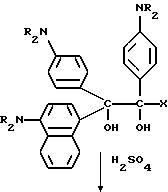
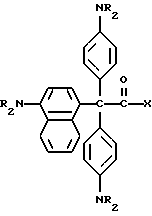
Поскольку имеется таким образом описанное изобретение, различные изменения и модификации его легко будут очевидны специалистам данной области.



Изобретение относится к стабильным к воздействию света красителям, которые могут быть использованы в способах печати, получения фотоизображений, системах безопасности. Описывается композиция прекрасителя, содержащая молекулу прекрасителя, включающую краситель, ковалентно связанный с трансорбером излучения, образованным из селективного для длины волны сенсибилизатора, ковалентно связанного с фотореактором, генерирующим реакционную способность молекулы, причем молекула прекрасителя является бесцветной и образовывает цвет при обработке излучением. Технический результат: достижение стабильности красителя к действию света. 4 с. и 21 з.п. ф-лы, 3 табл.
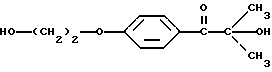
или 1-гидроксициклогексанфенилкетон, имеющий следующую формулу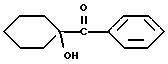
4. Композиция прекрасителя по п.1, отличающаяся тем, что селективный для длины волны сенсибилизатор представляет фталоилглицин, имеющий формулу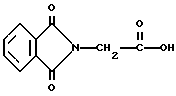
или 4-(4-гидроксифенил)бутан-2-он, имеющий следующую формулу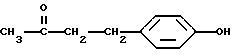
5. Композиция прекрасителя по п. 1, отличающаяся тем, что трансорбер излучения представляет 2-(п-(2-метиллактоил)фенокси)этил-1,3-диоксо-2-изоиндолинацетат, имеющий формулу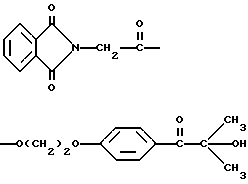
эфир фталоилглицилциклогексилфенилкетона, имеющий формулу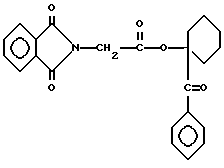
2-гидрокси-2-метил-4'-(2-(п-(3-оксобутил)фенокси)этокси)пропиофенон, имеющий формулу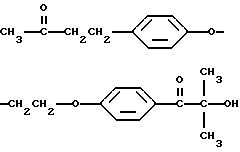
или 4-(п-((4-бензоилциклогексил)окси)фенил)-2-бутанон, имеющий формулу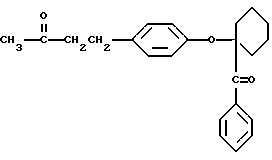
6. Композиция прекрасителя по п. 1, отличающаяся тем, что краситель представляет кристаллический фиолетовый и молекула прекрасителя имеет следующую формулу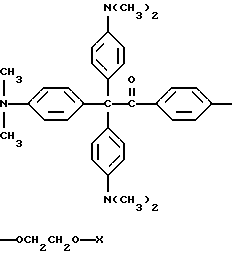
где X представляет трансорбер излучения.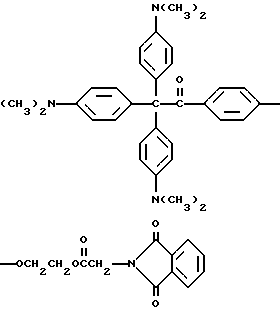
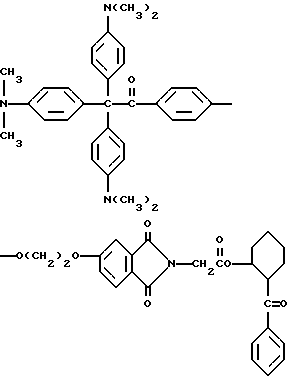
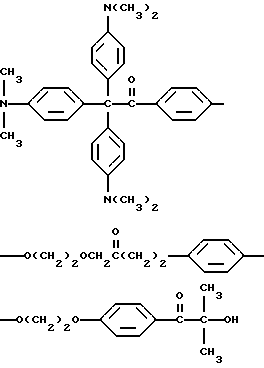
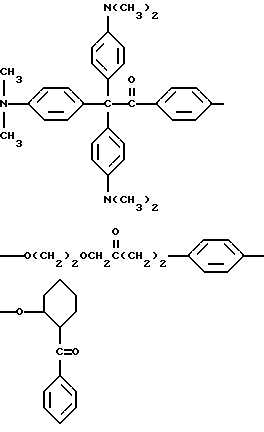
или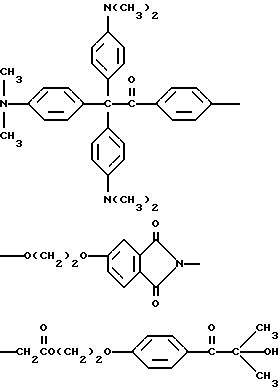
8. Композиция прекрасителя по п. 1, отличающаяся тем, что молекула прекрасителя имеет формулу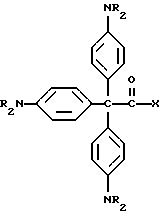
или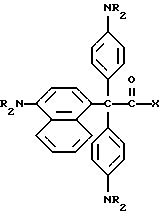
где X представляет трансорбер излучения;
R представляет водород, метильную или этильную группу.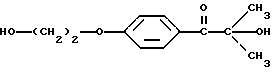
или 1-гидроксициклогексанфенилкетон, имеющий следующую формулу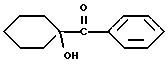
12. Способ по п. 9, отличающийся тем, что селективный для длины волны сенсибилизатор представляет фталоилглицин, имеющий следующую формулу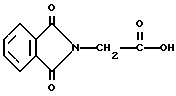
или 4-(4-гидроксифенил)бутан-2-он, имеющий следующую формулу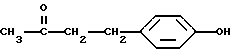
13. Способ по п. 9, отличающийся тем, что трансорбер излучения представляет собой 2-(п-(2-метиллактоил)фенокси)этил-1,3-диоксо-2-изоиндолинацетат, имеющий формулу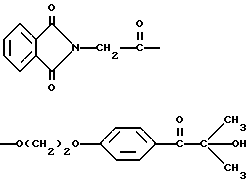
эфир фталоилглицилциклогексилфенилкетона, имеющий формулу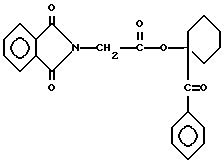
2-гидрокси-2-метил-4'-(2-(п-(3-оксобутил)фенокси)этокси)пропиофенон, имеющий формулу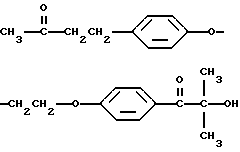
или 4-(п-((4-бензоилциклогексил)окси)фенил)-2-бутанон, имеющий формулу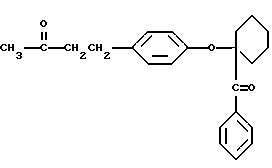
14. Способ по п.9, отличающийся тем, что краситель представляет собой кристаллический фиолетовый и молекула прекрасителя имеет следующую формулу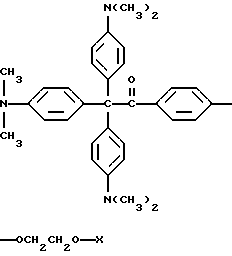
где X представляет трансорбер излучения.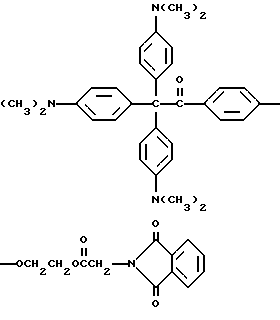
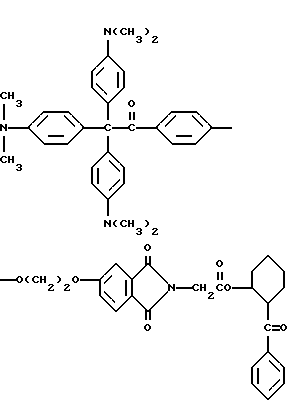
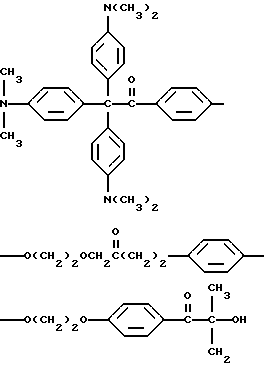
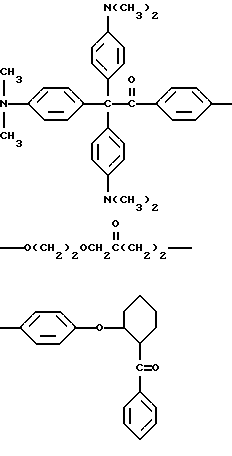
или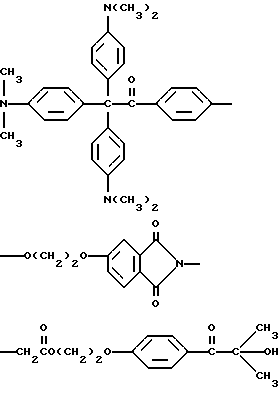
16. Композиция изменяемого красителя, содержащая лейкокраситель, смешанный с трансорбером излучения, содержащим селективный для длины волны сенсибилизатор, ковалентно связанный с фотореактором, генерирующим реакционноспособную разновидность молекулы.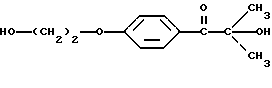
или 1-гидроксициклогексанфенилкетон, имеющий формулу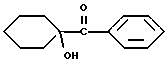
19. Композиция изменяемого красителя по п.16, отличающаяся тем, что селективный для длины волны сенсибилизатор представляет фталоилглицин, имеющий следующую формулу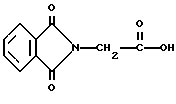
или 4-(4-гидроксифенил)бутан-2-он, имеющий следующую формулу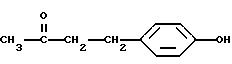
20. Композиция изменяемого красителя по п.16, отличающаяся тем, что трансорбер излучения представляет собой 2-(п-(2-метиллактоил)фенокси)-этил-1,3-диоксо-2-изоиндолинацетат, имеющий формулу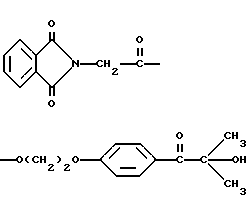
эфир фталоилглицилциклогексилфенилкетона, имеющий формулу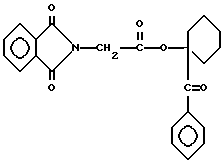
или 2-гидрокси-2-метил-4'-(2-(п-(3-оксобутил)фенокси)этокси)пропиофенон, имеющий формулу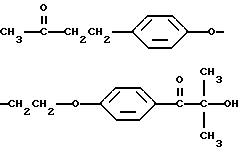
или 4-(п-((4-бензоилциклогексил)окси)фенил)-2-бутанон, имеющий формулу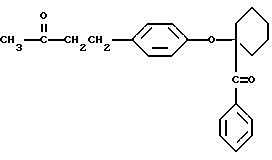
21. Способ проявления цвета композиции, содержащей лейкокраситель и трансорбер излучения путем обработки излучением при длине волны и уровне дозировки, достаточных для необратимого изменения лейкокрасителя, отличающийся тем, что используют композицию по п.16.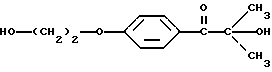
или 1-гидроксициклогексанфенилкетон, имеющий следующую формулу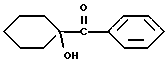
24. Способ по п.21, отличающийся тем, что селективный для длины волны сенсибилизатор представляет собой фталоилглицин, имеющий следующую формулу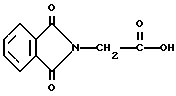
или 4-(4-гидроксифенил)бутан-2-он, имеющий следующую формулу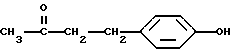
25. Способ по п.21, отличающийся тем, что трансорбер излучения представляет собой 2-(п-(2-метиллактоил)фенокси)-этил-1,3-диоксо-2-изоиндолинацетат, имеющий формулу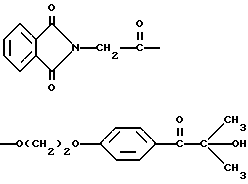
эфир фталоилглицилциклогексилфенилкетона, имеющий формулу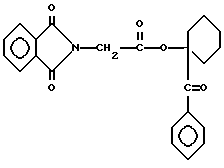
2-гидрокси-2-метил-4'-(2-(п-(3-оксобутил)фенокси)этокси)пропиофенон, имеющий формулу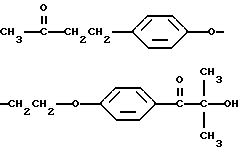
или 4-(п-((4-бензоилциклогексил)окси)фенил)-2-бутанон), имеющий формулу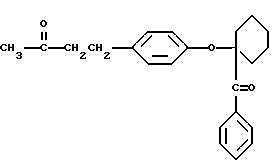
Приоритет по пунктам:
05.06.95 - по пп.1 - 5, 9 и 16 - 21;
29.05.96 - по пп.1 - 25.
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| ЕЛЬЦОВ А.В | |||
| Органические фотохромы | |||
| - Л.: Химия, 1982, с.3 - 5. | |||
Авторы
Даты
2001-07-20—Публикация
1996-06-05—Подача