Изобретение относится к области технологии получения лекарственных препаратов, а именно к способу получения производных (солей, эфиров или амидов) замещенных 2- (фениламино)фенилуксусной кислоты, которые могут быть использованы в качестве препаратов различного назначения (например, натриевая, рубидиевая или цезиевая соли 2-(2,6-дихлорфениламино)фенилуксусной кислоты являются анальгезирующими, противовоспалительными, противоревматическими средствами; цинковая соль обладает наряду с перечисленными свойствами также и противоязвенным действием).
Известно несколько способов получения производных 2- (фениламино)фенилуксусной кислоты, причем практически во всех описанных способах ключевым промежуточным продуктом является соответствующий дифениламин.
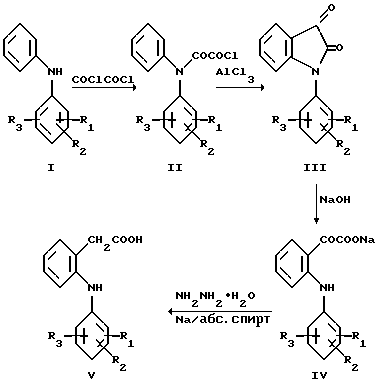
Так, например, один из способов получения замещенных 2- (фениламино)-фенилуксусной кислоты (V), где R1 = низший алкил или алкоксигруппа, галоген, трифторметильная группа; R2, R3 = водород, низший алкил, галоген (см. Швейц. пат N 485667, кл. C 07 C 101/44, 1970) включает ацилирование соответствующего дифениламина (I) оксалилхлоридом, внутримолекулярную циклизацию получающегося при этом соединения (II), гидролиз 1-фенилиндолин-2,3-диона (III) и последующее восстановление карбонильной группы в образующемся соединении (IV) гидразингидратом в присутствии металлического натрия с образованием замещенной 2-(фениламино)фенилуксусной кислоты (V), на базе которой могут быть получены различные производные, в частности натриевая соль 2-(2,6- дихлорфениламино)фенилуксусной кислоты, представляющая собой известный препарат ортофен.
К числу недостатков указанного способа относится необходимость работы с оксалилхлоридом, низкая стабильность которого является одной из причин низкого выхода и плохого качества промежуточного ацильного производного (II), что в свою очередь оказывает влияние на выход и качество конечной кислоты (V).
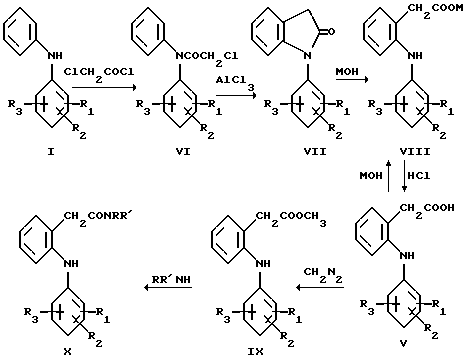
Наиболее близким по технической сущности является способ получения производных замещенной 2-(фениламино)фенилуксусной кислоты, в частности 2-(фениламино)-фенилацетамидов (X) (см. Швейц. пат. N 473770, кл. C 07 C 103/06, 1969), который предполагает хлорацетилирование дифениламина (I) до хлорацетильного производного (VI), внутримолекулярную циклизацию N-хлорацетилдифениламина (VI), гидролиз 1-фенилиндолин-2-она (VII) и выделение 2- (фениламино)фенилуксусной кислоты (V), этерификация которой с последующей обработкой образующегося эфира (IX) амином приводит к получению соответствующих амидов (X).
К числу недостатков указанного способа относится низкий выход целевых проектов (V), (IX) и (X). Так, например, выход 2-(2,6- дихлорфениламино)фенилуксусной кислоты (V, R1=2-Cl, R2=6-Cl, R3=Н) составляет около 35% в пересчете на исходный дифениламин. Недостатком указанного способа является также использование большого объема хлорацетилхлорида (30 молей на 1 моль дифениламина).
Кроме того, полученные по известному способу (см. Швейц. пат. N 473770, кл. C 07 C 103/06, 1969) продукты (V), (IX) и (X) имеют неудовлетворительное качество, обусловленное наличием примесей.
Задачей настоящего изобретения является повышение выхода и получение более чистых производных 2-(фениламино)фенилуксусной кислоты, включая препараты на основе неорганических, органических или смешанных солей 2-(2,6-дихлорфениламино)-фенилуксусной кислоты общей формулы (VIII, R1=2-Cl, R2= 6-Cl, R3=H), например, натриевой соли, известной как препарат ортофен (VIII, M=Na).
Поставленная задача решается благодаря тому, что:
- количество хлорацетилхлорида при получении замещенного N-хлорацетилдифенилдиамина (Vl) не превышает 5 молей на 1 моль исходного дифениламина, причем хлорацетилирование проводят либо в среде хлорацетилхлорида, либо в среде органического растворителя, объем которого не превышает 4 объемов самого хлорацетилхлорида;
- после гидролиза индолинона (VII) осуществляют промежуточное выделение из водно-спиртовой среды соли производного 2- (фениламино)фенилуксусной кислоты (VIII), для чего используют смесь смешивающегося и несмешивающегося с водой растворителей.
Циклизация N-хлорацетилфениламинов (VI) может быть осуществлена в плаве хлористого алюминия или смеси хлористого алюминия и хлористого натрия.
Гидролиз 1-(фенил)индолин-2-она (VII) осуществляют водно-спиртовой щелочью. В качестве спирта могут быть использованы метанол, этанол, пропиловый или изопропиловый спирты. В качестве основания могут быть использованы гидроокиси щелочных, щелочноземельных металлов и магния.
Дополнительная очистка солей (VIII) может быть осуществлена перекристаллизацией из водного или водно-спиртового раствора при pH= 6-11.
Для получения и очистки неорганических (цинковых и т.п.), органических (например, замещенных аммониевых) или смешанных солей производных 2-(фениламино)-фенилуксусной кислоты (VIII) могут быть также использованы стандартные процессы мембранной технологии, например ультра- и диафильтрации, обратного осмоса. При этом могут быть использованы полиамидные, поливинилсульфоновые, полисульфоновые, на основе регенерированной целлюлозы мембраны с номинальной задерживающей способностью 500-1000D.
Для перевода 2-(фениламино)фенилуксусной кислоты (V) в различные соли (VIII) используют также обычные методы, например нейтрализацию ее соответствующими основаниями или их смесями.
Существенным отличием настоящего изобретения является значительное снижение количества хлорацетилхлорида по отношению к дифениламину на стадии хлорацетилирования. Это обеспечивает повышение выхода и качества не только промежуточного хлорацетильного производного (VI), но и целевых продуктов (V), (VIII), (IX) и (X). Хлорацетилирование дифениламина (I) может быть осуществлено при этом либо в среде хлорацетилхлорида, либо в среде органического растворителя, объем которого не превышает 4 объемов самого хлорацетилхлорида.
В отличие от прототипа особенностью настоящего изобретения является также промежуточное выделение соли (VIII) из водно-спиртового раствора в присутствии несмешивающегося с водой органического растворителя, что обеспечивает высокую степень чистоты соединения (VIII) и за счет этого высокое качество кислоты (V) и ее производных типа (IX) и (X).
Содержание основного вещества в указанных продуктах может быть при необходимости увеличено за счет дополнительной перекристаллизации.
Перевод образующейся после гидролиза соли (VIII) в свободную кислоту может быть осуществлен стандартным способом, например подкислением водного раствора соли соляной кислотой до pH=0-2. В свою очередь на основе кислоты (V) необходимые производные (IX), (X) и соли (VIII) 2-(фениламино)фенилуксусной кислоты могут быть синтезированы известными способами (см. например, Швейц. пат. N 473770, кл. C 07 C 103/06, 1969; Европ. пат. N 521393, кл. C 07 C 229/42, 1993; Европ. пат. N 400558, кл. C 07 C 229/42, 1994; Европ. пат. N 498011, кл. C 07 C 229/58, 1992).
Настоящее изобретение иллюстрируется следующими примерами.
I. Синтез 2-(фениламино)фенилуксусной кислоты (V).
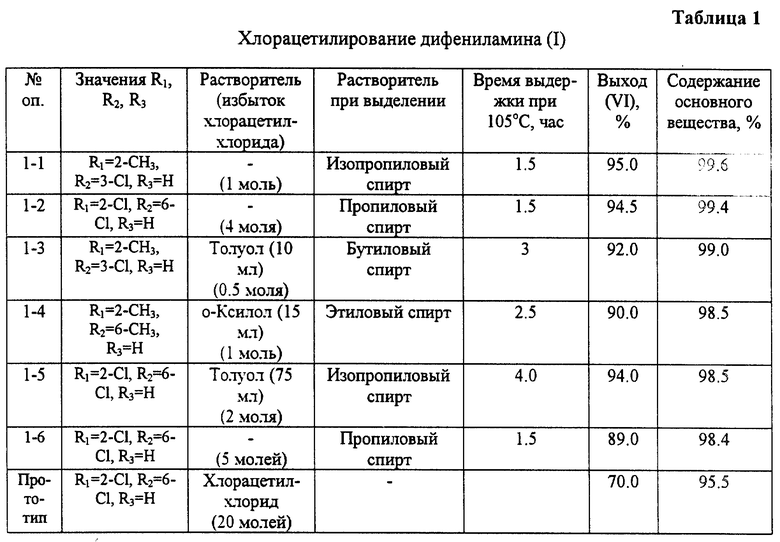
1. Хлорацетилирование дифениламина (I).
20,9 г (0.088 моля) 2,6-дихлордифениламина (I, R1=2-Cl, R2=6-Cl, R3=H) и 14.5 мл (0.125 моля) хлорацетилхлорида нагревают в течение часа при перемешивании до 105oC и при этой температуре перемешивают еще 2,5 часа. Далее температуру реакционной массы снижают до 70-75oC, прикапывают в течение 15 минут 44 мл изопропилового спирта и кипятят в течение одного часа. Полученную суспензию охлаждают до 18-20oC, кристаллический осадок отфильтровывают, отжимают на фильтре, промывают в три приема 16,5 мл изопропилового спирта. Осадок сушат при 100oC и получают 26,2 г (96%) N-хлорацетил-2,6-дихлордифениламина (VI, R1=2-Cl, R2=6-Cl, R3=Н), представляющего собой кристаллический порошок бежевого цвета, имеющий после перекристаллизации из метанола т.пл. 145-146oC.
Аналогичным образом осуществляют хлорацетилирование других замещенных дифениламинов. Вместо хлорацетилхлорида используют также смесь хлорацетилхлорида с растворителем, объем которого не превышает 4 объемов хлорацетилхлорида. При выделении вместо изопропилового спирта может быть использован метиловый, этиловый, пропиловый, изопропиловый или бутиловый спирты (см. табл. 1).
5. Циклизация N-хлорацетилдифениламинов (VI).
9,5 г (0.03 г-моля) N-хлорацетил-2,6-дихлордифениламина (VI, R1=2-Cl, R2= 6-Cl, R3=Н) и 6,48 г (0.049 г-моля) хлористого алюминия в течение 20 минут нагревают до 130-138oC и далее при перемешивании нагревают до 150oC в течение 2 часов. Затем реакционную массу охлаждают до 100-110oC, выливают на 300 мл горячего (70-80oC) раствора 5%-ной уксусной, или серной, или соляной кислоты. Полученную массу перемешивают 10 минут, суспензию фильтруют, осадок промывают 180 мл воды в три приема. После перекристаллизации из метанола получают 16,4 г (95%) 1-(2,6- дихлорфенил)индолин-2-она (VII, R1=2-Cl, R2=6-Cl, R3=Н) с т. пл. 126-127oC.
Аналогичным образом проводят циклизацию других замещенных N-хлорацетилдифениламинов, в том числе при использовании смеси хлористого алюминия с хлористым натрием.
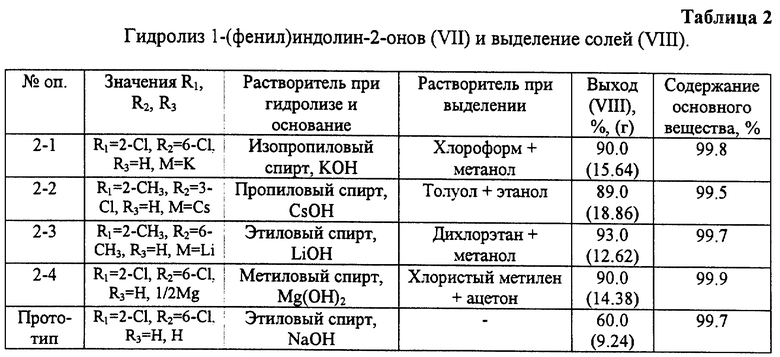
6. Гидролиз 1-фенилиндолин-2-онов (VII) и выделение солей (VIII).
14,6 г 1-(2,6-Дихлорфенил)индолин-2-она (VII, R1=2-Cl, R2=6-Cl, R3=Н) растворяют в смеси 200 мл изопропилового (или пропилового, этилового, метилового) спирта, добавляют при нагревании 4,2 г едкого натра и 130 мл воды и кипятят около 5-ти часов до отсутствия исходного вещества в пробе по ТСХ. После завершения реакции отгоняют около 220 мл азеотропной смеси спирта с водой и в образовавшуюся массу при температуре около 80oC приливают смесь 32 мл хлороформа и 5 мл метанола, перемешивают около 5-ти минут, охлаждают до 10-15oC и фильтрацией образовавшейся суспензии выделяют продукт реакции. Осадок промывают в три приема смесью 23 мл хлороформа и 3 мл метанола, после чего перекристаллизацией из смеси п-ксилолизопропиловый спирт-вода в соотношении 3: 1: 1 и из воды получают натриевую соль 2 (2,6-дихлорфениламино)фенилуксусной кислоты (VIII, R1=2-Cl, R2=6-Cl, R3=H, M=Na) с выходом 92% или 15.36 г при содержании основного вещества 99.9% в расчете на исходный 1 -(2,6-дихлорфенил)индолин-2-он.
Аналогичным образом при использовании других замещенных 1- (фенил)индолин-2-онов (VII) и оснований получают соответствующие соли (VIII). При выделении после гидролиза может быть использована смесь других органических растворителей, варианты которых представлены в таблице 2.
Содержание солей замещенной 2-(фениламино)фенилуксусной кислоты (VIII), то есть чистота продукта, определялось методом высокоэффективной жидкостной хроматографии (ВЭЖХ) с использованием колонки Nucleosil 10 C18 в системе метанол-0.1% орто-фосфорная кислота (60:40).
Контроль за протеканием реакции гидролиза 1-фенилиндолин-2- она (VII) осуществлялся методом ТСХ на пластинах Silufol UV 254, элюент бензол:хлороформ=2:1. Для проведения контроля методом ТСХ реакционную массу подкисляют и экстрагируют эфиром. При проведении реакции по предлагаемому способу получают продукт, который содержит по данным ТСХ только пятно замещенной 2- (фениламино)фенилуксусной кислоты с Rf= 0.1-0.15, тогда как по прототипу продукт содержит по данным ТСХ наряду с замещенной 2- (фениламино)фенилуксусной кислотой пятно 1-фенилиндолин-2-она (VII) с Rf= 0.35-0.56.
7. Получение замещенной 2-(фениламино)фенилуксусной кислоты (V).
0.05 моля натриевой (литиевой, калиевой и т.п.) соли 2-(фениламино)фенилуксусной кислоты растворяют в 150 мл дистиллированной воды, полученный раствор подвергают очистной фильтрации, после чего фильтрат подкисляют с помощью соляной кислоты до величины pH~1-2. Выпавший осадок отфильтровывают, промывают дистиллированной водой и в случае необходимости перекристаллизовывают из хлороформа. Выход соответствующей 2-(фениламино)фенилуксусной кислоты с содержанием основного вещества 99.5-99.9% составляет не менее 99% или 14.66 г для случая натриевой соли 2-(2,6-дихлорфениламино)фенилуксусной кислоты (VIII, R1=2-Cl, R2=6-Cl, R3=H, M=Na).
8. Получение солей замещенной 2-(фениламино)фенилуксусной кислоты (VIII).
Соли получают по известной методике (см. например, Европ. пат. N 521393, кл. C 07 C 229/42,1993; Европ. пат. N 400558, кл. C 07 C 229/42, 1994; Европ. пат. N 498011, кл. C 07 C 229/58,1992).
9. Получение метилового эфира замещенной 2-(фениламино)фенилуксусной кислоты (IX).
Продукт получают по известной методике (см. Швейц. пат. N 473770, кл. C 07 C 103/06, 1969) обработкой соответствующей кислоты (V) диазометаном в абсолютном эфире.
10. Получение амидов замещенной 2-(фениламино)фенилуксусной кислоты (X).
Амиды получают по известной методике (см. Швейц. пат. N 473770, кл. C 07 C 103/06, 1969) обработкой соответствующего метилового эфира (IX) подходящими аминами.
Таким образом, заявляемый способ обеспечивает получение производных 2-(фениламино)фенилуксусной кислоты с более высоким выходом (89-93%) по сравнению с прототипом (60%) при одновременном улучшении качества (отсутствие примесей по ТСХ).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННОГО ДИФЕНИЛАМИНА | 1999 |
|
RU2178784C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ФЕНИЛУКСУСНОЙ КИСЛОТЫ | 2000 |
|
RU2273628C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 2-(ФЕНИЛАМИНО)-2-ИМИДАЗОЛИНОВ | 1997 |
|
RU2131872C1 |
| ПОЛЯРИЗАТОР | 1999 |
|
RU2152634C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЮМИНИЕВЫХ И ГАЛЛИЕВЫХ КОМПЛЕКСОВ ФТАЛОЦИАНИНФОСФОНОВЫХ КИСЛОТ | 1999 |
|
RU2181735C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БЕНЗИДИНА | 2004 |
|
RU2260583C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФОЗАМЕЩЕННЫХ ФТАЛОЦИАНИНОВ | 1999 |
|
RU2181736C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ТРАНС-6-[2-ЗАМЕЩЕННЫЙ-ПИРРОЛ-1-ИЛ)АЛКИЛ]-ПИРАН-2-ОНА, ИХ ДИГИДРОКСИСОДЕРЖАЩИХ КИСЛОТ И СОЛЕЙ, ГИДРОКСИ- ИЛИ 1,3-ДИОКСАН ИЛИ ПИРРОЛСОДЕРЖАЩИЕ КАРБОНОВЫЕ КИСЛОТЫ В КАЧЕСТВЕ ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ ДЛЯ ПОЛУЧЕНИЯ УКАЗАННЫХ ПРОИЗВОДНЫХ ПИРАН-2-ОНА | 1994 |
|
RU2138497C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3,4-ДИАЛКОКСИБЕНЗИЛЦИАНИДА | 1998 |
|
RU2149868C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,6-ДИХЛОРДИФЕНИЛАМИНА | 1992 |
|
RU2061676C1 |
Изобретение относится к области технологии получения лекарственных препаратов, а именно к способу получения производных (солей, эфиров или амидов) замещенных 2-(фениламино)фенилуксусной кислоты, которые могут быть использованы в качестве препаратов различного назначения. Описывается способ получения производного 2-(фениламино)фенилуксусной кислоты, включающий хлорацетилирование хлорацетилхлоридом замещенного дифениламина, внутримолекулярную циклизацию полученного N-хлорацетилдифениламина, гидролиз 1-фенилиндолин-2-она, выделение соответствующей 2-(фениламино)-фенилуксусной кислоты, этерификацию и реакцию с аминами. Отличие способа состоит в том, что при хлорацетилировании количество хлорацетилхлорида не превышает 5 молей на 1 моль дифениламина. После гидролиза в водно-спиртовой среде осуществляют промежуточное выделение соли производного 2-(фениламино)фенилуксусной кислоты, для чего используют смесь смешивающегося и несмешивающегося с водой растворителей. Технический результат - получение целевых продуктов с более высоким выходом при одновременном улучшении качества. 2 з.п.ф-лы, 2 табл.
| Экранирующее устройство | 1973 |
|
SU473770A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2-АНИЛИНОНИКОТИНО- ВОЙ или N-ФЕНИЛАНТРАНИЛОВОИ КИСЛОТ ИЛИ ИХ СОЛЕЙ | 0 |
|
SU365884A1 |
| ПРОИЗВОДНЫЕ 2-(2,6-ДИГАЛОФЕНИЛАМИНО)ФЕНИЛУКСУСНОЙ КИСЛОТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2109009C1 |
| Устройство для определения газовыделения из отбитого угля | 1971 |
|
SU521393A1 |
| Кристаллизатор | 1974 |
|
SU498011A1 |
| Экономайзер | 0 |
|
SU94A1 |
Авторы
Даты
2001-08-20—Публикация
1999-10-06—Подача