В нормальной ткани имеется равновесие между синтезом и деградацией. Внеклеточный матрикс деградирует под воздействием протеаз, которые относятся по меньшей мере к трем группам матричных металлопротеаз. Это коллагеназы, желатиназы и стромлизины. В норме имеются специфические ингибиторы этих катаболических ферментов такие, как α2 макроглобулины и ММР (=тканевый ингибитор металлопротеаз ММР), таким образом, избыточная деградация внеклеточного матрикса не происходит. Относящейся к протеазам группой являются адамализины. Известным членом группы адамализинов является ТАСЕ (TNF-α-конвертирующий фермент).
Охарактеризовано, по меньшей мере 11 различных и все же высокогомологичных видов ММР, включая интерстициальную коллагеназу фибробластов (MMP-1, HFC), нейтрофильную коллагеназу (ММР-8, HNC), две желатиназы, стромлизины (такие, как HSL-1) и HPUMP (в качестве недавнего обзора смотри Birkedal-Hansen, Н. , Moore, W.G.I., Bodden, М.К., Windsor, L.J., Birkedal-Hansen, В., DeCarlo, A., Engler, J.A., Critical Rev. Oral Biol. Med. (1993), 4, 197-250. Эти протеиназы имеют ряд одинаковых структурных и функциональных признаков, но различаются в их специфичности в отношении субстрата. Только HNC и HFC способны к расщеплению нативных трехспиральных коллагенов типа I, II и III по одной связи с образованием фрагментов, составляющих 3/4 и 1/4 длины нативной цепи. Это приводит к понижению температуры плавления коллагенов и делает их доступными для последующего воздействия других матричных расщепляющих ферментов.
Однако неконтролируемая избыточная деградация этого матрикса представляет собой характерную черту многих патологических состояний, например, входит в клиническую картину ревматоидного артрита, остеоартрита, множественного склероза, имеет место при образовании метастазов опухоли, язве роговицы, воспалительных заболеваниях и инвазиях, а также при заболеваниях костей и зубов.
Можно предположить, что введение ингибиторов матричных металлопротеаз будет благоприятно сказываться на патогенезе этих заболеваний. В настоящее время ряд соединений известен в литературе (см., например, обзорную статью Nigel R.A., Beeley et al. Curr. Opin ther. Patents 4 (1), 7, (1994), или они описаны в патентной литературе, в основном это пептиды с остатком гидроксамовой кислоты, тиолом или фосфиновой группой в качестве группы, связывающей цинк, (см. , например, среди других WO-A-9260/9563 от Glycomed, ЕР-А-497192 от Hoffman-LaRoche, WO-A-9005719 от British Biotechnology, EP-A-489577 от Celltech, EP-A-320118 от Beecham, US-A-4595700 от Searle).
Некоторые из этих соединений имеют высокую активность в качестве ингибиторов матричных металлопротеаз, но только обладают очень низкой оральной доступностью. Было обнаружено, что заявленные новые производные барбитуровой кислоты очень эффективны в качестве ингибиторов матричных металлопротеаз и имеют хорошую оральную доступность.
Следовательно, настоящее изобретение относится к веществам общей формулы I
в которой X, Y и Z являются кислородом,
R1 представляет группу W-V, в которой
W является валентной связью или прямой или разветвленной C1-C4-алкильной группой,
V является моноциклом, выбранным из фенила, необязательно замещенного гидрокси, низшим алкилом, низшим алкокси, фенилом, фенокси; пиридила, пиперидинила, тиофенила, имидазолила или бициклом, выбранным из нафтила, хинолинила, тетрагидрохинолила, тетрагидроизохинолила, бензимидазолила, индолила, каждый из которых может быть замещен, или
W-V является С1-С20-алкильной группой, необязательно замещенной аминогруппой, гидрокси, низшей ациламиногруппой, карбоксигруппой, аминокарбонилом, низшим алкиламинокарбонилом, аминокарбонил-низшималкиламинокарбонилом, низшим алкилом, низшим алкоксилом, низшим алкоксиалкоксилом,
R2 и R3 оба являются водородом,
R4 и R5 обозначают независимо друг от друга A-D, где А карбоксиамидом, алкоксикарбонилом, амино или аминокарбонилом, необязательно один или два раза замещенными низшим алкилом, нитрилом, оксогруппой, тиокарбоксамидом, алкокситиокарбонилом, алкилмеркаптокарбонилом, фосфоном, алкилфосфоном, диалкилфосфоном, алкилсульфониламидом, их фармакологически приемлемые соли или их эфиры карбоновых кислот,
при условии, что
когда -NR4R5 представляет незамещенное пиперидиновое кольцо, тогда R1 не может быть фенилом, метилом, этилом, пропилом, алкилом или кротонилом и, когда -NR4R5 представляет диэтиламиногруппу, тогда R1 не может быть метилом, этилом или кротонилом.
Предпочтительны следующие соединения формулы I:
Соединение формулы I, в котором моноцикл G обозначает фенил, пиридил, пиримидинил или пиридазинил.
Соединение формулы I, в котором W в R1 обозначает радикал метил, этил или бутил; V обозначает радикал фенил, пиридил, имидазолил
или
W-V обозначает радикалы н-октил, н-децил или бифенил.
Соединение формулы I, в котором азот, R4 и R5 образуют пиперазин или пиперидин, оба из которых замещены в 4- положении.
Соединение формулы I, которое представляет собой 5-(4'-бифенил)-5-[N-(4-нитрофенил) пиперазинил] барбитуровую кислоту.
Объектом изобретения также является фармацевтическая композиция, обладающая активностью ингибитора матричных металлопротеаз, включающая по меньшей мере одно соединение формулы I по одному из п.п. 1-5 и дополнительно обычные вещества-носители и вспомогательные вещества.
Изобретение относятся к соединениям формулы I: 
в которой
X, Y и Z являются кислородом,
R1 представляет группу W-V, в которой
W является валентной связью или прямой или разветвленной С1-С4-алкильной группой,
V является моноциклом, выбранным из фенила, необязательно замещенного гидрокси, низшим алкилом, низшим алкокси, фенилом, фенокси; пиридила, пиперидинила, тиофенила, имидазолила или бициклом, выбранным из нафтила, хинолинила, тетрагидрохинолила, тетрагидроизохинолила, бензимидазолила, индолила, каждый из которых может быть замещен, или
W-V является С1-С20-алкильной группой, необязательно замещенной аминогруппой, гидрокси, низшей ациламиногруппой, карбоксигруппой, аминокарбонилом, низшим алкиламинокарбонилом, аминокарбонил-низшималкиламинокарбонилом, низшим алкилом, низшим алкоксилом, низшим алкоксиалкоксилом,
R2 и R3 оба являются водородом,
R4 и R5 обозначают независимо друг от друга A-D, где А представляет связь, C1-С8-алкил, С1-С4-ацил, который может прерываться гетероатомами, выбранными из О, SO2, и, в котором алкильная группа может быть замещена аминогруппой; сульфонил, аминокарбонил, алкоксикарбонил, оксикарбонил,
D представляет собой водород, моноцикл, выбранный из фенила, пиридила, пиперидинила, циклогексила, фурила, имидазолила, пирролидинила, тиофенила, или бицикл, выбранный из нафтила, индолила, тетрагидрохинолила, флуоренила, каждый из которых может быть замещен
или R4 и R5 вместе с атомом азота, с которым они соединены, представляют кольцо, которое необязательно может прерываться дополнительным атомом N,
упомянутое кольцо необязательно может быть замещено один или несколько раз гидроксилом, алкоксилом, амино, алкиламино, диалкиламино, нитрилом или E-G,
где E представляет валентную связь, С1-С4 алкил, который необязательно замещен гидрокси; С2-С4-алкенил;
G представляет водород, 6-членный ароматический моноцикл, имеющий 0, 1 или 2 атома азота, причем остальные атомы в моноцикле являются атомами углерода, где моноцикл является незамещенным или замещенным заместителем, выбранным из группы, состоящей из галогена, -NH2, -NO2, -SO2NH2, -SO2CH3, ацетила и циано,
радикалы, перечисленные для R1, R4 и R5 могут быть необязательно один или несколько раз замещены галогеном, гидроксилом, алкилом, гидроксиалкилом, алкоксилом, алкилтиогруппой, алкилсульфинилом, алкилсульфонилом, амино, алкиламино, диалкиламино, нитрогруппой, карбоксилом, карбоксиамидом, алкоксикарбонилом, амино или аминокарбонилом, необязательно один или два раза замещенными низшим алкилом, нитрилом, оксогруппой, тиокарбоксамидом, алкокситиокарбонилом, алкилмеркаптокарбонилом, фосфоном, алкилфосфоном, диалкилфосфоном, алкилсульфониламидом и их фармакологически приемлемые соли для получения фармацевтической композиции, обладающей активностью ингибировать матричные металлопротеазы.
В частности, для получения фармацевтической композиции, обладающей активностью ингибировать адамализины.
Соединения формулы I, фармакологически приемлемые соли или их пролекарства, могут быть использованы для получения фармацевтических средств.
Среди перечисленных значений радикалов дополнительно можно указать следующее.
Под моноциклами, перечисленными в случае R1, R4 и R5, понимаюся насыщенные или ненасыщенные кольца с 3-8, предпочтительно с 5-7 атомами углерода, которые необязательно прерываются один или несколько раз гетероатомами, такими как азот, кислород или сера, особенно радикалы циклопентил, циклогексил, циклогептил, морфолинил, тиаморфолинил, пиперидинил, пиперазинил, тетрагидрофуранил, тетрагидропиранил, фенил, пиридил, пиpимидинил, пиридазинил, пиразинил, фурил, тиофенил, имидазолил, тиазолил, оксазолил, изотиазолил, изоксазолил, 1,2,3-триазолил или 1,2,4-триазолил. Помимо всего прочего, в качестве заместителей могут подразумеваться низший алкил, алкоксил и галоген.
Под бициклами, перечисленными для R1, R4 и R5 понимается конденсированный бицикл или бицикл типа моноцикл1-L-моноцикл2, где L обозначает валентную связь, С1-С4-алкилгруппу, С2-С4-алкенилгруппу, кислород или -С(O)-группу.
Предпочтигельно бицикл является радикалом таким, как радикал нафтил, тетрагидронафтил, декалинил, хинолинил, изохинолинил, тетрагидрохинолинил, тетрагидроизохинолинил, индолил, бензимидазолил, индазолил, оксиндолил, бензофуранил, бензотиофенил, бензтиазолил, бензоксазолил, пуринил, бифенил или (4-фенокси фенил и особенно нафтил, бифенил, хинолинил, изохинолинил, тетрагидрохинолинил, индолил или бензимидазолил.
Радикалы, перечисленные для R1, R4 и R5, необязательно могут быть один или несколько раз замещены галогеном, гидроксилом, тиогруппой, алкилом, гидроксиалкилом, алкоксилом, алкилтиогруппой, алкилсульфинилом, алкилсульфонилом, амино, алкиламино, диалкиламино, нитрогруппой, карбоксилом, карбоксиамидом, алкоксикарбонилом, аминогруппой или аминокарбонилом, необязательно один или дважды замещенными низшим алкилом, нитрилом, оксогруппой, тиокарбоксиамидом, алкокситиокарбонилом алкмеркаптокарбонилом, фосфоном, алкилфосфоном, диалкилфосфоном, алкилсульфониламидо, ариламино, арилом, гетарилом, арилоксилом, арилтиогруппой, арилсульфинилом, арилсульфонилом или ацилом.
В этом случае предпочтительны галоген, гидрокси-, оксо-, тио-, алкокси-, алкилтио-, амино-, аминокарбонил-, карбоксил-или ацилгруппы.
Низший алкил представляет C1-C6-алкил, предпочтительно метил, этил, пропил, изопропил или трет.-бутил.
Низший ацил в радикалах R2 и R3, более всего представляет -С(O)-С1-С6-алкил или -С(O)Н, предпочтительно ацетильную группу.
Алкильные радикалы в R1, R4 и R5 необязательно могут прерываться один или несколько раз гетероатомами (О, S, NH).
Алкил в радикалах R4 и R5 обозначает таковой или в комбинации с радикалом алкоксилом, алкилтиогруппой, арилсульфонилом, алкилсульфонилом, алкиламинокарбонилом, ариламинокарбонилом, алкиламино, алкоксикарбонилом, арилоксикарбонилом, алкиламинотиокарбонилом, ариламинотиокарбонилом, радикал с прямой, разветвленной цепью, насыщенный или ненасыщенный с 1-11, предпочтительно 1-8 атомами углерода, такой, как, например, радикал метил, этил, пропил, пентил, октил, аллил, пропаргил, 2,4-пентадиенил, изопропил, вторичный бутил, 3-метилбутил, 2-гидроксигексил и особенно метил, пропил, изопропил, пентил, октил, аллил, 3-метилбутил, 2-гидроксигексил и пропаргил.
Арил, также в комбинации с арилоксилом, арилтиогруппой, арилсульфонилом, ариламинокарбонилом, арилоксикарбонилом, ариламинотиокарбонилом понимается как радикал фенил или нафтил, которые могут необязательно быть замещены галогеном, низшим алкилом или алкоксилом.
С1-С20-алкильной группой, перечисленной для R1, является насыщенный радикал с прямой или разветвленной цепью такой, как, например, метил, этил, пропил, бутил, пентил, октил, децил, ундецил, изобутил, 3-метилбутил или 7-метилоктил. В качестве заместителей более всего следует иметь ввиду радикалы гидроксил и амин. Алкильные цепи могут один или несколько раз прерываться кислородом, азотом или серой. Наиболее предпочтительным гетероатомом для прерывания является кислород (эфирная связь) или -C(O)NH-(амидная связь). Наиболее предпочтительными радикалами, прерывающимися гетероатомом, являются -(CH2-CH2O)n-(CH2)mH и n=2 или 3, m-1 или 2.
W в R1 предпочтительно является радикалом метилом, этилом, бутилом или гексилом; V особенно является радикалом фенилом, пиридилом, имидазолилом, которые необязательно могут быть более всего замещены низшим алкилом, гидроксилом, алкоксиамидом, сульфонамидом или галогеном. Наиболее предпочтительными радикалами для R1 являются радикал С6-С12-алкил или радикал -(CH2)n-С6H4-(CH2)mH, где m и n равны или меньше 8, (CH2)-группа необязательно прерывается кислородом, серой или NH, и один или два атома углерода фенильного кольца замещены гетероатомами N. Алкильная, арильная, гетарильная группы необязательно замещены небольшими полярными заместителями.
Наиболее предпочтительными радикалами в отношении R1 являются радикалы типа n-октила, n-децила, бифенила или октила или децила, имеющие два или три гетероатома кислорода, как, например, 2-(2-(2-метоксиэтокси)этокси)этил, 2-(2-этоксиэтокси) этил или типа бифенила, имеющие один или два гетероатома азота. Связывающий моноцикл необязательно замещен в орто-положении и концевой моноцикл бифенила или радикал типа бифенила необязательно замещен в орто- или пара-положении небольшим полярным заместителем, таким, как -NH2, -NO2, -SO2NH2, -SO2CH3, ацетилом, гидроксилом, метокси-, этокси-, или нитрильной группой. Более предпочтительно замещение в пара-положение концевого моноцикла.
Под галогеном понимается хлор, бром, йод и предпочтительно хлор.
Гетарильные радикалы, перечисленные для R4 и R5, предпочтительно означают кольца пиридина, пиразина, пиперазина, имидазола, тиазола, тиофена или индола, предпочтительно это пиридиновое, имидазольное и тиофеновое кольцо.
Ацильный радикал, перечисленный для R4 и R5, означает радикал с 1-10, предпочтительно 6-8 атомами углерода, такой, например, как радикал гексаноил или октаноил. Алкильная группа может прерываться один или несколько раз гетероатомами или гетероатомными группами, подобными S, О, NH, SO2, амидо или карбонилом. Эти радикалы могут замещаться аминогруппами, алкильными группами, арильными группами, арилалкильными группами, алкиламиногруппами, диалкиламиногруппами, алкоксигруппами и ароматическими соединениями. В этом случае это могут быть остатки аминокислот, предпочтительно, остаток фенилаланина или триптофана.
Если R4 и R5 вместе образуют кольцо с атомом азота, с которым они соединены, то это 5-7-членные кольца, предпочтительно 6-членное кольцо. Предпочтительны кольца пиперидина, пиперазина, тетрагидрохинолина и тетрагидроизохинолина, бицикло (9.4.0) пентадецила и 1,2,3,4-тетрагидробензо (g) изохинолина.
Если соединения, имеющие общую формулу I, содержат один или несколько асимметричных атомов углерода, оптически активные соединения с общей формулы I, также являются предметом настоящего изобретения.
Независимо друг от друга предпочтительным значением для X, Y, Z является кислород, для R2 и R3 - это водород. Более предпочтительна комбинация, если X, Y и Z каждый является кислородом и R2 идентичен с R3, и оба являются водородом.
Предпочтительно, чтобы R4 и R5 - оба не представляли водород.
Термин "несколько" в отношении гетероатомов в моноциклах или бициклах предпочтительно означает один, два или три, более предпочтительно один или два атома, наиболее предпочтительным гетероатомом является азот.
Термин "несколько" в отношении заместителей или замещения предпочтительно означает от одного до пяти таковых, более предпочтительно один, два или три, наиболее предпочтительно один или два.
Термин "гетероатом" в отношении алкильной или ацильной групп означает предпочтительно кислород или NH, более предпочтительно кислород.
Заместители моноциклов или бициклов R1, R4 и R5, представляют собой галоген, нитрогруппу, гидроксил, алкоксил, амино, алкиламино, диалкиламино, галогенметил, дигалогенметил, тригалогенметил, фосфоно, алкилфосфоно, диалкилфосфоно, SO2NH2, SO2NH (алкил)2, SO2N (алкил)2, SO2 (алкил), ацетил, формил, нитрил, COOH, COO-алкил, -ОС(O)-алкил, -NHC(O)O-алкил, ОС(O)O-арил, NHC(S)NH2, -NHC(S)NH-алкил, -NHC(O)-арил.
Предпочтительной кольцевой структурой, образуемой азотом, R4 и R5, является пиперазин или пиперидин, которые оба замещены предпочтительно в 4-м положении. В случае пиперидина 4-ое положение необязательно замещено вторым заместителем гидроксилом, амино, алкиламино, диалкиламино или алкоксилом. 4-ое положение пиперидина также может образовать двойную связь с заместителем в 4-ое положении.
Предпочтительными заместителями в 4-ое положении пиперидина или пиперазина являются 6-членные ароматические моноциклы, которые более предпочтительно замещены в пара-положении небольшими полярными заместителями такими, как гидроксил, низший алкоксил, амино, низший алкиламино, низший диалкиламино, нитрогруппа, нитрил, SO2NH2, SO2NH низший алкил, SO2 низший алкил. 6-членный ароматический моноцикл предпочтительно связан с 4-м положением через валентную связь или пространственную группу низшего алкила.
В случае, если R4 является водородом, низшим алкилом, низшим алкиларилом, тогда предпочтительно R5 является производным ацила, предпочтительно замещенным моноциклом или низшим алкиларилом; или -CHR50-CHR51-NR52-R53, R50 и R51 независимо друг от друга являются водородом, низшим алкилом, низшим алкоксилом. R52 означает водород или низший алкил, R53 означает 6-членный ароматический моноцикл, который необязательно один или несколько раз замещен и связан с азотом предпочтительно через валентную связь или пространственную группу низшего алкила.
Наиболее предпочтительными комбинациями значений в общей формуле I являются
X равен Y равен Z равен кислороду и
R2 равен R3 равен водороду и
R1 равен радикалу типа н-октила, н-децила, бифенила или октила, или децила, имеющих два или три гетероатома кислорода, подобно радикалам 2-(2- (2-метоксиэтокси)этокси)этил, 2-(2-этоксиэтокси)этил или типа бифенила, имеющих один или два гетероатома азота; где мостиковый моноцикл необязательно замещен в орто-положении и концевой моноцикл бифенила или радикал типа бифенила необязательно замещен в орто- или предпочтительно в пара-положении небольшим полярным заместителем типа NH2, -NO2, -SO2NH2, -SO2CH3, ацетильной, гидроксильной, метоксильной, этоксильной или нитрильной группы и
R4 и R5 образуют с азотом, к которому они присоединены, пиперазин или пиперидин, которые оба замещены в 4 положении кольцом фенила, пиридила или пиразидила, которое предпочтительно замещено в пара-положении небольшим полярным заместителем; в случае пиперидина 4 положение может быть дополнительно замещено гидроксилом, низшим алкоксилом, нитрилом или амино, который может быть моно- или дизамещенным низшим алкилом.
Соединения общей формулы I могут быть синтезированы хорошо известными способами, предпочтительными тем, что
а) соединения общей формулы II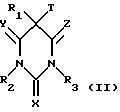
в которых X, Y, Z, R1, R2 и R3 имеют вышеупомянутые значения и Т представляет уходящую группу такую, как Hal или OSO2R6. Hal означает хлор, бром или йод и R6 означает радикал арил или метил, реагируют с соединением общей формулы III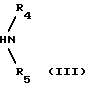
в котором R4 и R5 имеют вышеупомянутые значения и необязательно превращаются в фармакологически приемлемые соли или
b) соединения общей формулы IV
в которых R1, R4 и R6 имеют вышеупомянутые значения, Y и Z независимо друг от друга представляют кислород, серу или NH группу и R7 = метилу, этилу или фенилу, реагируют с соединением общей формулы V
в котором R2, R3 и X имеют вышеупомянутые значения и необязательно превращаются в фармакологически приемлемые соли или
в случае, когда R4 и/или R5 представляют радикал ацил, алкилсульфонил, арилсульфонил, алкиламинокарбонил, ариламинокарбонил, алкоксикарбонил, арилоксикарбонил, алкиламинотиокарбонил или ариламинотиокарбонил
с) соединение общей формулы VI
в котором X, Y, Z, R1, R2 и R3 имеют вышеупомянутые значения, реагирует с соединением общей формулы VII или VIII
R6 --- D --- Hal (VII) R8N===C===A (VIII),
в котором R8 представляет необязательно замещенный радикал алкил или арил, Д=С(O), О-С(О), SO2 или валентную черточку. Hal = хлор, бром или йод, и А представляет кислород или серу
и необязательно превращается в фармакологически приемлемые соли.
Соединения общей формулы II известны в литературе. Так, например, 2,4,6-пиримидиновые трионы, бромированные в 5-м положении, могут быть синтезированы реакцией соответствующих диалкиловых эфиров броммалоновой кислоты с мочевиной (например, Acta Chim. Acad. Sci. Hung. 107, 2, 139, 1981). Соответствующие бромированные или хлорированные соединения общей формулы II можно получить в реакции 2,4,6-пиримидиновых трионов, замещенных R1 в 5-м положении, с бромом (аналогично J. pr. Chemie, 136, 329 (1933) или J.Chem. Soc. 1931, 1870) или хлористым сульфурилом (J. Chem. Soc. 1938, 1622). Аналогичным способом можно синтезировать 2-имино-4,6- пиримидин-дионы общей формулы II, соответственно галогенированные в 5-м положении аналогично Collect. Czech. Comm. 48, 1, 299, (1933). Реакция 2-тиа-4,6-пиримидин-дионов, замещенных R1 в 5-м положении, бромом в ледяной уксусной кислоте (аналогично Am. Chem. J. 34, 186) приводит к образованию соединений общей формулы II, соответственно бромированных в 5-м положении.
Амины общей формулы III коммерчески доступны и обычно известны в литературе.
Соединения с общей формулой IV реагируют по известным методам с мочевинами (см. , например, J. Med. Chem. 10, 1078, 1967) Helvetica Chim. Acta 34, 459, 1959 или Pharmacie, 38, 1, 65, (1983), тиомочевинами (смотри, например, Indian J. Chem. 24, 10, 1094, 1985 или J. Het. Chem. 18, 3, 635, (1981) или гуанидинами (см., например. Collect. Czech. Chem. Comm. 45, 12, 3583, 1980) общей формулы V.
Реакции обычно проводят в спирте таком, как метанол, этанол или бутанол в присутствии соответствующего алкоголята натрия при температуре между 40oC и 100oC и в случае гуанидинов при температуре до 200oC (под давлением). В случае тиомочевин процесс часто проводят в присутствии ацетилхлорида (также в качестве растворителя).
Соединения общей формулы IV известны из литературы, или могут быть получены по способам, известным из литературы. Они могут быть синтезированы, например, в результате слабого кислотного гидролиза соответствующих эфиров бислактима (смотри J. Chem. Soc. Chem. Comm., 5, 400, (1990). Другие методы синтеза описаны, например, в Farmaco Ed. Sci., 31, 7, 478, (1976) или Aust. J. Chem., 23, 6, 1229, (1970).
Мочевины, тиомочевины и гуанидины общей формулы V имеются в продаже.
Соединения общей формулы VI можно легко синтезировать в реакции соответствующего замещенного ацетамидомалонового эфира по способу b) и последующего гидролитического отщепления ацетильной группы (см. Can. J.Chem. 42, 3, 605, 1964).
Хлориды карбоновых кислот общей формулы VII известны, или могут быть синтезированы с помощью широко известных методов из соответствующих карбоновых кислот. Реакцию обычно проводят с хлористым тионилом или трехбромистым фосфором или пятибромистым или пятихлористым фосфором в инертных растворителях таких, как дихлорметан, диэтиловый эфир, диоксан или тетрагидрофуран при температуре от 0oC до 50oC, предпочтительно между 20oC и 40oC.
Эфиры хлормуравьиной кислоты общей формулы VII известны в литературе, и могут быть получены широко известными методами из соответствующих спиртов реакцией с фосгеном или дифосгеном. Реакцию проводят в инертных растворителях таких, как диэтиловый эфир, дихлорметан, диоксан, тетрагидрофуран или толуол при температуре между -20oC и 20oC. В случае фосгена реакцию проводят в присутствии оснований, обычно третичных аминов таких, как, например, триэтиламин или пиридин.
Хлориды сульфокислоты общей формулы VII известны и могут быть синтезированы аналогично описанным методам из соответствующих сульфокислот в реакции с пятихлористым фосфором или хлористым тионилом. Реакцию обычно проводят в инертном растворителе таком, как, например, диметилформамид или также без растворителя при температуре от 20oC до 180oC, предпочтительно при 50-100oC.
Изоцианаты общей формулы VIII известны, или могут быть синтезированы способами, известными в литературе. Так, например, соответствующие алкилгалогениды общей формулы R8-Hal могут реагировать с цианатом калия аналогично Synthesis, 1978, 760. Дополнительными методами являются реакция амидов кислот с общей формулой R8-CONH2 с оксалилхлоридом до термического разложения азида кислоты с общей формулой R8-CON3 или реакция амина с общей формулой R8-NH2 с фосгеном (аналогично Ann. Chem. 562, 110).
Изотиоцианаты общей формулы VIII известны в литературе, или могут быть синтезированы аналогично известным способам. Амин общей формулы R8-NH2 предпочтительно вводят в реакцию с сероуглеродом в щелочных условиях аналогично Chem. Веr. 74, 1375.
Реакцию галогенидов карбоновых кислот, галогенидов сульфокислоты или эфиров хлормуравьиной кислоты общей формулы VII с аминами общей формулы VI обычно проводят в растворителе таком, как дихлорметан, диметилформамид или пиридин с добавлением вспомогательного основания такого, как триэтиламин или 4- диметиламинопиридин при температуре между -10oC и 50oC, предпочтительно при комнатной температуре.
Соединения общей формулы I могут включать один или несколько хиральных центров и следовательно могут быть в рацемической или оптически активной форме. Рацематы можно разделить известными методами на энантиомеры. Предпочтительно дистереоизомерные соли, которые можно разделить кристаллизацией, образуются из рацемических смесей в реакции с оптически активной кислотой такой, например, как Д- или L-винная кислота, миндальная кислота, яблочная кислота, молочная кислота или камфарсульфокислота или с оптически активным амином таким, например, как Д- или L- α -фенил-этиламин, эфедрин, хинидин или цинхонидин.
Соли щелочных металлов, соли щелочно-земельных металлов, подобно солям Ca или Mg, соли аммония, ацетаты или гидрохлориды в основном используют в качестве фармакологически приемлемых солей, которые получают обычным путем, например, растиранием соединений с неорганическими и органическими основаниями или неорганическими кислотами такими, как, например, гидроксид натрия, гидроксид калия, водный аммиак, C1-С4-алкиламины такие, например, как триэтиламин или соляная кислота. Соли обычно очищают переосаждением из воды/ацетона.
Новые веществу формулы I и их соли по изобретению можно назначать энтерально или парентерально в жидкой или твердой форме. В этой связи можно принимать во внимание все обычные формы для назначения, например, такие, как таблетки, капсулы, таблетки с покрытием, сиропы, растворы, суспензии и т.д. Предпочтительно воду, включающую добавки такие, как стабилизаторы, солюбилизаторы и буферы, которые обычны для инъекционных растворов, используют в качестве инъекционной среды.
Такими добавками являются, например, винный и цитратный буфер, этанол, комплексообразующие агенты (такие, как этилендиаминтетрауксусная кислота и ее нетоксичные соли), высокомолекулярные полимеры (такие, как жидкая окись полиэтилена) для регуляции вязкости. Жидкие вещества-носители для инъекционных растворов должны быть стерильными) и предпочтительно расфасованы в ампулы. Твердыми веществами-носителями являются, например, крахмал, лактоза, маннит, метилцеллюлоза, тальк, высокодисперсные кремниевые кислоты, высокомолекулярные жирные кислоты (такие, как стеариновая кислота), желатины, агар-агар, фосфат кальция, стеарат магния, животные и растительные жиры, твердые высокомолекулярные полимеры (такие, как полиэтиленгликоли); пригодные препараты для орального применения могут необязательно включать ароматизаторы и подсластители.
Дозировка может зависеть от различных факторов таких, как путь назначения, виды, возраст и/или индивидуальное состояние здоровья. Дозы, которые назначают ежедневно, составляют примерно 10-1000 мг/человека, предпочтительно 100-500 мг/человека, и можно принимать однократно или разделить на несколько назначений.
Пролекарствами соединений настоящего изобретения являются таковые, которые in vivo превращаются в фармакологически активные соединения. Наиболее распространенными пролекарствами являются эфиры карбоновых кислот.
По настоящему изобретению дополнительно к соединениям, упомянутым в примерах, и соединениям, которые можно получить, комбинируя значения заместителей, упомянутые в формуле изобретения, предпочтительны следующие производные барбитуровой кислоты:
1. 5-(N-бензил-N-октил)-5-фенил-барбитуровая кислота
2. 5-(N-бензил-N-фенэтил)-5-фенил-барбитуровая кислота
3. 5-(N-бензил-N-[2-(4-пиридил)этил]-5-фенил-барбитуровая кислота
4. 5-(N-бензил-N-[2-(3-пиридил)этил] -5-фенил-барбитуровая кислота
5. 5-(N-бензил-N-[2-(2-пиридил) этил] -5-фенил-барбитуровая кислота
6. 5-(N-бензил-N-[2-(2-тиофенил)этил]-5-фенил-барбитуровая кислота
7. 5-[N-(3-метилбутил)-N-(3-фенилпропил)] -5-фенил-барбитуровая кислота
8. 5-(N-бензил-N-[3-(4-пиридил)пропил])-5-фенил-барбитуровая кислота
9. 5-(N-бензил-N-[2-(2-имидазолил)этил])-5-фенил-барбитуровая кислота
10. 5-(N-бензил-N-[2-(1-имидазолил)этил])-5-фенил-барбитуровая кислота
11. 5-(N-бутил-N-фенилаланин)-5-фенил-барбитуровая кислота
12. 5-(N-бутил-N-триптофанил)-5-фенил-барбитуровая кислота
13. 5-(N-бензил-N-циклогексил)-5-фенил-барбитуровая кислота
14. 5-[N-бензил-N-(2-пиридил)]-5-фенил-барбитуровая кислота
15. 5-[N-бутил-N-(4-пиперидинил)]-5-фенил-барбитуровая кислота
16. 5-[N-бензил-N-(2-имидазолил)]-5-фенил-барбитуровая кислота
17. 5-(N-октил-N-фенил)-5-фенил-барбитуровая кислота
18. 5-[N-(2-нафтил)-N-пропил]-5-фенил-барбитуровая кислота
19. 5-[N-(4-тетрагидрохинолинил)-N-пропил]-5-фенил-барбитуровая кислота
20. 5-[N-бензил-N-(2-тиофенил)]-5-фенил-барбитуровая кислота
21. 5-[N-(3-метилбутил)-N-[3-(4-пиридил)пропил)] -5-фенил- барбитуровая кислота
22. 5-[N-(7-метилоктил)-N-[3-(2-пиридил) пропил)]-5-фенил-барбитуровая кислота
23. 5-(N-(2-гидроксигексил)-N-[3-(3-пиридил)пропил] ) -5-фенил-барбитуровая кислота
24. 5-(N-бензил-N-гексаноил)-5-фенил-барбитуровая кислота
25. 5-(N-бензил-N-октаноил)-5-фенил-барбитуровая кислота
26. 5-(N-бензил-N-октансульфонил) -5-фенил-барбитуровая кислота
27. 5-[N-бутил-N-(2-нафтилсульфонил)]-5-фенил- барбитуровая кислота
28. 5-(N-гексилоксикарбонил-N-пропил)-5- фенил-барбитуровая кислота
29. 5-[N-(4-метокси-фенилсульфонил) -N-гексил]-5-фенил-барбитуровая кислота
30. 5-[N-4-бутокси- фенилсульфонил)]-N-гексил]-5-фенил-барбитуровая кислота
31. 5-[N-бензил-N-(2-фенэтил)]-5-(4-пиридил)барбитуровая кислота
32. 5-[N-бензил-N-(2-фенэтил)]-5-(2-пиридил) барбитуровая кислота
33. 5-(N,N-дипентил)-5-(4-пиперидинил)барбитуровая кислота
34. 5-(N,N-диоктил)-5-(2-тиофенил)барбитуровая кислота
35. 5-(N-бензил-N-[2-(2-пиридил)этил]-5-(3-имидазолил)барбитуровая кислота
36. 5-[1-(4-гидрокси)пиперидинил]-5-(4-пиридил) барбитуровая кислота
37. 5-[1-(4-гидрокси)пиперидинил]-5-(3-пиридил)барбитуровая кислота
38. 5-[1-(4-гидрокси) пиперидинил]-5-(2-пиридил) барбитуровая кислота
39. 5-[1-(4-гидрокси) пиперидинил]-5-(4-пиперидинил) барбитуровая кислота
40. 5-[1-(4-гидрокси) пиперидинил]-5- (тиофенил) барбитуровая кислота
41. 5-[1-(4-гидрокси)пиперидинил]-5-(4-имидазолил) барбитуровая кислота
42. 5-бензил-5-[1-(4-гидрокси) пиперидинил]барбитуровая кислота
43. 5-[1-(4-гидрокси) пиперидинил]-5-(2-фенэтил)барбитуровая кислота
44. 5-[1-(4-гидрокси)пиперидинил]-5-(1-нафтил)барбитуровая кислота
45. 5-[1-(4-гидрокси)пиперидинил] -5-(2-нафтил)барбитуровая кислота
46. 5-(2-хинолинил)-5-[1- (4-гидрокси)пиперидинил]барбитуровая кислота
47. 5-[1-(4-гидрокси)пиперидинил]-5-(1-изохинолинил)барбитуровая кислота
48. 5-[1-(4-гидрокси)пиперидинил]-5-(2-тетрагидро-хинолинил) барбитуровая кислота
49. 5-(2-индолил)-5-[1-(4-гидрокси) пиперидинил]барбитуровая кислота
50. 5-(2-бензимидазолил)-5-[1-(4-гидрокси)пиперидинил]-барбитуровая кислота
51. 5-(1-[4-(2-гидроксиэтил)пиперазинил]) -5-октил-барбитуровая кислота
52. 5-децил-5-(1-[4-(2-гидроксиэтил)пиперазинил])барбитуровая кислота
53. 5-(1-[4-(2-гидроксиэтил)пиперазинил]) -5-ундецил-барбитуровая кислота
54. 5-(1-[4-(2-гидроксиэтил)пиперазинил])-5-(7-метил-октил) барбитуровая кислота
55. 5-(1-[4-(2-гидроксиэтил)пиперазинил])-5-(8-гидроксиоктил) барбитуровая кислота
56. 5-(8-аминооктил)-5-(1-[4-(2- гидроксиэтил) пиперазинил])барбитуровая кислота
57. 5-(1-[4-(2- гидроксиэтил)пиперазинил] )-5-(4-фенэтил)барбитуровая кислота
58. 5-(1-[4-(2-гидроксиэтил)пиперазинил])-5-(4-фенилбутил) барбитуровая кислота
59. 5-(1-[4-(2-гидроксиэтил) пиперазинил])-5-(6-фенилгексил)барбитуровая кислота
60. 5-(1-[4-(2-гидроксиэтил) пиперазинил])-5-[6- (4-метилфенил)гексил] барбитуровая кислота
61. 5-(1-[4- (2-гидроксиэтил)пиперазинил])-5-(2-пиридилметил)барбитуровая кислота
62. 5-(1-[4-(2-гидроксиэтил)пиперазинил])-5- (4-имидазолилметил)барбитуровая кислота
63. 5-(1-[4- (2-гидроксиэтил)пиперазинил])-5-(1-имидазолилметил)барбитуровая кислота
64. 5-фенил-5-[1-(4-пропил)пиперазинил]барбитуровая кислота
65. 5-фенил-5-(1-тетрагидрохинолинил)барбитуровая кислота
66. 5-фенил-5-(1-тетрагидроизохинолинил)барбитуровая кислота
67. 5-фенил-5-[2-(1,2,3,4-тетрагидробензо (g)изохинолинил]барбитуровая кислота
68. 5-[2-(2-аза-бицикло[9.4.0]пентадецил)]-5-фенил-барбитуровая кислота
69. 5-[2-(2,11-диаза-12-оксо-бицикло [9.4.0] пентадецил)]-5-фенил-барбитуровая кислота
70. 5-(1-[4-(1-оксо- пропил)]-пиперидинил)-5-фенил-барбитуровая кислота
71. 5-[1-(3- оксо-4-пропил)]пиперидинил]-5-фенил-барбитуровая кислота
72. 5-фенил-5-[1-(4-пропил)пиперазинил]барбитуровая кислота
73. 5-[1-(3,5-дигидрокси-4-пропил)пиперидинил] -5-фенил-барбитуровая кислота
74. 5-(4-хлорфенил)-5-[1-(4-гидрокси-пиперидинил] барбитуровая кислота
75. 5-(4-хлорбензил)-5-[1-(4-гидрокси) пиперидинил]барбитуровая кислота
76. 5-[1-(4-гидрокси) пиперидинил] -5-(4-метоксибензил)-барбитуровая кислота
77. 3-метил-5-[1-(4-гидрокси)пиперидинил]-5-фенил-барбитуровая кислота
78. 1-изопропил-5-[1-(4-гидрокси)пиперидинил] -5-фенил- барбитуровая кислота
79. 3-ацетил-5-[1-(4-гидрокси)пиперидинил] -5-фенил-барбитуровая кислота
80. 5-[1-(4-метокси)пиперидинил] -5-фенил-2-тио-барбитуровая кислота
81. 2-имино-5-[1-(4-метокси)пиперидинил]-5-фенил-барбитуровая кислота
82. 5-[1-(4-метокси)пиперидинил] -5-фенил-2,4, 6-триимино-барбитуровая кислота
83. 4,6-диимино-5-[1-(4-метокси)пиперидинил] -5-фенил- барбитуровая кислота
84. 5-[1-(4-метокси)пиперидинил] -5-фенил- 2,4,6-тритио-барбитуровая кислота
85. 5-(6-аминогексил)-5-[N- (2-гидроксиэтил)пиперазинил] барбитуровая кислота
86. 5-(6-формиламиногексил)-5-[N-(2-гидроксиэтил)пиперазинил] барбитуровая кислота
87. 5-(6-ацетиламиногексил)-5-[N- (2-гидроксиэтил)пиперазинил]барбитуровая кислота
88. 5-[7-(этоксикарбонил)гептил]-5-[N-(2-гидроксиэтил)- пиперазинил]барбитуровая кислота
89. 5-(8-гидроксиоктил)-5-[N- (2-гидроксиэтил)пиперазинил]барбитуровая кислота
90. 5-(7-карбоксигептил)-5-[N-(2-гидроксиэтил) пиперазинил]барбитуровая кислота
91. 5-(7-аминокарбонил)гептил]-5- [N-(2-гидроксиэтил) пиперазинил]барбитуровая кислота
92. 5-[3-((аминокарбонилметил)аминокарбонил)пропил] -5-[N- (2-гидроксиэтил)пиперазинил]барбитуровая кислота
93. 5-[6-(метиламино)гексил]-5- [N-(4-нитрофенил)пиперазинил]барбитуровая кислота
94. 5-[4-(н-пропилокси)бутил]-5-[N-(4-нитрофенил)пиперазинил] барбитуровая кислота
95. 5-[2-(2-(2-метоксиэтокси)этокси)этил] -5-[N-(4-нитрофенил)пиперазинил]барбитуровая кислота
96. 5-[2-(2-(этокси)этокси)этил] -5-[N-(4-нитрофенил) пиперазинил]барбитуровая кислота
97. 5-децил-5-[N-(4-нитрофенил)пиперазинил]барбитуровая кислота
98. 5-октил-5-[N-(4-гидроксисульфонил)фенил) пиперазинил] барбитуровая кислота
99. 5-октил-5-[N-(4- аминосульфонил)фенил)пиперазинил]барбитуровая кислота
100. 5-октил-5-[N-(4-цианофенил)пиперазинил]барбитуровая кислота
101. 5-октил-5-[N-(4-карбоксифенил)пиперазинил] барбитуровая кислота
102. 5-октил-5-[N-(4-бутоксикарбонил) фенил)пиперазинил] барбитуровая кислота
103. 5-октил-5-[N-(4-амидино)фенил)пиперазинил]барбитуровая кислота
104. 5-октил-5-[N-(4-(аминотиокарбонил)фенил)пиперазинил] барбитуровая кислота
105. 5-октил-5-[N-(4-(метилсульфонил)фенил)пиперазинил] барбитуровая кислота
106. 5-октил-5-[N-(4-(аминокарбонил)фенил) пиперазинил] -барбитуровая кислота
107. 5-октил-5-[N-(4- метилкарбонил)фенил)пиперазинил]-барбитуровая кислота
108. 5-октил-5-[N-(4-(диметилфосфонил)фенил)пиперазинил] барбитуровая кислота
109. 5-октил-5-[N-(4-(амино)фенил) пиперазинил]барбитуровая кислота
110. 5-октил-5-[N-(4-(ацетиламино)фенил)пиперазинил]- барбитуровая кислота
111. 5-октил-5-[N-(4-(трифторацетиламино)фенил) пиперазинил]барбитуровая кислота
112. 5-октил-5-[N-(4- (метилсульфониламино)фенил)пиперазинил]барбитуровая кислота
113. 5-октил-5-[N-(5-нитропирид-2-ил)пиперазинил]барбитуровая кислота
114. 5-октил-5-[N-(N-оксипирид-4-ил)пиперазинил] барбитуровая кислота
115. 5-октил-5-[N-(4-(5-триазолил) фенил)пиперазинил]барбитуровая кислота
116. 5-октил-5-[(N- бензоил-N-бензил)амино]барбитуровая кислота
117. 5-[4-(фенил) фенил]-5-[(N-бензоил-N-бензил)амино]-барбитуровая кислота
118. 5-(4-[4-нитрофенил)пиперазинил] -5-октил-барбитуровая кислота Масс-спектр (ионизация электронным ударом): m/е=445, расчетная 445,23;
тонкослойная хроматография: Rf=0,61 (силикагель, дихлорметан/метанол 9: 1).
119. N-бензил-3-(4-нитро-фенил)- N-(2,4,6-триоксо-5-фенил-гексагидро-пиримидин-5-ил)акриламид
120. 5-[4-(фенил)фенил] -5-[(N-бензоил-N-бензил)амино] -барбитуровая кислота
Тонкослойная хроматография: Rf=0,36 (силикагель, гептан/метилэтилкетон 1:1);
ЯМР (CDCl3): 8,4 (широкий синглет 2H); 7,0-7,4 (м., 15H); 4,5 (с., 2H).
121. N-бензил-2-(3-бром-фенил)-N-(2,4,6- триоксо-5-фенил-гексагидро-пиримидин-5-ил)ацетамид
ПРИМЕР 1 5-(1-[4-(2-гидрокcиэтил)пипepaзинил] )-5-фeнил- барбитуровая кислота
5-бром-5-фенил-барбитуровую кислоту (Acta Chim. Acad.
Sci. Hung. 107, 139-45, 1981) (7 ммоль) и N-(2-гидрокси- этил)пиперазин (8 ммоль) суспендируют в 40 мл абсолютного этанола. Через 3 часа кипячения с обратным холодильником, его концентрируют под вакуумом. Остаток очищают хроматографией на силикагеле (этилацетат/метанол 3:1). Бесцветные кристаллы получают при перекристаллизации из изопропанола. Выход 56%; т.пл.: 238-40oC (разложение).
ПРИМЕР 2
5-(1-[4-(4-метилфенил)метил]пиперазинил]-5-фенил- барбитуровая кислота
5-бром-5-фенил-барбитуровую кислоту (7 ммоль) и N-(метил-p- толил)пиперазин (8 ммоль) суспендируют в 40 мл абсолютного этанола. Через 2 часа кипячения с обратным холодильником, его концентрируют под вакуумом. Остаток растирают в порошок с диэтиловым эфиром, высушивают на вакуум-фильтре, вновь промывают 20 мл диэтилового эфира и высушивают. Сырой продукт очищают хроматографией на силикагеле (ацетон). Получают бесцветные кристаллы. Выход 72%; т.пл.: 247-248oC.
ПРИМЕР 3
5-(1-[4-(4-(4-метилфенил))бутил] пиперазинил] -5-фенил- барбитуровая кислота
4-(р-толил)бутилбромид
Соединение получают аналогично описанному в литературе. Synth. Commun., 22, 20, 2945-8, 1992. Выход 91% в форме бесцветного масла.
Фенил-(4-р-толил) бутил) малоновой кислоты диэтиловый эфир
Диэтиловый эфир фенилмалоновой кислоты (8,8 ммоль), растворенный в 5 мл абсолютного тетрагидрофурана, по каплям добавляют к 20 мл абсолютного тетрагидрофурана и гидрида натрия (9,7 ммоль). Затем через 15 минут добавляют 4-р-толилбутилбромид (8,8 ммоль), растворенный в 10 мл абсолютного тетрагидрофурана. В течение трех дней нагревают с обратным холодильником. Растворитель концентрируют под вакуумом. Остаток переводят в 50 мл этилацетата и экстрагируют водой 2х50 мл. Органическую фазу высушивают над сульфатом магния, фильтруют и концентрируют при выпаривании. Ее очищают хроматографией на силикагеле (гептан/этилацетат 9:1). Выход 55% в форме бесцветного масла.
5-1-[4-(4-(4-метилфенил)) бутил]пиперазинил)-5-фенил- барбитуровая кислота
Мочевину (4,6 ммоль) и диэтиловый эфир фенил-(4-(p-толил) бутил) малоновой кислоты (3,1 ммоль) добавляют к раствору этилата натрия (6,2 ммоль) в абсолютном этаноле. В течение 12 часов нагревают с обратным холодильником, затем концентрируют под вакуумом и осадок переносят в 15 мл воды. С помощью 6N соляной кислоты доводят pH смеси до 1-2 и экстрагируют этилацетатом 2х30 мл. Органическую фазу высушивают над сульфатом магния, фильтруют и концентрируют выпариванием. Остаток очищают хроматографией на силикагеле (гептан/этилацетат 3:1).
Выход бесцветных кристаллов 46%; т.пл.: 163-165oC.
ПРИМЕР 4
5-(1-[4-(2-гидроксиэтил)пиперидинил])-5-фенил- барбитуровая кислота
14,6 г (50 ммоль) диэтилового эфира фенилмалоновой кислоты и затем 10 г (166 ммоль) мочевины медленно добавляют к 1,3 г натрия в 40 мл метанола при перемешивании. Нагревают в течение 2 часов при слабом кипячении. В этом процессе образуется осадок. Его охлаждают до 10-15oC, затем медленно смешивают с 12,9 г (100 ммоль) 4-(2-гидроксиэтил) пиперидина, 13,8 г (100 ммоль) карбоната калия и 2,87 мл (112,3 ммоль) брома. Смесь перемешивают в течение 2 часов при 10-15oC, затем медленно нагревают до кипения и кипятят в течение 1 часа с обратным холодильником. После охлаждения ее выливают в 240 мл 1N азотной кислоты, раствор один раз промывают толуолом и нейтрализуют насыщенным раствором ацетата натрия. Выпадает в осадок жирная масса, которую переводят в горячий этанол. Горячий раствор обрабатывают активным углем и смешивают с теплой водой, пока не появится помутнение. После охлаждения кристаллы отфильтровывают. Выход 7,3 г = 44%; т.пл.: 222-223oC.
ПРИМЕР 5
5-фенил-5-(1-пиперидинил)барбитуровая кислота
5-фенил-5-(1-пиперидинил)барбитуровую кислоту с выходом 92%; т.пл.: 244-246oC получают аналогично примеру 4, используя пиперидин вместо 4-(2-гидроксиэтил)пиперидина.
ПРИМЕР 6
5-[1-(4-гидрокси)пиперидинил]-3-фенил-барбитуровая кислота
5-[1-(4-гидрокси)пиперидинил] -5-фенил-барбитуровую кислоту с выходом 39%; т.пл.: 241-242oC (из этанола) получают аналогично примеру 4, используя 4-гидрокси-пиперидин вместо 4-(2- гидроксиэтил)пиперидина.
ПРИМЕР 7
5-[1-(4,4-диметил)пиперидинил]-5-фенил-барбитуровая кислота
5-[1-(4,4-диметил)пиперидинил] -5-фенил-барбитуровую кислоту с выходом 69%; т. пл.: 238-240oC (из этанола/воды) получают аналогично примеру 4, используя 4,4-диметилпиперидин вместо 4-(2-гидроксиэтил) пиперидина.
ПРИМЕР 8
5-[1-(4-метил)пиперидинил]-5-фенил-барбитуровая кислота
5-[1-(4-метил)пиперидинил] -5-фенил-барбитуровую кислоту с выходом 87%; т.пл.: 208-209oC (из метанола/воды) получают аналогично примеру 4, используя 4-метил-пиперидин вместо 4-(2- гидроксиэтил)пиперидина.
ПРИМЕР 9
5-[1-(4-метокси)пиперидинил]-3-фенил-барбитуровая кислота
5-[1-(4-метокси)пиперидинил]-5-фенил-барбитуровую кислоту с выходом 67%; т. пл.: 184-185oC (из этанола/воды) получают аналогично примеру 4, используя 4-метокси-пиперидин вместо 4-(2-гидроксиэтил) пиперидина.
ПРИМЕР 10
5-этил-5-[1-(4-мeтил)пиперидинил]барбитуровая кислота
14,1 г (75 ммоль) диэтилового эфира этилмалоновой кислоты и затем 15 г (264 ммоль) мочевины медленно добавляют к 1,95 г натрия в 60 мл метанола при перемешивании. После кипячения в течение 2 часов образуется осадок. Его охлаждают до 10-15oC и последовательно медленно смешивают с 15 г (15 ммоль) 4-метилпиперидина, 21 г (150 ммоль) карбоната калия и 4,3 мл (168 ммоль) брома. Смесь перемешивают в течение 2 часов при этой температуре, медленно доводят до кипения и нагревают в течение 1 часа с обратным холодильником. После охлаждения ее выливают в 360 мл 1N азотной кислоты, раствор один раз промывают толуолом и смешивают с избытком насыщенного раствора ацетата натрия. Высаженный осадок перекристаллизовывают из этанола с добавлением активного углерода. Выход: 4,4 г = 23%; т.пл.: 194- 195oC.
ПРИМЕР 11
5-этил-5-[1-(4-метокси) пиперидинил] барбитуровая кислота
5-этил-5-[1-(4-метокси) пиперидинил] барбитуровую кислоту с выходом 15%; т. пл. 201-202oC (из этанола) получают аналогично примеру 10, используя 4-метоксипиперидин вместо 4-метилпиперидина.
ПРИМЕР 12
5-этил-5-[1-(4-гидрокси)пиперидинил]барбитуровая кислота
5-этил-5-[1-(4-гидрокси)пиперидинил] барбитуровую кислоту с выходом 5%; т. пл. : 110-112o (из этанола) получают аналогично примеру 10, используя 4-гидроксипиперидин вместо 4-метоксипиперидина.
ПРИМЕР 13
5-этил-5-[1-(4-(2-гидpoкcиэтил)пиперидинил)]барбитуровая кислота
5-этил-5-[1-(4-(2-гидроксиэтил)пиперидинил)] барбитуровую кислоту с выходом 17%; т. пл.: 238-240oC (из метанола) получают аналогично примеру 10, используя 4-(2-гидроксиэтил)пиперидин вместо 4-метилпиперидина.
ПРИМЕР 14
5-(4-метоксифенил)-5-[N-(2-гидpoкcиэтил) пиперазинил]барбитуровая кислота
а) получение этил 4-метоксифенилацетата
Раствор 4-метоксифенилуксусной кислоты (2 г) и пара-толуолсульфокислоты (230 мг) в 30 мл этанола кипятят с обратным холодильником в течение 2 часов. Растворитель выпаривают при пониженном давлении, и остаток суспендируют в насыщенном водном растворе кислого углекислого натрия и дважды экстрагируют этилацетатом. Органические экстракты собирают, промывают водой и высушивают над сульфатом натрия с образованием после выпаривания растворителя при пониженном давлении 2,14 г продукта.
b) получение этил 4-метоксифенилмалоната
Смесь этил 4-метоксифенилацетата (27,8 г) и натрия (3,68 г) в 90 мл диэтилугольного эфира кипятят с обратным холодильником в течение 3 часов, затем растворитель выпаривают при пониженном давлении и остаток разбавляют водой и нейтрализуют уксусной кислотой. Водную фазу экстрагируют дважды диэтиловым эфиром. Органические экстракты объединяют и дважды промывают 1N гидроокисью натрия и один раз водой, затем органическую фазу высушивают над сульфатом натрия и концентрируют досуха. Получают 34,2 г продукта.
с) получение 5-(4-метоксифенил)барбитуровой кислоты
К раствору 660 мг натрия в 50 мл этанола добавляют 3,86 г этил 4-метоксифенилмалоната и 1,28 г мочевины. Реакционную смесь кипятят с обратным холодильником в течение 3 часов. Выпадает белый осадок, который собирают фильтрованием и вновь растворяют в 15 мл воды. Раствор подкисляют до pH 1-2 добавлением 6N соляной кислоты. Выпадает белый осадок, который отфильтровывают и промывают на фильтре водой. После высушивания под вакуумом при 50oС в течение нескольких часов, получают 2,2 8 г продукта.
d) получение 5-бром-5-(4-метоксифенил)барбитуровой кислоты
К суспензии 5-(4-метоксифенил)барбитуровой кислоты (222 мг) в 3 мл воды, охлажденной до 0-5oC в ледяной бане, добавляют 136 мкл 48% бромистоводородной кислоты и 56 мкл брома по каплям. Через 1 час при температуре ниже 10oC, выпавший осадок собирают фильтрованием и промывают на фильтре водой. Осадок высушивают в течение нескольких часов под вакуумом при 50oC, для получения 283 мг продукта.
е) получение титульного соединения
Раствор 5-бром-5-(4-метоксифенил)барбитуровой кислоты (11,5 г) и N-(2-гидроксиэтил)пиперазина (15,755 г) в 260 мл метанола кипятят с обратным холодильником примерно в течение 2 часов, затем выпавший осадок собирают фильтрованием, вновь растворяют в 100 мл метанола и нагревают с обратным холодильником в течение 1 часа. Осадок вновь отфильтровывают и высушивают при 80oC под вакуумом для получения 9 г продукта, содержащего 8-9% метанола. Осадок растворяют в 40 мл 1N соляной кислоты, затем раствор подщелачивают 3,42 г кислого углекислого натрия и охлаждают при 0-5oC в течение 4 часов. Продукт выделяют фильтрованием и высушивают под вакуумом при 80oC в течение нескольких часов с образованием 8,55 г чистого продукта; т.пл. 247-248oC.
1H-ЯМР в d6-AMCO: 2,36 ppm (m, 6H); 2,55 ppm (m, 4H); 3,44 ppm (q, 2H); 3,74 ppm (s, 3H); 4,33 ppm (t, 1H); 6,95 ppm (d, 2H); 7,3 ppm (d, 2H); 11,54 ppm (br s, 2H).
ПРИМЕР 15
5-[3-(4-метоксифенил)пропил]-5-[4-(2- гидроксиэтил)пиперазинил]барбитуровая кислота.
а) получение 3-(4-метоксифенил)пропионилхлорида
К суспензии 3-(4-метоксифенил)пропионовой кислоты (10 г) в 150 мл толуола добавляют 8 мл хлористого тионила и смесь нагревают до 64oC в течение 4 часов. Растворитель выпаривают при пониженном давлении и остаток вновь растворяют в толуоле и концентрируют досуха. Эту стадию повторяют дважды. Получают 11 г продукта в виде желтого масла.
b) получение 5-[3-(4-метоксифенил)пропионил]барбитуровой кислоты
К суспензии барбитуровой кислоты (6,4 г) в 48 мл пиридина по каплям добавляют 11 г 3-(4-метоксифенил) пропионилхлорида и смесь перемешивают при комнатной температуре в течение 18 часов. Реакционную смесь выливают на лед и подкисляют до pH 1 с добавлением 6N соляной кислоты. Выпадает осадок, который фильтруют и вновь суспендируют в метаноле. Суспензию перемешивают в течение 15 минут, затем отделяют фильтрованием осадок с образованием 12,2 г продукта; т.пл.: 248-250oC.
с) получение 5-[3-(4-метоксифенил)пропил]барбитуровой кислоты
К суспензии 10 г 5-[3-(4-метоксифенил)пропионил] барбитуровой кислоты в 100 мл уксусной кислоты добавляют порционно 4,5 г цианборгидрида натрия, затем смесь нагревают до 60oC. Через 1 час реакционную смесь охлаждают до комнатной температуры и выливают на лед. Через 30 минут фильтрованием получают осадок, который высушивают под вакуумом при 50oC с образованием 8,74 г продукта; т.пл.: 195-197oC.
d) получение 5-бром-5-[3-(4-метоксифенил)пропил] барбитуровой кислоты
Смесь 5-[3-(4-метоксифенил) пропил] барбитуровой кислоты (2,5 г), N-бромсукцинимида (2 г) и перекиси дибензоила (каталитическое количество) в 110 мл четыреххлористого углерода кипятят с обратным холодильником в течение 1 часа, затем осадок отделяют фильтрованием. Осадок вновь растворяют в этилацетате и фильтруют через слой силикагеля для того, чтобы удалить остаток сукцинимида. Органическую фазу концентрируют досуха и остаток кристаллизуют из смеси диэтилового эфира/четыреххлористого углерода. Выпадает бледно-желтый осадок, который собирают фильтрованием и высушивают под вакуумом при 60oC с образованием 2,8 г продукта; т.пл.: 113-114oC.
е) получение титульного соединения
Смесь 5-бром-5-[3-(4- метоксифенил)пропил]барбитуровой кислоты (710 мг) и N-(2-гидроксиэтил)пиперазина (281 мг) в 25 мл этанола кипятят с обратным холодильником в течение 4 часов. Растворитель выпаривают при пониженном давлении и остаток распределяют между 1N соляной кислотой и этилацетатом. Водную фазу подщелачивают до pH 6-7 и экстрагируют этилацетатом. Органическую фазу концентрируют досуха и остаток кристаллизуют из этилацетата с образованием 30 мг продукта.
1H-ЯМР в d6-ДМСО: 1,32 ppm (m, 2H); 1,86 ppm (m, 2H), 2,33 ppm (m, 6H); 2,45 ppm (m, 2H); 2,53 ppm (m, 4H); 3,43 ppm (q, 2H); 3,7 ppm (s, 3H); 4,35 ppm (t, 1H); 6,8 ppm (d, 2H); 7,04 ppm (d, 2H); 11,53 ppm (br s, 2H).
ПРИМЕР 16
5-фенил-5-[4-(2-гидpoкcэтилиден)пиперидинил] барбитуровая кислота
а) получение 4-(этоксикарбонилметилиден)пиперидина
К суспензии гидрида натрия (2,6 г) в 30 мл тетрагидрофурана, охлажденного до 0oC и хранимого под азотом, по каплям добавляют 13 мл триэтилфосфоноацетата, растворенного в 10 мл тетрагидрофурана. Затем температуру доводят до комнатной и перемешивают в течение 30 минут. Смесь вновь охлаждают до 0oC и по каплям добавляют раствор, полученный при порционном добавлении к раствору 4-пиперидонмоногидрата гидрохлорида (10 г) в ТГФ, 2,6 г натрия гидрида, профильтровывают для удаления образовавшегося хлорида натрия. В конце добавления, температуру доводят до комнатной и продолжают перемешивать в течение 20 часов. Растворитель упаривают при пониженном давлении и остаток вновь растворяют в этилацетате и промывают 1N соляной кислотой. Водную фазу экстрагируют этилацетатом и хлороформом, затем ее подщелачивают до pH 9-10 добавлением 20% гидроксида натрия и экстрагируют хлороформом. Водную фазу затем высаливают и вновь экстрагируют три раза хлороформом. Объединенные экстракты высушивают над сульфатом натрия и выпаривают с образованием 7,1 г продукта в форме желтого масла.
b) получение 4-(гидроксиэтилиден)пиперидина
К раствору 15 мл DIBAL (1,5 М раствор в толуоле) в 20 мл толуола по каплям добавляют 0,976 г 4-(этоксикарбонилметилиден) пиперидина, растворяют в нескольких миллилитрах толуола. Реакционную смесь перемешивают при комнатной температуре в течение 2 часов, затем охлаждают до 0-5oC и по каплям добавляют метанол, пока заметно образование газа. Смесь концентрируют до небольшого объема и добавляют диэтиловый эфир: выпадает белый осадок, который отфильтровывают. Органическую фазу концентрируют досуха, вновь растворяют в диэтиловом эфире и вновь фильтруют. Чистый раствор концентрируют досуха с образованием 500 мг продукта.
с) получение титульного соединения
Смесь 5-бром-5-фенилбарбитуровой кислоты (2,45 г), 4- гидроксиэтилиден)пиперидина (1,053 г) и триэтиламина (1,15 мл) в 50 мл этанола кипятят с обратным холодильником в течение 2 часов. Растворитель выпаривают при пониженном давлении и остаток очищают хроматографией на силикагеле (40 г; элюент: этилацетат/петролейный эфир 8:2) с образованием 450 мг продукта.
1H-ЯМР в d6-ДМСО: 2,13 ppm (m, 4H); 2,55 ppm (m, 4H); 3,89 ppm (d, 2H); 4,46 ppm (br s, 1H); 5,24 ppm (t, 1H); 7,42 ppm (m, 5H); 11,6 pp, (br s, 2H).
50 мг 5-фенил-5- [4-(2- гидроксиэтил)-1, 2,5,6-тетрагидропиридинил] барбитуровой кислоты получают в качестве побочного продукта.
1H-ЯМР в d6-ДМСО: 1,96 ppm (m, 2H); 2,09 ppm (t, 2H); 2,64 ppm (t, 2H); 3,00 ppm (m, 2H); 3,47 ppm (q, 2H); 4,43 ppm (t, 1H); 5,3 ppm (m, 1H); 7,4 ppm (s, 5H); 11,63 ppm (br s, 2H).
ПРИМЕР 17
5-фенил-5-[N-(2-гидроксиэтил)пиперазинил]-2- тиобарбитуровая кислота
а) получение диэтил 2-бром-2-фенилмалоната
К раствору диэтил 2-фенилмалоната (15 мл) в 200 мл тетрагидрофурана, хранимого при 0oC и атмосфере азота, добавляют 3,475 мг гидрида натрия и смесь выдерживают 30 минут при перемешивании при 0oC, затем температуру доводят до комнатной. После охлаждения вновь до 0oC, в реакционную смесь добавляют 14,3 г N-бромсукцинимида. Через примерно 15 минут выпадает белый осадок, который отфильтровывают и фильтрат концентрируют досуха с образованием остатка, который вновь растворяют в хлороформе и высушивают над сульфатом натрия. Растворитель выпаривают при пониженном давлении с образованием 15,66 г продукта.
b) приготовление диэтил 2-фенил-2-[4-(2-гидроксиэтил) пиперазинил] малоната
Раствор диэтил 2-бром-2-фенилмалоната (16,8 г) в 150 мл диметилсульфоксида нагревают до 90-100oC, затем добавляют N-(2- гидроксиэтил)пиперазин (27,9 г) и реакционную смесь нагревают в течение дополнительных 4 часов. Смесь выливают в воду и три раза экстрагируют этилацетатом. Объединенные органические экстракты промывают 1N соляной кислотой. Водную фазу подщелачивают 1N гидроксидом натрия до pH 8-9 и дважды экстрагируют этилацетатом. Органические экстракты собирают и промывают насыщенным водным раствором хлорида натрия и высушивают над сульфатом натрия. После удаления растворителя при пониженном давлении, остаток кристаллизуют из диэтилового эфира/петролейного эфира 1:1 с образованием 6,5 продукта; т.пл.: 63-64oC.
с) получение титульного соединения
К раствору натрия (27 мг) в 3 мл этанола добавляют 218 мг диэтил 2-фенил-2-[4-(2-гидроксиэтил)пиперазинил] малоната и 288 мг тиомочевины, затем смесь кипятят с обратным холодильником в течение 13 часов. Реакционную смесь охлаждают до комнатной температуры и добавляют 140 мкл уксусной кислоты, затем растворитель выпаривают при пониженном давлении. Остаток вновь растворяют в смеси этилацетата/метанола 9:1. Выпавший осадок отделяют фильтрованием и фильтрат концентрируют досуха и очищают хроматографией на силикагеле(элюент: от этилацетата до этилацетата/метанола 9:1), с образованием после кристаллизации из этилацетата 30 мг продукта; т.пл.: > 250oC.
1H-ЯМР в d6-ДМСО: 2,4 ppm (m, 6H); 2,59 ppm (m, 4H); 3,46 ppm (q, 2H); 4,4 ppm (t, 1H); 7,4 ppm (m, 5H); 12,5 ppm (br s, 2H).
ПРИМЕР 18
5-фенил-5-[N-(2-гидроксиэтил)пиперазинил]-2- азобарбитуровая кислота.
К раствору натрия (70 мг) в 5 мл этанола добавляют 218 мг диэтил 2-фенил-2-[4-(2-гидроксиэтил)пиперазинил] малоната (пример 4 - пункт b) и 172 мг гуанидин гидрохлорида и смесь кипятят с обратным холодильником в течение 8 часов. Затем добавляют еще 57 мг гуанидин гидрохлорида и смесь кипятят с обратным холодильником еще 6 часов. Доводят температуру до комнатной и добавляют уксусную кислоту, пока не произойдет нейтрализация, выпадает осадок, который отфильтровывают. Фильтрат концентрируют досуха и повторно растворяют в этаноле, из которого при добавлении этилацетата выпадает осадок. Через 1 час при -4oC получают фильтрованием белый осадок и его перекристаллизуют из метанола (2 мл) с образованием после высушивания в вакууме при 90oC в течение 4 часов 78 мг продукта; т.пл.: > 250oC.
1H-ЯМР в d6-ДМСО: 2,33 ppm (m, 6H); 2,54 ppm (m, 4H); 3,41 ppm (t, 2H); 4,33 ppm (br s, 1H); 7,00 ppm (br s, 1H); 7,33 ppm (m, 5H); 7,5 ppm (br s, 1H); 11,4 ppm (br s, 1H).
ПРИМЕР 19
5-бензил-5-[N-(2-гидpoкcиэтил)пиперазинил] барбитуровая кислота
а) получение 5-бензилиденбарбитуровой кислоты
Суспензию 5 г барбитуровой кислоты в 50 мл воды нагревают до того, как произойдет полное растворение, затем добавляют 4,3 мл бензальдегида. Смесь кипятят с обратным холодильником в течение 1 часа, затем фильтрованием отделяют осадок, несколько раз промывают водой и высушивают в вакууме при 100oC с образованием 8,17 г продукта; т.пл.: > 258oC.
b) получение 5-бензилбарбитуровой кислоты
К суспензии 5-бензилиденбарбитуровой кислоты (4 г) в 200 мл метанола порционно добавляют 1,4 г боргидрида натрия. Через 10 минут после конца добавления, добавляют 100 мл воды и смесь подкисляют 1N соляной кислотой до pH 2. Растворитель выпаривают и водную фазу экстрагируют этилацетатом. Объединенные экстракты высушивают над сульфатом натрия и концентрируют досуха. Кристаллизуется 3,6 г продукта; т.пл.: 207-209oC.
с) получение 5-бром-5-бензилбарбитуровой кислоты
К суспензии 5-бензилбарбитуровой кислоты (1,7 г) в 15 мл воды, охлажденной до 0-5oC, добавляют 1 мл 48% бромистоводородной кислоты, с последующим добавлением в реакционную смесь по каплям 0,437 мл брома. Через 1 час перемешивания при температуре ниже 10oC, выпадает осадок, который отделяют фильтрованием и промывают водой. Получают 2,17 г продукта; т.пл.: 164-166oC.
d) получение титульного соединения
Раствор 5-бром-5-бензилбарбитуровой кислоты (2,15 г) и N-(2- гидроксиэтил)пиперазина в 50 мл этанола кипятят с обратным холодильником в течение 4 часов, затем охлаждают до комнатной температуры и добавляют 4 мл триэтиламина. Растворитель выпаривают и белый осадок вновь растворяют в смеси этилацетата/метанола 3: 1. Кристаллизуется оранжевый твердый осадок, который выделяют фильтрованием. После перекристаллизации из этанола получают 0,62 г продукта, который отделяют фильтрованием. После перекристаллизации из этанола получают 0,62 г продукта; т.пл.: 243-246oC.
1H-ЯМР в d6-ДМСО: 2,43 ppm (t, 2H); 2,58 ppm (m, 4H); 3,03 ppm (m, 4H); 3,34 ppm (s, 2H); 3,49 ppm (q, 2H); 4,5 ppm (t, 1H); 7,13 ppm (m, 5H); 8,8 ppm (br s, 2H).
ПРИМЕР 20
5-[N-(2-гидроксиэтил)пиперазинил] -5-(4-гидpoкcифeнил) барбитуровая кислота
а) получение 5-(4-гидроксифенил)барбитуровой кислоты
К суспензии 5-(4-метоксифенил)барбитуровой кислоты (222 мг) в 5 мл метиленхлорида, хранимого при -5/-10oC и в атмосфере азота, по каплям добавляют трехбромистый бор (473 мкл) в 2 мл метиленхлорида. Перемешивание продолжают еще 2 часа при -5oC, затем температуру доводят до комнатной и перемешивают еще 20 часов. Реакционную смесь вновь охлаждают до 0oC в ледяной бане и подщелачивают до pH 9-10 добавлением по каплям 5% гидроксида натрия. Водную фазу отделяют, фильтруют через слой целита, охлаждают в ледяной бане и подкисляют до pH 1 с помощью 37% соляной кислоты. Выпадает осадок, который отделяют через 1 час фильтрованием и высушивают в вакууме при 60oC с образованием 215 мг продукта.
b) получение 5-[4-(третбутилдиметилсилилокси)фенил] барбитуровой кислоты
К раствору 5-(4-гидроксифенил)барбитуровой кислоты (1,9 г) и третбутилдиметилсилилхлорида (4,68 г) в 20 мл безводного диметилформамида добавляют 4,4 г имидазола и смесь нагревают до 55oC в течение 5 часов. Затем температуру доводят до комнатной и реакционную смесь выливают в 1N соляную кислоту и дважды экстрагируют этилацетатом. Объединенные органические экстракты промывают водой и высушивают над сульфатом натрия. При концентрировании раствора выпадает белый осадок, который хранят в течение ночи при 0oC, затем фильтруют с образованием 2,185 г продукта.
с) получение 5-бром-5-[(4-третбутилдиметилсилилокси)фенил] барбитуровой кислоты
К суспензии 5-[4-(третбутилдиметилсилиокси)фенил] барбитуровой кислоты (330 мг) и перекиси дибензоила (каталитическое количество) в 10 мл четыреххлористого углерода добавляют 210 мг N-бромсукцинимида. Смесь перемешивают при комнатной температуре в течение 1 часа, затем растворитель выпаривают и остаток очищают хроматографией на силикагеле (элюент: петролейный эфир/этилацетат 8:2) с образованием 260 мг продукта.
d) получение 5-[N-(2-гидроксиэтил)пиперазинил] -5-[(4- третбутилдиметилсилилокси)фенил]барбитуровой кислоты
Раствор 5-бром-5-[(4-третбутилдиметилсилилокси)фенил] - барбитуровой кислоты (260 мг) и N-(2-гидроксиэтил)пиперазина (98 мг) в 5 мл этанола кипятят с обратным холодильником в течение 1 часа, затем доводят температуру до комнатной и добавляют 0,3 мл триэтиламина. Растворитель выпаривают и остаток очищают хроматографией на силикагеле (25 г; элюент: этилацетат/метанол 3:1) с образованием после кристаллизации из этилацетата, 170 мг продукта; т.пл.: 220-221oC.
е) получение титульного соединения
Смесь 5-[N-(2-гидроксиэтил)пиперазинил] -5-[(4- третбутилдиметилсилилокси)фенил] барбитуровой кислоты (148 мг), фторида тетрабутиламмония (1,1 М в ТГФ; 0,6 мл) и уксусной кислоты (290 мкл) в 10 мл тетрагидрофурана перемешивают в течение 2 часов 30 минут при 0oC, затем растворитель выпаривают и остаток очищают хроматографией на силикагеле (12 г, элюент: этилацетат/метанол 3: 1), с образованием после кристаллизации из этилацетата и перекристаллизации из смеси этилацетата/метанола 40 мг продукта, т.пл.: > 25oC.
1H-ЯМР в d6-AMCO: 2,37 ppm (m, 6H); 2,55 ppm (m, 4H); 3,45 ppm (q, 2H); 4,35 ppm (t, 1H); 6,76 ppm (d, 2H); 7,17 ppm (d, 2H); 9,72 ppm (s, 1H); 11,47 ppm (br s, 2H).
ПРИМЕР 21
5-[N-(2-гидpoкcиэтил)пиперазинил] -5-(3-гидроксифенил) барбитуровая кислота
а) получение этил 3-гидроксифенилацетата
Суспензию 3-гидроксифенилуксусной кислоты (5,4 г) и пара- толуолсульфокислоты (650 мг) в 80 мл этанола кипятят с обратным холодильником в течение 4 часов, растворитель затем выпаривают и остаток растворяют в этилацетате и промывают дважды насыщенным водным раствором кислого углекислого натрия. Органическую фазу высушивают над сульфатом натрия и растворитель выпаривают с образованием 6,08 г продукта в виде желтого масла.
b) получение этил 3-(третбутилдиметилсилилокси) фенилацетата
К раствору этил 3-гидроксифенилацетата (6 г) и третбутилдиметилсилилхлорида (6 г) в 80 мл безводного диметилформамида добавляют 5,66 г имидазола и смесь перемешивают при комнатной температуре в течение 1 часа 30 минут. Затем реакционную смесь выливают в воду и дважды экстрагируют этилацетатом. Объединенные органические экстракты высушивают над сульфатом натрия и концентрируют досуха с образованием 10 г продукта в виде желтого масла.
с) получение диэтил 3-(третбутилдиметилсилилокси)фенилмалоната
К раствору этил 3-(третбутилдиметилсилилокси)фенилацетата (10 мг) в 25 мл диэтилкарбоната порционно добавляют 0,86 т натрия и смесь кипятят с обратным холодильником в течение 2 часов. Растворитель выпаривают и остаток выливают в воду (90 мл). pH доводят до pH=6 уксусной кислотой и смесь экстрагируют диэтиловым эфиром. Органическую фазу высушивают над сульфатом натрия и концентрируют досуха с образованием 10 г оранжевого масла, которое очищают хроматографией на силикагеле (элюент: петролейный эфир/этилацетат 95:5), с образованием 2,45 г продукта.
d) получение 5-[3-(третбутилдиметилсилилокси)фенил] барбитуровой кислоты
К раствору диэтил 3-(третбутилдиметилсилилокси) фенилмалоната (1,5 г) в 15 мл этанола добавляют 0,445 г этилата натрия и 0,295 г мочевины и смесь кипятят с обратным холодильником в течение 3 часов. Реакционную смесь охлаждают до комнатной температуры и образовавшийся твердый осадок фильтруют. Осадок вновь растворяют в воде, pH доводят до pH 1-2 6 N соляной кислотой и выпавший осадок извлекают фильтрованием. Фильтрат концентрируют для удаления этанола, затем раствор подщелачивают и экстрагируют этилацетатом. Органическую фазу концентрируют досуха с образованием 250 мг остатка, который объединяют с ранее отфильтрованным осадком (350 мг). Полученный таким образом остаток включает смесь продукта наряду с десилилированным производным.
Подобный остаток (550 мг) растворяют в 5 мл безводного диметилформамида и добавляют последовательно 790 мг третбутилдиметилсилилхлорида и 745 мг имидазола. Смесь нагревают до 55oC в течение 5 часов. Добавляют еще 75 мг имидазола и 79 мг третбутилдиметилсилилхлорида и продолжают нагревание еще час. Затем реакционную смесь выливают в 1 N соляную кислоту и три раза экстрагируют этилацетатом. Объединенные органические экстракты промывают водой и высушивают над сульфатом натрия. Раствор концентрируют, и выпадает белый осадок. 710 мг продукта выделяют фильтрованием.
е) получение 5-[3-третбутилдиметилсилилокси)фенил]-5- бромбарбитуровой кислоты
Смесь 5-[3-(третбутилдиметилсилилокси)фенил] барбитуровой кислоты (680 мг), N-бромсукцинимида (432 мг) и перекиси дибензоила (каталитическое количество) в 10 мл четыреххлористого углерода перемешивают при комнатной температуре в течение 1 часа. Растворитель выпаривают и остаток очищают хроматографией на силикагеле (элюент: этилацетат/гексан 7:3) с образованием 550 мг продукта; т.пл.: 170-172oC.
f) получение 5-[N-(2-гидроксиэтил)пиперазинил]-5-[3- третбутилдиметилсилилокси)фенил]барбитуровой кислоты
Раствор 5-[3-(третбутилдиметилсилилокси)фенил] -5-бром- барбитуровой кислоты (444 мг) и N-(2-гидроксиэтил)пиперазина (420 мг) в 10 мл метанола перемешивают при комнатной температуре в течение 5 часов, затем растворитель выпаривают и остаток очищают хроматографией на силикагеле (13 г; элюент: этилацетат/метанол 3:1) с образованием 70 мг продукта.
g) получение титульного соединения
К раствору 5-[N-(2-гидроксиэтил)пиперазинил]-5-[3- (третбутилдиметилсилилокси) фенил]барбитуровой кислоты (170 мг) в 12 мл тетрагидрофурана, хранимого при 0oC и в атмосфере азота, добавляют 333 мкл уксусной кислоты и 0,69 мл фтористого тетрабутиламмония. Смесь перемешивают в течение 3 часов, затем растворитель выпаривают и остаток очищают хроматографией на силикагеле (15 г; элюент: этилацетат/метанол 4:1), с образованием после кристаллизации из метанола 35 мг продукта; т.пл.: 219-221oC.
1H-ЯМР в d6-ДМСО: 2,37 ppm (m, 6H); 2,59 ppm (m, 4H); 3,45 ppm (q, 2H); 4,35 ppm (t, 1H); 6,74 ppm (m, 2H); 6,92 ppm (t, 1H); 7,18 ppm (t, 1H); 9,62 ppm (s, 1H); 11,54 ppm (br s, 2H).
ПРИМЕР 22
5-[N-(2-гидроксиэтил)пиперазинил]-5-(4-метилфенил) барбитуровая кислота
а) получение 5-(4-метилфенил)барбитуровой кислоты
К раствору натрия (184 мг) в 12 мл этанола добавляют 0,95 мл диэтил 2-(4-метилфенил)малоната и 360 мг мочевины, затем смесь кипятят с обратным холодильником в течение 3 часов. Выпадает белый осадок, который отфильтровывают и вновь растворяют в 4 мл воды. Раствор подкисляют до pH 1-2 добавлением 6N соляной кислоты. Выпадает белый осадок, который собирают фильтрованием, промывают 15 мл воды и высушивают под вакуумом. Получают 619 мг продукта; т.пл.: 271oC.
b) получение 5-бром-5-(4-метилфенил)барбитуровой кислоты
К суспензии 5-(4-метилфенил) барбитуровой кислоты (218 мг) в 2 мл воды при 10oC при перемешивании, добавляют 136 мкл 48% бромистоводородной кислоты, затем 56 мкл брома по каплям и перемешивают в течение 3 часов. Образовавшийся осадок выделяют фильтрованием и промывают водой, затем высушивают под вакуумом с образованием 270 мг продукта; т.пл.: 210-213oC.
с) получение титульного соединения
Раствор 5-бром-5-(4-метилфенил)барбитуровой кислоты (3,1 г) и N-(2-гидроксиэтил)пиперазина (1,53 г) в 60 мл этанола кипятят с обратным холодильником в течение 3 часов. Растворитель выпаривают и остаток растворяют в 1N соляной кислоте и дважды промывают этилацетатом. Водную фазу подщелачивают 1N гидроксидом натрия и экстрагируют этилацетатом. Органические экстракты концентрируют досуха и остаток очищают хроматографией на силикагеле (100 г, элюент: этилацетат/метанол 3:1) с образованием после выпаривания растворителя 1,97 г продукта в форме гидробромида.
Свободное основание получают обработкой суспензии (200 мл) соли в этилацетате 50 мл насыщенного водного раствора кислого углекислого натрия и экстракцией водной фазы этилацетатом. При концентрировании досуха объединенных органических экстрактов получают 1,18 г продукта.
1H-ЯМР в d6-ДМСО: 2,3 ppm (s, 3H); 2,35 ppm (m, 6H); 2,57 ppm (m, 4H); 3,45 ppm (q, 2H); 4,35 ppm (t, 1H); 7,19 ppm (d, 2H); 7,28 ppm (d, 2H); 11,55 ppm (br s, 2H).
ПРИМЕР 23
5-октил-5-[N-(2-гидроксиэтил)пиперазинил] барбитуровая кислота
а) получение диэтил 2-октилмалоната
К раствору 2,63 г натрия в 100 мл этанола по каплям добавляют раствор 19,1 мл диэтилмалоната в 10 мл этанола. В смесь последовательно добавляют 20,4 мл 1-бромоктана, растворенного в 10 мл этанола, затем смесь кипятят с обратным холодильником в течение 6 часов. Реакционную смесь концентрируют до небольшого объема и остаток распределяют между насыщенным водным раствором моногидрофосфата натрия (200 мл) и этилацетата (200 мл). Органическую фазу промывают 75 мл воды и 75 мл насыщенного водного раствора хлорида натрия, высушивают над сульфатом натрия и концентрируют досуха с образованием 3,18 г продукта в виде масла.
1H-ЯМР в CDCl3: 0,80-0,95 ppm (m, 3H); 1,15-1,40 ppm (m, 18H); 1,88 ppm (q, 2H); 3,33 ppm (t, 1H); 4,19 ppm (q, 4H).
b) получение 5-октилбарбитуровой кислоты
К раствору натрия (5,32 г) в 400 мл безводного этанола добавляют раствор диэтил 2-октилмалоната (31,5 г) в 50 мг этанола и последовательно 10,27 г мочевины, затем смесь кипятят с обратным холодильником в течение 2 часов 30 минут. Смесь быстро охлаждают до комнатной температуры и образовавшийся осадок отделяют фильтрованием и промывают диэтиловым эфиром. Затем осадок растворяют в 200 мл воды и подкисляют 6N соляной кислотой до pH 1,5-2. Выпадает осадок. В смесь добавляют 200 мл этилацетата и перемешивают в течение 2 часов, затем добавляют еще 800 мл теплого этилацетата. Органическую фазу отделяют и водную фазу промывают 200 мл этилацетата. Объединенные органические фазы промывают 250 мл насыщенного раствора хлорида натрия, высушивают над сульфатом натрия и концентрируют досуха. Получают 21,03 г продукта.
1H-ЯМР в d6-ДМСО: 0,77-0,80 ppm (m, 3H); 1,23 ppm (s, 12H); 1,80-1,95 ppm (m, 2H); 3,52 ppm (t, 1H); 11,15 ppm (s, 2H).
с) получение 5-бром-5-октилбарбитуровой кислоты
К суспензии 5-октилбарбитуровой кислоты (20 г) в 120 мл воды, охлажденной до 0-5oC, добавляют 12 мл 48% бромистоводородной кислоты и последовательно по каплям 4,72 мл брома. Через 2 часа перемешивания образовавшийся белый осадок отделяют фильтрованием, промывают водой и распределяют между 200 мл диэтилового эфира и 100 мл воды. Водную фазу экстрагируют дополнительно 50 мл диэтилового эфира. Объединенные органические фазы промывают 75 мл насыщенного водного раствора хлорида натрия, высушивают над сульфатом натрия и концентрируют досуха. Получают 25,8 г продукта в форме белого осадка.
1H-ЯМР в d6-AMCO: 0,78-0,90 ppm (m, 3H); 1,10-1,38 ppm (m, 12H); 2,20-2,34 ppm (m, 2H); 11,80 ppm (s, 2H).
d) получение титульного соединения
К раствору 5-бром-5-октилбарбитуровой кислоты (23,52 г) в 70 мл диметилсульфоксида, в атмосфере азота и при температуре 5-10oC по каплям добавляют N-(2-гидроксиэтил)пиперазин (36,2 мл), затем смесь перемешивают при комнатной температуре в течение 2 часов 30 минут. Реакционную смесь выливают в воду (1 л) при перемешивании и охлаждают в ледяной бане. Образовавшийся белый осадок получают фильтрованием, промывают водой и высушивают в вакууме при 40oC с образованием после кристаллизации из этанола (140 мл) 10,91 г продукта в форме белого осадка; т.пл.: 183-184oC.
1H-ЯМР в d6-AMCO: 0,75-0,88 ppm (m, 3H); 0,90-1,10 ppm (m, 2H); 1,12-1,30 ppm (m, 10H); 1,75-1,90 ppm (m, 2H); 2,23-2,40 ppm (m, 6H); 2,45-2,60 ppm (m, 4H); 3,45 ppm (br t, 2H); 4,35 ppm (br s, 1H); 11,55 ppm (s, 2H).
ПРИМЕР 24
5-нафтил-5-[N-(2-гидроксиэтил)пиперазинил] барбитуровая кислота
а) получение этил 2-нафтилацетата
К раствору 2-нафтилуксусной кислоты (5 г) в 50 мл этанола добавляют 0,5 г пара-толуолсульфокислоты, затем реакционную смесь кипятят с обратным холодильником в течение 4 часов. Растворитель выпаривают и остаток растворяют в диэтиловом эфире, дважды промывают насыщенным водным раствором кислого углекислого натрия и один раз рассолом, затем объединенные органические экстракты высушивают над сульфатом натрия и концентрируют досуха. Получают 5,64 г продукта в виде желтого масла.
b) получение диэтил 2-нафтилмалоната
К раствору этил 2-нафтилацетата (2 г) в 23,3 мл диэтилкарбоната при перемешивании и комнатной температуре порцией добавляют 0,232 г натрия. Реакционную смесь кипятят с обратным холодильником в течение 2 часов 30 минут, затем концентрируют для удаления непрореагировавшего диэтилкарбоната и добавляют 20 мл холодной воды. Полученную смесь подкисляют уксусной кислотой до слабой кислотности, затем три раза экстрагируют диэтиловым эфиром. Объединенные органические экстракты высушивают над сульфатом натрия и растворитель выпаривают для образования после перекристаллизации из диэтилового эфира (19 мл), 1,015 г продукта в форме белого осадка.
с) получение 5-нафтилбарбитуровой кислоты
В раствор натрия (0,32 г) в 30 мл безводного этанола добавляют диэтил 2-нафтилмалонат (2 г) и последовательно мочевину (0,63 г). Смесь кипятят с обратным холодильником в течение 2 часов, затем образовавшийся осадок отделяют фильтрованием, затем его растворяют в 7 мл воды и подкисляют до pH 1 6 N соляной кислотой. Через 30 минут перемешивания выпадает белый осадок, который отфильтровывают и промывают водой. Осадок высушивают в течение ночи под вакуумом, при 40oC с образованием 0,96 г продукта.
d) получение 5-бром-5-нафтилбарбитуровой кислоты
Суспензию 5-нафтилбарбитуровой кислоты (0,2 г) в 1,5 мл 95% этанола охлаждают до 0oC и при перемешивании по каплям добавляют 48% бромистоводородную кислоту (0,5 мл) и последовательно 4,4 мкл брома. Через 4 часа перемешивания при комнатной температуре отфильтровывают осадок и промывают водой, затем высушивают под вакуумом при 40oC в течение ночи. Получают 0,25 г продукта.
е) получение титульного соединения
К суспензии 5-бром-5-нафтилбарбитуровой кислоты (0,24 г) в 3,5 мл этанола добавляют раствор N-(2-гидроксиэтил)-пиперазиона (0,112 г) в 1,5 мл этанола. Реакционную смесь кипятят с обратным холодильником в течение 5 часов, затем охлаждают до комнатной температуры и выделившийся осадок отфильтровывают. В фильтрат добавляют 100 мкл триэтиламина, затем растворитель упаривают с образованием 0,364 г осадка, который перекристаллизуют из смеси метанола (4,5 мл) и этилацетата (10 мл). Полученный осадок (70 мг) промывают при перемешивании смесью этилацетата/воды в течение 2 часов и высушивают в вакууме при 40oC в течение 8 часов с образованием 60 мг продукта.
1H-ЯМР в d6-ДMCO: 2,3-2,5 ppm (m, 6H); 2,6 ppm (m, 4H); 3,45 ppm (m, 2H); 4,35 ppm (t, 1H); 7,4-8,1 ppm (m, 7H); 11,65 ppm (s, 2H).
ПРИМЕР 25
5-(4'-бифенил)-5-[N-(2-гидроксиэтил) пиперазинил]барбитуровая кислота
а) получение этил (4'-бифенил)ацетата
В суспензию (4'-бифенил) уксусной кислоты (6,4 г) в 60 мл этанола добавляют 1,1 г пара-толуолсульфокислоты, затем реакционную смесь кипятят с обратным холодильником в течение 4 часов 30 минут. Растворитель упаривают, остаток растворяют в диэтиловом эфире и полученную органическую фазу три раза промывают насыщенным водным раствором кислого углекислого натрия и один раз рассолом. Затем органическую фазу высушивают над сульфатом натрия и растворитель выпаривают с образованием 7,1 г продукта в виде желтого масла.
b) получение диэтил (4'-бифенил)малоната
К раствору этил (4'-бифенил) ацетата (7,1 г) в 60 мл диэтилкарбоната в атмосфере азота порцией добавляют натрий (0,734 г), затем нагревают при 120oC в течение 3 часов. Растворитель упаривают и остаток растворяют в 65 мл холодной воды и подкисляют уксусной кислотой до pH 5-6. Водную фазу три раза экстрагируют диэтиловым эфиром и объединенные органические экстракты высушивают над сульфатом натрия и концентрируют досуха. Остаток очищают хроматографией на силикагеле (элюент: петролейный эфир/диэтиловый эфир 9,4:0,6) с образованием 7,05 продукта; т.пл.: 51-53oC.
с) получение 5-(4'-бифенил)барбитуровой кислоты
К раствору натрия (0,322 г) в 40 мл безводного этанола добавляют диэтил (4'-бифенил)малонат (2,2 г) и последовательно мочевину (0,63 г). Реакционную смесь кипятят с обратным холодильником в течение 3 часов 30 минут, затем охлаждают до комнатной температуры и осадок выделяют фильтрованием. Полученный осадок вновь растворяют в 40 мл теплой воды и полученную водную фазу подкисляют до pH 1 6N соляной кислотой. Образовавшийся осадок перемешивают в течение 15 минут, затем отфильтровывают и сушат под вакуумом при 60oC. Получают 1,1 г продукта; т.пл.: > 240oC.
d) получение 5-бром-5-(4'-бифенил)барбитуровой кислоты
К суспензии 5-(4'-бифенил)барбитуровой кислоты (0,28 г) в 1,4 мл воды, охлажденной до 0oC и при перемешивании по каплям добавляют 0,14 мл 48% бромистоводородной кислоты и последовательно 55,5 мкл брома. Температуру доводят до комнатной и перемешивание продолжают в течение 1 часа. Взвешенный осадок выделяют фильтрованием, промывают водой и высушивают под вакуумом при 60oC в течение 2 часов с образованием 0,336 г продукта; т.пл.: 203-205oC.
е) получение титульного соединения
К суспензии 5-бром-5-(4'-бифенил)барбитуровой кислоты (0.323 г) в 4,4 мл этанола добавляют 0,14 г N-(2-гидроксиэтил) пиперазина и реакционную смесь кипятят с обратным холодильником в течение 2 часов. Взвешенный осадок отфильтровывают и полученный прозрачный раствор обрабатывают 125 мкл триэтиламина, затем растворитель выпаривают. Остаток вновь растворяют в 2 мл этанола, из которого кристаллизуется осадок, который перемешивают в течение 30 минут, затем отфильтровывают. Остаток перекристаллизуют из этанола с образованием 100 мг чистого продукта; т.пл.: 225-226oC.
1H-ЯМР в d6-ДМСО: 2,3-2,5 ppm (m, 6H); 2,65 ppm (m, 4H); 3,45 ppm (m, 2H); 4,4 ppm (s, 1H); 7,3-7,8 ppm (m, 9H); 11,6 ppm (s, 2H).
ПРИМЕР 26
5-(4'-бифенил)-5-[4-(нитрофенил)пиперазинил] барбитуровая кислота
К раствору 5-бром-5-(4'-бифенил)барбитуровой кислоты (0,359 г, пример 25, пункт d) в 9 мл метанола добавляют 0,622 г N-(4- нитрофенил)пиперазина и смесь кипятят с обратным холодильником примерно в течение 2 часов. Растворитель упаривают и остаток распределяют между водой и этилацетатом. Органическую фазу отделяют, промывают рассолом и высушивают над сульфатом натрия. Растворитель выпаривают при пониженном давлении с образованием 0,74 г осадка, который очищают хроматографией на силикагеле (элюент: метиленхлорид/ацетон 9:1) с образованием 400 мг продукта; т.пл.: 181oC.
1H-ЯМР в d6-ДМСО: 2,8 ppm (m, 4H); 3,5 ppm (m, 4H); 7,00 ppm (d, 2H); 7,3-7,85 ppm (m, 9H); 8,05 ppm (d, 2H); 11,7 ppm (s, 2H).
ПРИМЕР 27
5-(4'-феноксифенил)-5-[N-(2-гидроксиэтил)пиперазинил] барбитуровая кислота
а) получение N-[4'-феноксибензил)тиокарбонил]морфолина
Смесь (4'-феноксифенил)метилкетона (19,1 г), морфолина (20 мл) и серы (4,32 г) кипятят с обратным холодильником в течение 24 часов, затем экстрагируют диэтиловым эфиром. Органическую фазу концентрируют досуха с образованием после кристаллизации из смеси петролейного эфира/этилацетата 8:2 (600 мл), 12,2 г продукта; т.пл.: 75-77oC.
в) получение (4'-феноксифенил)уксусной кислоты
Суспензию N-[(4'-феноксибензил)тиокарбонил] морфолина (1,725 г) в 87 мл 10% гидроксида калия кипятят с обратным холодильником в течение 8 часов 30 минут, затем температуру реакционной смеси доводят до комнатной температуры и подкисляют 1N соляной кислотой. Выпавший белый осадок перемешивают в течение 30 минут и отфильтровывают. Осадок промывают водой и высушивают под вакуумом с образованием 1,095 г продукта; т.пл.: 70-72oC.
с) получение этил (4'-феноксифенил)ацетата
К суспензии (4'-феноксифенил) уксусной кислоты (0,456 г) в 4 мл этанола добавляют пара-толуолсульфокислоту (0,076 г) и полученную смесь кипятят с обратным холодильником в течение 2 часов. Растворитель упаривают, остаток растворяют в диэтиловом эфире и органическую фазу промывают насыщенным водным раствором кислого углекислого натрия и затем рассолом. Органическую фазу сушат над сульфатом натрия и концентрируют досуха с образованием 0,458 г продукта в форме коричневого масла.
d) получение 5-(4'-феноксифенил)барбитуровой кислоты
К раствору этилата натрия (0,27 г) в 3 мл безводного этанола добавляют 0,657 г этил (4'-феноксифенил)ацетата, растворенного в 5 мл этанола, затем мочевину (0,18 г). Реакционную смесь кипятят с обратным холодильником в течение 2 часов 30 минут, затем охлаждают до комнатной температуры и суспендированное твердое вещество отфильтровывают. Осадок вновь растворяют в 8 мл воды и раствор подкисляют 1N соляной кислотой. Выпавший твердый осадок отделяют фильтрованием с образованием 0,165 г продукта; т.пл. > 240oC.
е) получение 5-бром-5-(4'-феноксифенил)барбитуровой кислоты
К суспензии 5-(4'-феноксифенил)барбитуровой кислоты (48 мг) в 0,23 мл воды, охлажденной до 0oC и при перемешивании, добавляют 23 мкл 48% бромистоводородной кислоты и последовательно 9 мкл брома. Через 2 часа при комнатной температуре добавляют еще 9 мкл брома и перемешивание продолжают в течение 2 часов. Взвешенный осадок выделяют фильтрованием и промывают водой с образованием после высушивания под вакуумом при 60oC, 57 мг продукта; т.пл.: 125-126oC.
f) получение титульного соединения
К раствору 5-бром-5-(4'-феноксифенил)барбитуровой кислоты (50 мг) в 0,2 мл метанола добавляют по каплям раствор N-(2- гидроксиэтил)пиперазина (52 мг) в 0,6 мл метанола и смесь перемешивают в течение 2 часов. Белый осадок собирают фильтрованием и высушивают под вакуумом при 60oC в течение ночи. Получают 42,6 мг продукта; т.пл. > 240oC.
1H-ЯМР в d6-ДMCO: 2,2- 2,45 ppm (m, 6H); 2,55 ppm (m, 4H); 3,45 ppm (m, 2H); 4,4 ppm (t, 1H); 6,9-7,7 ppm (m, 9H); 11,6 ppm (s, 2H).
ПРИМЕР 28
5-децил-5-[N-(2-гидpoкcиэтил)пиперазинил] барбитуровая кислота
а) получение диэтилдецилмалоната
К раствору натрия (0,46 г) в 10 мл безводного этанола добавляют 3,35 мл диэтилмалоната в 3 мл этанола и последовательно раствор децилбромида (4,15 мл) в 3 мл этанола. Реакционную смесь кипятят с обратным холодильником в течение 4 часов, затем осадок отфильтровывают и фильтрат концентрируют досуха. Остаток вновь растворяют в насыщенном водном растворе кислого сернокислого натрия и экстрагируют этилацетатом. Органический экстракт высушивают над сульфатом натрия и растворитель выпаривают. Полученный остаток используют как таковой в последующей реакции.
b) получение 5-децилбарбитуровой кислоты
К раствору диэтилдецилмалоната по пункту а) в 40 мл этанола добавляют 2,72 г этилата натрия и затем 1,8 г мочевины. Реакционную смесь кипятят с обратным холодильником в течение 2 часов, затем осадок отфильтровывают и вновь растворяют в 40 мл воды. Полученный водный раствор подкисляют 6N соляной кислотой. Выпавший твердый осадок отделяют фильтрованием и высушивают под вакуумом при 40oC в течение ночи с образованием 2,152 г продукта; т.пл.: 190oC.
с) получение 5-бром-5-децилбарбитуровой кислоты
К суспензии 5-децилбарбитуровой кислоты (0,537 г) в 2,9 мл воды при перемешивании при комнатной температуре добавляют по каплям 0,29 мл 48% бромистоводородной кислоты. Смесь охлаждают до 0oC и по каплям добавляют 0,113 мл брома. Реакционную смесь перемешивают при комнатной температуре в течение 1 часа 30 минут, затем белый осадок отфильтровывают и затем промывают водой. Осадок распределяют между водой и диэтиловым эфиром, органическую фазу отделяют, промывают рассолом и в конце высушивают над сульфатом натрия. При выпаривании растворителя при пониженном давлении получают 0,62 г продукта.
d) получение титульного соединения
К раствору 5-бром-5-децилбарбитуровой кислоты (0,619 г) в 1,3 мл диметилсульфоксида при перемешивании при 0oC, по каплям добавляют 0,93 г N-(2-гидроксиэтил)пиперазина в 0,7 мл диметилсульфоксида, затем реакционную смесь перемешивают при комнатной температуре в течение 1 часа. Затем смесь охлаждают до 0oC и добавляют 30 мл воды. Отделившийся белый осадок перемешивают в течение 1 часа, затем собирают фильтрованием и высушивают под вакуумом при 50oC. Получают 0,309 г продукта; т.пл.: 181-182oC.
1H-ЯМР в d6-ДМСО: 0,85 ppm (t, 3H); 0,9-1,1 ppm (m, 2H); 1,15-1,4 ppm (m, 14H); 1,8-1,9 ppm (m, 2H); 2,2-2,45 ppm (m, 6H); 2,55 ppm (m, 4H); 3,45 ppm (m, 2H); 4,35 ppm (t, 1H); 11,55 ppm (s, 2H).
ПРИМЕР 29 5-гексадецил-5-[N-(2-гидpoкcиэтил) пиперазин]барбитуровая кислота
Титульное соединение получают аналогичным способом, как соединение в примере 28.
ПРИМЕР 30
5-эйкоксил-5-[N-(2-гидроксиэтил)пиперазин]барбитуровая кислота
Титульное соединение готовят аналогичным способом, как соединение в примере 28.
ПРИМЕР 31
5-(4-бутоксифенил)-5-[4-(2-гидроксифенил)пиперазинил]барбитуровая кислота
Т.пл.: 184-185oC.
1H-ЯМР в d6-AMCO: 0,91 ppm (t, 3H); 1,4 ppm (m, 2H); 1,67 ppm (m, 2H); 2,36 ppm (m, 6H); 2,55 ppm (m, 4H); 3,44 ppm (q, 2H); 3,95 ppm (t, 2H); 4,37 (t, 1H); 6,95 ppm (d, 2H); 7,28 ppm (d, 2H); 11,5 ppm (br s, 2H).
Соединение готовят как описано в примере 14. Единственное различие заключается в том, что начальным материалом является этил 4-бутоксифенилацетат, который можно приготовить, начиная с 4-гидроксифенилуксусной кислоты, путем этерификации этанолом (см. пример 14-а) и последующего алкилирования этил 4-гидроксифенилацетата и бутилбромидом по известным методам.
ПРИМЕР 32
В результате способов получения, описанных в спецификации и предыдущих примерах, синтезируют соединения, которые охарактеризованы масс-спектроскопией (см. табл. 1).
ПРИМЕР 33
Для того, чтобы определить ингибирование ММР, например, HNC, каталитический домен (выделение и очистку см., например, у Schnierer, S., Kleine, Т., Gote, Т. , Hillemann, А., Knauper, V., Tshesche, H.,Biochem. Biophys. Res. Commun. (1993) 191, 319-326) инкубировали с ингибиторами, имеющими различные концентрации. Затем методом, аналогичным Grams F. et al., FEBS, 335, 1993, 76-80, определяли первоначальную скорость реакции превращения стандартного субстрата.
Результаты оценивали при построении кривой зависимости соответствующей скорости реакции против концентрации ингибитора. Константу ингибирования определяли графическим методом как отрицательный участок оси абсцисс по Dixon, М., Biochem. J. (1953) 55, 170-202.
Синтетическим субстратом коллагеназы является гептапептид, который сопряжен на C-конце с DNP (динитрофенолом). Упомянутый остаток DNP подавляет стерическим экранированием флуоресценцию смежного триптофана в гептапептиде. После отщепления трипептида, включающего DNP-группу, флуоресценция триптофана усиливается. Следовательно протеолитическое расщепление субстрата определяется по показаниям флуоресценции.
а) первый метод
Методику проводили при 25oC в свежеприготовленном 50 мМ Трис буфере (pH 8,0), обработанном дитиозоном для удаления следов тяжелых металлов. Добавили 4 мМ CaCl2 и буфер насытили аргоном. Маточные растворы адамализина II получали центрифугированием белка из суспензии, полученной в результате осаждения сернокислым аммонием, и последующим разбавлением в буфере для анализа. Маточные растворы коллагеназы разбавляли буфером для анализа. Концентрации ферментов определяли спектрофотометрически ( ε280 = 2,8•104M-1 см-1, ε288 = 2,2 • 104 M-1 см-1) и маточные растворы хранили на холоде. Этот раствор разбавляли 1: 100 для получения конечной концентрации для анализа 16 нМ. Использовали флуорогенный субстрат DNP-Pro-Leu-Gly-Leu-Trp-Ala-D- Arg-NH2 с Кm, равной 52 мкМ при концентрации 21,4 мкМ; для определения Ki также использовали концентрацию 12,8 мкМ. Флуоресценцию субстрата определяли при длинах волн возбуждения и эмиссии, равных λ =320 и 420 нм соответственно, на спектрофотометре (Perkin Elmer, Model 650-40), снабженным термостатированной клеточной камерой. Гидролиз субстрата проводили в течение 10 минут сразу же после внесения фермента. Все реакции ставили в трех параллелях. Значение Ki ингибиторов определяли по пересечению точек прямых линий, полученных на основе графиков V0/Vi против [концентрации ингибитора], в то время значения IC50 рассчитывали по графикам Vi/V0 [концентрация ингибитора] нелинейной регрессией с простым грубым взвешиванием.
b) Второй метод
Буфер для анализа:
50 мМ Трис/HCl pH 7,6 (Трис=Трис- (гидроксиметил)-аминометан)100 мМ NaCl/10 мМ CaCl2/5% МеОН (необходимы самого высшего качества).
Фермент: 8 нМ каталитического домена (Met80-Gly242) человечьей нетрофильной коллагеназы.
Субстрат: 10 микроМ DNP-Pro-Leu-Gly-Leu-Trp-Ala-D-Arg- NH2.
Общий объем пробы для анализа: 1 мл.
Приготовили раствор фермента и ингибитора в буфере (25oC) для анализа. Реакцию начинали непосредственно при внесении в раствор субстрата. Расщепление флуорогенного субстрата прослеживали с помощью флуоресцентной спектроскопии при длине волн возбуждения и эмиссии 280 и 350 нм соответственно. IC50 выражали в виде концентрации ингибитора, которая необходима, чтобы уменьшить скорость реакции наполовину по сравнению с реакцией без ингибитора.
Таблица 2: показывает найденные значения IC50.
Данные по токсичности для соединения примера 26:
LD50 = > 1000 мг/кг
Все другие соединения настоящего изобретения имеют сходный с приведенным уровень токсичности.







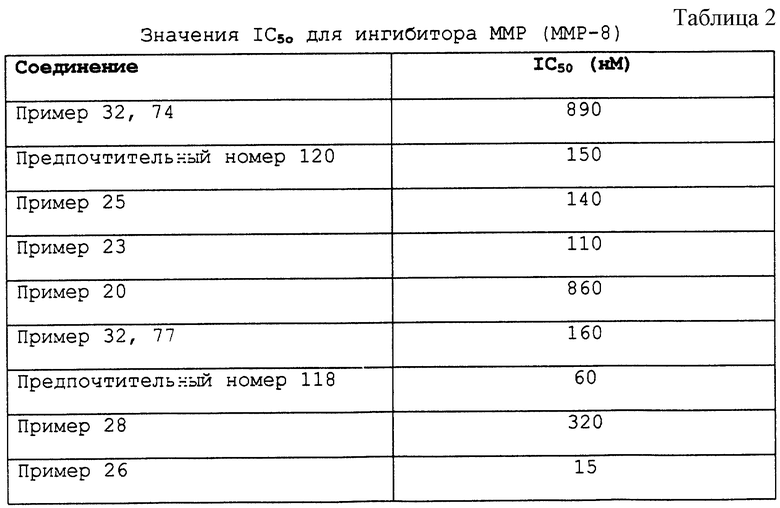
Изобретение относится к новым производным барбитуровой кислоты и фармацевтической композиции, обладающей активностью ингибирования металлопротеаз. Новые производные барбитуровой кислоты соответствуют общей формуле I, в которой X, Y, Z являются кислородом, R1 представляет группу W-V, где W является валентной связью или прямой или разветвленной С1-С4-алкильной группой, V является моноциклом, выбранным из необязательно замещенного фенила, пиридила, пиперидила, тиофенила, имидазолила, или бициклом, выбранным из нафтила, хинолинила, тетрагидрохинолила, тетрагидроизохинолила, бензимидазолила или индолила, каждый из которых может быть замещен, или W-V является необязательно замещенной С1-С20-алкильной группой, R2, R3 оба являются водородом, R4, R5 обозначают независимо друг от друга A-D, где А и D имеют различные значения, указанные в формуле изобретения, или R4, R5 вместе с атомом азота, с которым они связаны, образуют кольцо, которое может прерываться дополнительно атомом N и может быть замещено, как указано в формуле изобретения. Фармацевтическая композиция включает по меньшей мере одно соединение формулы I и дополнительно обычные вещества-носители и вспомогательные вещества. 3 с. и 5 з.п. ф-лы, 2 табл.

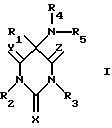
в которой X, Y и Z являются кислородом;
R1 представляет группу W-V, в которой W является валентной связью или прямой или разветвленной С1-С4-алкильной группой, V является моноциклом, выбранным из фенила, необязательно замещенного гидрокси, низшим алкилом, низшим алкокси, фенилом, фенокси; пиридила, пиперидинила, тиофенила, имидазолила или бициклом, выбранным из нафтила, хинолинила, тетрагидрохинолила, тетрагидроизохинолила, бензимидазолила, индолила, каждый из которых может быть замещен, или W-V является С1-С20-алкильной группой, необязательно замещенной аминогруппой, гидрокси, низшей ациламиногруппой, карбоксигруппой, аминокарбонилом, низшим алкиламинокарбонилом, аминокарбонил-низшим алкиламинокарбонилом, низшим алкилом, низшим алкоксилом, низшим алкоксиалкоксилом;
R2 и R3 оба являются водородом;
R4 и R5 обозначают независимо друг от друга A-D, где А представляет связь, C1-C8-алкил, С1-С4-ацил, который может прерываться гетероатомами, выбранными из О, SO2, и в котором алкильная группа может быть замещена аминогруппой; сульфонил, аминокарбонил, алкоксикарбонил, оксикарбонил, D представляет собой водород, моноцикл, выбранный из фенила, пиридила, пиперидинила, циклогексила, фурила, имидазолила, пирролидинила, тиофенила, или бицикл, выбранный из нафтила, индолила, тетрагидрохинолила, флуоренила, каждый из которых может быть замещен, или R4 и R5 вместе с атомом азота, с которым они соединены, представляют кольцо, которое необязательно может прерываться дополнительным атомом N, упомянутое кольцо необязательно может быть замещено один или несколько раз гидроксилом, алкоксилом, амино, алкиламино, диалкиламино, нитрилом или E-G, где Е представляет валентную связь, C1-C4-алкил, который необязательно замещен гидрокси; С2-С4-алкенил; G представляет водород, 6-членный ароматический моноцикл, имеющий 0, 1 или 2 атома азота, причем остальные атомы в моноцикле являются атомами углерода, где моноцикл является незамещенным или замещенным заместителем, выбранным из группы, состоящей из галогена, -NH2, -NO2, -SO2NH2, -SО2СН3, ацетила и циано;
радикалы, перечисленные для R1, R4 и R5 могут быть необязательно один или несколько раз замещены галогеном, гидроксилом, алкилом, гидроксиалкилом, алкоксилом, алкилтиогруппой, алкилсульфинилом, алкилсульфонилом, амино, алкиламино, диалкиламино, нитрогруппой, карбоксилом, карбоксиамидом, алкоксикарбонилом, амино или аминокарбонилом, необязательно один или два раза замещенными низшим алкилом, нитрилом, оксогруппой, тиокарбоксамидом, алкокситиокарбонилом, алкилмеркаптокарбонилом, фосфоном, алкилфосфоном, диалкилфосфоном, алкилсульфониламидом,
их фармакологически приемлемые соли или их эфиры карбоновых кислот, при условии, что когда -NR4R5 представляет незамещенное пиперидиновое кольцо, тогда R1 не может быть фенилом, метилом, этилом, пропилом, алкилом или кротонилом и, когда -NR4R5 представляет диэтиламиногруппу, тогда R1 не может быть метилом, этилом или кротонилом.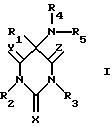
в которой X, Y и Z являются кислородом;
R1 представляет группу W-V, в которой W является валентной связью или прямой или разветвленной С1-С4-алкильной группой, V является моноциклом, выбранным из фенила, необязательно замещенного гидрокси, низшим алкилом, низшим алкокси, фенилом, фенокси; пиридила, пиперидинила, тиофенила, имидазолила или бициклом, выбранным из нафтила, хинолинила, тетрагидрохинолила, тетрагидроизохинолила, бензимидазолила, индолила, каждый из которых может быть замещен, или W-V является С1-С20-алкильной группой, необязательно замещенной аминогруппой, гидрокси, низшей ациламиногруппой, карбоксигруппой, аминокарбонилом, низшим алкиламинокарбонилом, аминокарбонил-низшим алкиламинокарбонилом, низшим алкилом, низшим алкоксилом, низшим алкоксиалкоксилом;
R2 и R3 оба являются водородом;
R4 и R5 обозначают независимо друг от друга A-D, где А представляет связь, С1-С8-алкил, С1-С4-ацил, который может прерываться гетероатомами, выбранными из О, SO2, и в котором алкильная группа может быть замещена аминогруппой; сульфонил, аминокарбонил, алкоксикарбонил, окси-карбонил, D представляет собой водород, моноцикл, выбранный из фенила, пиридила, пиперидинила, циклогексила, фурила, имидазолила, пирролидинила, тиофенила, или бицикл, выбранный из нафтила, индолила, тетрагидрохинолила, флуоренила, каждый из которых может быть замещен, или R4 и R5 вместе с атомом азота, с которым они соединены, представляют кольцо, которое необязательно может прерываться дополнительным атомом N, упомянутое кольцо необязательно может быть замещено один или несколько раз гидроксилом, алкоксилом, амино, алкиламино, диалкиламино, нитрилом или E-G, где Е представляет валентную связь, С1-С4-алкил, который необязательно замещен гидрокси; С2-С4-алкенил; G представляет водород, 6-членный ароматический моноцикл, имеющий 0, 1 или 2 атома азота, причем остальные атомы в моноцикле являются атомами углерода, где моноцикл является незамещенным или замещенным заместителем, выбранным из группы, состоящей из галогена, -NH2, -NO2, -SO2NH2, -SO2СН3, ацетила и циано;
радикалы, перечисленные для R1, R4 и R5 могут быть необязательно один или несколько раз замещены галогеном, гидроксилом, алкилом, гидроксиалкилом, алкоксилом, алкилтиогруппой, алкилсульфинилом, алкилсульфонилом, амино, алкиламино, диалкиламино, нитрогруппой, карбоксилом, карбоксиамидом, алкоксикарбонилом, амино или аминокарбонилом, необязательно один или два раза замещенными низшим алкилом, нитрилом, оксогруппой, тиокарбоксамидом, алкокситиокарбонилом, алкилмеркаптокарбонилом, фосфоном, алкилфосфоном, диалкилфосфоном, алкилсульфониламидом,
и их фармакологически приемлемые соли для получения фармацевтической композиции, обладающей активностью ингибировать матричные металлопротеазы.
| KNABE, JOACHIM ET AL | |||
| Derivatives of barbituric acid.XXXII | |||
| Control nervous system activity of racemic and optically active barbituric acid with basic substituents | |||
| Chemical Absracts, Columbus Ohio, US, 1983, v.98, № 1, 375z | |||
| Способ получения производных диалуровой кислоты | 1981 |
|
SU1080743A3 |
| @ -Аминофлуоресцеинтиокарбамилэтиламид 5-изоамил-5-(5 @ -карбоксипентил)барбитуровой кислоты в качестве реагента для поляризационного флуороиммуноанализа барбамила | 1991 |
|
SU1825793A1 |
| DE 1246743 A, 08.02.1968 | |||
| Способ сборки резино-кордных изделий | 1978 |
|
SU763145A1 |
Авторы
Даты
2001-12-27—Публикация
1996-12-20—Подача