Изобретение относится к медицине, в частности к клинической и экспериментальной медицине, и может быть использовано при лечении больных с заболеваниями большого дуоденального сосочка (БДС).
Многочисленные работы исследователей достоверно показали, что трансдуоденальная папиллосфинктеротомия является более радикальной операцией, чем супрадуоденальный или супрапапиллярный холедоходуоденоанастомоз, так как помимо устранения непроходимости БДС позволяет удалить камни из желчных протоков, провести ревизию протока поджелудочной железы, не оставляет "слепого поданастомозного мешка". Совершенствование техники операции и улучшение ее результатов сделало папиллосфинктеротомию операцией выбора на желчных путях (П. Н. Напалков с соавт. 1980; Б.А.Королев, Д.Л.Пиковский 1990; Jones S. 1987). Однако по данным Г.А.Клименко (1998) после трансдуоденальной папиллосфинктеротомии отмечается высокий процент осложнений как в раннем, так и позднем послеоперационном периоде и достигает 10-28%.
Существует несколько способов трансдуоденальной папиллосфинктеропластики. Наиболее распространенный выполняется путем рассечения большого дуоденального сосочка в секторе 11 часов через все слои и наложения на края разреза узловых швов с использованием общехирургической техники.
Для уменьшения количества осложнений папиллосфинктеропластики Ю.А.Тетеревлев (1986) предложил не накладывать швы на медиальную стенку разреза и уделять внимание наиболее щадящим способам манипуляций.
Н. Г. Григорьев (1986) предложил выполнять папиллосфинктеропластику без мобилизации двенадцатиперстной кишки (ДНК), а пластику БДС проводить путем наложения узловых швов на края рассеченной стенки БДС на атравматической игле.
Применение механического шва танталовыми скобками по данным А.И.Краковского при папиллосфинктеропластике позволило облегчить технику операции, уменьшить количество осложнений, сократить время оперативного вмешательства.
Кроме того, была предложена методика лазерной папиллосфинктеротомии, которая отличается от классической модели меньшей травматизацией, надежным гемостазом и биологической сваркой слоев рассеченных тканей, что дало основание авторам считать способ разновидностью папиллосфинктеропластики (О.К. Скобелкин с соавт. 1990). Но следует отметить, что у трети больных лазерная папиллосфинктеропластика была дополнена отдельными узловыми швами т.е. использовалась общехирургическая техника.
Недостатками перечисленных способов являются развитие анастомозита, лигатурных свищей, инкрустация лигатур желчными солями и образование канкрементов (Н.А.Назаренко 1981; О.Б.Милонов 1982).
Одним из путей улучшения результатов вмешательств на желчных путях является применение эндоскопической техники. Несмотря на широкое внедрение последней, по данным ряда авторов, остается 7-14% случаев, когда невозможно выполнить вмешательство на БДС при помощи эндоскопической техники (В.П. Глобай 1976; Sottomayor et al. 1977). К недостаткам метода можно отнести отсутствие возможности выполнения пластики рассеченных тканей. A Goinard, Pelissier (1982) считают эндоскопическую папиллосфинктеротомию более опасной и травматичной процедурой, чем открытая папиллосфинктеропластика.
За прототип нами взят способ Н.А.Пострелова с соавт. (А.с. 1124937 СССР, МКИ А 61 В 17/00 "Способ папиллосфинктеропластики"). Суть способа заключается в послойном сшивании рассеченных тканей двухрядным адаптирующим швом. Первый ряд швов - адаптация слизистых оболочек терминального отдела общего желчного протока (ОЖП) и ампулы БДС. Второй ряд швов накладывали на мышечные пучки сфинктера и слизистую оболочку ДПК. Операцию проводили с использованием оптического увеличения и сверхтонкой синтетической нити некапиллярного типа размером 8/0 на атравматической игле.
Недостатками данного метода являются:
1. Сопоставление краев рассеченной стенки БДС осуществляется путем наложения швов на слизистую оболочку ДПК и ампулы БДС. Это способствует проникновению микрофлоры в рану через дефекты - проколы в слизистой оболочке, инфицированию ее и образованию соединительно-тканного рубца.
2. Заживление раны вторичным натяжением с образованием рубца нарушает функцию сфинктерного аппарата. При этом возможно возникновение его недостаточности, рефлюкса дуоденального содержимого в желчные протоки и развитие холангита.
3. При грубых рубцовых изменениях в дуоденальном сосочке и терминальном отделе общего желчного протока методика не применима, т.к. после иссечения рубцовой ткани образуется значительный диастаз между краями раны, не позволяющий сопоставить их без нарушения желчеоттока в ДПК.
В основу разработанного способа положено применение микрохирургической техники оперирования на БДС. Новизна и отличия заключаются в том, что рассечение сосочка проводили в секторе 13-14 часов с сохранением слизистой оболочки печеночно-поджелудочной ампулы, на каждой стороне разреза сшивают мышечные пучки сфинктера, подслизистые основы ДПК и ампулы без захвата в шов слизистых оболочек.
Этим достигается наименьшая травматизация сфинктера терминального отдела общего желчного и панкреатического протоков, а также сохранение клапанного аппарата слизистой оболочки печеночно-поджелудочной ампулы. При выполнении пластики происходит подворачивание слизистой оболочки, уменьшение раневого дефекта и достигаются условия для восстановления слизистой оболочки ДПК.
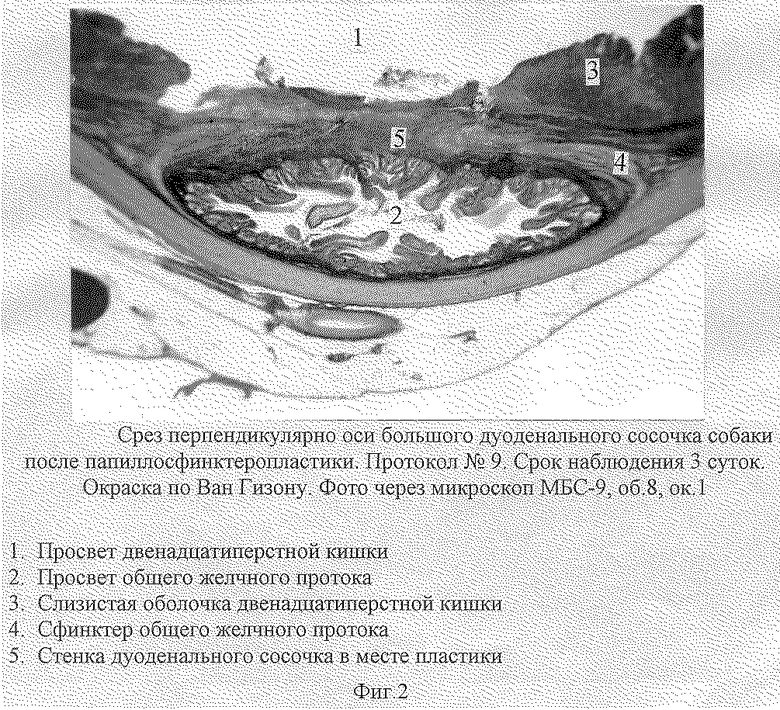
Техника выполнения способа следующая. На беспородных собаках разного пола и веса под тиопенталовым наркозом проводили лапаротомию косым разрезом в правом подреберье по Федорову. Переднюю стенку двенадцатиперстной кишки рассекали продольно в проекции БДС. С использованием напольного операционного микроскопа (увеличение 10-15 крат) послойно рассекали слизистую оболочку и подслизистую основу ДПК, мышечную оболочку сфинктера и частично подслизистую основу ОЖП, таким образом, оставляя интактной слизистую оболочку ампулы БДС и ОЖП. Далее на рассеченные края накладывали отдельные узловые или непрерывные микрохирургические швы. В шов захватывали подслизистую основу ДПК, мышечные пучки сфинктера и подслизистую основу ампулы БДС и ОЖП (см. фиг. 1). Рану на стенке ДПК ушивали узловыми или непрерывным однорядными микрохирургическими швами. Операционную рану ушивали наглухо.
Предложенный способ применили на 25 беспородных собаках весом 8-25 кг, которым проводили трансдуоденальную папиллосфинктеропластику по предложенной методике. В послеоперационном периоде животные вели себя активно, лекарственные препараты не назначали. Животных наблюдали в сроки от 1 суток до б месяцев. Оценку результатов исследования проводили при помощи эндоскопического и рентгенологического исследования, а также путем изготовления гистотопограмм после эвтаназии животных.
В процессе наблюдения животные клинически здоровы. При эндоскопическом исследовании виден дуоденальный сосочек с устьем обычных размеров и неизмененной слизистой вокруг. Кверху от сосочка имеется борозда с восстановленной слизистой оболочкой, лигатуры отсутствуют. Желчь выделяется порционно, обычной консистенции и цвета.
При рентгенографии желчные протоки нерасширены, контрастное вещество поступает свободно в ДПК. При проведении пробы на дуоденобилиарный рефлюкс (давление 100-200 мм вод. ст.) водорастворимое контрастное вещество в желчные протоки не поступает.
На гистотопограммах в сроки 3-7 суток происходит восстановление слизистой оболочки ДИК. Стенка дуоденального сосочка в месте рассечения состоит из слизистой оболочки ДПК, тонкого слоя подслизистой основы БДС и слизистой оболочки ОЖП. Отмечено отсутствие деформации и сужения просвета ОЖП и ДПК (см. фиг.2).
Примеры конкретного применения
Протокол операции N16. Беспородная собака весом 9 кг. Под тиопенталовым наркозом произведена лапаротомия косым разрезом по Федорову. Двенадцатиперстная кишка рассечена продольно в проекции БДС. Сосочек рассечен кверху в секторе 13 часов послойно до слизистой ОЖП. Пластика выполнена по описанной методике. Стенка двенадцатиперстной кишки ушита однорядным микрохирургическим швом. Брюшная стенка ушита послойно наглухо. В послеоперационном периоде (срок наблюдения 1 месяц) животное клинически здорово. При проведении пробы на дуоденобилиарный рефлюкс при внутридуоденальном давлении 180 мм вод. ст. рефлюкс в ОЖП не отмечен. На холангиограмме внепеченочные желчные протоки нерасширены, контраст свободно поступает в двенадцатиперстную кишку. После эвтаназии животного на секционном материале устье нерасширено, обычной формы, слизистая вокруг сосочка не изменена, кверху видна борозда с восстановленной слизистой. Печень и поджелудочная железа не изменены, обычного цвета и консистенции. На гистотопограммах отмечено полное восстановление слизистой оболочки ДПК в месте рассечения стенки БДС. Стенка печеночно-поджелудочной ампулы состоит из слизистой оболочки ОЖП, подслизистой основы и слизистой оболочки ДПК. Деформаций и сужений просвета ОЖП и ДПК не выявлено. Ткань поджелудочной железы сохраняет свою обычную структуру.
В клинической практики способ был применен у больных со стенозом БДС. Приводим два клинических наблюдения.
Пример 1. Больная В., 56 лет, оперирована в октябре 1998 года в районной больнице по поводу флегманозного калькулезного холецистита, холедохолитиаза, механической желтухи, гнойного холангита. Наряду с холедохолитиазом обнаружен стеноз большого дуоденального сосочка. Выполнена холецистэктомия, холедохолитотомия, дренирование общего желчного протока по А.В.Вишневскому. После купирования клиники острого холангита больная переведена в 1 городскую больницу для дальнейшего лечения. По дренажной трубке из d.choledochus выделялось до 400-500 мл желчи. При попытке пережать дренажную трубку вскоре возникали распирающие боли в правом подреберье. На фистулохолангиограмме - картина стеноза БДС подтверждена: отмечалось заполнение контрастным веществом внутрипеченочных желчных протоков, общий желчный проток расширен до 2 см. Конфигурация дистального отдела протока имела форму "писчего пера", протяженность сужения 2,5 см. Контраст поступал в ДПК узкой полоской. Эндоскопическая папилосфинктеротомия по техническим причинам не выполнена. Больная оперирована через 4 недели после первой операции 10.11.98 г. произведена трансдуоденальная папилосфинктеротпластика по описанной методике.
В послеоперационном периоде на 2-е сутки по холедохостоме выделилось 100 мл желчи, через 2 недели дренаж из общего желчного протока удален. На фистулохолангиограмме, выполненной перед удалением дренажа, диаметр d.choledochus 1 см, контрастное вещество свободно поступает в ДПК, рефлюкса его во внутрипеченочные желчные протоки нет. При эндоскопическом осмотре через 20 дней после операции виден дуоденальный сосочек обычной формы, на передней стенке его незначительное втяжение слизистой в виде бороздки до 2,5 см. При проведении релаксационной дуоденографии контрастное вещество в желчные протоки не поступает. Выписана с выздоровлением.
Пример 2. Больная Г., 52 лет, поступила в клинику по поводу хронического калькулезного холецистита, осложненного механической желтухой. В течение 5 последних месяцев неоднократно возникавшие приступообразные боли в правом подреберье сопровождались преходящей механической желтухой. При эндоскопическом осмотре двенадцатиперстной кишки патологических изменений не обнаружено, в просвете желчь. УЗИ внепеченочных желчных протоков: желчный пузырь деформирован, небольших размеров, в просвете множество канкрементов. Общий желчный проток расширен до 15 мм, в просвете также канкременты. Билирубин крови - 125 мкмоль/л. 15.02.99 г. операция: холецистэктомия, холедохолитотомия, трансдуоденальная папиллосфинктеропластика по описанной методике, холедохостомия на дренаже Кера. При ревизии обнаружено: ОЖП диаметром 16 мм, на операционной холангиограмме - конусовидное сужение в дистальном отделе протока, контраст поступает в ДПК в виде узкой полоски. Калибровочный зонд диаметром 2 мм проходит в ДПК с некоторым сопротивлением. Заполнилось контрастным веществом внутрипеченочное билиарное дерево.
Послеоперационный период протекал без осложнений. На 15 сутки дренажная трубка удалена. На фистулохолангиограмме проходимость контрастного вещества в ДПК хорошая, внутрипеченочные желчные протоки не заполнились. При эндоскопическом осмотре просвета ДПК через 1 месяц после операции БДС обычных размеров и формы, отмечается порционное поступление желчи. Выписана с выздоровлением.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПАПИЛЛОСФИНКТЕРОТОМИИ | 2007 |
|
RU2334472C1 |
| СПОСОБ ЭНДОСКОПИЧЕСКОЙ ПАПИЛЛОСФИНКТЕРОТОМИИ | 2011 |
|
RU2463975C1 |
| СПОСОБ ХОЛЕДОХО-, И ГЕПАТИКОЕЮНОСТОМИИ | 1996 |
|
RU2122361C1 |
| СПОСОБ ХОЛЕДОХОЕЮНОСТОМИИ | 1996 |
|
RU2122360C1 |
| СПОСОБ ЛЕЧЕНИЯ ХОЛЕДОХОЛИТИАЗА И СТЕНОЗА БОЛЬШОГО ДУОДЕНАЛЬНОГО СОСОЧКА (БДС) | 2002 |
|
RU2221497C2 |
| СПОСОБ ГАСТРОДУОДЕНОАНАСТОМОЗА | 2001 |
|
RU2197903C2 |
| СПОСОБ ГАСТРОЕЮНОАНАСТОМОЗА | 2001 |
|
RU2201716C2 |
| Способ лечения острого панкреатита | 2018 |
|
RU2688720C1 |
| СПОСОБ ЭНДОСКОПИЧЕСКОЙ СФИНКТЕРОСОХРАНЯЮЩЕЙ НЕТИПИЧНОЙ ПАПИЛЛОТОМИИ ПРИ ХОЛЕДОХОЛИТИАЗЕ | 2021 |
|
RU2771260C1 |
| СПОСОБ ГАСТРОДУОДЕНОАНАСТОМОЗА | 2002 |
|
RU2212195C1 |
Изобретение относится к медицине, хирургии, может быть использовано при лечении больных со стенозом большого дуоденального сосочка. Рассекают сосочек в передневерхнем сегменте в секторе 13-14 часов. Сохраняют при этом слизистую печеночно-поджелудочной ампулы. Сшивают мышечные кучки сфинктера, подслизистые основы двенадцатиперстной кишки и печеночно-поджелудочной ампулы на каждой стороне разреза без захвата в шов слизистой. Способ позволяет снизить травматичность вмешательства и сохранить клапанный аппарат слизистой оболочки печеночно-поджелудочной ампулы. 2 ил.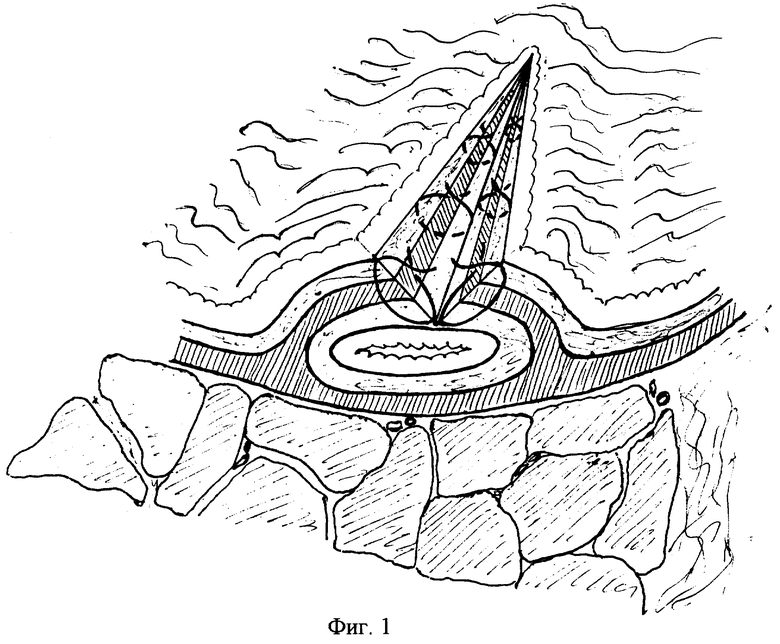
Способ папиллосфинктеропластики путем наложения микрохирургического шва, отличающийся тем, что рассечение сосочка проводят в передневерхнем сегменте в секторе 13-14 ч, с сохранением слизистой оболочки печеночно-поджелудочной ампулы, сшивают мышечные пучки сфинктера, подслизистые основы двенадцатиперстной кишки и печеночно-поджелудочной ампулы на каждой стороне разреза, без захватывания в шов слизистой.
| Способ папиллосфинктеропластики | 1982 |
|
SU1124937A1 |
Авторы
Даты
2002-02-20—Публикация
1999-08-25—Подача