Изобретение относится к медицине и ветеринарии, а именно к лекарственным препаратам для парентерального применения с широким спектром биологической активности.
Известны лекарственные препараты для парентерального применения, содержащие в качестве активного вещества соли N-акридонуксусной кислоты.
Так, лекарственный препарат для парентерального применения (патент РФ 2031650, А 61 К 31/33, 17.03.92 "Противовирусное лекарственное средство и способ его получения") содержит в качестве активного вещества натриевую соль акридонуксусной кислоты, растворенную в трис-буфере, и в качестве стабилизатора - трилон Б (динатриевую соль этилендиаминтетрауксусной кислоты).
Известен лекарственный препарат "Неовир" (М.Д. Машковский, Лекарственные средства, 13-е изд., Харьков, Торсинг, 1997, т.2, с.352), который содержит в качестве активного вещества натриевую соль N-акридонуксусной кислоты в концентрации 12,5 мас.%, а в качестве стабилизатора - лимонную кислоту.
Известные лекарственные препараты на основе натриевой соли N-акридонуксусной кислоты обладают интерфероногенной активностью, однако вызывают местнораздражающий и болевой эффект, обусловленный высоким значением рН, а также являются светочуствительными и, следовательно, неустойчивыми при изготовлении и хранении готовой лекарственной формы.
Известен также лекарственный препарат для парентерального применения на основе 1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)] -аммоний-Д-глюцитола в виде 22,5%-ного водного раствора, обладающий широким спектром биологической активности ("Циклоферон 12,5% для инъекций: итоги и перспективы клинического применения", изд. "Аполлон", СПб, 1999 г.).
Лекарственный препарат указанного состава выбран в качестве прототипа.
Однако данный препарат в ряде случаев не обладает достаточной биологической активностью, особенно при лечении хронических заболеваний системного характера.
Кроме того, данный препарат не является стабильным. Так, в процессе его изготовления на стадиях розлива, запайки и термической стерилизации ампул, а также при хранении на свету активное вещество разлагается с образованием осадка, что делает лекарственную форму непригодной для использования.
Задачей изобретения является повышение биологической активности лекарственного препарата для парентерального применения при одновременном повышении стабильности лекарственной формы в процессе производства и хранения.
Поставленная задача решается тем, что лекарственный препарат для парентерального применения, содержащий в качестве активного вещества 1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)] -аммоний-Д-глюцитол, в качестве растворителя - воду для инъекций, согласно изобретению, дополнительно содержит в качестве стабилизатора - N-метилглюкамин при следующем соотношении компонентов, мас.%:
1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)] - аммоний-Д-глюцитол - 8,5-25,0
N-метилглюкамин - 0,05-1,00
Вода для инъекций - До 100
Заявляемый лекарственный препарат для парентерального применения содержит в качестве активного вещества 1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)]-аммоний-Д-глюцитол, известный как биологически активное вещество, обладающее иммуномодулирующим действием (ЕА патент 000382, С 07 Н 5/06, 22.01.98 г).
В качестве стабилизатора заявляемый лекарственный препарат содержит
N-метилглюкамин (ФС 42-2465-89), который известен как солеобразователь.
Авторами настоящего изобретения впервые показано влияние N-метилглюкамина в свободном состоянии как на биологическую активность лекарственного препарата, так и на его физико-химические свойства.
Технический результат изобретения заключается в том, что добавление N-метилглюкамина в свободном состоянии к раствору соли акридонуксусной кислоты (1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)] -аммоний-Д-глюцитол) приводит к увеличению проникающей способности активного вещества внутрь клетки через мембрану и способствует связыванию его с внутриклеточными структурами, что повышает биологическую активность препарата.
Так же при добавлении N-метилглюкамина в свободном состоянии к раствору соли акридонуксусной кислоты происходит процесс самоструктурирования раствора с образованием крупных межмолекулярных комплексов, что приводит к повышению фотостабильности и термостабильности лекарственной формы.
Таким образом, заявляемый лекарственный препарат для парентерального применения при экспериментально установленном оптимальном соотношении компонентов является препаратом, обладающим повышенной биологической активностью, а также фото - и термостабильностью в процессе производства и хранения.
Изобретение осуществляют следующим образом.
Для приготовления 100 л лекарственного препарата берут 70 л воды для инъекций, 22,5 кг 1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)]-аммоний-Д-глюцитола.
Полученную смесь перемешивают до полного растворения компонентов, затем добавляют 0,5 кг N-метилглюкамина до достижения рН 7,6 и воду для инъекций до получения объема 100 л. Полученный раствор фильтруют через стерилизующий фильтр типа "Палл", разливают в стерильные емкости объемом 1, 2 и 5 мл. Выход готового препарата 96,5%.
Емкость объемом 5 мл содержит 22,5 мас.% 1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)] -аммоний-Д-глюцитола; 0,5 мас.% N-метилглюкамина и 77,00 мас.% воды для инъекций.
В табл. 1-7 представлены результаты экспериментальных и клинических исследований заявляемого лекарственного препарата для парентерального применения.
В табл. 1,2 - данные по выбору оптимального состава и по исследованию биологической активности заявляемого лекарственного препарата.
В табл. 3,4,5 - результаты экспериментальных исследований фото- и термостабильности заявляемого препарата.
В табл. 6,7 - результаты лечебной эффективности заявляемого препарата.
Опыт 1. Перед выбором оптимального соотношения компонентов, входящих в заявляемый препарат, было определено допустимое содержание каждого компонента.
Допустимое содержание активного вещества (1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)] -аммоний-Д-глюцитол) установили путем экспериментальных исследований по эффективной разовой дозе, которая составляет 434-1279 мг на человека массой 70 кг, что соответствует концентрации раствора 8,5-25,0 мас.% для однократно вводимого объема 5 мл.
Допустимое содержание стабилизатора (N-метилглюкамина), которое обеспечивает физиологически приемлемый уровень рН 7,8-8,0, составляет 0,05-1,00 мас.%.
Выбор оптимального соотношения компонентов, входящих в заявляемый препарат, проводили на 70 кроликах породы шиншилла массой 2,8-3,3 кг, разбитых на 14 групп по 5 животных, и исследовали действие 14 вариантов состава лекарственного препарата с содержанием 1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)]-аммоний-Д-глюцитола в пределах от 8,5 до 34,2 мас.% и с содержанием N-метилглюкамина от 0,05 до 1,00 мас.%.
Оптимальные пределы содержания активного вещества определяли по отсутствию местнораздражающего действия при введении внутримышечно 5 мл препарата (максимально переносимая доза).
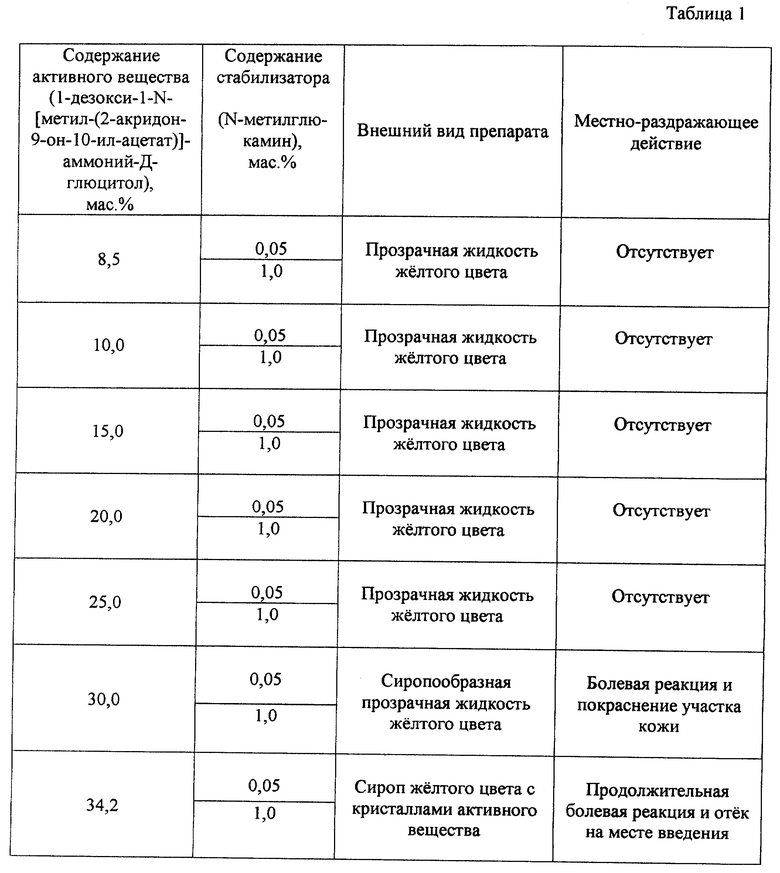
Полученные результаты представлены в табл. 1.
Заявляемый лекарственный препарат не вызывает местнораздражающего действия при внутримышечном введении при содержании активного вещества 8,5-25,0 мас.% и содержании N-метилглюкамина 0,05-1,00 мас.%.
При этом препарат представляет собой прозрачную жидкость желтого цвета.
При содержании активного вещества 30 мас.% на месте введения препарата наблюдалась болевая реакция и покраснение участка кожи. С увеличением содержания активного вещества до 34,2 мас.% при различном содержании стабилизатора наблюдалась продолжительная болевая реакция и отек на месте введения препарата, при этом он представляет собой сироп желтого цвета с кристаллами активного вещества.
Таким образом, оптимальным соотношением компонентов для решения поставленной задачи в лекарственном препарате для парентерального применения является состав со следующим соотношение компонентов, мас.%:
1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)] - аммоний-Д-глюцитол - 8,5-25,0
N-метилглюкамин - 0,05-1,00
Вода для инъекций - До 100
Исследования биодоступности и биологической активности заявляемого препарата проводили в опытах 2 и 3.
Опыт 2. Биодоступность заявляемого лекарственного препарата оценивали по степени проникновения активного вещества (1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)] -аммоний-Д-глюцитол) внутрь клетки путем исследования лимфоцитов, разделенных на Т- и В-субпопуляции, периферической крови доноров.
Для фракционирования лимфоциты пропускали через стерильную колонку с синтетическим волокном, после чего сорбированные на волокне В-лимфоциты смывали 0,1%-ным раствором натриевой соли этилендиаминтетраацетата (ЭДТА).
Клетки были инкубированы с водными растворами прототипа и заявляемого препарата в разведении 1:1000.
О степени проникновения активного вещества внутрь клетки через мембрану оценивали по характерной флюоресценции при ультрафиолетовом облучении с помощью люминесцентного микроскопа.
Исследования лимфоцитов под микроскопом показали, что в прототипе проникновение активного вещества внутрь клеток было небольшим, так как флюоресценция клеток была слабой, а свечение ядра не наблюдалось.
После отмывки клеток 0,1%-ным раствором ЭДТА флюоресценция клеток отсутствовала, что говорит о слабом связывании активного вещества с внутриклеточными структурами.
При исследовании лимфоцитов, инкубированных с заявляемым препаратом, в клетках наблюдалось яркое сине-зеленое свечение, особенно заметное в ядрах, которое не исчезало при двукратной отмывке клеток 0,1%-ным раствором ЭДТА.
Данный факт свидетельствует о влиянии N-метилглюкамина на повышение биодоступности заявляемого лекарственного препарата за счет проникновения активного вещества внутрь клетки и последующем связывании с ядром.
Опыт 3. Биологичесскую активность заявляемого лекарственного препарата по сравнению с прототипом оценивали по динамике образования суммарной рибонуклеиновой кислоты (РНК), отражающую общую активность клетки.
В качестве тест-системы использовали стандартную культуру клеток моноцитов И-397. Клетки выращивали в пластиковых пробирках на ростовой среде RPMI 1640 с 20%-ной фетальной телячьей сывороткой, в конечной концентрации моноцитов 2•107 клеток/мл. Затем клетки инкубировали при температуре 37oС в атмосфере 5%-ного углекислого газа в 96-луночной планшете с последующей сменой питательной среды в течение 7 дней.
Равное количество клеток брали через 2, 4, 6 и 8 ч инкубации с препаратом, изготовленным согласно прототипу, и заявляемым препаратом с различным содержанием стабилизатора и выделяли в них суммарную РНК (Chomczynski P., Sachi N.. "One-step metod for RNA isolation from cells and tissues". Analytical Biochemystry, 1987, v.162, N2, p.156-159).
Количество суммарной РНК определяли спектрофотометрически по оптической плотности инкубированного раствора при длине волны 260 нм.
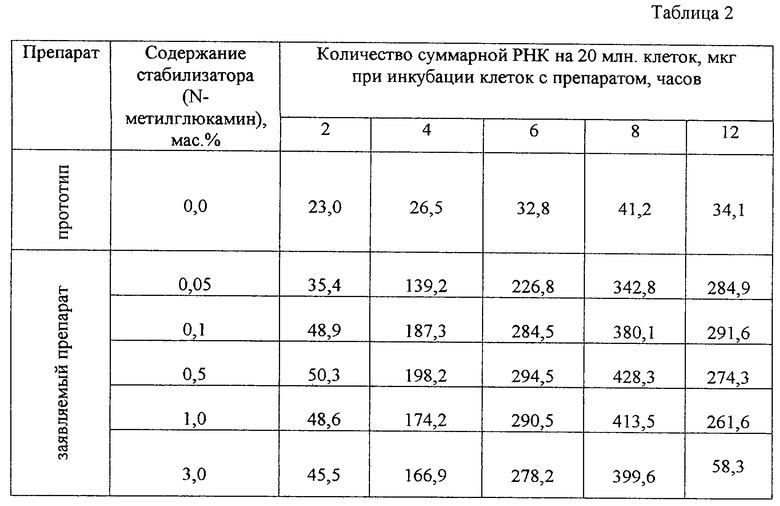
Результаты исследований, приведенные в табл.2 ,показывают, что при инкубации клеток моноцитов с прототипом происходило нарастание количества суммарной РНК и через 8 ч достигало максимальной величины, в 1,8 раза превышающей исходный уровень.
Динамика образования суммарной РНК в инкубированном растворе с заявляемым препаратом при содержании стабилизатора в интервале от 0,05 до 3,0 мас.% была следующая.
При содержании стабилизатора от 0,05 до 1,0 мас.% происходило резкое нарастание суммарной РНК, достигало максимального значения через 8 ч и в 9,2-10,4 раза превышало исходный уровень.
При дальнейшем увеличении содержания N-метилглюкамина от 1,0 до 3,0 мас. % динамика образования РНК заметно снижалась.
Снижение динамики образования суммарной РНК наблюдалось также через 12 ч после инкубирования растворов при разном содержании N-метилглюкамина.
Таким образом, динамика образования суммарной РНК показывает, что биологическая активность заявляемого препарата превышает биологическую активность прототипа.
Стабильность заявляемой лекарственной формы исследовали в опытах 4 и 5.
Опыт 4. Оценка фотостабильности заявляемого лекарственного препарата по сравнению с прототипом проводилась путем облучения ртутной лампой со спектром, аналогичным солнечному свету, мощностью 300 Вт в течение 6 ч в стандартной кварцевой кювете объемом 10 мл.
Фотостабильность препаратов определяли визуально по изменению окраски раствора, выпадению осадка, а также по количественному содержанию активного вещества после центрифугирования осадка и продуктов разложения путем спектрофотометрического определения характерного максимума при 255 нм.
Фотостабильным считали препарат, выдержавший экспозицию более 2 ч без помутнения и разложения активного вещества.
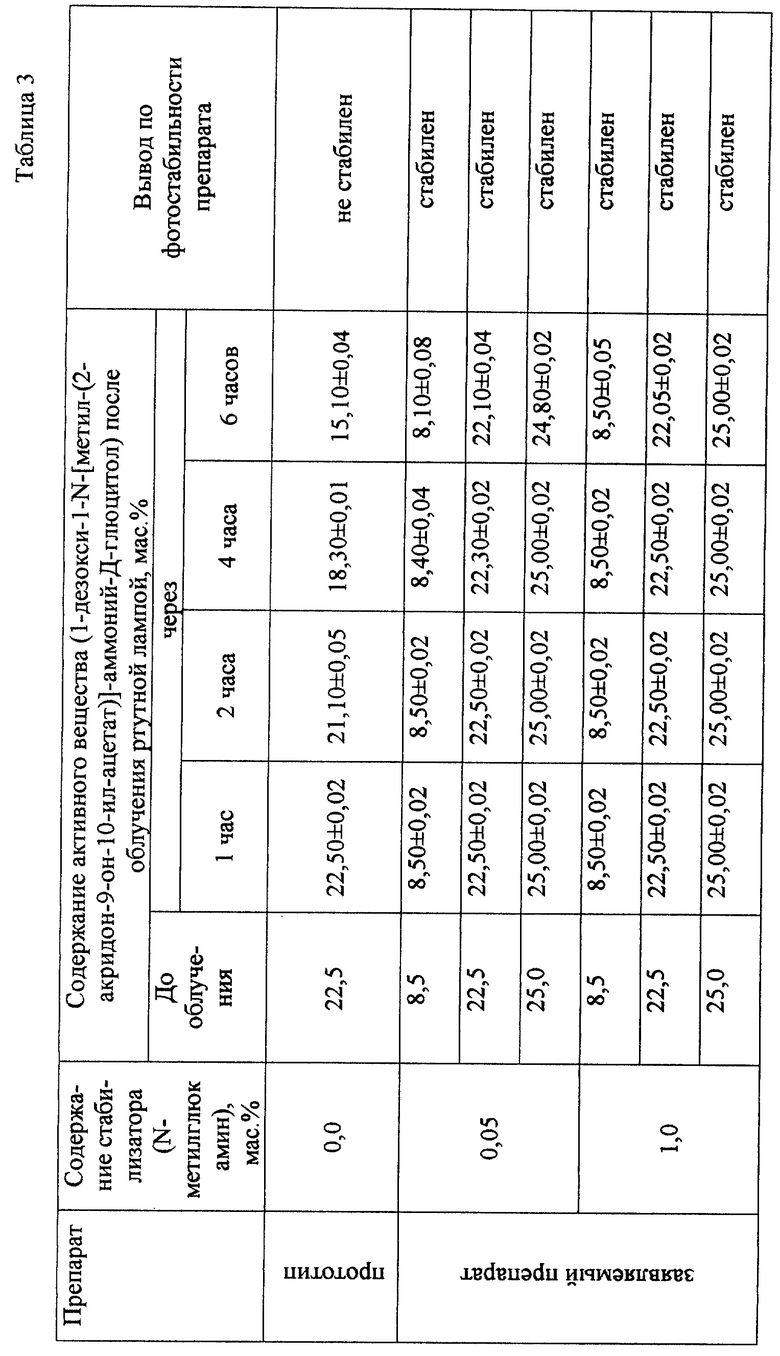
Полученные результаты эксперимента представлены в табл. 3.
Лекарственный препарат, изготовленный согласно прототипу, был стабилен в течение 1 ч, при этом концентрация активного вещества снизилась на 6,2%.
Заявляемый лекарственный препарат был стабилен 2 ч, при содержании активного вещества в пределах от 8,5 до 25,0 мас.% и содержании N-метилглюкамина 0,05 маc.%.
При содержании N-метилглюкамина 1,0 мас.% заявляемый препарат был стабилен 6 ч, при этом уровень содержания активного вещества не изменялся.
Исследование влияния N-метилглюкамина на физико-химические свойства заявляемого препарата проводили путем определения интегральных показателей - осмоляльности и относительной вязкости раствора.
Как правило, при увеличении концентрации, связанной с добавлением вещества к готовому раствору, его вязкость и осмоляльность также увеличиваются.
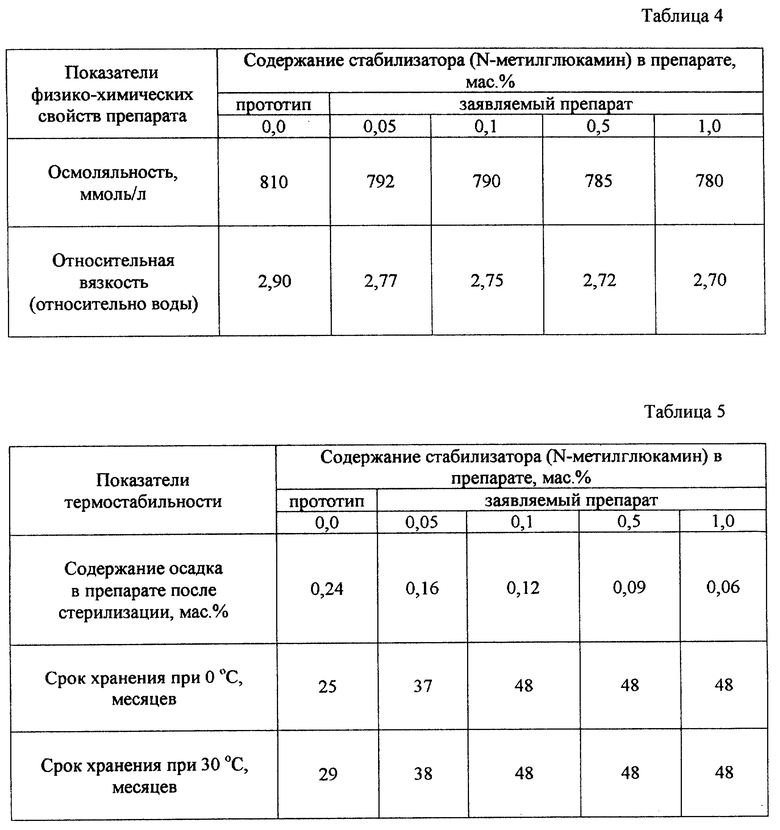
Данные исследования, представленные в табл. 4, показывают, что при увеличении содержания N-метилглюкамина в заявляемом препарате наблюдалось уменьшение осмоляльности и вязкости: при содержании N-метилглюкамина 0,05 мас.% осмоляльность раствора снизилась на 18 ммоль/л, а при содержании N-метилглюкамина 1,0 мас.% - на 30 ммоль/л.
Относительная вязкость раствора снижается при содержании N-метилглюкамина 0,05 мас.% - на 4,5%, а при содержании N-метилглюкамина 1,0 мас.% - на 6,9%.
Таким образом, с повышением содержания N-метилглюкамина от 0,05 до 1,0 мас.% наблюдается повышение фотостабильности заявляемого препарата при одновременном снижении его осмоляльности и вязкости, что объясняется процессом структурирования раствора с образованием крупных межмолекулярных комплексов.
Опыт 5. В данном опыте исследовали влияние N-метилглюкамина на термостабильность заявляемого препарата в условиях промышленной стерилизации и его стабильность при последующем хранении.
В заявляемом лекарственном препарате для парентерального применения активное вещество (1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)]-аммоний-Д-глюцитол) является термически нестабильным соединением.
В условиях промышленной стерилизации ампул происходит частичная деструкция акридонуксусной кислоты с образованием примеси N-метилакридона. В процессе хранения ампул, особенно на холоде происходит кристаллизация из раствора нерастворимого в воде N-метилакридона и препарат не может быть применен для парентерального введения из-за возможных побочных реакций - болевого шока, образования инфильтрата и васкулита.
Для оценки термоустойчивости и стабильности при хранении использовали две серии стеклянных ампул объемом 5 мл. Одна серия - с раствором, изготовленным согласно прототипу. Другая серия - с раствором, изготовленным согласно заявляемому препарату, с содержанием активного вещества 22,5 мас.% и с содержанием стабилизатора в пределах 0,05-1,0 мас.%.
Серии ампул с указанными растворами подвергали стерилизации острым паром (120 oС, 30 мин) в автоклаве. После стерилизации определяли количество примеси N-метилакридона методом высокоэффективной жидкостной хроматографии на хроматографе "Миллихром-1".
Затем ампулы с растворам хранили в темном месте при 0 и 30oС в течение 4 лет. Раз в месяц ампулы просматривали в отраженном свете и определяли наличие осадка N-метилакридона. За срок хранения серии принимали период, при котором не происходило выпадения осадка.
Результаты исследования, представленные в табл. 5, показывают, что при стерилизации ампул с прототипом происходит термическая деструкция активного вещества с образованием N-метилакридона в концентрации 0,24 мас.%. После стерилизации ампул с заявляемым препаратом образование N-метилакридона уменьшается на 66,6%.
В результате хранения при температуре 0oС N-метилакридон выпадает в осадок в прототипе через 25 месяцев, а в заявляемом препарате - через 37 месяцев. В результате хранения при температуре 30oС осадок N-метилакридона в прототипе образуется через 29 месяцев, а в заявляемом препарате - через 38 месяцев.
При увеличении содержания N-метилглюкамина от 0,1 до 1,0 мас.% срок хранения заявляемого препарата при обеих температурах составляет 48 месяцев.
Таким образом, проведенные исследования показали, что использование N-метилглюкамина в качестве стабилизатора повышает термостабильность и увеличивает срок хранения препарата.
Заявляемый лекарственный препарат для парентерального применения при установленном оптимальном соотношении компонентов обладает фото- и термостабильностью в процессе производства и хранения.
Эффективность лечебного действия заявляемого препарата оценивали при лечении больных псориазом, которое является хроническим заболеванием системного характера.
Лечение псориаза в стадии обострения осуществляли у 41 человека - мужчин в возрасте от 18 до 58 лет, разделенных на 2 группы (опытную и контрольную). Длительность заболевания составила от 2 до 20 лет. У всех больных наблюдалось наличие папулезно-бляшечных элементов с выраженной инфильтрацией и шелушением. Патологические очаги были локализованы преимущественно на коже туловища, конечностей и волосистой части головы.
Лечение проводили путем внутримышечных инъекций по 4 мл 1 раз в сутки на 1,2,4,6,8,10 дни в контрольной группе (20 больных) - прототипом, в опытной группе (21 больной) - заявляемым препаратом с содержанием активного вещества (1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)] -аммоний-Д-глюцитол), соответствующим содержанию его в прототипе (22,5 мас.%) и с содержанием стабилизатора (N-метилглюкамина) 0,5 мас.%.
Эффективность лечения оценивалась по клиническим показателям на 10 день лечения и по времени, прошедшем до следующего обострения (среднее время ремиссии), а также по иммунологическим показателям (содержанию цитокинов в сыворотке крови).
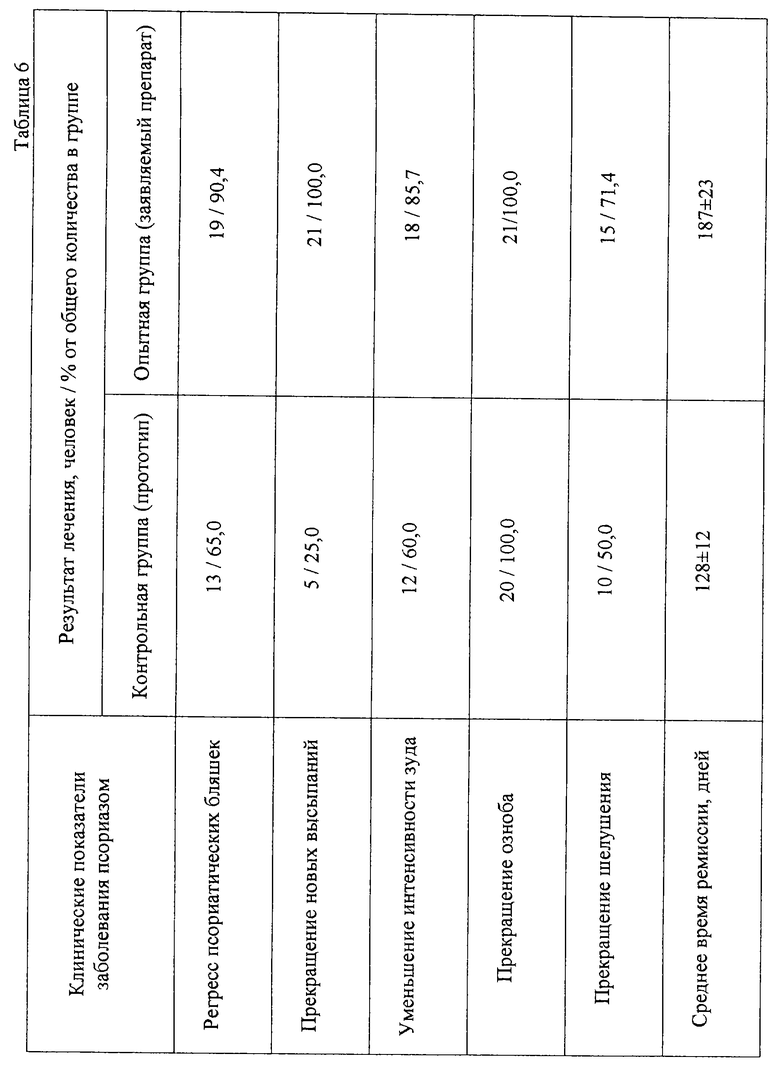
Результаты лечения представлены в табл. 6 и 7.
В контрольной группе (прототип) в результате лечения у 65% больных регрессировали псориатические очаги и исчезло чувство зуда, у 50% прекратилось шелушение кожи. Среднее время ремиссии составило 128 дней.
У 12 больных улучшения клинических показателей было подтверждено иммунологическими показателями.
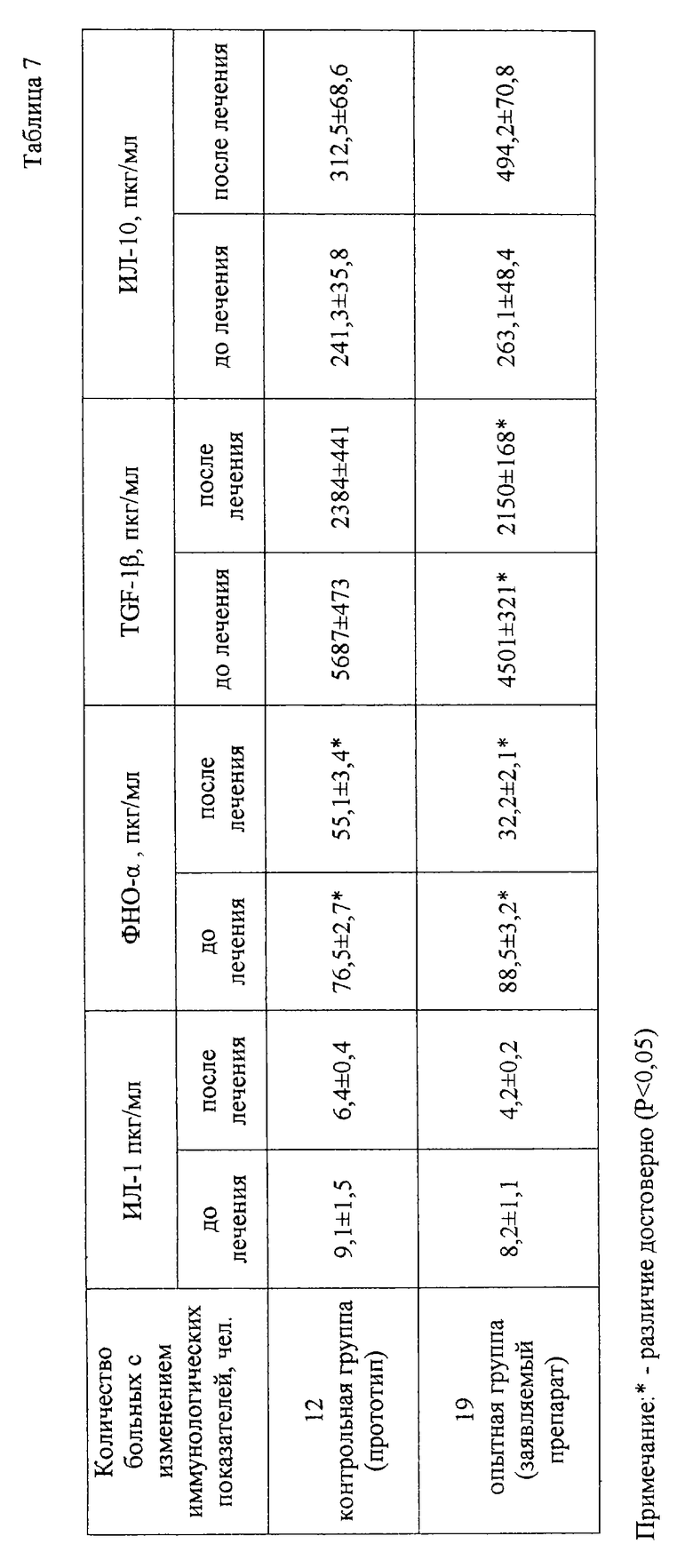
У больных контрольной группы в результате лечения уровень провоспалительных цитокинов ИЛ-1, ФНО-α и гранулоцитарно-макрофагального колонестимулирующего фактора TGF-1β снизилась в 1,4; 1,38 и 2,38 раза соответственно. Уровень противоспалительного цитокина ИЛ-10 возрос в 1,29 раза.
В опытной группе (заявляемый препарат) у 100% больных прекратилось образование новых высыпаний и исчезло чувство зуда, у 90,4% больных регрессировали псориатические очаги. Среднее время ремиссии увеличилось по сравнению с прототипом и составило 187 дней.
У 19 больных улучшение клинических показателей было подтверждено иммунологическими показателями.
Анализ динамики цитокинового статуса показал (табл.7), что при лечении заявляемым препаратом происходит снижение уровня провоспалительных цитокинов ИЛ-1, ФНО-α и TGF-1β в 1,9; 2,7 и 2,1 раза соответственно. Уровень противоспалительного цитокина ИЛ-10 возрос в 1,87 раза.
Таким образом, результаты лечения в опытной группе больных оказались лучше, чем в контрольной. Применение заявляемого препарата способствовало значительному улучшению клинической картины заболевания и увеличению среднего времени ремиссии заболевания, что свидетельствует о повышении эффективности лечения псориаза.
Лекарственный препарат для парентерального применения заявляемого состава является препаратом, обладающим повышенной биологической активностью при стабильности лекарственной формы в процессе производства и хранения.
Изобретение относится к медицине, а именно к созданию лекарственных средств для парентерального применения. Лекарственный препарат содержит в качестве активного вещества 1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)]-аммоний-Д-глюцитол в качестве стабилизатора - N-метилглюкамин, в качестве растворителя - воду для инъекций при следующем соотношении компонентов, мас. %: 1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)] -аммоний-Д-глюцитол 8,5-25,0%, N-метилглюкамин 0,05-1,00%, вода для инъекций - до 100%. Технический результат: повышение биологической активности препарата и стабильности его лекарственной формы в процессе производства и хранения. 7 табл.
Лекарственный препарат для парентерального применения, содержащий в качестве активного вещества 1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)] -аммоний-Д-глюцитол, в качестве растворителя - воду для инъекций, отличающийся тем, что он дополнительно содержит в качестве стабилизатора N-метилглюкамин при следующем соотношении компонентов, мас. %:
1-дезокси-1-N-[метил-(2-акридон-9-он-10-ил-ацетат)] - аммоний-Д-глюцитол - 8,5 - 25,0
N-метилглюкамин - 0,05 - 1,00
Вода для инъекций - До 100
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| С.Пб., 1999 | |||
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОПУХОЛЕВЫХ ЗАБОЛЕВАНИЙ | 1993 |
|
RU2076710C1 |
| СОЛИ 1-ДЕЗОКСИ-1-N-МЕТИЛАМИНОГЕКСАСПИРТОВ С N-АКРИДОНУКСУСНОЙ КИСЛОТОЙ, ОБЛАДАЮЩИЕ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ, И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 1998 |
|
RU2135474C1 |
| US 5925630 А, 20.07.1999 | |||
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| КОВАЛЕНКО А.Л | |||
| и др | |||
| Физико-химические и фармацевтические свойства N-метилглюкамина и его применение в фармацевтической технологии | |||
| Фармация | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
Авторы
Даты
2002-05-10—Публикация
2001-02-22—Подача