Изобретение относится к области медицины, конкретно, к антибактериальному веществу эритромицину.
Эритромицин - антибиотик, продуцируемый Streptomyces erythreus или другими родственными микроорганизмами. Он один из первых антибиотиков-макролидов, вошедших в медицинскую практику. Эритромицин эффективен в отношении грамположительных и некоторых грамотрицательных микроорганизмов (стафилококки, пневмококки, стрептококки, гонококки, менингококки); действует также на бруцеллы, риккетсии, возбудителей трахомы и сифилиса; слабо или совсем не влияет на большинство грамотрицательных бактерий, микобактерии, мелкие и средние вирусы, грибы. В терапевтических дозах эритромицин действует бактериостатически.
Несмотря на то, что в последние годы группа антибиотиков-макролидов значительно расширилась и создан ряд полусинтетических макролидов, превосходящих по лечебной эффективности первые антибиотики-макролиды, эритромицин не утратил своего значения и до сих пор широко применяется в медицинской практике при лечении пневмонии, пневмоплевритов и других заболеваний легких; при септических состояниях, рожистом воспалении, мастите, остеомиелите, перитоните, гнойном отите и других гнойно-воспалительных процессах; при лечении гонореи, сифилиса, профилактике и лечении ревматизма и др.
Эритромицин впервые защищен патентом США 2653899, 1953 г., в котором описан эритромицин-основание, его соли и способ его получения. Никакие лекарственные формы в патенте не упомянуты.
Выявление высокой антимикробной активности эритромицина привело к созданию различных лекарственных форм как на основе самого эритромицина, так и его производных (солей, амидов др.): капсул, таблеток, сиропов, гранул, парентеральных суспензий и растворов, мазей, свечей. Наибольшее распространение в медицинской практике нашли таблетки эритромицина по 0,1 г и 0,25 г, покрытые оболочкой (Машковский М.Д. "Лекарственные средства", "Новая Волна", 2000 г., т.2, стр. 259).
В патенте США 3485914, 1969 г. описан способ получения фармацевтического препарата, содержащего антибиотик с замедленным терапевтическим действием, и препарат, полученный этим способом. Препарат предназначен для орального применения, выполнен в виде гранул, содержащих ядро из смеси антибиотика, поливинилпирролидона и шеллака, и оболочку, покрывающую ядро, состоящую из поливинилпирролидона и шеллака. Весовое соотношение антибиотика, поливинилпирролидона и шеллака 10:0,9-1,2:0,4-0,6. Ядро может содержать наполнитель - тальк или силикат, или их смесь. Каждый грамм гранул содержит 550-700 мг антибиотика. Наиболее предпочтительным антибиотиком является эритромицин и его соли. Недостатком данного препарата является медленно наступающий терапевтический эффект, а также использование отдельных устаревших ингредиентов (например, шеллака).
В патенте США 3865935, 1975 г. описана таблетированная форма эритромицина в виде твердой кишечно-устойчивой формы, содержащей: а) гранулы, включающие эритромициновое основание и нетоксичные носители для него, быстро растворимые или диспергирующиеся в воде или кислой среде, б) безводный цитрат натрия или дигидрат цитрата натрия, в) по крайней мере один смазывающий агент, г) по крайней мере один разделяющий агент.
Ингредиенты смешивают в следующем соотношении: 5-20 частей связующего (преимущественно, поливинилпирролидон или гидроксипропилметилцеллюлоза); 12-35 частей дезинтегрирующего агента (преимущественно микрокристаллическая целлюлоза, крахмал, метилцеллюлоза, карбоксиметилцеллюлоза, тальк); 0-0,16 частей буфера (едкий натрий, едкое кали) совместно с 0-0,8 частями фосфата натрия (фосфата калия); 100 частями эритромицинового основания. Сухие гранулы комбинируют со следующими добавками: гранулы с эритромицином - 320 частей, дигидрат натрия цитрат - 300 частей, амберлит IRP-88 - 15 частей, стеарат магния - 3 части. Смесь таблетируют. Указано, что таблетки производят немедленное действие после попадания в желудочно-кишечный тракт. Недостатком данных таблеток является малый срок годности - 9 месяцев.
В патенте США 4340582, 1982 г. описаны таблетки эритромицина с покрытием, растворяющимся в кишечнике. Ядро содержит 250 частей основания эритромицина в форме его дигидрата, 35-100 частей хорошо растворимой в воде нетоксичной соли для перорального введения и 40-165 частей смазывающих веществ, связующих, разбавителей и дезинтеграторов. В качестве этих вспомогательных веществ используют поливинилпирролидон, микрокристаллическую целлюлозу, цитрат натрия, полисахариды (лактоза), тальк, кукурузный крахмал, амберлит IRP-88. Ядро покрыто оболочкой, которую наносят из раствора 16-25 частей фталата гидроксипропилметилцеллюлозы в смеси этанола и воды, содержащей красители, пигменты, пластификаторы и вкусовые вещества. В связи с тем, что в последние годы ужесточились требования к качеству лекарственных препаратов, появились новые показатели качества как в зарубежных фармакопеях, так и особенно в Госфармакопее XI изд., таблетки эритромицина, описанные в патенте США N 4340582, не соответствуют всем предъявляемым требованиям.
Задачей изобретения является создание антибактериальной фармацевтической композиции на основе эритромицина, удовлетворяющей всем требованиям Госфармакопеи XI издания, обладающей высокой биодоступностью и сроком годности не менее двух лет.
Это достигается антибактериальной фармацевтической композицией, содержащей в качестве действующего вещества терапевтически эффективное количество эритромицина, специально подобранные целевые добавки (разрыхлители, связующие), а сами таблетки-ядра покрыты кишечно-растворимой оболочкой.
В качестве целевых добавок используют крахмал, поливинилпирролидон, твин-80, соли стеариновой кислоты при следующем соотношении компонентов, % от массы эритромицина:
Крахмал - 40,95-71,33
Поливинилпирролидон - 3,53-4,77
Твин-80 - 2,78-3,84
Соль стеариновой кислоты - 1,39-1,95
Крахмал предпочтительно использовать картофельный и/или кукурузный; поливинилпирролидон предпочтителен высокомолекулярный, а в качестве соли стеариновой кислоты -стеарат магния и/или кальция.
Антибактериальная фармацевтическая композиция выполнена в твердой форме, преимущественно в виде таблетки, покрытой оболочкой.
Оболочка включает следующие ингредиенты, г на 1 таблетку-ядро:
Ацетилфталилцеллюлоза - 0,00925-0,01483
Касторовое масло - 0,00054-0,00595
Двуокись титана - 0,00085-0,00398
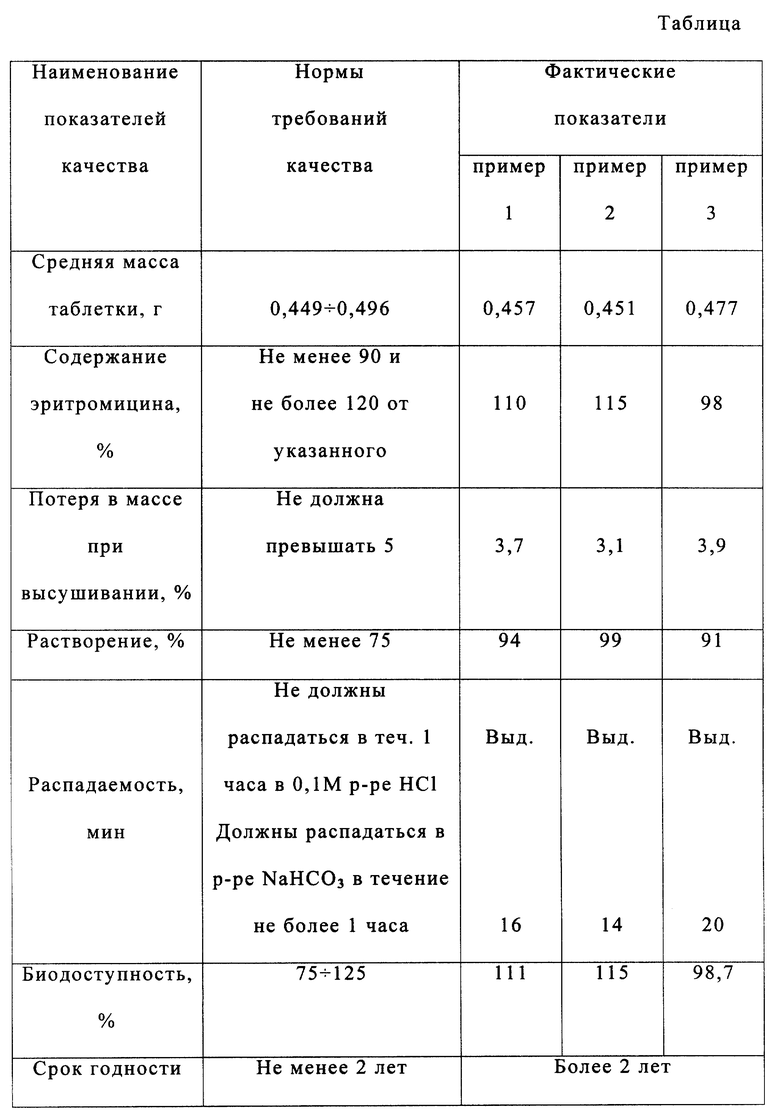
Заявляемое соотношение компонентов найдено экспериментальным путем, является оптимальным и позволяет получить технический результат, соответствующий поставленной задаче: таблетки эритромицина соответствуют всем требованиям Госфармакопеи XI изд., нормативным требованиям на эритромицин, обладают высокой биодоступностью и сроком годности не менее двух лет (см. таблицу).
Одним из способов получения таблеток является способ с влажным гранулированием, включающий следующие этапы: смешение порошков, увлажнение, смешение, гранулирование, сушку, опудривание, прессование ("Технология лекарственных форм", т.2 под редакцией Ивановой Л., М.: Медицина, 1991 г., с. 142).
Способ получения таблеток эритромицина заключается в следующем: смесь порошков эритромицина, поливинил-пирролидона, крахмала увлажняют сначала 33%-ным раствором твина-80, затем 5%-ным крахмальным клейстером и пропускают через гранулятор. Влажный гранулят сушат при 55-60oС до содержания остаточной влаги 3-5%. Высушенные гранулы пропускают через гранулятор, размолотые гранулы опудривают смесью крахмала и соли стеариновой кислоты и таблетируют на таблеточной машине. Таблетки-ядра покрывают пленкообразующим составом, состоящим из смеси ацетилфталилцеллюлозы, растворенной в смеси ацетона и спирта, двуокиси титана и касторового масла. Все это в совокупности дает возможность получить таблетки эритромицина, соответствующие всем требованиям Госфармакопеи XI издания, нормативным документам на эритромицин, легко высвобождающие действующее вещество, что обеспечивает его высокую биодоступность и в то же время срок годности таблеток не менее двух лет (см. таблицу).
Следующие примеры иллюстрируют изобретение.
Пример 1. Смешивают порошки 103,2 г эритромицина, 4,47 г поливинилпирролидона и 60,0 г кукурузного крахмала, перемешивают до однородности и увлажняют сначала 33%-ным раствором твина-80 (из 3,55 г твина-80), затем 5%-ным крахмальным клейстером (из 3,4 г кукурузного крахмала) и потом доувлажняют водой в количестве 8 мл. Полученную массу тщательно перемешивают и пропускают через гранулятор. Влажный гранулят высушивают при 55-60oС до остаточной влаги 3-5%, высушенные гранулы пропускают через гранулятор. Полученную массу опудривают смесью 2,5 г кукурузного крахмала и 1,8 г стеарата магния, готовую таблеточную массу таблетируют на таблеточной машине. Получают 385 таблеток с общей массой 173,1 г и содержанием в одной таблетке 0,258г±2% эритромицина. На полученные ядра наносят пленкообразующий состав, содержащий гомогенизированную смесь 5,182 г ацетилфталилцеллюлозы, растворенной в смеси 75,0 г ацетона и 19,4 г спирта, 2,076 г касторового масла и 1,394 г двуокиси титана. Наслаивание продолжают до получения пленки удовлетворительной толщины. Полученные таблетки отвечают всем нормативным требованиям, имеют высокую биодоступность и срок годности более двух лет (см. таблицу).
Пример 2. Получение таблеток эритромицина осуществляют по примеру 1, исходя из 103,2 г эритромицина, 60,3 г картофельного крахмала, 4,035 г поливинилпирролидона, 3,25 г твина-80, 1,64 г стеарата магния. Получают 387 таблеток-ядер с общей массой 166,4 г и содержанием в одной таблетке 0,261 г ±1,8% эритромицина. Полученные таблетки покрывают пленкообразующим составом, содержащим смесь 4,69 г ацетилфталилцеллюлозы, 1,884 г касторового масла и 1,262 г двуокиси титана. Полученные таблетки по всем показателям соответствуют всем нормативным требованиям (см. таблицу).
Пример 3. Получение таблеток эритромицина осуществляют по примеру 1, исходя из 103,2 г эритромицина, 73,5 г картофельного крахмала, 4,9 г поливинилпирролидона, 3,95 г твина-80 и 1,97 г стеарата кальция. Получают 385 таблеток с общей массой 180,96 г и содержанием в одной таблетке 0,249±1,5% эритромицина. Полученные таблетки-ядра покрывают пленкообразующим составом, содержащим 5,706 г ацетилфталилцеллюлозы, 1,105 г касторового масла и 1,532 г двуокиси титана. Полученные таблетки соответствуют всем нормативным требованиям по всем показателям (см. таблицу).
Композиция содержит в качестве действующего вещества терапевтически эффективное количество эритромицина и в качестве целевых добавок, % от массы эритромицина: крахмал 40,95-71,33, поливинилпирролидон 3,53-4,77, Твин-80 2,78-3,84 и соль стеариновой кислоты 1,39-1,95. Таблетка-ядро покрыта пленкообразующей оболочкой. Оболочка изготовлена из смеси ацетилфталилцеллюлозы, касторового масла и двуокиси титана. Способ получения таблеток осуществляется путем влажного гранулирования с последующим покрытием таблетки-ядра пленкообразующим составом. Таблетки эритромицина с покрытием соответствуют всем требованиям Госфармокопии Х1, легко высвобождают действующее вещество, что обеспечивает высокую биодоступность эритромицина. Срок годности таблеток эритромицина составляет не менее двух лет. 2 с. и 6 з.п. ф-лы, 1 табл.
Крахмал - 40,95 - 71,33
Поливинилпирролидон - 3,53 - 4,77
Твин-80 - 2,78 - 3,84
Соль стеариновой кислоты - 1,39 - 1,95
2. Композиция по п. 1, отличающаяся тем, что в качестве крахмала она содержит картофельный и/или кукурузный крахмал.
Ацетилфталилцеллюлоза - 0,00925 - 0,01483
Касторовое масло - 0,00054 - 0,00595
Двуокись титана - 0,00085 - 0,00398
7. Способ получения антибактериальной композиции в форме таблеток, отличающийся тем, что при получении композиции, охарактеризованной в любом из пп. 1-6, смешивают терапевтически эффективные количества эритромицина с поливинилпирролидоном и крахмалом, увлажняют смесь сначала 33%-ным раствором твина-80, затем 5%-ным крахмальным клейстером, гранулируют, сушат влажный гранулят, проводят сухую грануляцию, опудривание массы смесью крахмала и соли стеариновой кислоты, таблетирование и покрытие таблеток-ядер пленкообразующей оболочкой, приготовленной из смеси ацетилфталилцеллюлозы, касторового масла и двуокиси титана.
| US 4340582 А, 20.07.1982 | |||
| EP 0689840 А, 03.01.1996 | |||
| US 4925675 А, 15.05.1990 | |||
| ПРЕПАРАТ "ЭРИДИН" ДЛЯ ЛЕЧЕНИЯ БРОНХОПНЕВМОНИИ ТЕЛЯТ | 1986 |
|
RU1424170C |
| US 3689645 А, 05.09.1972. | |||
Даты
2002-05-27—Публикация
2001-07-17—Подача