Изобретение относится к области получения новых гетероциклических о-дикарбонитрилов. о-Дикарбонитрилы могут быть использованы для получения гексазоцикланов-флуорофоров, в качестве фрагмента-донора для получения гексазоцикланов-бифлуорофоров и гексазоцикланов-трифлуорофоров. Такие гексазоцикланы перспективны для использования в качестве активных сред жидких и твердых лазеров, сцинтилляторов, особенно для индикации жесткого излучения, для трансформации коротковолнового излучения в длинноволновое при передаче информации по волоконно-оптическим линиям связи, для увеличения мощности солнечных батарей, для защиты ценных бумаг, для изготовления рекламных щитов и т.д.
Известно использование фталонитрила совместно с незамещенным родамином для получения гексазоциклана (Силинг С.А., Феофанов Б.Н., Барашков Н.Н. и др. Полигексазоцикланы на основе гетероциклических диаминов. // Высокомолек. соед. Б. 1988, т. 30, 4, с. 286-291).
Данный гексазоциклан обладает следующими спектральными характеристиками: полоса излучения 540 нм при возбуждении в полосу 312 нм.
Задачей, решаемой настоящим изобретением, является получение новых гетероциклических о-дикарбонитрилов.
Заявляются гетероциклические о-дикарбонитрилы общей формулы: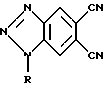
где R -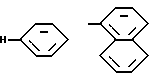
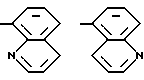
К заявляемьм соединениям относятся: 1Н-1,2,3-бензотриазол-5,6-дикарбонитрил (I):
1 -фенил- 1Н-1,2,3-бензотриазол-5,6-дикарбонитрил (II):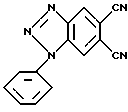
1 -(1 -нафтил)- 1Н-1,2,3-бензотриазол-5,6-дикарбонитрил (III):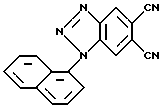
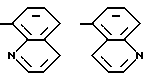
1 -(8-хинолил)- 1Н-1,2,3-бензотриазол-5,6-дикарбонитрил (IV):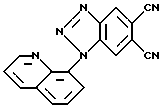
1 -(5-хинолил)-1Н-1,2,3-бензотриазол-5,6-дикарбонитрил (V):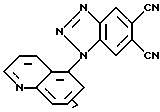
Данные соединения получают реакцией диазотирования N-R-4,5-диаминофталонитрилов с последующей циклизацией по схеме:
Данную реакцию проводят в среде уксусной кислоты при температуре 60-70oС в течение 0,5-0,6 ч.
Изобретение иллюстрируется следующими примерами:
Пример 1. К 30 мл 50%-ной уксусной кислоты добавляют 1,58 г (0,01 моль) 4,5-диаминофталонитрила. Затем к полученной суспензии при интенсивном перемешивании в один прием добавляют 0,69 г (0,01 моль) нитрита натрия, предварительно растворенного в 5 мл воды. Полученную смесь нагревают до 60oС и выдерживают при этой температуре в течение 0,5 ч. После охлаждения до комнатной температуры отфильтровывают образовавшийся осадок, промывают его 50 мл воды и кристаллизуют из этанола.
Получают 1,4 г (83,1% от теории) 1H-1,2,3-бензотриазол-5,6-дикарбонитрила. Это желтый кристаллический порошок, Тпл 237-239oС.
Найдено, %: С 56,78; Н 1,82; N 41,34.
Вычислено, %: С 56,80; Н 1,79; N 41,41; C8H3N5 .
1Н ЯМР ([2Н6] ДМСО): δ, м.д.: 14,70 (s, 1H), 8,85 (s, 2H).
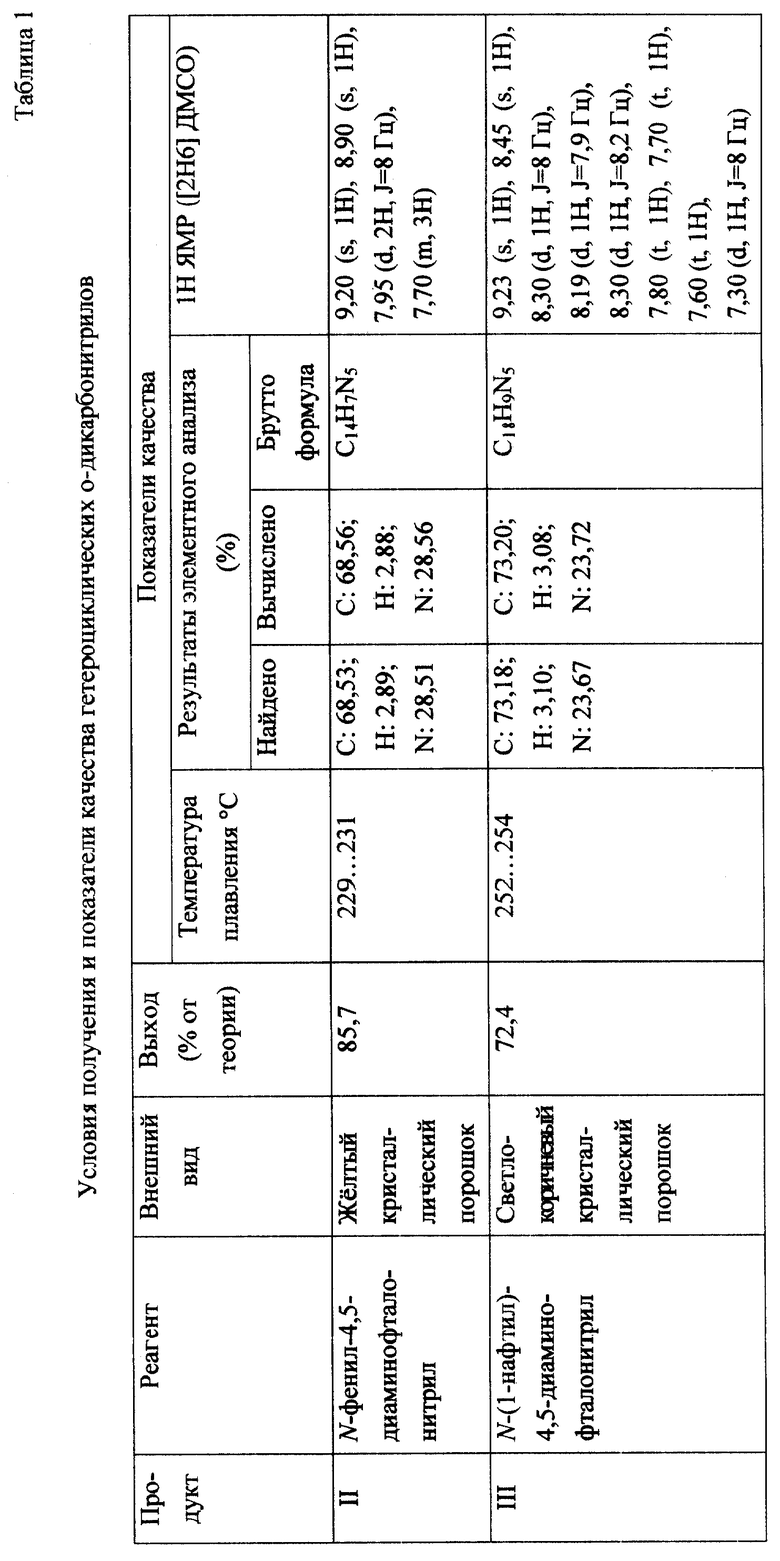
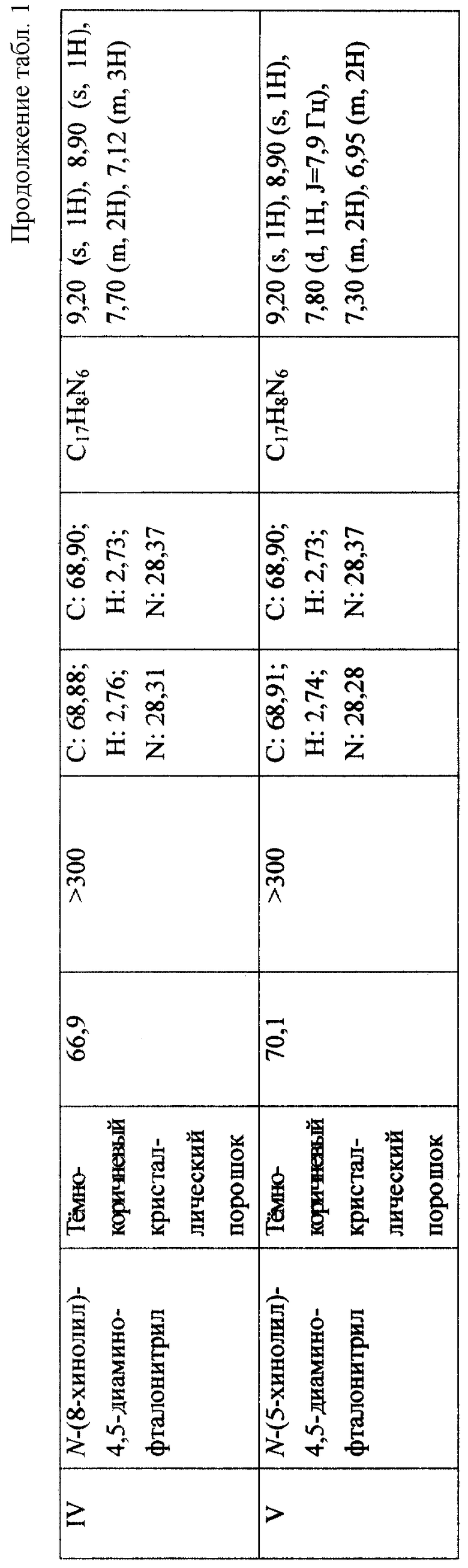
Примеры 2 - 5. Реакцию проводят аналогично примеру 1, за исключением того, что в качестве реагента (4,5-диаминофталонитрила) соответственно используются эквимолярные количества N-фенил-4,5-диаминофталонитрила, N-(1-нафтил)-4,5-диаминофталонитрила, N-(8-хинолил)-4,5-диаминофталонитрила, N-(5-хинолил)-4,5-диаминофталонитрила. Условия и результаты проведенных синтезов представлены в табл. 1.
Пример 6. Конденсация I с родамином 123. В колбу, снабженную мешалкой, термометром, обратным холодильником и капилляром для ввода аргона, загружают 1,7 г (0,01 моль) I, 3,8 г (0,01 моль) родамина 123 и 10 г фенола. Полученную смесь медленно нагревают при перемешивании до 175-185oС. Образовавшийся расплав выдерживают при перемешивании в токе аргона до прекращения выделения аммиака. После окончания реакции реакционную смесь выливают в 20 мл этанола, выпавший осадок отфильтровывают, промывают 3 мл этанола и сушат при Т=60oС в течение 2 ч, затем в вакууме над Р2О5. Получают 4,6 г (93% от теории) гексазоциклана.
Найдено, %: С 69,83; Н 3,66; N 16,80.
Вычислено, %: С 69,86; Н 3,65; N 16,86 (C58H36N12O6).
В ИК-спектре гексазоциклана отсутствует полоса 2220 см-1 -C≡N, присутствует полоса 680 см-1 - C=N-.
Структурная формула гексазоциклана, полученного на основе I и родамина 123: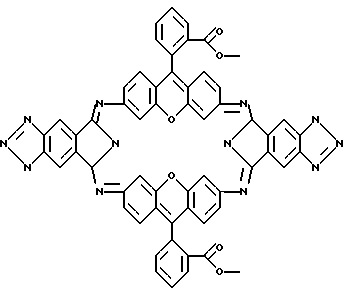
Макрогетероцикл, полученный на основе I и родамина 123, имеет следующие спектральные характеристики: максимумы спектра излучения - 433 и 502 нм при максимумах спектра поглощения - 316 и 361 нм.
Примеры 7 - 10. Реакцию проводят аналогично примеру 6, за исключением того, что вместо фталонитрила I используются эквимолярные количества других фталонитрилов II - V.
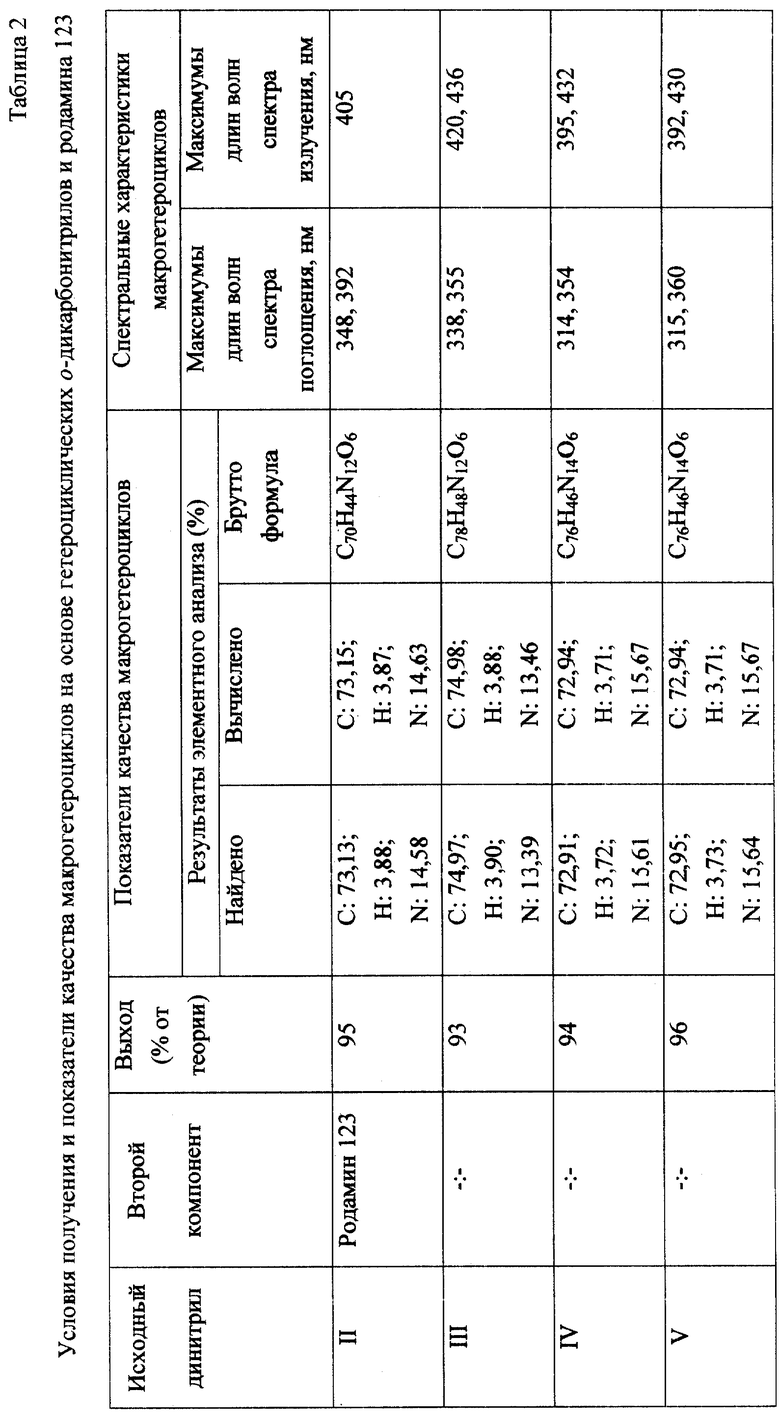
Условия и результаты проведенных синтезов, а также спектральные характеристики полученных макрогетероциклов представлены в табл.2.1
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2001 |
|
RU2183627C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2001 |
|
RU2185378C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2001 |
|
RU2204563C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2004 |
|
RU2266289C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2004 |
|
RU2266286C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2000 |
|
RU2165929C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2003 |
|
RU2246491C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2003 |
|
RU2238276C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2001 |
|
RU2200733C2 |
| 2,2'-ДИФЕНИЛ-3,3'-(N-ФЕНИЛЕН)БИС(6,7-ХИНОКСАЛИНДИКАРБОНИТРИЛ) | 2001 |
|
RU2200735C1 |
Описываются новые гетероциклические о-дикарбонитрилы формулы I
где R - водород, фенил, нафтил или хинолил. Данные соединения могут быть использованы для получения гексазоцикланов-флуорофоров, в качестве фрагмента-донора для получения гексазоцикланов-бифлуорофоров и гексазоцикланов-трифлуорофоров. Такие гексазоцикланы перспективны для использования в качестве активных сред жидких и твердых лазеров, сцинтилляторов, особенно для индикации жесткого излучения, для трансформации коротковолнового излучения в длинноволновое при передаче информации по волоконно-оптическим линиям связи, для увеличения мощности солнечных батарей, для защиты ценных бумаг, для изготовления рекламных щитов и т.д. 2 табл.
Гетероциклические о-дикарбонитрилы общей формулы
где
| Cилинг С.А | |||
| и др | |||
| Полигексазоцикланы на основе гетероциклических диаминов | |||
| Высокомолекулярные соединения, 1988, т | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| ЗАМЕЩЕННЫЕ 1-ФЕНИЛ-ИЛИ 1-ПИРИДИНИЛ-БЕНЗОТРИАЗОЛЫ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ БОРЬБЫ С НЕЖЕЛАТЕЛЬНЫМИ РАСТЕНИЯМИ | 1994 |
|
RU2144531C1 |
| Станок для притирки пробковых кранов и тому подобных изделий | 1956 |
|
SU107216A1 |
| ГРЕЙФЕР | 1946 |
|
SU69685A1 |
Авторы
Даты
2002-06-20—Публикация
2001-06-22—Подача