Область техники
Изобретение относится к новому веществу KF-1040, обладающему ингибирующей активностью в отношении метаболизма липидов, а также к способу получения такого вещества.
Предшествующий уровень техники
Известны лекарства против ожирения и лекарства против гиперлипидемии. Например, центрально действующие аноректики обычно подавляют аппетит, что может однако быть вредным для здоровья из-за снижения аппетита. В связи с этим следовало ожидать разработки нового лекарства против ожирения или терапевтического препарата против гиперлипидемии, который не проявляет побочного действия.
С другой стороны, недавно стало ясно, что гидролиз сфингомиелина, являющегося одним из липидов, составляющих биомембрану, принимает участие во внутриклеточном проведении сигнала цитокином, таким как интерлейкин 1β или фактор некроза опухолей α [Y. A. Hannun, J. Biol. Chem., 269, 3125-3128 (1994) и R. Kolesnick & D.W. Golde, Cell, 77, 325-328 (1994)] и во внутриклеточном проведении сигнала при активации Т-клеток [L.M. Boucher et al, J. Exp. Med. , 18, 2059-2068 (1995) и A. Ochi, Medicinal Immunol., 28, 397-401 (1994)] и играет роль в таких заболеваниях, как атеросклероз, воспаления, тромбоз и тому подобное и в ответственных за это механизмах иммунорегуляции. Однако профилактическое или терапевтическое лекарство для этих заболеваний до сих пор практически не было создано в отношении специфичного и эффективного ингибирования сфингомиелазы, гидролазы сфингомиелина.
Цели изобретения
Увеличение в последние годы количества больных с заболеваниями, связанными с образом жизни, поставило большие проблемы перед терапевтической и профилактической медициной. Особенно заболевания ожирением и гиперлипидемией в результате накопления триацилглицеринов из-за недавно возникшей традиции обильного питания могут часто вести к более серьезным заболеваниям, таким как атеросклероз, жировое перерождение печени, гипертония, диабет, коронарная недостаточность сердца, удар, заболевание желчного пузыря, остеоартрит, проблемы дыхания и некоторые виды рака.
Ожирение относится к физическому состоянию, при котором запасенный жир, состоящий преимущественно из триглицеридов, избыточно накапливается в теле, что принято приписывать повышенному синтезу триацилглицеринов, вызывающему избыточную аккумуляцию жира в жировой ткани. Также полагают, что триацилглицеролемия запускается облегчением синтеза триацилглицеринов в кишечнике и печени, вызывающим таким образом липопротеинемию с высокой концентрацией триацилглицеринов в крови. Таким образом полагают, что любое соединение, проявляющее ингибирующее действие на диацилглицерол:ацилтрансферазу, которая участвует в избирательном синтезе триацилглицеринов, может обладать способностью подавлять накопление триацилглицеринов в жировой ткани и крови и может быть эффективным при лечении этих заболеваний.
В этом случае, как представляется, для терапии ожирения и гиперлипидемии, а также дегенеративных заболеваний, таких как атеросклероз и тому подобных, происходящих из них, имеет смысл предложить вещество, активное в отношении ингибирования диацилглицерол:ацилтрансферазы.
Более того, ожидается также, что вещество, обладающее способностью ингибировать сфингомиелиназу, которая вызывает гидролиз сфингомиелина, структурного липида биомембран, может быть полезно в качестве лекарства против атеросклероза, тромбоза и воспаления, а также в качестве иммуносупрессора, действующего на основе нового механизма функционирования, не выявленного ранее.
Средства достижения целей изобретения
Изобретатели провели исследования метаболических продуктов, продуцируемых микроорганизмами, и нашли, что вещества/ которые обладают способностью ингибировать диацилглицерол:ацилтрансферазу и сфингомиелиназу, продуцируются в культуральной среде при культивировании идентифицированного нового штамма грибов KF-1040, выделенного из морских водорослей. Эти активные соединения, способные ингибировать метаболизм липидов, были затем выделены из указанной выше культуральной среды и очищены, затем была определена их химическая структура, представленная формулами (I) и (II), показанными ниже. Так как вещества, представленные этими формулами (I) и (II), не были известны ранее, изобретатели назвали их как "вещество A KF-1040" и "вещество В KF-1040", соответственно, которые обозначаются в общем виде как "вещество KF-1040".
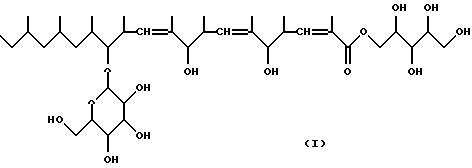
Настоящее изобретение полностью основано на сведениях, представленных выше, и оно относится к веществу KF-1040, включающему вещество А KF-1040, представленное следующей формулой (I), а именно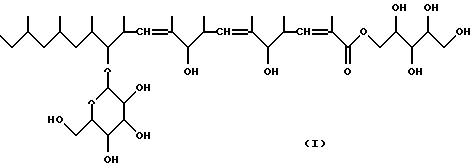
и вещество В KF-1040, представленное следующей формулой (II), а именно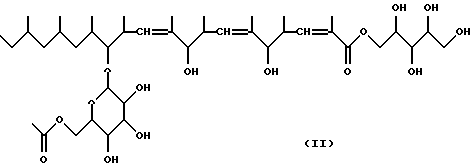
Настоящее изобретение дополнительно относится к способу получения нового вещества KF-1040, включающему культивирование микроорганизма, который принадлежит к роду Gliocladium и обладает способностью продуцировать в культуральную среду вещество A KF-1040 и/или вещество В KF-1040, вызывая аккумуляцию в культуральной среде конечного вещества А KF-1040 и/или вещества В KF-1040, и выделение вещества А KF-1040 и/или вещества В KF-1040 из культуральной среды.
Настоящее изобретение также относится к способу получения вещества KF-1040, в котором микроорганизм, который принадлежит к роду Gliocladium и обладает способностью продуцировать вещество А KF-1040 и/или вещество В KF-1040, представляет собой Gliocladium sp. KF-1040 (FERM BP-6251). Настоящее изобретение дополнительно относится к микроорганизму, который принадлежит к роду Gliocladium и обладает способностью продуцировать вещество А KF-1040 и/или вещество В KF-1040.
Микроорганизм, обладающий способностью продуцировать вещество KF-1040, представленное формулой (I) и (II) (обозначаемое здесь далее как "гриб, продуцирующий вещество KF-1040"), принадлежит к роду Gliocladium и, например, штамм грибов Gliocladium sp. KF-1040, выделенный изобретателями, представляет собой пример, наиболее эффективно используемый в соответствии с настоящим изобретением. Таксономические свойства этого продуцирующего штамма KF-1040 представлены ниже:
1. Морфологические свойства
Этот штамм относительно хорошо растет в среде, содержащей 50% морской воды (с концентрацией солей 3,4%), такой как картофельный агар с глюкозой, агар на отваре кукурузной муки, агар на солодовом экстракте, агарной среде Miura и агар на основе крахмала и морской воды с избытком конидий.
При микроскопическом исследовании колонии, растущей на агаровой среде на отваре кукурузной муки, гифа является прозрачной и имеет перегородку. Конидиофор принимает как кистеобразную, так и мутовчатую формы. Кистеобразный конидиофор (имеющий длину 100-200 мкм) поднимается прямо или ответвляется от основной гифы и образует на верхушечном конце или на ветках нескольких кистей циклические фиалиды размером 2,5-3,0 мкм • 10-23 мкм, на которых образуется конидиальная масса.
С другой стороны, мутовчатый конидиофор (имеющий длину 25-50 мкм) поднимается прямо от основной гифы и образует на верхушечном конце или на разветвляющихся фиалидах (размером 3,0-5,0 мкм • 17-25 мкм) форму удлиненной колбы или конуса, обращенного вверх верхушкой, из которого образуется единая конидиальная масса. Конидий бесцветен и имеет форму эллипсоида или удлиненного эллипсоида размером 2,5-3,0 мкм • 3,0-5,0 мкм, редко с острой верхушкой на одном конце для кистеобразного конидиофора. При мутовчатой форме конидиофор бесцветен и имеет форму эллипсоида или удлиненного эллипсоида размером 2,5-3,0 мкм • 6,0-8,5 мкм.
2. Характеристика культивирования на различных средах
Результаты визуального наблюдения за состоянием культуры этого штамма при культивировании в различных культуральных средах при 25oС в течение 14 дней даны в представленной таблице.
3. Физиологические свойства
(1) Условия оптимального роста
Условиями оптимального роста настоящего штамма являются: рН 4-8, температура 17-27oС, *концентрация морской воды 0-50%.
*: применяли 3,4%-ную концентрацию солей естественной морской воды.
(2) Условия роста
Диапазон роста штамма представляет собой: рН 3-10, температура 9-32oС, *концентрация морской воды 0-200%.
*: применяли 3,4%-ную концентрацию солей естественной морской воды.
(3) Природа: аэробная
Как показано выше, морфологические свойства, условия культивирования и физиологические свойства настоящего штамма KF-1040 представляют собой указанное выше, изобретатели провели сравнение этого штамма с известными штаммами грибов и смогли идентифицировать его как штамм, принадлежащий к роду Gliocladium и обозначаемый как Gliocladium sp. KF-1040. Этот штамм был депонирован 6 февраля 1998 г. в Национальном институте биологических наук и технологии человека, Агентства промышленной науки и технологии, Министерства международной науки и технологии под депозитарным номером FERM Р-16629 и заново депонирован 12 февраля 1998 г. в Национальном институте биологических наук и технологии человека. Агентства промышленной науки и технологии, Министерства международной науки и технологии, расположенном в 1-3, Higashi 1-Chome, Tsukuba-shi, Ibaraki-ken, Япония, под регистрационным номером FERM BP-6251 из исходного депозита для передачи по запросу на хранение на основе Будапештского соглашения.
Так как гриб, продуцирующий вещество KF-1040, применяется в соответствии с настоящим изобретением, то указанный выше штамм Gliocladium sp. KF-1040 включает каждый штамм, который принадлежит к роду Gliocladium, и продуцирует вещества KF-1040, представленные формулами (I) и (II), приведенными выше (далее обозначаемые в общем виде как "вещество KF-1040", если ничего больше специально не оговорено), включая природные мутанты, искусственные мутанты, возникающие в результате облучения рентгеновскими лучами и УФ лучами и путем мутационного воздействия таким соединением, как N-метил-N'-нитро-N-нитрозогуанидин и 2-аминопурин, гибридные штаммы и генно-инженерные штаммы.
При практическом применении настоящего изобретения грибы, продуцирующие вещество KF-1040, принадлежащие к роду Gliocladium, культивируют в культуральной среде. В качестве источников питания, подходящих для продукции вещества KF-1040, применяют питательную среду, содержащую ассимилируемые микроорганизмом источники углерода, ассимилируемые микроорганизмом источники азота и, если необходимо, добавки, включающие неорганические соли и витамины. В качестве источника углерода могут быть включены отдельно или в сочетании сахариды, такие как глюкоза, фруктоза, мальтоза, лактоза, галактоза, декстрин и крахмал, и растительные масла, такие как соевое масло и т.п.
В качестве источника азота могут быть применены отдельно или в сочетании пептон, экстракт дрожжей, мясной экстракт, порошок сои, порошок хлопчатника, жидкость от вымоченного зерна, солодовый экстракт, казеин, аминокислоты, мочевина, соли аммония и нитраты. Кроме того, в адекватном количестве могут быть добавлены соли, такие как фосфаты, соли магния, соли кальция, соли натрия и соли калия, так же как соли тяжелых металлов, такие как соли железа, соли марганца, соли меди, соли кобальта и соли цинка, и витамины, а также другие добавки, пригодные для продукции вещества KF-1040.
При культивировании, когда сталкиваются с феноменом усиленного пенообразования, может быть добавлен, если необходимо, агент, снижающий пенообразование, на основе, например, жидкого парафина, животного масла, растительного масла, силикона и поверхностно-активного вещества. Обычно благоприятно проведение культивирования в жидкой культуральной среде, тогда как жидкая и твердая среды могут применяться до тех пор, пока они содержат источники питания, указанные выше. При производстве в небольшом масштабе может быть удобна культура во флаконе. Для получения вещества, являющегося целью изобретения, в больших, промышленных масштабах предпочтительна аэрируемая культура с перемешиванием, так же как в других продуктах ферментации.
В случае культивирования, выполняемого в большом резервуаре, предпочтительно выполнять его таким образом, чтобы продуцирующий гриб в первую очередь инокулировали в относительно небольшое количество культуральной среды для культивирования в ней, для того, чтобы избежать снижения роста гриба, и культуральную смесь затем переносят в большой резервуар для воздействия на производство культуры. Здесь возможно, чтобы состав культуральной среды был тем же самым или состав среды прекультивирования и среды для продуцирования вещества отличался один от другого. Если необходимо, состав культуры для них может быть изменен.
В случае, если культивирование ведут в условиях аэрации с перемешиванием, могут быть соответствующим образом использованы способы, включающие механическое перемешивание с помощью импеллера или других приспособлений, вращение или встряхивание ферментера, перемешивание толчками или барботирование воздуха. Аэрацию проводят при стерилизации воздуха.
Температуру культуры можно соразмерно менять в пределах, в которых продуцирующий вещество KF-1040 гриб способен продуцировать вещество KF-1040, но обычно культивирование проводят при температуре в диапазоне 20-30oС, предпочтительно около 27oС. Культивирование обычно проводят при рН 5-8, предпочтительно около 7. Продолжительность культивирования может меняться в зависимости от состояния каждой отдельной культуры, но обычно в течение 10-20 дней.
Продуцированное таким способом вещество KF-1040 присутствует в выросшем таким образом мицелии и в культуральном фильтрате. Для очистки вещества KF-1040 из культуральной массы всю культуральную массу целиком экстрагируют смешиваемым с водой растворителем, таким как ацетон, и экстракт подвергают упариванию под вакуумом для удаления органического растворителя, после чего полученный остаток экстрагируют не смешиваемым с водой органическим растворителем, таким как этилацетат.
В дополнение к упомянутому выше способу экстракции, для достижения разделения вещества KF-1040 на индивидуальные компоненты и его очистки могут быть использованы в подходящем сочетании или повторно известные процедуры, используемые для очистки жирорастворимых веществ, такие как, например, адсорбционная хроматография, гель-фильтрационная хроматография, тонкослойная хроматография, центрифужная противоточная распределительная хроматография, высокоэффективная жидкостная хроматография.
Физико-химические свойства вещества A KF-1040 согласно настоящему изобретению представлены ниже:
1) Природа: белый порошок.
2) Молекулярный вес: 776 (по данным масс-спектрометрии бомбардировкой быстрыми атомами).
3) Молекулярная формула: C40H72O14.
4) Удельное вращение: [α]
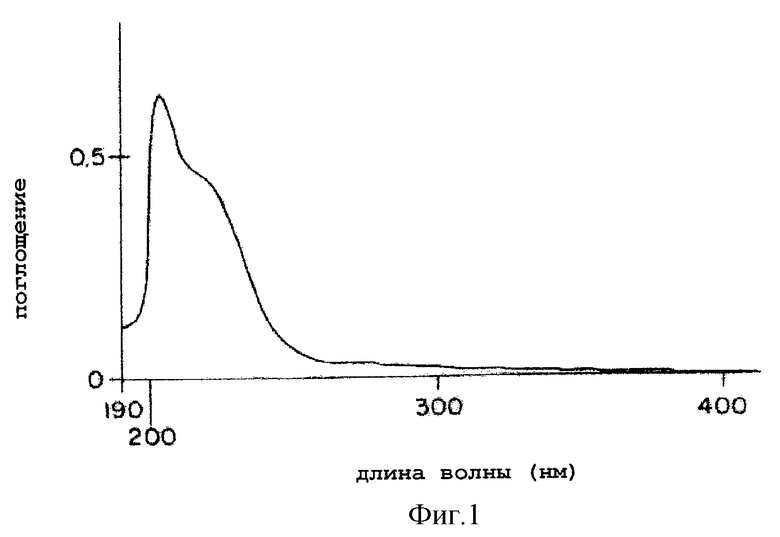
5) Максимум поглощения в УФ (в метаноле): фиг.1, при 203 нм (ε = 24900), 220 нм (ε = 18000) и 275 нм (ε = 1200).
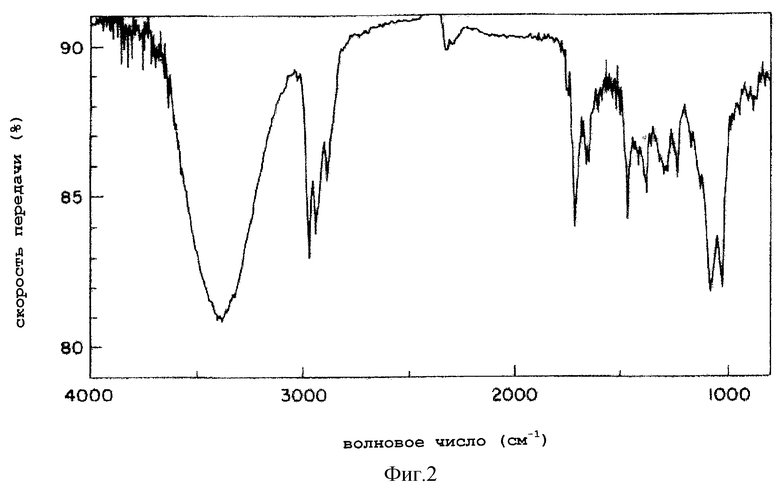
6) Максимум поглощения в ИК области (таблетка KBr): фиг.2, при 1637 см-1 и 3434 см-1.
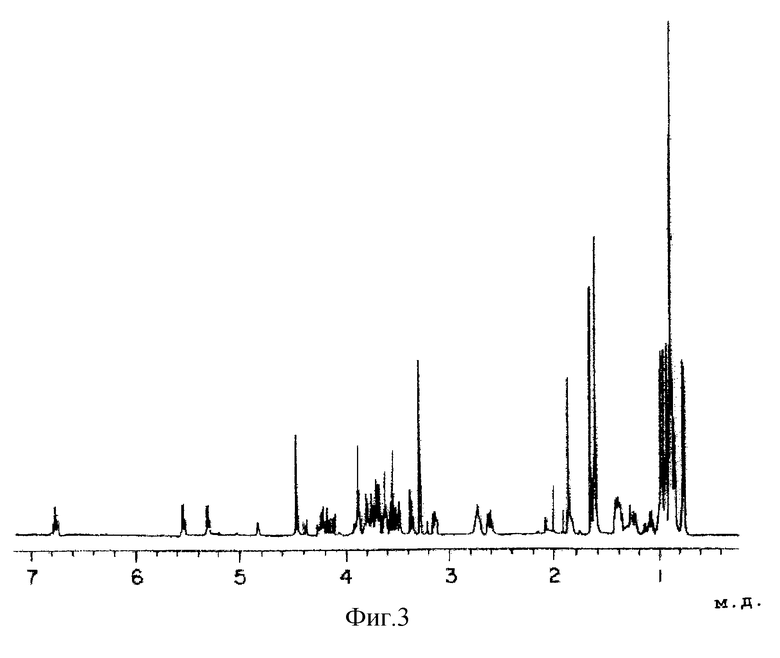
7) Протонный ЯМР-спектр (в метаноле с тяжелым водородом): как показано на фиг.3.
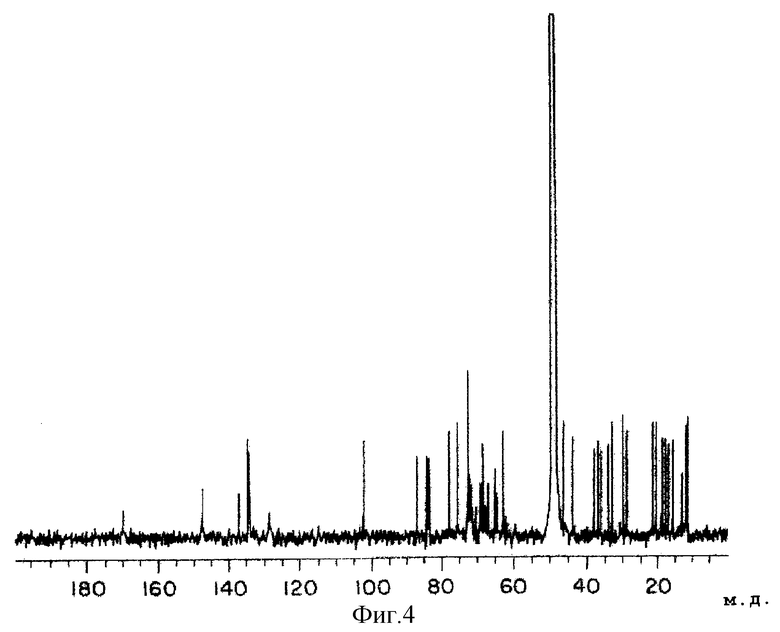
8) 13С-ЯМР-спектр (в метаноле с тяжелым водородом): как показано на фиг. 4.
9) Растворимость в растворителях: растворим в метаноле, бензоле, хлороформе и этилацетате; плохо растворим в воде и гексане.
10) Цветная реакция: положительная на серную кислоту и на фосфорномолибденовую кислоту.
11) Кислая или щелочная природа: нейтральная.
В результате рассмотрения физико-химических свойств, данных спектрального анализа вещества A KF-1040, представленных выше, была определена химическая структура вещества A KF-1040, которая представлена следующей формулой (I):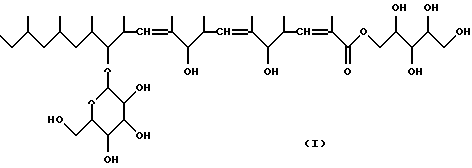
Физико-химические свойства вещества В KF-1040 согласно настоящему изобретению представлены ниже:
1) Природа: белый порошок.
2) Молекулярный вес: 818 (по данным масс-спектрометрии бомбардировкой быстрыми атомами).
3) Молекулярная формула: C42H74O15.
4) Удельное вращение: [α]
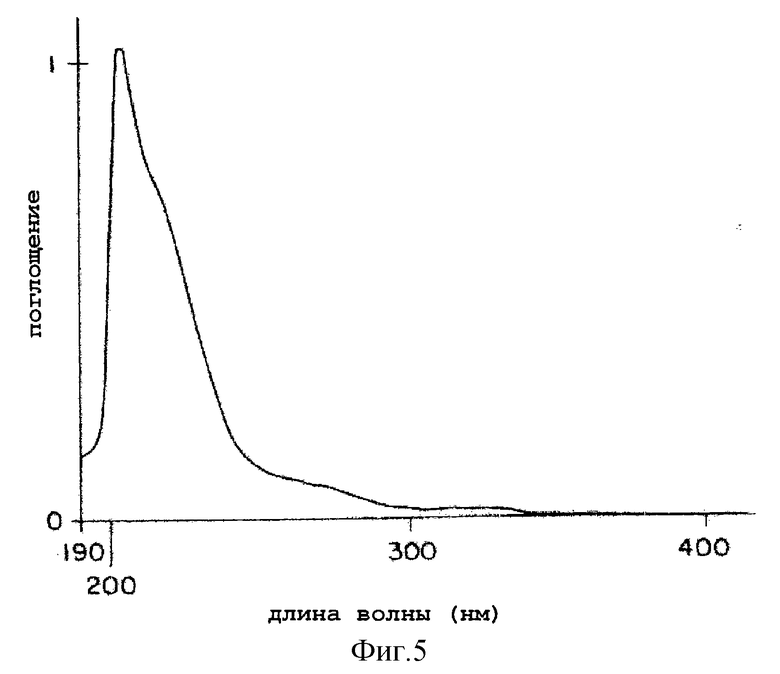
5) Максимум поглощения в УФ (в метаноле): фиг.5, при 204 нм (ε = 43000), 218 нм (ε = 30300) и 272 нм (ε = 2900).
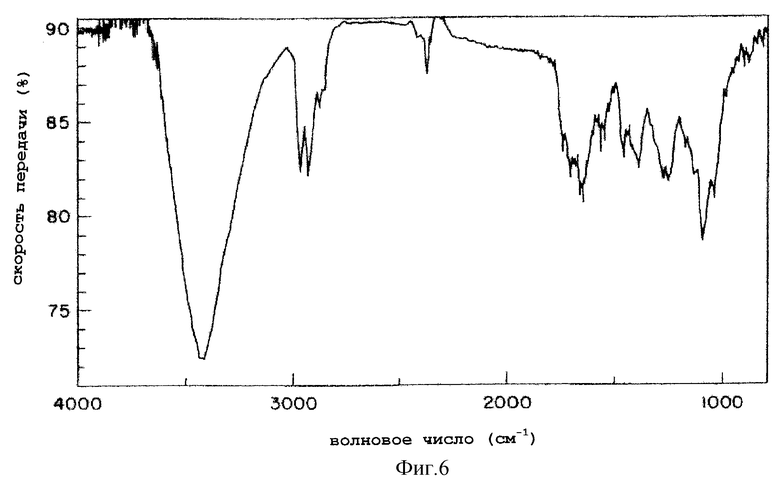
6) Максимум поглощения в ИК области (таблетка KBr): фиг.6, при 1633 см-1 и 3417 см-1.
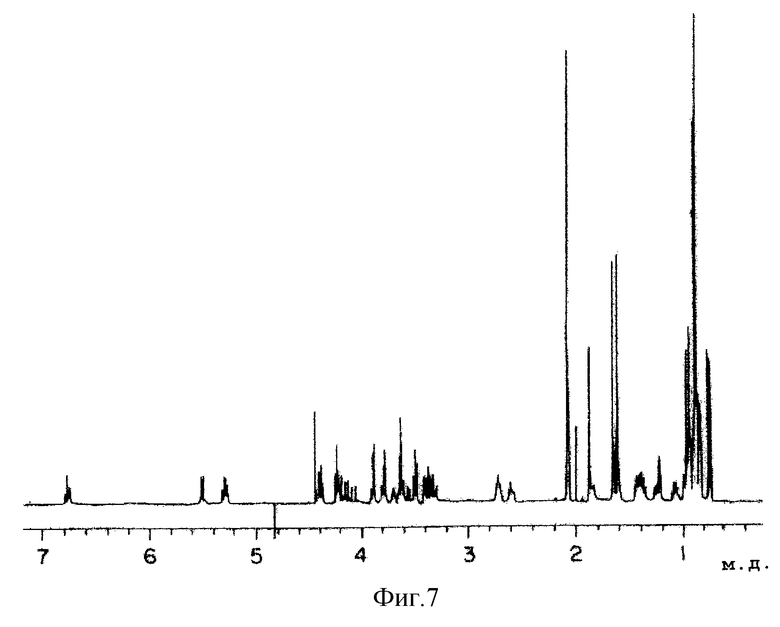
7) Протонный ЯМР-спектр (в метаноле с тяжелым водородом): как показано на фиг.7.
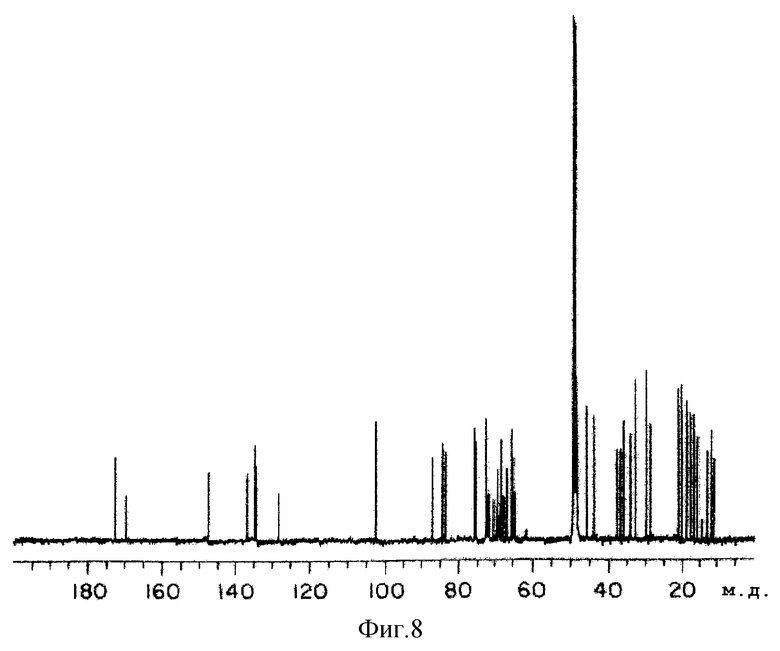
8) 13С-ЯМР-спектр (в метаноле с тяжелым водородом): как показано на фиг. 8.
9) Растворимость в растворителях: растворим в метаноле, бензоле, хлороформе и этилацетате; плохо растворим в воде и гексане.
10) Цветная реакция: положительная на серную кислоту и на фосфорно-молибденовую кислоту.
11) Кислая или щелочная природа: нейтральная.
В результате рассмотрения физико-химических свойств, данных спектрального анализа вещества В KF-1040, представленных выше, была определена химическая структура вещества В KF-1040, которая представлена следующей формулой (II):
В ходе описания, представленного выше и направленного на детали различных физико-химических свойств вещества А KF-1040 и вещества В KF-1040, было выяснено, что в литературе не сообщалось ни об одном соединении, обладающем свойствами, соответствующими идентифицированным выше свойствам. Поэтому вещества KF-1040 следует считать новыми веществами.
Теперь перейдем к описанию, направленному на биологическую природу вещества A KF-1040 и вещества В KF-1040.
(1) Ингибирующее действие в отношении диацилглицерол:ацилтрансферазы крысиного происхождения
Активность диацилглицерол: ацилтрансферазы определяли с помощью модифицированного метода Mayorek and Bar-Tana [J. Biol. Chem., 260, 6528-6532 (1985)].
Итак, в качестве источника фермента использовали микросомальную фракцию, полученную из печени крысы. К 175 мМ Трис-НСl буферу (рН 8,0), содержащему 8 мМ MgCl2, 1 мг/мл бычьего сывороточного альбумина и 2,5 мМ диизопропилфторфосфата, добавляли 0,75 мМ диолеоилглицерина и 30 мкМ [1-14C]-пальмитоил-СоА (0,02 мкКи), и суммарный объем доводили до 200 мкл, после чего ферментативную реакционную смесь инкубировали при 23oС в течение 15 минут. Общие липиды экстрагировали смесью хлороформ/метанол и индивидуальные липиды выделяли с помощью ТСХ (используя кизельгель GF254 и петролейный эфир/диэтиловый эфир/уксусную кислоту в соотношении 80/20/1 в качестве подвижной фазы) с последующим измерением радиоактивности триацилглицериновой фракции с помощью Radioscanner (фирмы AMBIS System Inc.) для определения активности диацилглицерол:ацилтрансферазы.
Расчет концентрации лекарства, соответствующей 50%-ному ингибированию этого фермента, дает величину 16 мкг/мл для вещества А KF-1040 и 9,0 мкг/мл для вещества В KF-1040.
(2) Ингибирующее действие в отношении образования триацилглицерина в клетках человеческого происхождения (клетках Raji, ведущих происхождение от человеческой лимфомы Беркитта)
Оценку влияния веществ на образование триацилглицерина проводили в соответствии со способом Tomoda et al. [J. Biol. Chem., 266, 4214-4219 (1991)] , используя клетки человеческого происхождения (клетки Raji, ведущие свое начало от человеческой лимфомы Беркитта).
Дисперсию клеток Raji с концентрацией клеток 2,7•106 на миллилитр, содержащую 0,36 нМ [1-14C]-олеиновой кислоты (0,02 мкКи) в присутствии или в отсутствие вещества, доводили до суммарного объема 200 мкл, после чего инициировали реакцию при 37oС в течение 30 минут. Общие липиды экстрагировали смесью (2/1) хлороформ/метанол. Последующие процедуры проводили тем же способом, что и в описанном выше эксперименте (1) "ингибирующее действие в отношении диацилглицерол:ацилтрансферазы крысиного происхождения".
Расчет концентрации лекарства, соответствующей 50%-ному ингибированию образования триацилглицерина, дает величину 10 мкг/мл для вещества A KF-1040 и 10 мкг/мл для вещества В KF-1040.
(3) Ингибирующее действие в отношении нейтральной сфингомиелиназы из мозга крысы
Оценку влияния веществ на нейтральную сфингомиелиназу из мозга крысы проводили в соответствии с модифицированным способом Murakami & Arima [J. Neurochem., 52, 611-618 (1989)].
Итак, в качестве источника фермента использовали мембранную фракцию, полученную из мозга крысы, и к ней добавляли 20 мМ HEPES-NaOH буферный раствор (рН 7,4), 6, 5 мМ MgCl2, 0,1% тритон Х-100 и 25 мкМ [N-метил-3H]-сфингомиелина (0,006 мкКи), смесь доводили до суммарного объема 50 мкл. После проведения реакции при 37oС в течение 30 минут к реакционной смеси добавляли 200 мкл смеси хлороформ/метанол (объемное соотношение 1/2) для отделения продукта реакции [3Н]-фосфохолина от исходного материала [3Н]-сфингомиелина. Слой супернатанта помещали в 50 мкл сосуд. Для определения активности нейтральной сфингомиелиназы количественно измеряли [3Н] -фосфохолин с помощью жидкостного сцинтилляционного счетчика.
Расчет концентрации вещества KF-1040, соответствующей 50%-ному ингибированию этого фермента, дает величины 4,2 мкг/мл для вещества А KF-1040 и 6,1 мкг/мл для вещества В KF-1040.
(4) Влияние на кислую сфингомиелиназу из плаценты человека
Оценку влияния веществ на кислую сфингомиелиназу из плаценты человека проводили в соответствии со способом Jones et al [Biochem. Journal, 195, 373-382 (1981)] с частичной модификацией.
Итак, в качестве источника фермента использовали кислую сфингомиелиназу из плаценты человека (продукт фирмы Sigma), куда добавляли 250 мМ буферный раствор ацетата натрия (рН 5,0), 0,1% NP-40 (фирмы Sigma), 25 мкМ [N-метил-3H]-сфингомиелина (0,006 мкКи) и различные концентрации вещества, и суммарный объем смеси доводили до 50 мкл. После проведения реакции при 37oС в течение 30 минут к реакционной смеси добавляли 200 мкл смеси хлороформ/метанол (объемное соотношение 1/2) для отделения продукта реакции [3Н] -фосфохолина от исходного материала [3H]-сфингомиелина. Слой супернатанта помещали в 50 мкл сосуд. [3Н]-Фосфохолин количественно определяли с помощью жидкостного сцинтилляционного счетчика для установления активности кислой сфингомиелиназы.
Расчет концентрации вещества KF-1040, соответствующей 50%-ному ингибированию этого фермента, дает величины 48 мкг/мл для вещества А KF-1040 и 24 мкг/мл для вещества В KF-1040.
Как описано выше, новое вещество согласно настоящему изобретению проявляет активность в отношении ингибирования диацилглицерол:ацилтрансферазы и сфингомиелиназы и, следовательно, полезно для профилактики и терапии больных с заболеваниями, относящимися к атеросклерозу, ожирению, тромбозу, воспалениям и иммунофункциональному расстройству.
Краткое описание чертежей
На фиг. 1 показан УФ спектр поглощения (в метаноле) вещества А KF-1040 согласно настоящему изобретению.
На фиг.2 показан ИК спектр поглощения (с KBr) вещества А KF-1040 согласно настоящему изобретению.
На фиг. 3 показан протонный ЯМР спектр (в тяжелом метаноле) вещества А KF-1040 согласно настоящему изобретению.
На фиг.4 показан 13С-ЯМР спектр (в тяжелом метаноле) вещества А KF-1040 согласно настоящему изобретению.
На фиг. 5 показан УФ спектр поглощения (в метаноле) вещества В KF-1040 согласно настоящему изобретению.
На фиг.6 показан ИК спектр поглощения (с KBr) вещества В KF-1040 согласно настоящему изобретению.
На фиг. 7 показан протонный ЯМР спектр (в тяжелом метаноле) вещества В KF-1040 согласно настоящему изобретению.
На фиг.8 показан 13С-ЯМР спектр (в тяжелом метаноле) вещества В KF-1040 согласно настоящему изобретению.
Пример
Два 500-мл сосуда Эрленмейера, каждый из которых был загружен 100 мл жидкой культуральной среды (рН 6,0), полученной растворением 2,0% глюкозы, 0,5% полипептона (от Nippon Seiyaku К.К.), 0,2% дрожжевого экстракта (от Oriental Kobo Kogyo К.К.), 0,05% 7-гидрата сульфата магния, 0,1% первичного кислого фосфорнокислого калия и 0,1% агара в 50%-ной естественной морской воде, инокулировали каждый образцом одной петли штамма Gliocladium sp. KF-1040 (FERM BP-6251), после чего инокулированную среду культивировали при 27oС в течение 4 дней при встряхивании.
Полученную культуральную среду использовали в качестве посевного материала для культивирования. В каждый из 60 сосудов Роукса емкостью по 1000 мл загружали по 300 мл жидкой культуральной среды (рН 6,0), полученной растворением 100 г/л картофельного агара и 1,0% глюкозы в 50%-ной естественной морской воде. После стерилизации и охлаждения каждый флакон инокулировали в асептических условиях 3 мл посевного материала для культивирования, после чего инокулированную смесь культивировали при 27oС в течение 16 дней в спокойном состоянии.
К объединенной культуральной жидкости добавляли 18 литров ацетона и тщательно встряхивали, после чего концентрировали при пониженном давлении и концентрированную таким образом жидкость экстрагировали этилацетатом. Слой экстракта подвергали концентрированию при пониженном давлении, в результате чего было получено 2,2 грамма сырого продукта. Этот сырой продукт растворяли в небольшом количестве ацетонитрила и полученный раствор наносили на колонку ODS (200 г, от Senshu Kagaku К.К., ODS-SS-1020T), наполненную 30% ацетонитрилом в воде. После промывки колонки 50%-ным ацетонитрилом в воде колонку элюировали 60%-ным ацетонитрилом в воде и затем 70%-ным ацетонитрилом в воде. Из элюатов с помощью концентрирования при пониженном давлении получено 87 мг сырого продукта вещества А и 104 мг сырого продукта вещества В.
Каждый из сырых продуктов фракционировали с помощью высокоэффективной жидкостной хроматографии (Shiseido Capsulepack, колонка ODS-SG, 20 мм • 250 мм, скорость тока = 6,0 мл/мин; детектирование: 215 нм в УФ с использованием в качестве элюента 70% ацетонитрила в воде). Собирали, соответственно, фракцию, элюируемую с временем удерживания 17 минут для вещества А, и фракцию, элюируемую с временем удерживания 23 минуты для вещества В. Каждую фракцию обрабатывали удалением органического растворителя и экстракцией водного слоя этилацетатом, в результате чего было получено 16 мг вещества A KF-1040 и 40 мг вещества В KF-1040.
Результат изобретения
Как подробно описано выше, новое вещество KF-1040 согласно настоящему изобретению проявляет активность в отношении ингибирования диацилглицерол: ацилтрансферазы и сфингомиелиназы и, следовательно, как можно ожидать, полезно для профилактики и терапии больных с заболеваниями, относящимися к атеросклерозу, ожирению, тромбозу, воспалениям и иммунофункциональному расстройству.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЕ WK-5344А И СОЕДИНЕНИЕ WK-5344B, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРОДУЦИРУЮЩИЙ ИХ ШТАММ STREPTOMYCES SP. WK-5344 FERM BP-6668 | 1999 |
|
RU2201964C2 |
| ГРУППА СОЕДИНЕНИЙ К04-0144, ОБЛАДАЮЩИХ АНТИМИКРОБНОЙ АКТИВНОСТЬЮ И УСИЛИВАЮЩИМ ДЕЙСТВИЕМ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2006 |
|
RU2394105C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ПОДАВЛЕНИЯ ЗАРАЖЕНИЯ И ПРОЛИФЕРАЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2002 |
|
RU2250770C2 |
| Способ получения антибиотика 76- @ | 1982 |
|
SU1276248A3 |
| ЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ И ЕГО СОЛЬ | 2009 |
|
RU2482130C2 |
| СПОСОБ ПОЛУЧЕНИЯ МАКРОЛИДНОГО СОЕДИНЕНИЯ И ШТАММЫ STREPTOMYCES SP., MORTIERELLA SP. И MICROMONOSPORACEAE | 2003 |
|
RU2330069C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2-АМИНО-4(ГИДРОКСИМЕТИЛ)-3А,5,6,6А-ТЕТРАГИДРО-4H-ЦИКЛОПЕНТ-[D]-ОКСАЗОЛ-4, 5,6-ТРИОЛА И ПРОДУЦИРУЮЩИЕ ЕГО ШТАММЫ АКТИНОМИЦЕТА MICROMONOSPORA И АКТИНОМИЦЕТА AMYCOLATOPSIS | 1992 |
|
RU2120997C1 |
| СОЕДИНЕНИЕ САХАРА | 1996 |
|
RU2193039C2 |
| Штамм базидиального гриба Trametes hirsuta - продуцент этилового спирта | 2015 |
|
RU2614263C1 |
| ГИДРОКСИЛИРОВАНИЕ КОМПАКТИНА ДО ПРАВАСТАТИНА С ПОМОЩЬЮ MICROMONOSPORA | 2000 |
|
RU2235780C2 |

Изобретение относится к новому веществу KF-1040, включающему вещество KF-1040A, представленное формулой (I), и вещество KF-1040В, представленное формулой (II), и способу их получения, который включает культивирование микроорганизмов штамма Gliocladium sp. FERM ВР-62516, способного продуцировать вещества KF-1040A и KF-1040В. В результате происходит аккумуляция этих веществ KF-1040A и/или KF-1040В в жидкой культуре и их выделение из культуры. Благодаря способности ингибировать активность диацилглицеролтрансферазы и сфингомиелиназы указанные выше вещества полезны для предотвращения и лечения атеросклероза, ожирения, тромбоза, воспаления и заболеваний, связанных с нарушениями иммунной функции. 3 с. ф-лы., 1 табл., 8 ил.
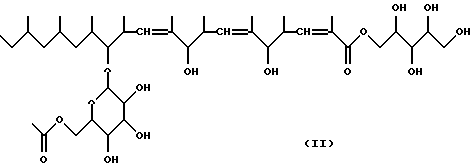
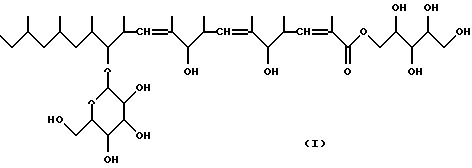
и вещество В KF-1040, представленное следующей формулой (II):
2. Способ получения вещества КF-1040, характеризующийся культивированием штамма Gliocladium sp. FERM BP-6251, способного продуцировать в культуральную среду вещество А КF-1040 и вещество B КF-1040, накоплением и выделением этих веществ из культуральной среды.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ получения (3,7-диметил-окта-2,6-диен-1,4-диол)-1-0- @ - @ -глюкопиранозида | 1983 |
|
SU1162813A1 |
Авторы
Даты
2002-07-10—Публикация
1998-02-16—Подача