Изобретение относится к новым соединениям формулы (I), обладающим ингибирующими репликацию ВИЧ свойствами. Изобретение также относится к способам получения таких новых соединений, фармацевтическим композициям, содержащим указанные новые соединения, а также к применению указанных соединений в качестве лекарственного средства.
Соединения, близкие по структуре к настоящим новым соединениям, известны из уровня техники. DE-2121694, опубликованный 25 ноября 1971, описывает некоторые s-триазины, используемые в качестве противовоспалительных, транквилизирующих, противовирусных, спазмолитических, гипогликемических, диуретических и вазодиляторных средств и для модификации секреции гормона коры надпочечников. В DE-2226474, опубликованном 22 февраля 1973, описаны производные диамино-1,3,5-триазина, обладающие повышающей гормональную секрецию активностью и противовоспалительным действием. Замещенные триазины, обладающие диуретической активностью, опубликованы в Guioca, Ann. Pharm. Fr., 31: 283-292 (1973). Ряд 2,4-диамино-триазинов получен Келарев и др. Хим. Гетероцикл. Соед. , 1392-1397 (1987) и Келарев и др. Хим. Гетероцикл. Соед., 1395-1399 (1992). Получение 2-амино-4-бензил-6-o-толуидино-s-триазина описано Yuki Y. et al., Kobunshi Kagaku, 26:141-147 (1969). Применение аралкилгуанаминов, в частности 2-амино-4-анилино-6-бензил-s-триазина, для производства смол описано в US-2817614, выданном 24 декабря 1957.
Неожиданно было обнаружено, что соединения формулы (I) эффективно ингибируют репликацию вируса иммунодефицита человека (ВИЧ) и, следовательно, могут использоваться для лечения индивидуумов, инфицированных ВИЧ.
Настоящее изобретение касается применения соединений формулы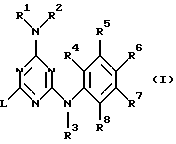
и их фармацевтически приемлемых аддитивных солей с кислотой и стереохимически изомерных форм, где
R1 и R2, каждый независимо, выбраны из водорода, гидрокси, амино, C1-6алкила, C1-6алкилокси, C1-6алкилкарбонила, C1-6алкилоксикарбонила, Аr1, моно- или ди(C1-6алкил) амино, моно- или ди(C1-6алкил) аминокарбонила, дигидро-2(3Н)-фуранона, C1-6алкила, замещенного одним или двумя заместителями, каждый из которых независимо выбран из амино, имино, аминокарбонила, аминокарбониламино, гидрокси, гидрокси C1-6алкилокси, карбоксила, моно- или ди(С1-6алкил) амино, C1-6алкилоксикарбонила и тиенила, или R1 и R2, взятые вместе, могут образовывать пирролидинил, пиперидинил, морфолинил, азидо или моно- или ди (C1-6алкил) амино С1-4алкилиден;
R3 обозначает водород, Аr1, C1-6алкилкарбонил, C1-6алкил, C1-6алкилоксикарбонил, C1-6алкил, замещенный C1-6алкилокси-карбонилом, и
R4, R5, R6, R7 и R8, каждый, независимо выбраны из водорода, гидрокси, галогена, C1-6алкила, C1-6алкилокси, циано, аминокарбонила, нитро, амино, тригалогенметила или тригалогенметилокси;
L обозначает C1-10алкил, С3-10алкенил, С3-10алкинил, С3-7циклоалкил или L обозначает C1-10алкил, замещенный одним или двумя заместителями, независимо выбранными из С3-7циклоалкила; индолила или индолила, замещенного одним, двумя, тремя или четырьмя заместителями, каждый из которых независимо выбран из галогена, C1-6алкила, C1-6алкилокси, циано, аминокарбонила, нитро, амино, тригалогенметила, тригалогенметилокси, C1-6алкилкарбонила; фенила или фенила, замещенного одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбран из галогена, гидрокси, C1-6алкила, C1-6алкилокси, циано, аминокарбонила, нитро, амино, тригалогенметила, тригалогенметилокси, C1-6алкилкарбонила, и
Ar1 - фенил или фенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, C1-6алкила, C1-6алкилокси, циано, нитро или трифторметила;
для получения лекарственного средства для лечения субъектов, страдающих от инфекции ВИЧ (вируса иммунодефицита человека).
Изобретение также касается новых соединений формулы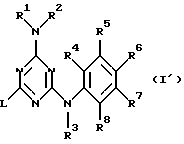
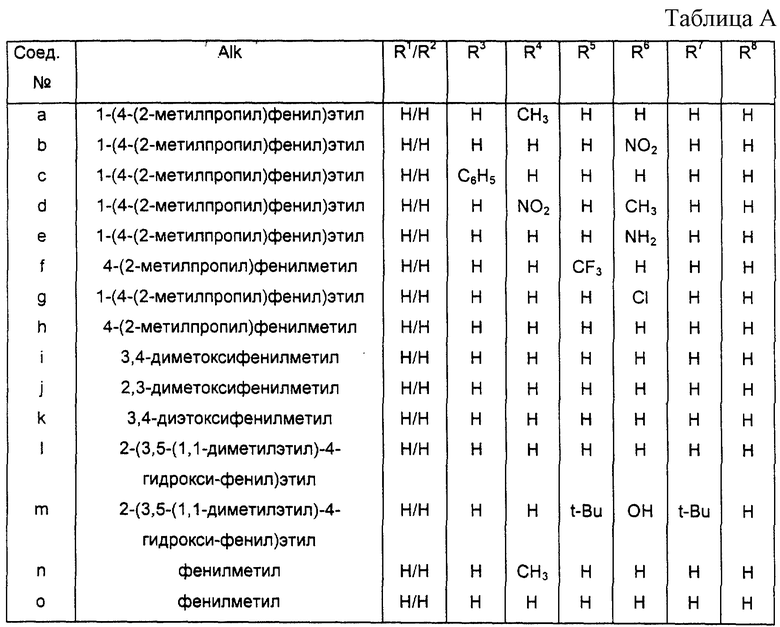
их фармацевтически приемлемых аддитивных солей с кислотой и стереохимически изомерных форм, где заместители такие же, как указаны для формулы (I), при условии, что соединения от (а) до (о) (см. табл. А) не включены.
Условие предназначено для исключения соединений от (а) до (f), которые описаны в DE-2121694 и DE-2226474; соединения (g), описанного в DE-2226474; соединений от (h) до (k), описанных Guioca, Ann. Pharm. Fr., 31:283-292 (1973); соединений (1), описанных Келарев В.И. и др., Хим. Гетероцикл. Соед. , 1392-1397 (1987); соединения (m), описанного в Келарев В.И. и др., Хим. Гетероцикл. Соед. , 1395-1399 (1992); соединения (n), описанного Yuki Y. et al. , Kobunshi Kagaku, 26: 141-147 (1969), и соединения (о), описанного в US-2817614.
Как используется в предшествующих определениях и далее здесь, галоген обозначает фтор, хлор, бром и иод, C1-2алкил включает метил и этил, C1-3алкил обозначает насыщенные углеводородные радикалы с линейной или разветвленной цепью, имеющие от 1 до 3 атомов углерода, такие как, например, метил, этил, пропил и т.п.; С1-4алкил обозначает насыщенные углеводородные радикалы с линейной или разветвленной цепью, как определено для C1-3алкила, а также их более высокие гомологи, содержащие 4 атома углерода, такие как, например, бутил и т.п.; C1-6алкил обозначает насыщенные углеводородные радикалы с линейной или разветвленной цепью, как определено для С1-4алкила, а также более высокие гомологи их, содержащие 5 или 6 атомов углерода, такие как, например, пентил или гексил; С3-6алкил обозначает насыщенные углеводородные радикалы с линейной или разветвленной цепью, имеющие от 3 до 6 атомов углерода, такие как, например, пропил, бутил, пентил, гексил и т.п.; С2-6алкил обозначает насыщенные углеводородные радикалы с линейной или разветвленной цепью, как определено для С3-6алкила, а также этил; C1-10алкил обозначает насыщенные углеводородные радикалы с линейной или разветвленной цепью, как определено для С1-6алкила, а также их более высокие гомологи, содержащие от 7 до 10 атомов углерода, такие как, например, гептил, октил, нонил и децил; С1-4алкилиден обозначает двухвалентные углеводороды с линейной или разветвленной цепью, имеющие от 1 до 4 атомов углерода, такие как, например, метилен, этилиден, пропилиден, бутилиден и т.п.; С3-7циклоалкил является родовым понятием для циклопропила, циклобутила, циклопентила, циклогексила и циклогептила; С3-10алкенил обозначает углеводородные радикалы с линейной или разветвленной цепью, содержащие одну двойную связь и имеющие от 3 до 10 атомов углерода, такие как, например, 2-пропенил, 2-бутенил, 2-пентенил, 3-пентенил, 3-метил-2-бутенил, 3-гексенил, 3-гептенил, 2-октенил, 2-ноненил, 2-деценил и т.п., при этом атом углерода, прикрепленный к триазиновому кольцу, является предпочтительно алифатическим атомом углерода; С3-10алкинил обозначает углеводородные радикалы с линейной или разветвленной цепью, содержащие одну тройную связь и имеющие от 3 до 10 атомов углерода, такие как, например, 2-пропинил, 2-бутинил, 2-пентинил, 3-пентинил, 3-метил-2-бутинил, 3-гексинил, 3-гептинил, 2-октинил, 2-нонинил, 2-децинил и т.п., при этом атом углерода, прикрепленный к триазиновому кольцу, является предпочтительно алифатическим атомом углерода; C1-6алкандиил характеризует двухвалентные насыщенные углеводородные радикалы с линейной или разветвленной цепью, имеющие от 1 до 6 атомов углерода, такие как, например, метилен, 1,2-этандиил, 1,3-пропандиил, 1,4-бутандиил, 1,5-пентандиил, 1,6-гександиил и их разветвленные изомеры.
Фармацевтически приемлемые аддитивные соли с кислотой, указанные выше, обозначают терапевтически активные нетоксичные солевые формы присоединения кислот, которые могут давать соединения формулы (I) или (I'). Соединения формулы (I) или (I'), которые имеют свойства оснований, могут быть преобразованы в их фармацевтически приемлемые аддитивные соли с кислотой путем обработки указанной основной формы подходящей кислотой. Подходящие кислоты включают, например, неорганические кислоты, такие как галогенводородные кислоты, например гидрохлорная или гидробромная кислота; серная; азотная; фосфорная и подобные кислоты; или органические кислоты, такие как, например, уксусная, пропановая, гидроксиуксусная, молочная, пировиноградная, щавелевая, малоновая, янтарная (т.е. бутандиовая кислота), малеиновая, фумаровая, яблочная, винная, лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламовая, салициловая, п-аминосалициловая, памовая и подобные кислоты.
Термин аддитивные соли также включает гидраты и сольватные аддитивные формы, которые способны образовывать соединения формулы (I) или (I'). Примерами таких форм являются, например, гидраты, алкоголяты и т.п.
Термин стехиометрически изомерные формы соединений формулы (I) или (I'), указанные выше, обозначает все возможные соединения, полученные из тех же атомов, соединенных в той же последовательности связей, но имеющие различные трехмерные структуры, которые не являются взаимозаменяемыми, которые могут иметь соединения формулы (I) или (I'). Если не оговорено или не указано иного, химическое обозначение соединения охватывает смесь всех возможных стереохимически изомерных форм, которые может иметь указанное соединение. Указанная смесь может содержать все диастереомеры и/или энантиомеры основной молекулярной структуры указанного соединения. Все стереохимически изомерные формы соединений формулы (I) или (I') как в чистом виде, так и в смеси друг с другом входят в объем настоящего изобретения.
Некоторые из соединений формулы (I) или (I') могут также существовать в таутомерных формах. Такие формы, хотя и не указаны определенно в формуле выше, входят в объем настоящего изобретения.
При использовании далее термина "соединения формулы (I) или (I')" подразумевают, что он включает также все фармацевтически приемлемые аддитивные соли с кислотой и все стереоизомерные формы.
Особой группой соединений являются соединения формулы (I-P), и она включает такие соединения формулы (I) или (I'), где R1 и R2, каждый, независимо выбраны из водорода, C1-6алкила, Аr1 или моно- или ди(C1-6алкил) аминокарбонила; или
R1 и R2, взятые вместе, могут образовывать пирролидинил, пиперидинил или морфолинил;
R3 обозначает водород, C1-6алкил или Аr1; и
Аr1 обозначает фенил или фенил, замещенный 1, 2 или 3 заместителями, каждый из которых независимо выбран из галогена, C1-6алкила, C1-6алкилокси, циано, нитро или трифторметила; и L - радикал формулы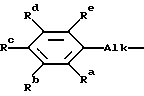
где Alk обозначает C1-6алкандиил;
Rа, Rb, Rc, Rd, Re, R4, R5, R6, R7 и R8, каждый, независимо, выбраны из водорода, галогена, С1-6алкила, C1-6алкилокси, циано, аминокарбонила, нитро, амино, тригалогенметила или тригалогенметилокси; или
Ra и Rb, взятые вместе, могут образовывать двухвалентный радикал формулы
-CH=CH-NR9- (a-1),
-NR9-CH=CH- (a-2),
где R9 обозначает водород или С1-4алкил.
Другую особую группу соединений образуют соединения формулы (I-P), из которых исключены соединения от (а) до (о), указанные соединения представлены формулой (I'-Р).
Представляющими интерес соединениями являются соединения формулы (I'), где NR1R2 имеет иное значение, чем амино.
Другими представляющими интерес соединениями являются такие соединения формулы (I'), где L обозначает C1-10алкил, С3-10алкенил, С3-10алкинил, С3-7циклоалкил; или L обозначает C1-10алкил, замещенный одним или двумя заместителями, независимо выбранными из С3-7циклоалкила; индолил или индолил, замещенный одним, двумя, тремя или четырьмя заместителями, каждый из которых независимо выбран из галогена, C1-6алкила, C1-6алкилокси, циано, аминокарбонила, нитро, амино, тригалогенметила, тригалогенметилокси, C1-6алкилкарбонила; фенил, замещенный одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбран из галогена, C1-3алкила, С3-6алкилокси, циано, аминокарбонила, нитро, амино, тригалогенметила, тригалогенметилокси, C1-6алкилкарбонила.
Еще одними представляющими интерес соединениями являются такие соединения формулы (I), к которым применимо одно из следующих ограничений:
1) R4 обозначает гидрокси, галоген, С2-6алкил, C1-6алкилокси, циано, аминокарбонил, амино, тригалогенметил или тригалогенметилокси; или
2) R5 обозначает гидрокси, галоген, C1-3алкил, C1-6алкилокси, циано, аминокарбонил, нитро, амино или тригалогенметилокси; или
3) R6 обозначает С2-6алкил, C1-6алкилокси, циано, аминокарбонил, нитро, тригалогенметил или тригалогенметилокси; или
4) R7 обозначает гидрокси, галоген, C1-3алкил, C1-6алкилокси, циано, аминокарбонил, нитро, амино, тригалогенметил или тригалогенметилокси; или
5) R8 обозначает гидрокси, галоген, С1-6алкил, C1-6алкилокси, циано, аминокарбонил, нитро, амино, тригалогенметил или тригалогенметилокси.
Частными случаями соединений являются такие соединения формулы (I) или (I'), где L обозначает С3-10алкенил или C1-2алкил, замещенный одним или двумя заместителями, независимо выбранными из С3-7циклоалкила; индолил или индолил, замещенный одним, двумя, тремя или четырьмя заместителями, каждый из которых независимо выбран из галогена, C1-6алкила, C1-6алкилокси, циано, аминокарбонила, нитро, амино, тригалогенметила, тригалогенметилокси, C1-6алкилкарбонила; фенил или фенил, замещенный одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбран из галогена, гидрокси, C1-6алкила, C1-6алкилокси, циано, аминокарбонила, нитро, амино, тригалогенметила, тригалогенметилокси, C1-6алкилкарбонила; более конкретно, где L обозначает С5-8алкенил или С1-2алкил, замещенный одним или двумя заместителями, независимо выбранными из циклопропила; индолил или индолил, замещенный одним, двумя, тремя или четырьмя заместителями, каждый из которых независимо выбран из галогена, гидрокси, C1-6алкила, C1-6алкилокси, тригалогенметила, тригалогенметилокси, C1-6алкилкарбонила.
Также частными случаями соединений являются соединения формулы (I) или (I'), где R4, R7 и R8 обозначает водород, и R5 и R6, каждый, независимо, обозначает водород, циано, галоген или аминокарбонил; более конкретно, где R4, R5, R7 и R8 обозначают водород, и R6 обозначает циано.
Другими частными случаями соединений являются соединения формулы (I) или (I'), где R1 и R2, каждый, независимо выбраны из водорода; гидрокси; амино; C1-6алкила; C1-6алкилокси; C1-6алкилкарбонила; Аr1; моно- или ди(C1-6алкил) аминокарбонила; дигидро-2(3Н)-фуранона; C1-6алкила, замещенного одним или двумя заместителями, каждый из которых независимо выбран из амино, имино, аминокарбонила, аминокарбониламино, гидрокси, гидрокси C1-6алкилокси, карбоксила, моно- или ди(C1-6алкил) амино, C1-6алкилоксикарбонила и тиенила; или R1 и R2, взятые вместе, образуют азидо или моно- или ди (C1-6алкил) аминоС1-4алкилиден; более конкретно, где R1 обозначает водород и R2 обозначает водород; гидрокси; амино; C1-6алкил; C1-6алкилокси; C1-6алкилкарбонил; C1-6алкилоксикарбонил; Аr1; моно- или ди (C1-6алкил) аминокарбонил; дигидро-2(3Н)-фуранон; C1-6алкил, замещенный одним или двумя заместителями, каждый из которых независимо выбран из амино, имино, аминокарбонила, аминокарбониламино, гидрокси, гидрокси C1-6алкилокси, карбоксила, моно- или ди(C1-6алкил) амино, C1-6алкилоксикарбонила или тиенила.
Предпочтительной группой соединений являются такие соединения формулы (I) или (I'), где L обозначает 2,6-дихлорфенилметил.
Другую предпочтительную группу соединений образуют такие соединения формулы (I) или (I'), где R3 обозначает водород, R4, R5, R7 и R8 обозначает водород и R6 обозначает циано.
Еще одну группу предпочтительных соединений образуют такие соединения формулы (I) или (I'), где R1 обозначает водород и R2 обозначает водород или гидрокси.
Более предпочтительными являются такие соединения формулы (I) или (I'), где L обозначает 2,6-дихлорфенилметил, R3 обозначает водород, R4, R5, R7 и R8 обозначают водород и R6 обозначает циано.
Наиболее предпочтительными соединениями являются 4-[[4-амино-6-[(2,6-дихлорфенил)метил] -1,3,5-триазин-2-ил] амино]бензонитрил; 4-[[4-[(2,6-дихлорфенил)метил]-6-(гидроксиамино)-1,3,5-триазин-2-ил] амино]бензонитрил и их фармацевтически приемлемые аддитивные соли с кислотами.
Обычно соединения формулы (I) могут быть получены в соответствии со способами, описанными в DE-2121694 и DE-2226474 и Guioca, Ann. Pharm. Fr., 31:283-292 (1973).
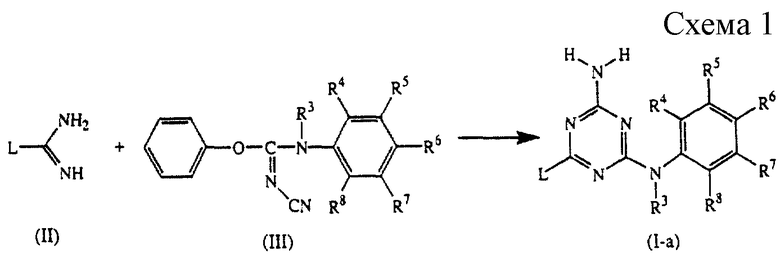
Соединения формулы (I-а), являющиеся соединениями формулы (I), где R1 и R2 обозначают водород, могут быть получены путем взаимодействия промежуточного соединения формулы (II) с промежуточным соединением формулы (III) в реакционно-инертном растворителе, таком как, например, N,N-диметилформамид (см. схему 1 в конце описания).
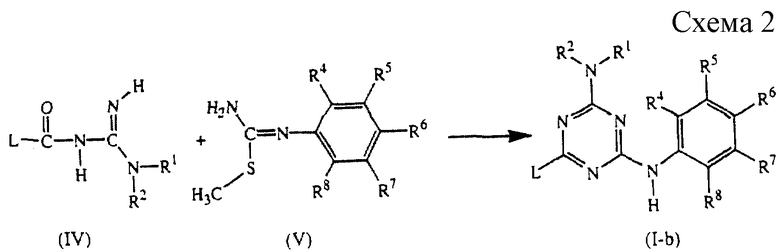
Соединения формулы (I-b), являющиеся соединениями формулы (I), где R3 обозначает водород, могут быть получены путем взаимодействия промежуточного соединения формулы (IV) с промежуточным соединением формулы (V) в реакционно-инертном растворителе, таком как, например, N,N-диметилформамид (см. схему 2 в конце описания).
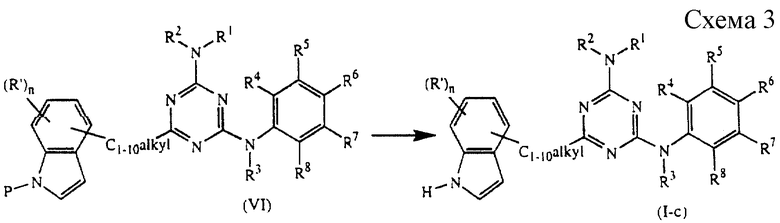
Соединения формулы (I), где L обозначает С1-10алкил, замещенный индолилом или индолилом, замещенным одним, двумя, тремя или четырьмя заместителями, каждый из которых независимо выбран из галогена, C1-6алкила, C1-6алкилокси, циано, аминокарбонила, нитро, амино, тригалогенметила, тригалогенметилокси, C1-6алкилкарбонила, причем указанные заместители представлены (R')n, где n - от 1 до 4, и указанные соединения представлены формулой (I-с), могут быть получены путем снятия защиты промежуточного соединения формулы (IV), где Р является подходящей защитной группой, такой как, например, толуолсульфонилоксигруппа или тому подобное, согласно известным методикам удаления защитных групп, таким как кипячение с обратным холодильником в реакционно-инертном растворителе, например в воде, метаноле или их смеси, в присутствии основания, например, карбоната калия или тому подобное (см. схему 3 в конце описания).
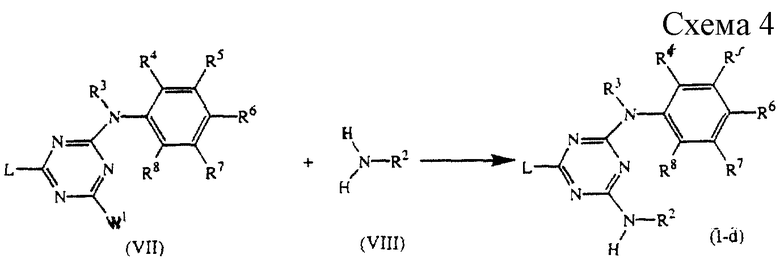
Соединения формулы (I), где R1 обозначает водород, представленные формулой (I-d), могут быть получены путем взаимодействия промежуточного соединения формулы (VII), где W1 обозначает подходящую уходящую группу, такую как, например, галоген, с аминопроизводным формулы (VIII) в реакционно-инертном растворителе, таком как, например, 1,4-диоксан и тому подобное, в присутствии подходящего основания, такого как, например, гидроксид натрия, триэтиламин или N,N-диизопропилэтиламин или тому подобное (см. схему 4 в конце описания).
В случае когда R2 содержит гидроксигруппу, можно подходящим образом осуществить вышеуказанное взаимодействие с защищенной формой промежуточного соединения (VIII), гидроксигруппа которого имеет подходящую защитную группу Р, которая является, например, группой триалкилсилила, с последующим удалением защитной группы согласно известным методикам.
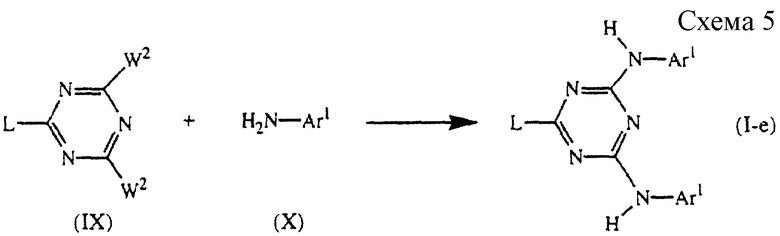
Соединения формулы (I), где R1 и R3 обозначает водород, а R2 и часть молекулы С6 (R4R5R6R7R8) являются идентичными, представленные формулой (I-е), могут быть получены путем взаимодействия промежуточного соединения формулы (IX), где W2 обозначает подходящую уходящую группу, такую как, например, галоген или тому подобное, с промежуточным соединением формулы (X) в реакционно-инертном растворителе, таком как, например, 1,4-диоксан (см. схему 5 в конце описания).
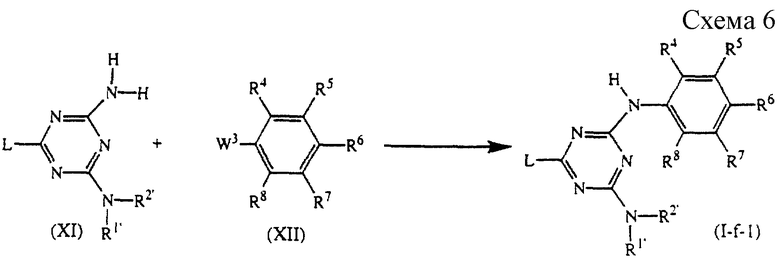
Соединения формулы (I), где R1 и R2 иные, чем водород, и они представлены R1′ и R2′ соответственно, причем указанные соединения, представленные формулой (I-f-1), могут быть получены путем взаимодействия промежуточного соединения формулы (XI) с промежуточным соединением формулы (XII), где W3 - подходящая уходящая группа, такая как, например, галоген, в реакционно-инертном растворителе, таком как, например, N,N-диметилформамид или N,N-диметилацетамид, и в присутствии подходящего основания, такого как, например, гидрид натрия или карбонат калия (см. схему 6 в конце описания).
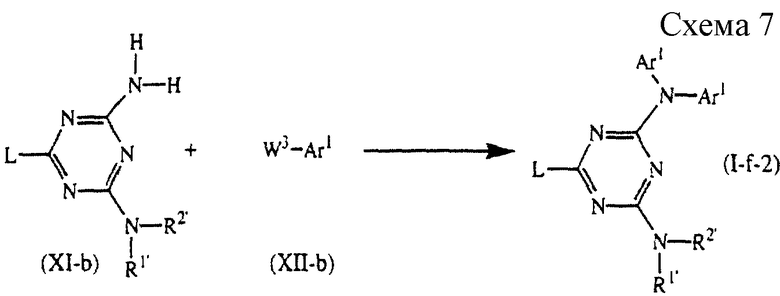
В случае когда промежуточное соединение (XII) ограничено для W3 - Ar1(XII-b) и R3 - водород, время реакции может быть установлено образованием дизамещенных аналогов, представленных формулой (I-f-2) (см. схему 7 в конце описания).
Соединения формулы (I) могут быть также получены путем преобразования соединений формулы (I) друг в друга согласно известным в данной области реакциям превращения групп.
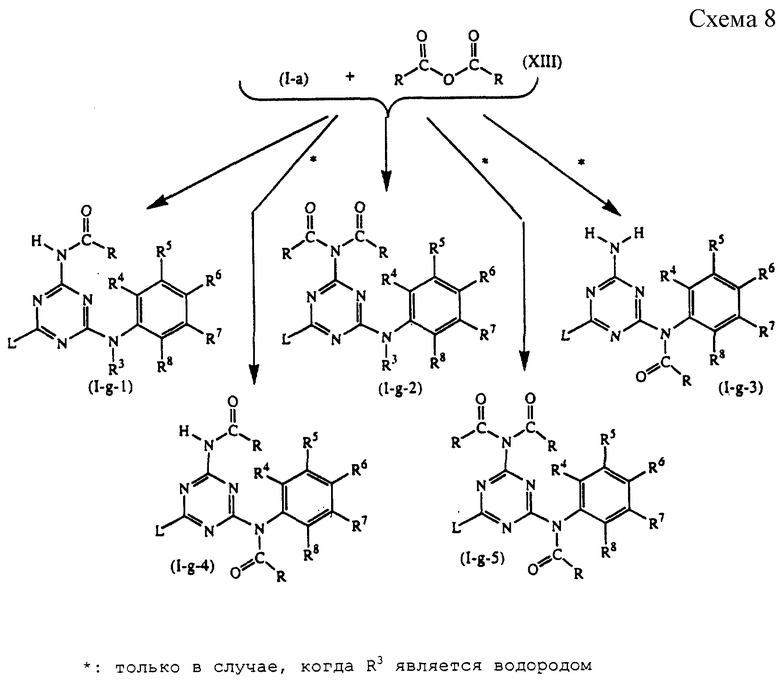
Например, соединения формулы (I-а) могут быть подвергнуты взаимодействию с ангидридом формулы (XIII), где R имеет такие значения, что -C(=O)-R является частью определения R1 или R2, согласно способу, описанному в Arch. Pharm. (Waldheim) 1986, 319, 275, с получением таким образом соединений формулы (I-g). По этой реакции время кипячения с обратным холодильником является существенным; более продолжительные периоды времени приводят к более низкому выходу монозамещенных конечных продуктов и повышенному образованию ди- и, где возможно, тризамещенных конечных продуктов (см. схему 8 в конце описания).
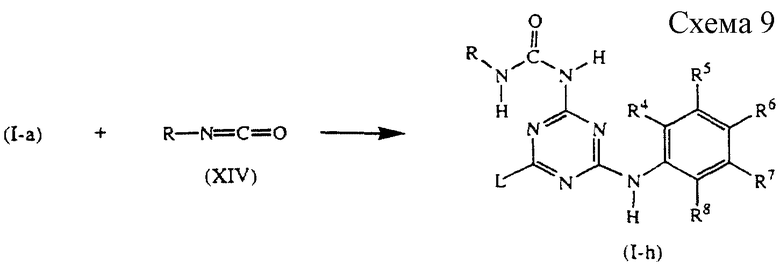
Соединения формулы (I-а) могут быть также подвергнуты взаимодействию с реагентом формулы (XIV) в реакционно-инертном растворителе, таком как, например, N,N-диметилформамид, в присутствии подходящего основания, такого как, например, гидрид натрия (см. схему 9 в конце описания).
Некоторые из промежуточных соединений, указанных выше, являются коммерчески доступными или могут быть получены согласно известным методикам, в то время как другие промежуточные соединения считаются новыми. Промежуточные соединения формулы (II) могут быть получены путем взаимодействия цианопроизводного формулы (XV) с хлоридом аммония (XVI) или его функциональным производным в реакционно-инертном растворителе, таком как, например, толуол, и в присутствии подходящего катализатора, такого как, например, триметилалюминий (см. схему 10 в конце описания).
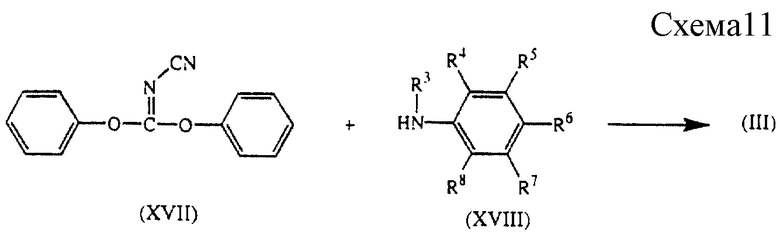
Промежуточные соединения формулы (III) обычно могут быть получены путем взаимодействия дифенил-N-цианокарбонимидата формулы (XVII), который может быть получен согласно Webb R.L. et al., J. Heterocyclic Chem., 19:1205-1206 (1982), с производным анилина формулы (XVIII) в реакционно-инертном растворителе, таком как, например, N,N-диметилформамид ( см. схему 11 в конце описания).
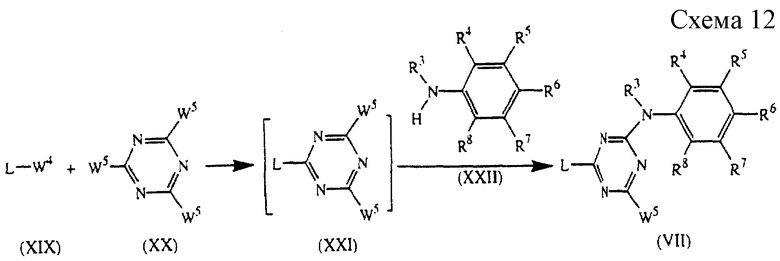
Промежуточные соединения формулы (VII) могут быть получены путем приготовления вначале реактива Гриньяра промежуточного соединения формулы (XIX), где W4 является подходящей уходящей группой, такой как, например, галоген, например бром, в присутствии магния в реакционно-инертном растворителе, таком как, например, простой диэтиловый эфир, и последующего взаимодействия указанного реактива Гриньяра с промежуточным соединением формулы (XX), где W5 является подходящей уходящей группой, такой как, например, галоген, например хлор, в реакционно-инертном растворителе, таком как, например, бензол, с получением таким образом промежуточного соединения формулы (XXI). Может быть удобным проведение вышеуказанного взаимодействия в инертной атмосфере, такой как, например, атмосфера аргона. Промежуточное соединение (XXI) может быть выделено из реакционной среды или может быть далее подвергнуто взаимодействию in situ с промежуточным соединением формулы (XXII) в реакционно-инертном растворителе, таком как, например, 1,4-диоксан, и в присутствии подходящего основания, такого как, например, диизопропилэтанамин или т.п., с получением таким образом промежуточного соединения формулы (VII). Промежуточные соединения формулы (VII) считаются новыми (см. схему 12 в конце описания).
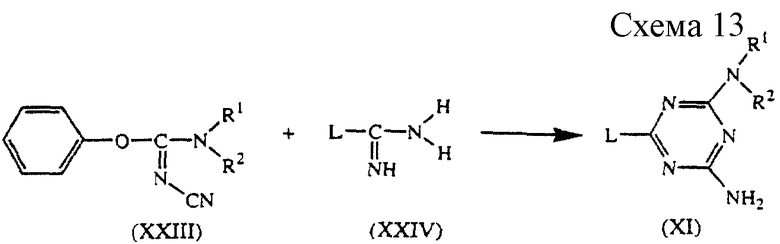
Промежуточные соединения формулы (XI) могут быть получены путем взаимодействия промежуточного соединения формулы (XXIII) с промежуточным соединением формулы (XXIV) в реакционно-инертном растворителе, таком как, например, N,N-диметилформамид (см. схему 13 в конце описания).
Соединения формулы (I) и некоторые из промежуточных соединений могут иметь один или несколько стереоизомерных центров в своей структуре, представленные R или S конфигурацией.
Соединения формулы (I), полученные описанными выше способами, могут быть синтезированы в виде смеси стереоизомерных форм, в частности в виде рацемических смесей энантиомеров, которые могут быть отделены друг от друга следующими известными методиками разделения. Рацемические соединения формулы (I) могут быть преобразованы в соответствующие диастереомерные солевые формы путем взаимодействия с подходящей хиральной кислотой. Указанные диастереомерные солевые формы затем разделяют, например, путем селективной или фракционной кристаллизации, и энантиомеры высвобождают с помощью щелочи. Альтернативный путь разделения энантиомерных форм соединений формулы (I) включает жидкостную хроматографию с использованием хиральной стационарной фазы. Указанные стереохимически чистые изомерные формы могут быть также получены из соответствующих стереохимически чистых изомерных форм подходящих исходных продуктов при условии, что реакция протекает стереоспецифически. Если желателен конкретный стереоизомер, целесообразно было бы синтезировать указанное соединение стереохимическими методами получения. В этих методах преимущественно должны использоваться энантиомерно чистые исходные вещества.
Соединения формулы (I) проявляют антиретровирусные свойства, в частности против вируса иммунодефицита человека (ВИЧ), который является этилогическим агентом синдрома приобретенного иммунодефицита (СПИД) у людей. Вирус ВИЧ преимущественно заражает клетки Т-4 человека и разрушает их или изменяет их нормальную функцию, особенно координацию иммунной системы. В результате инфицированный пациент имеет постоянно снижающееся число клеток Т-4, которые, сверх того, ведут себя аномально. Таким образом, система иммунной защиты оказывается не способной к борьбе с инфекциями и новообразованиями, и инфицированный ВИЧ субъект обычно умирает от инфекций условно-патогенными микроорганизмами, таких как пневмония, или от рака. Другие состояния, связанные с инфекцией ВИЧ, включают тромбоцитопению, саркому Капоши и инфекцию центральной нервной системы, характеризующуюся прогрессирующей демиелинизацией, следствием чего является деменция и такие симптомы, как прогрессирующие расстройство артикуляции, атаксия и дезориентировка. Инфекция ВИЧ также ассоциируется с периферической невропатией, прогрессирующей распространенной лимфаденопатией (PGL) и комплексом, относящимся к СПИД (ARC).
Настоящие соединения также показывают активность против штаммов ВИЧ-1, которые имеют приобретенную резистентность к известным ненуклеозидным ингибиторам обратной транскриптазы. Они также имеют небольшой, но не связывающий аффинитет к α-1 кислотному гликопротеину человека.
Благодаря их антиретровирусным свойствам, в частности их свойствам против ВИЧ, особенно их анти-ВИЧ-1-активности, соединения формулы (I), их фармацевтически приемлемые соли и стереохимически изомерные формы могут использоваться при лечении индивидуумов, инфицированных ВИЧ, и для профилактики этих индивидуумов. Обычно соединения по настоящему изобретению могут использоваться при лечении теплокровных животных, инфицированных вирусами, существование которых опосредуется ферментом обратной транскриптазой или зависит от нее. Состояния, которые можно предотвратить или лечить соединениями по настоящему изобретению, особенно состояния, связанные с ВИЧ и другими патогенными ретровирусами, включают СПИД, относящийся к СПИД комплекс (ARC), прогрессирующую распространенную лимфаденопатию (PGL), а также хронические заболевания ЦНС, вызываемые ретровирусами, такие как, например, опосредуемая ВИЧ деменция и рассеянный склероз.
Поэтому соединения по настоящему изобретению могут быть использованы как лекарственные средства против вышеупомянутых состояний. Указанное применение как лекарственного средства или способ лечения содержит системное введение ВИЧ-инфицированным субъектам количества, эффективного для борьбы с состояниями, связанными с ВИЧ и другими патогенными ретровирусами, особенно ВИЧ-1.
Настоящие соединения могут быть включены в состав различных фармацевтических форм для целей введения. Указанные фармацевтические формы или композиции считаются новыми и, следовательно, составляют другой аспект настоящего изобретения. А также получение указанных композиций составляет еще один аспект настоящего изобретения. В качестве подходящих композиций могут быть указаны все композиции, обычно используемые для системно вводимых лекарств. Для получения фармацевтических композиций этого изобретения эффективное количество конкретного соединения, возможно в виде аддитивной соли с кислотой, в качестве активного ингредиента объединяют в тонкой смеси с фармацевтически приемлемым носителем, который может иметь большое разнообразие форм в зависимости от формы препарата, желаемого для введения. Такие фармацевтические композиции желательны в виде подходящей стандартной лекарственной формы, в частности для введения перорально, ректально, чрескожно или путем парентеральной инъекции. Например, при получении композиций в виде пероральной лекарственной формы может быть использована любая обычная фармацевтическая среда, такая как, например, вода, гликоли, масла, спирты и тому подобное, в случае жидких пероральных препаратов, таких как суспензии, сиропы, эликсиры и растворы; или твердые носители, такие как крахмалы, сахара, каолин, смазки, связующие, разрыхляющие средства и тому подобное, в случае порошков, пилюль, капсул и таблеток. Ввиду легкости их введения таблетки и капсулы представляют наиболее предпочтительные пероральные стандартные лекарственные формы, в этом случае обязательно используют твердые фармацевтические носители. Для парентеральных композиций носитель будет обычно содержать стерильную воду, по меньшей мере в большей части, хотя могут быть включены другие ингредиенты, например, для облегчения растворимости. Могут быть получены, например, растворы для инъекций, в которых носитель содержит физиологический раствор, раствор глюкозы или смесь физиологического раствора и раствора глюкозы. Могут быть приготовлены также суспензии для инъекций, в этом случае могут быть использованы подходящие жидкие носители, суспендирующие вещества и т.п. Также включенными являются твердые препаративные формы, которые предназначены для преобразования непосредственно перед использованием в жидкие препаративные формы. В композициях, пригодных для чрескожного введения, носитель необязательно содержит средство, улучшающее проницаемость и/или подходящее смачивающее вещество, возможно в сочетании с подходящими добавками иной природы в очень небольших количествах, такие добавки не оказывают заметного вредного воздействия на кожу.
Особенно удобно получать вышеуказанные фармацевтические композиции в виде стандартной лекарственной формы для легкого введения и единообразия дозирования. Стандартная лекарственная форма, как используется здесь, относится к физически дискретным единицам, пригодным как единичные дозы, каждая единица содержит заранее определенное количество активного ингредиента, рассчитанное на получение желательного терапевтического эффекта, в сочетании с необходимым фармацевтическим носителем. Примерами таких стандартных лекарственных форм являются таблетки (включая таблетки с ядром или покрытые таблетки), капсулы, пилюли, упаковки порошка, облатки, растворы или суспензии для инъекций и тому подобное и разделенные наборы их.
Специалисты по лечению ВИЧ-инфекции в состоянии определить эффективное суточное количество исходя из представленных здесь результатов испытаний. Обычно предполагается, что эффективное суточное количество должно быть от 0,01 мг/кг до 50 мг/кг массы тела, более предпочтительно от 0,1 мг/кг до 10 мг/кг массы тела. Может быть целесообразным вводить необходимую дозу в виде двух, трех, четырех или более суб-доз через подходящие интервалы в течение суток. Указанные суб-дозы могут быть в виде стандартных лекарственных форм, например, содержащих от 1 до 1000 мг и, в особенности, от 5 до 200 мг активного ингредиента на единичную лекарственную форму.
Точная дозировка и частота введения зависят от используемого конкретного соединения формулы (I), серьезности состояния, которое лечат, возраста, массы и основного физического состояния конкретного пациента, а также другого медикаментозного лечения, которому может быть подвергнут индивидуум, что хорошо известно специалистам в этой области. Более того, очевидно, что указанное эффективное суточное количество может быть уменьшено или увеличено в зависимости от реакции подвергающегося лечению субъекта и/или в зависимости от оценки лечащего врача, предписывающего соединения по данному изобретению. Интервалы эффективного суточного количества, указанные выше, являются поэтому только ориентировочными, и их не следует понимать как ограничение объема или применения изобретения в какой-либо мере.
Сочетание антиретровирусного соединения и соединения формулы (I) также может быть использовано как лекарственное средство. Таким образом, настоящее изобретение также относится к продукту, содержащему (а) соединение формулы (I) и (б) другое антиретровирусное соединение, как к комбинированному препарату для одновременного, раздельного или последовательного применения в лечении против ВИЧ. Различные лекарства могут быть объединены в единый препарат вместе с фармацевтически приемлемыми носителями. Указанными другими антиретровирусными соединениями могут быть известные антиретровирусные соединения, такие как нуклеозидные ингибиторы обратной транскриптазы, например зидовудин (3'-азидо-3'-дезокситимидин, AZT), диданозин (дидезоксиинозин, ddI), залцитабин (дидезоксицитидин, ddC) или ламивудин (3'-тиа-2'-3'-дидезоксицитидин, 3ТС) и т.п.; ненуклеозидные ингибиторы обратной транскриптазы, такие как сурамин, пентамидин, тимопентин, кастаноспермин, декстран (декстран сульфат), фоскарнет-натрий (фосфоноформиат тринатрия), невирапин (11-циклопропил-5,11-дигидро-4-метил-6Н-дипиридо[3,2-b: 2', 3'-е][1,4]диазепин-6-он, такрин (тетрагидроаминоакридин) и т. п.; соединения типа TIBO (тетрагидро-имидазо[4,5,1-jk] [1,4] бензодиазепин-2(1Н)-он и тион), например (S)-8-хлор-4,5,6,7-тетрагидро-5-метил-6-(3-метил-2-бутенил)-имидазо-[4,5,1-jk][1,4]бензодиазепин-2(1Н)-тион); соединения типа α-APA (α-анилинофенилацетамид), например α-[(2-нитрофенил)амино] -2,6-дихлорбензолацетамид и т. п.; ТАТ-ингибиторы, например Р0-5-3335.и т.п.; ингибиторы протеазы, например индинавир, ритановир, саквиновир и т.п., или иммуномодулируеющие агенты, например левамизол и т.п.
Следующие примеры предназначены для того, чтобы иллюстрировать, но не ограничивать сферу действия настоящего изобретения.
Экспериментальная часть
Ниже "КТ" обозначает комнатную температуру, "ДХМ" обозначает дихлорметан, "ДМФ" обозначает N,N-диметилформамид и "АЦН" обозначает ацетонитрил.
А. Получение промежуточных соединений
Пример А.1
а) Смесь 4-циано-анилина (2,48 г) и дифенил-N-циано-карбонимидата (5,0 г) в ДМФ (25 мл) перемешивают 20 часов при 110oС в токе аргона. Добавляют воду и полученный осадок отфильтровывают с получением коричневатого твердого вещества. Эту фракцию перекристаллизовывают из АЦН. Осадок отфильтровывают и сушат, получая 1,67 г (30%) фенил-N'-циано-N-(4-цианофенил)карбамимидата (промежуточное соединение 1). Подобным путем получают фенил-N'-циано-N-(3-циано-фенил)карбамимидат (промежуточное соединение 2); фенил-N'-циано-N-(4-хлорфенил)карбамимидат (промежуточное соединение 3) и О-фенил-N'-циано-N, N-диметилкарбаимидат (промежуточное соединение 7).
б) Смесь промежуточного соединения (7) (0,01746 моль) и 2,6-дихлорбензолэтанимидамида (0,01746 моль) в ДМФ (30 мл) перемешивают в течение 24 часов при 85oС. После охлаждения реакционную смесь гасят H2O и осадок отфильтровывают и сушат, получая 5,00 г (96,0%) 6-[(2,6-дихлорфенил)метил]-N2-диметил-1,3,5-триазин-2,4-диамина (промежуточное соединение 31).
Пример А.2
а) Смесь NH4Cl (2,55 г) в толуоле (100 мл) перемешивают и охлаждают на ледяной бане в токе аргона. Добавляют Al(СН3)3/толуол (23,9 мл; 2,0 М) и полученную смесь перемешивают в течение 1,5 часов при КТ. Добавляют 5-Хлор-1[(4-метилфенил)-сульфонил] -1Н-индол-4-ацетонитрил, который может быть получен согласно Matsumoto et al., Heterocycles, 24(11), 31 57-3162 (1986), (3,0 г) и реакционную смесь перемешивают в течение 24 часов при 80oС. Затем реакционную смесь выливают в суспензию 96 г силикагеля в ДХМ (200 мл), перемешивают, фильтруют и осадок на фильтре промывают метанолом (400 мл) и упаривают с получением 5,35 г белого твердого продукта. Твердый продукт растворяют в ДХМ, промывают 3 н. NaOH, сушат карбонатом калия, фильтруют и фильтрат упаривают, получая 2,80 г (89%, белый твердый продукт) 5-хлор-1[(4-метилфенил)-сульфонил] -1Н-индол-4-этан-имидамида (промежуточное соединение 4).
б) Смесь промежуточного соединениея (4) (2,61 г) и промежуточного соединения (1) (1,89 г) в ДМФ (25 мл) перемешивают в течение 24 часов при 65oС в токе аргона. Медленно добавляют воду и осадок фильтруют с получением 3,55 г не совсем белого твердого продукта. Твердый продукт перемешивают при кипячении с обратным холодильником в АЦН, охлаждают и фильтруют с получением 2,54 г (66%) белого твердого продукта. Образец 0,30 г перекристаллизовывают в метаноле, осадок отфильтровывают и сушат, получая 0,28 г (62%, белое твердое вещество) 4-[[4-амино-6-[(4-цианофенил)амино]-1,3,5-триазин-2-ил]метил] -5-хлор-1-[(4-
метилфенил)сульфонил]-lH-индола (промежуточное соединение 5).
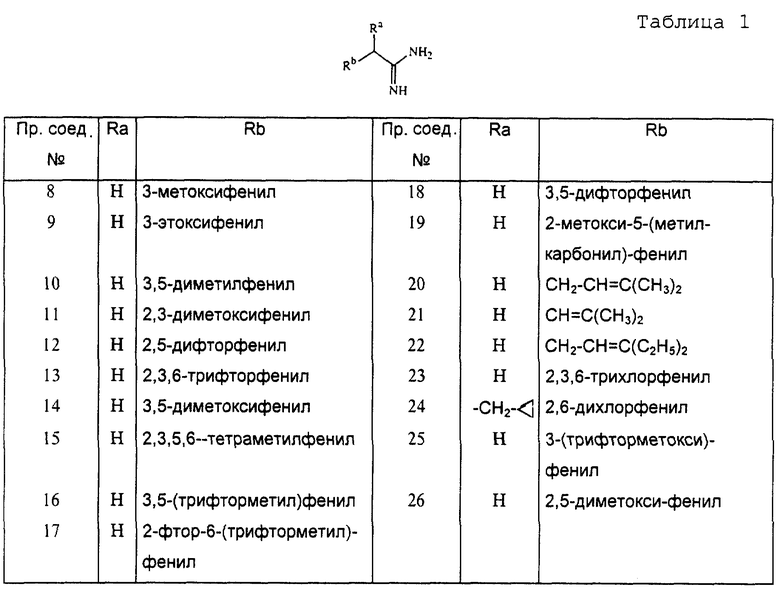
В таблице 1 перечислены промежуточные соединения, которые получают согласно способу, описанному в примере А.2а.
Пример А.3
К 4-цианофенил-тиомочевине (5,0 г) в ацетоне (100 мл) добавляют иодметан (1,76 мл). Реакционную смесь перемешивают в течение ночи при КТ. Осадок отфильтровывают, сушат и растворяют в ДХМ. Органический раствор промывают NН3 (водн. ) (избыток), сушат над карбонатом калия, фильтруют и растворитель упаривают, получая 4,53 г (84%, белое твердое продукт) метил-N'-(4-цианофенил) карбамимидотиоата (промежуточное соединение 6).
Пример А.4
а) Раствор 2-(бромметил)-1,3-дихлорбензола (около 10% от 0,383 моль) в диэтиловом эфире (240 мл) добавляют к магнию (0,383 моль) в диэтиловом эфире (240 мл) под аргоном. Когда начинается реакция, добавляют остальной 2-(бромметил)-1,3-дихлорбензол в диэтиловом эфире. Раствор перемешивают при КТ в течение 2,5 часов и затем добавляют посредством канюли к раствору 2,4,6-трихлор-1,3,5-триазина (0,319 моль) в бензоле (480 мл), поддерживая температуру ниже 15oС. Реакционную смесь перемешивают в течение одного часа на ледяной бане, затем в течение 2 часов при КТ. Добавляют раствор 4-амино-бензонитрила (0,351 моль) в N,N-диизопропилэтиламине (61,0 мл) и 1,4-диоксане (500 мл) и реакционную смесь перемешивают при КТ в течение 40 часов. Растворитель выпаривают. Добавляют воду и этилацетат. Раствор перемешивают, затем твердое вещество отфильтровывают, промывают этилацетатом и водой, получая 129,9 г 4-[[4-хлор-6-[(2,6-дихлорфенил)метил]-1,3,5-триазин-2-ил] амино] бензонитрила (промежуточное соединение 27; т.пл. 243-244oС).
Подобным путем получают 4-[[4-хлор-6-[(2,4-дихлорфенил)метил]-1,3,5-триазин-2-ил] амино]бензонитрил (промежуточное соединение 28) и 4-[[4-хлор-6-[(2-хлорфенил)метил] -1,3,5-триазин-2-ил] амино]бензонитрил (промежуточное соединение 29).
б) 2,4-дихлор-6-[(2,6-дихлорфенил)метил] -1,3,5-триазин (промежуточное соединение 30) получают согласно способу, описанному в примере А.4а, останавливают его перед добавлением 4-амино-бензонитрила.
В. Получение конечных соединений
Пример B.1
а) Промежуточное соединение (1) (1,66 г) добавляют к раствору 2,6-дихлорбензол-этанимидамида (1,29 г) в ДМФ (13 мл). Реакционную смесь перемешивают в течение трех дней при КТ, затем в течение двух дней при 60oС в токе аргона. Добавляют воду и осадок отфильтровывают. Эту фракцию кипятят с обратным холодильником в АЦН (500 мл), охлаждают и осадок отфильтровывают и сушат, получая 1,58 г (67%, белое твердое вещество) 4-[[4-амино-6-[(2,6-дихлорфенил) метил]-1,3,5-триазин-2-ил] амино]бензонитрила (соединение 1).
б) Соединение (1) (0,00135 моль) и ангидрид уксусной кислоты (20 мл) объединяют и нагревают с обратным холодильником в течение 10 минут. Затем реакционную смесь снимают с масляной бани и охлаждают до КТ. Осадок отфильтровывают, получая 0,25 г (45%) N-[4-[(4-цианофенил)амино]-6-[(2,6-дихлорфенил)метил]-1,3,5-триазин-2-ил]ацетамида (соединение 22).
Увеличение времени кипячения с обратным холодильником ведет к дизамещенному (соединение 40) и тризамещенному (соединение 41) аналогу соединения 22.
Пример В.2
Метанол (120 мл) добавляют к смеси промежуточного соединения (5) (2,35 г) и К2СО3 (9,19 г) в воде (40 мл). Полученную реакционную смесь перемешивают и кипятят с обратным холодильником 19 часов под аргоном. Добавляют воду (120 мл), осадок отфильтровывают и очищают хроматографией на колонке с силикагелем (элюент: ДХМ/2-пропанон 90/10).
Две желаемые фракции собирают и их растворитель выпаривают. Первую фракционную группу суспендируют в АЦН, охлаждают, отфильтровывают и сушат, получая 0,75 г (45%, твердое белое вещество) 4-[[4-амино-6-[(5-хлор-1Н-индол-4-ил)метил] -1,3,5-триазин-2-ил] амино] бензонитрила (соединение 8, т.пл. 267-268oС). Вторая колоночная фракционная группа дает 0,15 г 4-[[4-амино-6-[(5-хлор-1Н-индол-4-ил) метил] -1,3,5-триазин-2-ил] амино] бензамида (соединение 9). После 24 часов при КТ водный фильтрат фильтруют с получением 0,25 г соединения 9. Две фракции соединения 9 объединяют, растворяют в 500 мл нагреваемого с обратным холодильником метанола, фильтруют в горячем состоянии, фильтрат концентрируют до 50 мл, охлаждают и фильтруют, затем сушат, получая 0,25 г (14%) 4-[[4-амино-6-[(5-хлор-1Н-индол-4-ил)метил]-1,3,5-триазин-2-ил]амино]бензамида (соединение 9, т.пл. 204-205oС).
Пример В.3
Смесь соединения (1) (1,0 г) и гидрида натрия (0,11 г) в ДМФ (20 мл) перемешивают 20 минут при КТ в токе аргона. Затем по каплям добавляют 2-изоцианато-пропан (0,27 мл) в течение 30 мин и реакционную смесь перемешивают при КТ в течение ночи. Растворитель выпаривают и добавляют воду. Осадок фильтруют, промывают водой и диэтиловым эфиром и перекристаллизовывают из 1,4-диоксана. Осадок отфильтровывают и сушат, получая 0,95 г (85,1%) N-[4-[(4-циано-фенил)амино] -6-[(2,6-дихлорфенил)метил] -1,3,5-триазин-2-ил]-N'-(1-метилэтил)мочевины (соединение 6, т.пл. 267-268oС).
Пример В.4
Смесь N-[амино(метиламино)метил] -2,6-дихлорбензол-ацетамида (4,15 г) и промежуточного соединения 6 (3,05 г) в ДМФ (25 мл) перемешивают и кипятят с обратным холодильником в течение 20 часов. Растворитель выпаривают, остаток растворяют в ДМФ (25 мл) и нагревают при 80oС в течение 16 часов и при 100-108oС еще 66 часов. Реакционную смесь охлаждают, гасят водой, экстрагируют диэтиловым эфиром и промывают разбавленным NaOH, водой, солевым раствором и сушат над К2СО3. Растворитель выпаривают и остаток очищают флаш-хроматографией на колонке и перекристаллизовывают из 2-пропанола и в конце из метанола, получая 0,78 г (12,6%) 4-[[4-[(2,6-дихлорфенил)метил] -6-(метиламино)-1,3,5-триазин-2-ил] амино] бензонитрила (соединение 7, т.пл. 229-230oС).
Пример В.5
а) Промежуточное соединение (27) (0,00423 моль), 2-аминоацетамид (0,00431 моль), 1,4-диоксан (20 мл) и N,N-диизопропилэтиламин (0,00862 моль) объединяют и перемешивают при КТ в течение 16 часов под аргоном. Реакционную смесь гасят H2O и фильтруют. Остаток промывают Н2О, фильтруют и перекристаллизовывают из АЦН (200 мл). Осадок фильтруют и сушат, получая 0,75 г (41,4%) [N-[4-[(4-циано-фенил)амино] -6-[(2,6-дихлорфенил)метил] )-1,3,5-триазин-2-ил] аминоацетамида (соединение 14).
б) 4-[[4-[(2,6-дихлорфенил)метил]-6-гидразино-1,3,5-триазин-2-ил]амино] бензонитрил (соединение 15) получают подобным образом, как описано в примере В.5а, но N,N-диизопропилэтиламин не используют.
Пример В.6
а) Промежуточное соединение (27) (0,0128 моль), 1,4-диоксан (50 мл) и О-(триметилсилил)гидроксиламин (0,134 моль) объединяют под аргоном. Реакционную смесь перемешивают при КТ в течение 20 часов. Реакционную смесь концентрируют и добавляют ДХМ (50 мл), NaOH (1 н.; 50 мл) и НС1 (1 н.; 100 мл). Раствор перемешивают в течение одного часа. Осадок отфильтровывают и перекристаллизовывают из метанола. Осадок отфильтровывают и сушат, получая 2,96 г (59,8%) моногидрата моногидрохлорида 4-[[4-[(2,6-дихлорфенил)метил] -6-(гидроксиамино)-1,3,5-триазин-2-ил]амино]бензонитрила (соединение 21).
б) Соединение (21) (0,00227 моль) перемешивают в этилацетате (50 мл). Смесь промывают NаНСО3 (50 мл насыщенного раствора), затем промывают солевым раствором, сушат, фильтруют и растворитель упаривают. Остаток кристаллизуют из метанола, фильтруют и сушат, получая 0,60 г (70,6%) 4-[[4[(2,6-дихлорфенил)метил] -6-(гидроксиамино)-1,3,5-триазин-2-ил] амино] бензонитрила (соединение 33).
Пример В.7
Смесь промежуточного соединения (30) (0,068 моль) и 4-аминобензонитрила (0,0420 моль) в 1,4-диоксане (100 мл) перемешивают и кипятят с обратным холодильником в течение 16 часов под аргоном. Горячую реакционную смесь фильтруют и полученный фильтрат концентрируют. Остаток растворяют в ДХМ (30 мл). Осадок фильтруют и перекристаллизовывают из АЦН (250 мл). После охлаждения до КТ фильтрат концентрируют. Остаток распределяют между ДХМ/NaOH (3 н.). Полученный раствор сушат над К2СО3, фильтруют и растворитель упаривают. Остаток перекристаллизовывают из СНзОН. Осадок отфильтровывают и сушат, получая 1,00 г (5,0%) N,N'-[6-[(2,6-дихлорфенил)метил]-1,3,5-триазин-2,4-диил]бис[4-аминобензонитрил] (соединение 11).
Пример В.8
ДМФ (9,0 мл) и промежуточное соединение (31) (0,00295 моль) добавляют к гидриду натрия (0,00354 моль) под аргоном. Реакционную смесь перемешивают в течение 10 минут перед добавлением 4-фторбензонитрила (0,00301 моль) и нагревают при 80oС в течение 3,5 часов. После охлаждения до КТ реакционную смесь гасят Н2О. Осадок отфильтровывают, сушат и очищают флаш-хроматографией на колонках на силикагеле (элюент: ДХМ). Желательные фракции собирают и растворитель выпаривают, получая 4-[4-[(2,6-дихлорфенил)метил]-6-(диметиламино)-1,3,5-триазин-2-ил]амино]бензонитрил (соединение 10).
б) Промежуточное соединение (31) (0,00671 моль), диметилацетамид (20 мл), 4-фторбензонитрил (0,01007 моль) и К2СО3 (0,02685 моль) объединяют и кипятят с обратным холодильником 4 часа под аргоном. Реакционную смесь перемешивают и кипятят с обратным холодильником в течение ночи и гасят водой и экстрагируют ДХМ. Отделенный органический слой промывают солевым раствором, сушат, фильтруют и растворитель выпаривают. Остаток очищают флаш-хроматографией (элюент: ДХМ). Желаемые фракции собирают и растворитель упаривают. Остаток кристаллизуют из СН3ОН, перекристаллизовывают из АЦН и в конце обрабатывают СН3ОН. Осадок отфильтровывают и сушат, получая 0,32 г 4,4'-[[4-[(2,6-дихлорфенил)метил] -6-(диметиламино)-1,3,5-триазин-2-ил] амино]бисбензонитрил (соединение 38).
Пример В.9
Раствор гидрида натрия (0,00195 моль) в ДМФ (7 мл) добавляют к соединению (1) (0,00186 моль) и полученный раствор перемешивают в течение 5 минут под аргоном. Затем добавляют метиловый эфир хлоруксусной кислоты (0,0186 моль) и реакционную смесь нагревают до 70oС в течение 19 часов. Реакционную смесь затем гасят водой и полученное твердый продукт отфильтровывают. Остаток обрабатывают горячим АЦН, затем фильтруют, пока он еще горячий. Остаток из охлажденного фильтрата перекристаллизовывают из 1,4-диоксана. Осадок отфильтровывают, получая 0,16 г (19,4%) N-(4-цианофенил)-N-[4-амино-6-[(2,6-дихлорфенил)метил]-1,3,5-триазин-2-ил]глицина (соединение 39).
Пример В.10
Гидрид натрия (0,00150 моль), АЦН (5 мл), соединение 1 (0,00135 моль) в 1,4-диоксане (10 мл) и АЦН (10 мл) объединяют под аргоном. Раствор перемешивают 1 час. 1-Хлор-3-изоцианатопропан (0,00137 моль) добавляют. Реакционную смесь перемешивают 1 час. Добавляют 1-метил-пирролидинон (10 мл). Реакционную смесь перемешивают 16 часов. Затем смесь концентрируют. Концентрат распределяют между ДХМ/Н2О. Полученный раствор фильтруют, сушат над К2СО3, фильтруют, концентрируют и остаток обрабатывают NН3 в 1,4-диоксане (12 мл, 0,5 М) и нагревают под давлением при 55oС. Полученный раствор концентрируют и далее очищают флаш-хроматографией на колонках (элюент: ДХМ/СН3ОН 95/5). Чистые фракции собирают и растворитель выпаривают, получая 0,12 г (18,9%) N-[3-[[4-[(4-цианофенил)амино] -6-[(2,6-дихлорфенил)метил]-1,3,5-триазин-2-ил] амино]пропил]мочевины (соединение 23).
Пример В.11
NaOH (0,0128 моль), 1,4-диоксан (5 мл) и гуанидин (0,0128 моль) объединяют и перемешивают при КТ в течение 5 минут под аргоном. Затем добавляют промежуточное соединение 27 (0,00128 ммоль) и реакционную смесь перемешивают при КТ в течение 16 часов. Реакционную смесь гасят Н2О и перемешивают. Полученный осадок отфильтровывают и остаток перемешивают в кипящем с обратным холодильником метаноле, охлаждают и фильтруют, получая 0,34 г (64,3%) N-[4-[(4-цианофенил)амино] -6-[(2,6-дихлорфенил)метил] -1,3,5-триазин-2-ил]гуанидина (соединение 20).
Пример В.12
Смесь промежуточного соединения 27 (0,00256 моль) и 3-амино-1,2-пропандиола (0,00563 моль) в 1,4-диоксане (10 мл) и 1-метил-пирролидиноне (2 мл) перемешивают при КТ в течение 48 часов под аргоном. Реакционную смесь концентрируют, гасят ДХМ/Н20 и перемешивают. Осадок отфильтровывают, получая 1,12 г (86,9%)(±)-4-[(4-[(2,6-дихлорфенил)метил] -6-[(2,3-дигидроксипропил)амино]-1,3,5-триазин-2-ил]амино]бензонитрила (соединение 26).
Пример В.13
Соединение 1 (0,0016 моль) и 1,1-диметокси-N,N-диметилметанамин (21 мл) объединяют и тщательно перемешивают при окружающей температуре в течение 8 часов. Реакционную смесь фильтруют и собранный твердый продукт промывают простым эфиром (фракция А). Дополнительное соединение получают концентрированием фильтрата (фракция В). Фракции А и В объединяют и перекристаллизовывают из этанола, получая 0,15 г 4-[[4-[(2,6-дихлорфенил)метил] -6-[[(диметил-амино)метилен] -амино] -1,3,5-триазин-2-ил] амино] бензонитрила (соединение 62).
Пример В.14
Раствор соединения 13 (0,000519 моль), LiOH•H2O (0,000571 моль), метанола (5,0 мл) и H2O (5,0 мл) перемешивают при КТ в течение 16 часов под аргоном. Реакционную смесь концентрируют, повторно растворяют в H2O и подкисляют 1,0 н. НС1 (0,52 мл) и перемешивают в течение 3 дней. Затем раствор фильтруют и к фильтрату добавляют избыток 1 н. НС1 и СН3ОН и раствор перемешивают 16 часов. Полученный осадок отфильтровывают и сушат, получая 0,18 г (72,7%) %) N-[4-[(4-циано-фенил)амино]-6-[(2,6-дихлорфенил)метил]-1,3,5-триазин-2-ил]глицина (соединение 16).
Пример В.15
Смесь соединения 32 (0,00378 моль) в NН3 в диоксане (50 мл) нагревают в сосуде под давлением при 85oС в течение 9 дней. Растворитель упаривают и полученный остаток распределяют между ДХМ/H2O. Органический слой фильтруют, промывают этанолом и концентрируют до ±25 мл и фильтруют, получая 0,54 г (30,3%) (±)-2-[[4-[(4-цианофенил)-амино] -6-[(2,6-дихлорфенил)амино] -6-[(2,6-дихлорфенил)-метил] -1,3,5-триазин-2-ил] амино-4-гидроксибутанамида (соединение 34).
Пример В.16
Раствор промежуточного соединения 27 в диметилсульфоксиде обрабатывают NaN3 в одной порции и перемешивают при КТ в течение 28 часов. Реакционную смесь выливают на лед и затем фильтруют. Осадок промывают холодной водой и перекристаллизовывают из АЦН, получая 0,46 г 4-[[4-азидо-6-[(2,6-дихлорфенил)метил]-1,3,5-триазин-2-ил] амино]бензонитрила (соединение 68).
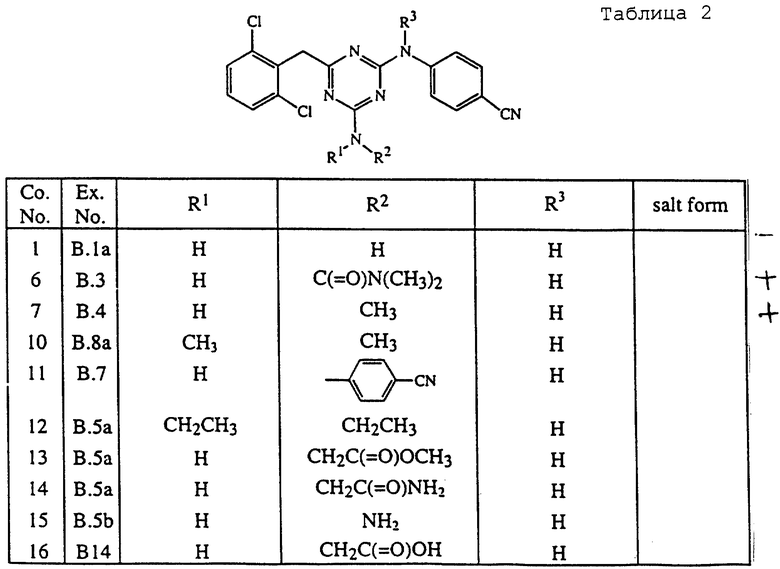
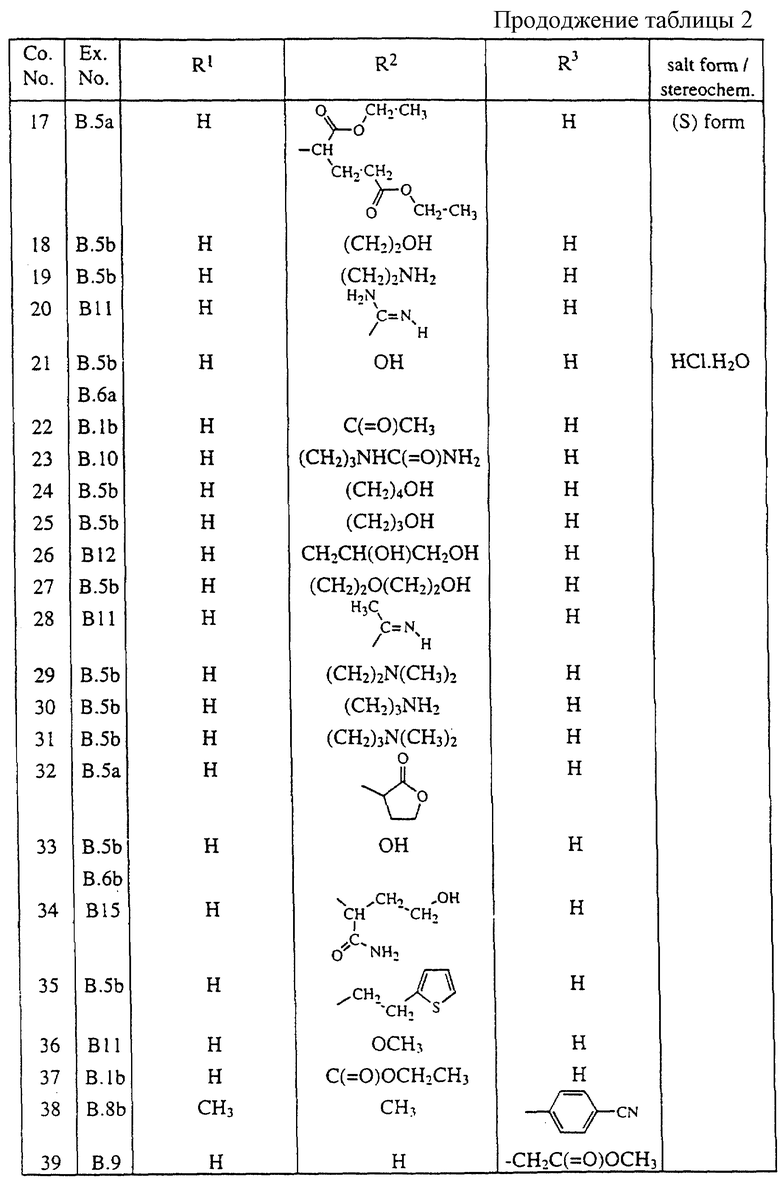
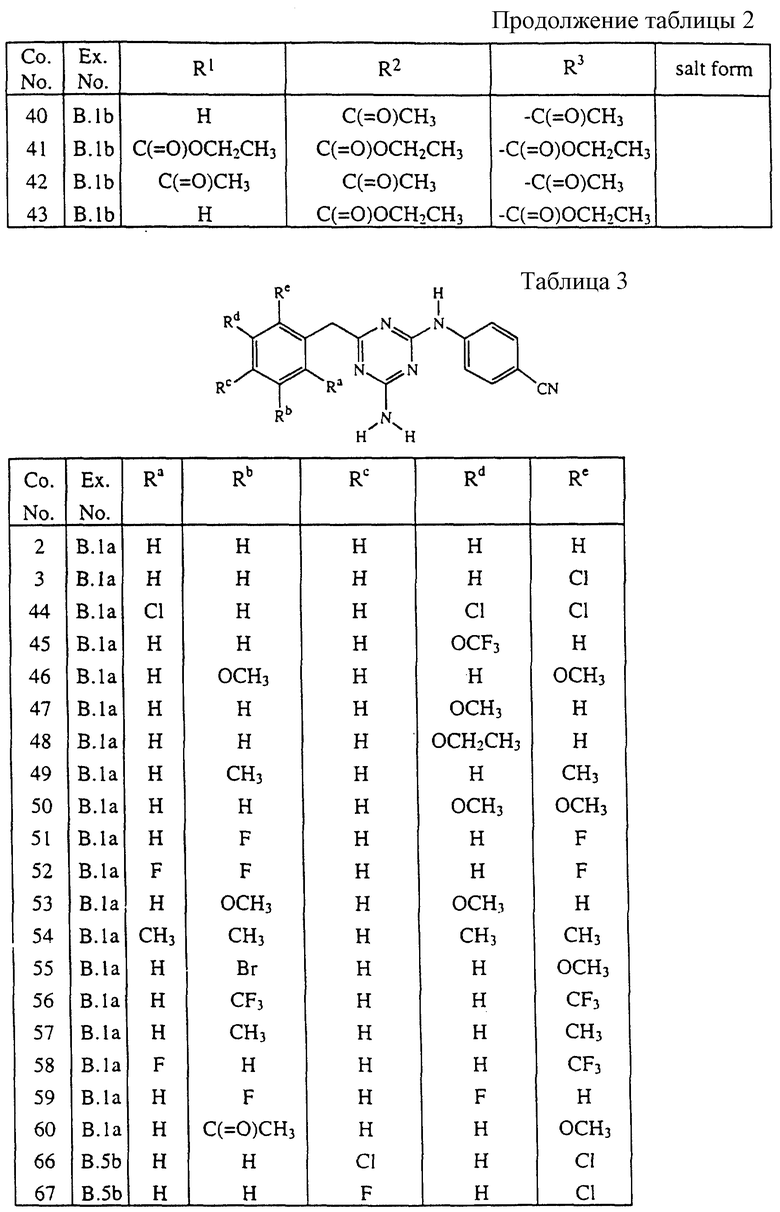
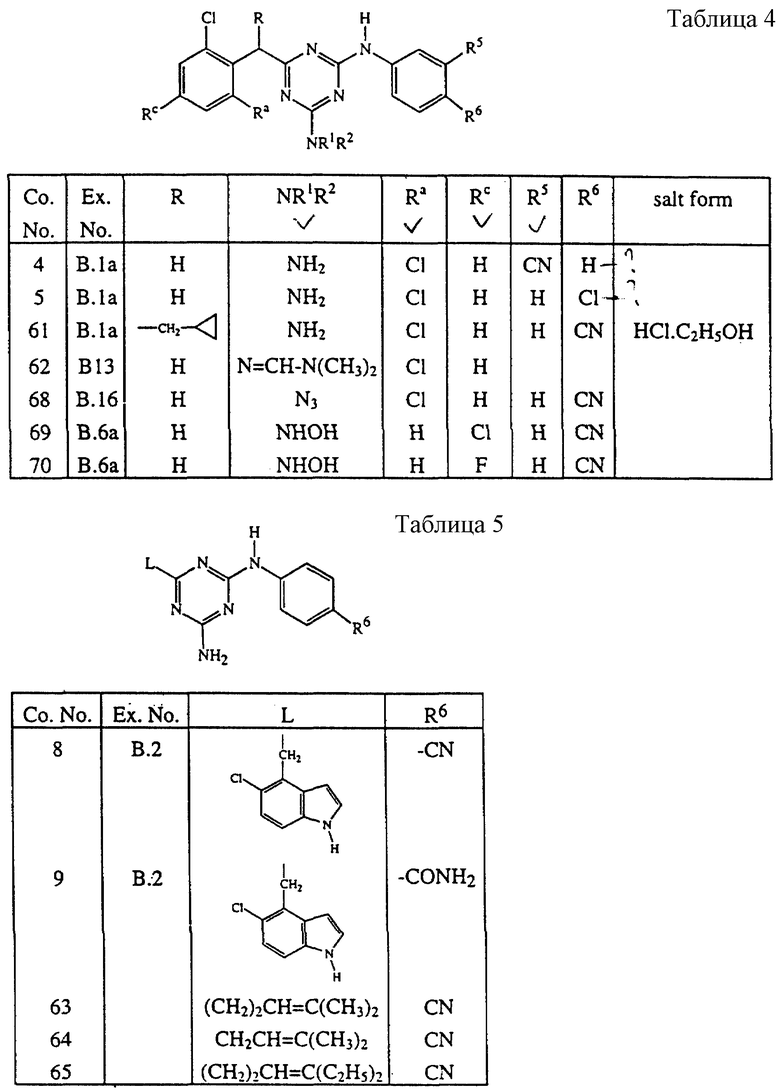
В таблицах 1 - 5 перечисляются соединения, которые получены согласно одному из вышеуказанных примеров.
В таблицах Со. No. - соединения, Ex. No. - примера, salt form/stereochem. - солевая форма/стереохим. (Прим. пер.)
С. Фармакологический пример
Пример С.1
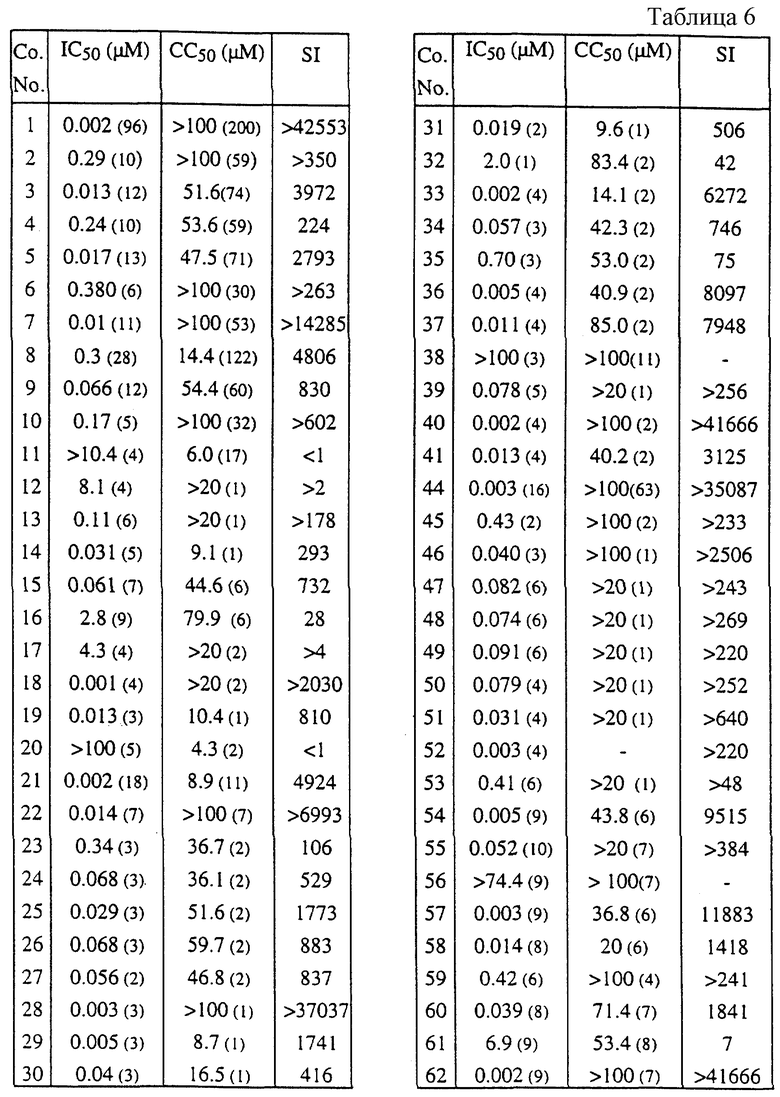
Для оценки in vitro агентов против ВИЧ применяют быструю чувствительную и автоматизированную аналитическую методику. Линия трансформированных ВИЧ-1 клеток Т-4, МТ-4, которые, как ранее обнаружено (Koyanagi et al., Int. J. Cancer, 36, 445-451, 1985), являются сильно восприимчивыми и подверженными ВИЧ инфекции, служит в качестве линии клеток-мишеней. Ингибирование ВИЧ-индуцированного цитопатического эффекта используют как конечную точку. Жизнеспособность как ВИЧ- (HIV), так и mock-инфицированных клеток анализируют спектрофотометрически посредством in situ восстановления бромида 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия (МТТ). 50%-ную цитотоксичную концентрацию (СС50 в мкМ) характеризуют как концентрацию соединения, которая снижает оптическую плотность mock-инфицированного контрольного образца на 50%. Защиту в процентах, которая достигается за счет соединения в ВИЧ-инфицированных клетках, рассчитывают по следующей формуле: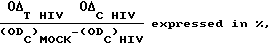
где (ODT)HIV - оптическая плотность, измеренная с заданной концентрацией испытуемого соединения в ВИЧ-инфицированных клетках; (ODC)HIV - оптическая плотность, измеренная для контрольных необработанных ВИЧ-инфицированных клеток; (ODC)MOCK - оптическая плотность, измеренная для контрольных необработанных mock-инфицированных клеток; все величины оптической плотности определяют при 540 нм. Дозу, обеспечивающую 50%-ную защиту согласно вышеуказанной формуле определяют как 50% ингибирующую концентрацию (IС50 в мкМ). Отношение СС50 к IС50 определяют как индекс селективности (SI). Показано, что соединения формулы (I) эффективно ингибируют ВИЧ-1. Специфические величины CC50, IC50 и SI приведены в Таблице 6; цифры в скобках в столбцах "IС50(мкМ)" и "СС50(мкМ)" указывают число экспериментов, использованных для расчета средних величин IC50 и СС50.
D. Примеры композиций
Следующие рецептуры дают примеры типичных фармацевтических композиций, пригодных для системного или местного введения животным или людям в соответствии с настоящим изобретением.
"Активный ингредиент" (A. I.), как используется в этих примерах, относится к соединению формулы (I) или его фармацевтически приемлемой аддитивной соли.
Пример D.1: таблетки, покрытые пленкой
Приготовление сердцевины таблетки
Смесь 100 г A.I., 570 г лактозы и 200 г крахмала хорошо смешивают и затем увлажняют раствором 5 г додецилсульфата натрия и 10 г поливинилпирролидона примерно в 200 мл воды. Влажную порошкообразную смесь просеивают, сушат и снова просеивают. Затем добавляют 100 г микрокристаллической целлюлозы и 15 г гидрированного растительного масла. Все это хорошо смешивают и прессуют в таблетки, получая 10000 таблеток, каждая из которых содержит 10 мг активного ингредиента.
Покрытие
К раствору 10 г метилцеллюлозы в 75 мл денатурированного этанола добавляют раствор 5 г этилцеллюлозы в 150 мл дихлорметана. Затем добавляют 75 мл дихлорметана и 2,5 мл 1,2,3-пропантриола. Расплавляют 10 г полиэтиленгликоля и растворяют в 75 мл дихлорметана. Последний раствор добавляют к предыдущему и затем добавляют 2,5 г октадеканоата магния, 5 г поливинилпирролидона и 30 мл концентрированной цветной суспензии и все вместе гомогенизируют. Сердцевины таблеток покрывают полученной таким образом смесью в глазировочном аппарате.
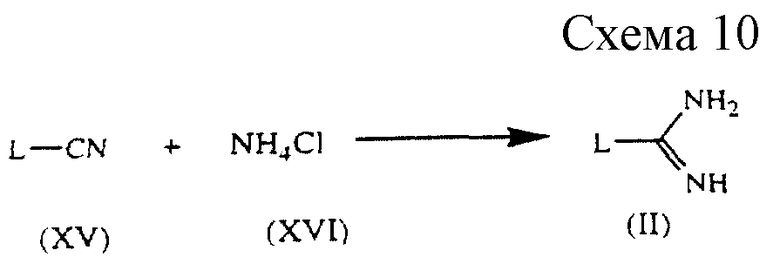
Описываются замещенные производные диамино-1,3,5-триазина общей формулы I или их фармацевтически приемлемые соли прибавления кислот или их стереохимически изомерные формы, где R1 и R2, каждый, независимо, обозначают водород; гидрокси; амино; С1-6алкилокси; С1-6алкилкарбонил; С1-6алкилоксикарбонил; фенил, замещенный цианогруппой; моно- или ди(С1-6алкил)аминокарбонил; дигидро-2 (3Н)фуранон; С1-6алкил, незамещенный или замещенный одним или двумя заместителями, каждый из которых независимо выбран из амино, имино, аминокарбонила, аминокарбониламино, гидрокси, гидрокси С1-6алкилокси, карбоксила, моно- или ди(С1-6алкил)амино, С1-6алкилоксикарбонила и тиенила; или R1 и R2, взятые вместе, могут образовывать азидо или моно- или ди (С1-6алкил) амино С1-4алкилиден; R3 обозначает водород; фенил, замещенный цианогруппой; С1-6алкилкарбонил; С1-6алкилоксикарбонил; С1-6алкил, незамещенный или замещенный С1-6алкилоксикарбонилом; R4 и R8, каждый, обозначают водород; R5 и R7 обозначают водород или циано; R6 означает циано или аминокарбонил; L обозначает С3-10алкенил или С1-10алкил, замещенный одним или двумя заместителям, независимо выбранными из С3-7циклоалкила, индолила, замещенного галогеном, фенила, незамещенного или замещенного 1-5 заместителями, каждый из которых независимо выбран из галогена, гидрокси, С1-6алкила, С1-6алкилокси, тригалогенметила, тригалогенметилокси, С1-6алкилкарбонила. Промежуточные соединения формулы VII, используемые в их синтезе фармацевтическая композиция, ингибирующая репликацию вируса иммунодефицита человека, способ ее получения и способы получения соединений I. 11 с. и 6 з.п.ф-лы, 7 табл.
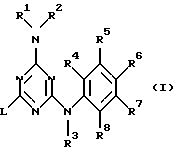
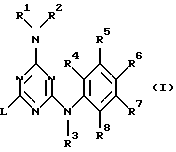
или их фармацевтически приемлемые соли прибавления кислот или их стереохимически изомерные формы,
где R1 и R2, каждый, независимо, обозначают водород; гидрокси; амино; C1-6алкилокси; C1-6алкилкарбонил; C1-6алкилоксикарбонил; фенил, замещенный цианогруппой; моно- или ди(C1-6алкил) аминокарбонил; дигидро-2(3Н)фуранон; C1-6алкил, незамещенный или замещенный одним или двумя заместителями, каждый из которых независимо выбран из амино, имино, аминокарбонила, аминокарбониламино, гидрокси, гидроксиС1-6 алкилокси, карбоксила, моно- или ди(C1-6алкил)амино, C1-6 алкилоксикарбонила и тиенила; или R1 и R2, взятые вместе, могут образовывать азидо или моно- или ди(C1-6алкил)аминоС1-4алкилиден;
R3 обозначает водород; фенил, замещенный цианогруппой; C1-6алкилкарбонил; C1-6алкилоксикарбонил; C1-6алкил, незамещенный или замещенный C1-6алкилоксикарбонилом;
R4 и R8, каждый, обозначают водород;
R5 и R7 обозначают водород или циано;
R6 означает циано или аминокарбонил;
L обозначает С3-10алкенил или C1-10алкил, замещенный одним или двумя заместителями, независимо выбранными из С3-7циклоалкила, индолила, замещенного галогеном, фенила, незамещенного или замещенного 1-5 заместителями, каждый из которых независимо выбран из галогена, гидрокси, C1-6алкила, C1-6алкилокси, тригалогенметила, тригалогенметилокси, C1-6алкилкарбонила.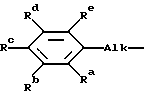
где Alk представляет собой C1-6алкандиил;
Ra, Rb, Rc, Rd, Re, каждый, независимо, выбран из водорода, галогена, C1-6алкила, C1-6алкокси, тригалогенметила или тригалогенметокси.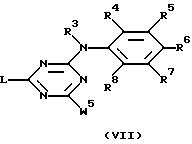
где W5 обозначает галоген;
L, R3, R4, R5, R6, R7 и R8 указаны в п.1.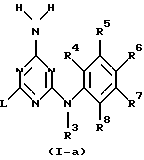
где L, R3, R4, R5, R6, R7 и R8 указаны в п.1,
заключающийся в том, что промежуточное соединение формулы (II)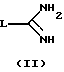
подвергают взаимодействию с промежуточным соединением формулы (III)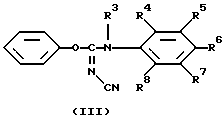
где R3, R4, R5, R6, R7 и R8 указаны выше,
в реакционно инертном растворителе, или, если желательно, преобразуют соединения формулы (I-а) друг в друга, следуя известным реакциям преобразования; и далее, если желательно, преобразуют соединения формулы (I-а) в соль прибавления кислоты путем обработки кислотой, или наоборот, преобразуют соль прибавления кислоты в свободное основание путем обработки щелочью; и, если желательно, получают их стереохимически изомерные формы.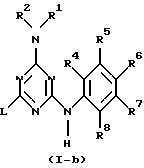
где L, R1, R2, R4, R5, R6, R7 и R8 указаны в п.1, заключающийся в том, что промежуточное соединение формулы (IV)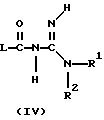
где L, R1 и R2 указаны выше,
подвергают взаимодействию с промежуточным соединением формулы (V)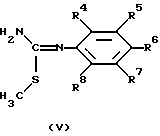
где R4, R5, R6, R7 и R8 указаны выше,
в реакционно инертном растворителе, или, если желательно, преобразуют соединения формулы (I-b) друг в друга, следуя известным реакциям преобразования; и далее, если желательно, преобразуют соединения формулы (I-b) в соль прибавления кислоты путем обработки кислотой, или наоборот, преобразуют соль прибавления кислоты в свободное основание путем обработки щелочью; и, если желательно, получают их стереохимически изомерные формы.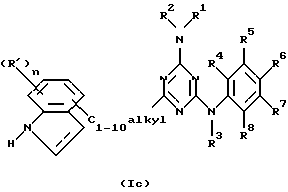
где n = 1;
R' обозначает галоген;
R1, R2, R3, R4, R5, R6, R7 и R8 указаны в п.1,
заключающийся в том, что удаляют защитную группу в промежуточном соединении общей формулы (VI)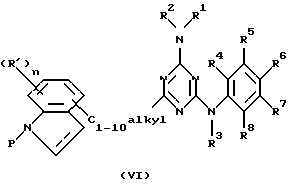
где Р обозначает подходящую удаляемую группу;
n, R1, R2, R3, R4, R5, R6, R7 и R8 указаны выше,
или, если желательно, преобразуют соединения формулы (1-с) друг в друга, следуя известным реакциям преобразования; и далее, если желательно, преобразуют соединения формулы (I-с) в соль прибавления кислоты путем обработки кислотой, или наоборот преобразуют соль прибавления кислоты в свободное основание путем обработки щелочью; и, если желательно, получают их стереохимически изомерные формы.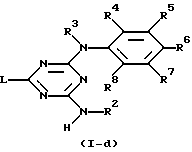
где L, R2, R3, R4, R5, R6, R7 и R8 указаны в п.1,
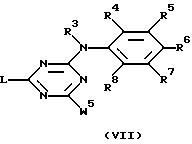
заключающийся в том, что промежуточное соединение формулы (VII)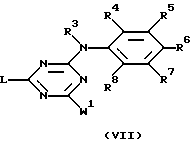
где W1 обозначает галоген;
R3, R4, R5, R6, R7 и R8 указаны выше,
подвергают взаимодействию с промежуточным соединением формулы (VIII)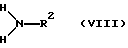
где R2 указан выше,
в реакционно инертном растворителе в присутствии подходящего основания и, в случае, когда R2 содержит защищенную гидроксигруппу, защитную группу удаляют, или, если желательно, преобразуют соединения формулы (I-d) друг в друга, следуя известным реакциям преобразования; и далее, если желательно, преобразуют соединения формулы (I-d) в соль прибавления кислоты путем обработки кислотой, или наоборот преобразуют соль прибавления кислоты в свободное основание путем обработки щелочью; и, если желательно, получают их стереохимически изомерные формы.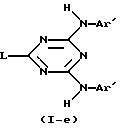
где Аr1 представляет собой фенил, замещенный циано;
L указан в п.1,
заключающийся в том, что промежуточное соединение формулы (IX)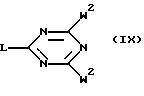
где W2 обозначает подходящую уходящую группу;
L указан выше,
подвергают взаимодействию с промежуточным соединением формулы (X)
H2N-Ar1 (X)
где Ar1 указан выше,
в реакционно инертном растворителе, или, если желательно, преобразуют соединения формулы (I-е) друг в друга, следуя известным реакциям преобразования; и далее, если желательно, преобразуют соединения формулы (I-е) в соль прибавления кислоты путем обработки кислотой, или наоборот преобразуют соль прибавления кислоты в свободное основание путем обработки щелочью; и, если желательно, получают их стереохимически изомерные формы.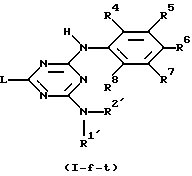
где R1′ и R2′ являются такими же, как R1 и R2, указанные в п.1, но иными, чем водород;
L, R4, R5, R6, R7 и R8 указаны в п.1,
заключающийся в том, что промежуточное соединение формулы (XI)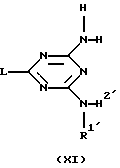
где L, R1′ и R2′ указаны выше,
подвергают взаимодействию с промежуточным соединением формулы (XII)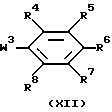
где W3 обозначает подходящую уходящую группу;
R4, R5, R6, R7 и R8 указаны выше,
в реакционно инертном растворителе и в присутствии подходящего основания, или, если желательно, преобразуют соединения формулы (I-f-1) друг в друга, следуя известным реакциям преобразования; и далее, если желательно, преобразуют соединения формулы (I-f-1) в соль прибавления кислоты путем обработки кислотой, или наоборот преобразуют соль прибавления кислоты в свободное основание путем обработки щелочью; и, если желательно, получают их стереохимически изомерные формы.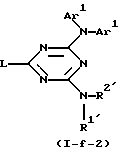
где L и Аr1 указаны в п.15;
R1′ и R2′ являются такими же, как R1 и R2, указанные в п.1, но иными, чем водород,
заключающийся в том, что промежуточное соединение формулы (XI-b)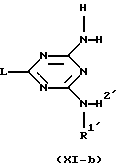
где L, R1′ и R2′ указаны выше,
подвергают взаимодействию с промежуточным соединением формулы (XII-b)
W3-Ar1, (XII-b)
где W3 обозначает подходящую уходящую группу;
Аr1 указан выше,
в реакционно инертном растворителе и в присутствии подходящего основания, или, если желательно, преобразуют соединения формулы (I-f-2) друг в друга, следуя известным реакциям преобразования; и далее, если желательно, преобразуют соединения формулы (I-f-2) в соль прибавления кислоты путем обработки кислотой, или наоборот преобразуют соль прибавления кислоты в свободное основание путем обработки щелочью; и, если желательно, получают их стереохимически изомерные формы.
| WO 9510506 A1, 20.04.1995 | |||
| RU 2058983 C1, 27.04.1996 | |||
| WO 9310116 A1, 27.05.1993 | |||
| Способ рафинирования олова от сурьмы и мышьяка | 1976 |
|
SU588762A1 |
Авторы
Даты
2002-08-10—Публикация
1997-09-30—Подача