Изобретение относится к области медицины, а именно к лепрологии, и может быть, в частности, использовано для лечения экспериментальной лепрозной инфекции.
Из практики медицины известен способ лечения экспериментальной лепрозной инфекции, состоящий в применении рифампицина: Rees R.J.W., Pearson J.M.H., Waters M. F.R. Experimental and clinical studies on rifampicin in treatment oflep-rosy//Brit. Med.J.-1970.-Vol.3.-P.89-92. Однако известный способ имеет следующие недостатки:
- длительность лечения,
- токсичность препарата.
Известен также способ лечения экспериментальной лепрозной инфекции рекомбинантным мышиным γ-интерфероном в сочетании с химиотерапевтическими средствами: Maw W.W., Tomioka H., Sato К., Saito H. Studies on therapeutic activity ofben-zoxazinorifamycin KRM-1648 in combination with other antimicrobial agents and biological response modifiers interferon-γ and granu-locyte-macrophage colony-stimulating factor against M. leprae infection in athymic nude mice.- Int J.Lepr.-1997.-Vol. 65, 3.-Р. 345-351.
К недостаткам известного способа можно отнести использование дорогостоящих препаратов.
Наиболее близким к предлагаемому является способ лечения экспериментальной лепрозной инфекции, заключающийся в том, что на организм мышей воздействуют диафенилсульфоном в дозе 100 мг/кг комбикорма со дня заражения и до окончания эксперимента: Shepard C.C. Effect of DDS on established infections with Mycobacterium leprae//Int. J. Lepr.- 1967.- Vol.35.- P.52-57. Однако известный способ имеет следующие недостатки:
- длительность применения препарата,
- токсичность препарата.
Этот способ принят авторами в качестве прототипа.
Сходство данного способа с предлагаемым заключается в том, что оба они относятся к лепрологии и что в организм мышей вводят диафенилсульфон.
Предлагаемое изобретение решает основную задачу: повышение эффективности лечения экспериментальной лепрозной инфекции. Сущность изобретения выражена совокупностью существенных признаков, достаточных для обеспечиваемого изобретением положительного результата.
Решение поставленной задачи заключается в том, что предлагается совокупность признаков, отличающихся от прототипа тем, что диафенилсульфон вводят в дозе 12,5 мг/кг массой тела мыши в комбинации с гептилгликозид мурамилдипептида в дозе от 150 до 450 мкг/кг массой тела мыши в течение 8 недель.
Лепра - хроническое инфекционное заболевание, характеризующееся дефектом клеточного иммунитета. Поэтому поиск средств патогенетической терапии, способных корригировать иммунологические дефекты, представляется актуальным. Изучение адъювантного действия бактерий показало, что их активность связана с гликопептидами, входящими в состав бактериальных оболочек, в частности мурамилдипептидом (МДП). К настоящему времени синтезированы производные МДП, сочетающие низкую токсичность с высокой иммуномодулирующей активностью, к числу которых относится гептилгликозид мурамилдипептида. До сих пор для лечения экспериментальной лепрозной инфекции данный препарат не применялся. Отличительной особенностью предлагаемого способа является то, что авторы впервые для лечения лепры применили гептилгликозид мурамилдипептида в соответствующей дозировке.
Предлагаемым способом достигается повышение эффективности лечения экспериментальной лепрозной инфекции при сочетанном применении гептилгликозида мурамилдипептида в дозе от 150 до 450 мкг/кг массы тела и диафенилсульфона в дозе 12,5 мг/кг массы тела. Экспериментально установлено отсутствие токсического действия препаратов на организм мышей. Применяемое в заявляемом способе терапевтическое воздействие гептилгликозида мурамилдипептида в комбинации с диафенилсульфоном является существенным отличием в подходе к лечению экспериментальной лепрозной инфекции. Это отличие позволило получить положительный результат в виде:
- значительного подавления локального размножения микобактерий лепры у мышей при экспериментальной лепрозной инфекции (в 1,9-2,4 раза по сравнению с прототипом) и, следовательно, сокращения сроков лечения;
- отсутствия проявлений токсического действия комбинации препаратов.
Предлагаемый способ был успешно апробирован в НИИ по изучению лепры МЗ РФ в течение 1996-1998 г. г. на 80 мышах линии СВА. Серия экспериментов, описанных в примерах 1-5, проводилась одновременно. Поэтому контрольная группа и группа мышей, получавших диафенилсульфон, являлись общими (таблицы 1-5). Ниже приводятся результаты апробации.
Пример 1.
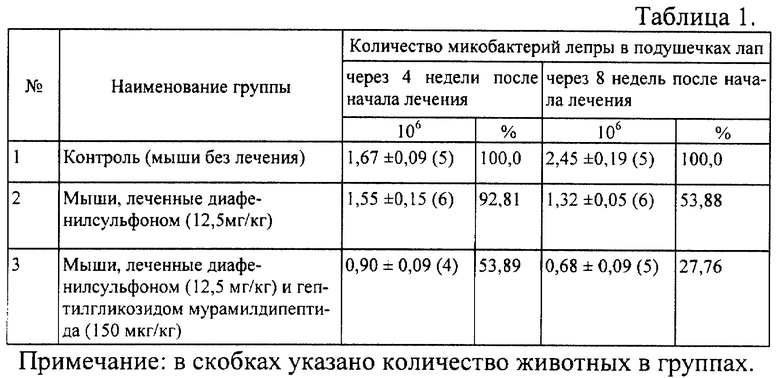
Мышей линии СВА массой тела 18-22 г, содержащихся в стандартных условиях вивария НИИЛ на стандартном пищевом режиме, заражали интраплантарно пассированными на мышах M. leprae (1 пассаж), полученными от нелеченого больного лепроматозным типом лепры, в количестве 104 микробных тел в 0,03 мл суспензии. Введение препаратов начинали через 10 неробных тел в 0,03 мл суспензии. Введение препаратов начинали через 10 недель после заражения, в логарифмическую фазу размножения возбудителя в месте инокуляции. Водный раствор гептилгликозида мурамилдипептида в дозе 150 мкг/кг массы тела вводили внутримышечно ежедневно в течение первой и пятой недель терапии. Диафенилсульфон в виде водной суспензии вводили интрагастрально в дозе 12,5 мг/кг массы тела ежедневно. Общая продолжительность лечения составила 8 недель. Забой животных производили по истечении 4 и 8 недель с начала лечения декапитацией с соблюдением правил эвтаназии, затем осуществляли подсчет количества микобактерий в мягких тканях лап мышей по методу Shepard, McRae (1968). Результаты микроскопических исследований приводятся в таблице 1.
Из таблицы 1 видно, что у мышей, получавших диафенилсульфон в дозе 12,5 мг/кг массы тела в течение 8 недель, количество микобактерий лепры в подушечках лап составило 1,32±0,05 млн/мл (или 53,88% от контроля). При лечении мышей диафенилсульфоном в сочетании с гептилгликозидом мурамилдипептида в дозе 150 мкг/кг массы тела в течение 8 недель количество микобактерий лепры в подушечках лап составило 0,68±0,09 млн/мл (или 27,76% от контроля). Таким образом, диафенилсульфон подавлял локальное размножение микобактерий лепры у мышей на 46,12%, а диафенилсульфон вместе гептилгликозидом мурамилдипептида - на 72,24%. Степень подавления локального размножения микобактерий лепры при лечении в течение 8 недель была выше, чем при лечении в течение 4 недель. Наиболее выраженный эффект наблюдался при использовании диафенилсульфона в сочетании с гептилгликозидом мурамилдипептида.
Пример 2.
Мышам, зараженным, как описано в примере 1, вводили водный раствор гептилгликозида мурамилдипептида в дозе 450 мкг/кг массы тела по той же схеме в комбинации с диафенилсульфоном в дозе 12,5 мг/кг массы тела. Результаты микроскопических исследований приведены в табл. 2.
Из таблицы 2 видно, что у мышей, получавших диафенилсульфон в дозе 12,5 мг/кг массы тела в течение 8 недель, количество микобактерий лепры в подушечках лап составило 1,32±0,05 млн/мл (или 53,88% от контроля). При лечении мышей диафенилсульфоном в сочетании с гептилгликозидом мурамилдипептида в дозе 450 мкг/кг массы тела в течение 8 недель количество микобактерий лепры в подушечках лап составило 0,54±0,08 млн/мл (или 22,04% от контроля). Таким образом, диафенилсульфон подавлял локальное размножение микобактерий лепры у мышей на 46,12%, а диафенилсульфон вместе гептилгликозидом мурамилдипептида - на 77,96%. Степень подавления локального размножения микобактерий лепры при лечении в течение 8 недель была выше, чем при лечении в течение 4 недель. Наиболее выраженный эффект наблюдался при использовании диафенилсульфона в сочетании с гептилгликозидом мурамилдипептида.
Пример 3.
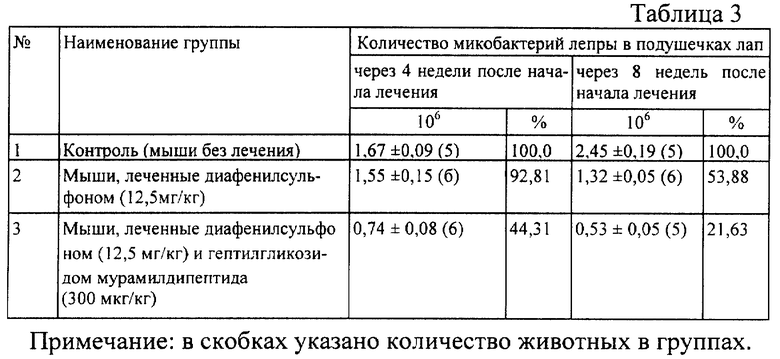
Мышам, зараженным, как описано в примере 1, вводили водный раствор гептилгликозида мурамилдипептида в дозе 300 мкг/кг массы тела по той же схеме в комбинации с диафенилсульфоном в дозе 12,5 мг/кг массы тела. Результаты микроскопических исследований приведены в табл. 3.
Из таблицы 3 видно, что у мышей, получавших диафенилсульфон в дозе 12,5 мг/кг массы тела в течение 8 недель, количество микобактерий лепры в подушечках лап составило 1,32±0,05 млн/мл (или 53,88% от контроля). При лечении мышей диафенилсульфоном в сочетании с гептилгликозидом мурамилдипептида в дозе 300 мкг/кг массы тела в течение 8 недель количество микобактерий лепры в подушечках лап составило 0,53±0,05млн/мл (или 21,63% от контроля). Таким образом, диафенилсульфон подавлял локальное размножение микобактерий лепры у мышей на 46,12%, а диафенилсульфон вместе гептилгликозидом мурамилдипептида - на 78,37%. Степень подавления локального размножения микобактерий лепры при лечении в течение 8 недель была выше, чем при лечении в течение 4 недель. Наиболее выраженный эффект наблюдался при использовании диафенилсульфона в сочетании с гептилгликозидом мурамилдипептида.
Пример 4.
Мышам, зараженным, как описано в примере 1, вводили водный раствор гептилгликозида мурамилдипептида в дозе 100 мкг/кг массы тела по той же схеме в комбинации с диафенилсульфоном в дозе 12,5 мг/кг массы тела. Результаты микроскопических исследований приведены в табл. 4.
Из таблицы 4 видно, что у мышей, получавших диафенилсульфон в дозе 12,5 мг/кг массы тела в течение 8 недель, количество микобактерий лепры в подушечках лап составило 1,32±0,05 млн/мл (или 53,88% от контроля). При лечении мышей диафенилсульфоном в сочетании с гептилгликозидом мурамилдипептида в дозе 100 мкг/кг массы тела в течение 8 недель количество микобактерий лепры в подушечках лап составило 1,03±0,11 млн/мл (или 42,04% от контроля). Таким образом, диафенилсульфон подавлял локальное размножение микобактерий лепры у мышей на 46,12%, а диафенилсульфон вместе гептилгликозидом мурамилдипептида - на 57,96%. При использовании заниженной дозы гептилгликозида мурамилдипептида в сочетании с диафенилсульфоном авторами не получено подавление локального размножения микобактерий лепры, которое наблюдалось при введении указанного препарата в дозе 150 мкг/кг. Степень подавления локального размножения микобактерий лепры при лечении в течение 8 недель была выше, чем при лечении в течение 4 недель. Наиболее выраженный эффект наблюдался при использовании диафенилсульфона в сочетании с гептилгликозидом мурамилдипептида.
Пример 5.
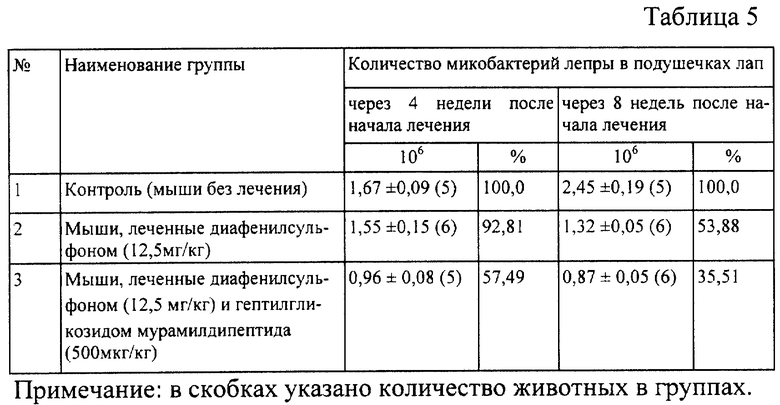
Мышам, зараженным, как описано в примере 1, вводили водный раствор гептилгликозида мурамилдипептида в дозе 500 мкг/кг массы тела по той же схеме в комбинации с диафенилсульфоном в дозе 12,5 мг/кг массы тела. Результаты микроскопических исследований приведены в табл. 5.
Из таблицы 5 видно, что у мышей, получавших диафенилсульфон в дозе 12,5 мг/кг массы тела в течение 8 недель, количество микобактерий лепры в подушечках лап составило 1,32±0,05 млн/мл (или 53,88% от контроля). При лечении мышей диафенилсульфоном в сочетании с гептилгликозидом мурамилдипептида в дозе 500 мкг/кг массы тела в течение 8 недель количество микобактерий лепры в подушечках лап составило 0,87±0,05 млн/мл (или 35,51% от контроля). Таким образом, диафенилсульфон подавлял локальное размножение микобактерий лепры у мышей на 46,12%, а диафенилсульфон вместе гептилгликозидом мурамилдипептида - на 64,49%. При использовании завышенной дозы гептилгликозида мурамилдипептида в сочетании с диафенилсульфоном авторами не получено подавление локального размножения микобактерий лепры, которое наблюдалось при введении указанного препарата в дозе 450 мкг/кг. Степень подавления локального размножения микобактерий лепры при лечении в течение 8 недель была выше, чем при лечении в течение 4 недель. Наиболее выраженный эффект наблюдался при использовании диафенилсульфона в сочетании с гептилгликозидом мурамилдипептида.
Анализируя данные, представленные в примерах 4 и 5, можно прийти к заключению, что наибольшее подавление локального размножения микобактерий лепры достигается у мышей, получавших гептилгликозид мурамилдипептида в дозе от 150 до 450 мкг/кг массы тела в комбинации с диафенилсульфоном в дозе 12,5 мг/кг массы тела. Использование гептилгликозида мурамилдипептида в дозах 100 и 500 мкг/кг в сочетании с диафенилсульфоном в дозе 12,5 мг/кг массы тела приводит к худшему терапевтическому эффекту по сравнению с приведенным выше диапазоном доз. Лечение указанными препаратами в течение 4 недель также оказалось недостаточно эффективным по сравнению с 8-недельным курсом.
Наблюдения за животными в ходе эксперимента показали отсутствие влияния исследуемого режима терапии на общее состояние мышей: животные сохраняли двигательную активность, имели хороший аппетит, опрятный внешний вид. Исследуемые дозы препаратов не вызывали существенных изменений гематологических и биохимических показателей у мышей.
Проведенный анализ патентной и научной литературы показал, что ранее терапия экспериментальной лепрозной инфекции посредством гептилгликозида мурамилдипептида в сочетании с диафенилсульфоном не проводилась.
Предлагаемым способом достигается повышение терапевтической эффективности по сравнению с прототипом в 1,9-2,4 раза. Применяемое в заявляемом способе терапевтическое воздействие гептилгликозида мурамилдипептида в комбинации с диафенилсульфоном является существенным отличием в подходе к лечению экспериментальной лепрозной инфекции. Это отличие позволило получить положительный результат в виде:
- значительного подавления локального размножения микобактерий лепры у мышей при экспериментальной лепрозной инфекции (в 1,9-2,4 раза по сравнению с прототипом) и, следовательно, сокращения сроков лечения;
- отсутствия проявлений токсического действия комбинации препаратов.
Осуществление предлагаемого способа не требует дорогостоящего оборудования, несложно в выполнении.
Предлагаемый способ может быть рекомендован для внедрения в лабораториях, занимающихся изучением воздействия иммунотропных препаратов на течение экспериментальных микобактериозов.
Авторами представлен ранее никем не предлагаемый способ лечения экспериментальной лепрозной инфекции, решающий основную задачу - повышение эффективности противолепрозной терапии. Таким образом, на основе предлагаемого способа может быть разработан способ комплексной терапии больных лепрой с использованием гептилгликозида мурамилдипептида в комбинации с диафенилсульфоном.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДЕЛИРОВАНИЯ ЛЕПРЫ | 1993 |
|
RU2098866C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ЛЕПРОЗНОЙ ИНФЕКЦИИ | 1995 |
|
RU2102482C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭКСПЕРИМЕНТАЛЬНОЙ ЛЕПРОЗНОЙ ИНФЕКЦИИ | 2006 |
|
RU2322991C1 |
| СПОСОБ ИММУНОПРОФИЛАКТИКИ ЭКСПЕРИМЕНТАЛЬНОЙ ЛЕПРОЗНОЙ ИНФЕКЦИИ | 1996 |
|
RU2135196C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭКСПЕРИМЕНТАЛЬНОЙ ЛЕПРОЗНОЙ ИНФЕКЦИИ | 2011 |
|
RU2467742C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ПРОТИВОЛЕПРОЗНЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2003 |
|
RU2242761C1 |
| СПОСОБ ДИАГНОСТИКИ ЛЕПРЫ | 1996 |
|
RU2124730C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКСТРАКТА, ОБЛАДАЮЩЕГО ПРОТИВОЛЕПРОЗНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2410111C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ДЕФЕКТА МАКРОФАГОВ | 1994 |
|
RU2105352C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГРУППЫ РИСКА РЕЦИДИВА ЛЕПРЫ | 1993 |
|
RU2082979C1 |


Изобретение относится к медицине, к лепрологии, может быть использовано для лечения лепрозной инфекции в эксперименте. Лабораторным мышам линии СВА интрагастрально вводят диафенилсульфон в дозе 12,5 мг/кг массы тела животных в комбинации с гептилгликозидом мурамилдипептида в дозе от 150 до 450 мг/кг массы тела в течение 8 недель. Данный способ повышает эффективность лечения экспериментальной лепрозной инфекции. 5 табл.
Способ лечения экспериментальной лепрозной инфекции, включающий введение лабораторным мышам диафенилсульфона, отличающийся тем, что диафенилсульфон вводят в дозе 12,5 мг/кг массы тела мыши в комбинации с гептилгликозидом мурамилдипептида в дозе от 150 до 450 мкг/кг массы тела в течение 8 недель.
| SHEPARD C.C | |||
| Effect of DDS on established infections with Mycobacterium leprae//Int | |||
| J.Lepr, 1967, p.52-57 | |||
| US 4963565, 16.10.1990 | |||
| ЖИВОТОВСКИЙ Б.Г | |||
| Применение диафенилсульфона в лечении больных туберкулезом легких | |||
| Дисс | |||
| к.м.н | |||
| - Астрахань, 1994, с.140-143 | |||
| ЛУЖНОВА С.А | |||
| Влияние диаминодифенилсульфона и рифампицина на биоритм уровня лимфоцитов у интактных мышей | |||
| - Проблемы туберкулеза, 1995, № 2, с.51-53 | |||
| ХИМИОТЕРАПИЯ ЛЕПРЫ | |||
| Доклад исследовательской группы ВОЗ | |||
| - М.: Медицина, 1995, с.31-34 | |||
| ХАЙДУКОВ С.В | |||
| и др | |||
| Макрофаги - основная мишень дисахаридсодержащих мурамилпептидов | |||
| - Иммунология, 1995, № 2, с.26-30. |
Авторы
Даты
2002-08-27—Публикация
1999-07-27—Подача