Изобретение относится к использованию некоторых соединений, особенно ингибиторов циклооксигеназы-2 (здесь и далее именуемых как "СОХ-2 ингибиторы") для лечения и профилактики опухолей, нарушений, связанных с опухолями и кахексии.
Кахексия представляет собой системное заболевание, основными симптомами которого являются прогрессирующая потеря веса, анемия, отеки, потеря аппетита и т. д. Она может проявляться как побочный эффект некоторых хронических заболеваний, таких как злокачественные опухоли, туберкулез, диабет, болезни крови, заболевания эндокринной системы, инфекции и синдром приобретенного иммунодефицита. Если кахексия является результатом наличия злокачественной опухоли, даже если введение противоопухолевых препаратов пациенту со злокачественной опухолью эффективно и наблюдается противоопухолевое действие, обычно не происходит улучшения в отношении кахексии из-за таких вредных эффектов, как миелотоксичность, которая может быть вызвана противоопухолевыми лекарствами.
Лечение кахексии часто очень затруднительно по следующим причинам. Так как по мере развития кахексии силы пациента значительно ослаблены, может оказаться невозможным продолжение лечения противоопухолевыми лекарствами (которые обычно отличаются высоким уровнем токсичности) и это становится, тем самым, препятствием для лечения злокачественной опухоли.
Для лечения симптомов кахексии часто дают пищевые добавки. Однако это часто усиливает развитие злокачественной опухоли и может сократить продолжительность жизни пациента.
В настоящее время не существует удовлетворительного способа лечения кахексии и существует все возрастающая необходимость в агентах, которые бы ослабляли симптомы кахексии.
Соединения формул (I) или (II), представленных ниже, которые наряду с некоторыми другими соединениями являются активными ингредиентами композиций настоящего изобретения, как известно, селективно ингибируют циклооксигеназу-2 (СОХ-2). Известно также, что они ингибируют продуцирование воспалительных цитокинов (особенно IL-1 и TNF-α), ингибируют продуцирование лейкотриенов (в частности, LTB4), ингибируют костную ресорбцию и обладают анальгетическим, противовоспалительным и антипиретическим действием (европейская патентная публикация 799823 А).
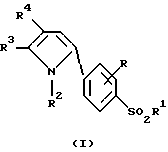
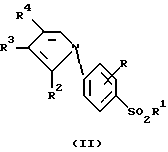
Ранее не было известно, что эти соединения могут быть использованы для лечения или профилактики кахексии.
Известно также, что некоторые другие активные ингредиенты, используемые в настоящем изобретении, а именно соединения формул (III), (IV), (V), (VI), (VII), (VIII), (IX), (X), (XII), (XIII) и (XIV), обладают селективной ингибирующей активностью против циклооксигеназы-2, оказывают ингибирующее действие на продуцирование лейкотриенов (в частности, LTB4), ингибирующее действие на костную резорбцию, обладают анальгезирующим действием, противовоспалительным действием и антипиретическим действием [международная публикация WO 95/00501, J.Med. Chem., 40, 1347 (1997), международная публикация WO 94/13635, Pharmacology, 55, 44 (1997), Prostaglandins, 47, 55 (1994), японская публикация Hei 9-52882, Jpn.J.Pharmacol, 67, 305 (1995), Inflamm. Res. , 47, Suppl. 3, S257 (1997), J.Med. Chem., 38, 4570 (1995), патент США 5474995, европейский патент 863134 и международная патентная публикация WO 98/06708] , однако ранее не было раскрыто, что эти соединения обладают действием против кахексии.
Из эпидемиологических исследований известно, что прием обычных NSAIDS (нестероидных противовоспалительных лекарств), которые являются ингибиторами СОХ-1 и СОХ-2, наиболее распространенным из которых является аспирин, и случаи возникновения рака ободочной кишки являются обратно пропорциональными. Кроме того, существует множество сообщений о том, что NSAIDS, такие как аспирин и сулиндак, обладают ингибирующей активностью против опухолевых метастаз и карциногенеза, что продемонстрировано в преклинических исследованиях. Некоторые NSAIDS были использованы в клинических исследованиях для предотвращения карциногенеза ободочной кишки.
Однако так как обычные NSAIDS неселективны в отношении СОХ-1 или СОХ-2, неизбежно возникновение вредных эффектов.
Поэтому было бы желательно обнаружить селективный ингибитор циклооксигеназы-2 для использования в качестве противоопухолевого агента, который обладал бы низким уровнем побочных эффектов.
Среди известных селективных СОХ-2 ингибиторов известно, что MF-трициклик [Oshima, M. et al. "Suppression of Intestinal Polyposis in APCΔ716 Knockout Mice by Inhibition of Cyclooxygenase 2 (COX-2)", Cell, 87, 803-809 (1996)], и целекоксиб [(Ready R.S. et а1. "Evaluation of Cyclooxygenase-2 Inhibitor for Potential Chemopreventive Properties in Colon Carcinogenesis", Cancer Res., 56, 4566-4569 (1996)] ингибируют возникновение полипоза ободочной кишки в эксперименте и что SC-58125 обладает ингибирующим действием на рост некоторых типов клеточных линий рака ободочной кишки человека [Sheng, H. et al. "Inhibition of Human Colon Cancer Cell Growth by Selective Inhibition of Cyclooxygenase-2", J. Clin. Invest., 99, 2254-2259 (1997)].
Однако в первом случае использованная экспериментальная система не является моделью установившегося рака ободочной кишки, и эти соединения способны лишь предотвращать возникновение полипоза на первой стадии рака ободочной кишки.
С другой стороны, в последнем случае единственной клеточной линией рака ободочной кишки, для которой наблюдалось ингибирующее действие в отношении роста клеточной линии рака ободочной кишки человека, была клеточная линия, которая экспрессирует циклооксигеназу-2 (клеточная линия рака ободочной кишки человека НСА-7), и было обнаружено, что клеточные линии рака ободочной кишки, в отношении которых не наблюдалось ингибирующей рост опухоли активности (НСТ-116) in vitro, не демонстрируют ингибирующих рост опухоли эффектов и in vivo. Поэтому будут или нет индуцируемые СОХ-2 ингибитором ингибирующие рост опухолевых клеток рака ободочной кишки эффекты проявляться in vivo, зависит от чувствительности использованных клеточных линий рака ободочной кишки по отношению к индуцированной СОХ-2 ингибитором ингибирующей рост клеточных линий активности in vitro. Таким образом, маловероятно, что ингибирующие рост опухолей эффекты СОХ-2 ингибиторов in vivo будут наблюдаться в отношении различных других раков, особенно тех раков, включающих раки ободочной кишки, которые устойчивы к ингибированию роста клеток in vitro, индуцированного СОХ-2 ингибитором и которые не экспрессируют циклооксигеназу-2.
Более того, ранее не было раскрыто использование комбинации селективного ингибитора циклооксигеназы-2 и производного 5-фторурацила для предотвращения или ингибирования роста опухолей.
Обнаружено, что некоторые производные 1,2-дифенилпиррола и близко родственные соединения обладают превосходной активностью в отношении предотвращения или ингибирования кахексии и что эти производные 1,2-дифенилпиррола эффективны для лечения или предотвращения связанных с опухолями нарушений, взятые отдельно или в комбинации с производным 5-фторурацила.
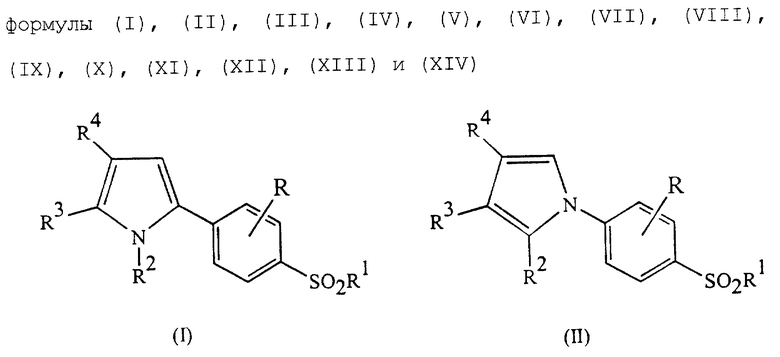
Так, в первом варианте осуществления настоящего изобретения предложен способ лечения или профилактики кахексии у млекопитающего, которым может быть человек, нуждающегося в таком лечении или профилактике, который включает введение указанному млекопитающему эффективного количества активного соединения, выбранного из группы, состоящей из соединений формул (I), (II), (III), (IV), (V), (VI), (VII), (VIII), (IX), (X), (XI), (XII), (XIII) и (XIV) (см. в конце описания),
где R представляет атом водорода, атом галогена или низшую алкильную группу;
R1 представляет низшую алкильную группу, аминогруппу или группу формулы NHRа (где Rа представляет группу, которая может быть отщеплена in vivo);
R2 представляет фенильную группу или группу, содержащую, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α и заместителей β, определенных ниже;
R3 представляет атом водорода, атом галогена, низшую алкильную группу или низшую алкильную группу, содержащую, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α;
R4 представляет атом водорода, низшую алкильную группу, низшую алкильную группу, содержащую, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α, циклоалкильную группу, арильную группу, определенную ниже, или аралкильную группу, определенную ниже;
указанная арильная группа является карбоциклической ароматической углеводородной группой, содержащей от 6 до 14 атомов углерода в одном или более ароматическом кольце, или такой группой, которая конденсирована с циклоалкильной группой, содержащей от 3 до 10 атомов углерода, и эта группа является незамещенной, или замещена, по крайней мере, одним заместителем, выбранным из группы, состоящей из заместителей α и заместителей β;
указанная аралкильная группа является низшей алкильной группой, которая замещена одной или более из арильных групп, определенных выше;
tBu представляет трет-бутильную группу;
Et представляет этильную группу; и
Рh представляет фенильную группу;
указанные заместители α выбирают из группы, состоящей из гидроксигрупп, атомов галогенов, низших алкоксильных групп и низших алкилтиогрупп; и
указанные заместители β выбирают из группы, состоящей из низших алкильных групп, алканоилоксигрупп, меркаптогрупп, алканоилтиогрупп, низших алкилсульфинильных групп, низших алкильных групп, содержащих, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α, циклоалкилоксигрупп, низших галоалкоксигрупп и низших алкилендиоксигрупп;
и их фармацевтически приемлемых солей.
Далее в настоящем изобретении предложен способ лечения или профилактики связанных с опухолями нарушений у млекопитающего, которым может быть человек, нуждающегося в таком лечении или профилактике, который включает введение указанному млекопитающему эффективного количества активного соединения, выбранного из группы, состоящей из соединений формулы (I) и (II), определенных выше.
Предпочтительными соединениями настоящего изобретения являются те соединения формулы (I) и (II) в которых:
(1) R представляет атом водорода, атом фтора, атом хлора или метильную группу, более предпочтительно атом водорода,
(2) R1 представляет метильную группу, аминогруппу или ацетиламиногруппу, более предпочтительно аминогруппу или ацетиламиногруппу,
(3) R2 представляет фенильную группу или фенильную группу, содержащую, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α1 и заместителей β1, более предпочтительно фенильную группу или фенильную группу, содержащую, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α1 и заместителей β2, еще более предпочтительно фенильную группу, в которой число заместителей составляет от 1 до 3,
(4) R3 представляет атом водорода, атом галогена, низшую алкильную группу или низшую алкильную группу, содержащую, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α1, более предпочтительно атом водорода, атом галогена, низшую алкильную группу или низшую алкильную группу, замещенную атомом галогена,
(5) R4 представляет атом водорода, низшую алкильную группу, низшую алкильную группу, содержащую, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α, циклоалкильную группу, арильную группу, арильную группу, содержащую, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α1 и заместителей β3, аралкильную группу или аралкильную группу, содержащую по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α1 и заместителей β3, более предпочтительно атом водорода, низшую алкильную группу, низшую алкильную группу, содержащую, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α2, циклоалкильную группу, арильную группу, арильную группу, содержащую, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α2 и заместителей β4, аралкильную группу, или аралкильную группу, содержащую, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α2 и заместителей β4.
Указанные заместители α1 выбирают из группы, состоящей из атомов галогенов, низших алкоксигрупп и низших алкилтио-групп.
Указанные заместители α2 выбирают из группы, состоящей из гидроксигрупп, атомов галогенов и низших алкоксигрупп.
Указанные заместители β1 выбирают из группы, состоящей из низших алкильных групп, меркаптогрупп, алканоилтиогрупп, низших алкильных групп, содержащих, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α1, низших галоалкоксигрупп и низших алкилендиоксигрупп.
Указанные заместители β2 выбирают из группы, состоящей из низших алкильных групп, меркаптогрупп, алканоилтиогрупп, низших алкильных групп, замещенных атомом галогена, низших галоалкоксигрупп и низших алкилендиоксигрупп.
Указанные заместители β3 выбирают из группы, состоящей из низших алкильных групп, низших алкильных групп, содержащих, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α и циклоалкилоксигрупп.
Указанные заместители β4 выбирают из группы, состоящей из низших алкильных групп, низших алкильных групп, замещенных атомом галогена, и циклоалкилоксигрупп.
В соединениях формул (I) и (II), где R, R3, заместители α, заместители α1 или заместители α2 представляют атом галогена, или где заместители β2 или заместители β4 представляют низшую алкильную группу, замещенную атомом галогена, атом галогена предпочтительно является атомом хлора, атомом брома, атомом фтора или атомом иода, предпочтительно атомом фтора, атомом хлора или атомом иода.
Если R, R1, R3, R4, заместитель β, заместитель β1, заместитель β2, заместитель β3 или заместитель β4 представляет низшую алкильную группу, или R3, R4, заместитель β, заместитель β1 или заместитель β3 представляет низшую алкильную группу, содержащую, по крайней мере, один заместитель, выбранный из группы, состоящей из заместителей α, или заместитель β2 или заместитель β4 представляет низшую алкильную группу, замещенную атомом галогена, алкильная группа или алкильная часть замещенной группы может быть алкильной группой с разветвленной или прямой цепью, содержащей от 1 до 6 атомов углерода, и примеры включают метил, этил, пропил, изопропил, бутил, изо-бутил, втор-бутил, трет-бутил, пентил, изопентил, 2-метилбутил, неопентил, 1-этилпропил, гексил, изогексил, 4-метилпентил, 3-метилпентил, 2-метилпентил, 1-метилпентил, 3,3-диметилбутил, 2,2-диметилбутил, 1,1-диметилбутил, 1,2-диметилбутил, 1,3-диметилбутил, 2,3-диметилбутил и 2-этилбутил. Из них предпочтительны разветвленные или неразветвленные алкильные группы, содержащие от 1 до 4 атомов углерода, более предпочтительны метильная и этильная группы. В R, R1 и R4 в качестве низшей алкильной группы особенно предпочтительна метильная группа.
Если заместитель β представляет алканоилоксигруппу или заместитель β, заместитель β1 или заместитель β2 представляет алканоилтиогруппу, алканоильная часть этих групп может быть, например, разветвленной или неразветвленной алканоильной группой, содержащей от 1 до 25 атомов углерода, такой как формил, ацетил, пропионил, бутирил, изобутирил, валерил, изовалерил, пивалоил, гексаноил, гептаноил, октаноил, нонаноил, деканоил, ундеканоил, лауроил, тридеканоил, миристоил, пальмитоил, стеароил, икозаноил, докозаноил и пентакозаноил. Из них предпочтительны те алканоильные группы, которые содержат от 1 до 12 атомов углерода, более предпочтительны те алканоильные группы, которые содержат от 1 до 6 атомов углерода, и еще более предпочтительны те алканоильные группы, которые содержат от 1 до 4 атомов углерода, и наиболее предпочтительны ацетильная и пропионильная группы.
Если R4 представляет циклоалкильную группу, предпочтительна циклоалкильная группа, содержащая от 3 до 8 атомов углерода, такая как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Из них предпочтительны циклоалкильные группы, содержащие от 3 до 7 атомов углерода, более предпочтительны циклоалкильные группы, содержащие от 3 до 6 атомов углерода, и наиболее предпочтительна циклопропильная группа.
Если R4 представляет арильную группу, эта арильная группа может быть карбоциклической ароматической углеводородной группой, содержащей от 6 до 14 атомов углерода, и может быть незамещенной или может быть замещена, по крайней мере, одним заместителем, выбранным из группы, состоящей из заместителей α и заместителей β. Такая группа может содержать одно ароматическое кольцо или может содержать два или более конденсированных колец. Примеры таких групп включают фенил, инденил, нафтил, фенантренил и антраценил. Из них предпочтительны фенильная и нафтильная группы, более предпочтительна фенильная группа. Вышеуказанная арильная группа может быть конденсирована с циклоалкильной группой, содержащей от 3 до 10 атомов углерода, и примеры таких конденсированных групп включают, например, 2-инданильную группу.
Если R4 представляет аралкильную группу, то алкильная группа, может быть любой из алкильных групп, определенных и представленных примерами выше в отношении R и т.д., и может быть замещена 1-3 арильными группами, как определено и представлено примерами выше. Такая группа может быть незамещенной или может быть замещена, по крайней мере, одним из заместителей α или β. Примеры таких групп включают бензил, фенэтил, 3-фенилпропил, 4-фенилбутил, 1-нафтилметил, 2-нафтилметил, дифенилметил, трифенилметил, 1-нафтилдифенилметил и 9-антрилметил. Из них предпочтительна алкильная группа, содержащая от 1 до 4 атомов углерода, которая замещена одной арильной группой, содержащей от 6 до 10 атомов углерода.
Если заместитель α, заместитель α1 или заместитель α2 представляет низшую алкоксигруппу, она может быть, например, алкоксигруппой с разветвленной или прямой цепью, содержащей, например, от 1 до 6 атомов углерода, такой, как метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси, пентилокси, изопентилокси, 2-метилбутокси, неопентил-окси, 1-этилпропокси, гексилокси, изогексилокси, 4-метилпентилокси, 3-метилпентилокси, 2-метилпентилокси, 1-метилпентилокси, 3,3-диметилбутокси, 2,2-диметилбутокси, 1,1-диметилбутокси, 1,2-диметилбутокси, 1,3-диметилбутокси, 2,3-диметилбутокси или 2-этилбутокси. Из них предпочтительны разветвленные или неразветвленные алкоксигруппы, содержащие от 1 до 4 атомов углерода, более предпочтительны метокси и этоксигруппы.
Если заместитель α или заместитель α1 представляет низшую алкилтиогруппу, она может быть разветвленной или неразветвленной алкилтиогруппой, содержащей от 1 до 6 атомов углерода, и ее примеры включают метилтио, этилтио, пропилтио, изопропилтио, бутилтио, изобутилтио, втор-бутилтио, трет-бутилтио, пентилтио, изопентилтио, 2-метилбутилтио, неопентилтио, 1-этилпропилтио, гексилтио, изогексилтио, 4-метилпентилтио, 3-метилпентилтио, 2-метилпентилтио, 1-метилпентилтио, 3,3-диметилбутилтио, 2,2-диметилбутилтио, 1,1-диметилбутилтио, 1,2-диметилбутилтио, 1,3-диметилбутилтио, 2,3-диметилбутилтио и 2-этилбутилтио. Из них предпочтительны разветвленные или неразветвленные алкилтиогруппы, содержащие от 1 до 4 атомов углерода, предпочтительно метилтио и этилтиогруппы.
Если заместитель β представляет низшую алкилсульфинильную группу, она может быть разветвленной или неразветвленной алкилсульфинильной группой, содержащей от 1 до 6 атомов углерода, такой как метилсульфинил, этилсульфинил, пропилсульфинил, изопропилсульфинил, бутилсульфинил, изобутилсульфинил, втор-бутилсульфинил, трет-бутилсульфинил, пентилсульфинил, изопентилсульфинил, 2-метилбутилсульфинил, неопентилсульфинил, 1-этилпропилсульфинил, гексилсульфинил, изогексилсульфинил, 4-метилпентилсульфинил, 3-метилпентилсульфинил, 2-метилпентилсульфинил, 1-метилпентилсульфинил, 3,3-диметилбутилсульфинил, 2,2-диметилбутилсульфинил, 1,1-диметилбутилсульфинил, 1,2-диметилбутилсульфинил, 1,3-диметилбутилсульфинил, 2,3-диметилбутилсульфинил и 2-этилбутилсульфинил. Из них предпочтительны разветвленные или неразветвленные алкилсульфинильные группы, содержащие от 1 до 4 атомов углерода.
Если заместитель β, заместитель β3 или заместитель β4 представляет циклоалкилоксигруппу, она может быть, например, циклоалкилоксигруппой, содержащей от 3 до 8 атомов углерода, такой как циклопропилокси, циклобутилокси, циклопентилокси, циклогексилокси, циклогептилокси и циклооктилоксигруппой. Из них предпочтительны циклоалкилоксигруппы, содержащие от 3 до 7 атомов углерода, более предпочтительны циклоалкилоксигруппы, содержащие от 5 до 6 атомов углерода, и наиболее предпочтительна циклопентилоксигруппа.
Если заместитель β, заместитель β1 или заместитель β2 представляет низшую галоалкоксигруппу, она является алкоксигруппой, которая может быть такой, как определена и представлена примерами выше в отношении заместителя α и т. д., и которая замещена, по крайней мере, одним атомом галогена, таким, как определен и представлен примерами выше. Примеры таких
групп включают фторметокси, дифторметокси, трифторметокси, 2-фторэтокси, 2-хлорэтокси, 2-бромэтокси, 2,2-дифторэтокси, 2,2,2-трифторэтокси, 2,2,2-трихлорэтокси, 3-фторпропокси, 4-фторбутокси, хлорметокси, трихлорметокси, иодометокси и бромметокси. Из них предпочтительны низшие галоалкоксигруппы, которые содержат от 1 до 4 атомов углерода, более предпочтительно фторметокси, дифторметокси, трифторметокси, 2-фторэтокси, 2-хлорэтокси, 2-бромэтокси, 3-фторпропокси, 4-фторбутокси, хлорметокси, трихлорметокси и бромметокси, и наиболее предпочтительны фторметокси, дифторметокси и трифторметокси группы.
Если заместитель β, заместитель β1 или заместитель β2 представляет низшую алкилендиоксигруппу, она может быть, например, разветвленной или неразветвленной алкилендиоксигруппой, содержащей от 1 до 6 атомов углерода, такой как метилендиокси, этилендиокси, триметилендиокси, тетраметилендиокси, пентаметилендиокси, гексаметилендиокси и пропилендиоксигруппа. Из них предпочтительны алкилендиоксигруппы, которые содержат от 1 до 4 атомов углерода, более предпочтительны метилендиокси и этилендиоксигруппы.
Если заместитель β2 или заместитель β4 представляет низшую алкильную группу, замещенную атомом галогена, она может быть алкильной группой, определенной и представленной примерами выше в отношении R и т.п., которые замещены, по крайней мере, одним атомом галогена, как также определено и представлено примерами выше. Примеры таких групп включают фторметил, дифторметил, трифторметил, 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, 2,2,2-трихлорэтил, 3-фторпропил, 4-фторбутил, хлорметил, трихлорметил, 2-хлорэтил, 3-хлорпропил, бромметил, 2-бромэтил, иодометил, 2-иодоэтил, хлордифторметил и бромдифторметил. Из них предпочтительны галоалкильные группы, содержащие от 1 до 4 атомов углерода, более предпочтительны, фторметил, дифторметил, трифторметил, 2-фторэтил, 3-фторпропил, 4-фторбутил, хлорметил, трихлорметил и бромметил, и наиболее предпочтительны фторметил, дифторметил и трифторметил.
Если Rа представляет группу, которая отщепляется in vivo, она является группой, которая может быть отщеплена в организме человека в физиологических условиях, таких как гидролиз, то есть является группой, продуцирующей свободную аминогруппу (-NH2) из группы формулы -NHRа (где Rа имеет указанные выше значения). С помощью следующего теста можно легко определить, может или нет группа отщепляться in vivo: подлежащее тестированию соединение вводят перорально или внутривенно экспериментальному животному, такому как крыса или мышь, и жидкость организма тестируют на присутствие или отсутствие соответствующего соединения, содержащего свободную аминогруппу, или его фармацевтически приемлемой соли.
Такие группы включают, например:
алканоильные группы, определенные и представленные примерами выше для заместителя β и т.п.;
низшие алкоксильные группы, в которых алкоксигруппа определена и представлена примерами выше для заместителя α и т.п., такая как метоксикарбонил, этоксикарбонил, пропоксикарбонил, изопропоксикарбонил, бутоксикарбонил, изобутоксикарбонил, трет-бутоксикарбонил, пентилоксикарбонил, гексилоксикарбонил и циклогексилоксикарбонил;
аралкилоксикарбонильную группу, в которой арил определен выше, и может быть незамещенным или может быть замещен одной или двумя низшими алкокси или нитрогруппами, такую как бензилоксикарбонил, 4-метоксибензилоксикарбонил, 3,4-диметоксибензилоксикарбонил, 2-нитробензилоксикарбонил и 4-нитробензилоксикарбонил;
алканоилоксиметильную группу, в которой алканоильная группа определена и представлена примерами выше для заместителя β и т.п., такую как формилоксиметил, ацетоксиметил, пропионилоксиметил, бутирилоксиметил, пивалоилоксиметил, валерилоксиметил, изовалерилоксиметил и гексаноилоксиметил;
низшую алкоксикарбонилоксиметильную группу, в которой алкоксигруппа определена и представлена примерами выше для заместителя α и т.п., такую как метоксикарбонилоксиметил, этоксикарбонилоксиметил, пропоксикарбонилоксиметил, изопропоксикарбонилоксиметил, бутоксикарбонилоксиметил, изобутоксикарбонилоксиметил и пентилоксикарбонилоксиметил; и
(2-oкco-l, 3-диоксолен-4-ил)метильную группу, которой в 5-положении диоксоленового кольца может быть замещена низшей алкильной группой или арильной группой, как определено и представлено примерами выше для R и R4 соответственно, такую как (5-фенил-2-оксо-1,3-диоксолен-4-ил)метил, [5-(4-метилфенил)-2-oкco-l,3-диоксолен-4-ил]метил, [5-(4-метоксифенил)-2-oкco-l,3-диоксолен-4-ил]метил, [5-(4-фторфенил]-2-оксо-1,3-диоксолен-4-ил]метил, [5-(4-хлорфенил)-2-оксо-1,3-диоксолен-4-ил] метил, (2-оксо-1,3-диоксолен-4-ил)метил, (5-метил-2-оксо-1,3-диоксолен-4-ил)метил, (5-этил-2-оксо-1,3-диоксолен-4-ил)метил, (5-пропил-2-оксо-1,3-диоксолен-4-ил)метил, (5-изопропил-2-оксо-1,3-диоксолен-4-ил)метил и (5-бутил-2-оксо-1,3-диоксолен-4-ил)метил.
Из них предпочтительны алканоильные группы, содержащие от 1 до 12 атомов углерода, алкоксикарбонильные группы, содержащие от 2 до 5 атомов углерода, аралкилоксикарбонильные группы, содержащие от 7 до 8 атомов углерода, алканоилоксиметильные группы, содержащие от 3 до 6 атомов углерода, алкоксикарбонилоксиметильные группы, содержащие от 3 до 6 атомов углерода и 5-замещенная (2-оксо-1,3-диоксолен-4-ил)метильная группа, более предпочтительны ацетил, пропионил, бутирил, изобутирил, валерил, изоваленил, пивалоил, метоксикарбонил, этоксикарбонил, бензилоксикарбонил, ацетоксиметил, пропионилоксиметил, метоксикарбонилоксиметил, этоксикарбонилоксиметил, (5-метил-2-оксо-1,3-диоксолен-4-ил)метил, и (5-фенил-2-оксо-1,3-диоксолен-4-ил)метил, и наиболее предпочтительна ацетильная группа.
Конкретные примеры R1 предпочтительно включают метил, этил, амино, ацетиламино, пропиониламино, бутириламино, изобутириламино, валериламино, изовалериламино, пивалоиламино, метоксикарбониламино, этоксикарбониламино, бензилоксикарбониламино, ацетоксиметиламино, пропионилоксиметиламино, метоксикарбонилоксиметиламино, этоксикарбонилоксиметиламино, (5-ме-тил-2-оксо-1,3-диоксолен-4-ил)метиламино и (5-фенил-2-оксо-1,3-диоксолен-4-ил)метиламиногруппы, более предпочтительны метил, амино и ацетиламиногруппы и наиболее предпочтительны амино и ацетиламиногруппы.
Конкретные примеры R2 предпочтительно включают:
незамещенную фенильную группу;
фенильные группы, содержащие от 1 до 3 заместителей, выбранных из меркаптогрупп, C1-C4 алканоилтиогрупп, атомов галогенов, C1-C4 алкильных групп, C1-C4 алкоксигрупп, C1-C4 алкилтиогрупп и C1-C4 алкилсульфинильных групп, такие как 4-меркаптофенил, 4-ацетилтиофенил, 4-пропионилтиофенил, 4-фторфенил, 4-хлорфенил, 4-бромфенил, п-толуил, 4-этилфенил, 4-метоксифенил, 4-этоксифенил, 4-метилтиофенил, 4-этилтиофенил, 4-метилсульфинилфенил, 4-этилсульфинилфенил, 3,4-дифторфенил, 2,4-дифторфенил, 3,4-дихлорфенил, 2,4-дихлорфенил, 3,4-диметилфенил, 3,4-диметоксифенил, 3-хлор-4-фторфенил, 3-хлор-4-метоксифенил, 3-фтор-4-метоксифенил, 3-метил-4-метоксифенил, 3,5-дихлор-4-метоксифенил и 4-метокси-3,5-диметилфенильная группы;
трифторметил-, дифторметокси- или трифторметоксизамещенные фенильные группы, такие как 4-трифторметилфенил, 4-дифторметоксифенил и 4-трифторметоксифенильная группы;
метилендиокси- или этилендиоксизамещенную фенильную группу, такую как 3,4-метилендиоксифенил и 3,4-этилендиок-сифенильная группы.
В том случае если R2 представляет замещенную фенильную группу, число заместителей предпочтительно равно 1-3, более предпочтительно равно 1 или 2.
Конкретные примеры R3 предпочтительно включают атомы водорода, атомы галогена, такие как фтор, хлор, бром и иод; C1-C4 алкильные группы, такие как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил и трет-бутил; и C1-C4 галоалкильные группы, такие как фторметил, хлорметил, бромметил, иодометил, дифторметил, трифторметил, 2-фторэтил, 3-фторпропил, 4-фторбутил, 2-хлорэтил и 3-хлорпропил, более предпочтительны атомы водорода; такие атомы галогена, как фтор, хлор, бром и иод; и метил, этил, фторметил, дифторметил, 2-фторэтил и 2-хлорэтил.
Конкретные примеры R4 предпочтительно включают атомы водорода; C1-C6 алкильные группы, такие как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил и гексил; причем любые из этих алкильных групп содержат заместитель, выбранный из гидрокси, галогена (такого как фтор, хлор, бром и иод) и C1-C4 алкокси (такой как метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси и трет-бутокси); С3-С7 циклоалкильные группы, такие как циклопропил, циклобутил, циклопентил, циклогексил и циклогептил; С6-С10 арильные группы, такие как фенил и нафтил, которые могут быть незамещенными или могут содержать один или более из следующих заместителей γ; С6-С10 арил C1-C4 алкильные группы, такие как бензил, фенэтил, 3-фенилпропил, 4-фенилбутил, 1-нафтилметил и 2-нафтилметил, которые могут быть незамещены или могут иметь один или более из следующих заместителей γ в арильной части;
заместители γ включают: атомы галогена, такие как фтор, хлор, бром и иод; C1-C4 алкильные группы, такие как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил и трет-бутил; C1-C4 галоалкильные группы, такие как фторметил, дифторметил, трифторметил, хлорметил, трихлорметил, хлородифторметил, 2-фторэтил, 2-хлорэтил, 2-бромэтил, 2-иодоэтил, 3-фторпропил и 4-фторпропил; C1-C4 алкоксигруппы, такие как метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси и трет-бутоксигруппы; и С3-С7 циклоалкилоксигруппы, такие как циклопропилокси, циклобутилокси, циклопентилокси, циклогексилокси и циклогептилоксигруппы.
Предпочтительные примеры R4 включают: атомы водорода; C1-C4 алкильные группы, такие как метил, этил, изопропил, бутил и изобутил; C1-C4 моно-, ди- или тригалоалкильные группы, такие как фторметил, дифторметил, хлордифторметил, бромдифторметил, трифторметил, 2-фторэтил и 2,2,2-трифторэтил; гидроксиметильные группы; C1-C4 алкоксиметильные группы, такие как метоксиметил и этоксиметил; С3-С6 циклоалкильные группы, такие как циклопропил, циклобутил, циклопентил и циклогексил; фенильные группы; моно- или дифторфенильные группы, такие как 4-фторфенил и 2,4-дифторфенил; моно- или диметоксифенильные группы, такие как 4-метоксифенил и 3,4-диметоксифенил; толильные группы, такие как п-толил и о-толил; циклопентилокси(метокси)фенильные группы, такие как 3-циклопентилокси-4-метоксифенил; трифторметилфенильные группы, такие как 4-трифторметилфенил; бензильные группы; замещенные бензильные группы, такие как 4-метоксифенил и 3-циклопентилокси-4-метоксибензил; фенэтильные группы; нафтильные группы, такие как 1-нафтил и 2-нафтил; и нафтилметильные группы, такие как 1-нафтилметил и 2-нафтилметил.
Некоторые соединения настоящего изобретения, особенно соединения формулы (I) и (II), имеют кислотную группу и, таким образом, могут образовывать соли с катионами. Природа соли не является критической для настоящего изобретения при условии, что она фармацевтически приемлема, то есть что эта соль не является менее активной (или неприемлемо менее активной), более токсичной (или неприемлемо более токсичной), нежели свободная кислота. Такие соли включают, например, соли щелочных металлов, таких как натрий, калий или литий; соли щелочно-земельных металлов, таких как кальций или магний; соли других металлов, таких как алюминий, железо, медь, цинк, никель или кобальт; другие неорганические соли, такие как аммониевые соли; соли органических аминов, таких как трет.-октиламин, дибензиламин, морфолин, глюкозамин, фенилглициновый алкиловый сложный эфир, этилендиамин, N-метилглюкамин, гуанидин, диэтиламин, триэтиламин, дициклогексиламин, N,N'-дибензилэтилендиамин, хлоропрокаин, прокаин, диэтаноламин, N-бензил-N-фенэтиламин, пиперазин, тетраметиламмоний или трис(гидроксиметил)аминометан.
Далее, когда соединения формулы (I) и (II) и их соли оставляют открытыми на воздухе, они могут адсорбировать влагу и образовывать гидраты. Такие гидраты также включены в объем изобретения.
Далее, соединения формулы (I) и (II) и их соли иногда абсорбируют некоторые типы растворителей, образуя сольваты, и такие сольваты также включены в объем настоящего изобретения.
Некоторые соединения формулы (I) и (II) настоящего изобретения могут содержать асимметрические атомы углерода в молекуле, и тогда существуют стереоизомеры R-конфигурации или S-конфигурации. Каждый из этих стереоизомеров и их смеси в любых желаемых соотношениях также включены в объем настоящего изобретения.
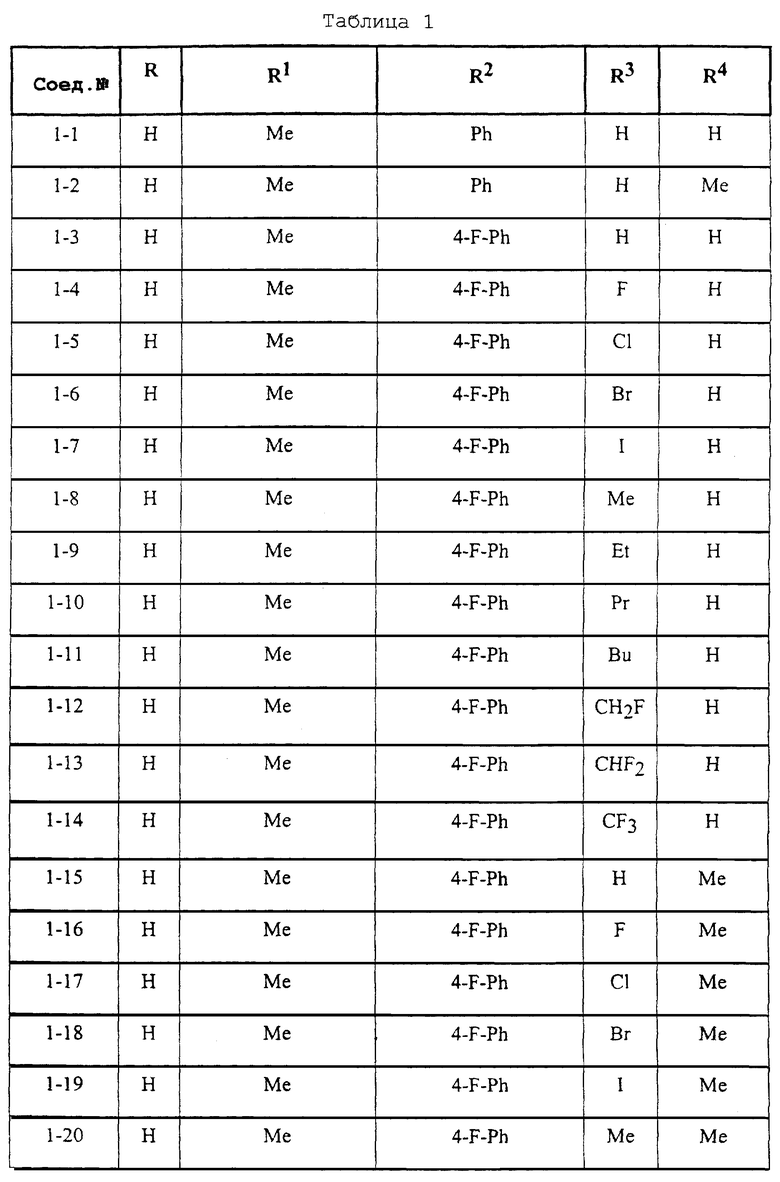
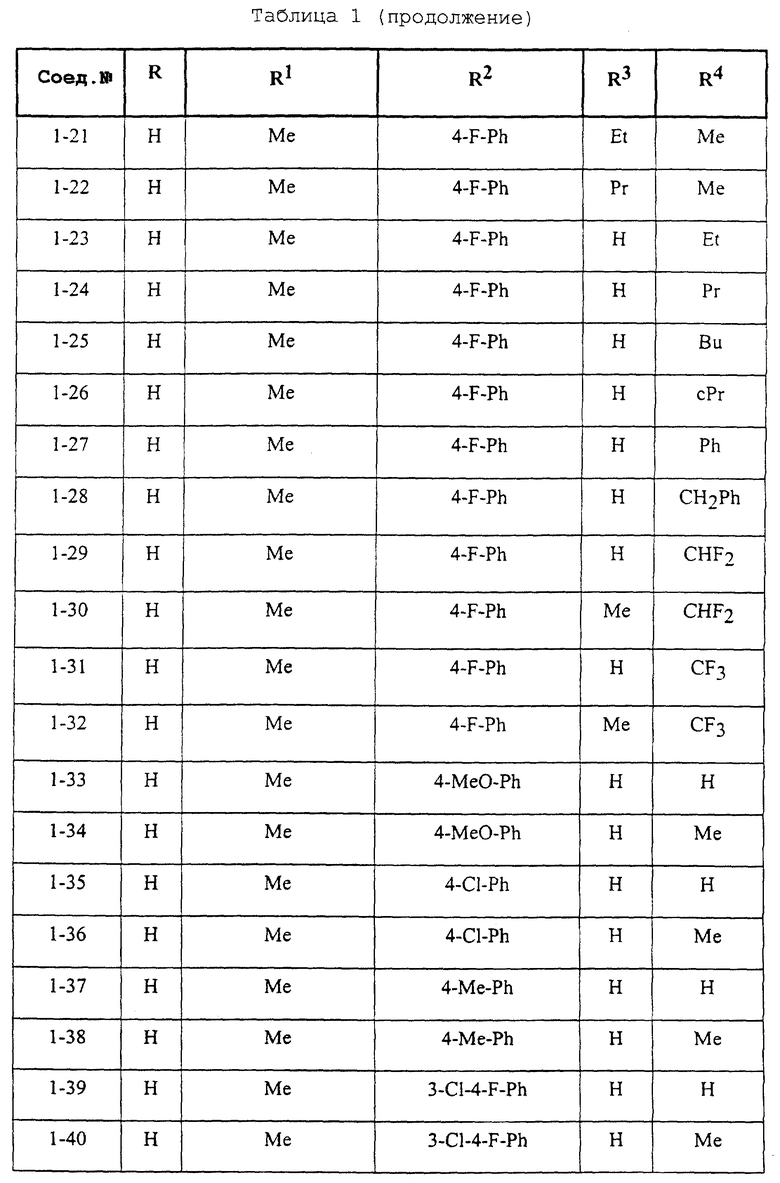
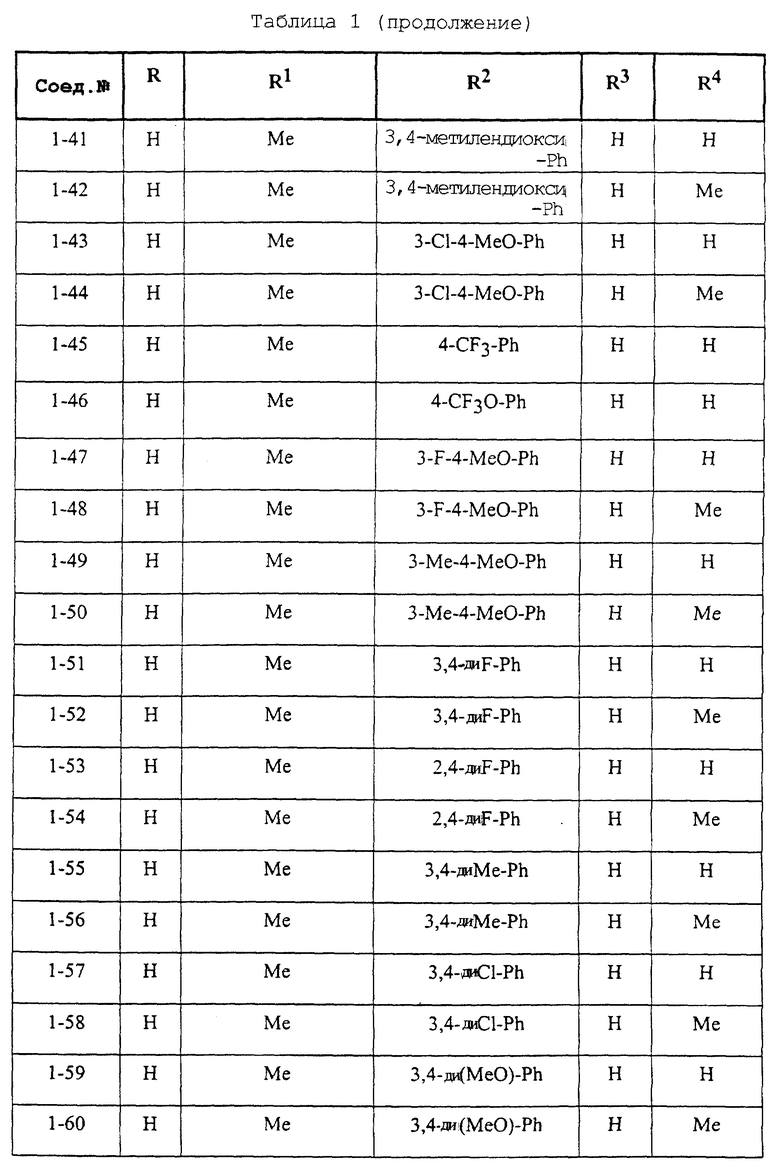
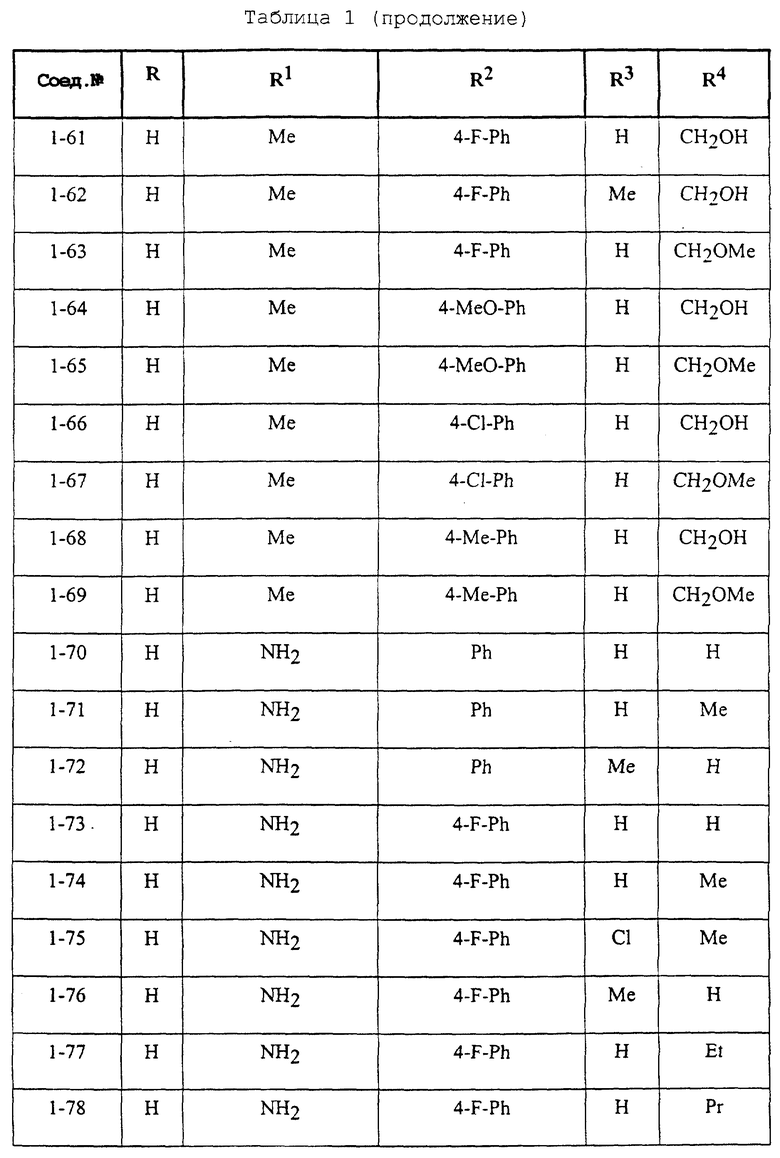
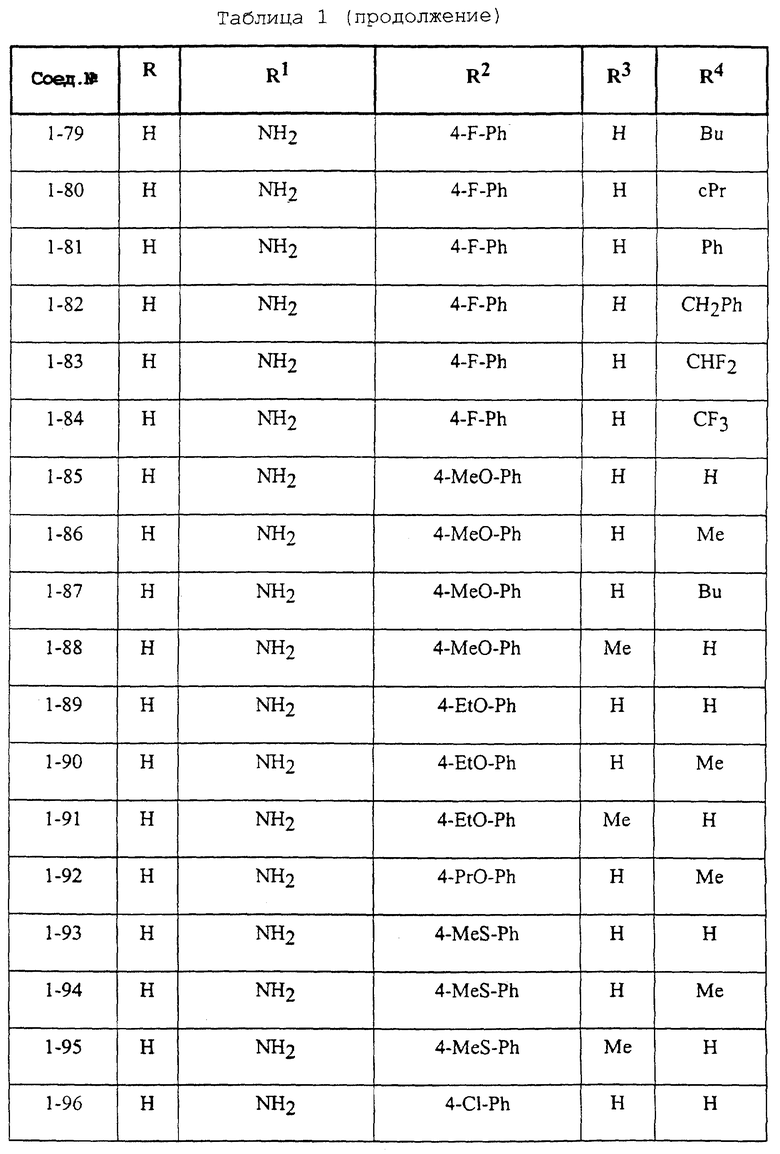
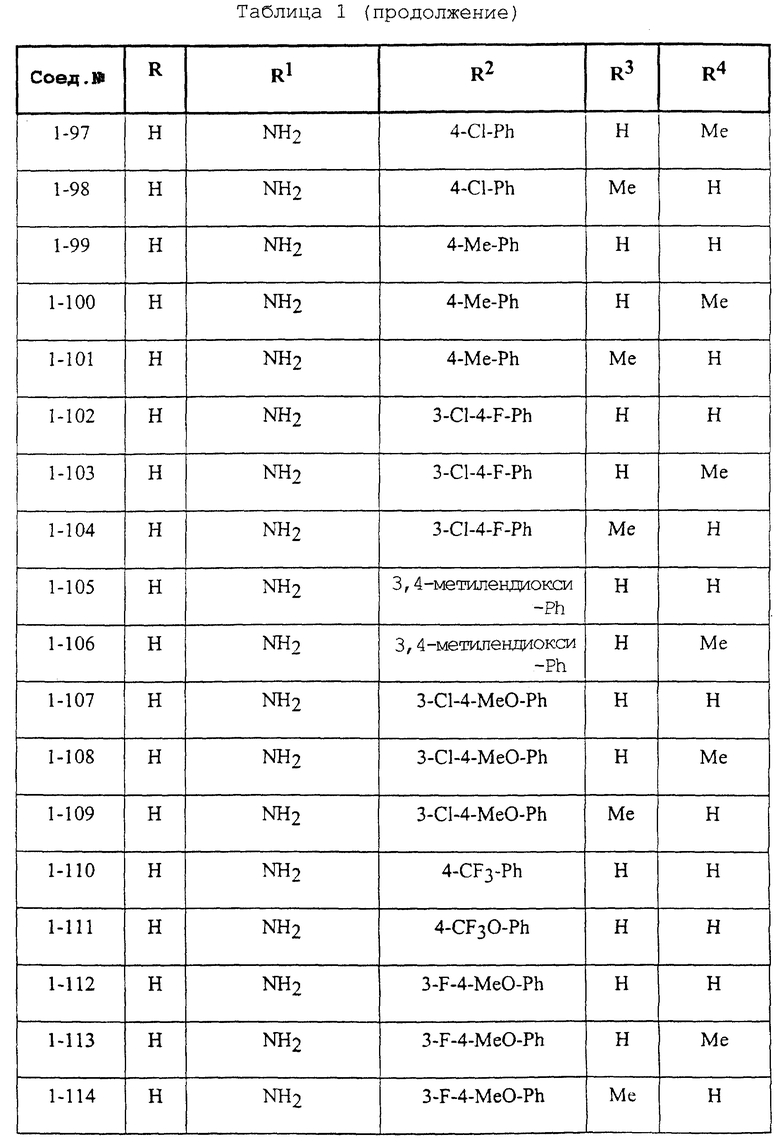
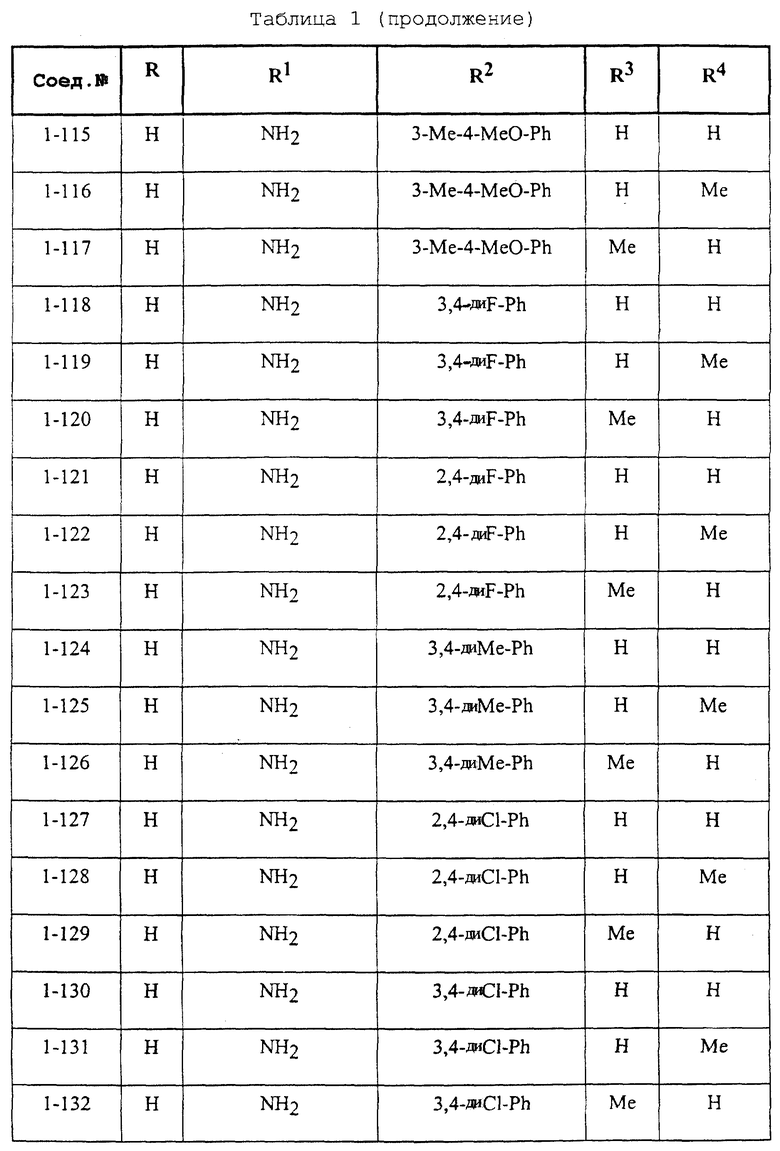
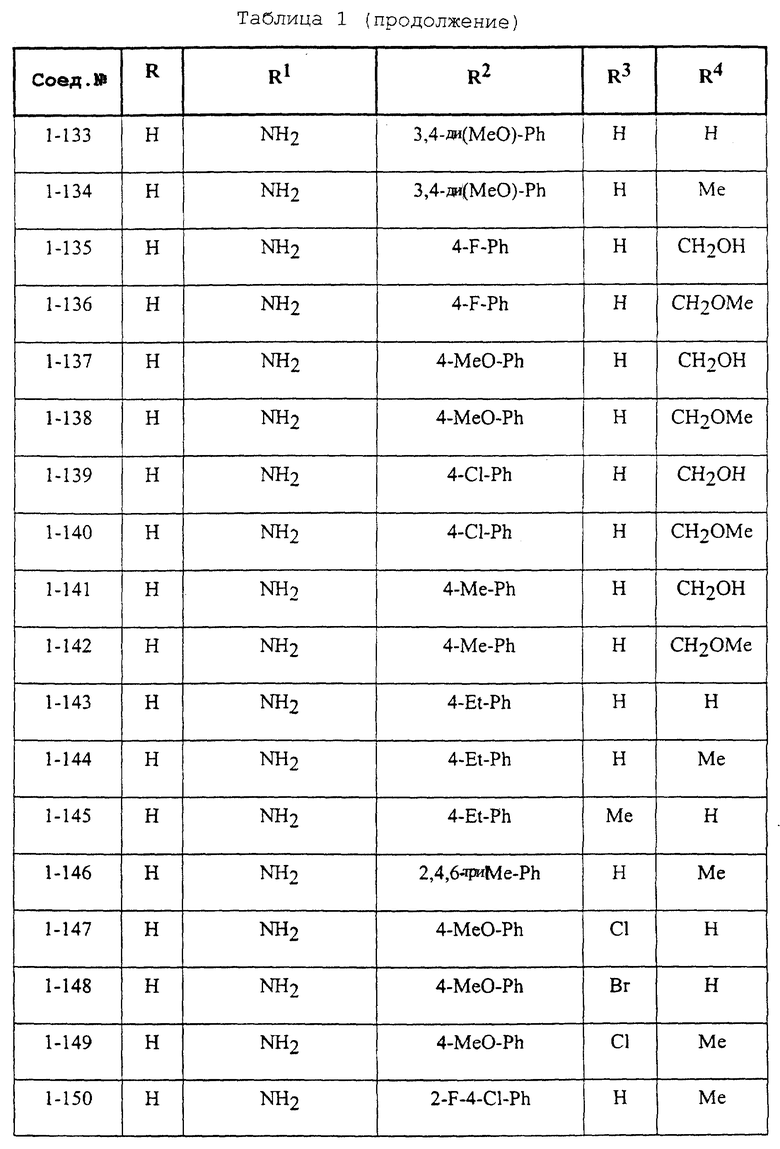
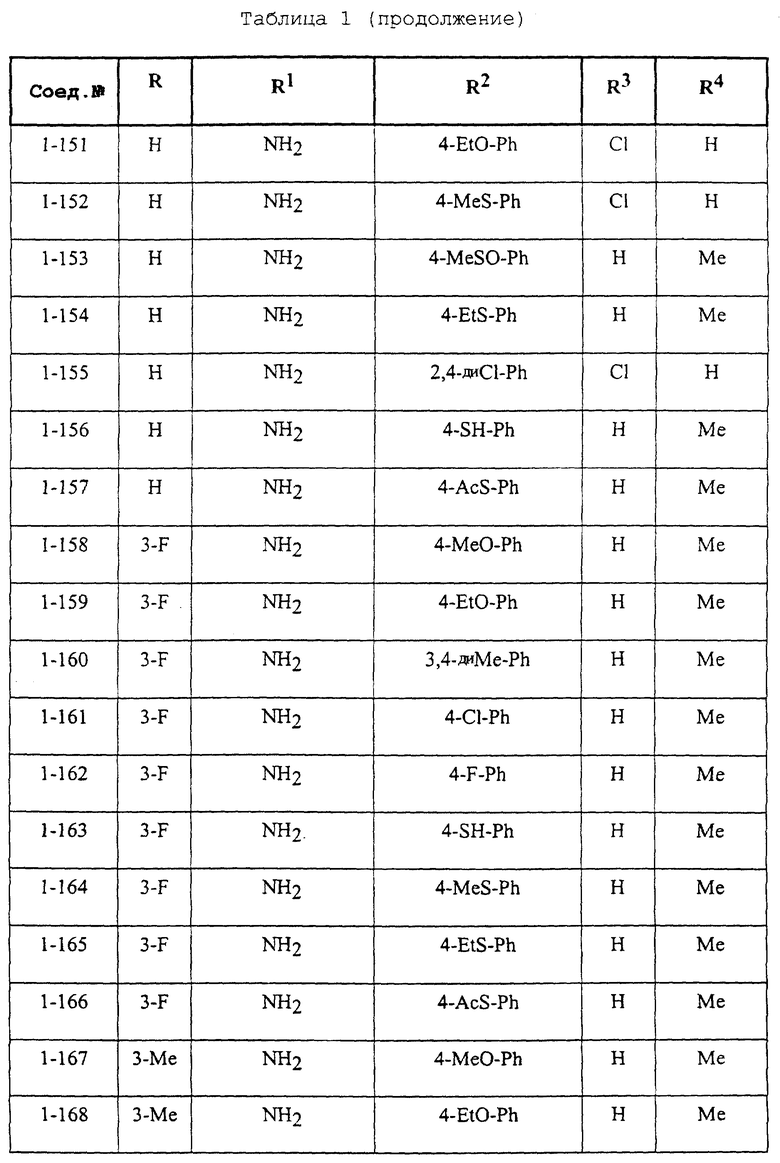
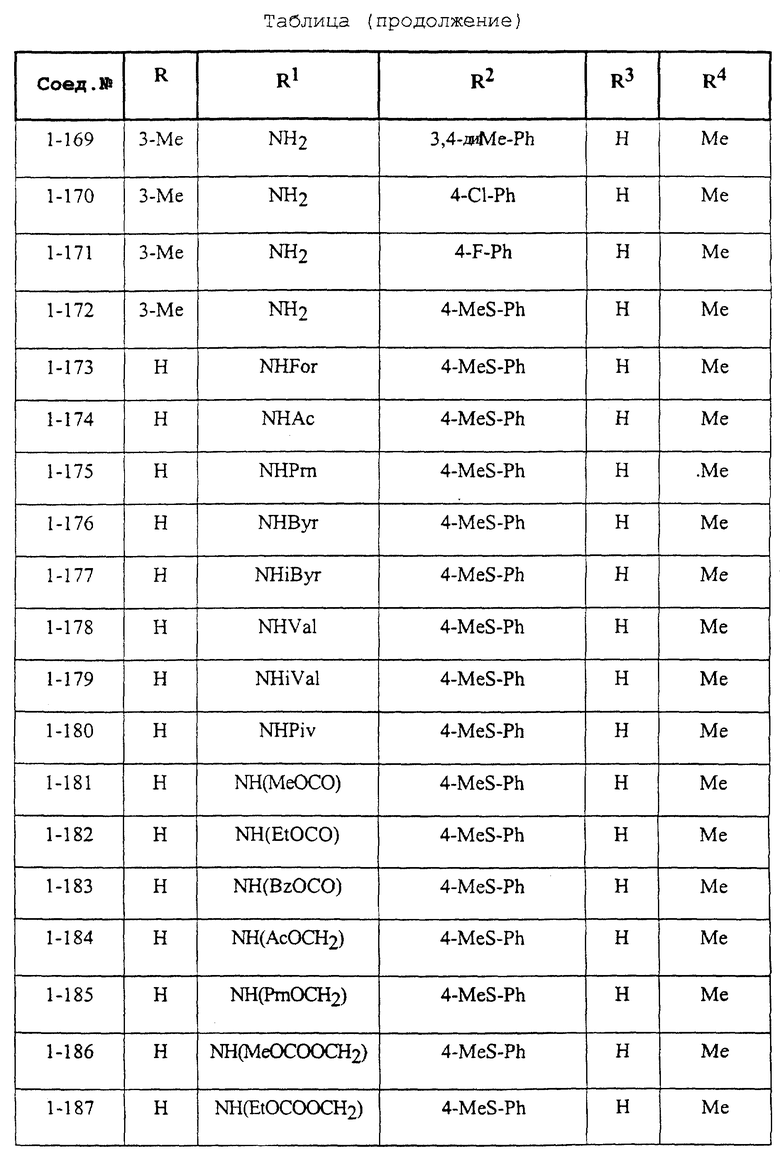
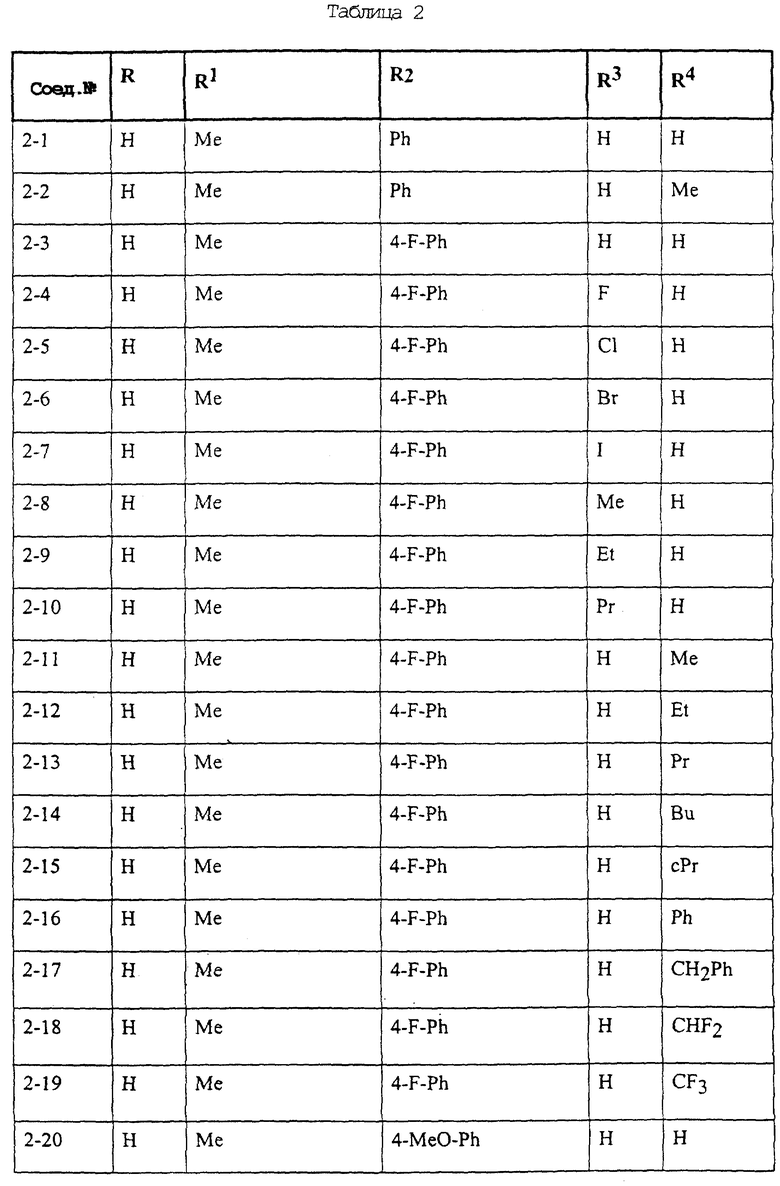
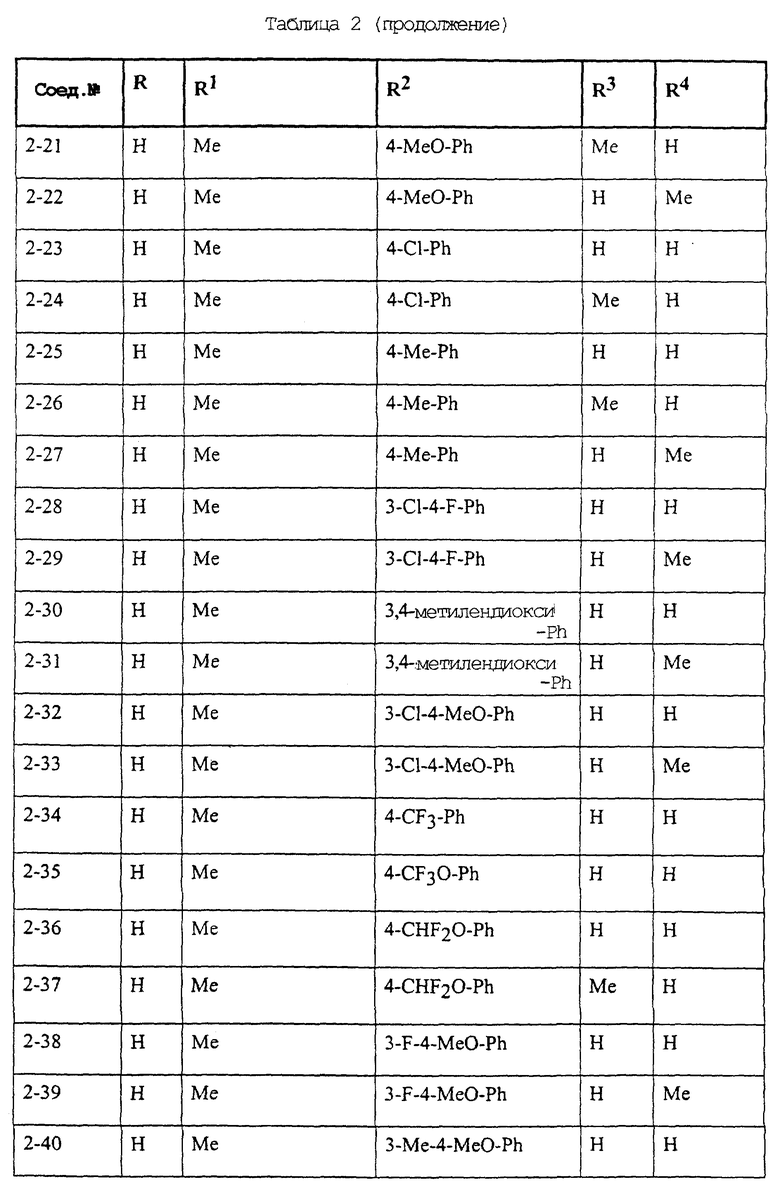
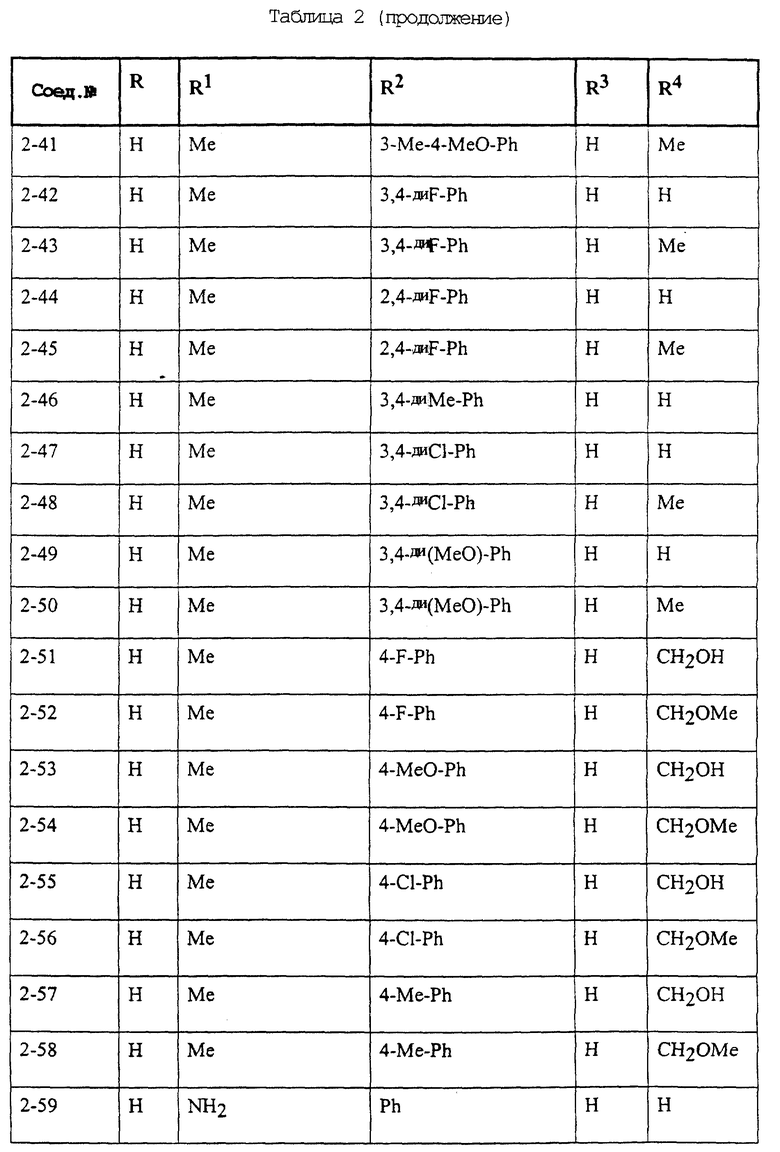
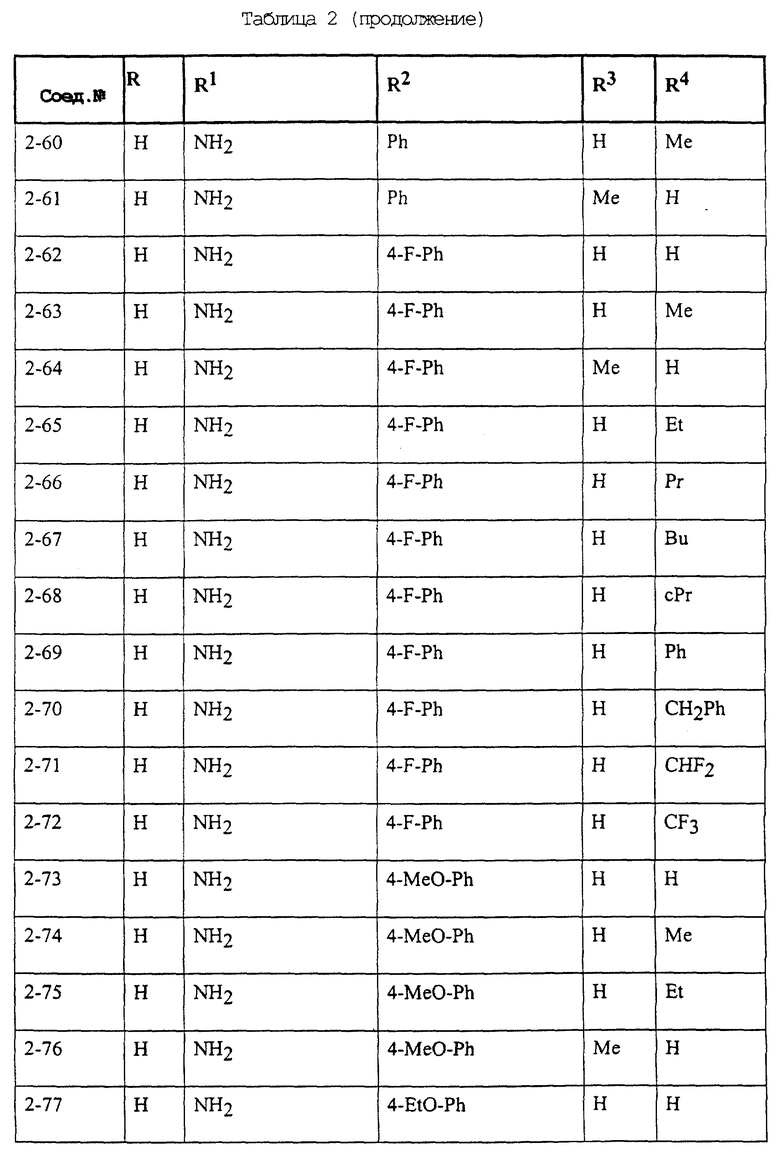
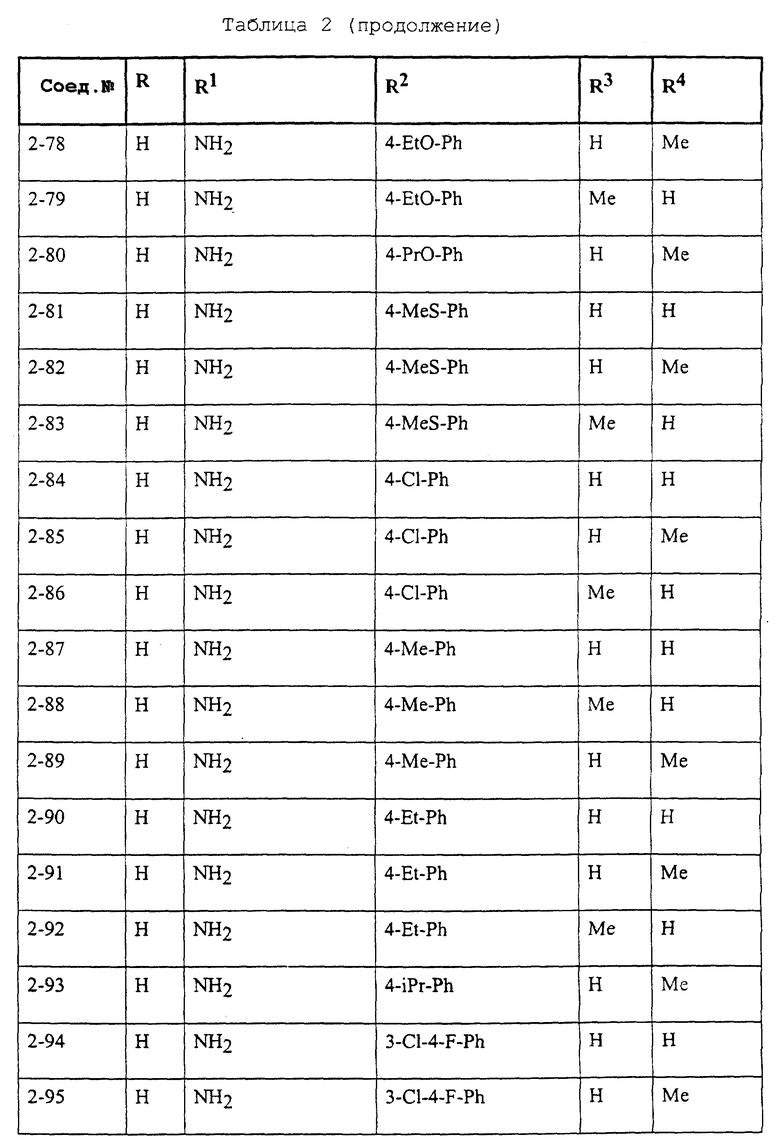
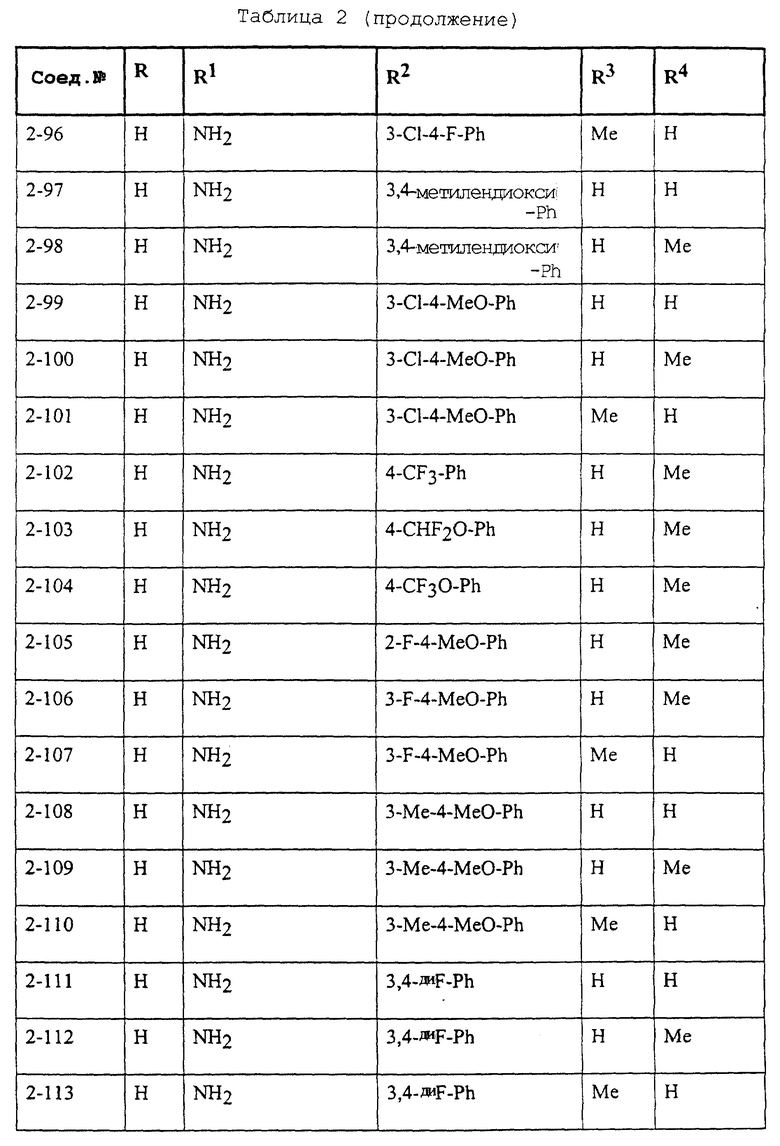
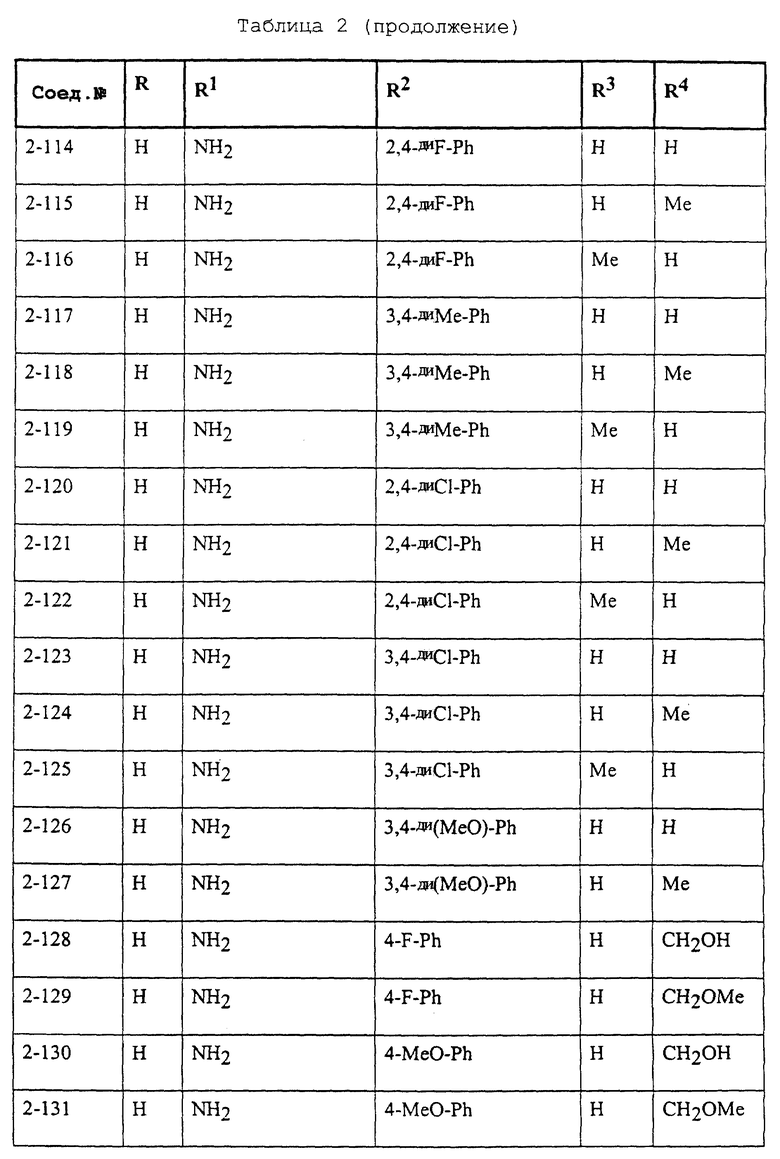
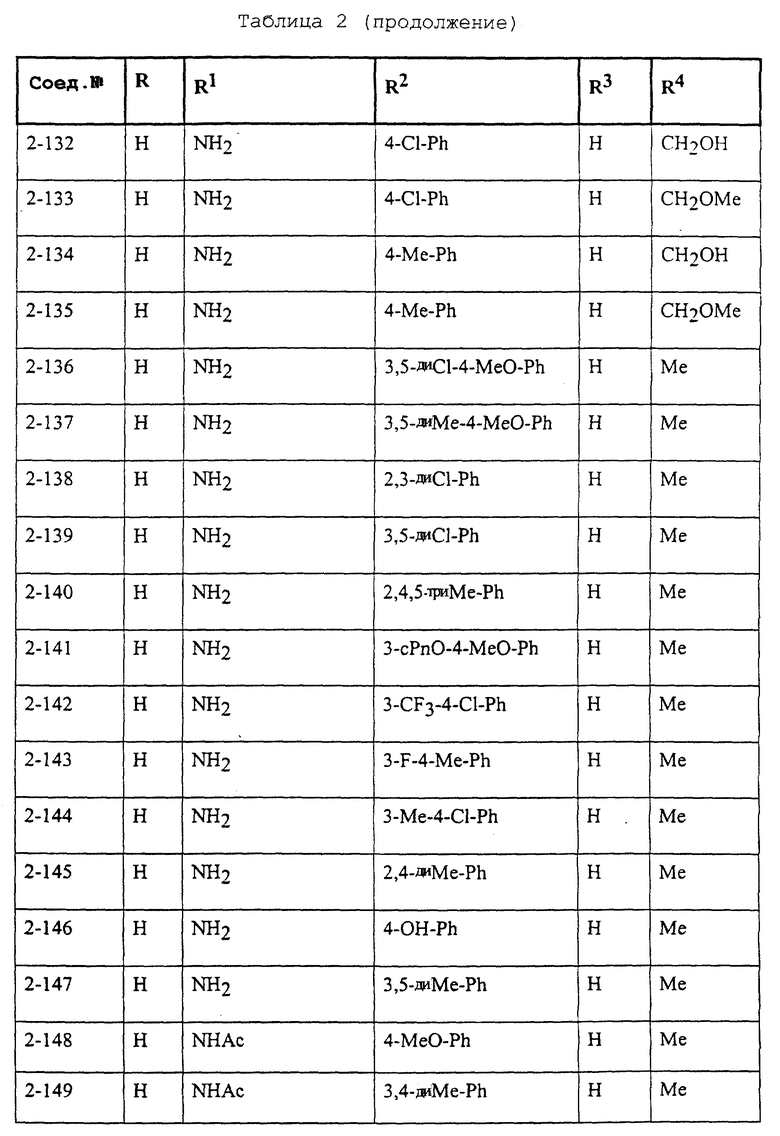
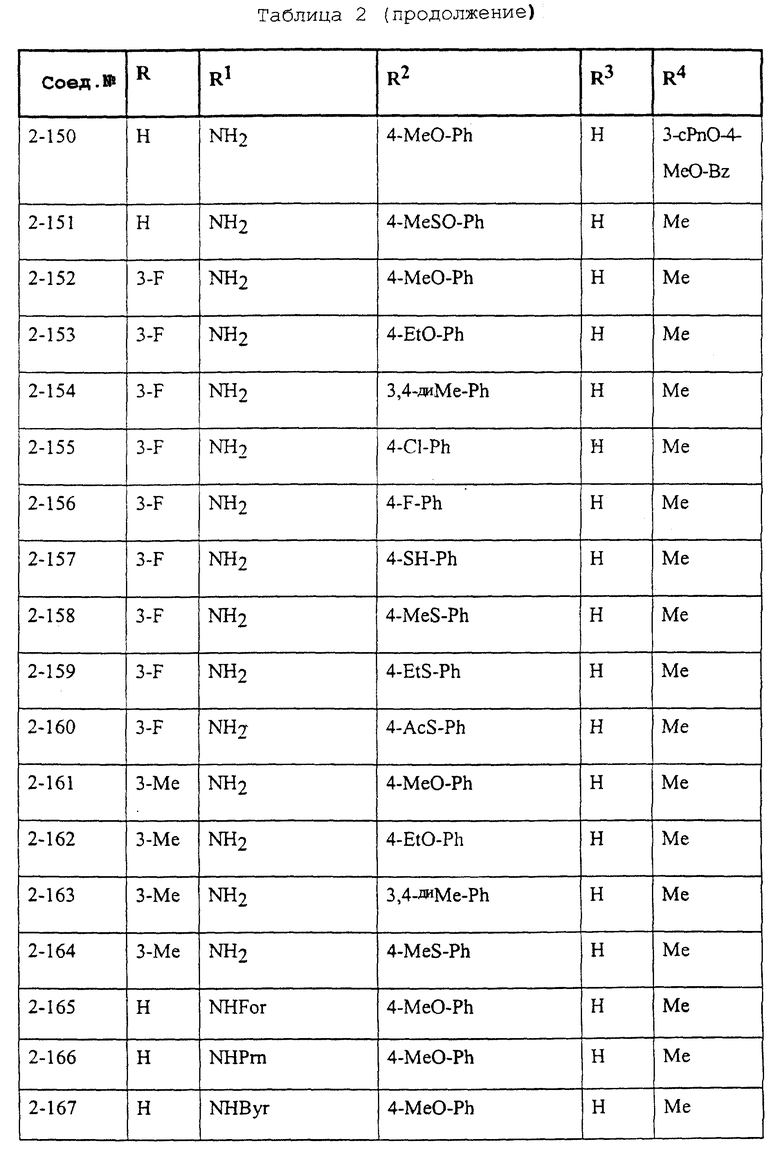
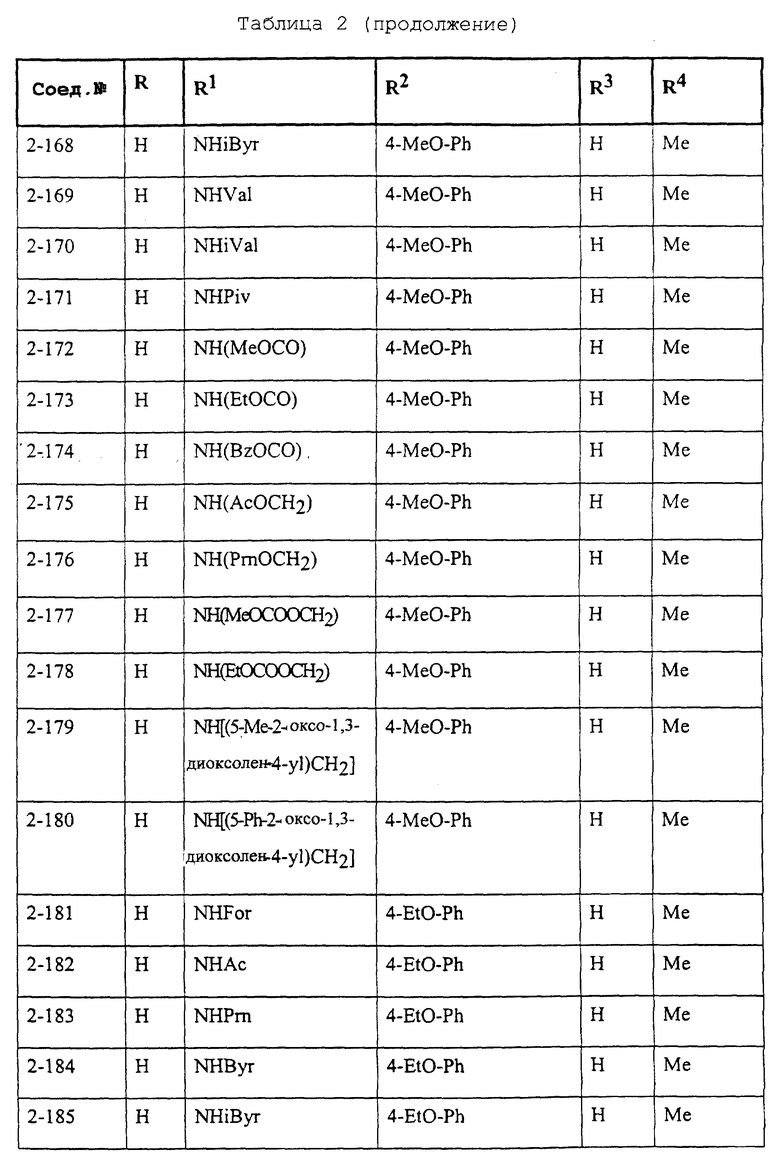
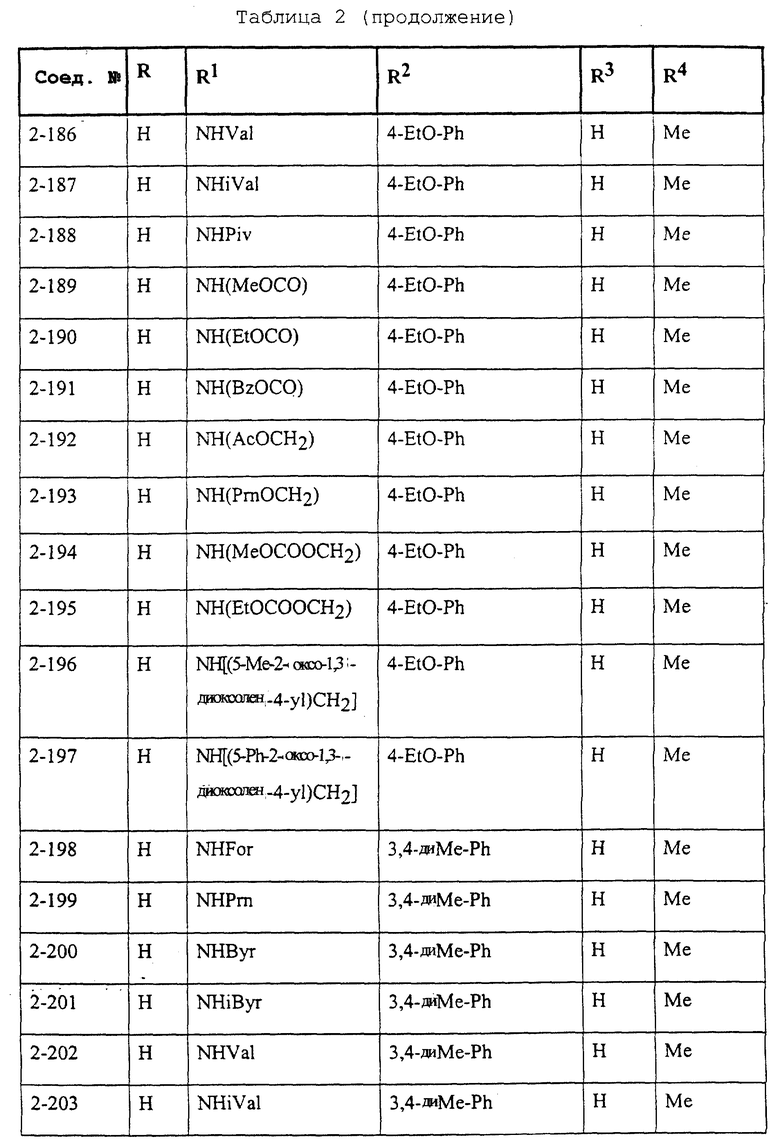
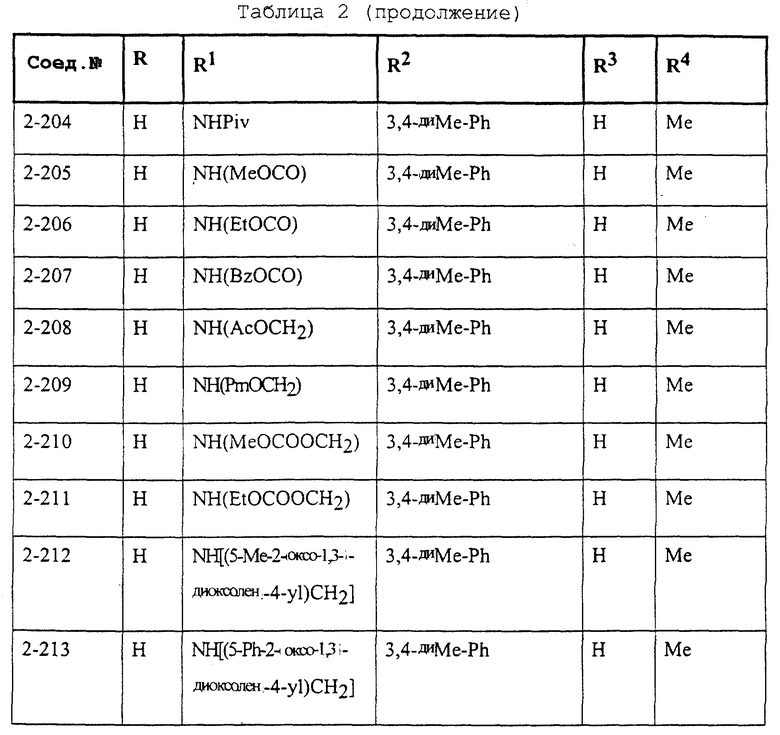
Конкретные примеры соединений формулы (I) и (II), используемые в способе, и композиции настоящего изобретения включают, например, те, которые представлены в таблице 1 [соединения формулы (1)] и таблице 2 [соединения формулы (II)].
В этих таблицах приняты следующие сокращения:
Ас ацетил; Вu бутил; Byr бутирил; iByr изобутирил; Bz бензил; Et этил; For формил; Me метил; Ph фенил; Piv пивалоил; сРn циклопентил; Рr пропил; сРr циклопропил; iPr изопропил; Рrn пропионил; iVal изовалерил; и Val валерил.
Из перечисленных выше соединений предпочтительньми являются:
1) 3-метил-2-(4-метилфенил)-1-(4-сульфамоилфенил)пиррол;
2) 4-метил-2-(4-метилфенил)-1-(4-сульфамоилфенил)пиррол;
3) 1-(4-фторфенил)-2-(4-сульфамоилфенил)пиррол;
4) 1-(4-фторфенил)-4-метил-2-(4-сульфамоилфенил)пиррол,
5) 5-фтор-1-(4-фторфенил)-2-(4-метилсульфонилфенил)пиррол;
6) 2-(4-метоксифенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
7) 1-(4-метоксифенил)-4-метил-2-(4-сульфамоилфенил)пиррол;
8) 4-этил-2-(4-метоксифенил)-1-(4-сульфамоилфенил)пиррол;
9) 2-(4-хлорфенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
10) 4-метил-2-(4-метилтиофенил)-1-(4-сульфамоилфенил)пиррол;
11) 2-(4-этоксифенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
12) 2-(4-метокси-3-метилфенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
13) 2-(3-фтор-4-метоксифенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
14) 4-метил-2-фенил-1-(4-сульфамоилфенил)пиррол;
15) 2-(3,4-диметилфенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
16) 2-(3-хлор-4-метоксифенил)-4-метил-1-(4-сульфамоилфенил) пиррол;
17) 4-метил-1-(4-метилтиофенил)-2-(4-сульфамоилфенил)пиррол;
18) 5-хлор-1-(4-метоксифенил)-2-(4-сульфамоилфенил)пиррол;
19) 1-(3,4-диметилфенил)-4-метил-2-(4-сульфамоилфенил)пиррол;
20) 5-хлор-1-(4-этоксифенил)-2-(4-сульфамоилфенил)пиррол;
21) 5-хлор-1-(4-метилтиофенил)-2-(4-сульфамоилфенил)пиррол;
22) 1-(4-этилтиофенил)-4-метил-2-(4-сульфамоилфенил)пиррол;
23) 2-(3,5-диметилфенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
24) 1-(4-меркаптофенил)-4-метил-2-(4-сульфамоилфенил)пиррол;
25) 1-(4-ацетилтиофенил)-4-метил-2-(4-сульфамоилфенил)пиррол;
26) 1-(4-ацетиламиносульфонилфенил)-4-метил-2-(4-метоксифенил)пиррол и
27) 1-(4-ацетиламиносульфонилфенил)-4-метил-2-(3,4-диметилфенил)пиррол.
Из них более предпочтительными соединениями являются:
2) 4-метил-2-(4-метилфенил)-1-(4-сульфамоилфенил)пиррол;
6) 2-(4-метоксифенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
9) 2-(4-хлорфенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
10) 4-метил-2-(4-метилтиофенил)-1-(4-сульфамоилфенил)пиррол;
11) 2-(4-этоксифенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
12) 2-(4-метокси-3-метилфенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
13) 2-(3-фтор-4-метоксифенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
15) 2-(3,4-диметилфенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
17) 4-метил-1-(4-метилтиофенил)-2-(4-сульфамоилфенил)пиррол;
26) 1-(4-ацетиламиносульфонилфенил)-4-метил-2-(4-метоксифенил)пиррол и
27) 1-(4-ацетиламиносульфонилфенил)-4-метил-2-(3,4-диметилфенил)пиррол.
Из них наиболее предпочтительными соединениями являются:
11) 2-(4-этоксифенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
15) 2-(3,4-диметилфенил)-4-метил-1-(4-сульфамоилфенил)пиррол;
17) 4-метил-1-(4-метилтиофенил)-2-(4-сульфамоилфенил)пиррол;
26) 1-(4-ацетиламиносульфонилфенил)-4-метил-2-(4-метоксифенил)пиррол и
27) 1-(4-ацетиламиносульфонилфенил)-4-метил-2-(3,4-диметилфенил)пиррол.
Соединения формулы (I), соединения формулы (II) и фармацевтически приемлемые соли этих соединений являются известными соединениями, а способ получения этих соединений раскрыт в Европейской патентной публикации ЕР 799823 А, которая включена сюда в качестве ссылки.
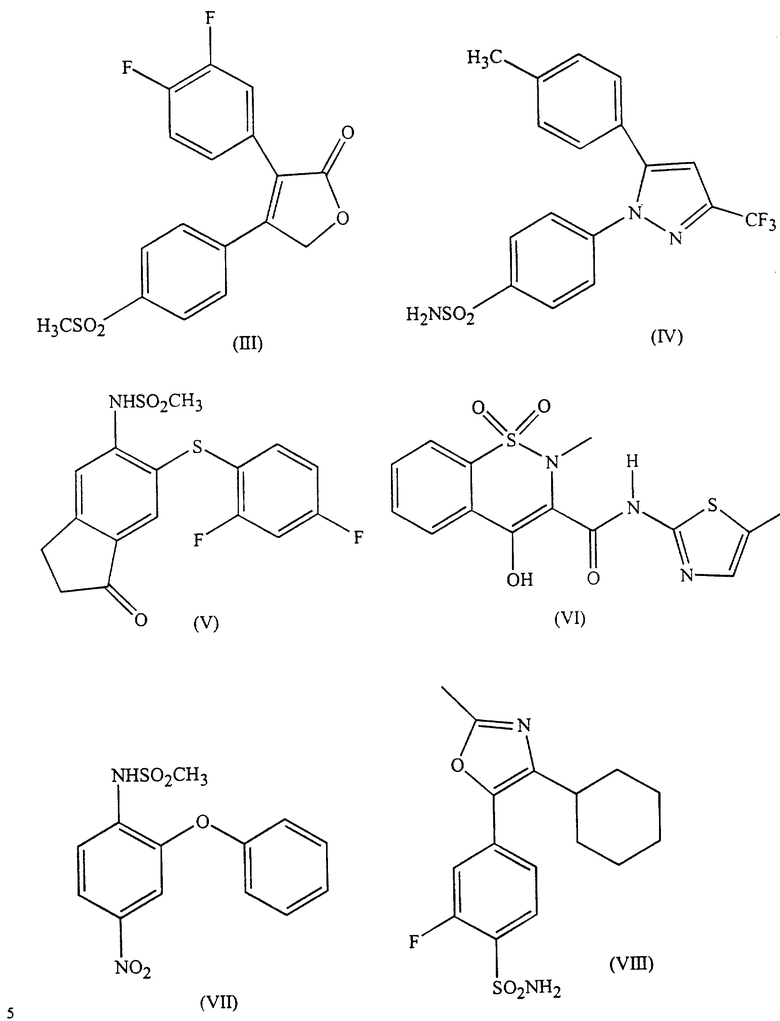
Соединения формул (III)-(XIV) имеют следующие химические названия:
(III) 3-(3,4-дифторфенил)-4-(4-метансульфонилфенил)-5Н-фуран-2-он,
(IV) 4-(5-толил-3-трифторметил-1Н-пиразол-1-ил)бензолсульфонамид,
(V) N-[6-(2,4-дифторфенилтио)-1-оксоиндан-5-ил]метансульфонамид,
(VI) 4-гидрокси-2-метил-N-(5-метилтиазол-2-ил)-2Н-1,2-бензотиазин-3-карбоксамид-1,1-диоксид,
(VII) N-(4-нитро-2-феноксифенил)метансульфонамид,
(VIII) 4-(4-циклогексил-2-метилоксазол-5-ил)-2-фторбензолсульфонамид,
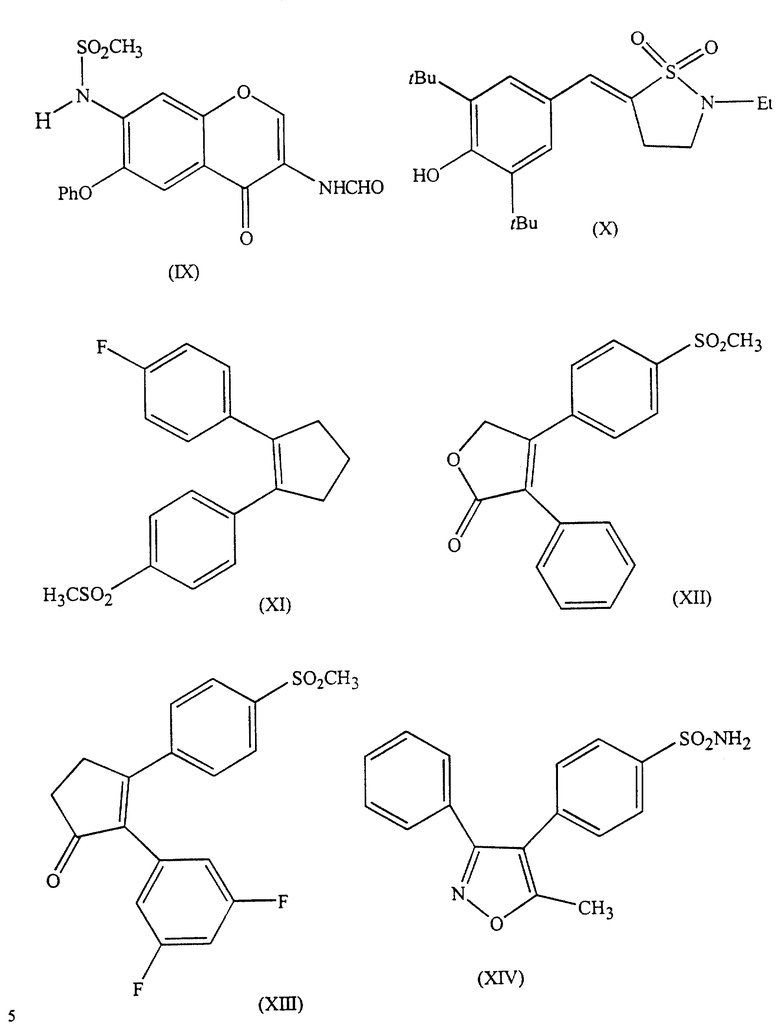
(IX) N-(3-формиламино-4-оксо-6-фенокси-4Н-1-бензопиран-7-ил)метансульфонамид,
(X) (Е)-2-этил-5-(3,5-ди-трет-бутил-4-гидрокси)бензилиден-1,2-изотиазолидин-1,1-диоксид,
(XI) 1-(4-метансульфонилфенил)-2-(4-фторфенил)циклопентен,
(XII) 3-фенил-4-(4-метансульфонилфенил)-5Н-фуран-2-он, и
(XIII) 2-(3,5-дифторфенил)-3-(4-метансульфонилфенил)-2-циклопентен-1-он,
(XIV) 4-[5-метил-3-фенилизоксазол-4-ил)бензолсульфонамид.
Эти соединения раскрыты в WO 95/00501, J. Med. Chem. 40, 1347 (1997), в международной публикации WO 94/13635, Pharmacology 55, 44 (1997), Prostaglandins, 47, 55 (1994), в японской публикации Hei 9-52882, Jpn. J.Pharmacol. , 67, 305 (1995), Inflamm. Res., 47, Suppl. 3, S257 (1997), J. Med. Chem., 38, 4570 (1995), ЕР 863134, US 5474995 или WO 98/06708, которые включены сюда в качестве ссылки.
Так как соединения настоящего изобретения обладают превосходной активностью в отношении профилактики или ингибирования кахексии и очень низкой токсичностью, их можно использовать в качестве профилактических и терапевтических агентов при кахексии. Их можно использовать для лечения связанных с опухолями нарушений и для ингибирования роста и/или метастаз опухолей.
Более того, при желании одно или более соединений настоящего изобретения [т. е. соединения формул (I)-(XIV) включительно] можно использовать вместе с одним или более другими агентами для профилактики или ингибирования роста опухолей, и соединения настоящего изобретения и другие агенты можно вводить одновременно, раздельно или последовательно.
Другой противоопухолевый агент предпочтительно выбирают из группы, состоящей из 5-фторурацила, цисплатина, тамоксифена, паклитаксела, доцетаксела и иринотекана. Особенно в случае одновременного введения соединение формулы (I) или (II) или их фармацевтически приемлемые соли и другой противоопухолевый агент могут быть включены в одну композицию.
Композиция настоящего изобретения может быть в любой удобной форме в зависимости от способа введения. Так, например, для перорального введения она может быть в форме таблеток, капсул, гранул, порошков или сиропов. Для неперорального введения она может быть в форме суппозиториев или препаратов для инъекций. Композиции получают в соответствии с известными способами, и они могут включать такие хорошо известные специалистам добавки, как, например, эксципиенты (например, органические эксципиенты, включая производные сахаров, таких как лактоза, сахароза, глюкоза, маннит и сорбит; производные крахмала, такого как кукурузный крахмал, картофельный крахмал, α-крахмал и декстрин; производные целлюлозы, такие как кристаллическая целлюлоза; гуммиарабик; декстран; и Пуллулан (Pullulan), неорганические эксципиенты, включая производные силиката, такие как легкий ангидрид кремниевой кислоты, синтетический алюмосиликат, силикат кальция и метааталюмосиликат магния; фосфаты, такие, как гидрофосфат кальция; карбонаты, такие как карбонат кальция; и сульфаты, такие как сульфат кальция), смазывающие агенты (например, стеариновую кислоту и ее соли металлов, включая стеариновую кислоту, стеарат кальция и стеарат магния; тальк, коллоидную двуокись кремния; воска, такие как пчелиный воск и спермацет; борную кислоту; адипиновую кислоту; такие сульфаты, как сульфат натрия; гликоль; фумаровую кислоту; бензоат натрия; DL-лейцин, натриевые соли жирных кислот; лаурилсульфаты, такие как натрийлаурилсульфат и магнийлаурилсульфат; кремниевую кислоту, например ангидрид кремниевой кислоты и гидрат кремниевой кислоты; и вышеуказанные производные крахмала), связывающие агенты (например, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, поливинилпирролидон, Макрогол (Macrool) и соединения, аналогичные вышеуказанным эксципиентам), разрыхляющие агенты, (например, производные целлюлозы, такие как гидроксипропилцеллюлоза с низкой степенью замещения, карбоксиметилцеллюлоза, кальцийкарбоксиметилцеллюлоза, натрийкарбоксиметилцеллюлоза с внутренними мостиками; химически модифицированные крахмал-целлюлозы, такие как карбоксиметилкрахмал, натрийкарбоксиметилкрахмал и поливинилпирролидон с мостиками), стабилизаторы (например, параоксибензоаты, такие как метилпарабен и пропилпарабен; спирты, такие как хлорбутанол, бензиловый спирт и фенилэтиловый спирт; бензалконийхлорид; фонолы, такие как фенол и крезол; тимеросал; дегидроуксусная кислота и сорбиновая кислота), корригенты (например, подслащивающие агенты, уксус и отдушки) и разбавители.
Дозы варьируются в зависимости от многих факторов, включая состояние и возраст пациента, тяжесть и природу нарушения, а также способ введения. Так например, в случае перорального введения желательно вводить 0,01 мг/кг (предпочтительно 0,1 мг/кг) в качестве нижнего предела и 50 мг/кг (предпочтительно 10 мг/кг) в качестве верхнего предела для взрослого пациента в день в виде одной дозы или в виде нескольких разделенных доз в зависимости от симптомов. В случае внутривенного введения желательно вводить 0,001 мг/кг (предпочтительно 0,01 мг/кг) в качестве нижнего предела и 10 мг/кг (предпочтительно 5 мг/кг) в качестве верхнего предела для взрослых пациентов в виде одной дозы или в виде разделенных доз в зависимости от симптомов.
Далее настоящее изобретение иллюстрируется следующими неограничивающими примерами и примерами препаративных форм.
ПРИМЕР 1
Тестирование действия против кахексии на мышах, имеющих клетки мышиного рака ободочной кишки Colon 26
В качестве тестируемых животных использовали мышей штамма CDF1 (самки, 8 недель). Их использовали группами по 10 для каждого теста. Каждому животному подкожно трансплантировали 1•106 клеток мышиного рака ободочной кишки Colon 26.
В качестве тестируемых соединений использовали соединения 1-94 и 2-78, представленные в таблицах 1 и 2 соответственно и имеющие формулы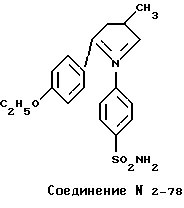
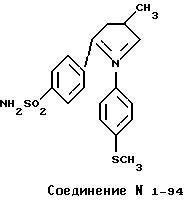
Каждое тестируемое соединение суспендируют в стерилизованной дистиллированной воде, содержащей 0,5% вес/объем карбоксиметилцеллюлозы (CMC), и его вводят перорально один раз в день, начиная со дня трансплантации раковых клеток.
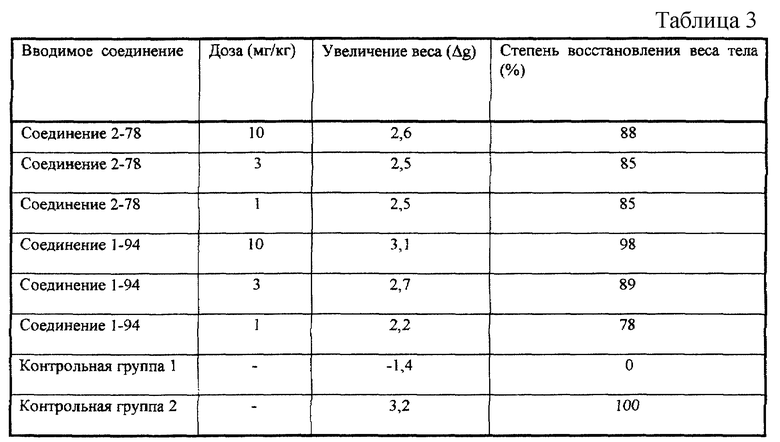
Каждое тестируемое животное взвешивают немедленно после трансплантации опухолевых клеток и вес (А г) регистрируют. Затем каждое животное взвешивают на 19 день после трансплантации опухолевых клеток, и вес (В г) регистрируют. Увеличение веса на 19 день после трансплантации раковых клеток рассчитывают как B-A=Δgt для тестируемых животных. Эксперимент повторяют для двух контрольных групп: первой контрольной группе (контрольная группа 1) трансплантируют опухолевые клетки, но не обрабатывают ни одним из тестируемых соединений и увеличение веса обозначают как Δgc1; второй контрольной группе (контрольная группа 2) не трансплантируют опухолевые клетки и не обрабатывают никакими тестируемыми соединениями, а увеличение веса обозначают как Δgc2. Степень восстановления веса тела определяют в соответствии со следующей формулой, основанной на увеличении веса на 19 день после трансплантации опухолевых клеток, и это значение используют как показатель антикахексиального действия.
Степень восстановления веса тела (%) = (Δgt-Δgc1)/(Δgc2-Δgc1)×100.
Результаты приведены в таблице 4.
Из приведенных результатов очевидно, что эти соединения ингибируют у мышей кахексию, связанную с опухолью, и снижают потерю веса.
ПРИМЕР 2
Тест на действие против кахексии у мышей, имеющих клетки мышиного рака ободочной кишки Colon 26
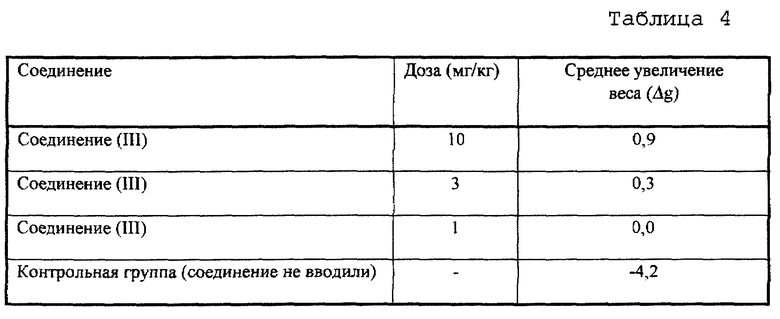
Повторяют методику примера 1, но используют соединение формулы (III) в качестве тестируемого соединения и сравнивают увеличение веса (Δgt) тестируемой группы животных, которой вводят соединение формулы (III), с увеличением веса контрольной группы (Δgc), которой были трансплантированы опухолевые клетки, но не введено противоопухолевое соединение. В качестве тестовых животных используют самок мышей штамма CDF1 в возрасте 16 недель. Увеличение веса определяют через 22 дня после трансплантации опухолевых клеток. Средний вес тела животных в каждой группе сразу после трансплантации опухолевых клеток составляет от 25 до 26 г. Результаты приведены в таблице 4.
Из представленных результатов ясно видно, что соединение формулы (III) ингибирует связанную с опухолью кахексию у мышей и снижает потерю веса.
ПРИМЕР 3
Тест на действие против кахексии у мышей, имеющих клетки мышиного рака ободочной кишки Colon 26
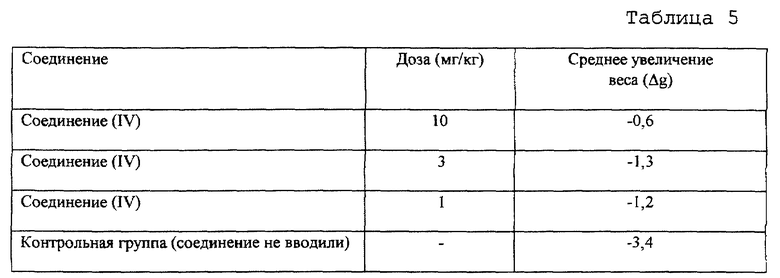
Повторяют методику примера 2, но в качестве тестируемого соединения используют соединение формулы (IV) и сравнивают увеличение веса (Δgt) в тестируемой группе животных, которым вводят соединение формулы (IV), с увеличением веса в контрольной группе животных (Δgc), которым трансплантируют опухолевые клетки, но которым не вводят противоопухолевое соединение. В качестве тестируемых животных используют самок мышей штамма CDF1 в возрасте 7 недель. Увеличение веса измеряют через 15 дней после трансплантации опухолевых клеток. Средний вес животных в каждой группе сразу после трансплантации опухолевых клеток составлял от 20 до 21 г. Полученные результаты приведены в таблице 5.
Из представленных результатов совершенно ясно, что соединение формулы (IV) ингибирует связанную с опухолью кахексию у мышей и снижает потери веса.
ПРИМЕР 4
Тест на действие против кахексии у мышей, имеющих клетки мышиного рака ободочной кишки Colon 26
Тестируемые соединения (соединения формул (V), (IV), (VII), (VIII), (IX), (X), (XI), (XII), (XIII) и (XIV)) вводят по схеме, описанной в примере 2. Эти соединения ингибируют кахексию у мышей, связанную с опухолью и уменьшают потери среднего веса тела.
ПРИМЕР 5
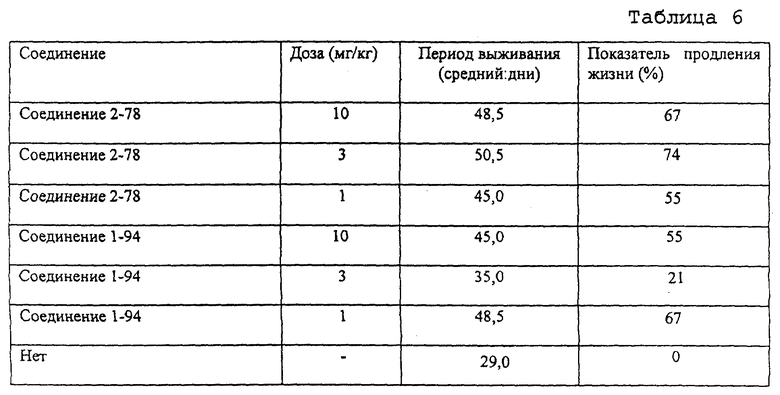
Тест на активность в отношении продления срока жизни
Наблюдения за мышами, использованными в примере 1, продолжают. Определяют показатель продления срока жизни на основании числа дней, в течение которых мышь выживает, и затем эту величину используют как показатель действия, продлевающего срок жизни для тестируемых соединений. Следует заметить, что в случае группы мышей, обработанных тестируемым соединением, пероральное введение соответствующего соединения один раз в день продолжают на 20 день после трансплантации опухолевых клеток, а также после этого.
Показатель продления срока жизни (%)=(St/Sc-1)(100
St - средняя величина времени выживания (дни) для группы мышей, обработанных тестируемым соединением.
Sc - средняя величина времени выживания (дни) для контрольной группы мышей, которым не трансплантировали опухолевые клетки.
Полученные результаты представлены в таблице 6.
Как следует из данных таблицы 6, соединения настоящего изобретения демонстрируют заметное действие в отношении продления жизни.
ПРИМЕР 6
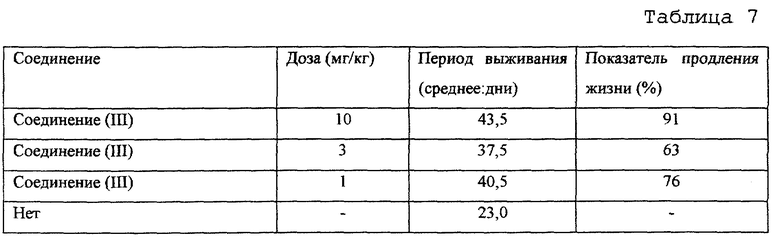
Тест на активность в отношении продления срока жизни
Повторяют эксперимент, описанный в примере 5, с животными, использованными в примере 2. В случае группы мышей, обработанных тестируемым соединением, пероральное введение соответствующего соединения один раз в день продолжают на 23 день после трансплантации опухолевых клеток и также после этого. Полученные результаты приведены в таблице 7.
ПРИМЕР 7
Тест на активность в отношении продления срока жизни
Повторяют эксперимент, описанный в примере 5, с животными, использованными в примерах 3 и 4. Соединения формул (IV), (V), (VI), (VII), (VIII), (IX), (X), (XI), (XII), (XIII) и (XIV) все ингибируют у мышей кахексию, связанную с опухолью, и демонстрируют заметное продление срока жизни.
ПРИМЕР 8
Тест с одновременным использованием противоопухолевого агента
Клетки мышиного рака ободочной кишки трансплантируют CDF1 мышам таким же образом, как в примере 1, с последующим введением тестируемых соединений (соединения 2-78 и 1-94) и соединений формул (III), (IV), (V), (VI), (VII), (VIII), (IX), (X), (XI), (XII), (XIII) и (XIV) и противоопухолевого агента (5-фторурацил или цисплатин).
Одновременное использование одного из соединений настоящего изобретения и противоопухолевого агента заметно ингибирует рост опухоли и кахексию, демонстрируя значительное действие в отношении продления срока жизни.
ПРИМЕР 9
Ингибирующее действие в отношении легочных метастаз клеток мышиной злокачественной меланомы B16-BL6
Группам мышей, каждая из которых включает десять мышей штамма C57BL/6 (самки, возраст 8 недель) трансплантируют внутривенно в хвостовую вену 3•104 клеток мышиной злокачественной меланомы B16-BL6.
Мышам при необходимости вводят внутривенно в хвостовую вену бактериальный липополисахарид (LPS) в количестве 3 мкг каждой за 1 час до трансплантации клеток меланомы с тем, чтобы ускорить образование в легких метастаз меланомы. [M. J. Anasagasti et al., J. Natl. Cancer Research, 89, 645-651 (1997)].
В качестве тестируемых соединений используют соединение 2-118, соединение формулы (IV), соединение формулы (V) и индометацин и каждый суспендируют в дистиллированной воде, содержащей 0,5 вес/об % карбоксиметилцеллюлозы (CMC), и эту суспензию вводят перорально в дозе 1 мг/кг/день в течение 5 дней, начиная со дня трансплантации клеток меланомы.
Соединение 2-118 является 2-(3,4-диметилфенил)-4-метил-1-(4-сульфамоилфенил)пирролом.
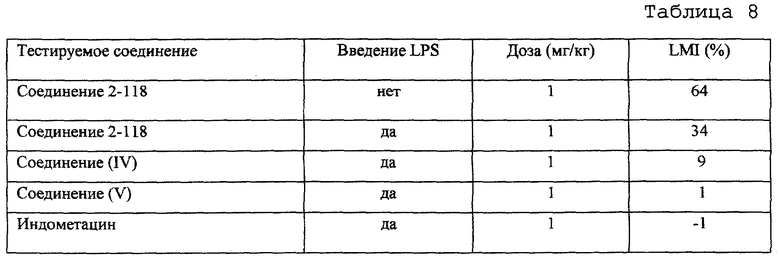
Ингибирующие активности в отношении легочных метастаз клеток меланомы оценивают в единицах степени ингибирования метастаз в легких (LMI%), подсчитывая количество колоний метастаз в легких на 10 день после внутривенной трансплантации клеток мышиной злокачественной меланомы B16-BL6 в хвостовую вену.
LMI(%)=(l-Nt/Nc)•100
Nt - количество колоний метастаз в легких на 10 день в группе мышей, которым ввели тестируемые соединения; и
Nc - количество колоний метастаз в легких на 10 день в группе мышей, которым не вводили тестируемые соединения. Полученные результаты представлены в таблице 8.
Из данных таблицы 8 очевидно, что соединения настоящего изобретения успешно ингибируют легочные метастазы клеток злокачественной мышиной меланомы B16-BL6 независимо от того, ускоряется или нет образование метастаз в легких за счет введения LPS (индуцирование воспалительной реакции).
В частности, соединение настоящего изобретения демонстрирует заметное ингибирование метастаз в легких, хотя соединение формулы (IV) и соединение формулы (V), которые являются СОХ-2-селективными ингибиторами, и индометацин, который является типичным NSAID, не проявляют такой ингибирующей активности в условиях, ускоряющих образование метастаз в легких индуцированном воспалительной реакции (что отражает ускорение образования метастаз опухоли при хирургическом удалении опухоли).
ПРИМЕР 10
Противоопухолевое действие в отношении клеток мышиной саркомы S-180
1•106 Клеток мышиной саркомы S-180 трансплантируют подкожно голым мышам штамма Ва1b/с (самки, возраст 8 недель) в группах по 10 мышей в каждой.
Тестируемое соединение, соединение 2-118, суспендируют в стерилизованной дистиллированной воде, содержащей 0,5% вес/об кароксиметилцеллюлозы (CMC), и вводят перорально один раз в день в течение 5 дней, начиная со дня трансплантации опухолевых клеток.
Противоопухолевую активность оценивают в соответствии со следующим уравнением для определения степени ингибирования роста опухоли (GI%) на 7 день после трансплантации
GI(%)=(l-Vt/Vс)•100
Vt - средний объем опухоли на 7 день в группе мышей, которым вводили тестируемое соединение.
Vc - средний объем опухоли на 7 день в контрольной группе необработанных мышей.
Объем опухоли определяют как 1/2 г•[длинная ось опухоли]•[короткая ось опухоли]2
Результаты теста приведены в таблице 9.
Из результатов таблицы 9 очевидно, что соединение настоящего изобретения ингибирует рост мышиных опухолевых клеток.
ПРИМЕР 11
Противоопухолевое действие в отношении клеток рака ободочной кишки человека КМ12-НХ
Клетки КМ12-НХ рака ободочной кишки человека ортотопически трансплантируют в слепую кишку голой мыши по способу Fu et al., [X.Fu et al., Anticancer Res., 12(1992)], используя голых мышей штамма Balb/c (самки, возраст 7 недель) в группах по 10 в каждой.
Более конкретно, в левом нижнем абдоминальном участке проводят рассечение у каждой из мышей при анестезии абацином, после чего сбоку к слепой кишке пришивают тонкий срез опухоли размером 5 мм, используя рассасывающиеся хирургические нити, для осуществления ортотопической трансплантации. Разрез зашивают, используя рассасывающиеся хирургические нити, и мышей согревают и соответствующим образом пробуждают от анестезии.
Тестируемое соединение суспендируют в стерилизованной дистиллированной воде, содержащей 0,5% вес/об карбоксиметилцеллюлозы (CMC) и вводят перорально в общем 9 доз, по одной дозе в день, с 3 по 7 дня после трансплантации опухолевых клеток и с 10 до 13 после трансплантации.
Противоопухолевую активность оценивают в соответствии со следующим уравнением для оценки степени ингибирования роста опухоли (GI%) на 14 день после трансплантации.
GI(%)=(l-Vt'/Vc')•100
V't - средний вес опухоли на 14 день в группе мышей, которым вводили тестируемое соединение.
V'c - средний вес опухоли на 14 день у мышей необработанной контрольной группы.
Полученные результаты представлены в таблице 10.
Из данных таблицы 10 очевидно, что соединение настоящего изобретения ингибирует рост клеток рака ободочной кишки человека в месте ортотопической трансплантации.
Далее иллюстрируется получение препаративных форм, содержащих соединения настоящего изобретения, следующими неограничивающими примерами.
ПРИМЕР 12
ПРИМЕР ПРЕПАРАТИВНОЙ ФОРМЫ 1
Капсулы
Смесь соединения настоящего изобретения, такого как соединение формулы (III), соединения 1-94, 2-78 или 2-118, приготавливают в перевариваемой масляной субстанции, такой как соевое масло, хлопковое масло или оливковое масло, и помещают в желатин, используя насос с положительным вытеснением, получая мягкие желатиновые капсулы, содержащие по 100 мг активного ингредиента. Затем полученные капсулы промывают и сушат.
ПРИМЕР 13
ПРИМЕР ПРЕПАРАТИВНОЙ ФОРМЫ 2
Таблетки
Таблетки изготавливают в соответствии с обычными способами, используя 100 мг соединения настоящего изобретения, такого как соединение формулы (III), соединения 1-94, 2-78 или 2-118, 0,2 мг коллоидной двуокиси кремния, 5 мг стеарата магния, 275 мг микрокристаллической целлюлозы, 11 мг крахмала и 98,8 мг лактозы.
В этом случае на таблетки при желании можно нанести покрытие.
ПРИМЕР 14
ПРИМЕР ПРЕПАРАТИВНОЙ ФОРМЫ 3
Инфекции
1,5 мас.% соединения настоящего изобретения, такого как соединение формулы (III), соединение 1-94, 2-78 или 2-118, перемешивают в 10 об.% пропиленгликоля, а затем доводят до постоянного объема, добавляя воду для инъекций, после чего стерилизуют, получая препарат для инъекций.
ПРИМЕР 15
ПРИМЕР ПРЕПАРАТИВНОЙ ФОРМЫ 4
Суспензии
Суспензии приготавливают так, чтобы они содержали 100 мг соединения настоящего изобретения, такого как соединение формулы (III), соединения 1-94, 2-78 или 2-118, которые измельчают до тонкого порошка, 100 мг натрийкарбоксиметилцеллюлозы, 5 мг бензоата натрия, 1,0 г раствора сорбита (Japanese Pharmacopoeia) и 0,025 мл ванилина в 5 мл суспензии.



Изобретение относится к медицине, в частности к онкологии, и касается применения некоторых селективных ингибиторов циклооксигеназы-2 для лечения и профилактики кахексии. Изобретение позволяет существенно ослабить симптомы кахексии, снизить побочные эффекты и дает возможность продолжения лечения противоопухолевыми препаратами. 6 з.п.ф-лы, 10 табл.
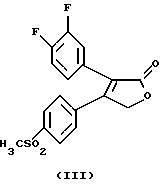
соединения формулы (IV)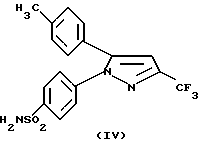
соединения формулы (V)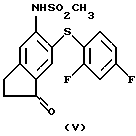
или их фармацевтически приемлемой соли в качестве активного ингредиента для получения лекарственного средства для лечения или профилактики кахексии у млекопитающих.
Приоритет по пунктам и признакам:
21.07.1998. по п. 1, соединения: 2-(3,4-диметилфенил)-4-метил-1-(4-сульфамоилфенил)пиррола, 2-(4-этоксифенил)-4-метил-1-(4-сульфамоилфенил)пиррола, 4-метил-1-(4-метилтиофенил)-2-(4-сульфамоилфенил)пиррола, по пп. 2-4;
24.09.1998 пп.1, 5-7 остальные признаки.
| US 5317019, 31.05.1994 | |||
| US 5208018, 04.05.1993 | |||
| US 5593991, 14.01.1997 | |||
| WO 9413635, 18.02.1997 | |||
| US 5474995, 12.12.1995 | |||
| Устройство для ковки кольцевых поковок | 1979 |
|
SU863134A1 |
| Вихревой пылеуловитель | 1979 |
|
SU799823A2 |
Авторы
Даты
2002-10-10—Публикация
1998-12-23—Подача