Изобретение относится к белкам для новых АТР (АТФ)-чувствительных калиевых каналов (βIR), которые экспрессируются в панкреатических β-клетках и секретирующих инсулин клеточных линиях человеческого и мышиного происхождения, и к генам, кодирующим их, при этом упомянутые белки и гены являются полезными в качестве диагностических и лечебных средств при диабете и т.п. и также при разработке таких средств.
Этиология диабета известна, главным образом, вследствие нарушений секреции инсулина в панкреатических β-клетках. Следовательно, ожидается, что выяснение молекулярного механизма секреции инсулина играет важную роль при выяснении причин диабета и разработке лекарственных препаратов против диабета, но детали такого молекулярного механизма еще не известны.
Выяснено, что АТР-чувствительный калиевый канал (КАТР-канал), присутствуя на клеточной мембране, играет ведущую роль в клеточных функциях, таких как секреция и мышечные сокращения, посредством конъюгирования состояния метаболизма в клетках с мембранным потенциалом. Например, в 1983 подтверждено, что КАТР-канал присутствует в сердечной мышце [Noma, A., Nature 305: 147 (1983)] , в панкреатических β-клетках [Cook, D.L. et al., Nature 311: 271 (1984), Misler, S. et al., Proc. Natl, Acad. Sci. U.S.A. 83: 7119 (1986)] , гипофизе [Bernardi, H. et al., Proc. Natl. Acad. Sci. U.S.A., 90: 1340 (1993)] , скелетных мышцах [Spruce, A. E. et al., Nature, 316: 736 (1985)] и т.п.
В частности, в панкреатических β-клетках АТР, образовавшийся при метаболизме глюкозы, является причиной притока ионов из кальциевого канала благодаря запиранию КАТР-канала, что вызывает деполяризацию, приводящую в результате к секреции инсулина. Из этого очевидно, что КАТР-канал играет ведущую роль в регуляции секреции инсулина.
КАТР -канал принадлежит к семейству калиевых каналов, проявляющих электрофизиологически внутреннюю ректификацию, на основании чего семейство калиевых каналов, проявляющих внутреннюю ректификацию, подразделяют на пять подсемейств (ROMK1, IRK1, GIR1 и с КАТР-1 и uКАТР-1), основываясь на степени идентичности аминокислотной последовательности.
Несмотря на это, молекулярное строение КАТР-канала в панкреатических β-клетках не выяснено. Авторы настоящего изобретения обнаружили, что uКАТР-1, который является убиквитарным в различных тканях, экспрессируется в нормальных тканях, включая панкреатические β-клетки, но не экспрессируется в секретирующей инсулин клеточной линии.
С учетом вышесказанного автора настоящего изобретения исследовали калиевый канал, который должен специфично экспрессироваться в панкреатических β-клетках и в инсулин-секректирующей клеточной линии.
Белковая структура нового АТР-чувствительного калиевого канала, который специфически экспрессируется в панкреатических β-клетках, еще не выяснена в подробностях, хотя отсутствуют сведения об образовании комплексов с другими белками, например с новым калиевым каналом (uKATР-1), являющимся убиквитарным в тканях, и с сульфонилмочевиной, связывающей белок.
Чтобы осуществить выделение, идентификацию и функциональный анализ нового КАТР-канала, требуются весьма сложные методы, такие как методы молекулярной биологии, клеточной биологии и электрофизиологические методы.
Поскольку это так, авторы настоящего изобретения широко и всесторонне использовали такие методы, чтобы выделить геномы человека и мыши, кодирующие изоформу нового КАТР-канала (βIR), экспрессированного в панкреатических β-клетках и секретирующих инсулин в клеточных линиях человека и крысы, и кДНК, и также идентифицировать их аминокислотные последовательности (см. фиг. 1, 2, 3 и 4). После экспрессии идентифицированного белка βIR-канала в ооците Xenopus и в клеточных линиях млекопитающих, электрофизилогический анализ показал, что βIR-канал представляет собой АТР-чувствительный канал, проявляющий внутреннюю ректификацию.
Белки настоящего изобретения представляют собой новые АТР-чувствительные калиевые каналы (βIR), которые специфически экспрессируются в панкреатических β-клетках и инсулинсекретирующих клетках млекопитающих, и представляют собой изоформу нового АТР-чувствительного калиевого канала uКАТР-1, убиквитарно присутствующего и экспрессированного в различных тканях.
Настоящее изобретение охватывает аминокислотные последовательности для таких белков, последовательности оснований кодирующей ДНК, плазмиду, имеющую такие включенные последовательности, и, кроме того, рекомбинантные клетки (трансформанты), имеющие такую включенную плазмиду. Кроме того, настоящее изобретение охватывает изолированные βIR-гены и белки и их рекомбинантные белки, родственные им вещества, такие как агонисты и антагонисты, и лекарственные композиции, включающие диагностические и лекарственные средства для генотерапии.
Специфические к панкреатическим β-клеткам hβIR человеческого происхождения и mβIR, происходящий от мыши, состоят из 390 аминокислотных остатков [включая Met (инициирующий кодон АТG)] с молекулярной массой 43512 дальтон и 43559 дальтон соответственно, при этом они показывают 96% идентичность аминокислотной последовательности. Кроме того, βIR, происходящие от человека и крысы, обнаруживают 98%-ную идентичность аминокислотной последовательности с uКАТР-1 мышиного происхождения, а также 46%, 41%, 42% и 44.5% идентичность аминокислотной последовательности по отдельности с другими калиевыми каналами - IRK1, ROMK1, GIRK1 и с КАТР- 1, что указывает на то, что βIR, принадлежащие к одному и тому же подсемейству, такому как uКАТР-1, являются изоформой.
Кроме того, подтверждается, что вместо мотива Gly-Tyr-Gly (аминокислоты 132-134), сохраненного в пористой части (сегмент Н5) идентифицированных в настоящее время калиевых каналов внутренней ректификации, в βIR настоящего изобретения, как и в uКАТР-1, сохраняется общий мотив Gly-Phe-Gly.
Что касается аспартата (Asn), который является ключевой детерминантой для калиевых каналов с внутренней ректификацией, то uКАТР-1 имеет Asn-163, и βIR имеет Asn-153 во втором трансмембранном сегменте соответственно. βIR показывает высокую гомологию с uКАТР-1, но не существует внутриклеточного подобия между областями аминоконцов и карбоксильных концов и порообразующим сегментов (Н5). Во внутриклеточных областях βIR человеческого и мышиного происхождения существует два потенциальных сайта фосфорилирования протеинкиназы, зависящего от сАМР (Thr-224 и Ser-372), и пять сайтов фосфорилирования, зависящего от протеинкиназы с (Ser-3, Ser-37, Thr-336, Thr-345 и Ser-363) а также три потенциальных сайта фосфорилирования, зависящего от казеинкиназы-II (The-62, Thr-224 и Ser-354), при отсутствии N-связанного сайта гликозилирования во внеклеточной области.
Блоттинг-исследования РНК показали, что мРНК βIR экспрессируется с высоким уровнем частоты в панкреатических β-клетках и инсулин-секретирующей клеточной линии, но с низким уровнем в таких тканях, как сердце, скелетные мышцы и мозг. Кроме того, чтобы исследовать функциональные свойства βIR-канала, hβIR и mβIR экспрессируют в ооцитах Xenopus laevis.
У человека и у мыши экспрессируется синтезированная in vitro кРНК, что приводит к существенно возросшему притоку калиевого канала внутренней ректификации по сравнению с контрольной обработкой путем инъекции воды.
Как описано выше, βIR показывает высокую гомологию с uКАТР-1, и его мРНК экспрессируется в заметной степени в панкреатических β-клетках и инсулин-секретирующей клеточной линии, увеличивая, таким образом, вероятность того, что βIR может представлять собой основные АТР-чувствительные калиевые каналы в панкреатических β-клетках. При исследованиях по настоящему изобретению обнаружено, что βIR ингибируется сульфонилмочевинными лекарственными препаратами, которые в настоящее время широко применяются в качестве лечебных средств при диабете, что вносит вклад в осознание значения βIR в панкреатических β-клетках.
В частности, коэкспрессия βIR и сульфонилмочевинного рецептора показывает, что канал (βIR) проявляет АТР-чувствительность, причем его активность, в то же время, ингибируется сульфонилмочевинными лекарственными препаратами.
Следовательно, предполагается, что βIR и сульфонилмочевинный рецептор объединяются с образованием комплекса in vivo для раскрытия функции.
ДНК новых hβIR и mβIR по настоящему изобретению получают из библиотеки кДНК и геномной библиотеки. Геномные гены hβIR и rβIR характеризуются отсутствием интрона и локализуются на хромосоме 11р15.1.
Геном ДНК hβIR и rβIR также может быть получен путем зондирования геномных библиотек с использованием их кДНК и их фрагментов.
Выделенная ДНК hβIR, для получения мутантов, может быть легко подвергнута делеции, инсерции и замещению известными методами.
Например, мотив, который характерен для пористого сегмента βIR, может быть удален или замещен другой аминокислотой, и получен гомолог βIR. Гомолог, имеющий утраченный мотив, способен связываться с сульфонилмочевинным лекарственным средством, но не обладает функцией канала. Существует возможность давать гомолог βIR в качестве нейтрализующего средства пациенту с диабетом, который получил избыток сульфонилмочевинного лекарственного средства. Кроме того, возможно получить белок калиевого канала, проявляющий более сильную внутреннюю ректификацию, путем замещения мотивного сегмента βIR.
Выяснение аминокислотной последовательности βIR облегчает разработку более эффективного, но менее токсичного ингибитора βIR. Настоящее изобретение охватывает получение мутантов βIR и их агонистов и антагонистов.
Кроме того, используя известные технические приемы, легко присоединить нуклеотидные последовательности, кодирующие другие белки и синтетические пептиды, к ДНК hβIR или мутантам его ДНК по аминоконцу или по карбоксильному концу и получить посредством этого слитые белки, а именно производные βIR. Например, такие слитые белки получают в форме белка-предшественника и подвергают расщеплению in vivo или in vitro, чтобы обнаружить их функции. В дополнение к их изначально присущей функции слитым белкам можно придать свойства направленности на ткань или мембранной ориентации. В таком случае имеется в виду, что в объем изобретения входят связывающие сахара аминокислоты в таких слитых белках для образования с их помощью новой сахарной связи, обеспечивающей свойство ткань/мембранной ориентации. Настоящее изобретение также включает получение слитых белков, содержащих βIR.
Получение мутантов или производных βIR основано на использовании метода, хорошо известного как метод частично специфичной мутации [Adelman et al., DNA, 2: 183 (1983)].
Чтобы получить hβIR и mβIR, их мутанты и их производные в большом количестве, получают на основе известных методов воспроизводимые рекомбинантные плазмиды, кодирующие такие ДНК, и затем используют такие плазмиды для получения трансформированных клеток с последующим культивированием таких клеток-хозяев, при этом такие клетки-хозяева включают клетки микроорганизмов, дрожжей и животных.
Для клонирования дезоксирибонуклеотидов подходят прокариоты, такие как бактерин. Например, плазмида рВR322, полученная из E. соli, содержит ген, резистентный к ампициллину и тетрациклину, и может обеспечить практические средства идентификации трансформированных клеток. Кроме того, микробные плазмиды содержат промотор, который применим для экспрессии их собственных белков. Кроме прокариотов могут хорошо работать эукариоты, такие как дрожжи.
В частности при экспрессии в дрожжах вида Saccharomyces обычно используют плазмиду YRp7 [Steinchomb et al., Nature, 282: 39 (1979)).
Клетки животных также используют в качестве клеток-хозяев, и, в частности, проста для применения и является обычным способом инкубация клеток позвонков [Krause and Paterson, Tissue Culture, Academic Press (1973)]. В качестве клеточных линий упоминаются АlT-20, клетки HeLa, яичника китайского хомячка (СНО), СОМSM6, СOS-7 и т.п. Для регуляции функций плазмиды экспрессии в таких клеточных линиях используют промоторы полиомавируса, аденовируса 2, цитомегаловируса и ОВ-40, при этом рсMV представляет собой плазмиду, которая находит широкое применение в системах экспрессии клеток животных [Thomsen et al., PNAS, 81: 659 (1984)].
Последовательности ДНК для канального белка и hβIR и mβIR в соответствии с настоящим изобретением начинаются с инициирования кодона "АТG". В случаях, когда для синтеза такого канального белка используют рекомбинантные клетки, нет необходимости добавлять АTG к нужной ДНК, что делает манипуляцию легкой. В результате, когда βIR экспрессируется в прокариоте, трансформированном Е. соli, как правило, синтезируется белок с аминокислотной последовательностью, начинающейся c Met. N-Концевой Met полученного в результате белка может быть элиминирован в зависимости от цели применения.
В случаях, когда βIR синтезируют в рекомбинантных клетках животных, аналогично, биосинтезируется белок βIR (1-390), содержащий Met на N-конце, или белок βIR (2-390), имеющий элиминированный Меt на N-конце, и оба белка пригодны для отдельно обозначенных целей применения.
hβIR и его фрагменты могут быть введены животным с целью их иммунизации, чтобы посредством этого получить антитела. Иммунизация животных также позволяет продуцировать антитело из клеток, секретирующих нужное антитело.
Стало легко получать hβIR в больших количествах, что обеспечивает, таким образом, лучшее понимание того же процесса на молекулярном уровне. Соответственно, объяснение hβIR и его мутантов или аналогов увеличивает возможность разработка реагентов для исследования, диагностики или лечения, главным образом, при диабете.
Между прочим, βIR-белки являются пригодными для диагностики и лечения. А именно, такие белки могут быть использованы в методам исследования в веществе, которое вызывает агонистическое или антагонистическое действие βIR. Путем экспрессии βIR, например, в клетках животных можно проанализировать и проверить вещество, действующее как промотор или ингибитор его активности [Kayano, T. et al., J. Biоl. Chem. 265: 13276 (1990), Example 4].
Кроме того, получена подходящая информация о ДНК-последовательностях βIR, облегчающая получение дезоксибинуклеотидов для неполных последовательностей. Такие относительно короткие ДНК-последовательности обладают способностью к гибридизации с геном, который выбирается, и могут найти
применение в качестве зондов для нуклеиновых кислот. Для целей исследования гибридизации доступны известные методы, такие как соответствующее мечение с использованием в качестве меток радиоактивных веществ или ферментов, и зонды являются эффективными для детекции комплементарных ДНК в различных тканях.
Соответственно, зонды, полученные с использованием βIR, могут использоваться для продуцирования нуклеиновых кислот, способных к гибридизации с различными организмами и их тканями. Полученные в результате нуклеиновые кислоты могут быть такими же, как βIR или его изоформа или его аналоги, в то время как полученные зонды применимы при генной диагностике пациентов: у пациента для определения пораженного гена может быть проведено исследование нуклеотидных последовательностей, гибридизованных с таким зондом.
Прежде в качестве лечебного средства против диабета применялся блокатор (сульфонилмочевина) калиевого канала, и hβIR и его мутанты, производные и моноклональные тела к ним, так же, как и их агонисты, могут быть переработаны в фармацевтические препараты для получения лекарственных средств против диабета, в то время как в случае функциональной недостаточности самого hβIR они могут быть использованы в заместительной терапии, чтобы таким образом восполнить недостающую функцию.
Ген для hβIR, после того как он трансфецирован в векторе или исходных клетках, может вводиться людям, нуждающимся в лекарственном средстве для генотерапии.
Ниже приводятся примеры для более детальной иллюстрации настоящего изобретения со ссылками на прилагаемые чертежи.
На прилагаемых чертежах изображается следующее.
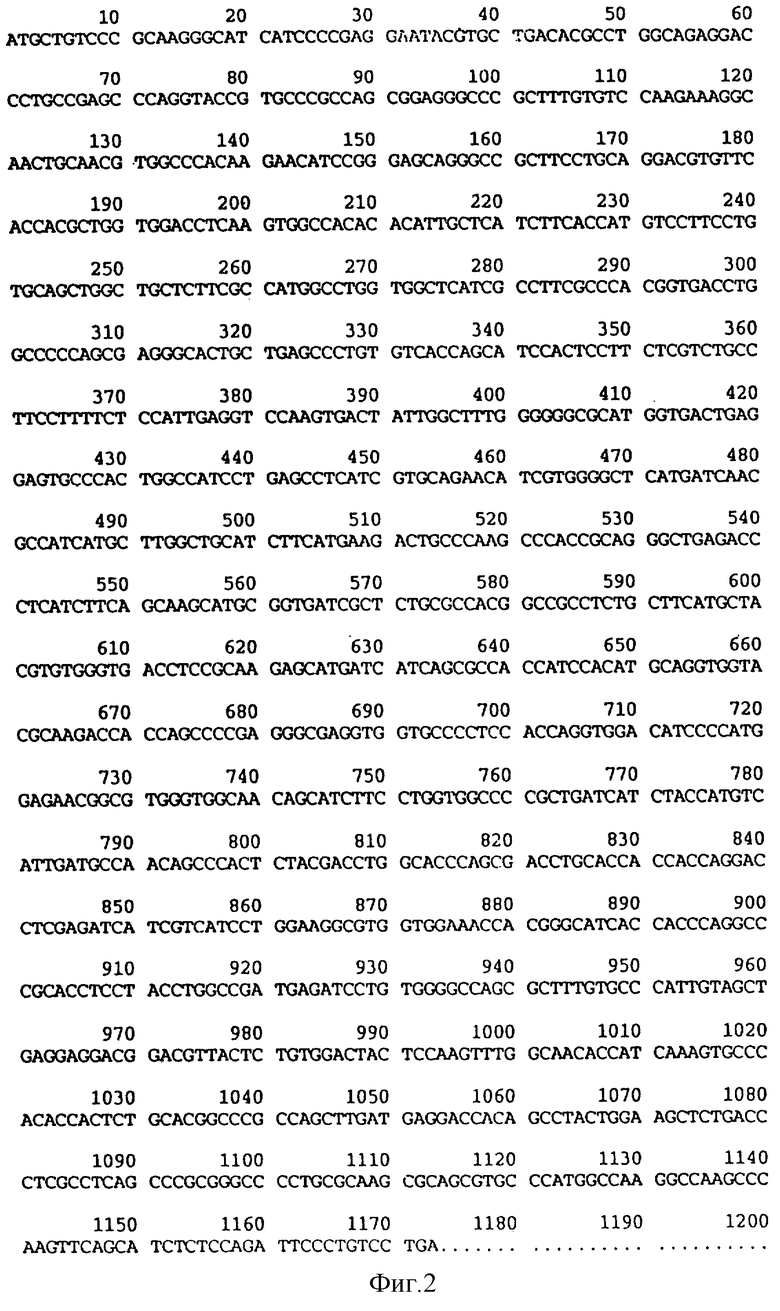
На фиг. 1 приводятся аминокислотные последовательности, соответствующие последовательностям оснований, показанным на фиг.2.
На фиг.2 приводится дезоксирибонуклеотидная последовательность βIR человеческого происхождения, полученного в примере 3.
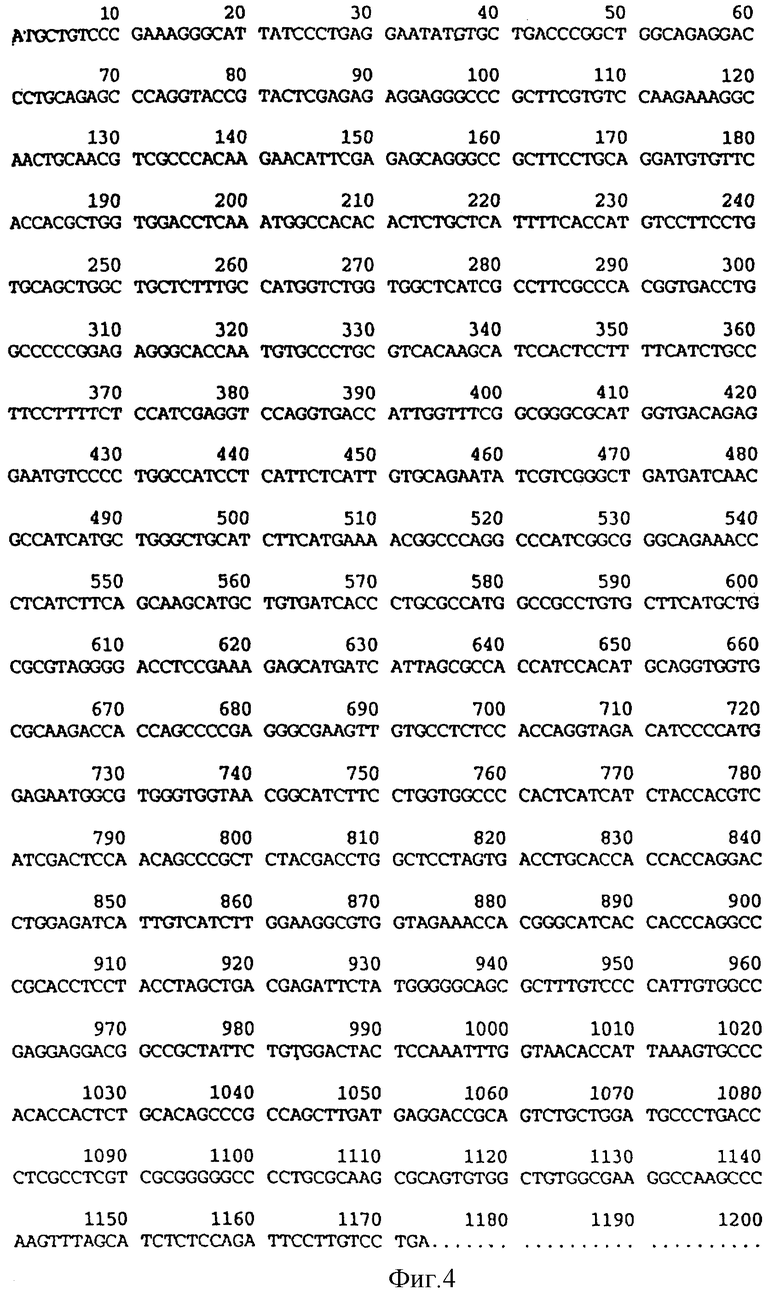
На фиг.3 дается аминокислотная последовательность, соответствующая дезоксирибонуклеотиду, изображенному на фиг.4.
На фиг.4 приводится дезоксирибонуклеотидная последовательность mβIR мышиного происхождения.
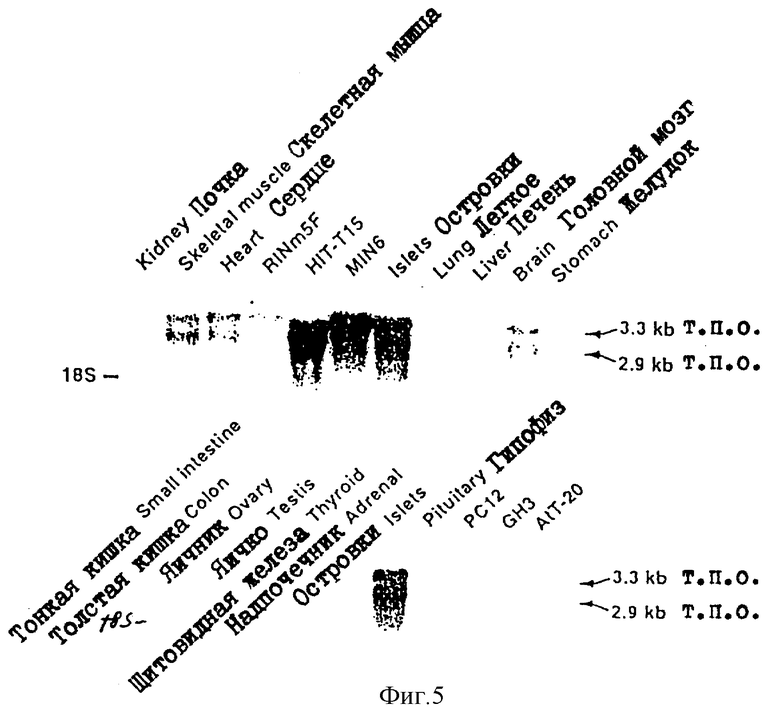
На фиг.5 приводятся результаты РНК-блоттинг-анализа мРНК βIR в различных тканях крысы, который описывается в примере 2.
На фиг.6 изображаются последовательности праймеров ПЦР (РСR), использованных в амплифицирующих субрайонах гена βIR человеческого происхождения, как описано в примере 3, со всеми праймер-последовательностями, показанными в направлении от 5'-конца к 3'-концу.
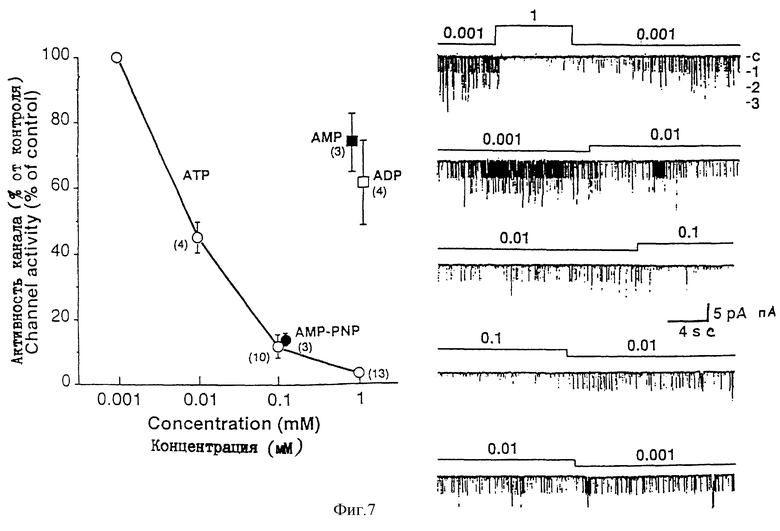
На фиг. 7 приводится АТР-чувствительность βIR-канала в соответствии с примером 4.
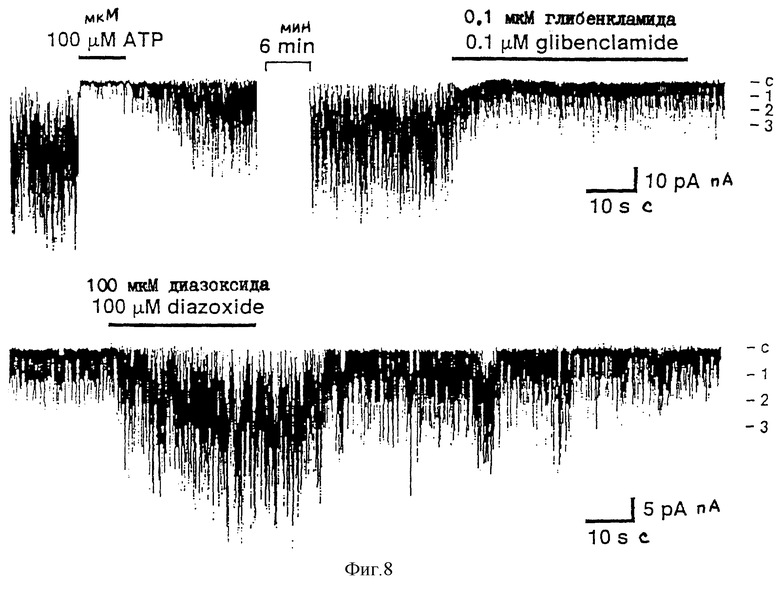
На фиг. 8 иллюстрируется ингибирование активности βIR-канала сульфонилмочевинным лекарственным средством (глибенкламидом), которое наблюдают в примере 4.
Пример 1
кДНК βIR-1 человеческого происхождения и клонирование гена
Принимая во внимание хорошо известный факт, что ген, кодирующий калиевый канал внутренней ректификации, утратил его интрон, выполняют скрининг пятна 7•105 γFIXXII геномной библиотеки человека. В качестве зонда используют кДНК крысиного uКАТР-1 полной длины, помеченную заР, при стандартных условиях гибридизации.
Гибридизационную подложку обрабатывают путем промывания 2•SSC/0,1% SDS при 42oС в течение 30 минут.
Используя в качестве зонда фрагмент ДНК человеческого βIR, меченной 32Р, проводят скрининг линии крысиных инсулинсекретирующих клеток при стандартных условиях гибридизации.
Гибридизационную подложку обрабатывают путем промывания 0,1•SSC/0,1% SDS при 50oС в течение 1 часа.
Две последовательности ДНК-цепей человеческого и мышиного происхождения идентифицируют методом терминации цепи дидезоксинуклеотида после субклонирования фрагментов соответствующей ДНК соответствующей длины в M13 mp18, mp19 и рGEМ3Z.
Пример 2
Блоттинг-анализ ДНК
По 20 мкг РНК, экстрагированных из разных тканей, за исключением гипофиза и щитовидной железы, из которых экстрагируют по 10 мкг РНК, денатурируют формальдегидом, подвергают электрофорезу в 1% агарозном геле и переносят на нейлоновую мембрану. Проводят гибридизацию, используя в качестве зонда меченную 32P ДНК hβIR/мРНК βIR в панкреатических β-клетках и секретирующей инсулин клеточной линии, а именно в MIN6 и НITT-15 соответственно экспрессируют с исключительно высоким уровнем (см. фиг.5).
Пример 4
PCR-SSCP и ДНК-последовательность
Геномную ДНК, собранную у двадцати здоровых японцев, подвергают РСR-SSCP-анализу.
Используют шесть пар меченных Су-5 олигонуклеотидов для усиления кодирующей белок области гена hβIR-1 человеческого происхождения (см. фиг.6).
ПЦР осуществляют в 10 мкл раствора, содержащего 0,1 мкг геномной ДНК, 10 пикомоль смыслового и антисмыслового праймеров, 10 нмоль/л КСl, 20 ммоль/л трис-НСl (рН 8,2), 2,0 ммоль/л MgCl2, 6 нмоль/л (NH4)aSO4, 0,1% тритона Х-100, 0,01% бычьего сывороточного альбумина, 200 мкмоль каждого дНТФ (dNTP) и 0,25 Е (U) БОЕ (Pfu) ДНК-полимеразы.
После первой денатурационной обработки при 94oС в течение 3 минут образцу дают возможность расти в 40 циклах в ПЦР-системе Gene Amp 9600 с последующими денатурацией при 94oС в течение 30 секунд, отжигом при 65 или 60oС в течение 15 секунд и элонгацией при 72oС в течение 30 секунд. Реакционный раствор, содержащий образец, греют при 94oС в течение 3 минут и подвергают электрофоретическому разделению в 5% полиакриламидном геле, после чего секвенируют ДНК с помощью автоматического секвенатора.
Пример 4
Электрофизиологический анализ
Коэкспрессируют βIR и сульфонилмочевинный рецептор в клетках СОS-1, чтобы провести электрофизиологический анализ, и наблюдают за активностью калиевого канала, которая подавляется в зависимости от концентрации АТР (см. фиг. 7). Кроме того, обнаруживается, что активность калиевого канала ингибируется глибенкламидом - сульфонилмочевинным лекарственным препаратом, что также наблюдают (см. фиг.8). Чтобы выделить кДНК, кодирующую uКАТР-1 человеческого происхождения, выполняют поиск в библиотеке кДНК легкого человека, используя в качестве зонда меченную 32Р кДНК ruКАТР-1 крысиного происхождения. Полученный в результате клон подвергают субклонированию в М13mp18, M13mp19 и рGEV3Z с последующим секвенированием оснований по методу обрыва цепи.



Изобретение относится к биотехнологии и касается белков АТР-чувствительного калиевого канала, дезоксирибонуклеотидов и экспрессирующей плазмиды. Сущность изобретения включает новые белки АТР-чувствительного калиевого канала человеческого и мышиного происхождения, имеющие аминокислотную последовательность, показанную на фиг.1 и 3 соответственно, дезоксирибонуклеотиды, кодирующие указанные аминокислотные последовательности, имеющие последовательность оснований, показанных на фиг.2 и 4 соответственно, а также экспрессирующую плазмиду, включающую указанные дезоксирибонуклеотиды. Преимущество изобретения заключается в определении последовательностей новых белков АТР-чувствительного калиевого канала и определении последовательностей оснований дезоксирибонуклеотидов, их кодирующих. 5 с. и 2 з.п.ф-лы, 8 ил.
| US 5356775 A, 18.10.1994 | |||
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| Экономайзер | 0 |
|
SU94A1 |
| NOBUYA JNAGAKI et al., Cloning and Functional characterization of a Novel ATP-sensitive potassium chanel ubiguitously expressed in Rat tissues including pancreatic islets, pituitary, skeletal muscle and Heart, J | |||
| of Biol | |||
| Chem., 1995, v.270, №11, рр.5991-5994. | |||
Авторы
Даты
2002-10-10—Публикация
1996-09-17—Подача