4-1ВВ является индуцибельным Т-клеточным рецептором, который принадлежит к суперсемейству рецепторов нервных факторов роста. Этот новый антиген экспрессируется на поверхности активированных селезеночных Т-клеток и тимоцитов. Внеклеточный домен этого трансмембранного белка типа I гомологичен членам суперсемейства рецепторов нервных факторов роста. Цитоплазматический домен содержит последовательность, гомологичную сайту связывания специфичной для Т-клеток тирозинкиназы р561ck.
Роль 4-1ВВ in vivo остается неясной, хотя имеются данные в пользу того, что он является сигнальной молекулой при активации Т-клеток. Например, сшивание 4-1ВВ с моноклональным антителом 53А2 на анти-СD-3-стимулированных Т-клетках приводит к усилению пролиферации Т-клеток в 2-10 раз (Pollok et al., J. Immunol. 151:1255 (1993)). Кроме того, Zhou et al., Immunol. Letters 41: 177-184 (1994) показали, что 4-1ВВ экспрессирован на активированных внутриэпителиальных Т-лимфоцитах кишечника (IELS) и что активированные IELS, стимулированные анти-4-lBB моноклональным антителом, могут повышать уровень цитотоксичности по отношению к анти-CD-4-секретирующим гибридомным клеткам. Сшивание анти-4-lBB антитела также усиливает пролиферацию IELS.
Были идентифицированы по меньшей мере два возможных кандидата на роль лиганда 4-1ВВ. Chalupny et al. (Proc. Natl. Cad.Sci.USA 89:10360-10364 (1992)) применили растворимый слитой белок 4-1ВВ с иммуноглобулином, чтобы показать, что 4-1ВВ связывается с белком внеклеточного матрикса (ЕМС). Goodwin et al. (Eur. J. Immunol. 23:2631 (1993)) сообщили о выделении кДНК лиганда мушиного 4-1ВВ (4-1-BB-L), который является членом семейства лигандов с С-терминальной амнокислотной гомологией, к которым относятся ФНО, лимфотоксин альфа и бета, CD40-L, Cd27-L, CD30-L и Fas-L.
Были клонированы человеческий аналог (hu4-lBB) мышиного 4-1ВВ и человеческий аналог (hu4-1-BB-L) мышиного 4-1-BB-L (Alderson et al., Eur. J. Immunol. 24: 2219-2227 (1994)). Как моноклональное антитело к hu4-1BB, так и клетки, трансфицированные hu4-1-BB-L, индуцировали сильный пролиферативный ответ в первичных Т-клетках, костимулированных митогеном.
Таким образом, существует потребность в разработке и получении антагонистов 4-1ВВ. Именно это явилось задачей настоящего изобретения.
Краткое описание изобретения
Одной из задач изобретения является подавление первичного и вторичного гуморального ответа на антиген у хозяина, включающий введение хозяину эффективной дозы анти-4-1-BB антитела.
Другой задачей изобретения является получение композиций, содержащих моноклональные антитела 1D8, 3В8 или 3Е1.
Другой задачей изобретения является получение композиции, содержащей анти-4-1-BB антитело при том, что данное антитело подавляет антительный ответ на эритроциты барана in vivo.
Еще одной задачей изобретения является блокирование зависимого от Т-клеток иммунного ответа у хозяина, включающий введение хозяину эффективной дозы анти-4-1-BB антитела.
Другой задачей изобретения является усиление цитотоксической активности лимфоцитов в отношении опухолевых клеток у хозяина, включающий введение хозяину эффективной дозы анти-4-1-BB антитела.
Еще одной задачей изобретения является усиление развития цитотоксических Т-клеток у хозяина, включающий введение хозяину эффективной дозы анти-4-1-BB антитела.
Еще одной задачей изобретения является лечение хозяина, страдающего от обусловленного Т-клетками аутоиммунного заболевания, включающий введение хозяину эффективной дозы анти-4-1-BB антитела.
Краткое описание фигур
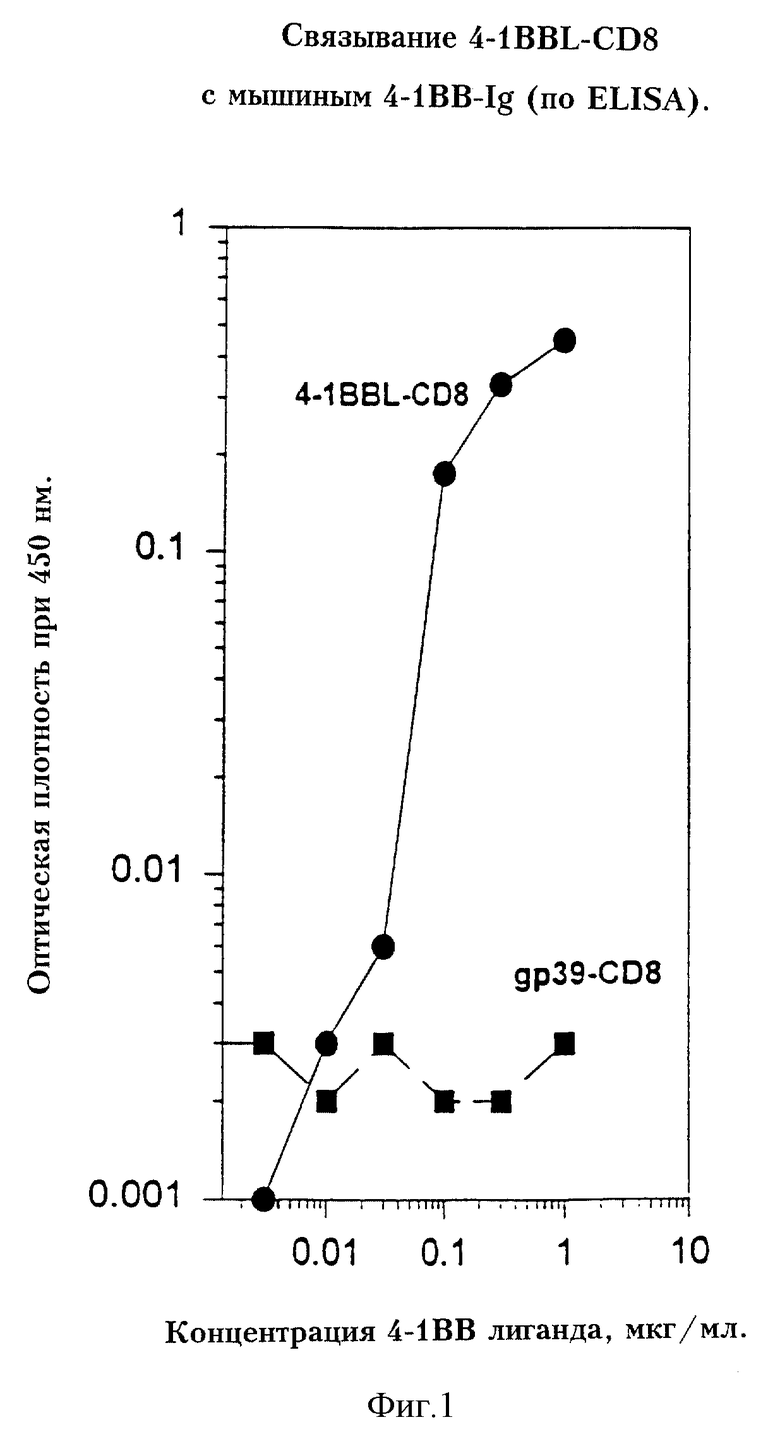
На фиг.1 представлен график, отражающий связывание мышиного 4-1ВВ лиганда с иммобилизованным 4-1RB.
На фиг. 2 представлен график, отражающий блокирование анти-4-1BB моноклональными антителами (МКА) связывания 4-1ВВ с лигандом.
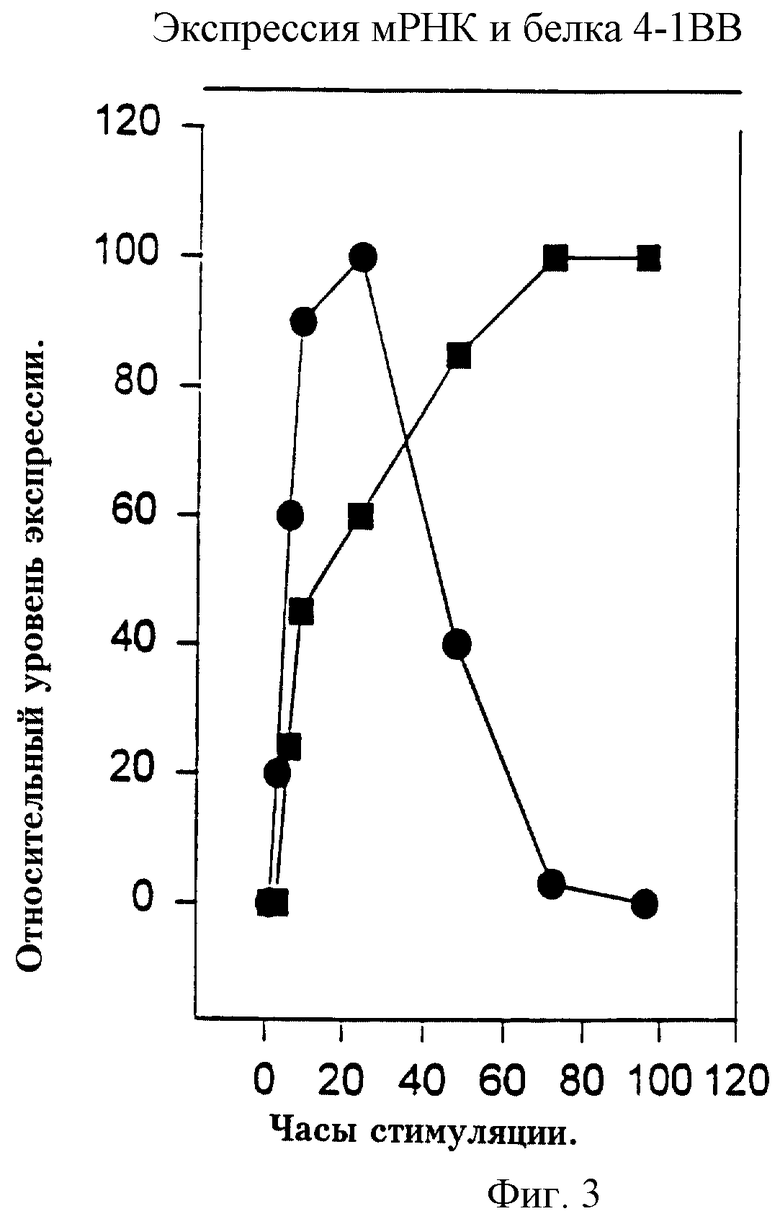
На фиг.3 представлен график, отражающий экспрессию 4-1ВВ активированными Т-клетками как функцию времени, прошедшего после стимуляции. Кружками представлено количество мРНК 4-1 ВВ. Квадратами представлено количество рецептора 4-1ВВ на поверхности активированных клеток Т-клеточной линии DO.11.10.
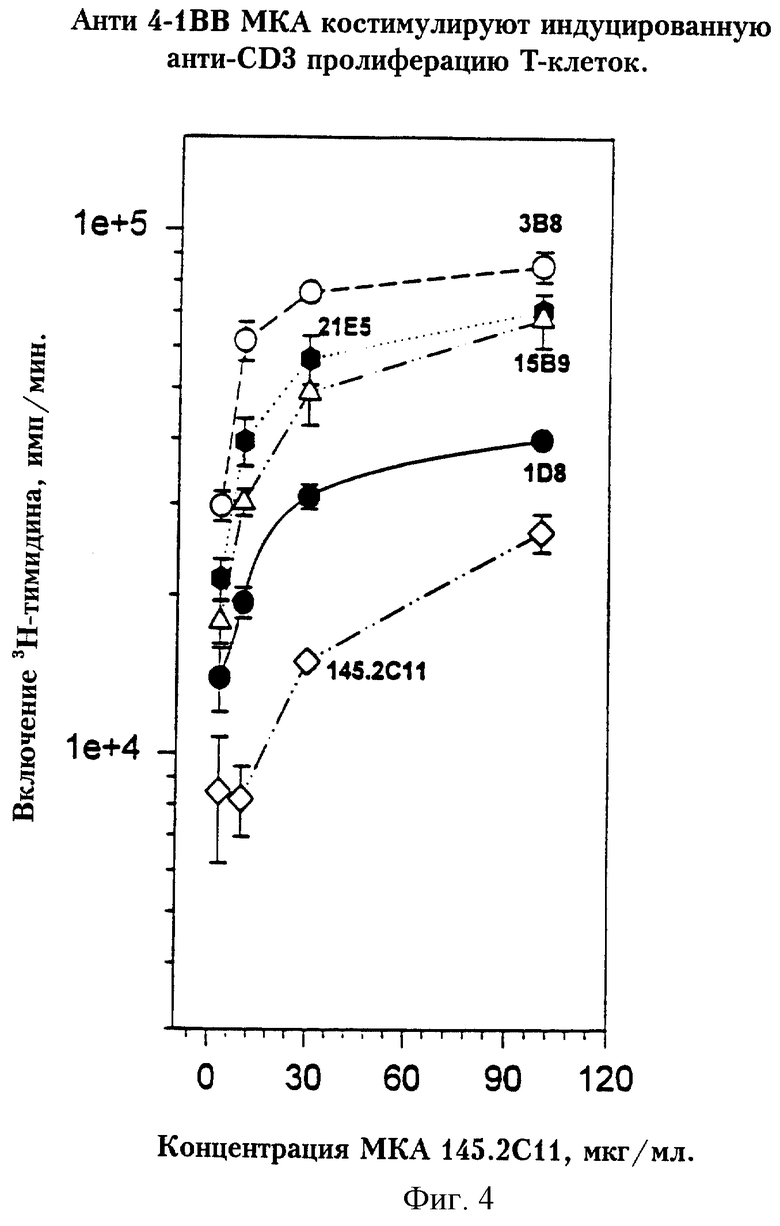
На фиг.4 представлен график, отражающий костимуляцию активации Т-клеток субоптимальными дозами анти-CD3 моноклональными антителами 145.2С11 и анти-4-1BB моноклональными антителами.
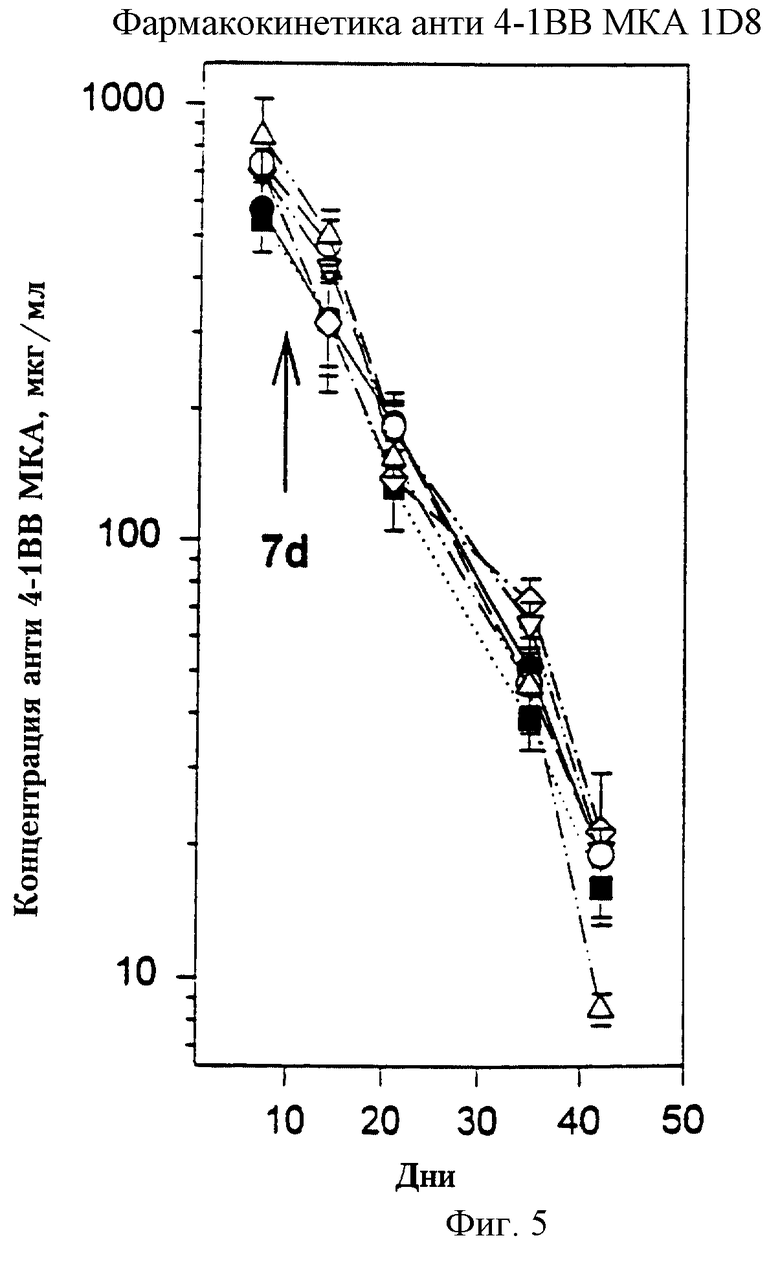
На фиг. 5 представлен график, отражающий фармакокинетику анти-4-1BB моноклональных антител 1D8. Каждый символ относится к отдельной мыши.
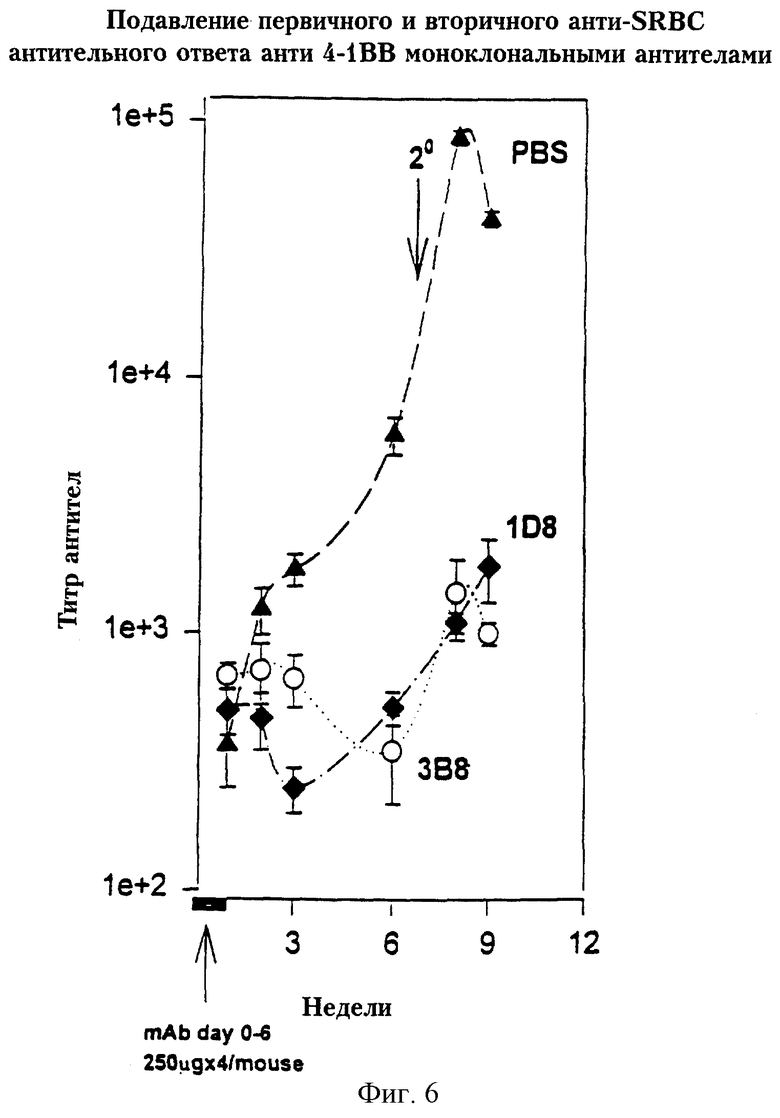
На фиг.6 представлен график, отражающий подавление анти-4-1BB антителами первичного и вторичного ответа на эритроциты барана.
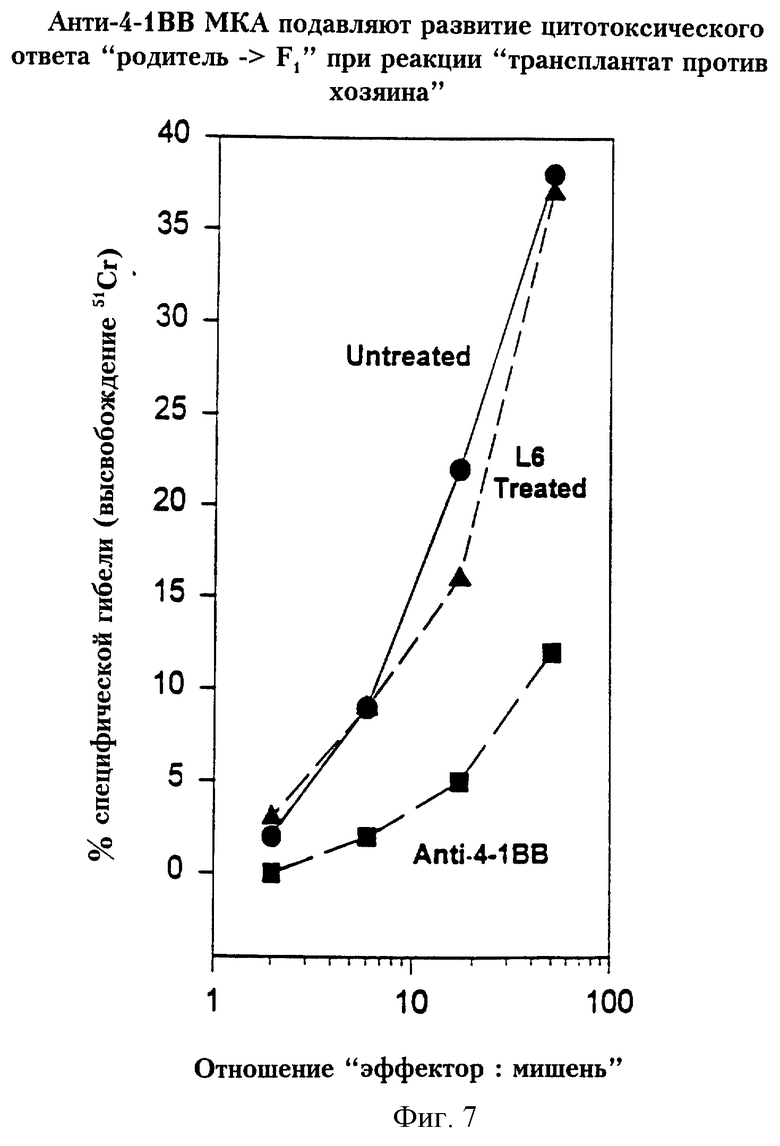
На фиг. 7 представлен график, отражающий подавление образования цитотоксических Т-клеток.
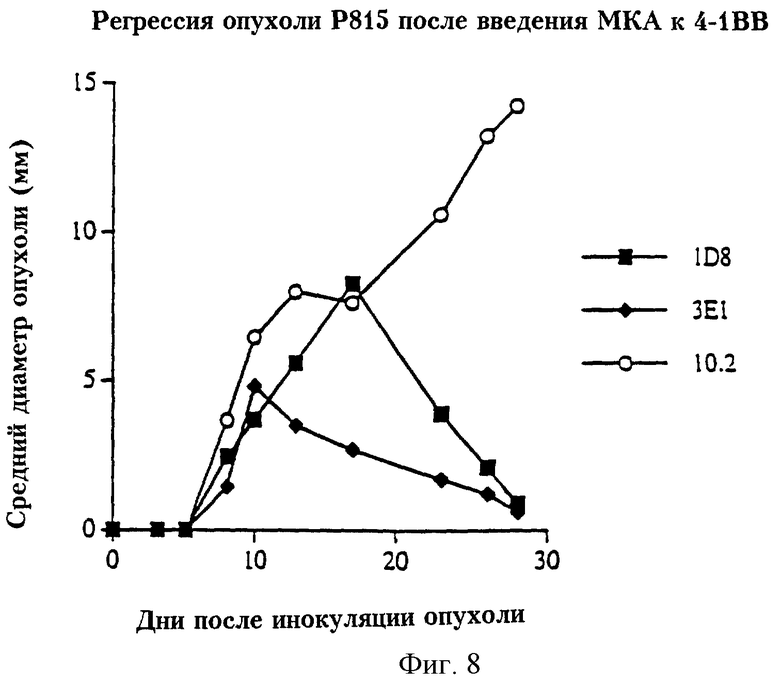
На фиг.8 представлен график, отражающий регрессию опухоли Р815 после лечения МКА к 4-1ВВ.
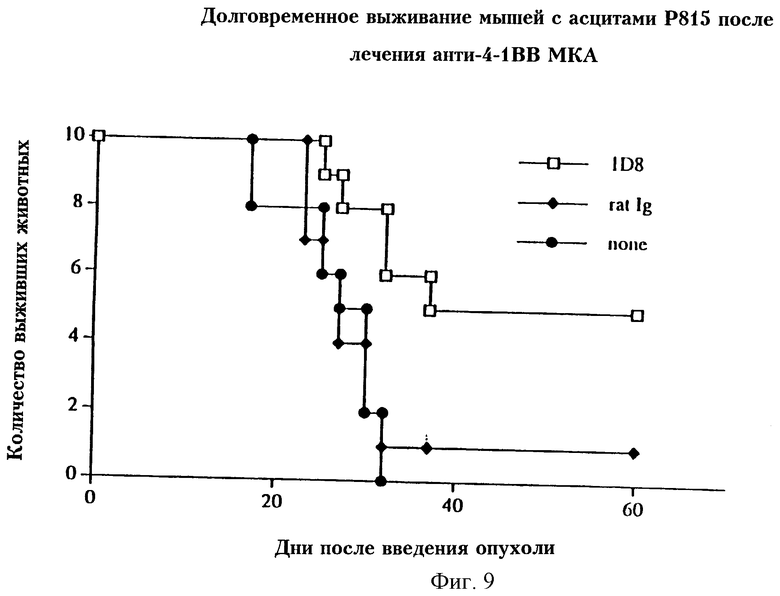
На фиг.9 представлен график, отражающий долговременное выживание мышей с асцитами Р815 после лечения анти-4-1BB МКА.
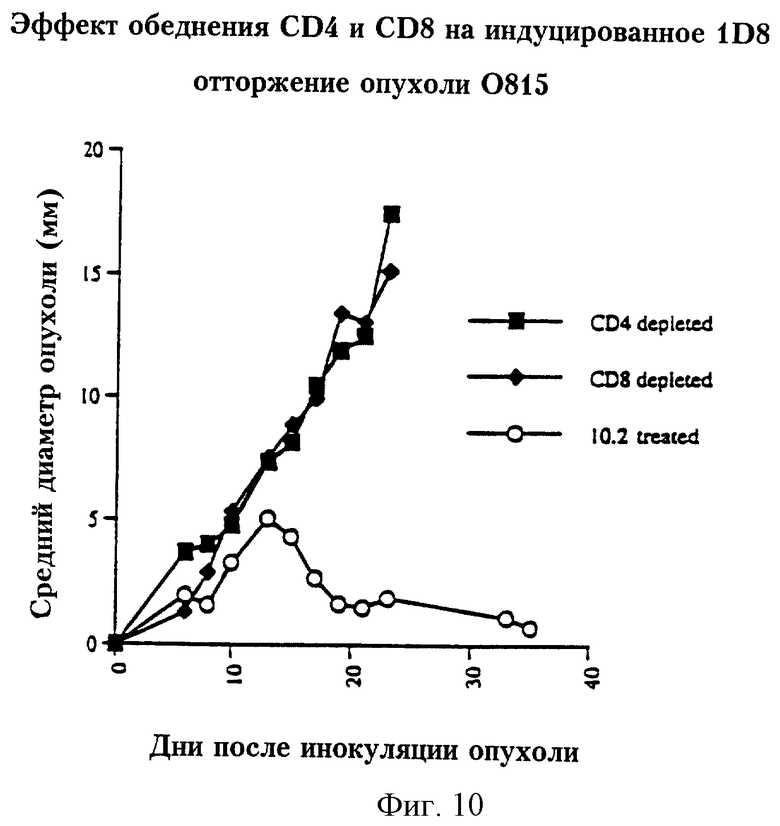
На фиг. 10 представлен график, отражающий эффект истощения CD4 и CD8 в 1D8-индуцированном отторжении опухолевых клеток Р815.
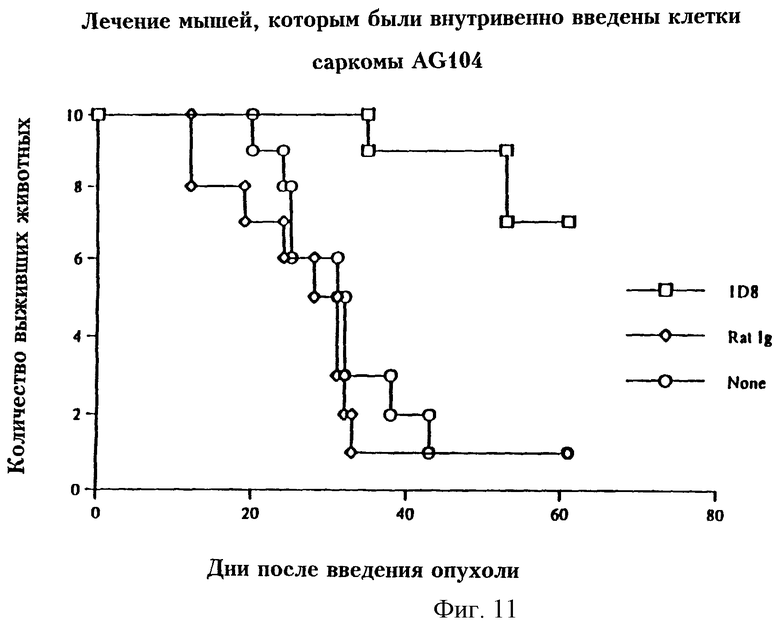
На фиг. 11 представлен график, отражающий лечение мышей, которым внутривенно вводили саркомные клетки AG104.
На фиг. 12А-12С представлено: на фиг.12А - подавление in vivo цитотоксического ответа при реакции "трансплантат против хозяина" (GvHD); на фиг. 12В - ускорение обусловленной цитотоксическими клетками гибели спленоцитов BDF1 под действием анти-4-1BB МКА; и на фиг.12С - повышение процента CD8+ клеток у мышей с реакцией "трансплантат против хозяина".
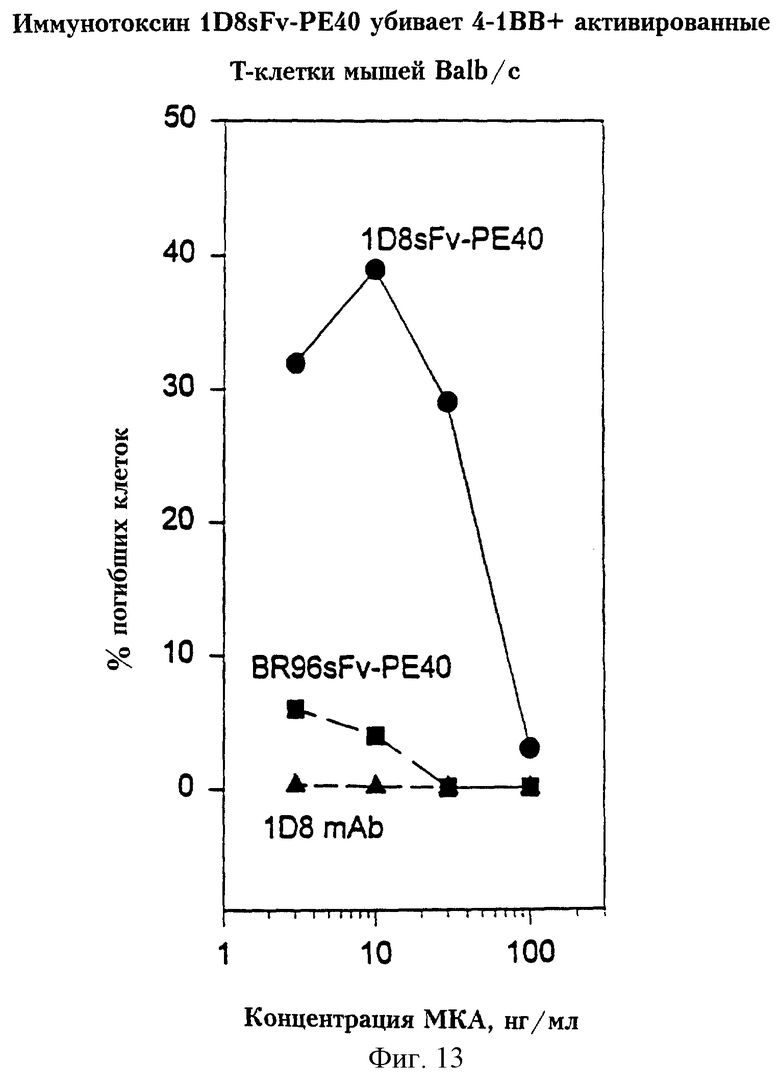
На фиг.13 представлен график, отражающий "убийство" активированных мышиных Т-клеток иммунотоксином анти-4-1ВВ-РЕ40.
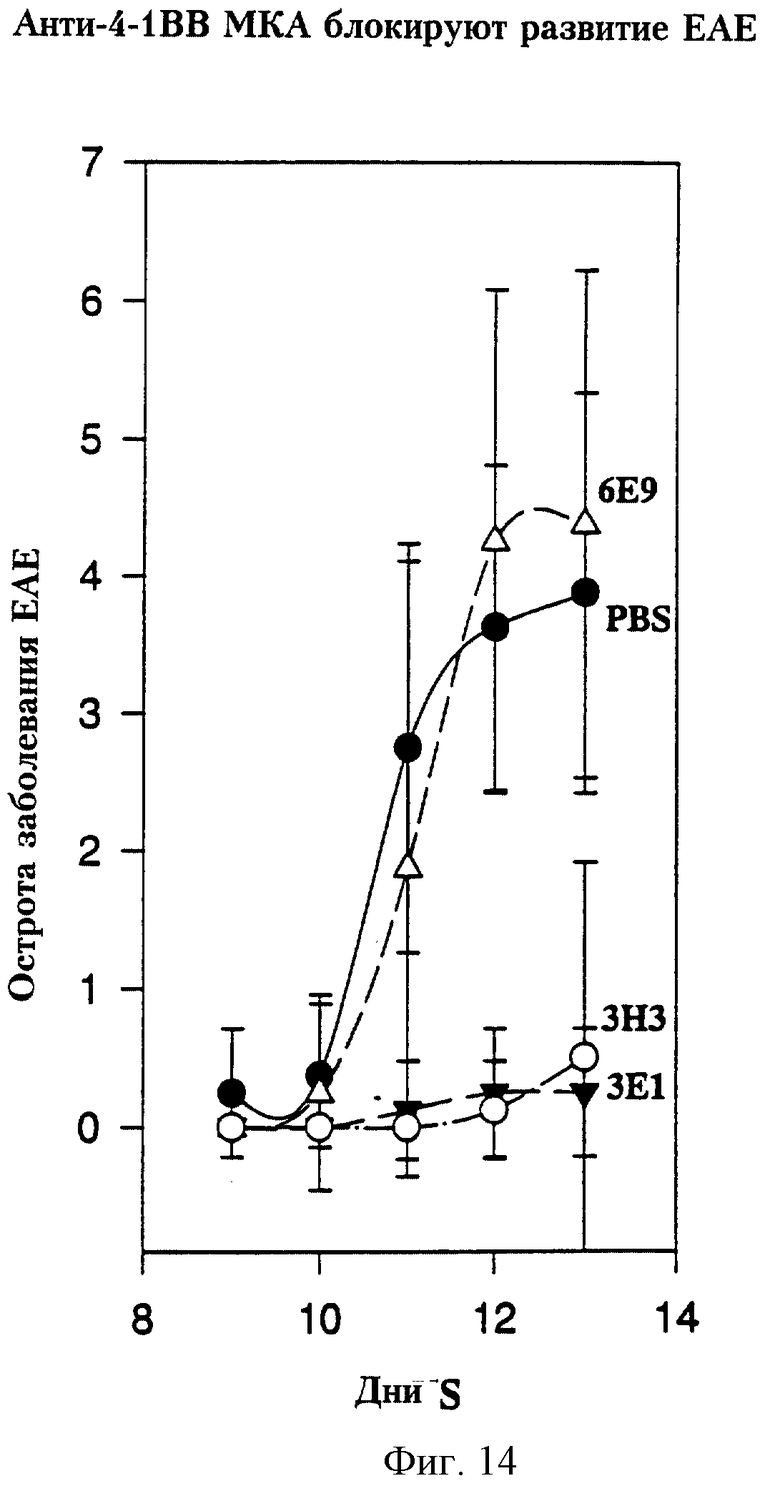
На фиг.14 представлен график, отражающий способность анти-4-1BB антител блокировать развитие эксперментального аутоиммунного энцефаломиелита.
Описание конкретных вариантов осуществления изобретения
Иммуносупрессивная терапия обычно используется для контроля воспаления, лечения рака и при пересадке органов. Применение традиционных способов лечения, таких как использование адренокортикоидных гормонов и их индуктора адренокортикотропного гормона, химиотерапевтических агентов и радиотерапии, может приводить к неспецифической иммуносупрессии и иммунодефицитам. Таким образом, существует настоятельная потребность в разработке альтернативных путей иммуносупрессии. Заявленные в настоящем изобретении антитела дают возможность предпочтительно нацеливаться на конкретные полипептиды, в частности 4-1ВВ, экспрессируемые на Т-клетках.
Используемый в настоящем описании термин "4-1ВВ" обозначает поверхностный белок 4-1ВВ мышиных клеток и гомологи данного белка, присутствующие у других видов, включая человека. Хотя определенная гомология по аминокислотной последовательности ожидается для гомологов различных видов, степень этой гомологии может быть низкой и достигать 50%. Таким образом, гомологи 4-1ВВ можно определить как трансмембранные белки, экспрессируемые на активированных Т-клетках и имеющие по меньшей мере 50%-ную гомологию по аминокислотной последовательности с мышиным 4-1ВВ. Кроме того, это определение 4-1ВВ также включает аллели 4-1ВВ и гомологов, 4-1ВВ и гомологи с консервативными заменами аминокислот, а также растворимые формы 4-1ВВ и гомологов.
Используемый в настоящем описании термин "гуморальный ответ" обозначает иммунную реакцию, которая может быть передана сывороткой и которая обычно обусловлена наличием специфического антитела. Термины "первичный" и "вторичный" иммунный ответ обозначают соответственно первый контакт хозяина с антигеном и последующие контакты. Обычно при гуморальном иммунном ответе главным классом антител при раннем первичном ответе (т.е. в первую неделю) являются IgM, тогда как IgG являются главным классом антител при вторичном ответе.
Моноклональные антитела согласно настоящему изобретению могут принадлежать к любому классу, но предпочтительно являются IgG или IgM.
Для введения человеку, т. е. как компонент композиций для лечения in vivo, моноклональные антитела согласно настоящему изобретению являются антителами преимущественно человеческого происхождения с тем, чтобы снизить иммуногенность, и используются в по существу очищенном виде. Термин "преимущественно человеческого происхождения" означает, что иммуноглобулиновая часть композиции обычно содержит не менее чем около 70% последовательности антитела человека, предпочтительно не менее чем около 80% последовательности антитела человека и наиболее предпочтительно - не менее чем около 90% или более последовательности антитела человека. Когда упоминается "антитело", подразумевается, что в молекуле могут дополнительно присутствовать неиммуноглобулиновые последовательности при том, что молекула сохраняет способность связывать 4-1ВВ.
При необходимости можно соединить антигенсвязывающие районы (например F(ab')2, вариабельные или гипервариабельные (определяющие комплементарность) районы) моноклональных антител нечеловеческого происхождения, таких как мышиные моноклональные антитела, полученные против человеческого гомолога 4-1ВВ, с константными областями (Fc) или со скелетными районами с использованием методов рекомбинантных ДНК, получая тем самым молекулы, в которых преобладает человеческий компонент. Эти методы известны из уровня техники и описаны, например, в патенте США N 4816397, публикациях ЕР 173494 и 239400. Альтернативно можно выделить последовательность ДНК, которая кодирует человеческое моноклональное антитело или его часть, которое специфически связывает 4-1ВВ путем скрининга библиотеки ДНК из В-клеток человека согласно общей методике, описанной Huse et al., Science 246:1275-1281 (1989) и в патенте WO 90/14430, с последующим клонированием и амплификацией последовательности, которая кодирует антитело (или связывающий фрагмент) нужной специфичности. В качестве другого варианта осуществления можно получить одноцепочечные связывающие полипептиды, которые связывают 4-1ВВ. Эти одноцепочечные полипептиды можно получить клонированном и соединением вариабельных областей тяжелых и легких цепей моноклональных антител, связывающих 4-1ВВ. Способы получения одноцепочечных связывающих полипептидов подробно описаны, например, в патенте США N 4946778.
В контексте настоящего изобретения термины "лечение" или "обработка" подразумевают: (1) предотвращение нежелательных симптомов или патологических состояний у субъекта, предрасположенного к данным нежелательным симптомам или патологическим состояниям, но у которого они еще не диагностированы; (2) подавление нежелательных симптомов или патологических состояний, т.е. остановка их развития; или (3) облегчение или ослабление нежелательных симптомов или патологических состояний, т.е. регрессию нежелательных симптомов или патологических состояний. Количество композиции, полученной согласно настоящему изобретению, которое достаточно для достижения любой из перечисленных целей, обозначается как "эффективное количество" и предусматривает как профилактическое, так и терапевтическое применение композиций.
Антитела, полученные согласно настоящему изобретению, применимы для профилактики или лечения заболеваний или патологических состояний, при которых показана иммуносупрессивная терапия и к которым относятся (без ограничений перечисленными) воспалительные заболевания кишечника, рассеянный склероз, аутоиммунный диабет, ревматоидный артрит, заболевание "трансплантат против хозяина", системная красная волчанка, другие Т-клеточные аутоиммунные заболевания и рак.
Моноклональные антитела и другие соединения, полученные согласно настоящему изобретению, могут вводиться в качестве компонентов в фармацевтические композиции, содержащие терапевтическое или профилактическое количество по меньшей мере одного моноклонального антитела или его связывающего фрагмента в сочетании с фармацевтически эффективным носителем.
Для приготовления фармацевтических композиций, применимых при осуществлении данных способов, должен быть использован фармацевтический носитель, который может быть любым совместимым, нетоксическим веществом, приемлемым для доставки больному антител или их связывающих фрагментов, или терапевтических соединений, определяемых в соответствии со способами, изложенными в настоящем изобретении. Стерильная вода, спирт, жиры, воски, инертные твердые вещества и даже липосомы можно использовать в качестве носителей. В состав фармацевтических композиций могут входить фармацевтически приемлемые адъюванты (буферные агенты, диспергирующие агенты). Антитела и их фармацевтические композиции особенно удобны для парентерального введения, например внутривенного, внутриартериального, внутримышечного или подкожного. Однако применимы также интраназальные или другие аэрозольные варианты. Концентрация такого соединения, как антитело, в составе для введения может варьировать в широких пределах, например, от менее чем 0,5%, обычно около 1%, до 15% или 20% и более по весу. Концентрацию выбирают на основе таких критериев, как объем жидкости, вязкость и т.д., которые предпочтительны для конкретного способа введения. Практические способы получения композиций для введения известны или очевидны квалифицированному специалисту и описаны более подробно, например, в Remington's Pharmaceutical Science. 17th Ed., Mack Publishing Co., Easton PA (1985).
Соединения, применяемые согласно настоящему изобретению для подавления иммунного ответа на антиген или антигены, можно вводить с профилактической или лечебной целью. При профилактических назначениях композиции вводят больному, для которого высока вероятность контакта с определенным антигеном или антигенами, таким как больным, подвергшимся пересадкам органов и тканей (включая переливания крови или сыворотки) или лечению такими иммуногенными соединениями, как антибиотики. Введение соединений согласно настоящему изобретению может осуществляться до контакта с антигеном или антигенами или же одновременно с таким контактом. Для предотвращения возобновляющихся заболеваний и их последствий композиции можно вводить ежедневно, еженедельно или согласно другим графикам поддерживающей терапии. Расписание введений также зависит от дозировок и их эффективности, цели терапии и общего состояния здоровья пациента. Лечащий врач, дантист или другой специалист здравоохранения выберет дозировку и характер введения, т.е. способ введения и будет ли оно единичным или многократным.
Для терапевтических применений соединения, полученные согласно настоящему изобретению, вводят больному, уже страдающему от нежелательных симптомов или патологии в таких количествах, которые достаточны для того, чтобы хотя бы частично подавить иммунный ответ на антиген(ы). Количество, достаточное для достижения этой цели, определяют как "терапевтически эффективную дозу". Эффективные для такого использования количества будут зависеть от того, какое соединение используется, от способа введения, от остроты нежелательных симптомов или патологических состояний и от общего состояния здоровья пациента. Определение эффективного количества соединения, подавляющего иммунный ответ на антиген, может быть осуществлено способами, известными из уровня техники. Например, при помощи хорошо известных диагностических методов in vitro можно определить снижение количества антиген-специфического иммуноглобулина и тем самым судить об эффективности исследуемых композиций.
Антиген (или антигены), в контакт с которыми вступает человек-хозяин, являются преимущественно зависимыми от Т-клеток. Большинство антигенов являются зависимыми от Т-клеток, т.е. для развития иммунного ответа на них необходимо участие Т-клеток. Т-независимые антигены обычно представляют собой большие полимерные молекулы с множественными, повторяющимися антигенными детерминантами. Часто Т-независимые антигены обладают митогенными свойствами.
В качестве одного из вариантов осуществления изобретения, полученные согласно настоящему изобретению анти-4-1BB антитела можно использовать в аффинной хроматографии для очистки 4-1ВВ полипептидов, таких как внеклеточная область 4-1ВВ, растворимые формы 4-1ВВ и слитые белки 4-1ВВ с другими молекулами, такими как иммуноглобулины. Анти-4-1ВВ-антитела, полученные согласно настоящему изобретению, могут быть помечены путем присоединения репортерной молекулы, такой как флуоресцеин, щелочная фосфатаза и им подобные, и использованы для визуализации 4-1ВВ на клеточной поверхности. Антитела, помеченные радиоактивной меткой, можно использовать для количественной оценки 4-1ВВ на клетках. В качестве других вариантов осуществления изобретения можно назвать использование анти-4-1BB-антител в конкурентных тестах с лигандами 4-1ВВ.
Следующие примеры приведены только для целей иллюстрации и не ограничивают объем изобретения.
ПРИМЕРЫ
I. Иммунизация и способы отбора
Для иммунизации и скрининга был сконструирован слитый белок, состоящий из внеклеточной части молекулы мышиного 4-1ВВ и константного района Ig человека (патент ЕР 0595659). Слитый белок 4-1BBIg содержал сайт разрезания тромбиновой протеазой между 4-1ВВ и Ig частями молекулы. Для иммунизации слитый белок разрезали тромбиновой протеазой и пропускали через колонку с белком А, чтобы удалить неразрезанный белок и фрагменты Ig. Несвязавшийся материал, полученный в результате данной процедуры и представленный несколькими полосами при анализе SDS-PAGE, использовали для иммунизации.
Гибридомы "крыса-мышь" были получены и скринированы с применением стандартных методов. В качестве партнеров для слияния использовали иммунные клетки селезенки и мышиную миелому AG8 (Kearney et al., J. Immunol. 123: 1548-1550 (1974). Атитела были получены в результате двух независимых слияний. МКА 3В8 и 1D8 были получены в результате слияния, которому предшествовала имунизация по следующей схеме: две инъекции 20 мкг белка в адъюванте RIBI (RIBI Immunochemical) в подушечки лап в дни 0 и 3; третья инъекция 20 мкг белка в PBS в подушечки лап в день 10; и на 13-й день дренировали подколенный лимфатический узел и проводили слияние. Другие МКА были получены в результате второго слияния клеток селезенки после 4-х внутрибрюшинных инъекций 20 мкг белка в адъюванте RIBI в течение 5 месяцев. Внутривенные инъекции в дозе 30 мкг проводили за 17 и 3 дня до слияния.
II. Характеристика анти-4-1BB антител
Первоначально антитела идентифицировали по специфическому связыванию слитого белка 4-1BBIg в стардартной ELISA. Специфичность антител определяли согласно дополнительным критериям: (1) по связыванию с клетками COS, экспрессирующими полноразмерную молекулу 4-1ВВ, но не с мнимотрансфицированными клетками COS; (2) по связыванию с клетками гибридомы D0-11-10, активированными к экспрессии 4-1ВВ (активация в течение 12 часов 10 нг/мл РМА и 0,5 мкг/мл иономицина). По изотипу антитело 3В8 относилось к крысиным IgM, тогда как все другие антитела имели изотип IgG2a, как определено с помощью изотип-специфических пероксидазных реагентов (Zymed) в ELIZA с белком 4-1BBIg.
III. Очистка антител
Моноклональные антитела (МКА) 3В8 (IgM) очищали аффинно на колонке с анти-каппа цепью (mAb RG7 (АТСС Т1В 172). МКА элюировали буфером для элюции Immunopure Ig (Pierce), а затем диализовали против фосфатного буферного раствора (PBS). Материал, очищенный на RG7, содержал некоторое количество свободных легких цепей, которые очищались вместе с интактными антителами. Все другие антитела очищали на белке G (Gammabind Plus, Pharmacia). Для элюции антител использовали буфер для элюции Immunopure Ig. Перед использованием антитела диализовали против PBS.
IV. Подавление моноклональными антителами связывания лиганда
Для изучения подавления связывания лиганда молекулой 4-1ВВ в качестве суррогатной молекулы использовали растворимый слитый белок, состоящий из внеклеточной части лиганда 4-1ВВ с карбоксиконца и внеклеточной части мышиного CD8 с аминоконца. ДНК, кодирующая внеклеточную часть мышиного лиганда 4-1ВВ (остатки 104-309), была получена полимеразной цепной реакцией с использованием "верхнего" праймера, содержащего сайт BamHI (5'-GCGGCGGATCCCCGCACCGAGCCTCGGCCAGCG-3') и "нижнего" праймера, содержащего сайт XbaI (5'-CGCTCTAGAGGATAGTTCTCATTCCCATGG-3'). Фрагмент ДНК мышиного лиганда 4-1ВВ был клонирован в рамку в вектор CDM7(B-), содержащий внеклеточный домен CD8, за которым следовал сайт BamHI. Эта молекула была обозначена как лиганд 4-1ВВ (4-1-BBL). Способность анти-4-1BB МКА блокировать связывание лиганда с молекулой 4-1ВВ оценивали при помощи ELISA и клеточных тест-систем. 4-1-BBL был очищен на аффинной колонке с анти-CD8 моноклональными антителами 53,6 (АТСС TIB 105) с элюцией 40% пропиленгликолем/60% Tris (pH 7,0)/ 1,25 М (NH4)2SO4 и диализован против фосфатного буферного раствора (PBS). Очищенный материал в условиях восстанавливающего SDS-PAGE мигрировал в виде преобладающей широкой полосы с приблизительным молекулярным весом 55000. При HPLC гель-фильтрации материал элюировался в виде трех пиков. Преобладающий пик имел приблизительный молекулярный вес 300000.
Тесты ELISA на подавление связывания 4-1-BBL проводили следующим образом. Белок 4-1-BBL сорбировали на ячейках плат для ELISA в концентрации 0,1 мкг/мл в PBS в течение ночи при 4oС, блокировали растворителем для образцов (Genetic Systems) и инкубировали с очищенным антителом 1 час. Затем добавляли лиганд и смесь МКА и лиганда инкубировали еще 1 час. Платы отмывали и инкубировали с биотинилированными МКА 56,3 (анти-CD8), а затем - с конъюгатом стрептавидин-пероксидаза хрена (HRPO). На подавление связывания указывало уменьшение сигнала в ELISA. Титрование связывания лиганда с 4-1BBIg показано на фиг. 1. Контрольный слитый мышиный белок pg39-CD8 не связывал 4-1ВВ, тогда как лиганд 4-1ВВ специфически связывал 4-1ВВ дозозависимым образом. Фиг. 2 иллюстирирует способность МКА блокировать связывание лиганда с 4-1BBIg в аналогично поставленной ELISA.
V. Активация клеток D0-11-10 к продукции белка 4-1ВВ
Клетки Т-клеточной гибридомы D0-11-10 активировали к экспрессии молекулы 4-1ВВ обработкой РМА (10 нг/мл) и иономицином (0,5 мкг/мл) в течение различных интервалов времени, после чего определяли мРНК 4-1ВВ или экспрессию 4-1ВВ на поверхности клеток при помощи Нозерн-анализа и проточной цитофлуориметрии соответственно (фиг. 3). Необработанные клетки не связывали белок 4-1ВВ. Активированные клетки связывали белок 4-1ВВ, но не аналогичный слитый белковый конструкт gp39 и Lyta2a (Hollenbaugh et al., EMBO J. 11(12):4313-4321 (1992)). Анти-4-1BB антитела 1D8 и 3В8 связывались с клетками D0-11-10 только тогда, когда клетки были активированы. Преинкубация этих МКА с клетками D0-11-10 могла блокировать последующее связывание 4-1-BBL. Связывание 4-1-BBL клетками оценивали при помощи антисывороток, конъюгированных с анти-CD8 МКА (53,6) (Biosource).
В последующих экспериментах исследовали способность анти-4-1BB антител костимулировать активацию Т-клеток. Стимуляция покоящихся Т-клеток субоптимальными дозами анти-CD-3 МКА 145.2С11 в сочетании с 10 мкг/мл анти-4-1BB антител повышала пролиферацию клеток в 2,5-8 раз по сравнению с эффектом одних МКА 145.2С11 (фиг. 4). Имелась незначительная корреляция между аффинностью связывания или способностью блокировать связывание лиганда и способностью МКА костимулировать Т-клетки.
VI. Подавление развития анти-SRBC антительного ответа анти-4-1BB моноклональными антителами 1D8 и 3В8
Исследовали фармакокинетику анти-4-1BB МКА 1D8 при внутривенном введении в дозе 250 мг/мышь. Образцы сывороток собирали начиная с 8-го дня и по 42-й день, после чего их анализировали на присутствие анти-4-1BB МКА. Приведенные на фиг. 5 результаты показывают, что срок полужизни МКА 1D8 составляет 7 дней. Эти результаты также свидетельствуют о том, что у этих животных не образовывалось антикрысиных IgG (анти-1DS). Срок полужизни МКА 3В8, крысиных IgM антител, составлял 6,5 часов (данные не приведены).
Группе из пяти мышей вводили внутривенно зависимый от Т-клеток антиген - эритроциты барана (SRBC) и 250 мг антител 1D8 или 3В8. Дальнейшие инъекции антител проводили через день до 6-го дня. У каждой мыши на протяжении 7-ми недель периодически брали образцы сыворотки и определяли титр анти-SRBC антител. На 7-й неделе эксперимента мышам вводили вторую порцию SRBC, анти-4-1BB МКА более не вводили. На протяжении двух недель собирали образцы сывороток для определения анти-SRBC антител. Как 1D8, так и 3В8 блокировали первичный и вторичный ответ на SRBC (фиг.6). Эти эксперименты, в особенности результаты с 3В8, указывают на тот факт, что подобного рода обработка приводит к долговременному отсутствию ответа.
VII. Подавление образования цитотоксических Т-клеток
Для того чтобы определить важна ли экспрессия 4-1ВВ для других эффекторных функций Т-клеток определяли способность МКА 1D8 и нескольких других МКА, полученных в результате второго слияния, влиять на образование цитотоксических Т-клеток при острой реакции "трансплантат против хозяина". Селезеночные Т-клетки брали у мышей BDF1 (Н-2db) через 10 дней после внутривенного введения 107 селезеночных Т-клеток C57BL/6 (Н-b2). После 5 дней выращивания в культуре в присутствии рекомбинантного мышиного ИЛ-2 (R & D Systems) в концентрации 2-10 нг/мл, жизнеспособные Т-клетки проверяли на цитотоксичность против мишеней Iad (P815) или Iаb (EL4), меченных 51Сr. Приведенные на фиг.7 результаты показывают, что селезеночные Т-клетки мышей, которым вводили контрольные МКА или PBS, эффективно убивали мишени, несущие соответствующий гаплотип МНС класса II в соотношениях столь низких, как 3:1. Напротив, селезеночные Т-клетки мышей, которым вводили МКА 1D8, не были способны к цитотоксичности, пока отношение Е:Т не достигало 50:1, и даже тогда их "убивающая" способность была снижена до 75%. Аналогичные результаты были получены с МКА 22В6. При том, что МКА 3Е1 были весьма эффективны в подавлении, МКА 21Е5 были менее эффективны в подавлении образования/выживания ЦТК. Не обнаружено цитотоксичности в отношении мишеней EL-4(Iab) (данные не приведены). Подобные наблюдения не могут объясняться присутствием анти-4-1ВВ МКА в культурах, поскольку добавление таких антител в тесты на ЦТК не блокировало убийство ЦТК. Микроскопическое обследование культивируемых Т-клеток перед их добавлением к мишеням выявило полное отсутствие активированных клеток, большое количество мелких покоящихся клеток и много апоптозных или мертвых клеток, которые отсутствовали в контрольных культурах.
VIII. Усиление образования цитотоксических Т-клеток при реакции "трансплантат против хозяина" in vivo.
Как следует из описанных выше экспериментов, клетки мышей с реакцией "трансплантат против хозяина", обработанных анти-4-1BB МКА, оказались не способны проявить цитотоксическую активность по отношению к соответствующей мишени после 5 дней культивирования in vitro в присутствии ИЛ-2 или без него (данные не приведены), тогда как клетки контрольных мышей проявляли выраженный цитотоксических эффект в культуре в присутствии ИЛ-2. Это наблюдение оказалось неожиданным, поскольку постоянно отмечалась 1D8-индуцированная цитотоксичность на независимых опухолевых моделях in vivo с использованием как метастазирующих, так и неметастазирующих опухолей (фиг.8, 9, 10 и 11). Кроме того, селезенки, взятые у мышей с реакцией "трансплантат против хозяина", обработанных анти-41-ВВ антителами, были увеличены в 2-3 раза по сравнению с нормальными селезенками контрольных мышей, которым вводили другие антитела. Для изучения этого парадоксального явления были повторены эксперименты "трансплантат против хозяина" с той разницей, что в данном случае активность цитотоксических клеток оценивали немедленно после хирургического удаления селезенок с исключением наращивания цитотоксических Т-клеток in vitro в присутствии ИЛ-2. Результаты данного эксперимента существенно отличались от результатов, приведенных выше. На фиг. 12А можно увидеть, что анти-4-1BB МКА, 1D8 и 22В6, каждое из которых связывается с различными областями молекулы 4-1ВВ, повышали активность цитотоксических клеток почти в четыре раза по сравнению с контрольными животными с реакцией "трансплантат против хозяина". Напротив, МКА 21Е5 не оказывало явного эффекта на образование цитотоксических клеток, тогда как МКА 3Е1, один из наиболее сильных блокаторов связывания лиганда, полностью подавляло развитие цитотоксических клеток. Выраженный эффект МКА 1D8 и 22В6, выражающийся в усилении активности цитотоксических клеток, показан на фиг.12В, из которого видно значительное снижение общего числа жизнеспособных спленоцитов, которых удавалось извлечь из мышей, обработанных двумя данными МКА. Кроме того, фенотипический анализ спленоцитов показал, что у мышей, обработанных МКА 1D8, процент CD8+ Т-клеток повысился до 30% от общего числа клеток (фиг.12С), тогда как у мышей с реакцией "трансплантат против хозяина", которым вводили МКА 6Е9 (несвязывающие контрольные МКА того же изотипа) или которым совсем не вводили антител, количество CD8+ Т-клеток составляло от 5 до 8%. Исследования по картированию эпитопов анти-4-1BB МКА с использованием слитых белков 4-1ВВ, в которых были произведены замены доменов, показали, что МКА 1D8 уникально в том смысле, что оно связывается с мембранным проксимальным районом внеклеточного домена молекулы 4-1-ВВ, не участвующим в связывании 4-1BBL (данные не приведены).
IX. Ускорение развития цитотоксических Т-клеток
В данных экспериментах анти-4-1BB моноклональные антитела использовали для ускорение развития цитотоксических Т-клеток, которые затем убивали слабо иммуногенные или неиммуногенные, но сильно метастазирующие, опухоли.
На фиг.8 представлены результаты эксперимента, в котором группе из пяти мышей Ba1b/C в день 0 вводили подкожно 105 клеток мастоцитомы 10 5 Р815. Контрольным мышам вводили МКА 10.2. к человеческому CD5. Однако у мышей, которым вводили МКА 1D8 или 3Е1 (анти-4-1BB), опухоли быстро отторгались. Инъекции антител проводили внутрибрюшинно в дни 3 и 6 в дозе 400 мг/мышь.
Фиг.9 отражает долговременное выживание мышей с привитой опухолью Р815 и обработанных МКА 1D8.
Приведенные на фиг.10 данные показывают, что удаление Т-клеток CD4+ или CD8+ у мышей с привитой опухолью Р815 и обработанных МКА 1D8 делает их неспособными к отторжению опухоли. Эти результаты дают основания считать, что клетки CD4+ и CD8+ необходимы для эффективности МКА 1D8.
Результаты, представленные на фиг.11, демонстрируют, что клетки неиммуногенной саркомы AG104 могут быть убиты цитотоксическими лимфоцитами, индуцированными посредством стимуляции МКА 1D9. В этом опыте группе из 10 мышей Balb/c вводили подкожно 105 опухолевых клеток АG104. Моноклональные антитела вводили подкожно в дни 3 и 6, как описано выше. К 60-му дню 70% мышей выжили. Данный результат особенно примечателен, поскольку использованные опухолевые клетки особенно агрессивны.
X. Убийство активированных мышиных Т-клеток
В этом опыте был получен анти-4-1ВВ-РЕ40 иммунотоксин, для чего были клонированы вариабельные области МКА 1D8, из которых была взята единственная цепь Fv. Эта Sfv была затем использована для получения SFv-PE40 иммунотоксина (Siegall et al., Drug Dev. Res., 34:210-219 (1995). Проточной цитофлуориметрией показано, что данный иммунотоксин связывается только с 4-1BB+ активированными клетками. Приведенные на фиг.13 результаты показывают, что данный иммунотоксин специфически убивает активированные 4-1BB+ клетки дозозависимым способом, тогда как контрольный иммунотоксин такой активностью не обладает.
XI. Подавление развития ЕАЕ
В следующих экспериментах использована модель Т-клеточного аутоиммунного заболевания на мышах, т.е. развитие экспериментального аутоиммунного (или аллергического) энцефаломиелита (ЕАЕ) (см., например, Alvord, G.C. Jr., ed. Experimental Allergic Encephalomyelitis: A Useful Model for Multiple Sclerosis, Liss, NY (1984)).
Самкам мышей РЕ X SJE/F1 внутрикожно в день 0 вводили 100 мкл основного белка миелина из мозга кролика в концентрации 1 мг/мл в полном адъюванте Фрейнда. Внутривенно вводили 200 мкл коклюшного токсина в концентрации 1 мкг/мл в PBS.
Группе из восьми мышей вводили внутривенно в дни 0, 2 и 4 (200 мкг в концентрации 1 мг/мл) PBS, содержащий какие-либо одни из следующих моноклональных антител (все антитела крысиного происхождения, изотипа IgG2А): (а) контрольные МКА 6Е9 (крысиный античеловеческий gp39 MKA); (б) анти-4-l-BB МКА 3Е1; (в) анти-4-1-BB МКА 3Н3. О развитии ЕАЕ судили по параличу хвоста, за которым следовал паралич задних конечностей (в этот момент животных забивали по гуманным соображениям).
Представленные на фиг. 14 результаты свидетельствуют о способности анти-4-1-BB антител блокировать развитие ЕАЕ.
При том что настоящее изобретение подробно описано в примерах и иллюстрациях для облегчения понимания, очевидно, возможны определенные изменения и модификации, которые не выходят за рамки нижеследующей формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| РАСТВОРИМЫЕ МУТАНТНЫЕ МОЛЕКУЛЫ CTLA4 | 1998 |
|
RU2235555C2 |
| РАСТВОРИМЫЙ МУТАНТНЫЙ CTLA4 И ЕГО ПРИМЕНЕНИЕ | 2001 |
|
RU2283847C2 |
| СПОСОБЫ ЛЕЧЕНИЯ РЕВМАТИЧЕСКИХ ЗАБОЛЕВАНИЙ С ПРИМЕНЕНИЕМ РАСТВОРИМОГО CTLA4 | 2001 |
|
RU2287340C2 |
| СИНЕРГИЧЕСКИЕ СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ РАКА | 2001 |
|
RU2264217C2 |
| ПРИМЕНЕНИЕ ИНГИБИТОРОВ ИММУННЫХ КОНТРОЛЬНЫХ ТОЧЕК ПРИ НОВООБРАЗОВАНИЯХ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ | 2015 |
|
RU2726996C1 |
| ЛЕЧЕНИЕ РАКА ЛЕГКОГО С ПОМОЩЬЮ КОМБИНАЦИИ АНТИТЕЛА ПРОТИВ PD-1 И ДРУГОГО ПРОТИВОРАКОВОГО СРЕДСТВА | 2015 |
|
RU2695332C2 |
| АНТИТЕЛА ПРОТИВ АЛЬФА-СУБЪЕДИНИЦЫ ИЛ-7R И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2811912C2 |
| СПОСОБ ЛЕЧЕНИЯ СЕРДЕЧНО-СОСУДИСТОГО ЗАБОЛЕВАНИЯ С ПРИМЕНЕНИЕМ РАСТВОРИМОГО CTLA4 | 2004 |
|
RU2353384C2 |
| СПОСОБ И КОМПОЗИЦИИ ДЛЯ КЛЕТОЧНОЙ ИММУНОТЕРАПИИ | 2013 |
|
RU2700765C2 |
| Молекулы, связывающиеся с 4-1ВВ | 2011 |
|
RU2710717C2 |


Изобретение относится к медицине и касается способов и композиций для иммуномодуляции. Сущность изобретения заключается в том, что включает моноклональные антитела против поверхностного белка 4-1ВВ мышиных клеток, введение которых хозяину вызывает супрессию первичного и вторичного гуморального ответа. Изобретение включает два моноклональных антитела. Преимущество изобретения заключается в разработке нового подхода к иммуносупрессии при терапии рака. 9 с. и 11 з.п.ф-лы, 16 ил.
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| US 5474771 А, 12.12.1995 | |||
| ALDERSON M.R | |||
| et al., Molecular and Biological characterization of human 4-1BB and its Ligand, EUR | |||
| J | |||
| Immunol, 1994, 24(9), p.2219-2227. | |||
Авторы
Даты
2002-11-10—Публикация
1997-10-03—Подача