Изобретение относится к области иммунологии, в частности клинической иммунологии, и посвящено диагностике доклинических и клинически выраженных форм иммунологической недостаточности.
Известен комплекс способов и тестов для характеристики иммунного статуса и выявления иммунодефицитных состояний, отражающих процессы пролиферации и дифференциации клонов В- и Т-лимфоцитов в эффекторные клетки [1, 2, 3]. Для этого используют 8-12 маркеров, выявляющих основные субпопуляции Т- и В-лимфоцитов. Однако эти способы диагностируют лишь те формы дисфункции В- и Т-систем иммунитета, которые развиваются на поздних стадиях патологии и связаны с выраженными расстройствами процессов пролиферации и дифференциации аффинных к антигену клонов лимфоцитов. Ограниченные сроки жизни лимфоцитов, значительная вариабельность субпопуляционного состава лимфоцитов в крови, подверженность к индивидуальным и возрастным колебаниям, трудоемкость тестов, высокие экономические затраты, длительность получения результатов (48-72 часа), сложность интерпретации полученных результатов анализа не всегда позволяют выявлять иммунологическую недостаточность. К тому же эти тесты не диагностируют латентнотекущие формы ИН, развивающиеся на ранних этапах патологии.
Известно, что высокочувствительным индикатором, объективно отражающим формирование иммунного ответа организма на агрессию инфекционных и других агентов, являются антитела, поскольку от уровня специфических антител (в крови и секретах) и их протективной активности зависит устойчивость организма к патогенам, исход инфекционного процесса, эффективность профилактических прививок [2, 4, 5]. Более того, антитела раньше всех взаимодействуют с патогенами, образуя иммунные комплексы, которые индуцируют формирование селективного иммунного ответа с развитием локальных воспалительных процессов в местах внедрения этиотропных агентов. Таким образом, антитела являются решающим и мощным фактором приобретенного иммунитета, поскольку обеспечивают устойчивость организма к вирусам, бактериям, токсинам и другим патогенам за счет вовлечения в иммунный ответ защитных факторов естественного иммунитета (молекулярных и клеточных), которые без антител, сами по себе, лишены возможности селективно действовать на патогены.
В тоже время известно, что между количеством секретируемых аффинных к антигену антител и их протективной активностью не всегда отмечается корреляция. Например, при высоком титре антител к вирусу гриппа не всегда обеспечивается эффективная защита организма от этой инфекции. Это может быть связано с преимущественной секреции антител с низкой протективной активностью [2, 3, 6, 7] . Известно также, что на начальных этапах инфекционного процесса, а также у больных с хронически рецидивирующими инфекциями в фазе обострения обычно секретируемые антитела обладают низкой протективной активностью и низким авидитетом, в то время как в фазе выздоровления секретируются антитела с высокой протективной активностью и высоким авидитетом [6, 7, 12].
Однако определение протективной активности и авидитета антител по сей день является длительным (3-14 суток и более), сложным и трудоемким процессом, поскольку оно основано на биотестировании с использованием контрольных и опытных групп лабораторных животных или культуры тканей. К тому же, полученные результаты при биотестировании зависят от большого числа факторов и не всегда однозначно интерпретируются и совпадают с клиническими данными [2, 6].
Известен экспресс способ оценки функциональной активности В-системы иммунитета путем определения в сыворотке крови двух дискретных групп антител с высоким и низким авидитетом и определения наличия иммунологической недостаточности на основании снижения процента высокоавидных антител до 5-25% при норме 80-100% [9]. Этот способ взят за прототип.
Существенным недостатком прототипа является то, что дифференциация антител ведется только на основании их агглютинирующей способности в РПГА без учета функциональных и протективных свойств антител или их структурной организации, что значительно сужает диагностическую значимость выявляемой дисфункции В-системы иммунитета, не позволяет определить степень ее выраженности и оценить роль в патогенезе ВИД ассоциированных заболеваний.
Целью настоящего изобретения является разработка способа и набора для экспресс диагностики доклинических и клинически выраженных форм иммунологической недостаточности.
Указанная цель достигается тем, что низкоавидные нормальные и/или специфические антитела G класса трансформируют в высокоавидные с помощью физических, и/или химических, и/или биологических факторов и определяют до и после трансформирующего воздействия структурные, и/или функциональные, и/или протективные свойства антител, и/или содержание SH групп в IgG и по соотношению результатов, полученных до и после трансформации низкоавидных антител, для каждого показателя, соответственно, рассчитывают индекс модулирующего воздействия и определяют наличие иммунологической недостаточности, и/или степень ее выраженности, и/или судят о напряженности иммунитета, и/или эффективности формирующегося иммунного ответа организма, и/или оценивают степень дисфункции процесса созревания антител в плазматических клетках и/или дифференцируют с учетом клинических проявлений иммунодефицитных синдромов и их патогенеза четыре формы иммунологической недостаточности: две - (ЛИН-1 и ЛИН-2) в доклинической (латентнотекущей) стадии патологии и две - (ИН-1 и ИН-2) - в клинически выраженной стадии заболевания.
При этом показателями структурной характеристики IgG до и после трансформации низкоавидных антител в высокоавидные являются: устойчивость структуры макромолекулы и внутримолекулярных невалентных связей к диссипативным воздействиям, и/или доступность функциональных групп белка к селективным реагентам, и/или способность молекулы IgG взаимодействовать с белком А стафилококка, и/или моноклональными антителами к IgG, и/или связываться с лигандами пептидной природы, и/или чувствительность IgG к действию протеолитических ферментов, и/или химическим, и/или физическим воздействиям.
При этом показателями функциональных свойств IgG являются: функциональный аффинитет, и/или реакционная активность, и/или авидитет, и/или функциональный антагонизм антител.
Показателями протективных свойств IgG являются: способность антител образовывать крупные и средние иммунные комплексы, и/или способность антител активировать классический путь системы комплемента, и/или способность антител активировать клеточно-опосредованные механизмы защиты через Fc и CR рецепторы иммунокомпетентных клеток, и/или опсоническая активность, и/или вируснейтрализующая активность, и/или антитоксическая активность, и/или цитотоксическая активность антител.
Для трансформации низкоавидных антител в высокоавидные в качестве физических факторов воздействия используют оптические, и/или ультразвуковые, и/или рентгеновские, и/или электромагнитные излучения.
Для трансформации низкоавидных антител в высокоавидные в качестве химических факторов воздействия используют денатурирующие реагенты, и/или детергенты, и/или соли одновалентных, и/или двухвалентных, и/или тяжелых металлов, и/или восстановители, и/или окислители, и/или тиоловые, реагенты, и/или спирты, и/или антиоксиданты, и/или высокомолекулярные соединения, и/или коллоиды, и/или полимеры.
Для трансформации низкоавидных антител в высокоавидные в качестве биологических факторов воздействия используют компоненты системы комплемента, и/или антитела, и/или сывороточный альбумин, и/или белки, и/или пептиды.
Изменение в динамике индекса модулирующего воздействия в сторону уменьшения свидетельствует о снижении структурных, и/или функциональных, и/или протективных свойств антител, и/или увеличении степени дисфункции процесса созревания антител в плазматических клетках, и/или увеличении степени выраженности иммунологической недостаточности и перехода формы с меньшей степенью выраженности в форму с больше (ЛИН-1 или в ЛИН-2, или ИН-1 или ИН-2) и/или уменьшении напряженности иммунитета, а изменение в динамике индекса модулирующего воздействия в сторону увеличения свидетельствует о повышении структурных, и/или функциональных, и/или протективных свойств антител, и/или уменьшении степени дисфункции процесса созревания антител в плазматических клетках, и/или уменьшении степени выраженности иммунологической недостаточности и перехода формы с большей степенью выраженности в меньшую или норму, и/или повышении напряженности иммунитета, и/или иммунологической ремиссии.
В набор для экспресс-диагностики доклинических и клинически выраженных форм иммунологической недостаточности дополнительно введены агент, вызывающий трансформацию низкоавидных антител в высокоавидные, и две эталонные сыворотки, одна из которых содержит высокоавидные антитела, другая - низкоавидные антитела.
Агент, вызывающий трансформацию низкоавидных антител в высокоавидные, представляет собой денатурирующие реагенты, и/или детергенты, и/или соли одновалентных, и/или двухвалентных, и/или тяжелых металлов, и/или восстановители, и/или окислители, и/или тиоловые реагенты, и/или спирты, и/или антиоксиданты, и/или высокомолекулярные соединения, и/или коллоиды, и/или полимеры, и/или компоненты системы комплемента, и/или антитела, и/или сывороточный альбумин, и/или белки, и/или пептиды.
Кроме того, агента, вызывающего трансформацию низкоавидных антител в высокоавидные, представляет собой источник оптического, и/или ультразвукового, и/или рентгеновского, и/или электромагнитного излучения.
Благодаря разработанным подходам и способам диагностирования иммунологической недостаточности впервые была обнаружена ранее неизвестная форма иммунологической недостаточности, характеризующаяся преимущественным биосинтезом антител G класса с низким авидитетом и низким функциональным аффинитетом, неспособных оказывать протективный эффект.
Впервые было показано, что эффективность иммунного ответа лимитируется не расстройствами процессов активации, пролиферации и дифференциации аффинных к антигену клонов В-лимфоцитов в плазматические клетки, а в первую очередь расстройствами процесса созревания антител в плазматических клетках.
Супрессия этих механизмов, развивающаяся на самых ранних этапах агрессии патогенов, является причиной преимущественного биосинтеза антител с низким авидитетом (75-90%) неспособных выполнять протективные свойства, направленные на уничтожение и элиминацию чужеродных антигенов и патогенов из организма. Механизмы созревания антител, формирующие четвертичную структуру и авидитет антител в плазматических клетках, оказались самым ранимым звеном иммунной системы, дисфункция которого существенно лимитирует эффективность иммунного ответа организма на агрессию патогенов.
Персистенция антигенов и патогенов и циркулирующих иммунных комплексов в организме, связанная с нарастанием биосинтеза низкоавидных антител, ведет к ряду следствий, существенно увеличивающих спектр дисфункций иммунной системы организма. К ним относится:
- увеличение числа вовлеченных в иммунный ответ клонов В- и Т-лимфоцитов;
- усиление супрессии механизмов созревания антител в плазматических клетках;
- снижение аффинитета секретируемых антител;
- подавление активности антигенпрезентирующих клеток;
- снижение активности барьерных систем и повышение экспансии условно-патогенной микрофлоры;
- дисфункция субпопуляций Т-лимфоцитов, распознающих "свое" и "чужое";
- нарастанию числа фенотипически и генотипически измененных клеток и т. п.
Таким образом, дисфункция процесса созревания антител в ПК является триггерным механизмом развития ВИД-состояний и ассоцированных с ним заболеваний.
Благодаря возможности трансформации низкоавидных антител в высокоавидные удалось показать, что различия высокоавидных и низкоавидных антител обусловлены наличием в низкоавидных антителах дополнительных внутримолекулярных междоменных связей, ведущих к ограничению динамичности структуры макромолекулы и неспособности их поливалентно связываться с антигенами и выполнять эффекторные функции.
Селективное разрушение в низкоавидных антителах этих связей под действием трансформирующих воздействий ведет к существенным изменениям структуры, функциональной и протективной активности антител. Так, если до трансформации низкоавидные антитела, взаимодействуя с антигеном, образовывали мелкие, растворимые, непрочные иммунные комплексы, которые имели низкую аффинность к C1q компоненту комплемента, а также к Fc- и CR-клеточным рецепторам иммуннокомпетентных клеток (ИКК) и были неспособны активировать классический путь системы комплемента и клеточно-опосредованные механизмы неспецифической защиты, имели низкую опсоническую, антитоксическую, вируснейтрализующую, цитотоксическую активности, имели ограниченную динамичность макромолекулы и глубоко маскированные SH-группы, то в результате трансформации они приобретали способность образовывать средние и крупные прочные, трудно растворимые иммунные комплексы, при этом повышалась их аффинность к C1q компоненту комплемента, к Fc- и CR-клеточным рецепторам ИКК, они становились способными активировать классический путь системы комплемента, клеточно-опосредованные механизмы защиты, кроме того существенно повышалась их опсоническая, антитоксическая, вируснейтрализующая, цитотоксическая активности, а макроструктура приобретала высокую динамичность, при этом доступность SH-групп в IgG существенно возрастала.
Благодаря феномену трансформации впервые оказалось возможным количественно оценить "потенциальную", "нереализованную" активность значительной части (75-95%) секретируемых антител у больных с ВИД состояниями, которая ранее никем не выявлялась и не учитывалась. Впервые оказалось возможным объяснить давно известный феномен несоответствия между числом секретируемых к антигену антител и их протективной активностью. Чем выше степень несоответствия между содержанием антител и их протективной активностью до и после трансформации низкоавидных антител, тем выраженнее дисфункция процесса созревания антител в ПК и степень иммунологической недостаточности.
Наиболее адекватно это несоответствие оказалось возможным выразить с помощью цифрового выражения - индекса модулирующего воздействия Im, который рассчитывается как отношение величины того или иного показателя до и после трансформирующего воздействия, согласно формуле:
Im=А/Б,
где А - величина показателя до трансформации;
Б - величина показателя после трансформации;
Im - индекс модулирующего воздействия.
Величина индекса, близкая к 1,0, свидетельствует об исключительном содержании в пробе антител с высоким авидитетом, толерантных к действию трансформирующих факторов, высокой эффективности процесса созревания и биотрансформации антител в плазматических клетках, эффективности иммунного ответа, отсутствии иммунологической недостаточности, а индекс 0,5 и ниже свидетельствует о расстройствах процесса созревания антител и биотрансформации в плазматических клетках, наличии иммунологической недостаточности, низкой напряженности иммунитета.
Для того, чтобы объективно оценить степень иммунологической недостаточности, необходимо было оценить структурные, и/или функциональные, и/или протективные свойства антител до и после трансформирующего воздействия с помощью адекватных показателей.
В качестве показателей, характеризующих изменения структуры низкоавидных антител при действии трансформирующих факторов, были использованы: устойчивость структуры макромолекулы и внутримолекулярных невалентных связей к диссипативным воздействиям и/или доступность функциональных групп белка к селективным реагентам, и/или способность молекулы IgG взаимодействовать с белком А стафилококка, и/или моноклональными антителами к IgG, и/или связываться с лигандами пептидной природы, и/или чувствительность IgG к действию протеолитических ферментов, и/или химическим, и/или физическим воздействиям.
Показателями, адекватно отражающими функциональные свойства антител G класса, служили: функциональный аффинитет, и/или реакционная активность, и/или авидитет, и/или функциональный антагонизм антител.
Показателями протективных свойств IgG служили: способность антител образовывать крупные и средние иммунные комплексы, и/или способность антител активировать классический путь системы комплемента, и/или способность антител активировать клеточно-опосредованные механизмы защиты через Fc и CR-рецепторы иммунокомпетентных клеток, и/или опсоническая активность, и/или вируснейтрализующая активность, и/или антитоксическая активность, и/или цитотоксическая активность антител.
Благодаря разработке высокочувствительных критериев, позволяющих объективно следить за трансформацией низкоавидных антител в высокоавидные, был осуществлен широкий поиск индукторов трансформации. Такими индукторами (in vivo и in vitro) являются физические, и/или химические, и/или биологические факторы воздействия.
Выбор функциональных групп, в частности SH-групп, в качестве индикатора структурно-функциональной организации антител обусловлен тем, что их уровень адекватно отражает динамичность четвертичной структуры молекулы IgG и строго коррелирует (0,8-1,0) с авидитетом, функциональной аффинностью и протективной активностью антител.
Для трансформации низкоавидных антител в высокоавидные в качестве физических факторов воздействия были использованы оптические, и/или ультразвуковые, и/или рентгеновские, и/или электромагнитные излучения.
Для трансформации низкоавидных антител в высокоавидные в качестве химических факторов воздействия использовали денатурирующие реагенты, и/или детергенты, и/или соли одновалентных и/или двухвалентных, и/или тяжелых металлов, и/или восстановители, и/или окислители, и/или тиоловые реагенты, и/или спирты, и/или антиоксиданты, и/или высокомолекулярные соединения, и/или коллоиды, и/или полимеры.
Для трансформации низкоавидных антител в высокоавидные в качестве биологических факторов воздействия использовали компоненты системы комплемента, и/или антитела, и/или сывороточный альбумин, и/или белки, и/или пептиды.
В виду того, что дисфункция процесса созревания антител в плазматических клетках возникает на ранних этапах патологии и является триггерным механизмом, предопределяющим развитие расстройств процессов активации, пролиферации и дифференциации аффинных к антигенам клонов В- и Т-лимфоцитов и других звеньев иммунной системы, то в ряде случаев для определения степени выраженности ИН и вовлеченности дисфункции других звеньев иммунитета целесообразно дополнительное определение следующих показателей: абсолютного количества активированных В-лимфоцитов, и/или количества иммуноглобулинов (М и G класса), и/или аффинитета секретируемых антител, и/или определение уровня циркулирующих иммунных комплексов (ЦИК), и/или соотношения субпопуляций Т-лимфоцитов CD4 и CD8.
Поскольку между выраженностью иммунологической недостаточности и клиническими проявлениями существует причинно-следственная(ые) связь(и), то для постановки диагноза целесообразен учет клинических проявлений иммунологической недостаточности, в частности, степени выраженности иммунодефицитных синдромов (инфекционного, аллергического, аутоаллергического и др.), и/или дисбактериоза, и/или стадии развития болезни, и/или тяжести заболевания, и/или данных анамнеза. На основании совокупности данных, согласно разработанной нами классификации, становится возможным адекватное определение состояния иммунной системы и степени выраженности иммунологической недостаточности с дифференциацией четырех форм выраженности иммунологической недостаточности (двух в латентнотекущей стадии ЛИН-1, ЛИН-2 и двух в клинически выраженной стадии - ИН-1, ИН-2). Такая дифференциация иммунологической недостаточности крайне необходима для прогнозирования течения заболевания, его направленности, обоснования назначения цикла иммунокоррегирующей терапии, адекватной степени выраженности ИН.
Ниже приводятся конкретные примеры использования трансформации низкоавидных антител в высокоавидные под действием физических, химических и биологических факторов для диагностики доклинических и клинически выраженных форм иммунологической недостаточности.
Во всех нижеследующих примерах контроль трансформации низкоавидных IgG вели: а) на молекулярном уровне - на основании определения доступности функциональных групп белка, в частности SH, к селективным реагентам; б) на функциональном - путем определения реакционной способности нормальных и/или специфических к антигену антител.
1. Влияние физических, химических и биологических факторов на структурные и функциональные свойства антител G класса здоровых и больных со вторичным иммунодефицитом.
Пример 1.
Материалом для исследования служили:
а) сыворотка крови больного с выраженными явлениями иммунодефицита (ИД), содержащая 12% высокоавидных и 88% низкоавидных антител,
б) сыворотка крови донора, содержащая исключительно высокоавидные антитела,
в) препараты IgG, выделенные из исследуемых сывороток крови донора и больного
с ИД до и после действия на сыворотку физических, химических и биологических факторов.
Степень воздействия трансформирующих факторов подбиралась эмпирически с учетом структурных и/или функциональных изменений низкоавидных антител до выявления критической точки, после которой прекращались какие-либо структурно-функциональные изменения антител.
В качестве физического фактора воздействия использовали низкоинтенсивное некогерентное излучение в ИК-диапазоне. В качестве химического фактора воздействия использовали соль тяжелого металла. В качестве биологического фактора воздействия использовали сывороточный альбумин.
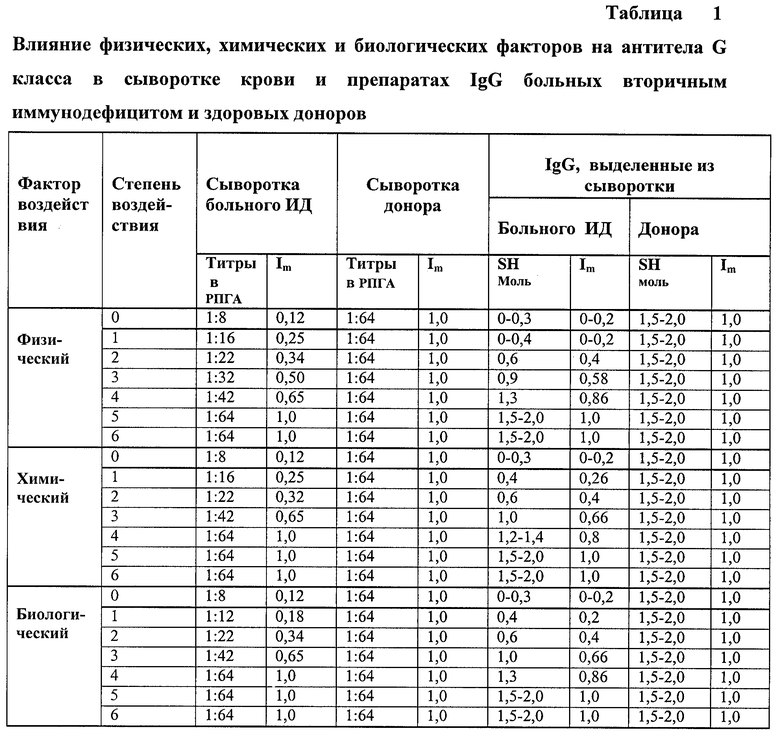
Из таблицы 1 видно, что процесс трансформации низкоавидных антител в высокоавидные стереотипен как для сыворотки крови, так и для препаратов IgG и не зависит от природы трансформирующих факторов.
Между степенью воздействия трансформирующего фактора и увеличением числа SH-групп в препаратах IgG (с 0-0,3 до 1,5-2,0 моль/моль белка) и/или нарастании титров нормальных антител в РПГА (с 1:8 до 1:64) прослеживается линейная зависимость.
Высокоавидные и низкоавидные антитела существенно различаются по количеству SH-групп, доступных к селективным реагентам, и по реакционной способности нормальных и/или специфических к антигену антител, выявляемых в РПГА. Эти различия носят выраженный дискретный характер.
Отражением степени трансформации низкоавидных антител в высокоавидные является индекс модулирующего воздействия, который коррелирует с интенсивностью воздействия. Достижение стабильного значения индекса свидетельствует о завершенности процесса трансформации низкоавидных антител.
Величина индекса, близкая к 1,0, является показателем исключительного содержания в пробе антител с высоким авидитетом, толерантных к трансформирующим воздействиям, и характерна для здоровых людей (доноров), величина индекса ниже 0,5 свидетельствует о наличии низкоавидных антител, чувствительных к действию трансформирующих факторов и характерна для больных с иммунодефицитом, остальное - промежуточное состояние.
Идентичность результатов процесса трансформации низкоавидных антител как в сыворотке крови, так и препаратах IgG свидетельствует о том, что в обоих случаях точкой приложения трансформирующего фактора являются исключительно низкоавидные антитела.
Исходя из данных эксперимента можно заключить, что:
а) антитела с высоким и низким авидитетом можно дифференцировать на основании структурных и/или функциональных свойств;
б) на основании величины индекса модулирующего воздействия можно количественно определить содержание низкоавидных антител;
в) на основании изменения содержания низкоавидных антител в результате трансформирующего воздействия можно определить наличие иммунологической недостаточности и оценить степень ее выраженности.
2. Роль функциональной аффинности в диагностике и патогенезе иммунодефицитных состояний.
2.1. Влияние трансформирующих факторов на функциональную аффинность низкоавидных антител G класса.
Селективность взаимодействия антител G класса определяется сродством активного центра антител к антигену, а также числом активных центров в антителах, взаимодействующих с антигеном, т.е. валентностью антител или функциональной аффинностью [10-12].
Интерес к функциональной аффинности диктовался тем, что только поливалентное связывание антител с антигеном обеспечивает реализацию эффекторных функций антител, т.е. их протективную активность. Такой способностью обладают только высокоавидные антитела.
Поскольку при иммунодефицитах 75-90% секретируемых антител G класса имеют низкий авидитет, то представлялось крайне важным выяснить:
а) имеется ли взаимосвязь между авидитетом и функциональным аффинитетом антител,
б) существует ли конкуренция между высокоаффинными и низкоаффинными к антигену антителами и как эта конкуренция сказывается на результатах иммунологических реакций,
в) как трансформация низкоавидных антител в высокоавидное отражается на их функциональной аффинности и протективной активности антител и можно ли эти различия использовать для диагностики иммунодефицитных состояний.
Для того, чтобы показать взаимосвязь между функциональной аффинностью антител и их авидитетом, а также существенные различия между реальной и потенциальной активностью антител, которая является главенствующим показателем иммунодефицита, нами были использованы следующие методы:
A) колоночная иммуносорбция, позволяющая количественно определять почти все аффинные к антигену антитела,
Б) агглютинация в РПГА, позволяющая по скорости появления и стабильности агглютинатов определять реакционную активность антител и выявлять наличие или отсутствие функционального антагонизма между антителами с высоким и низким аффинитетом,
B) оценка аффинности реакции АГ-АТ на основании определения физико-химических свойств циркулирующих иммунных комплексов (ЦИК) и/или их способности взаимодействовать с компонентами системы компонента и/или Fc- и CR-клеточными рецепторами иммунокомпетентных клеток.
2.2. Определение функциональной аффинности низкоавидных антител и влияния трансформирующего воздействия на их иммуносорбционную способность.
Для доказательства изменения функциональной аффинности низкоавидных антител после их трансформации в высокоавидные ниже приведены результаты исследований с использованием метода иммуносорбции.
Пример 2.
Материалом для исследования служили:
а) сыворотки пациентов с выраженными явлениями иммунодефицита, ассоциированного с поражением респираторных органов, которые содержали 25% высокоавидных антител и 75% - низкоавидных антител,
б) сыворотки здоровых доноров, содержащие 100% высокоавидных антител.
Каждая сыворотка (здорового донора и пациента с иммунодефицитом) была разделена на две равные части. Одна часть оставалась интактной и служила контролем, а другая - подвергалась действию трансформирующего фактора.
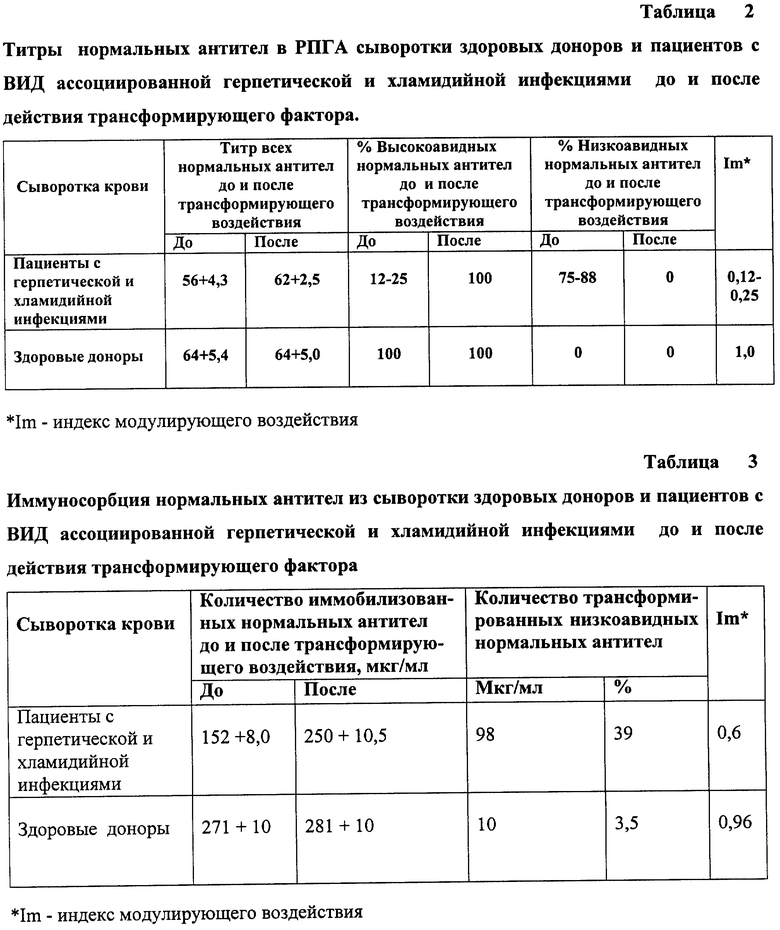
Количество аффинных к антигену антител как в контрольных, так и экспериментальных пробах определяли методом иммуносорбции. Кроме того было проведено определение содержания SH-групп в чистых препаратах IgG, элюированных с сорбента. Результаты представлены в таблицах 2 и 3.
Из таблиц 2 и 3 видно, что эффект трансформирующего воздействия наблюдался только на сыворотке больного ИД. Индекс модулирующего воздействия увеличился с 0,25 до 1,0.
Анализ результатов иммуносорбции сыворотки здорового донора показал, что сорбционная способность высокоавидных антител в результате трансформирующего воздействия совершенно не изменилась. В параллельных пробах (до и после трансформирующего воздействия) количества элюированных с сорбента аффинных антител были близки и составляли, соответственно 271+10 мкг и 281+10, т.е. индекс модулирующего воздействия был равен 0,96. Следовательно, в сыворотке здорового донора практически все антитела обладали не только высокой авидностью, но и высокой функциональной аффинностью к данному сорбенту.
Анализ результатов иммуносорбции сыворотки больного с ВИД до и после действия трансформирующего фактора показал, что сорбционная способность антител увеличилась с 152+8 мкг до 250 мкг. Это означает, что функциональная аффинность изменилась у 98 мкг, т.е. 60% низкоавидных антител. Индекс модулирующего воздействия соответствовал 0,6.
Однако величина индекса модулирующего воздействия, полученная в результате иммуносорбции, не совпадала со значениями, полученными методом РПГА, где индекс составлял 0,25. Это несоответствие свидетельствует о том, что у 20% трансформированных низкоавидных антител функциональная аффинность не изменилась и оставалась низкой для выявления их с помощью иммуносорбции.
Таким образом, предварительная трансформация низкоавидных антител с последующим этапом иммуносорбции позволила выявить несколько дискретных групп антител, различающихся по авидности и функциональной аффинности:
а) антитела с высоким авидитетом и высокой функциональной аффинностью, выявляемые в тривиальной постановке иммуносорбции;
б) антитела с высоким авидитетом, но низкой функциональной аффинностью;
в) антитела с низким авидитетом, но обладающих высокой функциональной аффинностью, которая проявляется только после трансформации низкоавидных антител в высокоавидное состояние;
г) антитела с низким авидитетом и низким функциональным аффинитетом, чувствительные к действию трансформирующих факторов, обнаруживаемые в РПГА, но не выявляющиеся (или теряющиеся) при иммуносорбции.
Таким образом, только с помощью трансформации низкоавидных антител в высокоавидные удалось доказать, что:
а) между авидитетом и функциональной аффинностью антител имеется выраженная взаимосвязь;
б) трансформация низкоавидных антител в высокоавидные ведет к повышению функциональной аффинности антител.
в) определение авидитета и функциональной аффинности антител могут быть использованы для диагностики иммунодефицитных состояний и контроля эффективности процесса созревания антител в плазматических клетках.
2.3. Диагностическая роль феномена функционального антагонизма между высокоаффинными и низкоаффинными антителами G класса.
Нами обнаружено, что у больных с иммунодефицитами при острых септических состояниях, гриппе, метастазировании опухолей, ВИЧ-инфицировании часто отмечается нестабильность формирующихся агглютинатов в РПГА, которые имеют выраженную тенденцию к разрушению. Оказалось, что нестойкость агглютинатов есть результат функционального антагонизма между антителами с высокой и низкой функциональной аффинностью за антиген, при этом антитела с низкой функциональной аффинностью и авидностью вытесняют из иммунных комплексов антитела с высокой аффинностью и авидитетом.
Ниже приводится пример определения степени выраженности иммунологической недостаточности на основании феномена функционального антагонизма между высоко- и низкоаффинными антителами за антиген.
Пример 3.
Материалом для исследования служила сыворотка крови больной М.С. (47 лет), страдающей раком матки IV стадии с метастазами в позвоночник, мочевой пузырь и толстый кишечник.
Результаты исследования в РПГА (см. табл. 4) показали, что в исходной сыворотке отмечаются:
а) увеличение уровня антителогенеза в 4 раза по сравнению с нормой,
б) резкое уменьшение процента высокоавидных антител - до 2-6%,
в) нарастание процента низкоавидных антител до 88-97%,
г) нестойкость агглютинатов и их разрушение, т.е. наличие выраженного функционального антагонизма между антителами к антигену.
В результате трансформации низкоавидных антител в высокоавидные произошло:
- увеличение функциональной аффинности антител,
- повышение прочности и стабильности агглютинатов (АГ-АТ),
- полное исчезновение феномена функционального антагонизма
Таким образом, феномен функционального антагонизма прежде всего зависит от авидитета антител.
Полученные данные позволяют заключить, что метастазирование протекает на фоне резко выраженной дисфункции процесса созревания антител в плазматических клетках, в результате чего антиидиотипические антитела неспособны тормозить рост опухолевых клеток.
2.4. Роль авидитета и функционального аффинитета антител в формировании циркулирующих иммунных комплексов (ЦИК) и их физико-химических свойств.
Судьба антигенов, микроорганизмов и других патогенов, проникающих через тканевые барьеры в организм, зависит от наличия в циркулирующей крови аффинных к антигену антител и их способности быстро и прочно образовывать иммунные комплексы (ЦИК). В одних случаях образуются крупные и средние трудно растворимые иммунные комплексы, которые быстро захватываются фагоцитами и элиминируются из организма, в других - мелкие, растворимые, длительно циркулирующие в кровяном русле, которые являются причиной развития иммунопатологических процессов в тканях и органах.
Ниже приведены результаты эксперимента по выяснению ведущей роли авидитета антител в формировании физико-химических свойств ЦИК.
Пример 4.
Материалом для исследования служили:
а) сыворотка доноров, содержащие только высокоавидные антитела,
б) сыворотка больных с выраженными явлениями вторичного иммунодефицита, ассоциированного с герпетической инфекцией, содержащих 75-88% низкоавидных антител и 12-25% высокоавидных антител.
Каждая сыворотка была разделена на две части. Одна - оставалась интактной, другая - подвергалась низкоинтенсивному оптическому облучению, ведущему к трансформации низкоавидных антител в высокоавидные.
Содержание высокоавидных и низкоавидных нормальных антител до и после трансформирующего воздействия, а также полноту трансформации контролировали с помощью РПГА.
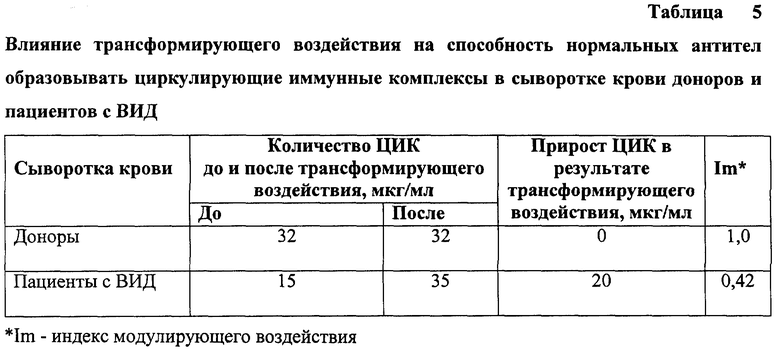
Количественная оценка образующихся в сыворотке ЦИК до и после трансформирующего воздействия проводилась с помощью общепринятого метода, основанного на способности полиэтиленгликоля (ПЭГ, м.м.4000) осаждать иммунные комплексы. Количество осажденного белка определяли спектрофотометрически (при длине волны 280 нм), предварительно растворив осадок в гидроокиси натрия. Расчет числа ЦИК вели на основании сопоставления результатов опытной пробы (в присутствии ПЭГ) с контрольной (в отсутствии ПЭГ).
Из таблицы 5 видно, что в сыворотке донора индекс модулирующего воздействия соответствовал 0,96-1,0, т.е. практически все антитела имели высокий авидитет. В параллельных пробах до и после трансформирующего воздействия количества осажденных ЦИК были идентичными. Следовательно, в сыворотке здорового донора практически все иммунные комплексы были образованы за счет высокоавидных антител и характеризовались высокой устойчивостью к действию трансформирующих факторов.
В сыворотке больного ИД индекс модулирующего воздействия соответствовал 0,12-0,25, т. е. трансформации подверглись 75-88% низкоавидных антител. В результате трансформации низкоавидных антител в высокоавидные количество осаждаемых иммунных комплексов увеличилось с 15 мкг до 35 мкг, т.е. в 2,5 раза, однако индекс модулирующего воздействия для ЦИК составил 0,42. Эта величина индекса не совпадала со значениями, полученными методом РПГА (0,25). Следовательно 20% трансформированных низкоавидных антител были неспособны к образованию осаждаемых в ПЭГ ЦИК.
Таким образом, только благодаря трансформации низкоавидных антител в высокоавидные удалось показать взаимосвязь между авидитетом антител, их функциональным аффинитетом и свойствами циркулирующих иммунных комплексов.
3. Взаимосвязь авидитета антител и их протективной активности на примере опсоно-фагоцитарной реакции.
Опсонизация бактерий представляет итог активной кооперации иммунных комплексов антител с системой комплемента и с Fc - и CR-рецепторами фагоцитов, в результате которой обеспечивается селективный захват и переработка антигенов и патогенов в фагоцитах. Однако, по сей день, нет достаточной ясности, в какой мере авидитет и функциональная аффинность антибактериальных антител влияют на опсоническую активность макрофагов.
Ниже приводится пример, подтверждающий ведущую роль авидитета антител и функциональной аффинности в феномене опсонизации бактерий в фагоцитах.
Пример 5.
Материалом для исследования служила кровь больной к Х.А., содержащая низкие титры антител к бруцеллам.
Имея возможность трансформировать низкоавидные антитела в высокоавидные, мы поставили цель выяснить, как отражается изменение авидитета антител к бруцеллам на их опсонической активности.
Свежая кровь в 2% растворе цитрата натрия центрифугировалась и разделялась на плазму и клеточную часть.
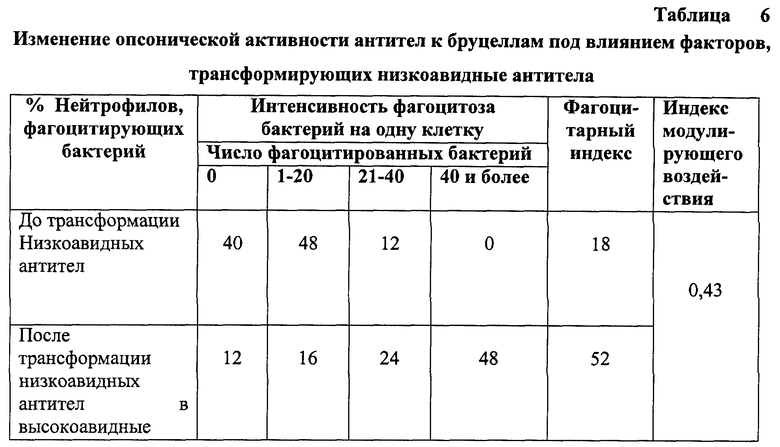
Для дальнейшего исследования плазма была разделена на две порции, одна оставалась интактной, а другая подвергалась трансформирующему воздействию. После чего, плазма обратно приливалась к клеточной суспензии и тщательно встряхивалась. В обе пробирки прибавляли взвесь термически убитых бруцелл и помещали в термостат при 37oС на 30 минут. Мазки готовили на предметных стеклах путем фиксации смесью Никифорова. Окраску мазков проводили по Романовскому-Гимза. Расчет цифрового показателя, отражающего обсонизацию, вели по четырем дискретным группам в зависимости от числа фагоцитированных бруцелл на один нейтрофил, а также на основании числа нейтрофиллов с фагоцитированными бактериями. Результаты исследования двух параллельных проб представлены в таблице 6.
Исследования показали, что в контрольной пробе из всех нейтрофилов только 12% обладало высокой фагоцитарной активностью, 48% - слабой активностью (от 1 до 20 бруцелл на одну клетку), а 40% нейтрофилов вообще не фагоцитировали бруцеллы.
После трансформации низкоавидных антител в высокоавидные произошло существенное увеличение фагоцитирования бруцелл. Интенсивное фагоцитирование бруцелл (21-40 и более) отмечалось у 72% нейтрофилов. При этом только 12% нейтрофилов не фагоцитировало бактерии.
Цифровой показатель, отражающий опсоническую активность нейтрофилов в интактной пробе, составлял 18, в трансформированной - 52, а индекс модулирующего воздействия соответствовал 0,34.
Таким образом, в результате трансформации антитела приобрели способность к:
а) опсонизации бактерий с существенным повышением аффинности ИК к компонентам системы комплемента и клеточным рецепторам нейтрофилов (Fc и CR),
б) активации поглотительной способности нейтрофилов, с дальнейшим их внутриклеточным перевариванием.
На примере опсоно-фагоцитарной реакции показана зависимость протективных свойств антител от их авидитета.
Более того, показана необходимость определения реальной и потенциальной опсонической активности антител, которая выражается величиной индекса модулирующего воздействия.
Величина индекса ниже 0,5 свидетельствует о риске развития генерализации инфекта в организме вследствие низкой протективной активности специфических антител, а величина индекса 05-1,0 - о высокой протективной активности секретируемых антител и высокой способности к элиминации патогенов из организма.
В таблице 7 представлены обобщенные данные, свидетельствующие, что трансформирующее воздействие ведет к существенным изменениям структурных, функциональных и протективных свойств низкоавидных антител.
Так, если до трансформации низкоавидные антитела, взаимодействуя с антигеном, образовывали мелкие, растворимые, непрочные иммунные комплексы, которые имели низкую аффинность к C1q компоненту комплемента, а также к Fc- и CR- клеточным рецепторам иммуннокомпетентных клеток (ИКК) и были неспособны активировать классический путь системы комплемента и клеточно-опосредованные механизмы неспецифической защиты, имели низкую опсоническую, антитоксическую, вируснейтрализующую, цитотоксическую активности, имели ограниченную динамичность макромолекулы и глубоко маскированные SH-группы, то в результате трансформации они приобретали способность образовывать средние и крупные прочные, трудно растворимые иммунные комплексы, при этом повышалась их аффинность к C1q компоненту комплемента, к Fc- и CR-клеточным рецепторам ИКК, они становились способными активировать классический путь системы комплемента, клеточно-опосредованные механизмы защиты, кроме того существенно повышалась их опсоническая, антитоксическая, вируснейтрализующая, цитотоксическая активности, а макроструктура приобретала высокую динамичность, при этом доступность SH-групп в IgG существенно возрастала (таблица 7).
Таким образом благодаря трансформации трансформации низкоавидных антител в высокоавидные впервые оказалось возможным объяснить давно известный феномен несоответствия между числом секретируемых к антигену антител и их протективной активностью, количественно оценить реальную и потенциальную активности антител и на основании их несоответствия судить о степени выраженности иммунологической недостаточности.
4. Дифференциация стадий и форм иммунологической недостаточности по степени их выраженности на основании патогенетического принципа и клинических проявлений иммунопатологических синдромов
Для диагностирования стадий и форм иммунологической недостаточности нами предлагается использование двух групп критериев, первая - характеризует интенсивность и эффективность селекционного отбора аффинных к антигенам клонов В-лимфоцитов и их дифференциацию в плазматические клетки, секретирующие антитела, вторая - характеризует процесс созревания антител в плазматических клетках.
В группу 1 входят следующие показатели:
а) абсолютное число В-лимфоцитов (CD 19+) и (CD 72+);
б) абсолютное количество в сыворотке крови нормальных и/или специфических к антигену антител,
в) содержание неспецифических иммуноглобулинов IgG и IgM классов;
г) аффинитет антител.
В группу 2 входят следующие показатели:
а) процентное содержание высокоавидных нормальных и/или специфических к антигену антител,
б) процентное содержание антител с низким авидитетом;
в) функциональная аффинность секретируемых антител;
г) содержание функциональных групп в IgG, выявляемых с помощью селективных реагентов;
д) уровень мелких циркулирующих иммунных комплексов;
е) выраженность функционального антагонизма между высокоаффинными и низкоаффинными антителами G класса;
ж) протективные свойства секретируемых антител G класса.
Помимо этого для оценки степени выраженности ИН и дифференциации форм ИН учитываются: клинические проявления иммунологической недостаточности, в частности, степени выраженности иммунодефицитных синдромов (инфекционного, аллергического, аутоаллергического и др.), и/или дисбактериоза, и/или стадии развития болезни, и/или тяжести заболевания, и/или анамнестических данных.
На основании вышеуказанных критериев нами разработана принципиально новая патогенентически обоснованная классификация с дифференциацией четырех форм выраженности иммунологической недостаточности (двух в латентнотекущей стадии ЛИН-1, ЛИН-2 и двух в клинически выраженной стадии - ИН-1, ИН-2). Такая дифференциация иммунологической недостаточности крайне необходима для прогнозирования течения заболевания, его направленности, обоснования назначения цикла иммунокоррегирующей терапии адекватной степени выраженности ИН.
4.1. Характеристика форм иммунологической недостаточности на основании патогенетического принципа.
4.1.1. Латентнотекущая форма иммунологической недостаточности 1-ой степени ЛИН-1).
ЛИН-1 - характеризуется биосинтезом антител с низким авидитетом (50-75%), низкой доступностью функциональных групп IgG к селективным реагентам, в частности SH-групп на 25-35%. Эти изменения отмечаются на фоне нормального или повышенного антителогенеза за счет антител G класса. При ЛИН-1 нарастает уровень мелких ЦИК, степень выраженности дисбактериоза, носительство патогенных возбудителей, повышается чувствительность к действию различных этиотропных факторов. Клинические проявления ЛИН-1 отсутствуют. Форма ЛИН-1 патогенетически связана с:
а) суперактивацией В-системы иммунитета за счет поступления в организм антигенов, которая выражается в увеличении числа активированных В-лимфоцитов и увеличении уровня антителогенеза;
б) расстройствами процесса созревания антител в плазматических клетках, индикатором которых является появление и нарастание в сыворотке крови и секретах антител с низким авидитетом.
4.1.2. Латентнотекущая форма иммунологической недостаточности 2-ой степени (ЛИН-2).
ЛИН-2 форма отличается от ЛИН-1 формы тем, что при ней отмечаются:
а) более выраженное увеличение процента активированных В-лимфоцитов;
б) нарастание уровня антител в крови;
в) нарастание выраженности расстройств процесса созревания антител в плазматических клетках, с увеличением процента низкоавидных антител;
г) снижение доступных функциональных групп в препаратах IgG на 35-40%.
Особенностью ЛИН-2 является отсутствие каких-либо клинических проявлений развивающейся дисфункции иммунитета. Иногда отмечается утомляемость при нагрузках, подверженность к простудным заболеваниям верхних дыхательных путей, развитию легких и средних форм дисбактериоза. На этом фоне эффективность профилактических прививок снижается в виду преимущественного биосинтеза антител с низким авидитетом, увеличивается риск развития поствакцинальных осложнений.
Таким образом, в основе патогенеза ЛИН-1 и ЛИН-2 форм лежат расстройства процессов созревания антител в плазматических клетках, развивающиеся на самых ранних этапах действия этиотропных агентов и ведущие к преимущественному биосинтезу антител с низким авидитетом.
4.1.3. Клинически выраженная форма иммунологической недостаточности 1-ой степени - (ИН-1)
ИН-1 - характеризуется прогрессивным снижением не только авидитета антител, но часто и снижением функционального аффинитета антител, проявляющегося в виде функционального антагонизма между высокоаффинными и низкоаффинными антителами. При этом отмечается появление клинической симптоматики ИН в виде острых или хронических инфекций и/или аллергических и воспалительных процессов с поражением респираторных органов, желудочно-кишечного тракта и т.п. Патогенетически эта форма ИН-1 тесно связана с ЛИН-2 и является фактически продолжением ее развития. Она сопровождается супрессией процессов активации, пролиферации и дифференциации В-лимфоцитов в плазматические клетки, вследствие чего падает аффинитет антител (истинный и функциональный). Часто происходит снижение образования антител IgA и IgG изотипов. Повышается степень выраженности дисбактериозов. Увеличивается количество мелких иммунных комплексов и их связывание с тканями и органами.
4.1.4. Клинически выраженная форма иммунологической недостаточности 2-ой степени - (ИН-2)
Если граница между ЛИН-2 и ИН-1 прослеживается на основании субклинических проявлений ИН-1, то дифференциация ИН-1 и ИН-2 расплывчата и основана на выраженности клинических проявлений иммунодефицитных синдромов.
ИН-2 форма характеризуется: суперактивацией В-системы иммунитета, нередко с супрессией антителогенеза, особенно IgA и IgG классов, иногда, нарастанием биосинтеза антител IgE класса, снижением истинного и функционального аффинитета антител, резко выраженной генерализацией патогенов в тканях и органах с развитием в них органных и системных поражений с клиническими проявлениями. Патогенез клинически выраженной формы иммунологической недостаточности связан с расстройствами процессов пролиферации и дифференциации В-лимфоцитов.
Благодаря предлагаемой классификации стадий и форм иммунологической недостаточности, основанной на патогенетическом принципе, открывается возможность объективного контроля за функциональной активностью иммунной системы, оценки степени ее дисфункции и разработки патогенетически обоснованных методов иммунокоррекции ВИД состояний и ассоциированных с ними заболеваниями.
Ниже приводятся примеры оценки степени выраженности иммунологической недостаточности на основании разработанных критериев при различных ВИД ассоциированных заболеваниях.
Пример 6.
Материалом для исследования служили:
сыворотки крови коров (68 гол.), инфицированных В-лимфотропным ретровирусом лейкоза крупного рогатого скота.
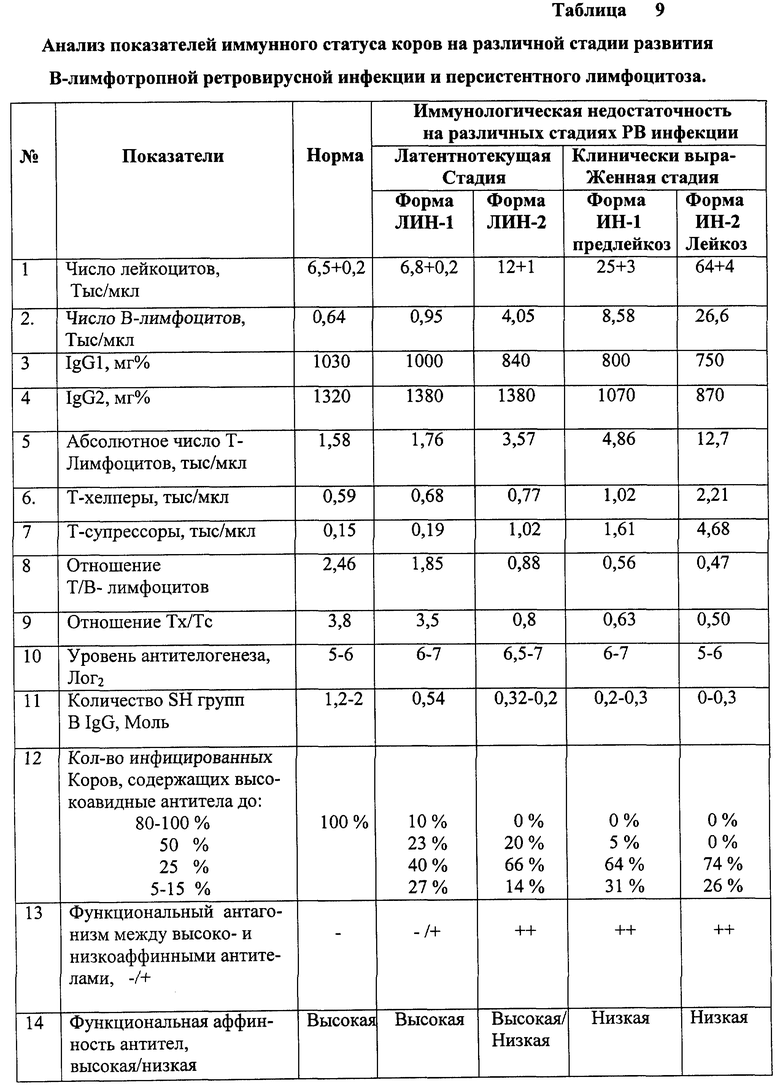
Исследование иммунного статуса проводили на различных стадиях развития В-лимфотропной ретровирусной инфекции и лейкозного процесса (латентная, предлейкоз, лейкоз).
Из приведенных данных в таблице 9 видно, что в латентной (доклинической) стадии развития ретровирусной инфекции со стороны клеточного иммунитета не отмечается каких-либо существенных изменений. Соотношение Тх к Тс остается без изменений. Изменения отмечаются лишь в В-системе иммунитета и проявляются в:
а) нарастании числа В-лимфоцитов (на 6-7%);
б) увеличении антителогенеза (в 2 раза);
в) резком снижении высокоавидных антител до 5-25% и нарастании низкоавидных (75-90%) антител у 67% инфицированных животных.
Таким образом на этой стадии развития ретровирусной инфекции нет расстройств процессов пролиферации и дифференциации Т- и В-клонов лимфоцитов, однако отмечаются существенные расстройства процесса созревания антител в плазматических клетках. В виду только наличия дисфункции процессинга антител при отсутствии расстройств процессов пролиферации и дифференциации субпопуляций В- и Т- лимфоцитов и клинических проявлений, данная форма иммунологической недостаточности может быть оценена как ЛИН-1 или ЛИН-2.
Прогрессия ретровирусной инфекции ведет к скачкообразному переходу из состояния компенсации в декомпенсацию, из доклинической стадии к клинически выраженную с расстройствами процессов пролиферации и дифференциации В-лимфоцитов. Число лейкоцитов возрастает в 2 раза, В-лимфоцитов - в 6,3 раза, процент высокоавидных антител снижается до 15-20% у 80% инфицированных животных. Отмечается снижение IgG1 подкласса на 20%. Отношение Тх/Тс падает с 3,8-3,5 до 0,8, число Т-супрессоров увеличивается в 6,8 раз в сравнении с нормой.
Дальнейшее развитие ретровирусной инфекции сопровождается экспоненциальным нарастанием расстройства пролиферации и дифференциации В-лимфоцитов и Т-супрессоров, появлением клонов со способностью автономного роста. Переход от "предлейкоза" к лейкозу идет на фоне ИН-1 или ИН-2.
Таким образом, показана правомерность использования предлагаемой принципиально новой классификации иммунологической недостаточности по степени выраженности на основе патогенетического принципа и разработанных нами критериев.
Пример 7.
Исследован иммунный статус больного (19 лет) атопическим дерматитом в фазе обострения.
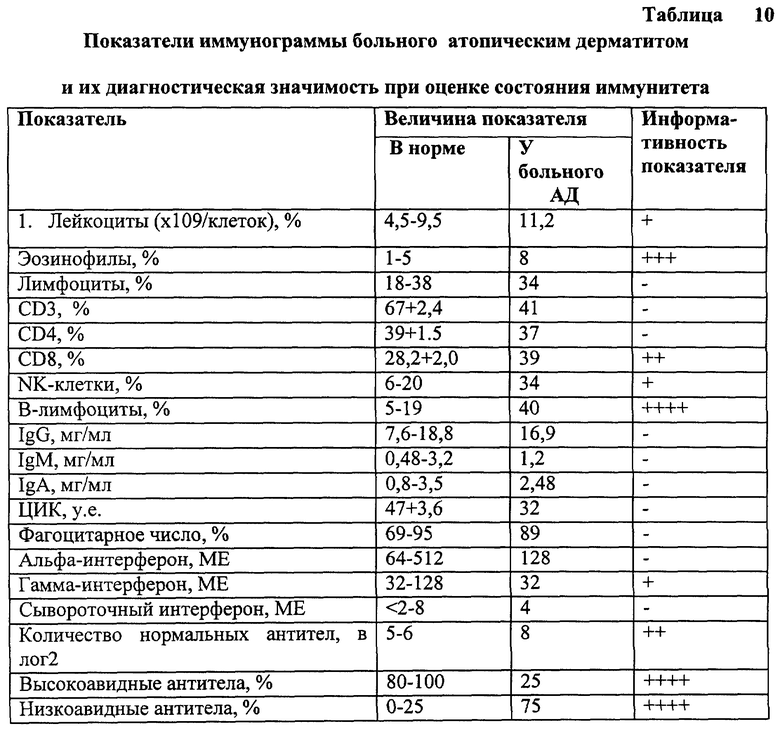
Цель исследования - отбор наиболее информативных показателей иммунограммы, отражающих течение атонического синдрома (таблица 10).
Как видно из таблицы 10 наиболее информативными оказались следующие показатели иммунограммы:
- процент В-лимфоцитов (СО 72);
- процент высокоавидных антител;
- процент низкоавидных антител;
- число эозинофилов в крови;
- увеличение CD 8 субпопуляции лимфоцитов;
- увеличение уровня антител в сыворотке крови в 2-4 раза в сравнении с нормой.
Остальные показатели иммунограммы больного оставались в пределах границ нормы.
Таким образом использование тривиальных методов оценки иммунного статуса у больных с атопическим синдромом является мало информативным.
5. Набор для экспресс диагностики доклинических и клинически выраженных форм иммунологической недостаточности.
Благодаря разработки критериев оценки структурных, функциональных и протективных свойств антител удалось получить принципиально новые представления о патогенезе развития иммунологической недостаточности и ее роли в ВИД ассоциированных заболеваниях. С помощью этих критериев было показано, что эффективность иммунного ответа лимитируется не расстройствами процессов активации, пролиферации и дифференциации аффинных к антигену клонов В-лимфоцитов в плазматические клетки, а в первую очередь расстройствами процесса созревания антител в плазматических клетках. Супрессия созревания антител в плазматических клетках, возникающая на самых ранних этапах агрессии патогенов, является причиной преимущественного биосинтеза антител с низким авидитетом и развитием ВИД состояний и ассоциированных с ним заболеваний.
Разработанные критерии были использованы для создания набора для экспресс диагностирования доклинических и клинически выраженных форм иммунологической недостаточности.
Широкое применение диагностического набора в клинической практике крайне важно для решения как минимум трех узловых задач, постоянно стоящих перед врачом и пациентом:
- есть или нет иммунологическая недостаточность у пациента;
- степень риска развития на фоне ИН патологии;
- решение вопроса о необходимости лечения.
Используя разработанный способ и диагностический набор на все эти вопросы в течение 2-х часов можно получить однозначные ответы. Преимущества разработанного способа и набора, в сравнении с тривиальными тест-системами оценки иммунного статуса, были проверены в клинической практике. Результаты сравнительного анализа представлены в таблицах 11 и 12.
Литература
1. Петров Р. В. , Лопухин Ю.В., Чередеев А.Н. Оценка иммунного статуса человека. М., 1984, 36 с.
2. Клиническая иммунология и аллергиология. Под ред. Л. Йегера, т. 1-3, М.: Медицина, 1990.
3. Новиков Д. К. , Новиков В.И. Оценка иммунного статуса. - Москва-Витебск, 1996, 282 с.
4. Петров Р.В., Хаитов P.M., Пинегин Б.В., Черноусов А.Т. Донозоологическая диагностика нарушений иммунной системы. - Иммунология, 1995, 2, 4-6.
5. Иммунологические методы. Под ред. Г. Фримеля, 1987, 472 с.
6. Иммунологическая диагностика вирусных инфекций. Под ред. Т.В. Пирадзе и Ц. Халонена. Совместное издательство СССР-Финляндия, М.: Медицина, 1985, 30с.
7. Райт А. Основы иммунологии. - Изд. Мир, М., 1991.
8. Незлин Р.С. Биохимия антител. - Изд. Наука, М., 1966, 295с.
9. Гевондян В. С., Гевондян Н.М. Экспресс-способ оценки функциональной активности В-системы иммунитета. Патент РФ 2137133, приоритет 24.07.1996. Бюллетень 25, 10.09.1999.
10. Стьюард М. Аффинность реакции антиген-антитело и ее биологическое значение. В Сб. : Структура и функция антител. Пер. с англ. под ред. Л. Глина, М. Стьюарда. М.: Мир, 1983, 113-144.
11. Кату Р. Конформация иммуноглобулинов в растворе. В книге Иммуноглобулины. Под ред. Г. Литмена, Р. Гуда, Изд. Мир, 1981, 58-113.
12. Каруш Ф. Сродство антител: пределы, изменчивость, роль поливалентности: в кн. Иммуноглобулины. Под ред. Г. Литмена, Р. Гуда, Изд. Мир, М., 1981, 121-159.





Изобретение относится к области медицины, в частности к иммунологии. Способ и набор обеспечивают экспресс-диагностику (в течение 2 ч) доклинических и клинически выраженных форм иммунологической недостаточности. Проводят определение в сыворотке крови или секретах наличие увеличения секреции низкоавидных антител относительно нормы, при этом в сыворотке крови, и/или лимфе, и/или секретах низкоавидные нормальные и/или специфические к антигену антитела G класса трансформируют в высокоавидные путем селективного воздействия на внутримолекулярные междоменные связи с помощью физических, и/или химических, и/или биологических факторов и определяют до и после трансформирующего воздействия структурные, и/или функциональные, и/или протективные свойства антител и/или содержание SH групп в IgG и по соотношению результатов, полученных до и после трансформации низкоавидных антител, для каждого показателя соответственно рассчитывают индекс модулирующего воздействия и судят о наличии иммунологической недостаточности и степени ее выраженности и/или форме иммунологической недостаточности - доклинической латентнотекущей (ЛИН-1 или ЛИН-2) или клинически выраженной (ИН-1 или ИН-2) и/или напряженности иммунитета и эффективности формирующегося иммунного ответа организма и степени дисфункции процесса созревания антител в плазматических клетках. 2 с. и 8 з.п. ф-лы, 12 табл.
| ЭКСПРЕСС-СПОСОБ ОЦЕНКИ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ B-СИСТЕМЫ ИММУНИТЕТА ПО ГЕВОНДЯН | 1996 |
|
RU2137133C1 |
| РОИТ А | |||
| Основы иммунологии | |||
| - М.: Мир, 1991, с.75-78, 69-70 | |||
| СПОСОБ ДИАГНОСТИКИ АУТОИММУННОЙ ПАТОЛОГИИ | 1991 |
|
RU2012887C1 |
| СПОСОБ ОЦЕНКИ ИММУНОЛОГИЧЕСКОЙ РЕАКТИВНОСТИ ОРГАНИЗМА | 1996 |
|
RU2126154C1 |
| RU 2058552 C1, 20.04.1996 | |||
| US 4665021 А, 12.05.1987 | |||
| US 5827750 A, 27.10.1998 | |||
| DE 3744674 A1, 10.11.1988. | |||
Авторы
Даты
2003-01-10—Публикация
2000-03-06—Подача