Область техники, к которой относится изобретение
Настоящее изобретение относится к классу металлокомплексов, лигандам для получения этих металлокомплексов и к полученным из них катализаторам полимеризации олефинов, особенно пригодным для применения в процессах полимеризации для получения полимеров путем полимеризации α-олефинов и смесей α-олефинов.
Предпосылки создания изобретения
Металлокомплексы ограниченной геометрии и способы их получения раскрыты в заявках в США сер. 545403, поданной 3 июля 1990 г. (ЕР-А-416815); сер. 547718, поданной 3 июля 1990 г. (ЕР-А-468651); сер. 702475, поданной 20 мая 1991 г. (ЕР-А-514828); сер. 876268, поданной 1 мая 1992 г. (ЕР-А-520732) и сер. 8003, поданной 21 января 1993 г. (WO 93/19104), а также US-A-5055438, US-A-5057475, US-A-5096867, US-A-5064802, US-A-5132380 и WO 95/00526. Принципы изобретений всех указанных выше патентов или соответствующих заявок на патенты США включены, таким образом, в данное описание путем ссылки.
В патентах США 5350817 и 5304614 раскрыты циркониевые комплексы с мостиковыми металлоценовыми лигандами, где две инденильные группы ковалентно связаны друг с другом посредством мостика, содержащего углерод или кремний, которые (комплексы) полезны для полимеризации пропилена.
В ЕР-А-577581 раскрыты несимметричные бис-Ср (циклопен-тадиенил) металлоценов с фторсодержащим лигандом, имеющим заместители, содержащие гетероатом.
У Е. Barsties, S. Schaible, M.-H. Prosenc, U. Rief, W. Roll, O. Weyland, B. Dorerer, H.-H. Brintzinger "J. Organo-metallic Chem.", 1996, 520, 63-68, и Н. Plenio, D. Birth "J. Organo-metallic Chem.", 519, 269-272 раскрыты системы, в которых циклопентадиенильное кольцо инденила является замещенным диметиламиногруппой в бис-индениле без мостиковой связи и с Si-мостиком, для получения изотактических полипропилена и полиэтилена.
У R. Leino, H.J.K. Luttikhedde, P. Lehmus, C.-E. Wilen, R. Sjoholm, A. Lehtonen, J. Seppala, J.H. Nasman "Macromolecules", 1997, 30, 3477-3488 раскрыты снабженные С2-мостиком бис-инденильные металлоцены с кислородом в 2-положении инденильной группы и у I.M. Lee, W.J. Gauthier, J. M. Ball, В. Iyengar, S. Collins "Organometallics", 1992, 11, 2115-2122 раскрыты снабженные С2-мостиком бис-инденильные металлоцены с кислородом в 5,6-положениях инденильной группы, а у N. Piccolravazzi, P. Pino, G. Consiglio, A. Sironi, M. Moret "Organometallics", 1990, 9, 3098-3105 раскрыты безмостиковые бис-инденильные металлоцены с кислородом в положениях 4 и 7 инденильной группы.
Считалось, что в противоположность углеродному или Н-замещению гетероатомное замещение в любом положении инденильной системы металлоценового комплекса при использовании в катализаторе полимеризации олефина делает катализатор менее активным, то есть производительность катализатора при полимеризации α-олефинов снижается, а полученный полимер имеет пониженную молекулярную массу с более низкой регулярностью молекулярной структуры. Предполагалось, что пониженная активность этого широкого класса катализаторов обусловлена взаимодействием неподеленной пары электронов гетероатома с активатором полимеризации при использовании сокатализатора на основе кислоты Льюиса, в результате чего Ср кольцо становится более электронодезактивированным, а также более пространственно затрудненным. См. Р. Foster, M.D. Rausch, J.C.W. Chien "J. Organometallic Chem.", 1996, 519, 269-272.
Описание неупорядоченного гетероатомного замещения в моно-Ср металлоценах найдено в ЕР-А-416815, WO 95/07942, WO 96/13529, патентах США 5096867 и 5621126 и родственных материалах.
До настоящего времени считалось, что гетероатомное замещение в металлоценовых комплексах для применения в качестве катализаторов полимеризации олефинов имеет недостатки, обусловленные нежелательными взаимодействиями неподеленной пары электронов гетероатома либо с атомом переходного металла или другой молекулой металлоцена, либо с другими компонентами каталитической системы.
Уже внесены многочисленные усовершенствования в различные металлоценовые комплексы, используемые в качестве катализаторов полимеризации олефинов. Однако все еще остаются проблемы эффективности и дезактивации катализатора в условиях высокотемпературной полимеризации. Желательно было бы обеспечить возможность получения полиолефинов с более высокими молекулярными массами. Желательно было бы также обеспечить возможность улучшения других физических характеристик полученных полимеров путем изменения замещения в циклопентадиенильной группе металлоценовых комплексов, применяемых в каталитических системах полимеризации олефинов.
Краткое изложение сущности изобретения
В соответствии с настоящим изобретением предлагаются металлокомплексы, соответствующие формуле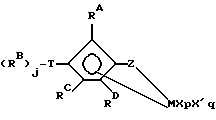
где М представляет металл одной из групп 3-13 Периодической таблицы элементов (лантаниды или актиниды), находящийся в формальной степени окисления +2, +3 или +4 и π-связанный с одной циклопентадиенильной группой (Ср), которая является циклической делокализованной π-связанной лигандной группой, имеющей 5 заместителей: RA; (RB)j-T, где j представляет 0, 1 или 2; RC; RD и Z, где RA, RB, RC и RD являются R группами; и где
Т представляет гетероатом, который ковалентно связан с Ср кольцом и с RB, когда j представляет 1 или 2, а когда j=0, то Т представляет F, Сl, Вr или I, когда j=1, Т представляет О или S, или N, или Р и RB имеет двойную связь с Т, и когда j=2, то Т представляет N или Р; и где
RB в каждом случае независимо представляет водород или группу, имеющую от 1 до 80 неводородных атомов, которая представляет собой гидрокарбил, гидрокарбилсилил, галогензамещенный гидрокарбил, гидрокарбилоксизамещенный гидрокарбил, гидрокарбиламинозамещенный гидрокарбил, гидрокарбилсилилгидрокарбил, гидрокарбиламино, ди(гидрокарбил)амино, гидрокарбилокси, причем каждый RB является необязательно замещенным одной или несколькими группами, независимо представляющими в каждом случае гидрокарбилокси, гидрокарбилсилокси, гидрокарбилсилиламино, ди(гидрокарбилсилил)амино, гидрокарбиламино, ди(гидрокарбил)амино, ди(гидрокарбил)фосфино, гидрокарбилсульфидо, гидрокарбил, галогензамещенный гидрокарбил, гидрокарбилоксизамещенный гидрокарбил, гидрокарбиламинозамещенный гидрокарбил, гидрокарбилсилил или гидрокарбилсилилгидрокарбил, имеющий от 1 до 20 неводородных атомов, или немешающую группу, имеющую от 1 до 20 неводородных атомов; и каждый из RA, RC и RD представляет водород или группу, имеющую от 1 до 80 неводородных атомов, которая представляет собой гидрокарбил, галогензамещенный гидрокарбил, гидрокарбилоксизамещенный гидрокарбил, гидрокарбиламинозамещенный гидрокарбил, гидрокарбилсилил, гидрокарбилсилилгидрокарбил, причем каждый RA, RC или RD является необязательно замещенным одной или несколькими группами, независимо представляющими в каждом случае гидрокарбилокси, гидрокарбилсилокси, гидрокарбилсилиламино, ди(гидрокарбилсилил)амино, гидрокарбиламино, ди(гидрокарбил) амино, ди(гидрокарбил)фосфино, гидрокарбилсульфидо, гидрокарбил, галогензамещенный гидрокарбил, гидрокарбилоксизамещенный гидрокарбил, гидрокарбиламинозамещенный гидрокарбил, гидрокарбилсилил или гидрокарбилсилилгидрокарбил, имеющий от 1 до 20 неводородных атомов, или немешающую группу, имеющую от 1 до 20 неводородных атомов; или, необязательно, два или более из RA, RB, RC и RD ковалентно связаны друг с другом с образованием одного или нескольких конденсированных колец или кольцевых систем, имеющих от 1 до 80 неводородных атомов для каждой R группы, причем одно или несколько конденсированных колец или кольцевые системы являются незамещенными или замещенными одной или несколькими группами, которые независимо в каждом случае представляют собой гидрокарбилокси, гидрокарбилсилокси, гидрокарбилсилиламино, ди(гидрокарбилсилил)амино, гидрокарбиламино, ди(гидрокарбил)амино, ди(гидрокарбил)фосфино, гидрокарбилсульфидо, гидрокарбил, галогензамещенный гидрокарбил, гидрокарбилоксизамещенный гидрокарбил, гидрокарбиламинозамещенный гидрокарбил, гидрокарбилсилил или гидрокарбилсилилгидрокарбил, имеющий от 1 до 20 неводородных атомов, или немешающую группу, имеющую от 1 до 20 неводородных атомов;
Z представляет двухвалентный фрагмент, связанный и с Ср, и с М посредством σ-связей, причем Z содержит бор или элемент группы 14 Периодической таблицы элементов, а также азот, фосфор, серу или кислород;
Х представляет анионную или дианионную лигандную группу, имеющую до 60 атомов, исключая класс лигандов, представляющих собой циклические делокализованные π-связанные лигандные группы;
X' в каждом случае представляет связывающее нейтральное основание Льюиса соединение, имеющее до 20 атомов;
р представляет 0, 1 или 2, причем значение его на два меньше, чем значение формальной степени окисления металла М, когда Х представляет анионный лиганд, а когда Х представляет дианионную лигандную группу, то р=1; и
q представляет 0, 1 или 2.
Вышеописанные комплексы могут существовать в виде отдельных кристаллов, необязательно в чистой форме, или в виде смеси с другими комплексами, в форме сольватированного аддукта, необязательно в растворителе, особенно органической жидкости, а также в форме димера или его хелатного производного, в котором хелатообразующим агентом является органический материал, предпочтительно нейтральное основание Льюиса, в частности тригидрокарбиламин, тригидрокарбилфосфин или их галогенированное производное.
В соответствии с настоящим изобретением предлагается также каталитическая система для полимеризации олефинов, полученная из компонентов, представляющих собой:
(A) катализатор, содержащий металлокомплекс, соответствующий одному из вышеописанных комплексов; и
(B) сокатализатор, содержащий активирующий сокатализатор, при молярном отношении (А) к (В) от 1:10000 до 100:1; или активацию компонента (А) с использованием активирующей технологии.
Другим вариантом осуществления настоящего изобретения является каталитическая система для полимеризации олефинов, полученная из компонентов, представляющих собой:
(А) катализатор, содержащий металлокомплекс, соответствующий одному из вышеописанных металлокомплексов; и
(В) сокатализатор, содержащий активирующий сокатализатор, при молярном отношении (А) к (В) от 1:10000 до 100:1,
причем металлокомплекс находится в форме радикал-катиона.
Еще в соответствии с настоящим изобретением предлагается способ полимеризации олефинов, включающий контактирование одного или нескольких С2-20 α-олефинов в условиях полимеризации с одной из вышеописанных каталитических систем.
Предпочтительным способом по настоящему изобретению является способ высокотемпратурной полимеризации олефинов в растворе, включающий контактирование одного или нескольких С2-20 α-олефинов в условиях полимеризации с одной из вышеописанных каталитических систем при температуре от примерно 100oС до примерно 250oС.
В объеме настоящего изобретения находятся полиолефиновые продукты, полученные описанным выше способом. Предпочтительные продукты имеют длинноцепочечную и короткоцепочечную молекулярную структуру.
В соответствии с настоящим изобретением предлагается также циклопентадиенилсодержащий лиганд одного из вышеописанных металлокомплексов, где лиганд находится в форме:
(A) свободного основания с 2 протонами, способными к депротонированию;
(B) дилитиевой соли;
(C) магниевой соли; и
(D) моно- или дисилированного дианиона.
В объеме этого варианта осуществления настоящего изобретения находится применение одного из указанных лигандов для синтеза с получением металлокомплекса по настоящему изобретению или для синтеза с получением металлокомплекса, содержащего металл из одной из групп 3-13 Периодической таблицы элементов (лантанидов или актинидов) и от 1 до 4 лигандов.
Предлагаемые катализаторы и способ обеспечивают высокоэффективное производство высокомолекулярных олефиновых полимеров в широких пределах условий полимеризации, в частности при повышенных температурах. Они особенно пригодны для полимеризации в растворе или в массе этилена и пропилена (ЭП полимеры), этилена и октена (ЭО полимеры), этилена и стирола (ЭС полимеры), пропилена и этилена, пропилена и диена (ЭПДМ полимеры), где диен представляет собой этилиденнорборнен, 1,4-гексадиен или подобный неконъюгированный (с несопряженными двойными связями) диен. Использование повышенных температур очень сильно повышает производительность таких процессов вследствие того, что повышенная растворимость полимера при повышенных температурах позволяет использовать повышенные степени конверсии (более высокая концентрация полимерного продукта) в рамках ограничений, налагаемых на оборудование для полимеризации в отношении вязкости раствора, и снижает затраты на энергию, необходимую на обезгаживание продукта реакции.
Катализаторы по настоящему изобретению могут быть также нанесены на носители и использованы в процессах полимеризации олефинов в суспензии или в газовой фазе. Катализатор может быть предварительно полимеризован с одним или несколькими олефиновыми мономерами на месте (in situ) в полимеризационном реакторе или в отдельном процессе с промежуточной регенерацией предварительно полимеризованного катализатора перед основным процессом полимеризации.
До настоящего времени считалось, что гетероатомное замещение непосредственно в циклопентадиенильной (Ср) группе, которая является циклической делокализованной π-связанной лигандной группой металлоценового комплекса, не оказывает благоприятного эффекта на полезность комплекса в каталитической системе для полимеризации олефинов. Однако теперь обнаружено, что предпочтительные металлоценовые комплексы по настоящему изобретению с гетероатомным замещением непосредственно в одиночной π-связанной Ср группе обладают необычными свойствами как катализаторы олефинов, позволяющими получать высокомолекулярные полимеры с требуемыми характеристиками при высокой активности катализатора. Особенно предпочтительными являются металлоценовые комплексы с гетероатомным замещением в положении 3.
Краткое описание фигур
Фиг. 1 - изображение кристаллической структуры дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато-(2-)-N-)-титана.
Фиг. 2 - изображение кристаллической структуры дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-метокси-1Н-инден-1-ил)силанаминато-(2-)-N-)титана.
Фиг. 3 - изображение кристаллической структуры [N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7a-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато-(2-)-N][(2,3,4,5-η)-2, 4-гексадиен)]-титана.
Подробное описание изобретения
Все ссылки в данном описании на Периодическую таблицу элементов относятся к Периодической таблице элементов, опубликованной с предупреждением об авторском праве издательством CRC Press, Inc., 1989. Кроме того, всякая ссылка на группу или группы подразумевает группу или группы в представленном в этой таблице виде с использованием системы ИЮПАК (IUPAC) для нумерации групп.
Олефины, о которых идет речь в данном описании, представляют собой С2-20 алифатические или ароматические соединения с винильной ненасыщенностью, а также циклические соединения, такие как циклобутен, циклопентен и норборнен, включая норборнен, замещенный в положениях 5 и 6 C1-20 гидрокарбильными группами. Включены также смеси таких олефинов, а также смеси таких олефинов с C4-40 диолефинами. Примеры последних соединений включают этилиденнорборнен, 1,4-гексадиен, норборнадиен и тому подобное. Предлагаемые в данном описании катализаторы и способы особенно пригодны для получения сополимеров этилена и 1-бутена, этилена и 1-гексена, этилена и стирола, этилена и пропилена, этилена и 1-пентена, этилена и 4-метил-1-пентена и этилена и 1-октена, а также тройных сополимеров этилена, пропилена и неконъюгированного диена, таких как, например, терполимеры ЭПДМ.
Предпочтительными группами X' являются моноксид углерода; фосфины, в частности триметилфосфин, триэтилфосфин, трифенилфосфин и бис(1,2-диметилфосфино)этан; P(ORi)3, где Ri представляет гидрокарбил, силил или их сочетание; простые эфиры, в частности тетрагидрофуран; амины, в частности пиридин, бипиридин, тетраметилэтилендиамин (ТМЭДА, TMEDA) и триэтиламин; олефины; и конъюгированные диены, имеющие от 4 до 40 углеродных атомов. Комплексы, содержащие последние группы X', включают те, в которых металл находится в формальной степени окисления +2.
Предпочтительными координационными комплексами по настоящему изобретению являются комплексы, соответствующие формуле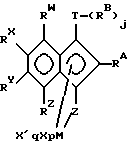
где RW, RX RY и RZ являются R группами, каждая из которых независимо представляет водород или группу, имеющую от 1 до 80 неводородных атомов, которая представляет собой гидрокарбил, галогензамещенный гидрокарбил, гидрокарбилоксизамещенный гидрокарбил, гидрокарбиламинозамещенный гидрокарбил, гидрокарбилсилил, гидрокарбилсилилгидрокарбил, причем каждый RW, RX, RY и RZ является необязательно замещенным одной или несколькими группами, независимо представляющими в каждом случае гидрокарбилокси, гидрокарбилсилокси, гидрокарбилсилиламино, ди(гидрокарбилсилил)амино, гидрокарбиламино, ди(гидрокарбил)амино, ди(гидрокарбил)фосфино, гидрокарбилсульфидо, гидрокарбил, галогензамещенный гидрокарбил, гидрокарбилоксизамещенный гидрокарбил, гидрокарбиламинозамещенный гидрокарбил, гидрокарбилсилил или гидрокарбилсилилгидрокарбил, имеющий от 1 до 20 неводородных атомов, или немешающую группу, имеющую от 1 до 20 неводородных атомов; или, необязательно, два или более из RW, RX, RY, RZ, RA и RB ковалентно связаны друг с другом с образованием одного или нескольких конденсированных колец или кольцевых систем, имеющих от 1 до 80 неводородных атомов для каждой R группы, причем одно или несколько конденсированных колец или кольцевые системы являются незамещенными или замещенными одной или несколькими группами, которые независимо в каждом случае представляют собой гидрокарбилокси, гидрокарбилсилокси, гидрокарбилсилиламино, ди(гидрокарбилсилил)амино, гидрокарбиламино, ди(гидрокарбил)амино, ди(гидрокарбил)фосфино, гидрокарбилсульфидо, гидрокарбил, галогензамещенный гидрокарбил, гидрокарбилоксизамещенный гидрокарбил, гидрокарбиламинозамещенный гидрокарбил, гидрокарбилсилил или гидрокарбилсилилгидрокарбил, имеющий от 1 до 20 неводородных атомов, или немешающую группу, имеющую от 1 до 20 неводородных атомов.
Предпочтительными RB группами являются те, в которых RB представляет гидрокарбил, гидрокарбилсилил, гидрокарбилоксизамещенный гидрокарбил, гидрокарбиламинозамещенный гидрокарбил и Т представляет О или N, более предпочтительными - те, в которых RB представляет гидрокарбил или гидрокарбилсилил и Т представляет О или N, и еще более предпочтительными - те, в которых RB представляет гидрокарбил или гидрокарбилсилил и Т представляет N.
Предпочтительными гетероатомсодержащими заместителями в 3-положении Ср являются те, в которых группа (RB)j-T представляет собой метокси, этокси, пропокси, метилэтилокси, 1,1-диметилэтилокси, триметилсилокси, 1,1-диметилэтил-(диметилсилил)окси, диметиламино, диэтиламино, метилэтиламино, метилфениламино, дипропиламино, дибутиламино, пиперидинил, морфолинил, пирролидинил, гексагидро-1Н-азепин-1-ил, гексагидро-1(2Н)-азоцинил, октагидро-1Н-азонин-1-ил или октагидро-1(2Н)-азецинил. Более предпочтительными являются те, в которых группа (RB)j-T представляет собой диметиламино, метилфениламино, пиперидинил или пирролидинил.
В еще одном варианте осуществления настоящего изобретения лиганд или металлокомплекс в дополнение к Ср или инденилу имеет одно или несколько конденсированных колец или кольцевые системы, которые содержат один или несколько кольцевых гетероатомов, которые представляют собой N, О, S или Р. Предпочтительными кольцевыми гетероатомами являются N или О, а более предпочтительным является гетероатом N.
Другие высокопредпочтительные комплексы соответствуют формуле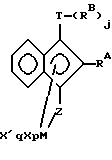
где символы - такие, как определенные выше, или более предпочтительные - формуле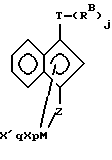
где символы - такие, как определенные выше.
Особенно предпочтительными являются металлокомплексы и их гетероатомсодержащие лиганды, где -Z- предстниляет -Z*-Y-, причем Z* связан с Ср и Y связан с М, и
Y представляет -О-, -S-, -NR*-, -PR*-;
Z* представляет SIR*2, CR*2, SIR*2SiR*2, CR*2CR*2, CR*=CR*, CR*2SiR*2, CR*2SiR*2CR*2, SiR*2CR*2SiR*2, CR*2CR*2SiR*2, CR*2CR*2CR*2 или GeR*2; и
R* в каждом случае независимо представляет водород или член, выбранный из гидрокарбила, гидрокарбилокси, силила, галогенированного алкила, галогенированного арила и их сочетаний, причем R* имеет до 20 неводородных атомов и, хотя это и не обязательно, две группы R* из Z (когда R* не является водородом) или группа R* из Z и группа R* из Y образуют кольцевую систему;
причем, когда р=2, q=0, M находится в формальной степени окисления +4 и Х в каждом случае независимо представляет метил, бензил, триметилсилилметил, аллил, пирролил или две группы Х вместе представляют 1,4-бутандиил, 2-бутен-1,4-диил, 2,3-диметил-2-бутен-1,4-диил, 2-метил-2-бутен-1,4-диил или ксилилдиил.
Также высокопредпочтительными являются металлокомплексы и их гетероатомсодержащие лиганды, где -Z- представляет -Z*-Y-, причем Z* связан с Ср и Y связан с М, и
Y представляет -О-, -S-, -NR*-, -PR*-;
Z* представляет SIR*2, CR*2, SIR*2SiR*2, CR*2CR*2, CR*=CR*; CR*2SiR*2, CR*2SiR*2CR*2, SiR*2CR*2SiR*2, CR*2CR*2SiR*2, CR*2CR*2CR*2 или GeR*2, и
R* в каждом случае независимо представляет водород или член, выбранный из гидрокарбила, гидрокарбилокси, силила, галогенированного алкила, галогенированного арила и их сочетаний, причем R* имеет до 20 неводородных атомов и, хотя это и не обязательно, две группы R* из Z (когда R* не является водородом) или группа R* из Z и группа R* из Y образуют кольцевую систему;
причем, когда р=1, q=0, M находится в формальной степени окисления +3 и Х представляет 2-(N,N-диметил)аминобензил, 2-(N,N-диметиламинометил)фенил, аллил, металлил, триметилсилилаллил.
Также высокопредпочтительными являются металлокомплексы и их гетероатомсодержащие лиганды, где -Z- представляет -Z*-Y-, причем Z* связан с Ср и Y связан с M, и
Y представляет -О-, -S-, -NR*-, -PR*-;
Z* представляет SiR*2, CR*2, SiR*2SiR*2, CR*2CR*2, CR*=CR*, CR*2SiR*2, CR*2SiR*2CR*2, SiR*2CR*2SiR*2, CR*2CR*2SiR*2, CR*2CR*2CR*2 или GeR*2; и
R* в каждом случае независимо представляет водород или член, выбранный из гидрокарбила, гидрокарбилокси, силила, галогенированного алкила, галогенированного арила и их сочетаний, причем R* имеет до 20 неводородных атомов и, хотя это и не обязательно, две группы R* из Z (когда R* не является водородом) или группа R* из Z и группа R* из Y образуют кольцевую систему;
причем, когда р=0, q=l, M находится в формальной степени окисления +2 и X' представляет 1,4-дифенил-1,3-бутадиен, 1,3-пентадиен или 2,4-гексадиен.
Для получения металлокомплексов по настоящему изобретению могут быть использованы самые разнообразные металлы, желательно металлы из одной из Групп 3-13 Периодической таблицы элементов (лантаниды или актиниды), которые находятся в формальной степени окисления +2, +3 или +4, более желательно металл из одной из Групп 3-13. Металлокомплексами по настоящему изобретению с несколько иными характеристиками являются те, в которых М представляет металл из одной из Групп 3-6, одной из Групп 7-9 или одной из Групп 10-12. Предпочтительными являются те, в которых М представляет металл из Группы 4, желательно Ti, Zr или Hf, из которых более предпочтительными являются Ti и Zr. Ti является наиболее высокопредпочтительным металлом, в частности, для применения в комплексах, которые содержат только один Ср-содержащий лиганд, являющийся гетероатомсодержащим лигандом по настоящему изобретению, а Zr является высокопредпочтительным для применения в комплексах, содержащих два Ср-содержащих лиганда, по крайней мере один из которых является гетероатомсодержащим лигандом.
В одном из вариантов является предпочтительным, чтобы Ti находился в формальной степени окисления +4, в другом варианте является предпочтительным, чтобы Ti находился в формальной степени окисления +3, и более предпочтительным является, чтобы Ti находился в формальной степени окисления +2.
В еще одном варианте является предпочтительным, чтобы Zr находился в формальной степени окисления +4 или же в формальной степени окисления +2.
С другой стороны, в соответствии с одним из вариантов настоящего изобретения является предпочтительным, когда Y представляет -NR*, более предпочтительным является -NR*, где R* представляет группу, имеющую первичный или вторичный углеродный атом, связанный с N. Является высокопредпочтительным, когда R* представляет циклогексил или изопропил.
Предпочтительным координационным комплексом является комплекс, соответствующий формуле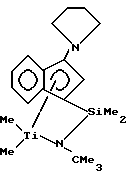
Иллюстративные производные металлов, которые могут быть использованы при осуществлении настоящего изобретения, включают:
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-2-этил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)- диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3, 3a,7a-η)-2-этил-6-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато-(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-4-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-5-этил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-6-(1-метилэтил)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато-(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-5-этил-6-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато-(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-5-бутил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-5-(1,1-диметилэтил)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато ( 2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-5-фенил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3, 4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-2-этил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-((1,2,3, 4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-4-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-5-этил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-6-(1-метилэтил)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато-(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-5-этил-6-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато-(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3, 3a,7a-η)-5-бутил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-((1,2,3, 4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-5-(1,1-диметилэтил)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3, 4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-5-фенил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-((1,2,3, 4-η)-1,3-пентадиен)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)- силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-2-этил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-2-этил-6-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-4-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-5-этил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-6-(1-метилэтил)-3-(1-пирролидинил)1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-5-этил-6-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-5-бутил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-5-(1,1-диметилэтил)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-5-фенил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а,7а-η)-2-этил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-циклогексил-1,1-диметил-1-((1,2,3,3a, 7a-η)-2-этил-6-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-4-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-циклогексил-1, 1-диметил-1-((1,2,3,3а, 7а-η)-5-этил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-6-(1-метилэтил)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-5-этил-6-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-5-бутил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а,7а-η)-5-(1,1-диметилэтил)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато-(2-)-N)диметилтитан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-5-фенил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,3а, 7а-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,3а, 7а-η)-2-этил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,3а, 7а-η)-2-этил-6-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато-(2-)-N)диметилтитан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,3а, 7а-η)-4-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,3а, 7а-η)-5-этил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,3а, 7а-η)-6-(1-метилэтил)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато-(2-)-N)диметилтитан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,3а, 7а-η)-5-этил-6-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато-(2-) -N)диметилтитан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,3а, 7а-η)-5-бутил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,3а, 7а-η)-5-(1,1-диметилэтил)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато-(2-)-N)диметилтитан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,3а, 7а-η)-5-фенил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-2-метил-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-) -N)диметилтитан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-2-этил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-2-этил-6-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)N)диметилтитан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-4-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-5-этил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-6-(1-метилэтил)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато-(2-)-N)диметилтитан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-5-этил-6-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)N)диметилтитан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-5-бутил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а,7а-η)-5-(1,1-диметилэтил)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-5-фенил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-метил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-этил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-фенил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(метилфенил)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-циклододецил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-1,1-диметил-N-(1-метилэтил)-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-бутил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил) -N-пропил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-метил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-этил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(1,1-диметил-N-фенил-1-((1,2,3,3a, 7a-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(1,1-диметил-N-(метилфенил)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-) -N)((1,2,3, 4-η)-1,3-пентадиен)титан
(N-циклододецил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N) ((1,2,3,4-η)-1,3-пентадиен)титан
(N-1,1-диметил-N-(1-метилэтил)-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-бутил-1,1-диметил-1- ((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен) титан
(1,1-диметил-N-пропил-1- ((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N) ((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3a,7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)-силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-метил-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-этил-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(1,1-диметил-N-фенил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(1,1-диметил-N-метилфенил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-циклододецил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)диметилтитан
((2-(диметиламино) фенил) метил)(N-1,1-диметил-N-(1-метил-этил)-1-((1,2,3, 3a,7a-η)-3-(1-пирролидинил)-1H-инден-1-ил)-силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-бутил-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(1,1-диметил-N-пропил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3, 3a,7a-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(гексагидро-1Н-азепин-1-ил)-1Н-инден-1-ил)силанаминато(2-) -N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7a-η)-3-гексагидро-1(2Н)-азоцинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(октагидро-1Н-азoнин-1-ил)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1- ((1,2,3,3а, 7а-η)-3-(октагидро-1(2Н)-азецинил)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(диметиламино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(диэтиламино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(дипропиламино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(дибутиламино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(этилметиламино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(метилфениламино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(метил(фенилметил)амино)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-((1,1-диметилэтил)метиламино)-1Н-инден-1-ил)силанаминато-(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(метил(1-метилэтил)амино)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3, 3a, 7a-η)-3-(дифенилфосфино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2, 3,3а, 7а-η)-3-(диметилфосфино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2, 3,3а,7а-η)-3-(метилфенилфосфино)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(диэтилфосфино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(бис(1-метилэтил)фосфино)-1Н-инден-1-ил)силанаминато(2-)-N) -диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-метокси-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7a-η)-3-этокси-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-пропокси-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-бутокси-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-((1,1-диметилэтил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(триметилсилокси)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-метилэтокси)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-фенокси-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(фенилтио)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(метилтио)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1 пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(гексагидро-1Н-азепин-1-ил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(гексагидро-1(2Н)-азоцинил)-1Н-инден-1-ил)силанаминато(2-) -N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(октагидро-1Н-азонин-1-ил)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(октагидро-1(2Н)-азецинил)-1Н-инден-1-ил)силанаминато(2-) -N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(диметиламино) -1Н-инден-1-ил)силанаминато(2-) -N)((1,2,3,4-η)1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(диэтиламино) -1Н-инден-1-ил)силанаминато(2-)-N)((1,2, 3,4 -η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7a-η)-3-(дипропиламино)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7a-η)-3-(дибутиламино)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η-,1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(этилметиламино)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(метилфениламино)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(метил(фенилметил)амино)-1Н-инден-1-ил)силанаминато(2-)-N)-((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1, 2,3,3а,7а-η)-3-((1,1-диметилэтил)метиламино)-1Н-инден-1-ил)силанаминато-(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(метил(1-метилэтил)амино)-1Н-инден-1-ил)силанаминато(2-)-N)-((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3a,7a-η)-3-(дифенилфосфино)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(диметилфосфино)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(метилфенилфосфино)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(диэтилфосфино)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(бис(1-метилэтил)фосфино)-1Н-инден-1-ил)силанаминато(2-)-N)-((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-метокси-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-этокси-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-l,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-
пропокси-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-бутокси-1Н-инден-1-ил)силанаминато(2-) -N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-((1,1-диметилэтил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил) -1,1-диметил-1-((1,2,3,3а,7а-η)-3-(триметилсилокси)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7a-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-метилэтокси)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-фенокси-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(фенилтио) -1H-инден-1-ил)силанаминато(2-) -N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(метилтио) -1Н-инден-1-ил)силанаминато(2-) -N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пиперидинил) -1Н-инден-1-ил)-силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(гексагидро-1Н-азепин-1-ил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3- (гексагидро-1(2Н)-азоцинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3- (октагидро-1Н-азонин-1-ил)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2, 3,3а, 7а-η)-3- (октагидро-1 (2Н) -азецинил) -1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3- (диметиламино) -1Н-инден-1-ил) -силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(диэтиламино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1- ((1,2, 3,3а, 7а-η)-3-(дипропиламино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3a,7a-η)-3-(дибутиламино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(этилметиламино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(метилфениламино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2, 3,3а,7а-η)-3-(метил(фенилметил)амино)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3a, 7a-η)-3-((1,1-диметилэтил)метиламине)-1Н-инден-1-ил)силанаминато-(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(метил(1-метилэтил)амино)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(дифенилфосфино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(диметилфосфино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(метилфенилфосфино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2, 3,3а,7а-η)-3-(диэтилфосфино)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(бис(1-метилэтил)фосфино)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-метокси-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-этокси-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-пропокси-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-бутокси-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-((1,1-диметилэтил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(триметилсилокси)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2, 3,3а,7а-η)-3-(1-метилэтокси)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-фенокси-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(фенилтио)-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(метилтио)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-дифенил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил) -1-метил-1-фенил-1-((1,2,3,3a, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-бис(1-метилэтокси)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диэтил-1-((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметокси-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-этокси-1-метил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-дифенил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил) -1-метил-1-фенил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-бис(1-метилэтокси)-1-((1,2,3,3а, 7а-η)-3- (1-пирролидинил) -1Н-инден-1-ил)силанаминато(2-) -N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диэтил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1,1-диметокси-1-((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1-этокси-1-метил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)-силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-
дифенил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)-силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1-метил-1-фенил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-бис (1-метилэтокси)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диэтил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)-силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметокси-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1-этокси-1-метил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)-силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил) титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил )бис((триметилсилил)метил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил) бис(2,2-диметилпропил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил) бис (бензол)(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил) силанаминато (2-)-N)((1,2,3,4-η)2,4-гексадиен)титан
((2-(диметиламино)метил)фенил)(N-циклогексил-1,1-диметил-1-((1, 2, 3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
дихлор(N-циклогексил-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)титан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил )бис((триметилсилил)метил)титан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил )бис(2,2-диметилпропил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол)(N-циклододецил-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-циклододецил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато (2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
((2-(диметиламино)метил)фенил)(N-циклододецил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
дихлор(N-циклододецил-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-циклододецил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил) титан
(N-циклододецил-1,1-диметил-1-((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил )бис((триметилсилил)метил)титан
(N-циклододецил-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил )бис(2,2-диметилпропил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил) бис (бензол)(N-метил-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)-силанаминато(2-)-N)титан
(N-метил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил) силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
((2-(диметиламино)метил)фенил)(N-метил-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил) силанаминато(2-)-N)титан
дихлор(N-метил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-метил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)- титан
(N-метил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис((триметилсилил)метил)титан
(N-метил-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис(2,2-диметилпропил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол)(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1-Н-инден-1-ил)силанаминато(2-)-N)титан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
((2-диметиламино)метил)фенил)(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
дихлор(1,1-диметил-N- (фенилметил)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)титан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис((триметилсилил)метил)титан
(1,1-диметил-N- (фенилметил)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис(2,2-диметилпропил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(-1-((1,2,3,3а, 7а-η)-3-(диметиламино)-1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)титан
(1-((1,2,3,3а,7а-η)-3-(диметиламино)-1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
((2-(диметиламино)метил)фенил)(1-((1,2,3,3а, 7а-η)-3-(диметиламино)-1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)титан
дихлор(1-((1,2,3,3а, 7а-η)-3-(диметиламино)-1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)титан
(1-((1,2,3,3а,7а-η)-3-(диметиламино)-1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)бис(фенилметил)титан
(1-((1,2,3,3а,7а-η)-3-(диметиламино)-1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)бис(фенилметил)бис((триметилсилил)метил)титан
(1- ((1,2,3,3а,7а-η)-3-(диметиламино)-1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)бис(фенилметил)бис(2,2-диметилпропил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)
-1,1-диметил-1-((1,2,3,3а,7a-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
((2-диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)-силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7a-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7a-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис((триметилсилил)метил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7a-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис(2,2-диметилпропил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-ди-метилэтил)-1,1-диметил-1-((1,2,3,3а, 7a-η)-3-(гексагидро-1H-азепин-1-ил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(гексагидро-1Н-азепин-1-ил)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(гексагидро-1Н-азепин-1-ил)-1Н-инден-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(гексагидро-1H-азепин-1-ил)-1Н-инден-1-ил)силанаминато-(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(гексагидро-1Н-азепин-1-ил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(гексагидро-1Н-азепин-1-ил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис((триметилсилил)метил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7a-η)-3-(гексагидро-1Н-азепин-1-ил)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис(2,2-диметилпропил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-метокси-1H-инден-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-метокси-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7a-η)-3-метокси-1Н-инден-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-метокси-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-метокси-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-метокси-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис-((триметилсилил)метил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-метокси-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис(2,2-диметилпропил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-этокси-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-этокси-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3a,7a-η)-3-этокси-1Н-инден-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-этокси-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7a-η)-3-этокси-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-этокси-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис-((триметилсилил)метил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-этокси-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис-(2,2-диметилпропил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-((1,1-диметилэтил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-((1,1-диметилэтил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)-((1,2,3,4-η)-2,4-гексадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-((1,1-диметилэтил) окси)-1H-инден-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-((1,1-диметилэтил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-((1,1-диметилэтил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)-бис(фенилметил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-((1,1-диметилэтил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)-бис(фенилметил)бис((триметилсилил)метил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-((1,1-диметилэтил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)-бис(фенилметил)бис(2,2-диметилпропил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)-титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(((1,1-диметилэтил) диметилсилил)окси)-1H-инден-1-ил)-силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис((триметилсилил)метил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)силанаминато(2-)-N)бис(фенилметил)бис(2,2-диметилпропил)титан
(N-(1,1-диметилэтил)-1-(((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)диметилсилил)метанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-(((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)метил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)этанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)тетраметилэтанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)-1,1,2,2-тетраметилдисиланаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-3-((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)пропанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)метанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)диметилметанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-метокси-1Н-инден-1-ил)германаминато(2-)-N)диметилтитан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1-(((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил) диметил-силил) метанаминато (2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-(((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)метил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-2-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил) этан-аминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-2-
((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)тетраметилэтанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-2-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)-1,1,2,2-тетраметилдисиланаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)-титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-3-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)пропанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)метанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1-((1,2,3,3а,7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)диметилметанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)фенил)метил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-метокси-1Н-инден-1-ил)германаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
(N-(1,1-диметилэтил)-1-(((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)диметилсилил)метанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-(((1,2,3,3а,7a-η)-3-[1-пирролидинил)-1Н-инден-1-ил)метил)силанаминато(2-)-N)-титан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)этанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)тетраметилэтанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)-1,1,2,2-тетраметилдисиланаминато(2-)-N)-титан
(N-(1,1-диметилэтил)-3-((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)пропанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1-((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)метанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)диметилметанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-метокси-1Н-инден-1-ил)германаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1-(((1,2,3,3а, 7а-η)-3-метокси-lH-инден-1-ил)диметилсилил)метанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-(((1,2,3,3а,7a-η)-3-метокси-1Н-инден-1-ил)метил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а,7a-η)-3-метокси-1H-инден-1-ил)этанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а,7а-η)-3-метокси-1H-инден-1-ил)тетраметилэтанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7a-η)-3-метокси-lH-инден-1-ил)-1,1,2,2-тетраметилдисиланаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-3-((1,2,3,3а,7a-η)-3-метокси-lH-инден-1-ил)пропанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-((1,2,3,3а,7а-η)-3-метокси-lH-инден-1-ил)метанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-((1,2,3,3а,7a-η)-3-метокси-lH-инден-1-ил)диметилметанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7a-η)-3-метокси-1Н-инден-1-ил)германаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-(((1,2,3,3а,7a-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)диметилсилил)метанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-(((1,2,3,3а, 7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)метил)-силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а,7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)этанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а,7a-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)тетраметилэтанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а,7a-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)-1,1,2,2-тетраметилдисиланаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-3-((1,2,3,3а,7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)пропанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-((1,2,3,3а,7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)метанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-((1,2,3,3а,7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)диметилметанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3, 3а, 7а-η)-3-(((1,1-диметилэтил)диметилсилил)окси)-1Н-инден-1-ил)германаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-(((1,2,3,3а, 7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)диметилсилил)метанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-(((1,2,3,3а,7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)метил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)этанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3, 3a,7a-η)-3-(1-пиперидинил)-1Н-инден-1-ил)тетраметилэтанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7a-η)-3-(1-пиперидинил)-1Н-инден-1-ил)-1,1,2,2-тетраметилдисиланаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-3-((1,2,3,3а, 7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)пропанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-((1,2,3,3а, 7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)метанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-((1,2,3,3а, 7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)диметилметанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)германаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-(((1,2,3,3а,7a-η)-3-(этилметиламино)-1Н-инден-1-ил)диметилсилил)метанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-(((1,2,3,3а,7а-η)-3-(этилметиламино)-1Н-инден-1-ил)метил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7a-η)-3-(этилметиламино)-1Н-инден-1-ил)этанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7а-η)-3-(этилметиламино)-1Н-инден-1-ил)тетраметилэтанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7а-η)-3-(этилметиламино)-1Н-инден-1-ил)-1,1,2,2-тетраметилдисиланаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-3-((1,2,3,3а, 7а-η)-3-(этилметиламино)-1H-инден-1-ил)пропанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-((1,2,3,3а, 7а-η)-3-(этилметиламино)-1Н-инден-1-ил)метанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-((1,2,3,3а, 7a-η)-3-(этилметиламино)-1Н-инден-1-ил)диметилметанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(этилметиламино)-1Н-инден-1-ил)германаминато(2-)-N)диметилтитан
(N-циклогексил-1-(((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)диметилсилил)метанаминато(2-)-N)диметилтитан
(N-циклогексил-1,1-диметил-1-(((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)метил)силанаминато(2-)-N)диметилтитан
(N-циклогексил-2-((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)этанаминато(2-)-N)диметилтитан
(N-циклогексил-2-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)тетраметилэтанаминато(2-)-N)диметилтитан
(N-циклогексил-2-((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)-1,1,2,2-тетраметилдисиланаминато(2-)-N)диметилтитан
(N-циклогексил-3-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)пропанаминато(2-)-N)диметилтитан
(N-циклогексил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)метанаминато(2-)-N)диметилтитан
(N-циклогексил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)диметилметанаминато(2-)-N)диметилтитан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)германаминато(2-)-N)диметилтитан
(N-этил-1-(((1,2,3,3a,7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)диметилсилил)метанаминато(2-)-N)диметилтитан
(N-этил-1,1-диметил-1-(((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)метил)силанаминато(2-)-N)диметилтитан
(N-этил-2-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)этанаминато(2-)-N)диметилтитан
(N-этил-2-((1,2,3,3а,7a-η)-3-(1-пирролидинил)-1H-инден-1-ил)тетраметилэтанаминато(2-)-N)диметилтитан
(N-этил-2-((1,2,3,3а, 7a-η)-3-(1-пирролидинил)-lH-инден-1-ил)-1,1,2,2-тетраметилдисиланаминато(2-)-N)диметилтитан
(N-этил-3-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-lH-инден-1-ил)пропанаминато(2-)-N)диметилтитан
(N-этил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-1H-инден-1-ил)метанаминато(2-)-N)диметилтитан
(N-этил-1-((1,2,3,3а,7а-η)-3-(1-пирролидинил)-lH-инден-1-ил)диметилметанаминато(2-)-N)диметилтитан
(N-этил-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)германаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-(((1,2,3,3а,7а-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)диметилсилил)метанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-(((1,2,3,3а, 7а-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)метил)силанаминато-(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7а-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)этанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7a-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)тетраметилэтанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,3а, 7а-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)-1,1,2,2-тетраметилдисиланаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-3-((1,2,3,3а, 7а-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)пропанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-((1,2,3,3а, 7a-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)метанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-((1,2,3,3а, 7а-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)диметилметанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7a-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)германаминато(2-)-N)-диметилтитан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η))-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)-((1,2,3,4-η)-2,4-гексадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)-((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато-(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)-диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)-бис(фенилметил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)-бис(фенилметил)бис((триметилсилил)метил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)-бис(фенилметил)бис(2,2-диметилпропил)титан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)-((1,2,3, 4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(1,1-диметил-N-(фенилметил)-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
дихлор(1,1-диметил-N-(фенилметил)-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-фенил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)-N-((трицикло(3,3,1,1,3,7)дец-1-ил))силанаминато (2-)-N)диметилтитан
(1,1-диметил-N-циклододецил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-диметил-N-(фенилметил)-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)бис-(фенилметил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
дихлор(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(1,1-диметил-N-(1-метилэтил)-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-этил-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
(N-этил-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(N-этил-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)-силанаминато(2-)-N)титан
дихлор(N-этил-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-этил-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пирролидинил) 2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(1,1-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-ди-метилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пиперидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пиперидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)-((1,2,3,4-η)-2,4-гексадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пиперидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пиперидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пиперидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пиперидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-пиперидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(метилфениламино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(метилфениламино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(метилфениламино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(метилфениламино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(метилфениламино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(метилфениламино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)бис(фенилметил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(метилфениламино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)бис(фенилметил)бис((триметилсилил)метил)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(метилфениламино)-2,4-циклопентадиен-1-ил)силанаминато-(2-)-N)бис(фенилметил)бис(2,2-диметилпропил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(1-((1,2,3,4,5-η)-3-(диметиламино)-2,4-циклопентадиен-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)титан
(1-((1,2,3,4,5-η)-3-(диметиламино)-2,4-циклопентадиен-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)-((1,2,3,4-η)-2,4-гексадиен)титан
(1-((1,2,3,4,5-η)-3-(диметиламино)-2,4-циклопентадиен-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)-((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(1-((1,2,3,4,5-η)-3-(диметиламино)-2,4-циклопентадиен-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)титан
дихлор(1-((1,2,3,4,5-η)-3-(диметиламино)-2,4-циклопентадиен-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато-(2-)-N)титан
(1-((1,2,3,4,5-η)-3-(диметиламино)-2,4-циклопентадиен-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)диметилтитан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)-1-((1,2,3,4,5-η)-3-(этилметиламино)-2,4-циклопентадиен-1-ил)-1,1-диметилсиланаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1-((1,2,3,4,5-η)-3-(этилметиламино)-2,4-циклопентадиен-1-ил)-1,1-диметилсиланаминато(2-)-N)-((1,2,3,4-η)-2,4-гексадиен)титан
(N-(1,1-диметилэтил)-1-((1,2,3,4,5-η)-3-(этилметиламино)-2,4-циклопентадиен-1-ил)-1,1-диметилсиланаминато(2-)-N)-((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1-((1,2,3,4,5-η)-3-(этилметиламино)-2,4-циклопентадиен-1-ил)-1,1-диметилсиланаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1-((1,2,3,4,5-η)-3-(этилметиламино)-2,4-циклопентадиен-1-ил)-1,1-диметилсиланаминато-(2-)-N)титан
(N-(1,1-диметилэтил)-1-((1,2,3,4,5-η)-3-(этилметиламино)-2,4-циклопентадиен-1-ил)-1,1-диметилсиланаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-((1,2,3,4,5-η)-3-(этилметиламино)-2,4-циклопентадиен-1-ил)-1,1-диметилсиланаминато(2-)-N)бис(фенилметил)титан
(N-(1,1-диметилэтил)-1-((1,2,3,4,5-η)-3-(этилметиламино)-2,4-циклопентадиен-1-ил)-1,1-диметилсиланаминато(2-)-N)-бис(фенилметил)бис((триметилсилил)метил)титан
(N-(1,1-диметилэтил)-1-((1,2,3,4,5-η)-3-(этилметиламино)-2,4-циклопентадиен-1-ил)-1,1-диметилсиланаминато(2-)-N)-бис(фенилметил)бис(2,2-диметилпропил)титан
(1,1-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-метокси-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-метокси-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-метокси-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-метокси-2,4-циклопентадиен-1-ил)-силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-l-((1,2,3,4,5-η)-3-метокси-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1, 2,3,4,5-η)-3-метокси-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-метокси-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)бис(фенилметил)титан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-((1,1-диметилэтил)окси)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-((1,1-диметилэтил)окси)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-((1,1-диметилэтил)окси)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1, 3-пентадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-((1,1-диметилэтил)окси)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-((1,1-диметилэтил)окси)-2,4-циклопентадиен-1-ил)силанаминато (2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-((1,1-диметилэтил)окси)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(гексагидро-1Н-азепин-1-ил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(гексагидро-1(2Н)-азоцинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(октагидро-1Н-азонин-1-ил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(октагидро-1(2Н)-азецинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(метил(фенилметил)амино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1, 2,3,4,5-η)-3-(1,1-диметилэтил)метиламино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(метил(1-метилэтил)амино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(метилфениламино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(диметилфосфино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(дифенилфосфино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-3-((1,2,3,4,5-η)-3-(метилфенилфосфино)-2,4-циклопентадиен-1-ил)силанаминато-(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-этокси-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-пропокси-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-метилэтокси)-2,4-циклопентадиен-1-ил)силанаминато-(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(фенокси)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(фенилтио)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(метилтио)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-метил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-5-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-метил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато-(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-метил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато-(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-метил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-метил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-метил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)
-1,1-диметил-1-((1,2,3,4,5-η)-2-пропил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-пропил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-пропил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметипамино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-пропил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-пропил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-пропил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-метил-4-этил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-метил-4-этил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-метил-4-этил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметипамино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-метил-4-этил-3-(1-пирродидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-метил-4-этил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2-метил-4-этил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(1,1'-(η4-1,3-бутадиен-1,4-диил)бис(бензол))(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-метилэтил)-4-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-метилэтил)-4-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((l,2,3,4,5-η)-3-(1-метилэтил)-4-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-метилэтил)-4-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(1-метилэтил)-4-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-3-(l-метилэтил)-4-(1-пирролидинил)-2,4-циклопентадиен-1-ил)-силанаминато(2-)-N)диметилтитан
(1,1'-(η4-1,3-бутадиен-1, 4-диил)бис(бензол))(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2,4,5-триметил-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)-титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2,4,5-триметил-(1-пирролидинил)-2,4-циклопентадиен-1-ил-силанаминато(2-)-N)((1,2,3,4-η)-2,4-гексадиен)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2,4,5-триметил-(1-пирролидинил)-2,4-циклопентадиен-1-ил)-силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2,4,5-триметил-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2,4,5-триметил-(1-пирролидинил)-2,4-циклопентадиен-1-ил)-силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,4,5-η)-2,4,5-триметил-(1-пирролидинил)-2,4-циклопентадиен-1-ил)-силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-метил-1-фенил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-дифенил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-бис(1-метилэтокси)-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)-силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1-этокси-1-метил-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметокси-1-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)этанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)-1,1,2,2-тетраметилэтанаминато-(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)-1,1,2,2-тетраметилдисиланаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-3-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)-пропанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)метиламинато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)-1,1-диметилметанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-2-((1,2,3,4,5-η)-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)-1,1-диметилгерманаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-4,5,6,7-тетрагидро-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7a-η)-4,5,6,7-тетрагидро-3-(метил(1-метилэтил)амино)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1, 2,3,3а, 7a-η)-4,5,6,7-тетрагидро-2-метил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-(1,1-диметилэтил)-1,1-диметил-1-((1, 2,3,3а, 7а-η)-4,5,6,7-тетрагидро-2,4,5-триметил-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-циклогексил-1,1-диметил-1-((1,2,3,3а, 7а-η)-4,5,6,7-тетрагидро-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(N-метил-1,1-диметил-1-((1,2,3,3а, 7a-η)-4,5,6, 7-тетрагидро-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-4,5,6,7-тетрагидро-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1, 1-диметилэтил)-1,1-диметил-1-((1,2,3,3a, 7a-η)-4,5,6,7-тетрагидро-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7a-η)-4,5,6,7-тетрагидро-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)титан
(N-(1,1-диметилэтил)-1,1-диметокси-1-((1,2,3,3а, 7a-η)-4,5,6,7-тетрагидро-3-(1-пирролидинил)-2,4-циклопентадиен-1-ил)силанаминато(2-)-N)диметилтитан
(1-((1,2,3,3а,6a-η)-3-(диметиламино)-1,4,5,6-тетрагидро-1-пенталенил)-N-(1,1-диметилэтил))-1,1-диметилсиланаминато(2-)-N)диметилтитан
(1-((1,2,3,3а,6a-η)-3-(диметиламино)-1,4,5,6-тетрагидро-1-пенталенил)-N-(1,1-диметилэтил))-1,1-диметилсиланаминато(2-)-N)((1,2,3,4-η)-1,3-пентадиен)титан
((2-(диметиламино)метил)фенил)(1-((1,2,3,3а, 6а-η)-3-(диметиламино)-1,4,5,6-тетрагидро-1-пенталенил)-(N-1,1-диметилэтил))-1,1-диметилсиланаминато(2-)-N)титан
(1-((1,2,3,3а,6а-η)-3-(диметиламино)-1,4,5,6-тетрагидро-1-пенталенил)-N-(1,1-диметилэтил))-1,1-диметоксисиланаминато(2-)-N)диметилтитан
(1-((1,2,3,3а,6а-η)-3-(диэтиламино)-1,4,5,6-тетрагидро-1-пенталенил)-N-(1,1-диметилэтил))-1,1-диметилсиланаминато-(2-)-N)диметилтитан
(N-циклогексил-(1-((1,2,3,3а,6а-η)-3-(диметиламино)-1, 4,5,6-тетрагидро-1-пенталенил))-1,1-диметилсиланаминато(2-)-N)диметилтитан
(1-((1,2,3,3а, 6а-η)-3-(диметиламино)-2-метил-1,4,5,6-тетрагидро-1-пенталенил)-N-(1,1-диметилэтил))-1,1-диметилсиланаминато(2-)-N)диметилтитан
(1-((1,2,3,3а, 6а-η)-3-(диметиламино)-4-метил-1,4,5,6-тетрагидро-1-пенталенил)-N-(1,1-диметилэтил))-1,1-диметилсиланаминато(2-)-N)диметилтитан
(1-((1,2,3,3а,6a-η)-3-(диметиламино)-4,5,6-триметил-1,4,5,6-тетрагидро-1-пенталенил)-N-(1,1-диметилэтил))-1,1-диметилсиланаминато(2-)-N)диметилтитан
(1-((1,2,3,3а, 6а-η)-4-этил-3-(диметиламино)-1, 4,5,6-тетрагидро-1-пенталенил)-N-(1,1-диметилэтил))-1,1-диметилсиланаминато(2-)-N)диметилтитан
Комплексы могут быть получены с использованием хорошо известных методов синтеза. Можно, но не обязательно, использовать восстановитель для получения комплексов с более низкой степенью окисления. Такой способ раскрыт в заявке США, серийный номер 8/241523, поданной 13 мая 1994 г., опубликованной как WO 95/00526 (содержание включено в данное описание путем ссылки). Реакции проводят в подходящем растворителе, не оказывающем вредного влияния на реакции, при температуре от -100 до 300oС, предпочтительно от -78 до 100oС, а наиболее предпочтительно от 0 до 50oС. Под используемым в данном описании термином "восстановитель" подразумевается металл или соединение, который(ое) в условиях восстановления заставляет металл М восстанавливаться от более высокой степени окисления до более низкой. Примерами подходящих металлических восстановителей являются щелочные металлы, щелочно-земельные металлы, алюминий и цинк, сплавы щелочных или щелочно-земельных металлов, такие как ртутно-натриевая амальгама и натрий-калиевый сплав. Примерами подходящих восстановителей-соединений являются нафталинид натрия, калийграфит, литийалкилы, литий- или калийалкадиенилы и реактивы Гриньяра. Наиболее предпочтительными восстановителями являются щелочные или щелочно-земельные металлы, в частности литий и магний.
Подходящая реакционная среда для образования комплексов включает алифатические и ароматические углеводороды, простые эфиры и циклические простые эфиры, особенно разветвленные углеводороды, такие как изобутан, бутан, пентан, гексан, гептан, октан и их смеси; циклические и алициклические углеводороды, такие как циклогексан, циклогептан, метилциклогексан, метилциклогептан и их смеси; ароматические и гидрокарбилзамещенные ароматические соединения, такие как бензол, толуол и ксилол, C1-4 диалкиловые эфиры, C1-4 диалкилэфирные производные (поли)алкиленгликолей и тетрагидрофуран. Пригодны также их смеси.
Один из способов синтеза гетероатомзамещенных циклопентадиенильных систем, полезных в качестве предшественников каталитических систем ограниченной геометрии (CGC), показан на представленной в конце описания схеме 1, где:
а) избыточный амин, бензол, нагревание с обратным холодильником в течение 24 ч (-Н2O) ; b) избыточный амин (8 экв), TiCl4 (1 экв) в CH2Cl2, 0oC, затем добавляют кетон и нагревают до 25oС; с) 1,05 экв H-BuLi/гексан при 25oС; d) 1,0-1,5 экв Cl-силан/ТГФ при 25oС; е) 2,05 экв H-BuLi/гексан при 25oС.
R, R', R'', R''', R'''', независимо выбранные в каждом случае, представляют Н (кроме находящихся на азоте, присоединенном непосредственно к циклопентадиенильному кольцу), алкил, циклоалкил, арил, алкарил, аралкил и не ограничиваются только лишь этими группами.
Гетероатомсодержащий заместитель имеет азот в 3-положении инденильной системы. 1-Инданон является подходящим исходным материалом для превращения в соответствующий енамин, хотя образование последнего не ограничивается использованием этого соединения. Енамины инданона обычно получают известными в данной области химии методами, включающими конденсацию вторичных аминов с кетоном (W.E. Noland, V. Kameswaran, J. Org. Chem. 1981, 46, 1940-1944). Соответствующий водный побочный продукт может быть азеотропно удален и использованием в качестве растворителя бензола или толуола в условиях нагревания с обратным холодильником и, необязательно, кислотного катализатора, такого как п-толуолсульфоновая кислота (О. Cervinka, The Chemistry of Enamines, часть 1, гл. 9; Z. Rappoport, Ed.; Wiley Interscience, Нью-Йорк, 1994, 468-500). С более стерически затрудненными кетонами, такими как 2-метил-1-инданон, или более летучими аминами, такими как диметиламин, может быть предпочтительным использование более сильных дегидратирующих реагентов, таких как хлорамиды титана (получаемые in situ из тетрахлорида титана и конденсационного амина) (R. Carlson, A. Nilsson, Acta. Chemica Scandinavica В 38, 1984, 49-53). Два указанных метода уже были использованы для получения енаминов, замещенных в 2- и 3-положениях индена (1-положение обычно связано с кремнием или другим связывающим фрагментом в последующих соединениях). Другой метод получения енаминов включает электрофильное аминирование карбанионов, таких как инденид лития (Е. Erdik; M, Ay Chem. Rev., 1989, 89, 1947-1980).
Для последующего образования высокочистых CGC-лигандов енамины, полученные указанными методами, должны быть высокочистыми и свободными от кетона, альдольных побочных продуктов и имеющих более высокую массу остаточных смол, обычно сопровождающих образование продукта. Ни один из вышеописанных методов не обеспечивает стабильного получения продукта, который можно использовать без какой-либо дополнительной очистки. Данными изобретателями обнаружено, что хроматографическая очистка с использованием силикагеля или оксида алюминия для флэш-хроматографии быстро промотирует гидролиз енамина в свободный амин и кетон (неудачный результат). Хотя эти соединения высокочувствительны к воде и воздуху, енамины этой природы могут быть очищены путем тщательной дробной перегонки или, иногда, путем перекристаллизации. В частности, быстрая перегонка енаминов инданона требуется для предотвращения термической полимеризации в перегонном аппарате при повышенной температуре. Для получения высокочистых CGC-лигандов является целесообразным преобразовать чистый енамин в его соответствующую анионную соль, поскольку енамины могут быть также светочувствительными.
1-Инданон является также предпочтительным исходным материалом для CGC-лигандов, замещенных кислородом в 3-положении. В частности, простые енольные эфиры в этом положении могут быть получены путем дегидратации подходящего полукеталя, который образуется in situ из инданона и спирта в присутствии кислотного катализатора (L.A. Paquette; A. Varadarajan; E. Bey J. Am. Chem. Soc. 1984, 106, 6702-6708). Енольные эфиры инданонов, подобно енаминовым аналогам, также подвержены гидролизу и очень чувствительны к кислороду. Наиболее целесообразным является их преобразование после очистки в соответствующие их анионные соли, как показано на представленной в конце описания схеме 2, где:
а) спирт, бензол, нагревание с обратным холодильником в течение 24 ч (-Н2О); b) 1,05 экв H-BuLi/гексан при 25oС; с) 1,0-1,5 экв Cl-силан/ТГФ при 25oС; d) 2,05 экв n-BuLi/гeксан при 25oС; и
R, R', R'', R''', R'''', независимо выбранные в каждом случае, представляют Н (кроме находящихся на кислороде), алкил, циклоалкил, арил, алкарил, аралкил и не ограничиваются только лишь этими группами.
После высокой очистки преобразование енамина в его соответствующую анионную соль может быть осуществлено путем осуществления взаимодействия с подходящим основанием подходящей силы в подходящем немешающем растворителе. При подходящих анаэробных безводных условиях часто твердую анионную соль можно отфильтровать, промыть и высушить, получив почти количественный выход. Аналогичным образом, енольные эфиры 1-инданона можно депротонировать до соответствующей анионной соли.
Образование лигандов ограниченной геометрии (CGC-лиганд) на основе гетероатомзамещенных инденов основано на методе анионного алкилирования, описанном Никиасом и др. (Nickias, Peter N.; Devore, David D.; Wilson, David R. ; PCT Int. Appl. (междунар. заявка PCT), WO 93/08199 Al 930429. CAN 119: 160577; Carpenetti, Donald W. ; Kloppenburg, Lioba; Kupec, Justin Т.; Petersen, Jeffrey L. Organometallics 1966, 15(6), 1572-81), в котором циклопентадиенильный анион подвергают взаимодействию с электрофилами, такими как галогенированные вторичные алкиламины или галогенированные вторичные силиламины, с получением соответствующего циклопентадиенилалкиламина или циклопентадиенилсилиламина. Галогенированные вторичные алкиламины или галогенированные вторичные силиламины включают, например, (трет-бутил)(хлордиметилсилил)амин, (трет-бутил)(хлордиметилсилилметил)амин, (трет-бутил)(бромметилдиметилсилил)амин, (трет-бутил)(2-хлорэтил)-амин, (хлордиметилсилил)(фенил)амин, (адамантил)(хлордифенилсилил)амин, (хлордиметилсилил)(циклогексил)амин, (бензил)(хлордиметилсилил)амин и (трет-бутил)(хлорметилфенилсилил)амин. Например, капельное введение литиевого производного анионной соли в ТГФ (тетрагидрофуран) в молярный избыток (трет-бутил)(хлордиметилсилил)амина в ТГФ с последующим стандартным удалением хлорида лития и избыточного электрофила часто дают высокочистый лиганд, который может быть далее использован без дополнительной очистки. Так называемый CGC-лиганд может быть преобразован в его нерастворимую дианионную соль путем осуществления взаимодействия свободного основания с двумя эквивалентами основания подходящей силы в подходящем немешающем растворителе.
Под подходящим немешающим растворителем в контексте настоящего изобретения подразумевается растворитель; который не мешает образованию целевого продукта или не совершает вредного взаимодействия с ним. Такие растворители, пригодные для получения анионных и дианионных солей по настоящему изобретению, включают (но не ограничиваются ими) алифатические и ароматические углеводороды, в частности неразветвленные и разветвленные углеводороды, такие как бутан, пентан, гексан, гептан, октан, декан у включая их разветвленные изомеры и их смеси; циклические и алициклические углеводороды, такие как циклогексан, циклогептан, метилциклогексан, метилциклогептан и их смеси; ароматические и гидрокарбилзамещенные ароматические соединения, такие как бензол, толуол, ксилол, этилбензол, диэтилбензол и их смеси; простые эфиры и циклические простые эфиры, в частности C1-6 диалкиловые эфиры, такие как диэтиловый эфир, дибутиловый эфир и метил-трет-бутиловый эфир, C1-6 диалкилэфирные производные (поли)алкиленгликолей, такие как диметоксиэтан, и диоксан и ТГФ и их смеси. Подходящими являются также смеси указанных выше растворителей.
Основания подходящей силы для получения дианионных солей по настоящему изобретению включают гидрокарбильные соли металлов Группы 1 и Группы 2, в частности алкильные или арильные соли лития или магния, такие как метиллитий, этиллитий, н-бутиллитий, втор-бутиллитий, трет-бутиллитий, фениллитий, метилмагнийхлорид, этилмагнийбромид, изопропилмагнийхлорид, дибутилмагний, (бутил)(этил)магний, дигексилмагний; металлы Группы 1 или Группы 2, такие, как литий, натрий, калий и магний; гидриды металлов Группы 1, Группы 2 или Группы 13, такие как гидрид лития, гидрид натрия, гидрид калия или литийалюминийгидрид; амидные комплексы с металлами Группы 1 или Группы 2, такие как литийдиизопропиламид, литийдиметиламид, литийгексаметилдисилазид, натрийамид и магнийдиизопропиламид.
Основания подходящей силы для получения анионных солей по настоящему изобретению включают указанные выше, а также алкоксидные комплексы с металлами Группы 1 или Группы 2, такие как этоксид натрия, трет-бутоксид натрия, бутоксид калия и амилат калия.
Другой возможный синтетический метод образования лиганда в виде свободного основания включает осуществление взаимодействия инденильной анионной соли с избытком бис-электрофила, например дихлордиметилсилана, в полярном апротонном растворителе, таком как ТГФ. Неожиданно было обнаружено, что этот метод хуже вышеописанной технологии для многих 3-гетероатомзамещенных лигандных систем тем, что часто образуется много ансалиганда (аддуктбисалкилирования), несмотря на использование избыточного электрофила, как показано ниже на схеме 3.
Осуществимость того или иного метода синтеза зависит от учета пространственных и электронных характеристик замещающих групп (R групп) и требует экспериментальной оценки в каждом случае.
Металлирование дианионной соли может быть осуществлено методами, хорошо описанными в данной области химии. Реакция дианионной соли в ТГФ с TiCl3 (ТГФ)3 с последующим окислением метиленхлоридом или дихлоридом свинца представляет собой хорошо разработанную процедуру (J. Okuda, S. Verch, Т.Р. Spaniol, R. Sturmer, Chem. Ber. , 1996, 129, 1429-1431, D.D. Devore EP 514828), которая дает комплекс дихлорида с титаном (IV). Дихлорид можно силилировать или гидрокарбилировать путем лигандного обмена с подходящим силилирующим или гидрокарбилирующим агентом, таким как метиллитий, метилмагнийхлорид, бензилкалий, аллиллитий, триметилсилилметиллитий, неопентилмагнийбромид и фениллитий. Более полный перечень подходящих силилирующих или гидрокарбилирующих агентов дан ниже.
Общий метод получения диенового комплекса с титаном (II) из соответствующего дихлорида титана (IV) уже описан Девором и соавторами (D.D. Devore, F. J. Timmers, D. L. Hasha, R.K. Rosen, T.J. Marks, P.A. Deck, C.L. Stern, Organometallics, 1995, 14, 3132-3134; D.D. Devore, F.J. Timmers, J.C. Stevens, R. D. Mussell, L.H. Crawford, D.R. Wilson, U.S. 5556928). Так, обработка дихлорида н-бутиллитием в присутствии подходящего диена дает аналогичный титан (II)-диеновый комплекс для гетероатомзамещенных систем.
Образование CGC комплексов металлов (III) по настоящему изобретению может быть осуществлено любым из нескольких методов синтеза, к которым относятся следующие. Взаимодействие в анаэробных безводных условиях дианионных солей с трехвалентными солями металлов, такими как комплексы металлов (III) Группы 4 с галогенидом или алкоксидом, может быть осуществлено с необязательным последующим силилированием или гидрокарбилированием подходящими силилирующими или гидрокарбилирующими агентами с образованием соответствующих CGC комплексов металлов (III) с галогенидом, алкоксидом, силилом или гидрокарбилом в соответствии с настоящим изобретением.
Другой метод синтеза включает восстановление подходящего CGC комплекса металла (IV) с дигалогенидом или диалкоксидом или предварительно моносилилированного или моногидрокарбилированного соответствующего CGC комплекса металла (IV) с силил- или гидрокарбилмоногалогенидом или -моноалкоксидом подходящим восстанавливающим агентом до соответствующего CGC комплекса металла (III) с галогенидом, алкоксидом, силилом или гидрокарбилом.
Установлено, что особенно подходящими методами синтеза CGC комплексов металлов(III) по настоящему изобретению являются те, что описаны Вильсоном (D. R. Wilson U.S. 5504224; 1996), описание которого включено в данное описание путем ссылки. Например, циклопентадиенильные лиганды могут быть вытеснены дианионными солями и/или (стабилизирующими) гидрокарбилирующими агентами из циклопентадиенилсодержащих комплексов металлов Группы 4 в степени окисления +3 с получением CGC комплексов металлов (III) по настоящему изобретению.
Подходящие восстановители для восстановления степени окисления металлов CGC комплексов металлов (IV) от +4 до +3 уже описаны выше и, в частности, включают цинк, алюминий и магний.
Подходящие силилирующие и гидрокарбилирующие агенты для CGC комплексов металлов (III) и CGC комплексов металлов (IV) по настоящему изобретению включают алкил, такой как метил, этил, пропил, бутил, неопентил и гексил; арил, такой как фенил, нафтил и дифенил; аралкил, такой как бензил, толил-метил, дифенилметил; алкарил, такой как толил и ксилил; аллил; силил- или алкилзамещенный аллил, такой как метилаллил, триметилсилилаллил, диметилаллил и триметилаллил; триалкилсилил, такой как триметилсилил и триэтилсилил; триалкилсилилалкил, такой как триметилсилилметил; пентадиенил; алкил- или силилзамещенный пентадиенил, такой как метилпентадиенил, диметилпентадиенил, триметилсилилпентадиенил, бис(триметилсилил)пентадиенил, циклогексадиенил и диметилциклогексадиенил; диалкиламиноалкарил, такой как o-(N,N-диметиламинометил)фенил, и диалкиламиноаралкил, такой как о-(N,N-диметиламино)бензил; соли металлов Группы 1, 2 или 13, предпочтительно соли лития, натрия, калия, магния и алюминия. Предпочтительные силилирующие и гидрокарбилирующие агенты включают триметилалюминий, метиллитий, метилмагнийхлорид, неопентиллитий, триметилсилилметилмагнийхлорид и фениллитий. Включены также гидрокарбилирующие агенты, содержащие стабилизирующую группу, в частности содержащие стабилизирующую группу гидрокарбилирующие агенты и соли содержащих стабилизирующую группу гидрокарбильных групп, описанные в U.S. 5504224, соли которых включают, например, бензилкалий, 2-(N,N-диметиламино)бензиллитий, аллиллитий и диметилпентадиенилкалий. Стабилизирующие группы дополнительно описаны в заявке сер. 8003, поданной в США 21 января 1993 г. (соответствует WO 93/19104), включенной в данное описание путем ссылки.
Предпочтительные галогениды или алкоксиды комплексов металлов (III) с галогенидом или алкоксидом и CGC комплексов металлов (III) с галогенидом или алкоксидом включают фторид, хлорид, бромид, йодид, метоксид, этоксид, изопропоксид, н-пропоксид, бутоксид и феноксид. Предпочтительные комплексы металлов (III) с галогенидом или алкоксидом включают хлорид титана (III), этоксид титана (III), бромид титана (III), изопропоксид титана (III), (дихлор)(изопропоксид)титана (III), а также комплексы вышеуказанных соединений с кислотой Льюиса, особенно их комплексы с простым эфиром, в частности их комплексы с диэтиловым эфиром, тетрагидрофураном и диметиловым эфиром этиленгликоля. Предпочтительные циклопентадиенилсодержащие комплексы металлов Группы 4 в степени окисления +3 включают трисциклопентадиенилтитан, бисциклопентадиенилтитанхлорид, бисциклопентадиенилтитанбромид, бисциклопентадиенилтитанизопропоксид, циклопентадиенилтитанхлорид, циклопентадиенилтитандифеноксид, циклопентадиенилтитандиметоксид и бис(триметилсилил)(трет-бутил)циклопентадинил)цирконийхлорид.
Лиганды по настоящему изобретению представляют собой 3-гетероатомзамещенные циклопентадиенилсодержащие лиганды, причем лиганд находится в форме:
(A) свободного основания с 2 протонами, способными к депротонированию;
(B) дилитиевой соли;
(C) магниевой соли; или
(D) моно- или дисилилированного дианиона.
В объем настоящего изобретения входит применение лиганда по настоящему изобретению для синтеза с получением металлокомплекса по настоящему изобретению, для синтеза с получением металлокомплекса, содержащего металл из одной из Групп 3-13 Периодической таблицы элементов (лантаниды или актиниды) и от 1 до 4 лигандов.
Лиганды по настоящему изобретению могут быть использованы в различных формах, включая соли, с различными группами, присоединенными в положении Z, в процессах синтеза, ведущих к образованию металлокомплексов, в которых металл взят из Группы 3-16 Периодической таблицы или лантанидов и в которых присутствует от одного до четырех указанных лигандов, отдельно или в сочетании с другими лигандами. Методы синтеза могут быть такими же или аналогичными тем, что описаны здесь для комплексов металлов Группы 4 по настоящему изобретению, а также различными другими методами синтеза, известными в данной области. Металлокомплексы полезны в качестве катализаторов в различных реакциях, включая реакции полимеризации олефинов.
Очевидно, что наименование этих металлокомплексов, а также нейтральных лигандов и различных интермедиатов сложно и вызывает сомнения и правила в различных системах для указанных названий развиваются. Поэтому рекомендуется ссылка на структурное представление. Как правило, при присоединении мостика комплекса ограниченной геометрии или мостикового бис-Ср комплекса в 1-положении гетероатом находится в 3-положении. Структурные представления не должны давать абсолютно точной интерпретации в отношении порядка, длины и прочности связей. Например, рентгеновские данные показывают, что N-Cp связи некоторых комплексов короче, чем можно было бы ожидать для одинарной связи, что указывает на, по крайней мере, частичный характер двойной связи в связи N-Cp.
Если лиганды используют в комплексах с присоединением только η5, когда мостик отсутствует, гетероатом в этих случаях можно назвать как находящийся в положении 1.
В объеме приведенного выше описания, касающегося лигандов, предпочтительные лиганды по настоящему изобретению соответствуют формуле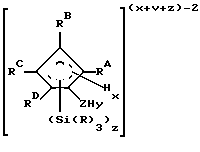
где х представляет 0 или 1, у представляет 0 или 1, z представляет 0 или 1, х+у представляет 0 или 1, x+z представляет 0 или 1, а другие символы - такие, как определенные выше, где пунктирная окружность внутри Ср кольца подразумевает различные возможности для характера двойной связи, частичного характера двойной связи или ароматического характера в подходящих случаях, в зависимости от значений для х, у и z.
Комплексы делают каталитически активными путем сочетания с активирующим сокатализатором или путем применения активирующей технологии. Подходящие для этой цели активирующие сокатализаторы включают полимерные и олигомерные алюмоксаны, в частности метилалюмоксан; метилалюмоксан, модифицированный триизобутилалюминием или изобутилалюмоксан; нейтральные кислоты Льюиса, такие как C1-45 гидрокарбилзамещенные соединения Группы 13, в частности соединения три(гидрокарбил)алюминия и три(гидрокарбил)бора и их галогенированные (включая пергалогенированные) производные, имеющие от 1 до 15 углеродных атомов в каждой гидрокарбильной или галогенированной гидрокарбильной группе, более предпочтительно перфторированные соединения три(арил)бора, а наиболее предпочтительно трис(о-нонафтордифенил)боран, трис(пентафторфенил)боран; неполимерные совместимые некоординирующиеся ионообразующие соединения (включая применение таких соединений в окислительных условиях), в частности применение аммониевых; фосфониевых, оксониевых, карбониевых, силилиевых или сульфониевых солей совместимых некоординирующихся анионов или ферроцениевых солей совместимых некоординирующихся анионов; электролиз в массе (описанный более подробно далее) и сочетание указанных выше сокатализаторов и технологий. Указанные активирующие сокатализаторы и активирующие технологии уже были описаны по отношению к другим металлокомплексам в следующих ссылочных материалах ЕР-А-277003, US-A-5153157, US-A-5064802, ЕР-А-468651 (эквивалент U. S. серийный 07/547718), ЕР-А-520732 (эквивалент U. S. сер. 07/876268) и ЕР-А-520732 (эквивалент U.S. сер. 07/884966, поданной 1 мая 1992 г.), которые включены в данное описание путем ссылки.
Особенно желательными активирующими сокатализаторами являются комбинации нейтральных кислот Льюиса, в частности комбинация триалкилалюминия, имеющего от 1 до 4 углеродных атомов в каждой алкильной группе, и галогенированного соединения три(гидрокарбил)бора, имеющего от 1 до 20 углеводородных атомов в каждой гидрокарбильной группе, в частности трис(пентафторфенил)борана, трис(о-нонафтордифенил)борана, другие комбинации таких смесей нейтральных кислот Льюиса с полимерным или олигомерным алюмоксаном и комбинации отдельной нейтральной кислоты Льюиса, в частности трис(пентафторфенил)борана, с полимерным или олигомерным алюмоксаном. Преимущество настоящего изобретения заключается в открытии того, что наиболее эффективная активация катализатора с использованием такой комбинации трис(пентафторфенил)борана с алюмоксаном происходит при пониженных уровнях содержания алюмоксана. Предпочтительные молярные отношения металлический (группа 4) комплекс: трис(пентафторфенил)боран: алюмоксан находятся в пределах от 1:1:1 до 1:5:5, а более предпочтительно от 1:1:1,5 до 1:5:3. Неожиданно эффективное применение более низких уровней содержания алюмоксана с металлокомплексами по настоящему изобретению позволяет получать олефиновые полимеры при высокой каталитической эффективности, используя меньше дорогого алюмоксанового сокатализатора. Кроме того, это обеспечивает получение полимеров с более низкими остаточными содержаниями алюминия и, следовательно, с большей чистотой.
Подходящие ионообразующие соединения, полезные в качестве сокатализаторов, в одном из вариантов осуществления настоящего изобретения содержат катион, который является кислотой Бренстеда, способной отдавать протон, и совместимый некоординирующийся анион А. Используемый в данном описании термин "некоординирующийся" означает анион или вещество, который(ое) либо не координируется с комплексом-предшественником, содержащим металл группы 4, и его каталитическим производным, либо лишь слабо координируется с такими комплексами, в результате чего остается достаточно лабильным, чтобы быть замещенным нейтральным основанием Льюиса. Некоординирующийся анион, в частности, относится к аниону, который, действуя как зарядоуравновешивающий анион в катионном металлокоплексе, не переносит анионный заместитель или его фрагмент к указанному катиону, в результате чего образуются нейтральные комплексы. "Совместимые анионы" являются анионами, которые не деградируют до нейтральности при распаде первоначально образованного комплекса и не создают помех при требуемой последующей полимеризации или других применениях комплекса.
Предпочтительными анионами являются те, которые содержат один координационный комплекс с зарядонесущим металлическим или металлоидным ядром, которое (анион) способно уравновешивать заряд активных видов катализаторов (катион металла), которые могут быть образованы при объединении двух компонентов. Кроме того, указанный анион должен быть достаточно лабильным, чтобы быть замещенным олефиновыми, диолефиновыми и ацетиленоненасыщенными соединениями или другими нейтральными основаниями Льюиса, такими как простые эфиры или нитрилы. Подходящие металлы включают (но не ограничиваются ими) алюминий, золото и платину. Подходящие металлоиды включают (но не ограничиваются ими) бор, фосфор и кремний. Соединения, содержащие анионы, которые имеют координационные комплексы с одним атомом металла или металлоида, разумеется, хорошо известны и многие, особенно соединения, содержащие один единственный атом бора в анионной части, коммерчески доступны.
Предпочтительно такие сокатализаторы могут быть представлены следующей общей формулой:
(L*-Н)d -(А)d-
где L* представляет нейтральное основание Льюиса;
(L*-H)+ представляет кислоту Бренстеда;
(A)d- представляет некоординирующийся, совместимый анион, имеющий заряд d-, и
d представляет целое число от 1 до 3.
Более предпочтительно (А)d- соответствует формуле
[M'Q4]
где М' представляет бор или алюминий в формальной степени окисления +3; и
Q в каждом случае независимо выбран из гидрида, диалкиламидо, галогенида, гидрокарбила, гидрокарбилоксида, галогензамещенного гидрокарбила, галогензамещенного гидрокарбилокси и галогензамещенного силилгидрокарбила (включая пергалогенированный гидрокарбил, пергалогенированный гидрокарбилокси и пергалогенированный силилгидрокарбил), причем Q имеет до 20 углеродных атомов при условии, что Q представляет галогенид в не более чем одном случае. Примеры
подходящих гидрокарбилоксидных групп Q раскрыты в патенте США 5296433, сущность изобретения которого включена в данное описание путем ссылки.
В более предпочтительном варианте d= 1, то есть противоион имеет единственный отрицательный заряд и является анионом А-. Содержащие бор активирующие сокатализаторы, которые особенно пригодны для получения катализаторов по настоящему изобретению, могут быть представлены следующей общей формулой:
(L*-H)+(BQ4)-,
где L* такой, как определенный выше;
В представляет бор в формальной степени окисления +3; и
Q представляет гидрокарбильную, гидрокарбилокси-, фторированную гидрокарбильную, фторированную гидроксикарбоксильную или фторированную силилгидрокарбильную группу, имеющую до 20 неводородных атомов, при условии, что Q представляет гидрокарбил не более чем в одном случае.
Наиболее предпочтительно Q в каждом случае представляет фторированную арильную группу, в частности пентафторфенильную группу.
Иллюстративными, но не ограничивающими, примерами ионообразующих соединений, содержащих катионы, способные отдавать протон, которые могут быть использованы в качестве активирующих сокатализаторов при получении катализаторов по настоящему изобретению, являются:
соли трехзамещенного аммония, такие как:
триметиламмония тетрафенилборат,
метилдиоктадециламмония тетрафенилборат,
триэтиламмония тетрафенилборат,
трипропиламмония тетрафенилборат,
три(н-бутил)аммония тетрафенилборат,
метилтетрадецилоктадециламмония тетрафенилборат,
N,N-диметиланилиния тетрафенилборат,
N,N-диэтиланилиния тетрафенилборат,
N,N-диметил(2,4,6-триметиланилиния)тетрафенилборат,
триметиламмония тетракис(пентафторфенил)борат,
триэтиламмония тетракис(пентафторфенил)борат,
трипропиламмония тетракис(пентафторфенил)борат,
три(н-бутил)аммония тетракис(пентафторфенил)борат,
три(втор-бутил)аммония тетракис(пентафторфенил)борат,
N,N-диметиланилиния тетракис(пентафторфенил)борат,
N,N-диэтиланилиния тетракис(пентафторфенил)борат,
N,N-диметил(2,4,6-триметиланилиния)тетракис(пентафторфенил)-борат,
триметиламмония тетракис(2,3,4,6-тетрафторфенил)борат,
триэтиламмония тетракис(2,3,4,6-тетрафторфенил)борат,
трипропиламмония тетракис(2,3,4,6-тетрафторфенил)борат,
три(н-бутил)аммония тетракис(2,3,4,6-тетрафторфенил)борат,
диметил(трет-бутил)аммония тетракис(2,3,4,6-тетрафторфенил)-борат,
N,N-диметиланилиния тетракис(2,3,4,6-тетрафторфенил)борат,
N,N-диэтиланилиния тетракис(2,3,4,6-тетрафторфенил)борат, и
N, N-диметил(2,4,6-триметиланилиния) тетракис(2,3,4,6-тетра-фторфенил)борат;
соли диалкиламмония, такие как:
ди(изопропил)аммония тетракис(пентафторфенил)борат, и дициклогексиламмония тетракис(пентафторфенил)борат ;
соли трехзамещенного фосфония, такие как:
триметилфосфония тетракис(пентафторфенил)борат,
три(о-толил)фосфония тетракис(пентафторфенил)борат, и
три(2,6-диметилфенил)фосфония тетракис(пентафторфенил)борат.
Предпочтительными являются соли тетракис(пентафторфенил)бораты моно- и дизамещенных длинноцепочечным алкилом аммониевых комплексов, особенно C14-C20 алкиламмониевых комплексов, в частности метилди(октадецил)аммония тетракис (пентафторфенил) борат и метилди(тетрадецил)аммония тетракис (пентафторфенил)борат.
Особенно предпочтительной группой активирующих сокатализаторов является трис(пентафторфенил)боран, N-R3, N-R4, анилиния тетракис(пентафторфенил)борат, где R3 и R4 независимо в каждом случае представляют замещенные или незамещенные насыщенные гидрокарбильные группы, имеющие от 1 до 8 углеродных атомов, (R1R2NHCH3)+(C6H4OH)B(C6F5)3 или (R1R2NHCH3) +В (С6F5)4, где R1 и R2 независимо в каждом случае представляют замещенные или незамещенные гидрокарбильные группы, имеющие от 12 до 30 углеродных атомов.
Другой подходящий ионообразующий активирующий сокатализатор содержит соль катионного окислителя и некоординирующегося совместимого аниона, представленную формулой
(Oxe+)d(Ad-)e,
где Oxe+ представляет катионный окислитель, имеющий заряд е+;
е представляет целое число от 1 до 3; и
Аd- и d - такие, как определенные ранее.
Примеры катионных окислителей включают ферроцений, гидрокарбилзамещенный ферроцений, Аg+ или Pb+2. Предпочтительными анионами Аd- являются анионы, определенные выше по отношению к активирующим сокатализаторам, содержащим кислоту Бренстеда, в частности тетракис(пентафторфенил)борат.
Еще один подходящий ионообразующий активирующий сокатализатор содержит соединение, являющееся солью иона карбения и некоординирующегося совместимого аниона, представленной формулой
©+A-,
где ©+ представляет C1-20 карбениевый ион; и
А- такой, как определенный ранее.
Предпочтительным карбениевым ионом является тритильный катион, а именно трифенилметилий.
И еще один подходящий ионообразующий активирующий сокатализатор содержит соединение, являющееся солью иона силилия и некоординирующегося совместимого аниона, представленной формулой
R3Si(X')q +A-,
где R3 представляет C1-10 гидрокарбил, а X', q и А- - такие, как определенные ранее.
Предпочтительными активирующими сокатализаторами, содержащими соль силилия, являются тетракиспентафторфенилборат триметилсилилия, тетракиспентафторфенилборат триэтилсилилия и их эфирозамещенные аддукты. Соли силилия уже были в общем описаны ранее в J. Chem Soc. Chem. Comm., 1993, 383-384; а также Lambert, J.B., et al., Organometallics, 1994, 13, 2430-2443. Применение вышеуказанных солей силилия в качестве активирующих сокатализаторов в дополнение к катализаторам полимеризации заявлено в заявке на патент США под названием "Silylium Cationic Polymerization Activators For Metallocene Complexes", поданной от имени David Neithamer, David Devore, Robert LaPointe and Robert Mussel 12 сентября 1994 г.
Некоторые комплексы спиртов, меркаптанов, силанолов и оксимов с трис(пентафторфенил)бораном также являются эффективными активаторами катализаторов и могут быть использованы в соответствии с настоящим изобретением. Такие сокатализаторы раскрыты в патенте США US 5296433.
Метод электролиза в массе включает электрохимическое окисление металлокомплекса при условиях электролиза в присутствии фонового электролита, содержащего не координирующийся инертный анион. В этом методе используют такие растворители, фоновые электролиты и электролитические потенциалы, чтобы во время реакции, по существу, не образовывались побочные продукты электролиза, делающие металлокомплекс каталитически неактивным. В частности, подходящими растворителями являются материалы, которые представляют собой жидкости в условиях электролиза (обычно при температурах от 0 до 100oС), способные растворять фоновый электролит и инертные. "Инертные растворители" - это те, которые не подвержены восстановлению или окислению в условиях реакции, используемых для электролиза. Для осуществления требуемой реакции электролиза обычно можно выбрать растворитель и фоновый электролит, на которые не оказывает вредного влияния электрический потенциал, используемый для требуемого электролиза. Предпочтительные растворители включают дифторбензол (все изомеры), диметоксиэтан (DME, ДМЭ) и их смеси.
Электролиз может быть проведен в стандартной электролитической ячейке, содержащей анод и катод (называемые также рабочим электродом и противоэлектродом соответственно). Подходящими конструкционными материалами для ячейки являются стекло, пластмасса, керамика и металл, покрытый стеклом. Электроды изготавливают из инертных электропроводящих материалов, под которыми подразумевают электропроводящие материалы, не подверженные вредному влиянию реакционной смеси или условий реакции. Предпочтительными инертными электропроводящими материалами являются платина и палладий. Обычно ячейка разделена посредством ионопроницаемой мембраны, такой как фритта из тонкодисперсного стекла, на отдельные камеры - камеру для рабочего электрода и камеру для противоэлектрода. Рабочий электрод погружают в реакционную среду, содержащую активируемый металлокомплекс, растворитель, фоновый электролит и любые другие материалы, необходимые для обеспечения умеренных условий электролиза или стабилизации полученного комплекса. Противоэлектрод погружают в смесь растворителя и фонового электролита. Требуемое напряжение может быть определено теоретическими расчетами или экспериментально путем развертки ячейки с использованием электрода сравнения (такого, как серебряный электрод), погруженного в электролит в ячейке. Определяют также базовый (фоновый) ток ячейки, т. е. ток, утекающий в отсутствие требуемого электролиза. Электролиз завершают при падении тока от требуемого уровня до базового уровня. Таким образом можно легко обнаружить полную конверсию исходного металлокомплекса.
Подходящими фоновыми электролитами являются соли, содержащие катион и совместимый некоординирующийся анион А-. Предпочтительными фоновыми электролитами являются соли, соответствующие формуле G+A-, где:
G+ представляет катион, нереакционноспособный по отношению к исходному и полученному комплексам, и
А- такой, как определенный ранее.
Примеры катионов (G+) включают тетрагидрокарбилзамещенные аммониевые или фосфониевые катионы, имеющие до 40 неводородных атомов. Предпочтительными катионами являются тетра(н-бутиламмоний)- и тетраэтиламмоний-катионы.
Во время активации комплексов по настоящему изобретению путем электролиза в массе катион фонового электролита проходит к противоэлектроду, а анион А- мигрирует к рабочему электроду и становится анионом полученного окисленного продукта. Растворитель или катион фонового электролита восстанавливается у противоэлектрода в молярном количестве, равном количеству окисленного металлокомплекса, образованного у рабочего электрода. Предпочтительными фоновыми электролитами являются такие соли, как тетракис(перфторарил)бораты; тетрагидрокарбиламмония, имеющие от 1 до 10 углеродных атомов в каждой гидрокарбильной или перфторарильной группе, в частности тетра(н-бутиламмоний)тетракис(пентафторфенил)борат.
Другим ранее раскрытым электрохимическим методом получения активирующих сокатализаторов является электролиз дисиланового соединения в присутствии источника некоординирующегося совместимого аниона. Этот метода более полно раскрыт и заявлен в ранее упомянутой заявке на патент США под названием "Silylium Cationic Polymerization Activators For Metallocene Complexes", поданной 12 сентября 1994 г.
Вышеописанную технологию электрохимического активирования и активирующие сокатализаторы можно также использовать в комбинации. Особенно предпочтительной комбинацией является смесь три(гидрокарбил)алюминия или три(гидрокарбил)борана, имеющего от 1 до 4 углеродных атомов в каждой гидрокарбильной группе, с олигомерным или полимерным алюмоксаном.
Используемое молярное отношение катализатор/сокатализатор предпочтительно находится в пределах от 1:10000 до 100:1; более предпочтительно от 1:5000 до 10:1, наиболее предпочтительно от 1:1000 до 1:1. Алюмоксан при использовании в качестве активирующего сокатализатора только его самого берут в большом количестве, обычно в молярном количестве, превышающем молярное количество металлокомплекса, по крайней мере, в 100 раз. Трис(пентафторфенил)боран при использовании в качестве активирующего сокатализатора берут в молярном отношении к металлокомплексу в пределах от 0,5:1 до 10:1, более предпочтительно от 1:1 до 6:1, а наиболее предпочтительно от 1: 1 до 5:1. Остальные активирующие сокатализаторы обычно используют в приблизительно эквимолярном с металлокомплексом количестве.
Процесс полимеризации может быть использован для полимеризации этиленненасыщенных мономеров, имеющих от 2 до 20 углеродных атомов, либо в отдельности, либо в сочетании. Предпочтительные мономеры включают моновинилиденовые ароматические мономеры, в частности стирол, 4-винилциклогексен, винилциклогексан, норборнадиен и C2-10 алифатические α-олефины, в частности этилен, пропилен, изобутилен, 1-бутен, 1-пентен, 1-гексен, 3-метил-1-пентен, 4-метил-1-пентен, 1-гептен и 1-октен, C4-40 диены и их смеси. Наиболее предпочтительными мономерами являются этилен, пропилен, 1-бутен, 1-гексен, 1-октен и смеси этилена, пропилена и неконъюгированного диена, в частности этилиденнорборнена.
В общем, полимеризация может быть осуществлена при хорошо известных в данной области техники условиях для реакций полимеризации с помощью катализаторов Циглера-Натта или Каминского-Синна, а именно при температурах 0-250oС, предпочтительно 30-200oС, и давлениях от атмосферного до 10000 атмосфер. Можно использовать, по желанию, условия процесса полимеризации в суспензии, в растворе, в газовой фазе, в массе, в твердой порошкообразной фазе или другого процесса. Можно, а при использовании катализаторов в газофазном процессе полимеризации или в суспензии желательно применять носитель, в частности диоксид кремния, оксид алюминия или полимер (особенно поли(тетрафторэтилен) или полиолефин). Носитель предпочтительно используют в количестве, обеспечивающем массовое отношение катализатор (на основе металла): носитель в пределах от 1:100000 до 1:10, более предпочтительно от 1: 50000 до 1: 20, а наиболее предпочтительно от 1:10000 до 1:30. Один такой процесс полимеризации включает контактирование, необязательно в растворителе, одного или нескольких α-олефинов с катализатором по настоящему изобретению в одном или нескольких резервуарах или трубчатых реакторах с непрерывным перемешиванием, соединенных последовательно или параллельно, или в отсутствие растворителя, необязательно в газофазном реакторе с псевдоожиженным слоем, и извлечение полученного полимера. Как хорошо известно в данной области техники, в газофазный реактор можно добавлять сконденсированный мономер или растворитель.
В большинстве реакций полимеризации используемое молярное отношение катализатор:полимеризуемые соединения находится в пределах от 10-12:1 до 10-1: 1, более предпочтительно от 10-9:1 до 10-5:1.
Подходящими растворителями для полимеризации являются инертные жидкости. Примеры включают углеводороды с неразветвленной и разветвленной цепью, такие как изобутан, бутан, пентан, гексан, гептан, октан и их смеси; циклические и алициклические углеводороды, такие как циклогексан, циклопентан, метилциклогексан, метилциклогептан и их смеси; перфторированные углеводороды, такие как перфорированные С4-10 алканы и тому подобное, и ароматические и алкилзамещенные ароматические соединения, такие как бензол, толуол, ксилол, этилбензол и тому подобное. Подходящими растворителями являются также жидкие олефины, которые могут действовать как мономеры или сомономеры и включают этилен, пропилен, бутадиен, 1-бутен, циклопентен, 1-гексан, 1-гептен, 4-винилциклогексен, винилциклогексан, 3-метил-1-пентен, 4-метил-1-пентен, 1,4-гексадиен, 1-октен, 1-децен, стирол, дивинилбензол, аллилбензол, винилтолуол (включая все изомеры в отдельности или в смеси) и тому подобное. Пригодны также смеси указанных растворителей.
Каталитические системы можно использовать в сочетании с, по крайней мере, одним дополнительным гомогенным или гетерогенным катализатором полимеризации в отдельных реакторах; соединенных последовательно или параллельно, для получения смесей полимеров, имеющих требуемые свойства. Пример такого процесса раскрыт в WO 94/00500, эквиваленте заявке США сер. 07/904770, а также заявке США сер. 08/10958, поданной 29 января 1993 г., описания которых включены в данное описание путем ссылки.
Используя каталитические системы по настоящему изобретению, можно легко получить сополимеры с высоким включением сомономеров и соответственно низкой плотностью, но все же имеющие низкий индекс расплава. То есть использование предлагаемых катализаторов, даже при повышенных температурах в реакторе, позволяет легко получать высокомолекулярные полимеры. Этот результат весьма желателен, потому что молекулярная масса α-олефиновых сополимеров может быть легко уменьшена путем использования водорода или подобного агента для передачи цепи, но увеличение молекулярной массы α-олефиновых сополимеров обычно может быть обеспечено только путем снижения температуры полимеризации в реакторе. А это не выгодно, потому что работа полимеризационного реактора при пониженных температурах значительно повышает расходы, так как для поддержания пониженной температуры реакции нужно отводить из реактора тепло, но в то же время необходимо добавлять тепло к вытекающему из реактора потоку, чтобы испарить растворитель. Кроме того, благодаря улучшенной растворимости полимера, пониженной вязкости раствора и более высокой концентрации полимера повышается производительность. Используя предлагаемые катализаторы, можно легко получить α-олефиновые гомополимеры и сополимеры с плотностями от 0,85 г/см3 до 0,96 г/см3 и скоростями течения расплава от 0,001 до 10,0 дг/мин при осуществлении высокотемпературного процесса.
Каталитические системы по настоящему изобретению особенно выгодны для производства этиленовых гомополимеров и сополимеров этилена и α-олефина с высокими уровнями длинноцепочечной разветвленности. Применение катализаторов по настоящему изобретению в непрерывных процессах полимеризации, в частности в непрерывном процессе полимеризации в растворе, позволяет использовать повышенные температуры в реакторе, которые благоприятствуют образованию полимерных цепей с концевым винилом, которые могут быть включены в растущий полимер с образованием длинноцепочечного ответвления. Применение каталитической системы по настоящему изобретению выгодно тем, что обеспечивает возможность экономичного производства сополимеров этилена и α-олефина с обрабатываемостью, подобной той, какую демонстрирует полиэтилен низкой плотности, полученный путем свободнорадикальной полимеризации при высоком давлении.
Предпочтительным способом по настоящему изобретению является способ высокотемпературной полимеризации олефинов в растворе, включающий контактирование одного или нескольких С2-20 α-олефинов при условиях полимеризации с использованием каталитической системы по настоящему изобретению при температуре от примерно 100oС до примерно 250oС. Более предпочтительной температурой для этого способа является температура в пределах от примерно 120oС до примерно 200oС, а еще более предпочтительной - температура в пределах от примерно 150oС до примерно 200oС.
Предлагаемая каталитическая система может быть с выгодой использована для получения олефиновых полимеров с улучшенной обрабатываемостью путем полимеризации только этилена или смесей этилена и α-олефина с низкими уровнями содержания вызывающего "Н"-разветвление диена, такого как норборнадиен, 1,7-октадиен или 1,9-декадиен. Уникальное сочетание повышенных температур в реакторе, высокой молекулярной массы (или низких индексов расплава) при высоких температурах в реакторе и высокой реакционноспособности сомономеров выгодно тем, что обеспечивает возможность экономичного производства полимеров, обладающих превосходными физическими свойствами и способностью к переработке. Такие полимеры предпочтительно содержат С3-20 α-олефин, включающий этилен, и "H"-разветвляющийся сомономер. В соответствии с предпочтительным вариантом такие полимеры получают путем полимеризации в растворе, а наиболее предпочтительно - путем осуществления непрерывного процесса полимеризации в растворе. В соответствии с другим вариантом такие полимеры могут быть получены путем газофазной полимеризации или путем полимеризации в суспензии.
Как было указано ранее, предлагаемая каталитическая система особенно полезна в производстве сополимеров ЭП и ЭПДМ с высокими выходом и производительностью. Используемый процесс полимеризации может быть осуществлен либо в растворе, либо в суспензии, как уже известно в данной области техники. Kaminsky, J. Poly. Sci., том 23, страницы 2151-64 (1985) описал применение растворимой каталитической системы бис(циклопентадиенил)цирконийдиметилалюмоксан для полимеризации в растворе эластомеров ЭП и ЭПДМ. В патенте US 5229478 раскрыт процесс полимеризации в суспензии с использованием подобных каталитических систем на основе бис(циклопентадиенил)циркония.
Вообще говоря, является желательным получать такие ЭП и ЭПДМ эластомеры в условиях повышенной реакционноспособности диенового мономерного компонента. Причина этого была объяснена в указанном выше патенте US 5229478 следующим образом (что все еще остается справедливым, несмотря на достигнутый в этом деле прогресс). Главным фактором, влияющим на производственные затраты и, следовательно, на полезность ЭПДМ, является стоимость диенового мономера. Диен более дорогой мономерный материал, чем этилен или пропилен. Кроме того, реакционноспособность диеновых мономеров при использовании уже известных металлоценовых катализаторов ниже, чем у этилена и пропилена. Следовательно, чтобы достигнуть требуемой степени включения диена для получения ЭПДМ с приемлемо высокой скоростью отверждения, необходимо использовать концентрацию диенового мономера (выраженную в процентах от общей концентрации присутствующих мономеров) в значительном избытке по сравнению с процентным содержанием диена, который должен быть включен в конечный ЭПДМ продукт. Поскольку значительные количества непрореагировавшего диенового мономера должны быть уловлены из вытекающего потока из полимеризационного реактора для возврата в цикл, то производственные затраты необязательно должны увеличиться.
Другим фактором увеличения стоимости производства ЭПДМ является то, что воздействие диена на катализатор полимеризации олефинов, особенно высоких концентраций диенового мономера, необходимых для обеспечения требуемого уровня включения диена в конечный ЭПДМ продукт, часто уменьшает скорость или активность, с которой катализатор заставляет протекать процесс полимеризации мономеров этилена и пропилена. Поэтому требовалось больше пропускать материала через реактор и больше времени на реакцию по сравнению с производством этилен-пропиленового эластомерного сополимера или другого α-олефинового эластомерного сополимера.
Предлагаемая каталитическая система выгодна тем, что позволяет повышать реакционную способность диена и благодаря этому получать ЭПДМ полимеры с высокими выходом и производительностью. Кроме того, каталитическая система по настоящему изобретению обеспечивает возможность экономичного производства ЭПДМ полимеров с содержанием диена до 20 массовых процентов или выше, которые обладают весьма желательными высокими скоростями отверждения.
Неконъюгированный диеновый мономер может быть неразветвленным, разветвленным или циклическим углеводородным диеном, имеющим от 6 до 15 углеродных атомов. Примерами подходящих неконъюгированных диенов являются неразветвленные ациклические диены, такие как 1,4-гексадиен и 1,6-октадиен; разветвленные ациклические диены, такие как 5-метил-1,4-гексадиен, 3,7-диметил-1,6-октадиен, 3,7-диметил-1,7-октадиен и смешанные изомеры дигидромирицена и дигидрооцинена; одноядерные алициклические диены, такие как 1,3-циклопентадиен, 1,4-циклогексадиен, 1,5-циклооктадиен и 1,5-циклододекадиен; и многоядерные алициклические (конденсированные и с мостиковой связью) диены, такие как тетрагидроинден, метилтетрагидроинден, дициклопентадиен; бицикло-(2,2,1)-гепта-2,5-диен; алкенил-, алкилиден-, циклоалкенил-и циклоалкилиденнорборнены, такие как 5-метилен-2-норборнен (MNB), 5-пропенил-2-норборнен, 5-изопропилиден-2-норборнен, 5-(4-циклопентил)-2-норборнен, 5-циклогексилиден-2-норборнен, 5-винил-2-норборнен и норборнадиен.
Из диенов, обычно используемых для получения ЭПДМ сополимеров, предпочтительными являются 1,4-гексадиен (HD), 5-этилиден-2-норборнен (ENB), 5-винилиден-2-норборнен (VNB), 5-метилен-2-норборнен (MNB) и дициклопентадиен (DCPD). Особенно предпочтительными диенами являются 5-этилиден-2-норборнен (ENB) и 1,4-гексадиен (HD).
Предпочтительные ЭПДМ эластомеры могут содержать примерно 20-90, более предпочтительно примерно 30-85, а наиболее предпочтительно примерно 35-80, массовых процентов этилена.
Альфа-олефинами, пригодными для получения эластомеров с этиленом и диенами, предпочтительно являются С3-16 альфа-олефины. Иллюстративными неограничивающими примерами таких альфа-олефинов являются пропилен, 1-бутен, 1-пентен, 1-гексен, 4-метил-1-пентен, 1-гептен, 1-октен, 1-децен и 1-додецен. Альфа-олефин обычно включают в ЭПДМ полимер в количестве примерно 10-80, более предпочтительно примерно 20-65, массовых процентов. Неконъюгированные диены обычно включают в ЭПДМ полимер в количестве примерно 0,5-20, более предпочтительно примерно 1-15, а наиболее предпочтительно примерно 3-12, массовых процентов. При желании можно включить одновременно более одного диена, например HD и ENB, с общим содержанием диенов в указанных выше пределах.
Каталитическая система может быть приготовлена в виде гомогенного катализатора путем добавления необходимых компонентов к раствору, в котором будут осуществлять полимеризацию методом полимеризации в растворе. Каталитическая система может быть также приготовлена и использована в виде гетерогенного катализатора путем адсорбирования необходимых компонентов на носителе, таком как силикагель, оксид алюминия и другой подходящий неорганический носитель. При изготовлении каталитической системы в гетерогенной форме, или на носителе, в качестве носителя предпочтительно используют диоксид кремния. Неорганические носители, такие как, например, диоксид кремния, могут быть обработаны соединениями алкилалюминия или другими средствами успокоения для уменьшения поверхностного содержания гидроксила носителя. Гетерогенную форму каталитической системы можно использовать в процессе газофазной полимеризации или полимеризации в суспензии. Практическим ограничением является то, что полимеризацию в суспензии осуществляют в жидких разбавителях при условиях, в которых полимерный продукт, по существу, нерастворим. Разбавителем для полимеризации в суспензии предпочтительно является один или несколько углеводородов с менее чем 5 углеродными атомами. При желании в качестве разбавителя можно использовать (полностью или частично) насыщенные углеводороды, такие как этан, пропан или бутан. Аналогичным образом, можно использовать (полностью или частично) в качестве разбавителя α-олефиновый мономер или смесь разных α-олефиновых мономеров. В соответствии с наиболее предпочтительным вариантом разбавитель содержит, по крайней мере в качестве основной части, α-олефиновый мономер или полимеризуемые мономеры.
Каталитическая система по настоящему изобретению может включать алюминийорганический компонент, который содержит алюмоксан, алкилалюминий или их комбинацию. Этот компонент может присутствовать в неактивирующем количестве и в основном действует как выноситель или он может взаимодействовать с катализатором, усиливая его активность, или может делать и то, и другое.
Понятно, что при наличии подходящих функциональных групп на катализаторе или сокатализаторе каталитической системы они могут быть ковалентно или ионно связаны с материалом носителя, представляющим собой полимер, неорганический оксид, галогенид металла или их смесь.
Предпочтительные носители для применения в настоящем изобретении включают высокопористые диоксиды кремния, оксиды алюминия, алюмосиликаты и их смеси. Наиболее предпочтительным материалом носителя является диоксид кремния. Материал носителя может быть в гранулированной, агломерированной, таблетированной или любой другой физической форме. Подходящие материалы включают (но не ограничиваются ими) кремнеземы, поставляемые ф. Grace Davison (отделение W.R. Grace & Co.) под названиями SD 3216.30, Davison Syloid 245, Davison 948 и Davison 962, ф. Crossfield под названием ES70 и ф. Degussa AG под названием Aerosil 812; и глиноземы производства ф. Akzo Chemicals Inc. под названием Ketzen Grade В.
Носители, пригодные для применения в настоящем изобретении, предпочтительно имеют площадь поверхности при определении путем азотной порометрии с использованием метода БЭТ (метод Брунауэра-Эммета-Теллера) от 10 до 1000 м/г, а предпочтительно от 100 до 600 м2/г. Пористость носителя при определении путем азотной адсорбции обычно составляет 0,1-3 см3/г, предпочтительно 0,2-2 см2/г. Средний размер частиц зависит от применяемого способа, но обычно находится в пределах от 0,5 до 500 мкм, предпочтительно от 1 до 100 мкм.
Известно, что и кремнезем, и глинозем от природы обладают небольшим количеством гидроксильных функциональных групп. При использовании в качестве носителя в настоящем изобретении эти материалы предпочтительно подвергают термической обработке и/или химической обработке, чтобы уменьшить их гидроксильное содержание. Типичные процессы термической обработки осуществляют при температуре от 30 до 1000oС (предпочтительно в интервале 250-800oС в течение 5 часов или больше) в течение от 10 минут до 50 часов в инертной атмосфере или при пониженном давлении. Типичные химические процессы обработки включают контактирование с содержащими кислоту Льюиса алкилирующими агентами, такими как соединения тригидрокарбилалюминия, соединения тригидрокарбилхлорсилана, соединения тригидрокарбилалкоксисилана или подобные агенты. Остаточные гидроксильные группы удаляют затем путем химической обработки.
Носитель может быть снабжен функциональными группами путем обработки силановым или хлорсилановым функционализирующим агентом с присоединением к нему боковых силановых -(Si-R)= или хлорсилановых -(Si-Cl)= функциональных групп, где R представляет C1-10 гидрокарбильную группу. Подходящими функционализирующими агентами являются соединения, которые вступают во взаимодействие с поверхностными гидроксильными группами носителя или реагируют с кремнием или алюминием матрицы. Примеры подходящих функционализирующих агентов включают фенилсилан, гексаметилдисилазан дифенилсилан, метилфенилсилан, диметилсилан, диэтилсилан, дихлорсилам и дихлордиметилсилан. Способы образования таких функционализированных кремнеземных и глиноземных соединений уже были раскрыты в патентах США 3687920 и 3879368, которые включены в данное описание путем ссылки.
Носитель может быть также обработан алюминиевым компонентом, выбранным из алюмоксана или соединения алюминия формулы AlR1 x'R2 y', где R1 независимо в каждом случае представляет гидрид или R, R2 представляет гидрид, R или OR, x' представляет 2 или 3, у' представляет 0 или 1 и сумма x' и у' равна 3. Примеры подходящих групп R1 и R2 включают метил, метокси, этил, этокси, пропил (все изомеры), пропокси (все изомеры), бутил (все изомеры), бутокси (все изомеры), фенил, фенокси, бензил и бензилокси. Алюминиевый компонент предпочтительно выбран из группы, состоящей из алюмоксанов и соединений три(С1-4гидрокарбил)алюминия. Наиболее предпочтительными алюминиевыми компонентами являются алюмоксаны, триметилалюминий, триэтилалюминий, триизобутилалюминий и их смеси.
Алюмоксаны (также называемые алюминоксанами) представляют собой олигомерные или полимерные оксисоединения алюминия, содержащие цепи чередующихся атомов алюминия и кислорода, причем алюминий несет на себе замещенную, предпочтительно алкильную, группу. Структуру алюмоксана, видимо, представляют следующие общие формулы: (-Al(R)-O)m' для циклического алюмоксана и R2Al-O (-Al (R)-O)m'-AlR2 для линейного соединения, где R - такой, как определенный выше, и m' представляет целое число от 1 до 50, предпочтительно, по крайней мере, 4. Алюмоксаны обычно являются продуктами реакции между водой и алкилалюминием, которые кроме алкильной группы могут содержать галогениды или алкоксиды. Взаимодействие нескольких разных соединений алкилалюминия, таких как, например, триметилалюминий и триизобутилалюминий, дает так называемые модифицированные или смешанные алюмоксаны. Предпочтительными алюмоксанами являются метилалюмоксан и метилалюмоксан, модифицированный незначительными количествами С2-4 алкильных групп, в частности изобутильных групп. Алюмоксаны обычно содержат исходное соединение алкилалюминия в количестве от незначительного до существенного.
Конкретные способы получения соединений типа алюмоксана путем контактирования алкилалюминия с неорганической солью, содержащей воду кристаллизации, раскрыты в патенте США 4542119. В конкретном предпочтительном варианте осуществляют контактирование алкилалюминия с регенерируемым водосодержащим веществом, таким как гидратный оксид алюминия, диоксид кремния или другое вещество. Это раскрыто в ЕР-А-338044. Таким образом, алюмоксан может быть введен в носитель путем осуществления взаимодействия гидратированного глиноземного или кремнеземного материала, необязательно уже функционализированного силаном, силоксаном, гидрокарбилоксисиланом или хлорсиланом, с три(С1-10 алкил)алюминием известными способами. Содержания упомянутых выше патентов и публикаций или соответствующих эквивалентных заявок США включены в данное описание путем ссылки.
Обработка носителя для необязательного введения также алюмоксана или триалкилалюминия включает осуществление контактирования его перед, после или одновремнно с введением комплекса или активированного катализатора с алюмоксаном или триалкилалюминием, в частности триэтилалюминием или триизобутилалюминием. Смесь можно, хотя и не обязательно, нагревать под инертной атмосферой в течение времени и при температуре, достаточных для прикрепления алюмоксана, триалкилалюминия, комплекса или каталитической системы к носителю. Обработанный носитель, содержащий алюмоксан или триалкилалюминий, можно, хотя и не обязательно, подвергать одной или нескольким стадиям промывки, чтобы удалить алюмоксан или триалкилалюминий, не прикрепленный к носителю.
Кроме контактирования носителя с алюмоксаном алюмоксан может быть образован in situ путем контактирования негидролизованного диоксида кремния или оксида алюминия или увлажненного диоксида кремния или оксида алюминия с триалкилалюминием необязательно в присутствии инертного разбавителя. Такой способ хорошо известен в данной области техники и раскрыт в ЕР-А-250600, US-A-4912075 и US-A-5008228, описания которых или соответствующих заявок в США включены в данное описание путем ссылки. Подходящие алифатические углеводородные, разбавители включают пентан, изопентан, гексан, гептан, октан, изооктан, нонан, изононан, декан, циклогексан, метилциклогексан и комбинации двух или более таких разбавителей. Подходящими ароматическими углеводородными разбавителями являются бензол, толуол, ксилол и другие алкильные или галогензамещенные ароматические соединения. Наиболее предпочтительно разбавитель представляет собой ароматический углеводород, в частности толуол. По окончании описанного процесса является желательным снизить остаточное гидроксильное содержание до уровня ниже 1,0 миллиэквивалента ОН на грамм носителя любым из ранее раскрытых способов.
Сокатализаторы по настоящему изобретению могут быть также при необходимости использованы в сочетании с три(гидрокарбил)алюминием, имеющим от 1 до 10 углеродных атомов в каждой гидрокарбильной группе, олигомерным или полимерным алюмоксаном, ди(гидрокарбил)(гидрокарбилокси)алюминием, имеющим от 1 до 10 углеродных атомов в каждой гидрокарбильной или гидрокарбилоксигруппой, или смесью вышеуказанных соединений. Указанные соединения алюминия обычно используют из-за их полезной способности выносить примеси, такие как кислород, вода и альдегиды, из полимеризационной смеси. Предпочтительные соединения алюминия включают соединения С2-6 триалкилалюминия, в частности те, в которых алкильные группы представляют собой этил, пропил, изопропил, н-бутил, изобутил, пентил, неопентил или изопентил и метилалюмоксан, модифицированный метилалюмоксан и диизобутилалюмоксан. Молярное отношение соединения алюминия к металлокомплексу составляет предпочтительно от 1:10000 до 1000: 1, более предпочтительно от 1:5000 до 100:1 и наиболее предпочтительно от 1:100 до 100:1.
Наоборот, полимеризацию в растворе проводят при условиях, в которых разбавитель действует как растворитель для соответственных компонентов реакции, в частности ЭП или ЭПДМ полимера. Предпочтительные растворители включают минеральные масла и различные углеводороды, которые представляют собой жидкость при температурах реакции. Иллюстративные примеры подходящих растворителей включают алканы, такие как пентан, изопентан, гексан, гептан, октан и нонан, а также смеси алканов, включая керосин и Изопар ЕТМ, поставляемый ф. "Еххоn Chemicals Inc."; циклоалканы, такие как циклопентан и циклогексан; и ароматические соединения, такие как бензол, толуол, ксилол, этилбензол и диэтилбензол.
Индивидуальные компоненты, а также регенерированные компоненты катализаторов всегда должны быть защищены от воздействия кислорода и влаги. Следовательно, компоненты катализаторов и катализаторы необходимо приготовлять и регенерировать в свободной от кислорода и влаги атмосфере. Поэтому реакции предпочтительно выполняют в присутствии сухого инертного таза, такого как, например, азот.
Этилен подают в реактор в количестве, обеспечивающем избыточное давление этилена по отношению к суммарному давлению паров α-олефиновых и диеновых мономеров. Содержание этилена в полимере определяется отношением избыточного давления этилена к общему давлению в реакторе. Обычно процесс полимеризации осуществляют при избыточном давлении этилена в пределах от примерно 10 до примерно 1000 фунтов на квадратный дюйм (70-7000 кПа), а наиболее предпочтительно от примерно 40 до примерно 400 фунтов на квадратный дюйм (30-300 кПа). Полимеризацию проводят обычно при температуре от 25 до 200oС, предпочтительно от 75 до 170oС, а наиболее предпочтительно от более чем 95 до 140oС.
Процесс полимеризации может быть периодическим или непрерывным. Предпочтительным является непрерывный процесс, при котором катализатор, этилен, α-олефин и, необязательно, растворитель и диен непрерывно подают в реакционную зону и непрерывно отводят из нее полимерный продукт. Термины "непрерывный" и "непрерывно" при использовании в данном контексте охватывают процессы, в которых введение реагентов и отвод продуктов осуществляют прерывисто с малыми правильными интервалами, так, что в отношении времени общий процесс является непрерывным.
Один из способов осуществления такого процесса полимеризации, никоим образом не ограничивающий объем изобретения, состоит в следующем. В реактор с мешалкой непрерывно подают пропиленовый мономер вместе с растворителем, диеновым и этиленовым мономерами. Реактор содержит жидкую фазу, состоящую в основном из этиленового, пропиленового и диенового мономеров вместе с растворителем или дополнительным разбавителем. При необходимости может быть добавлено небольшое количество вызывающего "Н"-разветвление диена, такого как норборнадиен, 1,7-октадиен или 1,9-декадиен. В жидкую фазу, находящуюся в реакторе, непрерывно вводят катализатор и сокатализатор. Температуру и давление в реакторе можно регулировать путем регулирования отношения растворитель/мономеры, скорости подачи катализаторов, а также посредством охлаждающих или нагревающих змеевиков, рубашек или того и другого. Скорость полимеризации регулируют изменением скорости подачи катализаторов. Содержание этилена в полимерном продукте определяется отношением этилена к пропилену в реакторе, которое регулируют путем изменения соответственных скоростей подачи этих компонентов в реактор. Молекулярную массу полимерного продукта регулируют, необязательно, путем регулирования других переменных полимеризации, таких как температура, концентрация мономеров, или потоком водорода, вводимого в реактор, как хорошо известно в данной области техники. Вытекающий поток из реактора вводят в контакт с подавителем катализаторов, таким как вода. Полимерный раствор нагревают, хотя это и не обязательно, и извлекают полимерный продукт путем отгона газообразного этилена и пропилена, а также остаточного растворителя или разбавителя при пониженном давлении и, если нужно, проведения другого удаления летучих веществ в оборудовании, таком как обезгаживающий экструдер. В непрерывном процессе среднее время пребывания катализатора и полимера в реакторе обычно составляет от 5 минут до 8 часов, предпочтительно от 10 минут до 6 часов.
При предпочтительном способе работы полимеризацию проводят в системе непрерывного действия для полимеризации в растворе, содержащей два реактора, соединенных последовательно или параллельно. В одном реакторе образуется продукт с относительно высокой молекулярной массой (Mw составляет от 300000 до 600000, более предпочтительно от 400000 до 500000), в то время как во втором реакторе образуется продукт с относительно низкой молекулярной массой (Mw 50000-300000). Конечный продукт представляет собой смесь из двух вытекающих из реактора потоков, которые объединяют до обезгаживания с получением однородной смеси двух полимерных продуктов. Такой процесс с двумя реакторами позволяет получать продукты с улучшенными свойствами. В предпочтительном варианте реакторы соединяют последовательно, то есть вытекающий поток из первого реактора направляют во второй реактор и в этот второй реактор добавляют свежий мономер, растворитель и водород. Условия в реакторах регулируют так, чтобы массовое отношение полимера, полученного в первом реакторе, к полимеру, полученному во втором реакторе, находилось в пределах от 20:80 до 80: 20. Кроме того, регулируют температуру во втором реакторе так, чтобы получить продукт с более низкой молекулярной массой. Эта система обеспечивает возможность выгодного производства ЭПДМ продуктов, имеющих широкий диапазон вязкостей по Муни, а также превосходные прочность и способность к переработке. Вязкость по Муни (ASTM D1646-94, ML1+4 @ 125oС) полученного продукта предпочтительно регулируют так, чтобы она находилась в пределах от 1 до 200, предпочтительно от 5 до 150, а наиболее предпочтительно от 10 до 110.
Способ по настоящему изобретению может быть с выгодой использован в газофазной сополимеризации олефинов. Газофазные процессы полимеризации олефинов, в частности гомополимеризация и сополимеризация этилена и пропилена и сополимеризация этилена с высшими α-олефинами, такими как, например, 1-бутен, 1-гексен, 4-метил-1-пентен, хорошо известны в данной области техники. Такие процессы используют в крупномасштабном производстве полиэтилена высокой плотности (HDPE, ПЭВП), полиэтилена средней плотности (MDPE, ПЭСП), линейного полиэтилена низкой плотности (LLDPE, ЛПЭНП).
Используемым газофазным процессом может быть, например, процесс, в котором в качестве реакционной зоны полимеризации используют механически перемешиваемый слой или слой, псевдоожиженный газовой фазой. Предпочтительным является процесс, в котором реакцию полимеризации осуществляют в вертикальном цилиндрическом полимеризационном реакторе, содержащем псевдоожиженный слой частиц полимера, поддерживаемый на перфорированной тарелке (газораспределительной решетке) или взвешенный над ней потоком псевдоожижающего газа.
Газ, используемый для псевдоожижения слоя, содержит мономер или мономеры, подлежащие полимеризации, а также служит в качестве теплообменной среды для отвода тепла реакции из слоя. Горячие газы выходят из верхней части реактора, обычно через успокоительную зону, известную также как зона снижения скорости, имеющая больший, чем у псевдоожиженного слоя, диаметр, причем в этой зоне мелкие частицы, захваченные газовым потоком, имеют возможность падать под действием силы тяжести обратно в слой. Может быть также целесообразным использовать циклон для удаления особо мелких частиц из горячего газового потока. Затем газ обычно возвращают в слой посредством воздуходувки или компрессора через один или несколько теплообменников для освобождения газа от тепла полимеризации.
Предпочтительный способ охлаждения слоя, в дополнение к охлаждению, обеспечиваемому охлажденным рецикловым газом, заключается в подаче в слой летучей жидкости, дающей эффект испарительного охлаждения, часто называемый как работа в режиме конденсации. Летучая жидкость, используемая в этом случае, может представлять собой, например, летучую инертную жидкость, например насыщенный углеводород, имеющий от примерно 3 до примерно 8, предпочтительно 4-6, углеродных атомов. В случае, когда мономер или сомономер сам представляет собой летучую жидкость или может быть сконденсирован с образованием такой жидкости, может быть целесообразной подача его в слой для обеспечения эффекта испарительного охлаждения. Примерами олефиновых мономеров, которые могут быть использованы указанным образом, являются олефины, содержащие
от примерно трех до примерно восьми, предпочтительно три-шесть, углеродных атомов. Летучая жидкость испаряется в горячем псевдоожиженном слое с образованием газа, который смешивается с псевдоожижающим газом. Если летучей жидкостью является мономер или сополимер, то она может быть подвержена некоторой полимеризации в слое. Испарившаяся жидкость выходит затем из реактора как часть горячего рециклового газа и поступает в сжимающую и тепло обменивающую часть рециркуляционного контура. Рециркулирующий газ охлаждают в теплообменнике и, если температура, до которой охлажден газ, ниже точки росы, жидкость выпадает из газа. Эту жидкость желательно непрерывно возвращать в псевдоожиженный слой. Возможно возвращать выпавшую жидкость в слой в виде капель, переносимых рециркулирующим газовым потоком. Такой способ описан, например, в ЕР 89691, US 4543399, WO 94/25495 и US 5352749, которые включены в данное описание путем ссылки. Особенно предпочтительный метод рециркуляции жидкости в слой заключается в отделении жидкости от рециркулирующего газового потока и введении ее опять непосредственно в слой, предпочтительно с использованием способа, обеспечивающего создание капель жидкости в слое. Такого типа способ описан в WO 94/28032 (ВР Chemicals), которая включена в данное описание путем ссылки.
Реакцию полимеризации в псевдоожиженном слое катализируют путем непрерывного или полунепрерывного введения катализатора. Такой катализатор может быть, как описано выше, нанесен на неорганический или органический несущий материал. Катализатор может быть также подвергнут предварительной полимеризации, например, путем полимеризации небольшого количества олефинового мономера в жидком инертном разбавителе с получением каталитического композита, содержащего частицы катализатора, внедренные в частицы олефинового полимера.
Полимер получают непосредственно в псевдоожиженном слое путем катализируемой сополимеризации мономера и одного или нескольких сополимеров на кипящих частицах катализатора, катализаторе на носителе или форполимере в псевдоожиженном слое. Запуск реакции полимеризации обеспечивают, используя слой предварительно отформованных частиц полимера, предпочтительно аналогичного целевому полиолефину, и кондиционируя слой путем сушки инертным газом (или азотом) перед введением катализатора, мономеров и всяких других газов, которые желательно иметь в рециркулирующем газовом потоке, таких как разбавляющий газ, водородный переносчик кинетической цепи или инертный конденсируемый газ при работе в режиме конденсации газовой фазы. Полученный полимер выгружают при необходимости из псевдоожиженного слоя непрерывно или периодически.
Газофазные процессы, пригодные для осуществления настоящего изобретения, предпочтительно являются непрерывными процессами, обеспечивающими непрерывную подачу реагентов в реакционную зону реактора и непрерывное удаление продуктов из реакционной зоны реактора, что обеспечивает создание установившейся среды в реакционной зоне реактора.
Обычно псевдоожиженный слой в газофазном процессе приводят в действие при температурах выше 50oС, предпочтительно в пределах от примерно 60oС до примерно 110oС, более предпочтительно от примерно 70oС до примерно 110oС.
Используемое при полимеризации молярное отношение сомономера к мономеру обычно зависит от требуемой плотности получаемой композиции и составляет около 0,5 или менее. При получении материалов с плотностью от примерно 0,91 до примерно 0,93 желательно, чтобы отношение сомономера к мономеру было меньше 0,2, предпочтительно меньше 0,05, еще более предпочтительно меньше 0,02 и даже меньше 0,01. Отношение водорода к мономеру обычно составляет менее примерно 0,5, предпочтительно менее 0,2, более предпочтительно менее 0,05, еще более предпочтительно менее 0,02 и даже менее 0,01.
Вышеуказанные пределы технологических переменных параметров годятся для газофазного процесса по настоящему изобретению и могут быть пригодными для других процессов, которые могут быть приспособлены для осуществления настоящего изобретения.
В ряде патентов и заявок на патенты описаны газофазные процессы, которые могут быть приспособлены для применения в способе по настоящему изобретению, в частности в патентах США 4588790, 4543399, 5352749, 5436304, 5405922, 5462999, 5461123, 5453471, 5032562, 5028670, 5473028, 5106804, в ЕР заявках 659773 и 692500 и в РСТ заявках WO 94/29032, WO 94/25497, WO 94/25495, WO 94/28032, WO 95/13305, WO 94/26793 и WO 95/07942, все они включены в данное описание путем ссылки.
Катализаторы, независимо от того, нанесены они на носитель или нет, по любому из вышеописанных методов могут быть использованы для полимеризации этилено- и/или ацетиленоненасыщенных мономеров, имеющих от 2 до 100000 углеродных атомов, отдельно или в сочетании. Предпочтительные мономеры включают C2-20 α-олефины, в частности этилен, пропилен, изобутилен, 1-бутен, 1-пентен, 1-гексен, 3-метил-1-пентен, 4-метил-1-пентен, 1-октен, 1-децен, длинноцепочечные макромолекулярные α-олефины и их смеси. Другие предпочтительные мономеры включают стирол, C1-4 алкилзамещенный стирол, тетрафторэтилен, винилбензоциклобутан, этилиденнорборнен, 1,4-гексадиен, 1,7-октадиен, винилциклогексан, 4-винилциклогексан, дивинилбензол и их смеси с этиленом. Длинноцепочечные макромолокулярные α-олефины представляют собой полимерные остатки с концевыми винильными группами, образованные in situ в ходе непрерывных реакций полимеризации в растворе. В подходящих условиях переработки такие длинноцепочечные макромолекулярные звенья легко полимеризуются в полимерный продукт вместе с этиленом и другими короткоцепочечными олефиновыми мономерами с образованием небольших количеств длинноцепочечных ответвлений в полученном полимере.
Катализаторы могут быть также использованы в сочетании с, по крайней мере одним, дополнительным гомогенным или гетерогенным катализатором полимеризации в тех же самых или в отдельных реакторах, соединенных последовательно или параллельно, для получения полимерных смесей, имеющих желательные свойства. Пример такого способа раскрыт в WO 94/00500 (эквивалент заявке в США серийный номер 07/904770), а также в заявке в США серийный номер 08/10958, поданной 29 января 1993 г., которые включены в данное описание путем ссылки.
Высокопредпочтительные комплексы по настоящему изобретению имеют гетероатом азота, присоединенный в положении 3 циклопентадиенильной группы. При использовании в каталитической системе для полимеризации олефинов с трис(пентафторфенил)бороном в качестве активирующего сокатализатора наблюдается необыкновенный голубой цвет. Это может быть обусловлено образованием радикал-катиона, в котором титан находится в формальной степени окисления (III), который может существовать в диамагнитной или парамагнитной форме, как показано ниже.
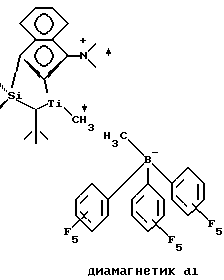
или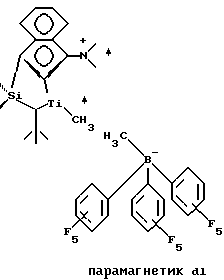
Не связывая себя какой-либо конкретной теорией механизма действия каталитической системы для полимеризации олефинов, содержащей этот комплекс, можно сказать, что имеет место полимеризация, в которой вышеуказанный Ti(III) радикал-катион является активным участником.
Для предпочтительных полиолефиновых полимерных композиций по настоящему изобретению, которые могут быть получены способами полимеризации по настоящему изобретению с использованием каталитических систем по настоящему изобретению, длинноцепочечное ответвление длиннее, чем короткоцепочечное ответвление, что является результатом включения одного или нескольких α-олефиновых сомономеров в главную цепь полимера. Эмпирический эффект наличия длинноцепочечного разветвления в сополимерах по настоящему изобретению проявляется в виде улучшенных реологических свойств, на что показывают более высокие энергии активации текучести и большие отношения I21/I2, чем можно было бы ожидать от других структурных свойств композиций.
Кроме того, высокопредпочтительные полиолефиновые сополимерные композиции по настоящему изобретению имеют противоположную молекулярную структуру, то есть существует максимум молекулярной массы, который имеет место в тех 50 процентах (по массе) композиции, которые имеют самое высокое процентное (по массе) содержание сомономеров. Еще более предпочтительными являются полиолефиновые сополимерные композиции, которые имеют также длинноцепочечные ответвления вдоль по главной цепи полимера, в частности в случае получения их с использованием каталитической системы по настоящему изобретению, имеющей один металлоценовый комплекс по настоящему изобретению, в одном реакторе в процессе полимеризации α-олефинового мономера с одним или несколькими олефиновыми сомономерами, особенно когда процесс непрерывен.
Измерение содержания сомономера в зависимости от логарифма молекулярной массы посредством GPC/FTIR
Содержание сомономера в зависимости от молекулярной массы измеряли используя в сочетании инфракрасный спектрометр с Фурье-преобразованием (FTIR, ИСФП) и гель-проникающий хроматограф (150oС) Уотерса (GPC, ГПХ). Настройка, калибровка и работа этой системы и способ обработки данных уже были описаны ранее (L. J. Rose et al., "Characterisation of Polyethylen Copolimers by Coupled GPC/FTIR" в "Characterisation of Copolimers", Rapra Technology, Shawbury UK, 1995, ISBN 1-85957-048-86). Чтобы характеризовать степень концентрации сомономера в высокомолекулярной части полимера, использовали GPC/FTIR для вычисления параметра, называемого коэффициентом распределения сомономера Cpf. Использовав стандартную методику, определяли также Мn и Мw по данным GPC (ГПХ).
Коэффициент распределения сомономера (GPC-FTIR)
Коэффициент Cpf распределения сомономера вычисляют по данным GPC/FTIR. Он характеризует отношение среднего содержания сомономера в более высокомолекулярных фракциях к среднему содержанию сомономера в более низкомолекулярных фракциях. Более высокие и более низкие молекулярные массы определяют как молекулярные массы выше или ниже средней молекулярной массы соответственно, то есть молекулярно-массовое распределение делят на две части равной массы. Cpf вычисляют по следующему уравнению: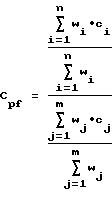
где ci представляет содержание сомономера в мольных долях и wi представляет нормализованную массовую долю при определении посредством GPC/FTIR для n значений данных FTIR выше средней молекулярной массы, cj представляет содержание сомономера в мольных долях и wj представляет нормализованную массовую долю при определении посредством GPC/FTIR для m значений данных FTIR ниже средней молекулярной массы. Лишь те массовые доли, wi или wj, которые связаны со значениями содержания мономера в мольных долях, используют для вычисления Cpf. Для правильного вычисления необходимо, чтобы n и m были больше или равны 3. Данные FTIR, соответствующие фракциям с молекулярной массой ниже 5000, не берут в расчет из-за неопределенности таких данных.
Для полиолефиновых сополимерных композиций по настоящему изобретению Cpf должен быть желательно равен или больше 1,10, более желательно равен или больше 1,15, еще более желательно равен или больше 1,20, предпочтительно равен или больше 1,30, более предпочтительно равен или больше 1,40, еще более предпочтительно равен или больше 1,50 и даже еще более предпочтительно равен или больше 1,60.
ATREF-DV
ATREF-DV уже описано в патенте США 4798081, который включен в данное описание путем ссылки, и в "Determination of Short-Chain Branching Distribution of Ethylen copolimers by Automated Analytical Temperature Rising Elution Fractionation" (Auto-ATREF), J. of Appl. Pol. Sci: Applied Polymer Symposium 45, 25-37 (1990). ATREF-DV - это аналитическая система со сдвоенным детектором, которая способна фракционировать полукристаллические полимеры, подобные линейному полиэтилену низкой плотности (LLDPE, ЛПЭНП), в зависимости от температуры кристаллизации с одновременной оценкой молекулярной массы фракции. Что касается фракционирования, то ATREF-DV аналогично фракционированию элюированием с повышением температуры (Temperature Rising Elution Fractionation) (TREF), которое уже было описано более 15 лет тому назад. Основное различие состоит в том, что этот метод аналитического TREF (ATREF) осуществляют в небольшом масштабе и фракции фактически не выделяют. Вместо этого используют обычный масс-детектор для жидкостной хроматографии (ЖХ), такой как инфракрасный одночастотный детектор для количественного определения распределения степени кристалличности в зависимости от температуры элюирования. Это распределение можно затем трансформировать в любое число областей, таких как частота короткоцепочечного разветвления, распределение сомономеров или, возможно, плотность. Таким образом, это трансформированное распределение можно затем интерпретировать по какой-либо структурной переменной, подобной содержанию сомономера, хотя обычное применение ATREF для сравнения различных линейных полиэтиленов низкой плотности часто осуществляют непосредственно в области температур элюирования.
Для получения данных ATREF-DV коммерчески доступный вискозиметр, в частности, приспособленный для ЖХ-анализа, такой как ViskotekТМ, связывают с ИК масс-детектором. Вместе эти два детектора для ЖХ могут быть использованы для вычисления характеристической вязкости элюента для ATREF-DV. Затем можно оценить средневязкостную молекулярную массу данной фракции, пользуясь подходящими константами Марка Хувинка (Mark Houwink), соответствующей характеристической вязкостью и подходящими коэффициентами для оценки концентрации фракции (дл/г), когда она проходит через детекторы. Таким образом, обычно ATREF-DV сообщает о массовой доле фракций полимера и о средневязкостной молекулярной массе в зависимости от температуры элюирования. Затем, пользуясь приведенным уравнением, вычисляют Mpf.
Коэффициент молекулярно-массового распределения
Коэффициент Mpf молекулярно-массового распределения вычисляют по данным TREF/DV. Он характеризует отношение средней молекулярной массы фракций с высоким содержанием сомономеров к средней молекулярной массе фракций с низким содержанием сомономеров. Более высокие и более низкие содержания сомономеров определяют как находящиеся соответственно ниже или выше средней температуры элюирования на TREF графике концентраций, то есть данные TREF делят на две части равной массы. Mpf вычисляют по следующему уравнению: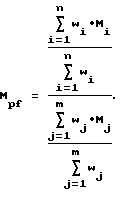
где Mi представляет средневязкостную молекулярную массу и wi представляет нормализованную массовую долю при определении посредством ATREF-DV для n значений данных во фракциях ниже средней температуры элюирования, Mj представляет средневязкостную молекулярную массу и wj представляет нормализованную массовую долю при определении посредством ATREF-DV для m значений данных во фракциях выше средней температуры элюирования. Лишь те массовые доли, wi или wj, которые связаны со средневязкостными молекулярными массами выше нуля, используют для вычисления Mpf. Для правильного вычисления необходимо, чтобы n и m были больше или равны 3.
Для полиолефиновых сополимерных композиций по настоящему изобретению Mpf должен быть желательно равен или больше 1,15, более желательно равен или больше 1,30, еще более желательно равен или больше 1,40, предпочтительно равен или больше 1,50, более предпочтительно равен или больше 1,60, еще более предпочтительно равен или больше 1,70.
Примеры
Специалистам в данной области техники будет понятно, что раскрытое в данном описании изобретение может быть осуществлено в отсутствие какого-либо компонента, который не был конкретно раскрыт. Следующие далее примеры являются дополнительной иллюстрацией изобретения и не должны рассматриваться как ограничивающие. Если не указано иное, все части и проценты выражены по массе.
Спектры 1H и 13С ЯМР были записаны на спектрометре Varian XL (300 МГц). Химические сдвиги определялись относительно ТМС или через остаточный СНСl3 в CDCl3 или остаточный C6HD5 в C6D6 относительно ТМС. Использовали тетрагидрофуран (ТГФ), диэтиловый эфир, толуол и гексан, проходящие через сдвоенные колонки, загруженные активированным оксидом алюминия и смешанным металлооксидным катализатором, нанесенным на оксид алюминия (катализатор Q-5® производства ф. "Engelhard Corp."). Все соединения (н-BuLi, реактивы Гриньяра) использовали в состоянии поставки фирмой "Aldrich Chemical Company". Все процессы синтеза осуществляли в атмосфере сухого азота с использованием комбинации бокса с перчатками и высоковакуумной технологии.
Пример А
Получение 1-N-пирролидининденида лития
В 150 мл гексана вводили 3,5 г l-N-пирролидининдена (может быть получен способом Ноланда и др. (Noland, et al., JOC, 1981, 46, 1940) (18,8 ммоль). К этому раствору прибавляли по каплям в течение 20 минут 9,5 мл nBuLi (2,0 М). Раствор перемешивали 24 часа с осаждением светло-желтого твердого вещества. Твердое вещество собирали путем фильтрования, промывали гексаном и высушивали в вакууме с получением 3,61 г (выход 100%) продукта.
Получение (N-трет-бутиламино)(диметил)(l-N-пирролидининденил)силана
В сухом боксе в круглодонной колбе перемешивали 100 мл ТГФ с 2,16 г ClSiMe2NHCMe3 (17,3 ммоль). К этому раствору прибавляли по каплям 50 мл тетрагидрофуранового раствора, содержавшего 3,30 г (34,9 ммоль) литий-1-N-пирролидининденида. Затем раствор перемешивали всю ночь. Удаляли при пониженном давлении растворитель, остаток экстрагировали гексаном, фильтровали и опять удаляли при пониженном давлении растворитель с получением 5,13 г продукта (выход 95%).
Получение дилитий(N-трет-бутиламино)(диметил)(1-N-пирролидининденил)силана
В сухом боксе смешивали 5,13 г (16,3 ммоль) (N-трет-бутиламино) (диметил)(1-N-пирролидининденил)силана с 100 мл гексана. К этому раствору прибавляли по каплям 16,3 мл (32,6 ммоль) nBuLi (2,0 М). По окончании прибавления nBuLi раствор перемешивали всю ночь. Полученный осадок собирали путем фильтрования и промывали гексаном с получением 5,32 г (выход 100%) желтого твердого вещества.
Получение [(N-трет-бутиламино)(диметил)(1-N-пирролидининденил)силан]титандихлорида
В сухом боксе растворяли 6,05 г (16,3 ммоль) TiCl3(THF)3 в 75 мл ТГФ. К этому раствору прибавляли при перемешивании 5,32 г (1,63 ммоль) дилитий(N-трет-бутиламино)(диметил)(1-N-пирролидининденил)силана в виде твердого вещества. Затем раствор перемешивали в течение 45 минут. По истечении этого времени прибавляли 2,27 г PbCl2 (8,2 ммоль) и раствор перемешивали в течение 45 минут. Затем удаляли при пониженном давлении ТГФ. Остаток экстрагировали толуолом, раствор фильтровали и толуол удаляли при пониженном давлении. Затем остаток растирали с гексаном и раствор охлаждали до -20oС в течение 3 часов. Голубой осадок собирали путем фильтрования и промывали холодным гексаном. Твердый продукт высушивали в вакууме с получением 5,08 г (выход 72%) продукта.
Получение [(N-трет-бутиламино)(диметил)(1-N-пирролидининденил)силан] титандиметила
В сухом боксе суспендировали 0,65 г [(N-трет-бутиламино) (диметил)(1-N-пирродидининденил)силан] титандихлорида (1,5 ммоль) в 50 мл Et2O. К этой суспензии прибавляли по каплям с перемешиванием в течение 20 минут 1,05 мл МеМgВr (3,0 М). По окончании прибавления МеМgBr раствор перемешивали в течение 40 минут. Затем Et2O удаляли при пониженном давлении, и остаток экстрагировали гексаном, раствор фильтровали, фильтрат выпаривали досуха при пониженном давлении с получением 0,47 г (выход 80%) продукта.
Полимеризация
В двухлитровый реактор Парра загружали 740 г растворителя Изопар-Е (Isopar-EТМ) в виде смешанных алканов (производство Exxon Chemicals Inc.) и 118 г 1-октенового сомономера. В качестве средства регулирования молекулярной массы вводили водород с расширением от перепада давления из питающего резервуара емкостью 75 мл при 25 фунтах на квадратный дюйм (2070 кПа). Реактор нагревали до температуры полимеризации (140oС) и насыщали этиленом при избыточном давлении 500 фунтов на квадратный дюйм (3,4 МПа). В сухом боксе предварительно смешивали подходящее количество катализатора и сокатализатора в виде 0,005 М растворов в толуоле. По истечении времени, необходимого для предварительного смешивания, раствор переносили в питающий резервуар для катализатора и вводили в реактор. Условия полимеризации поддерживали в течение 15 минут с подачей этилена по потребности. Полученный раствор извлекали из реактора и добавляли к нему связанный фенольный антиоксидант (IrganoxТМ 1010 производства Ciba Geigy Corporation). Образованные полимеры высушивали в вакуумной печи при 120oС в течение примерно 20 часов. Результаты представлены в табл. 1.
Общие условия проведения опытов для примеров 1-79.
Все опыты с использованием металлоорганических соединений проводили по методике с применением сухого бокса. Растворители (ТГФ, гексан, толуол, эфир) очищали путем пропускания через колонки с оксидом алюминия и Q5. C6D6 сушили под Na/K сплавом и подвергали вакуумной перегонке перед применением. ЯМР-спектры измеряли на приборе Varian XL-300 (FT 300 МГц, 1Н; 75 МГц, 13С). Данные 1H ЯМР- и 13С{ 1Н} ЯМР-спектров соотнесены с остаточными пиками растворителя и даны в м.д. (миллионные доли) относительно тетраметилсилана. Все значения J даны в Гц (герцах). Масс-спектры (EI) получали на приборе AutoSpecQFDP. Индан, NaBH4, MeMgI, n-BuLi, Me2SiCl2, NHz-t-Bu, 2-бромизобутирилбромид покупали у Aldrich Chemical Со. Все соединения использовали в состоянии получения. 3-метокси-1Н-инден (J. Am. Chem. Soc., 1984, 106, 6702), N-(1H-2-инденил)-N, N-диметиламин (Acta Chem Scand, 1973, 27, 4027), 1-(1Н-2-инденил)пирролидин (Acta Chem Scand, 1973, 27, 4027), трет-бутил(1H-2-инденилокси)диметилсилан (Organometallics, 1996, 15, 2450) получали способами, описанными в указанной литературе.
Пример 1
Получение 1,1',4,4'-тетраметил-2,3-дигидронафталина
Охлаждая бензол (500 мл) и 2,3-диметил-2,3-бутандиол (50,00 г, 341,9 ммоль) в ледяной бане, медленно прибавляли АlСl3 (100,30 г, 752,24 ммоль) в виде твердого вещества в течение 30 минут под потоком азота, в результате чего температура смеси никогда не превышала комнатную температуру. Смесь держали при комнатной температуре 30 минут и затем нагревали до 50oС в течение 1 часа. Важно тщательно контролировать реакцию путем ЖХ и прекращать ее после завершения. Незначительные изменения условий реакции приводят к изменению времени реакции. По истечении времени реакции смесь осторожно декантировали на раздробленный лед, чтобы оставить небольшую и более плотную маслянистую фазу. Затем верхнюю фазу реакционной смеси переносили в экстракционную воронку и промывали 1 М НСl (1•200 мл), насыщенным NaHCO3 (2•200 мл) и Н2O (1•200 мл). Затем органическую фракцию сушили над MgSO4. Смесь фильтровали и удаляли летучие вещества, в результате чего был выделен целевой продукт в виде прозрачного бесцветного масла (53,10 г, выход 82,5%).
1H ЯМР (СDСl3) δ 1,31 (с, 12Н), 1,71 (с, 4Н), 7,1-7,4 (м, 4Н).
13С ЯМР (CDCl3) δ 31,67, 34,19, 35,09, 125,50, 126,45, 144,76.
ГХ-МС: вычислено для C14H20 188,16, найдено 188,10.
Получение 2,3,5,7-тетрагидро-2,5,5,8,8-пентаметил-1Н-бенз(f)инден-1-она
1,1',4,4'-тетраметил-2,3-дигидронафталин (30,00 г, 159,3 ммоль) и 2-бромизобутирилбромид (36,62 г, 159,3 ммоль) перемешивали в СН2Сl2 (500 мл) при 0oС, медленно прибавляя АlСl3 (48,86 г, 366,4 ммоль) в виде твердого вещества под потоком азота в течение 30 минут. Затем этой смеси давали перемешиваться всю ночь при комнатной температуре. По истечении времени реакции смесь выливали на раздробленный лед. Органический слой отделяли и промывали 1 М НСl (1•200 мл), насыщенным NaHCO3 (2•200 мл) и H2O (1•200 мл). Затем органическую фракцию сушили над MgSO4, фильтровали и удаляли летучие вещества, в результате чего был выделен темный кристаллический остаток. Перекристаллизация из диэтилового эфира (0oС) дала целевой продукт в виде белого кристаллического твердого вещества (30,70 г, выход 75,2%).
1H ЯМР (CDCl3) δ 1,2-1,4 (м, 15Н), 1,71 (с, 4Н), 2,6-2,7 (м, 2Н), 3,34 (дд, 1Jн.н = 17,6 Гц, 3Jн.н =8,7 Гц, 1Н), 7,41 (с, 1Н), 7,76 (с, 1Н).
13С ЯМР (CDCl3) δ 16,50, 31,98, 32,09, 32,14, 34,58, 34,84, 35,25, 42,30, 121,92, 124,18, 133,85, 144,77, 149,94, 152,94, 209,05.
ГХ-МС: вычислено для C18H24O 256,18, найдено 256,15.
Получение 3-(диметиламино)-5,6,7,8-тетрагидро-2,5,5,8, 8-пентаметил-1Н-бенз (f)индена (1)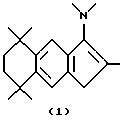
К раствору безводного диметиламина (12,8 г, 290 ммоль) в 200 мл гексана прибавляли по каплям ТiСl4 (6,6 г, 35,0 ммоль) с перемешиванием под азотом при температуре от -30 до -40oС. Когда в ходе этого процесса начинали образовываться большие куски твердого амида, прибавляли 2,3,5,7-тетрагидро-2,5,5,8,8-пентаметил-1Н-бенз(f)инден-1-он (4,98 г, 19,6 ммоль). Реакционной смеси давали возможность уравновеситься до 25oС и затем нагревали до 55oС с перемешиванием в течение 10 минут. 1Н ЯМР-анализ аликвоты показал отсутствие исходного материала. Раствор охлаждали до 10oС и прибавляли по каплям ацетон (приблизительно 500 мг, высушенных над молекулярными ситами  ) для разложения растворимого титанамидного комплекса. После введения конечного количества ацетона полностью исчез цвет и образовался TiO2. Оксид отфильтровывали через сухой Целит и отгоняли в вакууме растворитель с получением продукта (3,3 г, 11,6 ммоль) при выходе 60% в виде прозрачного масла, которое, простояв всю ночь, кристаллизовалось из гексана в виде светло-желтых призм (т. пл. 74-75,5oС).
) для разложения растворимого титанамидного комплекса. После введения конечного количества ацетона полностью исчез цвет и образовался TiO2. Оксид отфильтровывали через сухой Целит и отгоняли в вакууме растворитель с получением продукта (3,3 г, 11,6 ммоль) при выходе 60% в виде прозрачного масла, которое, простояв всю ночь, кристаллизовалось из гексана в виде светло-желтых призм (т. пл. 74-75,5oС).
1Н ЯМР (С6D6) δ 7,52 (2, 1H), 7,31 (с, 1Н), 3,03 (с, 2Н), 2,83 (с, 6Н), 1,97 (с, 3Н), 1,67 (с, 4Н), 1,35 (с, 6Н), 1,33 (с, 6Н).
13С{ 1Н} ЯМР (С6D6) δ 142,0, 142,7, 142,3 140,3, 139,7, 126,4, 121,7, 117,2, 43,3, 41,4, 36,0, 34,7, 34,6, 32,7, 32,6, 14,6.
ГХ-МС (El, m/e, процент I) 283 (М+, 35), 268 (М-СН3, 100), 238 (10).
Получение (3-(диметиламино)-5,6,7,8-тетрагидро-2,5,5, 8,8-пентаметил-1Н-бенз(f)инденил)лития (2)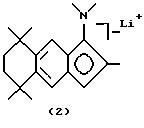
К перемешиваемому 3-(диметиламино)-5,6,7,8-тетрагидро-2, 5,5,8,8-пентаметил-1Н-бенз(f)индену (2,11 г, 7,46 ммоль) в гексане (75 мл) медленно прибавляли n-BuLi (4,10 мл 2,0 М раствора в гексане, 8,20 ммоль). Давали этой смеси перемешиваться всю ночь с образованием в течение этого периода бледно-желтого осадка. По окончании времени реакции целевой продукт собирали путем фильтрования, промывали гексаном и высушивали в вакууме с получением бледно-желтого твердого вещества, которое использовали без дальнейшей очистки или анализа (2,00 г, выход 93%).
Получение 1-(3-(диметиламино)-5,6,7, 8-тетрагидро-2,5,6, 7, 8-пентаметил-1Н-бенз(f)инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланамина (3)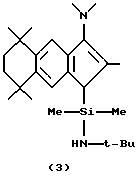
К раствору N-(трет-бутил)-N-(-1-хлор-1,1-диметилсилил)-амина (1,71 г, 10,3 ммоль) в ТГФ (50 мл) прибавляли по каплям (3-(диметиламино)-5,6,7,8-тетрагидро-2,5,5,8,8-пентаметил-1Н-бенз (f)инденил) литий (1,99 г, 6,87 ммоль) в ТГФ (30 мл). Этой смеси давали перемешиваться всю ночь. По окончании времени реакции удаляли летучие вещества и остаток экстрагировали гексаном и фильтровали. Удаление гексана дало целевой продукт в виде оранжевого масла (2,793 г, 98%).
1H ЯМР (С6D6) δ 0,024 (с, 3Н), 0,16 (с, 3Н), 1,06 (с, 9Н), 1,34 (с, 3Н), 1,39 (с, 4Н), 1,46 (с, 3Н), 1,71 (с, 3Н), 2,12 (с, 1Н), 2,20 (с, 3Н), 2,92 (с, 6Н), 3,08 (с, 1Н), 7,51 (с, 1Н), 7,63 (с, 1Н).
13С ЯМР (С6D6) δ 0,28, 1,47, 15,48, 32,57, 32,68, 32,75, 33,82, 34,50, 34,56, 35,89, 43,63, 47,57, 49,41, 116,99, 121,76, 132,70, 139,02, 140,98, 141,36, 146,14.
Получение (3-(диметиламино)-1-(((1,1-диметилэтил)амино)диметилсилил)-5,6,7,8-тетрагидро-2,5,6,7,8-пентаметил-1Н-бенз(f)инденил)лития, литиевая соль (4)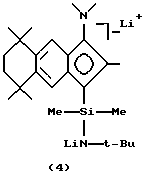
К перемешиваемому 1-(3-(диметиламино)-5,6,7,8-тетрагидро-2, 5,6,7, 8-пентаметил-1Н-бенз(f)инден-1-ил) -N- (1,1-диметилэтил)-1,1-диметилсиланамину (2,79 г, 6,77 ммоль) в гексане (75 мл) медленно прибавляли n-BuLi (16,24 ммоль, 6,50 мл 2,5 М раствора в гексане). Этой смеси давали перемешиваться всю ночь без образования в течение этого периода осадка. Затем раствор помещали в холодильник (-10oС) на 4 дня, в течение которых образовались бледно-желтые кристаллы. Раствор сливали, а оставшиеся кристаллы высушивали в вакууме и использовали без дальнейшей очистки или анализа (1,30 г, выход 45%).
Получение дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-(3-диметиламино)-5,6,7,8-тетрагидро-2,5,5,8,8-пентаметил-1Н-бенз-(f)инден-1-ил)силанаминато(2-)-N)титана (5)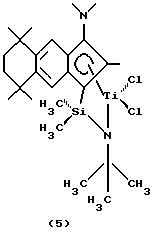
К суспензии TiCl3(THF)3 (1,14 г, 3,08 ммоль) в ТГФ (50 мл) прибавляли по каплям (3-(диметиламино)-1-(((1,1-диметилэтил)амино)диметилсилил)-5,6,7,8-тетрагидро-2,5,6,7,8-пентаметил-1Н-бенз(f)инденил)литий, литиевая соль (1,30 г, 2,08 ммоль) в ТГФ (30 мл). Этой смеси давали перемешиваться в течение 1 часа. Затем прибавляли PbCl2 (0,43 г, 1,54 ммоль) в виде твердого вещества и смеси давали перемешиваться еще час. По истечении времени реакции удаляли летучие вещества и остаток экстрагировали гексаном и фильтровали. Гексановый раствор концентрировали и помещали в холодильник (-10oС) на всю ночь, в течение которой образовались темно-фиолетовые кристаллы. Затем раствор сливали и кристаллы высушивали в вакууме (1,23 г, выход 76%).
1H ЯМР (С6D6) δ 0,59 (с, 3Н), 0,78 (с, 3Н), 1,26 (с, 3Н), 1,29 (с, 3Н), 1,32 (с, 3Н), 1,38 (с, 9Н), 1,44 (с, 3Н), 1,5-1,7 (м, 4Н), 2,35 (с, 3Н), 2,94 (с, 6Н), 7,79 (с, 1Н), 7,81 (с, 1Н).
13С ЯМР (С6D6) δ 5,62, 6,34, 18,34, 32,18, 32,33, 32,59, 32,84, 33,42, 34,94, 35,09, 43,46, 60,83, 92,03, 122,50, 125,80, 131,70, 134,08, 146,10, 147,80, 150,14.
Пример 2
Получение ( (3-диметиламино)-5,6,7,8-тетрагидро-2,5,5,8, 8-пентаметил-1H-бенз(f)инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)диметилтитана (6)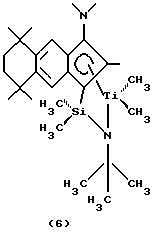
Дихлор(N- (1,1-диметилэтил) -1,1-диметил-1- (3-(диметиламино)-5,6,7,8-тетрагидро-2,5,5,8,8-пентаметил-1Н-бенз(f)инден-1-ил)силанаминато(2-)-N)титан (0,65 г, 1,23 ммоль) перемешивали в диэтиловом эфире (50 мл), медленно прибавляя МеМgВr (2,70 ммоль, 0,90 мл 3,0 М раствора в диэтиловом эфире). Этой смеси давали перемешиваться в течение 2 часов. По истечении времени реакции удаляли летучие вещества и остаток экстрагировали гексаном и фильтровали. Удаление гексана дало целевой продукт в виде оранжевого микрокристаллического твердого вещества (0,44 г, выход 74%).
1H ЯМР (С6D6) δ -0,12 (с, 3Н), 0,54 (с, 3Н), 0,75 (с, 3Н), 0,96 (с, 3Н), 1,21 (с, 3Н), 1,33 (с, 3Н), 1,35 (с, 3Н), 1,36 (с, 3Н), 1,52 (с, 9Н), 1,6-1,7 (м, 4Н), 2,11 (с, 3Н), 2,92 (с, 6Н), 7,65 (с, 1Н), 7,93 (с, 1Н).
13С ЯМР (С6D6) δ 5,92, 6,85, 15,48, 32,58, 32,76, 33,79, 34,51, 34,77, 35,26, 35,45, 44,47, 53,09, 53,97, 57,86, 83,82, 121,46, 124,92, 126,42, 131,45, 133,30, 142,64, 143,25, 144,51.
Пример 3
Получение 1-(3,5,6,7-тетрагидро-2-метил-втор-индацен-1-ил)пирролидина (7)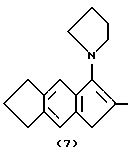
1,2,3,5,6,7-гексагидро-втор-индацен-1-он (7,0 г) обрабатывали 25 г пирролидина в 100 мл сухого бензола, как в примере 1, за исключением того, что прибавляли п-толуолсульфоновую кислоту (15 мг) в качестве катализатора. ГХ-анализ показал, что через 17 часов имела место конверсия в енамин, составляющая лишь 25% по площади, а 80%-ная (по площади) конверсия происходит через 64 часа. Дистилляция низкокипящего кетона дала две фракции енамина с отношением кетонов (проценты площади ГХ) 75:25 (3,1 г, т.к. (точка кипения) = 183-192oС @ 1 мм) и 85:15 (2,3 г, т.к. = 192-195oС @ 1 мм). Вязкий темный кубовый остаток растирали с гексаном с получением после удаления растворителя 650 мг темного масла, которое содержало 91% (по площади) енамина при определении путем ГХ-анализа. Этот материал был предназначен для образования литиевой соли:
1H ЯМР (CDCl3) δ 7,26 (с, 1Н), 7,18 (с, 1Н), 3,45 (м, 4Н), 3,21 (с, 2Н), 2,91 (м, 4Н), 2,15 (с, 3Н, 2-Ме), 2,05-2,17 (м, 2Н), 1,95 (м, 4Н).
13С {1Н} ЯМР (CDCl3) δ 141,3, 140,4, 139,3, 123,2, 121,9, 121,4, 118,4, 118,1, 115,2, 50,9, 41,5, 33,2, 32,6, 26,0, 25,3; ГХ-МС (El, m/e, процент I) 239 (М+, 30), 224 (М-СН3, 100), 169 (27) 155 (55).
Получение 1,2,3,7-тетрагидро-6-метил-5-(1-пирролидинил-втор-индаценил)лития (8)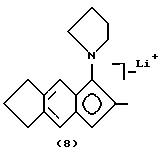
К перемешиваемому 1-(3,5,6,7-тетрагидро-2-метил-втор-индацен-1-ил)пирролидину (0,64 г, 2,93 ммоль) в гексане (25 мл) медленно прибавляли n-BuLi (3,00 ммоль, 1,50 мл 2,0 М раствора в циклогексане). Этой смеси давали перемешиваться в течение ночи с образованием за это время осадка. По истечении времени реакции получили после фильтрования и высушивания в вакууме целевой продукт в виде рыжевато-коричневого твердого вещества, которое использовали без дальнейшей очистки или анализа (0,55 г, выход 84%).
Получение N-(1,1-диметилэтил)-1,1-диметил-1-(1,5,6,7-тетрагидро-2-метил-3-(1-пирролидинил)-втор-индацен-1-ил)-силанамина (9)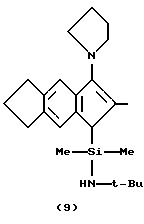
К раствору N-(трет-бутил)-N-(1-хлор-1,1-диметилсилил)-амина (1,02 г, 6,13 ммоль) в ТГФ (75 мл) прибавляли по каплям 1,2,3,7-тетрагидро-6-метил-5-(1-пирролидинил-втор-индаценил)литий (0,55 г, 2,46 ммоль) в ТГФ (25 мл). Этой смеси давали перемешиваться в течение ночи. По истечении времени реакции удаляли летучие вещества и остаток экстрагировали гексаном и фильтровали. Удаление гексана дало целевой продукт в виде зеленого масла (0,84 г, 99%).
1H ЯМР (CDCl3) δ -0,040 (с, 3Н), 0,060 (с, 3Н), 1,18 (с, 9Н), 1,9-2,2 (м, 6Н), 2,17 (с, 3Н), 2,8-3,0 (м, 4Н), 3,16 (с, 1Н), 3,2-3,3 (м, 2Н), 3,3-3,5 (м, 2Н), 7,23 (с, 1Н), 7,25 (с, 1Н).
Получение дихор(N-(1,1-диметилэтил)-1,1-диметил-1-((1, 2, 3, 3а, 8а-η) -1, 5, 6, 7-тетрагидро-2-метил-3- (1-пирролидинил) -втор-индацен-1-ил)силанаминато(2-)-N)титана (10)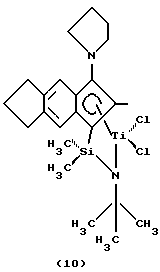
К перемешиваемому N-(1,1-диметилэтил)-1,1-диметил-1-(1,5,6,7-тетрагидро-2-метил-3-(1-пирролидинил)-втор-индацен-1-ил)силанамину (0,84 г, 2,43 ммоль) в гексане (50 мл) медленно прибавляли n-BuLi (4,86 ммоль, 2,43 мл 2,0 М раствора в циклогексане). Этой смеси давали перемешиваться в течение ночи с образованием за это время небольшого количества осадка. Удалив летучие вещества, получили темный остаток. Затем этот остаток растворяли в ТГФ (30 мл) и раствор прибавляли по каплям к суспензии ТiСl3(THF)3 (0,90 г, 2,43 ммоль) в ТГФ (50 мл). Этой смеси давали перемешиваться в течение 1 часа. Затем прибавляли PbCl2 (0,37 г, 1,32 ммоль) в виде твердого вещества и смеси давали перемешиваться еще 30 минут. По истечении времени реакции удаляли летучие вещества и остаток экстрагировали толуолом и фильтровали. Удаление толуола дало темный остаток. Этот остаток суспендировали в гексане и охлаждали до 0oС в течение ночи. Затем смесь фильтровали, получив в результате черное микрокристаллическое твердое вещество. Эту процедуру суспендирования в гексане с последующим охлаждением повторяли и полученное черное соединение высушивали в вакууме (0,37 г, выход 33%).
1H ЯМР (CDCl3) δ -0,78 (с, 3Н), 0,84 (с, 3Н), 1,32 (с, 9Н), 1,5-2,2 (м, 8Н), 2,59 (с, 3Н), 2,8-3,1 (м, 6Н), 3,8-4,0 (м, 2Н), 4,1-4,3 (м, 2Н), 7,42 (с, 1Н), 7,74 (с, 1Н).
Пример 4
Получение(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,8а-η)-1,5,6,7-тетрагидро-2-метил-3- (1-пирролидинил) -втор-индацен-1-ил)силанаминато(2-)-N)диметилтитана (11)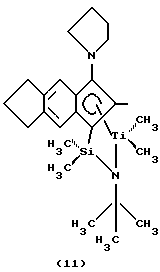
К перемешиваемому дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 8а-η) -1,5,6,7-тетрагидро-2-метил-3-(1-пирролидинил)-втор-индацен-1-ил)силанаминато(2-)-N)титану (0,37 г, 0,76 ммоль) в диэтиловом эфире (50 мл) медленно прибавляли МеМgВr (1,53 ммоль, 1,02 мл 3,0 М раствора в диэтиловом эфире). Этой смеси давали перемешиваться в течение 1 часа. По истечении времени реакции удаляли летучие вещества и остаток экстрагировали гексаном и фильтровали. Удаление гексана дало целевой продукт в виде красного твердого вещества
(0,11 г, выход 33%).
1H ЯМР (CDCl3) δ 0,038 (с, 3Н), 0,59 (с, 3Н), 0,74 (с, 3Н), 0,94 (с, 3Н), 1,54 (с, 9Н), 1,5-1,8 (м, 8Н), 2,21 (с, 3Н), 2,6-2,9 (м, 6Н), 3,2-3,2 (м, 2Н), 3,7-3,8 (м, 2Н), 7,53 (с, 1Н), 7,68 (с, 1Н).
Пример 5
Получение 1-(lH-инден-3-ил)пиперидина (12)
В соответствии с общим способом катализируемого титаном получения енамина из примера 7 сухой пиперидин (51,4 г, 600 ммоль) обрабатывали с использованием ТiСl4 (14,35 г, 75,7 ммоль) в 400 мл CH2Cl2 при 0oС. Прибавляли 1-инданон (10 г, 75,6 ммоль) при этой температуре и доводили реакционную смесь до 25oС. 1H ЯМР-анализ полученной аликвоты показал полное превращение в продукт. Удаляли растворитель путем выпаривания на роторном испарителе и полученное темное масло и остаток TiO2 растирали с 300 мл гексана. Раствор фильтровали через сухой Целит и выпаривали с получением неочищенного продукта (20 г темного масла). Продукт перегоняли через 6'' (152,4 мм) колонку Vigreaux с получением чистого продукта (11,01 г, 55,1 ммоль) при выходе 73% в виде светло-желтого масла (98%-ный по площади енамин согласно ГХ-анализу): т.к. = 143oС @ 1 мм.
1H (CDCl3) δ 7,41 (д, 2Н, J=7,7 Гц), 7,27 (т, 1Н, J=7,5 Гц), 7,18 (д, 1H, J = 7,5 Гц), 5,52 (д, 1Н, J = 2 Гц), 3,30 (д, 2Н, J=2 Гц), 3,04 (т, 4Н, J = 5,2 Гц), 1,74 (м, 4Н), 1,60 (м, 2Н).
13С{ 1Н} (CDCl3) δ 154,0, 144,4, 141,7, 125,6, 124,6, 124,1, 119,8, 108,8, 52,3, 35,8, 26,2, 24,9.
Получение (3-(1-пиперидинил)-1H-инденил)лития (13)
В 75 мл гексана растворяли 1-(1H-инден-3-ил)пиперидин (3,00 г, 15,1 ммоль) и к полученному раствору прибавили по каплям с помощью шприца в течение 5 минут 7,1 мл 2,5 М n-BuLi (1,09 экв). При добавлении первых 0,5 мл n-BuLi в растворе появлялся желтый осадок. Полученной суспензии давали перемешиваться в течение 24 часов. По истечении этого времени отфильтровывали твердое вещество, промывали его 50 мл гексана и давали высохнуть в вакууме в течение ночи, получив в результате целевой анион в виде желтого твердой вещества (2,96 г, 14,3 ммоль) с выходом 95%.
Получение N-(1,1-диметилэтил)-1,1-диметил-1-(3-(1-пиперидинил)-1Н-инден-1-ил)силанамина (14)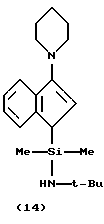
В 40 мл ТГФ растворяли (3-(1-пиперидинил)-1H-инденил)-литий (2,96 г, 14,4 ммоль) и прибавляли по каплям к раствору N-(трет-бутил)-N-(1-хлор-1,1-диметилсилил)амина (3,20 г, 19,3 ммоль) в 30 мл ТГФ в течение 45 минут с продолжением перемешивания в течение 25 часов. Раствор выпаривали в вакууме с получением темно-красного масла, которое растворяли в гексане (100 мл). Отфильтровывали из этого раствора LiCl и в течение ночи удаляли под вакуумом растворитель с получением N-(трет-бутил)-N-(1,1-диметил-1-(3-пиперидино-1Н-1-инде-нил)силил)амина (4,5 г, 13,7 ммоль) в виде темно-красного масла с выходом 95%.
1H (С6D6) δ 7,58 (т, 2Н, J = 5,7 Гц), 7,27 (т, 1Н, J = 7,5 Гц), 7,19 (д, 1Н, J = 7,5 Гц), 5,73 (д, 1Н, J = 2 Гц), 3,36 (д, 2Н, J = 2 Гц), 3,01 (м, 4Н), 1,63 (п, 4Н, J = 5,5 Гц), 1,44 (п, 2Н, J = 5,5 Гц), 1,09 (с, 9Н), 0,50 (широкий с, 1Н), 0,36 (с, 3Н), -0,05 (с, 3Н).
13С{ 1Н} (С6D6) δ 153,10, 146,1, 141,5, 124,7, 124,1, 123,8, 120,2, 112,2, 49,6, 44,2, 34,1, 26,7, 25,3, 0,4, -0,5.
Получение (1-(((1,1-диметилэтил)амино)диметилсилил)-3-(1-пиперидинил)-1H-инденил)лития, литиевая соль (15)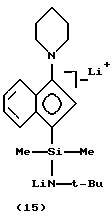
В сухом боксе в 65 мл гексана растворяли 4,73 г (14,4 ммоль) N-(1,1-диметилэтил)-1,1-диметил-1-(3-(1-пиперидинил)-1Н-инден-1-ил)силанамина. К полученному раствору прибавляли по каплям 17,00 мл (34 ммоль) n-BuLi (2 М). По окончании введения n-BuLi раствор перемешивали всю ночь. Полученный осадок собирали путем фильтрования, промывали гексаном (2•30 мл) и сушили при пониженном давлении с получением 4,70 г желтого твердого вещества. Выход 96%.
Получение дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1, 2,3,3а,7а-η)-3-( 1-пиперидинил) -1Н-инден-1-ил) силанаминато-(2-)-N)титана (16)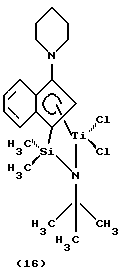
К суспензии ТiСl3(ТНF)3 (5,11 г, 13,8 ммоль) в 70 мл ТГФ прибавляли в течение 2 минут раствор (1-(((1,1-диметилэтил)-амино)диметилсилил)-3-(1-пиперидинил)-1H-инденил)лития, литиевая соль (4,70 г, 13,8 ммоль) в 35 мл ТГФ. Через 1 час смешивания прибавляли PbCl2 (2,50 г, 9,0 ммоль) в виде твердого вещества. Реакционную смесь перемешивали еще час. Затем удаляли при пониженном давлении растворитель. Остаток экстрагировали 70 мл толуола и фильтровали через стеклянную фритту со средним размером пор. Удаляли при пониженном давлении толуол и остаток растирали с 30 мл гексана. Черное кристаллическое твердое вещество собирали путем фильтрования, промывали гексаном (2•30 мл) и затем высушивали при пониженном давлении с получением 4,26 г продукта в виде красно-коричневого твердого вещества. Выход 69%.
1H (С6D6) δ 0,48 (с, 3Н), 0,64 (с, 3Н), 1,31 (м, 6Н), 1,38 (с, 9Н), 3,18 (м, 2Н), 3,58 (м, 2Н), 5,92 (с, 1Н), 6,98 (т, 1Н, 3Jн.н = 7,54 Гц), 7,09 (т, 1Н, 3Jн.н = 7,5 Гц), 7,52 (д, 1H, 3Jн.н = 8,5 Гц), 7,63 (д, 1H, 3Jн.н = 8,7 Гц).
13С{ 1Н} (С6В6) δ 1,35, 4,15, 24,35, 26,14, 32,88, 51,62, 61,46, 92,92, 111,79, 125,08, 128,67, 128,92, 135,42, 151,09.
МСВР (EI, М+): вычислено 444,1038, найдено 444,1033.
Пример 6
Получение(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитана (17)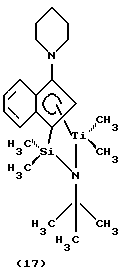
В сухом боксе в 40 мл Et2O растворяли 0,60 г дихлор(N-(1,1-диметилэтил) -1,1-диметил-1- ( (1,2,3, 3а, 7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титана (1,35 ммоль). К полученному раствору прибавляли по каплям с перемешиванием в течение 5 минут 0,95 мл (2,83 ммоль) МеМgI (3,0 М). По окончании введения MeMgI раствор перемешивали 60 минут. Затем удаляли при пониженном давлении Et2O и остаток экстрагировали гексаном (2•30 мл), раствор фильтровали и фильтрат выпаривали досуха при пониженном давлении с получением 0,40 г (выход 73%) красно-оранжевого твердого вещества.
1H (С6D6) δ -0,04 (с, 3Н), 0,45 (с, 3Н), 0,65 (с, 3Н), 0,94 (с, 3Н), 1,35 (м, 2Н), 1,50 (м, 9Н), 1,53 (ш.с, 4Н), 3,14 (м, 2Н), 3,24 (м, 2Н), 5,69 (с, 1Н), 6,88 (т, 1Н, 3Jн.н = 7,5 Гц), 7,06 (т, 1Н, 3Jн.н = 7,6 Гц), 7,5 (д, 1Н, 3Jн.н = 8,5 Гц), 7,64 (д, 1Н, 3Jн.н = 8,6 Гц).
13С{ 1Н} (С6D6) δ 2,40, 4,84, 24,94, 26,58, 34,68, 51,97, 52,41, 55,07, 58,31, 85,16, 108,91, 124,60, 125,02, 126,33, 128,18, 133,24, 146,27.
Пример 7
Получение (N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато(2-)-N)((2,3,4,5-η)-2,4-гексадиен)титана (18)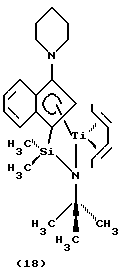
В 35 мл гексана растворяли дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пиперидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титан (0,50 г, 1,12 ммоль). К полученному раствору прибавляли сразу 1,28 мл (11,23 ммоль) 2,4-гексадиена с последующим прибавлением по каплям n-BuMgCl (1,35 мл, 2,69 ммоль). Смесь нагревали с обратным холодильником в течение 1,5 часов и затем удаляли в вакууме растворитель. Черный твердый остаток растворяли в 15 мл гексана, фильтровали и помещали в холодильник (-27oС) на три дня. Затем декантировали растворитель и крупные черные кристаллы промывали 4 мл холодного гексана и высушивали под вакуумом с получением 126 мг (выход 25%) продукта.
1H (С6D6) δ 0,73, (с, 3Н), 0,94 (с, 3Н), 1,09 (с, 9Н), 1,22 (д, 3Н, 3Jн.н = 54 Гц), 1,24 (м, 2Н), 1,37 (м, 4Н), 1,63 (м, 1Н), 1,79 (м, 1Н), 2,11 (д, 3Н, 3Jн.н = 5,4 Гц), 2,51 (м, 2Н), 2,87 (м, 2Н), 3,23 (дд, 1Н, 2Jн.н = 13,5 Гц, 3Jн.н = 9,6 Гц), 4,00 (дд, 1Н, 3Jн.н = 13,2 Гц, 3Jн.н = 9,9 Гц), 5,69 (с, 1Н), 6,69 (т, 1Н, 3Jн.н = 9,6 Гц), 6,83 (д, 1Н, 3Jн.н= 8,4 Гц), 6,94 (т, 1Н, 3Jн.н= 9,9 Гц), 7,88 (д, 2Н, 3Jн.н = 9,6 Гц).
13С{ 1Н} (С6D6) δ 4,11, 6,42, 15,53, 19,75, 24,64, 26,15, 34,98, 52,38, 56,43, 79,37, 80,48, 92,62, 101,21, 110,64, 112,81, 120,76, 121,54, 122,61, 123,40, 128,99, 129,50, 142,55.
Пример 8
Получение 1-(бромметил)-N-(1,1-диметилэтил)-1,1-диметилсиланамина (19)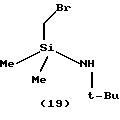
К перемешиваемому раствору 10,00 г (53,32 ммоль) (бромметил)хлордиметилсилана в 200 мл диэтилового эфира прибавляли 7,80 г (106,64 ммоль) трет-бутиламина в 10 мл эфира. Сразу же выпадало в осадок белое твердое вещество. Реакционную смесь перемешивали всю ночь, фильтровали через среднепористую фритту и удаляли при пониженном давлении растворитель с получением 11,06 г бесцветной жидкости. Выход 93%.
1H (С6D6) δ 0,13 (с, 6Н), 0,57 (ш.с, 1Н), 0,99 (с, 9Н), 2,25 (с, 2Н).
13С{1Н} (С6D6) δ -0,47, 19,75, 33,87, 49,51.
Получение N-(трет-бутил)-N-(1,1-диметил-1-((3-тетрагидро-1Н-1-пирролил-1Н-1-инденил)метил)силил)амина (20)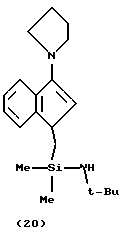
К перемешиваемому раствору 3,500 г (15,61 ммоль) 1-(бромметил)-N-(1,1-диметилэтил)-1,1-диметилсиланамина в 30 мл ТГФ прибавляли в течение 5 минут раствор 2,84 г (14,87 ммоль) литиевой соли 1-(1H-3-инденил)пирролидина в 30 мл ТГФ. Реакционная смесь почти сразу же темнела. Реакционную смесь перемешивали всю ночь и удаляли при пониженном давлении растворитель. Остаток экстрагировали 50 мл гексана и фильтровали. Удалив гексан, получили 4,88 г красного масла. Выход 100%.
1H (С6D6) δ 0,18 (с, 3Н), 0,18 (с, 3Н), 0,48 (с, 1Н), 0,84 (дд, 1Н, 2Jн.н = 14,6 Гц, 3Jн.н = 10,2 Гц), 1,10 (с, 9Н), 1,36 (дд, 1Н, 2Jн.н = 14,6 Гц, 3Jн.н = 4,4 Гц), 1,58 (м, 4Н), 3,26 (м, 4Н), 3,67 (м, 1Н), 5,25 (д, 1Н, 3Jн.н = 2,4 Гц), 7,20 (м, 2Н), 7,38 (д, 1Н, 3Jн.н = 7,1 Гц), 7,55 (д, 1Н, 3Jн.н =6,8 Гц).
13С{ 1Н} (С6D6) δ 2,97, 3,02, 22,72, 25,62, 34,14, 43,34, 49,49, 50,36, 108,05, 120,84, 123,44, 124,99, 126,04, 141,55, 148,68, 152,43.
Получение дилитиевой соли N-(1,1-диметилэтил)-1,1-диметил-1-((3-(1-пирролидинил)-1Н-инден-1-ил)метил)силанамина (21)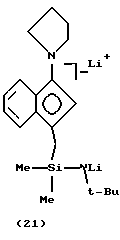
В сухом боксе смешивали 4,88 г (14,86 ммоль) N-(1,1-диметилэтил)-1,1-диметил-1-((3-(1-пирролидинил)-1Н-инден-1-ил)метил)силанамина с 70 мл гексана. К полученному раствору прибавляли в течение 2 минут 23,2 мл (37,2 ммоль) n-BuLi (1,6 М). В течение короткого промежутка времени появлялся желтый осадок. По окончании введения n-BuLi раствор перемешивали всю ночь. Полученный желтый осадок собирали путем фильтрования, промывали 80 мл гексана и высушивали при пониженном давлении с получением 5,05 г (выход 100%) желтого твердого вещества.
Получениедихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7a-η)-3-(1-пирролидинил)-1Н-инден-1-ил)метил)-силанаминато-(2-)-N)титана (22)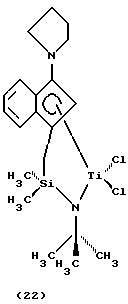
В сухом боксе в 80 мл ТГФ суспендировали 5,50 г (14,85 ммоль) TiCl3 (ТНF)3. К полученному раствору прибавляли в течение 5 минут раствор 5,05 г (14,85 ммоль) дилитиевой соли N-(1,1-диметилэтил)-1,1-диметил-1-((3-(1-пирролидинил)-1Н-инден-1-ил)метил)силанамина в 50 мл ТГФ. Затем раствор перемешивали 1 час. По истечении этого времени прибавляли 2,68 г PbCl2 (9,65 ммоль) и раствор перемешивали 60 минут. Затем удаляли при пониженном давлении ТГФ. Остаток экстрагировали 60 мл толуола, раствор фильтровали и толуол удаляли при пониженном давлении. Затем остаток растирали с 50 мл гексана и осадок собирали путем фильтрования на фритте, промывали 25 мл холодного гексана и высушивали под вакуумом с получением 3,65 г черного твердого вещества. Выход 55%.
1H (С6D6) δ 0,37 (с, 3Н), 0,51 (с, 3Н), 1,46 (с, 9Н), 1,53 (м, 4Н), 2,25 (д, 2Jн.н = 14,5 Гц), 2,49 (д, 2Jн.н = 14,5 Гц), 3,35 (м, 2Н), 3,62 (м, 2Н), 5,63 (с, 1Н), 7,07 (м, 2Н), 7,35 (м, 1Н), 7,56 (м, 1Н).
13С{ 1Н} (С6D6) δ 6,19, 7,08, 18,93, 25,88, 33,46, 50,42, 61,30, 100,59, 119,33, 120,91, 125,09, 126,07, 126,86, 127,42, 146,10.
Пример 9
Получение (N-(1,1-диметилэтил)-1,1-диметил-1-(((1,2,3,3а,7a-η) -3- (1-пирролидинил) -1Н-инден-1-ил) метил) -силанаминато-(2-)-N)диметилтитана (23)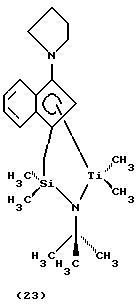
В сухом боксе в 40 мл Et2O растворяли 0,60 г дихлор(N-(1,1-диметилэтил) -1,1-диметил-1- ( ( (1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)метил)силанаминато-(2-)-N)титана (1,35 ммоль). К полученному раствору прибавляли по каплям с перемешиванием в течение 5 минут 0,945 мл (2,83 ммоль) MeMgI (3,0 М). Раствор менял цвет с черного на темно-красный. По окончании прибавления MeMgI раствор перемешивали в течение 1 часа. Затем удаляли при пониженном давлении Et2O и остаток экстрагировали гексаном (2•20 мл), раствор фильтровали и фильтрат выпаривали при пониженном давлении досуха с получением 0,35 г (выход 65%) черного твердого вещества.
1H (С6D6) δ 0,23 (с, 3Н), 0,38 (с, 3Н), 0,40 (с, 3Н), 0,82 (с, 3Н), 1,54 (м, 6Н), 1,60 (с, 9Н), 1,99 (д, 2Jн.н = 14,5 Гц), 2,22 (д, 2Jн.н = 14,5 Гц), 3,33 (м, 4Н), 5,32 (с, 1Н), 6,91 (м, 2Н), 7,22 (м, 1Н), 7,64 (м, 1Н).
13С{ 1Н} (С6D6) δ 6,55, 7,23, 17,21, 25,92, 35,21, 50,27, 51,89, 57,02, 58,18, 99,09, 108,85, 116,05, 122,14, 122,92, 123,66, 124,48, 125,53, 138,31.
Пример 10
Получение 1-(2-метил-1Н-3-инденил)пирролидина (24)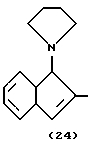
В 250 мл безводного бензола растворяли 2-метил-1-инденон (25 г, 171 ммоль). К полученному раствору прибавляли 50 мл пирролидина. Реакционную смесь нагревали с обратным холодильником с использованием ловушки Дина-Старка, заполненной молекулярными ситами 4 ангстрема, в течение 10 дней. ГХ-анализ показал, что степень превращения составляла около 70%. Отгоняли растворитель и остаток перегоняли при пониженном давлении (1,5 мм рт. столба). Первую фракцию получали при 84oС, а целевое соединение собирали при 126-132oС. Выход желтой жидкости составлял 16,28 г (48%).
1H (С6D6) δ 1,66 (м, 4Н), 2,02 (с, 3Н), 3,02 (с, 2Н), 3,29 (м, 4Н), 7,11 (т, 1Н, 3Jн.н = 7,0 Гц), 7,23 (м, 2Н), 7,45 (д, 2Jн.н = 7,7 Гц).
13С{ 1Н} (С6D6) δ 14,68, 25,61, 41,89, 50,92, 119,94, 123,68, 123,86, 124,10, 126,029, 142,61, 143,50, 145,00.
Получение (2-метил-1-(1-пирролидинил)-1H-инденил)лития (25)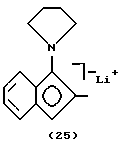
К перемешиваемому (1-(2-метил-1Н-3-инденил)пирролидину (16,276 г, 81,67 ммоль) в гексане (250 мл) прибавляли по каплям n-BuLi (98,0 ммоль, 49,0 мл 2,0 М раствора в циклогексане). Смеси давали перемешиваться всю ночь, в течение которой образовался осадок. По истечении времени реакции смесь фильтровали. Полученный целевой продукт в виде бледно-желтого твердого вещества промывали гексаном и высушивали под вакуумом, после чего использовали без дальнейшей очистки или анализа (14,51 г, выход 87%).
Получение N-(1,1-диметилэтил)-1,1-диметил-1-(2-метил)-3-(1-пирролидинил)-1Н-инден-1-ил)силанамина (26)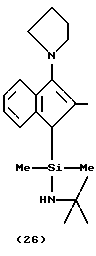
К раствору N-(1,1-диметилэтил)-1-хлор-1,1-диметилсиланамина (4,27 г, 25,75 ммоль) в 100 мл ТГФ прибавляли в течение 3 минут раствор (2-метил-1-(1-пирролидинил)-lH-инденил)лития (3,52 г, 17,17 ммоль) в 50 мл ТГФ. Цвет раствора становился желто-оранжевым. Реакционную смесь перемешивали всю ночь и затем удаляли при пониженном давлении растворитель. Продукт экстрагировали 80 мл гексана и фильтровали. Удаляли при пониженном давлении гексан и колбу присоединяли к линии высокого вакуума (10-4 мм рт. столба) на всю ночь, чтобы удалить избыточный исходный материал. Выход продукта составлял 5,54 г (98%).
1H (С6D6) δ -0,00 (с, 3Н), 0,09 (с, 3Н), 0,40 (с, 1Н), 1,04 (с, 9Н), 1,77 (м, 4Н), 2,21 (с, 3Н), 3,14 (с, 1Н), 3,25 (м, 2Н), 3,39 (м, 2Н), 7,15 (т, 1Н, 3Jн.н = 7,3 Гц), 7,23 (т, 1Н, 3Jн.н = 7,4 Гц), 7,48 (д, 1Н, 3Jн.н = 7,2 Гц), 7,50 (д, 1Н, 3Jн.н = 7,1 Гц).
13С{ 1Н} (С6D6) δ 0,17, 1,07, 15,63, 26,00, 33,81, 48,59, 50,00, 51,23, 119,52, 122,63, 123,86, 124,55, 133,96, 142,73, 143,12, 144,16.
Получение (1-(((1,1-диметилэтил)амино)диметилсилил)метил)-2-метил-3-(1-пирролидинил)-1H-инденил)лития, литиевая соль (27)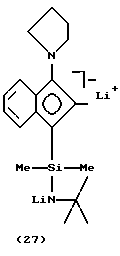
В сухом боксе в 100 мл гексана растворяли 5,54 г (16,36 ммоль) N-(1,1-диметилэтил)-1,1-диметил-1-(2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанамина. К полученному раствору прибавляли по каплям 16,0 мл (39,8 ммоль) n-BuLi (1,6 М). По окончании прибавления n-BuLi раствор перемешивали всю ночь. Полученный осадок собирали путем фильтрования, промывали 100 мл гексана и сушили при пониженном давлении с получением 4,51 г желтого твердого вещества. Выход 83%.
Получение дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η) -2-метил-3- (1-пирролидинил)-1Н-инден-1-ил)силамаминато(2-)-N)титана (28)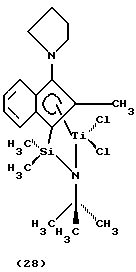
В сухом боксе в 80 мл ТГФ суспендировали 4,91 г (13,24 ммоль) ТiСl3(ТНF)3. К полученному раствору прибавляли в течение 5 минут раствор 4,91 г (13,24 ммоль) (1-(((1,1-диметилэтил) амино)диметилсилил)метил)-2-метил-3-(1-пирролидинил)-1H-инденил)лития, литиевая соль, в 30 мл ТГФ. Затем раствор перемешивали 55 минут. По истечении этого времени прибавляли 2,39 г PbCl2 (8,60 ммоль) и раствор перемешивали в течение 55 минут. Затем удаляли при пониженном давлении ТГФ. Остаток экстрагировали 70 мл толуола, раствор фильтровали и удаляли при пониженном давлении толуол. Остаток растирали с 40 мл гексана и осадок собирали путем фильтрования, промывали 40 мл гексана и высушивали под вакуумом с получением 3,38 г темно-серого твердого вещества. Выход 56%.
1H (C6D6) δ 0,62 (с, 3Н), 0,66 (с, 3Н), 1,38 (с, 9Н), 1,41 (м, 4Н), 2,50 (с, 3Н), 3,46 (м, 2Н), 3,83 (м, 2Н), 6,98 (т, 1Н, 3Jн.н = 7,6 Гц), 7,10 (т, 1Н, 3Jн.н = 7,5 Гц), 7,65 (т, 1Н, 3Jн.н = 8,6 Гц), 7,70 (т, 1Н, 3Jн.н = 8,8 Гц).
13С{ 1Н} (С6D6) δ 6,39, 6,49, 18,95, 25,99, 32,90, 52,36, 60,75, 94,47, 123,90, 126,95, 136,00, 147,75.
Пример 11
Получение(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а,7a-η)-2-метил-3-(1-пирролидинил) -1Н-инден-1-ил)силанаминато(2-)-N)диметилтитана (29)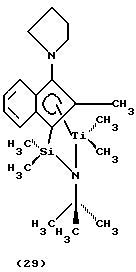
В сухом боксе в 40 мл Et2O растворяли 0,65 г (1,42 ммоль) дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-2-метил-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато-(2-)-N)-титана. К полученному раствору прибавляли по каплям с перемешиванием в течение 5 минут 1,00 мл (2,98 ммоль) МеМgI (3,0 М). Раствор менял цвет с черного на очень темно-красный. По окончании прибавления МеМgI раствор перемешивали в течение 1 часа. Затем удаляли при пониженном давлении Et2O и остаток экстрагировали гексаном (2•20 мл), раствор фильтровали и фильтрат выпаривали при пониженном давлении досуха с получением 0,45 г (выход 78%) красно-коричневого липкого остатка.
1H (С6D6) δ -0,03 (с, 3Н), 0,54 (с, 3Н), 0,64 (с, 3Н), 0,86 (с, 3Н), 1,50 (с, 9Н), 1,62 (м, 4Н), 2,15 (с, 3Н), 3,22 (м, 2Н), 3,58 (м, 2Н), 6,86 (т, 1Н, 3Jн.н = 7,6 Гц), 7,06 (т, 1Н, 3Jн.н = 7,5 Гц), 7,55 (д, 1Н, 3Jн.н = 8,8 Гц), 7,70 (д, 1Н, 3Jн.н =8,6 Гц).
13С{ 1Н} (С6D6) δ 6,35, 6,99, 16,41, 26,14, 34,47, 52,12, 52,58, 54,81, 57,92, 85,58, 124,36, 124,43, 125,04, 126,83, 127,86, 129,68, 132,79, 141,06.
Пример 12
Получение 1-хлор-N-циклогексил-1,1-диметилсиланамина (30)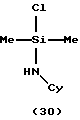
В сухом боксе в колбе емкостью 250 мл перемешивали 60,0 мл (490,89 ммоль) дихлордиметилсилана в примерно 80 мл ТГФ. К этому перемешиваемому раствору медленно прибавляли 6,00 г (57,08 ммоль) циклогексиламида лития в виде твердого вещества и раствор перемешивали всю ночь. После удаления под вакуумом ТГФ остался мутный раствор. К этому раствору прибавляли гексан и твердые вещества отфильтровывали и промывали гексаном. Затем из фильтрата удаляли под вакуумом гексан, получив в результате 9,18 г (выход 84%) прозрачного светло-желтого продукта.
1H (С6D6) δ 0,28 (с, 6Н), 0,82-1,20 (м, 6Н), 1,37-1,50 (м, 1Н), 1,50-1,60 (м, 2Н), 1,81 (д, 2Н, 3Jн.н = 10,0 Гц), 2, 64 (м, 1Н).
13С{1Н} (С6D6) δ 2,27, 25,65, 25,89, 38,04, 50,67.
Получение N-циклогексил-1,1-диметил-1-(3-(1-пирролидинил)-1Н-инден-1-ил)силанамина (31)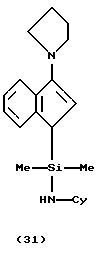
К раствору 1-хлор-N-циклогексил-1,1-диметилсиланамина (3,61 г, 18,83 ммоль) в 150 мл ТГФ прибавляли в течение 3 минут раствор 1-(lH-3-инденил)пирролидин, литиевая соль (3,00 г, 15,69 ммоль) в 50 мл ТГФ. Цвет раствора сразу становился темно-вишнево-красным. Реакционную смесь перемешивали всю ночь и затем удаляли при пониженном давлении растворитель. Продукт экстрагировали 60 мл гексана и фильтровали. Удаляли при пониженном давлении гексан и колбу присоединяли к линии высокого вакуума (10-4 мм рт. столба) на 4 часа, чтобы удалить избыточный исходный материал. Получили 5,23 г продукта. Выход 98%.
1H (С6D6) δ -0,01 (с, 3Н), 0,078 (с, 3Н), 0,36 (с, 1Н), 0,80-1,30 (м, 7Н), 1,41-1,92 (м, 8Н), 2,52 (м, 1Н), 3,27 (м, 4Н), 3,396 (с, 1Н), 5,384 (с, 1Н), 7,252 (м, 2Н), 7,586 (д, 1Н, 3Jн.н =7,1 Гц), 7,717 (д, 1Н, 3Jн.н = 7,4 Гц).
13С{1Н} (С6D6) δ -2,539, -1,771, 25,286, 26,021, 26,115, 39,071, 43,603, 50,682, 51,067, 104,480, 120,944, 123,736, 123,797, 124,557, 141,484, 146,923, 149,284.
Получение (1-((циклогексиламино)диметилсилил)-3-(1-пирролидинил)-1H-инденил)лития, литиевая соль (32)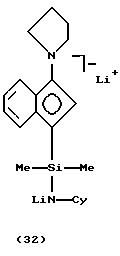
В сухом боксе растворяли в 100 мл гексана 5,23 г (15,36 ммоль) N-циклогексил-1,1-диметил-1-(3-(1-пирролидинил)-1Н-инден-1-ил)силанамина. К полученному раствору прибавляли по каплям 24 мл (39,39 ммоль) n-BuLi (1,6 М). По окончании прибавления n-BuLi раствор перемешивали всю ночь. Полученный осадок собирали путем фильтрования, промывали 100 мл гексана и высушивали при пониженном давлении с получением 5,11 г желтого твердого вещества. Выход 94%.
Получение дихлор(N-циклогексил-1,1-диметил-1-((1,2,3, 3а, 7а-η) -3- (1-пирролидинил) -1Н-инден-1-ил) силанаминато (2-) -N) титана (33)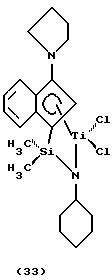
В сухом боксе в 80 мл ТГФ суспендировали 4,21 г (11,35 ммоль) TiCl3 (ТНF)3. К полученному раствору прибавляли в течение 5 минут 4,00 г (11,35 ммоль) раствор (1-((циклогексил-амино)диметилсилил)-3-(1-пирролидинил)-1H-инденил)лития, литиевая соль, в 25 мл ТГФ. Затем раствор перемешивали 45 минут. По истечении этого времени прибавляли 2,05 г PbCl2 (7,38 ммоль) и перемешивали раствор в течение 40 минут. Затем удаляли при пониженном давлении ТГФ. Остаток экстрагировали 70 мл толуола, раствор фильтровали и толуол удаляли при пониженном давлении. Остаток растирали с 30 мл гексана и осадок собирали путем фильтрования, промывали 30 мл гексана и высушивали под вакуумом с получением 3,79 г твердого вещества насыщенного фиолетово-черного цвета. Выход 73%.
1H (C6D6) δ 0,53 (с, 3Н), 0,62 (с, 3Н), 0,93 (м, 3Н), 1,18 (м, 2Н), 1,39-1,69 (м, 7Н), 2,01 (д, 1Н, 3Jн.н = 12 Гц), 2,19 (д, 1Н, 3Jн.н = 12 Гц), 3,21 (м, 2Н), 3,54 (м, 2Н), 4,601 (м, 1Н), 5,64 (с, 1Н), 7,02 (т, 1Н, 3Jн.н = 6,9 Гц), 7,08 (т, 1Н, 3Jн.н = 6,6 Гц), 7,60 (д, 1Н, 3Jн.н = 8,3 Гц), 7,65 (т, 1Н, 3Jн.н = 8,5 Гц).
13С{ 1Н} (С6D6) δ 1,11, 3,10, 25,67, 26,04, 26,38, 35,90, 50,49, 63,91, 89,43, 106,75, 125,48, 126,40, 126,92, 127,13, 128,67, 136,14, 147,71.
Пример 13
Получение (N-циклогексил-1, 1-диметил-1- ( (1, 2, 3, 3а, 7а-η) -3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитана (34)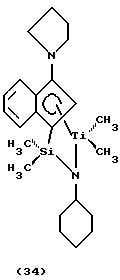
В сухом боксе в 40 мл Et2O растворяли 0,70 г дихлор(N-циклогексил-1,1-диметил-1- ( (1,2,3, 3а, 7а-η)-3- (1-пирролидинил)-1Н-инден-1-ил) силанаминато (2-)-N) титана (1,53 ммоль). К полученному раствору прибавляли по каплям с перемешиванием в течение 5 минут 1,07 мл (3,21 ммоль) МеМgI (3,0 М). Раствор менял цвет с черного на темно-красный. По окончании прибавления МеМgI раствор перемешивали в течение 1 часа. Затем удаляли при пониженном давлении Et2O и остаток экстрагировали гексаном (2•20 мл), раствор фильтровали и фильтрат выпаривали при пониженном давлении досуха с получением 0,50 г (выход 79%) красного кристаллического твердого вещества.
1H (С6D6) δ 0,04 (с, 3Н), 0,47 (с, 3Н), 0,63 (с, 3Н), 0,72 (с, 3Н), 1,10 (м, 1Н), 1,32 (м, 5Н), 1,54 (м, 5Н), 1,73 (м, 2Н), 2,04 (д, 1Н, 3Jн.н =6,0 Гц), 2,14 (д, 1Н, 3Jн.н=6,0 Гц), 3,26 (м, 2Н), 3,40 (м, 2Н), 4,37 (м, 1Н), 5,45 (с, 1Н), 6,88 (т, 1Н, 3Jн.н= 7,6 Гц), 7,02 (т, 1Н, 3Jн.н= 7,6 Гц), 7,50 (д, 1Н, 3Jн.н = 8,6 Гц), 7,78 (д, 1Н, 3Jн.н = 8,7 Гц).
13С{ 1Н} (С6D6) δ 1,68, 3,70, 25,84, 26,27, 26,82, 38,54, 38,69, 47,97, 50,64, 53,41, 61,15, 81,51, 104,79, 123,69, 124,98, 125, 127,87, 134,16, 142,79.
Пример 14
Получение (3-метокси-1Н-инденил)лития (35)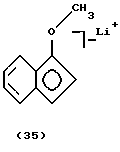
В 150 мл гексана растворяли 3-метокси-1Н-инден (9,65 г, 66,04 ммоль). К полученному раствору прибавляли в течение 10 минут 50 мл (80 ммоль) 1,6 М раствора n-BuLi. Через 20 часов перемешивания не совсем белое твердое вещество собирали на среднепористой фритте, промывали гексаном (3•30 мл) и высушивали при пониженном давлении с получением 9,72 г продукта. Выход 97%.
Получение N-(1,1-диметилэтил)-1-(3-метокси-1Н-инден-1-ил)-1,1-диметилсиланамина (36)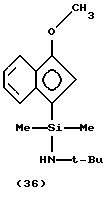
К раствору N-(трет-бутил)-N-(1-хлор-1,1-диметилсилил)-амина (3,27 г, 19,72 ммоль) в 100 мл ТГФ прибавляли в течение 30 минут раствор (3-метокси-1Н-инденил)лития (3,00 г, 19,72 ммоль) в 40 мл ТГФ. По окончании прибавления реакционную смесь перемешивали всю ночь. Затем удаляли при пониженном давлении растворитель. Остаток экстрагировали гексаном и раствор фильтровали. Затем удаляли при пониженном давлении растворитель с получением 5,20 г продукта. Выход 96%.
1H (С6D6) δ -0,08 (с, 3Н), 0,15 (с, 3Н), 1,07 (с, 9Н), 3,28 (с, 1Н), 5,35 (с, 1Н), 7,22 (м, 2Н), 7,52 (д, 1Н, 3Jн.н =7,9 Гц), 7,75 (д, 1Н, 3Jн.н =7,9 Гц).
13С{ 1Н} (С6D6) δ -0,56, 0,45, 34,08, 42,26, 49,64, 56,41, 100,90, 118,68, 123,62, 124,94, 125,13, 139,24, 144,80, 158,03.
Получение (1-(((1,1-диметилэтил)амино)диметилсилил)-3-метокси-1Н-инденил)лития, литиевая соль (37)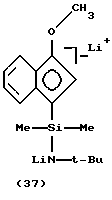
В сухом боксе смешивали 5,20 г (18,87 ммоль) N-(1,1-диметилэтил) -1-(3-метокси-1Н-инден-1-ил)-1,1-диметилсиланамина с 80 мл гексана. К полученному раствору прибавляли по каплям 23,6 мл (37,75 ммоль) n-BuLi (1,6 М). По окончании прибавления n-BuLi раствор перемешивали всю ночь. Полученный осадок собирали путем фильтрования, промывали 50 мл гексана и высушивали при пониженном давлении с получением 5,00 г продукта. Выход 92%.
Получениедихлор(N-(1,1-диметилэтил)-1-((1,2,3,3а,7а-η)-3-метокси-1Н-инден-1-ил)-1,1-диметилсиланаминато(2-)-N)-титана (38)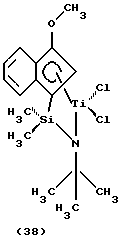
В 30 мл ТГФ растворяли (1-(((1,1-диметилэтил)амино)диметилсилил)-3-метокси-1Н-инденил)литий, литиевая соль (5,00 г, 17,40 ммоль). К полученному раствору прибавляли ТiСl3 (ТНF)3 (6,44 г, 17,40 ммоль) в виде твердого вещества. Через 1 час прибавляли PbCl2 (2,42 г, 8,70 ммоль) в виде твердого вещества. Затем реакционную смесь перемешивали еще час. Удаляли при пониженном давлении растворитель. Остаток экстрагировали 70 мл толуола и фильтровали. Удаляли при пониженном давлении толуол и остаток растирали с гексаном. Твердое вещество собирали путем фильтрования, промывали гексаном и сушили при пониженном давлении с получением 3,92 г продукта. Выход 57%.
1H (C6D6) δ 0,41 (с, 3Н), 0,58 (с, 3Н), 1,33 (с, 9Н), 3,71 (с, 3Н), 5,70 (с, 1Н), 7,00 (м, 2Н), 7,45 (д, 1Н, 3Jн.н =8,3 Гц), 7,60 (д, 1Н, 3Jн.н =8,3 Гц).
Пример 15
Получение (N- (1,1-диметилэтил) -1-( (1,2,3,3а, 7а-η) -3-метокси-1Н-инден-1-ил)-1,1-диметилсиланаминато(2-)-N)диметилтитана (39)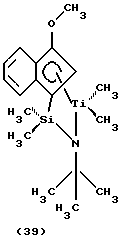
В 40 мл Et2O суспендировали 0,60 г дихлор(N-(1,1-диметилэтил) -1-( (1,2,3, 3а, 7а-η) -3-метокси-1Н-инден-1-ил) -1,1-диметилсиланаминато(2-)-N)титана (1,52 ммоль). К полученной суспензии прибавляли по каплям с перемешиванием в течение 20 минут 1,07 мл МеМgI (3,0 М). По окончании прибавления МеМgI раствор перемешивали в течение 40 минут. По истечении этого времени удаляли при пониженном давлении Et2O и остаток экстрагировали гексаном, раствор фильтровали и фильтрат выпаривали при пониженном давлении досуха с получением 0,46 г продукта. Выход 86%.
1Н (С6D6) δ -0,24 (с, 3Н), 0,41 (с, 3Н), 0,58 (с, 3Н), 0,83 (с, 3Н), 1,47 (с, 9Н), 3,54 (с, 3Н), 3,23 (м, 4Н), 5,46 (с, 1Н), 6,95 (м, 1Н), 7,06 (т, 1Н), 7,48 (д, 1Н, 3Jн.н = 8,5 Гц), 7,78 (д, 1Н, 3Jн.н =8,5 Гц).
Пример 16
Получение (1Н-инден-1-ил)дифенилфосфина (40)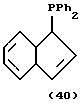
В сухом боксе к 180 мл эфирного раствора дифенилхлорфосфина (14,46 г, 65,52 ммоль) (дифенилхлорфосфин растворяли перед использованием (97oС @ 0,4 мм рт. столба)) прибавляли в течение 15 минут раствор инденида лития (8,00 г, 65,52 ммоль) в 50 мл ТГФ. После перемешивания в течение ночи отделяли путем фильтрования LiCl, получив в результате желтый раствор. Удаляли при пониженном давлении растворитель с получением не совсем белого твердого вещества. Это твердое вещество растирали с 40 мл гексана. Удаляли путем декантации гексан и твердое вещество высушивали при пониженном давлении с получением 16,43 г не совсем белого твердого вещества. Выход 84%.
Получение (1-(дифенилфосфино)-1H-инденил)лития (41)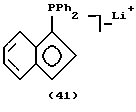
В смеси 60 мл эфира и 60 мл гексана растворяли (1Н-инден-1-ил)дифенилфосфин (5,00 г, 16,65 ммоль). К смеси прибавляли в течение 10 минут n-BuLi (7,35 мл, 18,31 ммоль). После перемешивания в течение ночи осадок не появлялся. Удаляли при пониженном давлении растворитель, получив в результате воскообразный желтый остаток. Этот остаток растирали с 120 мл гексана в течение 15 минут. Гексановый раствор сливали и остаток сушили при пониженном давлении с получением 4,45 г не совсем белого твердого вещества. Выход 87%.
Получение N-(1,1-диметилэтил)-1-(3-(дифенилфосфино)-1Н-инден-1-ил)-1,1-диметилсиланамина (42)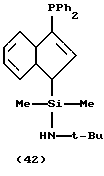
К раствору N-(трет-бутил)-N-(1-хлор-1,1-диметилсилил)-амина (3,37 г, 20,34 ммоль) в 100 мл ТГФ прибавляли в течение 15 минут (1-(дифенилфосфино)-1H-инденил)литий (4,45 г, 14,53 ммоль), растворенный в 40 мл ТГФ. После перемешивания в течение ночи получили красный раствор. Удаляли при пониженном давлении растворитель с получением красного масла. Остаток экстрагировали 35 мл гексана и фильтровали. Удалив гексан, получили 6,12 г красного масла. Выход 98%.
1H ЯМР (С6D6) δ -0,10 (с, 3Н), -0,07 (с, 3Н), 0,42 (с, 1Н), 1,01 (с, 9Н), 3,59 (м, 1Н), 6,56 (м, 1Н), 7,0-7,2 (м, 8), 7,54-7,66 (м, 6Н).
13Р{1Н} ЯМР (С6D6) δ -24,08.
Получение (1-(((1,1-диметилэтил)амино)диметилсилил)-3-(дифенилфосфино)-1H-инденил)лития, литиевая соль (43)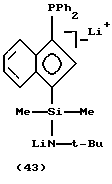
N-(1,1-диметилэтил)-1-(3-(дифенилфосфино)-1Н-инден-1-ил)-1,1-диметилсиланамин (6,73 г, 15,67 ммоль) перемешивали в гексане (100 мл), прибавляя по каплям n-BuLi. Полученной смеси давали перемешиваться всю ночь, в течение которой образовался не совсем белый осадок. По истечении времени реакции смесь фильтровали. В результате получили целевой продукт в виде не совсем белого твердого вещества, которое промывали гексаном и сушили под вакуумом, после чего использовали без дальнейшей очистки или анализа (6,04 г, выход 87%).
Получение дихлор (N- (1,1-диметилэтил) -1- ( (1,2,3, 3а, 7a-η) -3-(дифенилфосфино)-1Н-инден-1-ил)-1,1-диметилсиланаминато-(2-)-N)титана (44)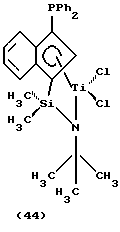
К суспензии ТiСl3 (ТНF)3 (2,52 г, 6,80 ммоль) в ТГФ (50 мл) прибавляли по каплям (1-(((1,1-диметилэтил)амино)диметилсилил)-3-(дифенилфосфино)-1H-инденил)литий, литиевая соль (3,00 г, 6,80 ммоль) в ТГФ (25 мл). Полученной смеси давали перемешиваться в течение 1 часа. Затем прибавляли PbCl2 (0,94 г, 3,40 ммоль) в виде твердого вещества и смеси давали перемешиваться еще час. По истечении времени реакции удаляли летучие вещества и остаток экстрагировали толуолом и фильтровали. Удаление толуола дало темно-красный маслянистый остаток. Этот остаток растворяли в смеси гексан-толуол (3/1 объем/объем) и вновь фильтровали. Повторяли эту процедуру, получив в результате гомогенный раствор, который охлаждали (-15oС) всю ночь, что привело к выпадению в осадок маслянистого остатка, который извлекали путем декантации раствора и сушки под вакуумом (3,13 г, выход 84%).
1H ЯМР (С6D6) δ 0,18, (с, 3Н), 0,54 (с, 3Н), 1,28 (с, 9Н), 6,48 (с, 1Н), 6,8-7,8 (м, 14Н).
31Р{1Н} ЯМР (С6D6) δ -17,49.
Пример 17
Получение(N-(1,1-диметилэтил)-1-((1,2,3,3а,7a-η)-3-(дифенилфосфино)-1Н-инден-1-ил)-1,1-диметилсиланаминато(2-)-N)диметилтитана (45)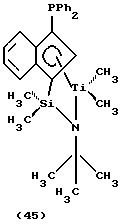
Дихлор(N-(1,1-диметилэтил)-1-((1,2,3,3а, 7a-η)-3-(дифенилфосфино)-1Н-инден-1-ил)-1,1-диметилсиланаминато(2-)-N)-титан (0,36 г, 0,660 ммоль) перемешивали в диэтиловом эфире (50 мл), прибавляя по каплям МеМgВr (1,46 ммоль, 0,49 мл 3,0 М раствора в диэтиловом эфире). Полученной смеси давали перемешиваться в течение 1 часа. По истечении времени реакции удаляли летучие вещества и остаток экстрагировали смесью гексан-толуол (1/1 об/об) и фильтровали. Затем удаляли под вакуумом летучие вещества, и остаток опять растворяли в гексане и фильтровали. Удаление гексана дало целевой продукт в виде темно-красного масла (0,18 г, выход 53%).
1H ЯМР (С6D6) δ -0,00 (с, 3Н), 0,23 (с, 3Н), 0,57 (с, 3Н), 1,18 (с, 3Н), 1,39 (с, 3Н), 6,17 (с, 1Н), 6,8-7,8 (м, 14Н).
Пример 18
Получение 1-(1H-инден-3-ил)пирролидина (46)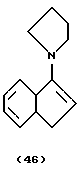
В соответствии с модификацией метода Ноланда и др. (Noland, W.E.; Kaneswaran, V, J. Org. Chem. 1981, 46, 1940-1944) в 3-горлую колбу емкостью 500 мл, снабженную навесной мешалкой, аппаратом Дина-Старка и холодильником под средой сухого N2, загружали 1-инданон (25,0 г, 0,189 моль) и 50 мл пирролидина, который уже был высушен над молекулярными ситами  Прибавляли бензол (200 мл, высушен над ситами
Прибавляли бензол (200 мл, высушен над ситами  ) и полученный раствор нагревали с обратным холодильником в течение 30 часов. По окончании этого периода 1H ЯМР-анализ аликвоты реакционной смеси показал отношение в мольных процентах целевого продукта к исходному материалу 93:7. Основную массу растворителя удаляли в вакууме и неочищенный темный продукт подвергали перегонке (6"-ая (152,4 мм) колонка Vigreaux) с получением чистого енамина в виде светло-желтого масла (24,3 г, 0,132 моль) с выходом 70%. Это соединение чувствительно и к воздуху, и к воде и потому было перенесено после перегонки в сухой бокс. Анализ путем капиллярной ГХ показал, что гексановый раствор дистиллята имеет чистоту 99% (по площади): т. к. = 125-127oС @ 2,0 мм, т. к. лит. = 118-120oС @ 1 мм.
) и полученный раствор нагревали с обратным холодильником в течение 30 часов. По окончании этого периода 1H ЯМР-анализ аликвоты реакционной смеси показал отношение в мольных процентах целевого продукта к исходному материалу 93:7. Основную массу растворителя удаляли в вакууме и неочищенный темный продукт подвергали перегонке (6"-ая (152,4 мм) колонка Vigreaux) с получением чистого енамина в виде светло-желтого масла (24,3 г, 0,132 моль) с выходом 70%. Это соединение чувствительно и к воздуху, и к воде и потому было перенесено после перегонки в сухой бокс. Анализ путем капиллярной ГХ показал, что гексановый раствор дистиллята имеет чистоту 99% (по площади): т. к. = 125-127oС @ 2,0 мм, т. к. лит. = 118-120oС @ 1 мм.
1H (С6D6) δ 7,61 (д, 1H, J = 7,4 Гц), 7,39 (д, 1Н, J = 7,4 Гц), 7,24 (т, 1H, J = 7,4 Гц), 7,17 (т, 1H, J = 7,4 Гц), 5,07 (с, 1H), 3,41 (м, 4Н), 3,31 (с, 2Н), 1,94 (м, 4).
13С{1Н} (С6D6) δ 149,9, 145,1, 141,6, 125,5, 124,2, 123,8, 120,3, 100,6, 50,2, 35,5, 25,2.
Получение (1-(1-пирролидинил)-1H-инденил)лития (47)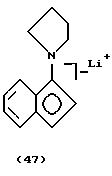
В сухом боксе смешивали 3,5 г (18,9 ммоль) 1-(1Н-инден-3-ил)пирролидина с 100 мл гексана. К полученному раствору прибавляли по каплям 9,5 мл (18,9 ммоль) n-BuLi (2,0 М). По окончании прибавления n-BuLi раствор перемешивали всю ночь. Полученный осадок собирали путем фильтрования, промывали гексаном и сушили при пониженном давлении с получением 3,61 г продукта. Выход 99%.
Получение N-(1,1-диметилэтил)-1,1-диметил-1-(3-(1-пирролидинил)-1Н-инден-1-ил)силанамина (48)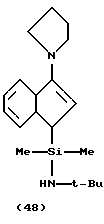
К раствору N-(трет-бутил)-N-(1-хлор-1,1-диметилсилил)-амина (2,86 г, 17,25 ммоль) в 100 мл ТГФ прибавляли в течение 30 минут раствор (1-(1-пирролидинил)-1H-инденил)лития (3,30 г, 17,25 ммоль) в 40 мл ТГФ. По окончании прибавления реакционную смесь перемешивали всю ночь. Затем удаляли при пониженном давлении растворитель. Остаток экстрагировали гексаном и раствор фильтровали. Затем удаляли при пониженном давлении растворитель с получением 5,13 г продукта. Выход 95%.
1H (С6D6) δ 0,07 (с, 3Н), 0,05 (с, 3Н), 1,27 (с, 9Н), 2,03 (м, 4Н), 3,43 (м, 4Н), 5,41 (с, 1Н), 7,24 (м, 2Н), 7,53 (д, 1Н, 3Jн.н = 7,7 Гц), 7,70 (д, 1Н, 3Jн.н = 7,7 Гц).
13С{ 1Н} (С6D6) δ 2,71, 4,28, 26,19, 34,93, 49,06, 50,68, 54,30, 58,00, 84,15, 104,16, 123,91, 124,50, 125,05, 133,58, 143,95.
Получение (1-(((1,1-диметилэтил)амино)диметилсилил)-3-1-пирролидинил)-1H-инденил)лития, литиевая соль (49)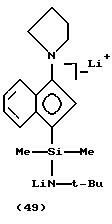
В сухом боксе смешивали 5,13 г (16,3 ммоль) N-(1-(1,1-диметилэтил)-1,1-диметил-1-(3-(1-пирролидинил)-1Н-инден-1-ил)-силанамина с 80 мл гексана. К полученному раствору прибавляли по каплям 16,3 мл (32,6 ммоль) n-BuLi (2,0 М). По окончании прибавления n-BuLi раствор перемешивали всю ночь. Полученный осадок собирали путем фильтрования, промывали 50 мл гексана и высушивали при пониженном давлении с получением 5,33 г продукта. Выход 100%.
Получение дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1, 2,3,3a,7a-η)-3-( 1-пирролидинил) -1Н-инден-1-ил) силанаминато-(2-)-N)титана (50)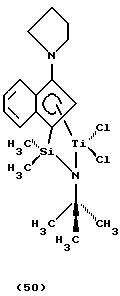
В 30 мл ТГФ суспендировали ТiСl3 (ТНF)3 (6,05 г, 16,32 ммоль). К полученному раствору прибавляли (1-(((1,1-диметилэтил) амино)диметилсилил)-3-(1-пирролидинил)-lH-инденил)литий, литиевая соль (5,33 г, 16,32 ммоль) в виде твердого вещества. Через 1 час прибавляли PbCl2 (2,27 г, 8,16 ммоль) в виде твердого вещества. Затем реакционную смесь перемешивали еще час. Удаляли при пониженном давлении растворитель. Остаток экстрагировали 70 мл толуола и фильтровали. Удаляли при пониженном давлении толуол и остаток растирали с гексаном. Твердое вещество собирали путем фильтрования, промывали гексаном и сушили при пониженном давлении с получением 5,08 г продукта. Выход 72%.
1H (С6D6) δ 0,67 (с, 3Н), 0,84 (с, 3Н), 1,316 (с, 9Н), 2,05 (ш.с, 4Н), 3,71 (ш.с, 2Н), 4,01 (ш.с, 2Н), 7,25 (м, 2Н), 7,63 (д, 1Н), 7,91 (д, 1Н).
13С{ 1Н} (С6D6) δ 1,58, 25,75, 32,97, 50,49, 61,05, 93,11, 106,51, 126,32, 126,89, 127,14, 129,00, 135,82, 149,54.
MCBP (EI, M+): вычислено 430,0881, найдено 430,0881.
Пример 19
Получение (N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7a-η) -3- (1-пирролидинил) -1Н-инден-1-ил) силанаминато (2-)-N)-диметилтитана (51)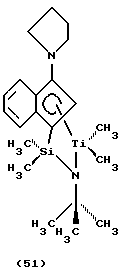
В 40 мл Et2O суспендировали 0,50 г дихлор(N-(1,1-диметилэтил) -1,1-диметил-1- ( (1,2,3, 3а, 7а-η) -3- (1-пирролидинил)-1Н-инден-1-ил) силанаминато (2-)-N) титана (1,15 ммоль). К полученной суспензии прибавляли по каплям с перемешиванием в течение 20 минут 0,77 мл МеМgI (3,0 M). По окончании прибавления МеМgI раствор перемешивали в течение 40 минут. По истечении этого времени удаляли при пониженном давлении Et2O и остаток экстрагировали гексаном, раствор фильтровали и фильтрат выпаривали при пониженном давлении досуха с получением 0,39 г продукта. Выход 86%.
1H (С6D6) δ 0,10 (с, 3Н), 0,50 (с, 3Н), 0,65 (с, 3Н), 0,75 (с, 3Н), 1,53 (с, 9Н), 3,23 (м, 4Н), 3,23 (м, 4Н), 5,43 (с, 1Н), 6,95 (т, 1Н, 3Jн.н = 7,9 Гц), 7,06 (т, 1Н, 3Jн.н = 7,9 Гц), 7,54 (д, 1Н, 3Jн.н = 8,5 Гц), 7,63 (д, 1Н, 3Jн.н= 8,5 Гц).
13С{ 1Н} (С6D6) δ 2,62, 2,71, 4,82, 4,90, 26,19, 34,90, 49,06, 50,58, 54,31, 58,00, 84,15, 104,15, 123,91, 124,49, 125,05, 125,63, 133,58, 143,95.
Пример 20
Получение (N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7a-η) -3- (1-пирролидинил) -1Н-инден-1-ил) силанаминато (2-) -N) -( (2,3,4,5-η)-2, 4-гексадиен) титана (52)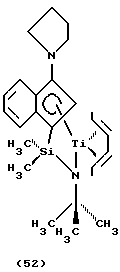
В сухом боксе смешивали 0,40 г дихлор(N-(1,1-диметилэтил) -1,1-диметил-1- ( (1,2,3, 3а, 7a-η) -3- ( 1-пирролидинил) -1Н-инден-1-ил)силанаминато(2-)-N)титана с 0,76 г 2,4-гексадиена и суспендировали в 50 мл гексана. К полученному раствору прибавляли 1,15 мл n-BuLi (1,6 М) и раствор нагревали с обратным холодильником в течение 2 часов. Затем раствор охлаждали до комнатной температуры, фильтровали и удаляли при пониженном давлении растворитель. Остаток растворяли в минимальном количестве гексана и охлаждали до -20oС всю ночь, получив в результате 0,16 г продукта. Выход 38%.
1H (С6D6) δ 0,77 (с, 3Н), 0,96 (с, 3Н), 1,14 (с, 9Н), 1,32 (м, 7Н), 1,61 (м, 1Н), 1,81 (м, 1Н), 2,12 (д, 3Н), 2,91 (м, 4Н), 3,45 (м, 1Н), 3,65 (м, 1Н), 5,30 (с, 1Н), 6,69 (м, 1Н), 6,96 (м, 1Н), 7,05 (д, 1Н, 3Jн.н = 8,5 Гц), 7,83 (д, 1Н, 3Jн.н =8,5 Гц).
13С{ 1Н} (С6D6) δ 4,22, 6,41, 15,88, 20,84, 25,58, 35,18, 49,66, 55,95, 78,03, 96,87, 109,79, 116,86, 112,86, 119,46, 122,15, 122,63, 122,90, 126,53, 126,92, 127,10, 128,88, 130,11, 130,76, 140,41.
Пример 21
Получение (N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7a-η) -3- (1-пирролидинил) -1Н-инден-1-ил) силанаминато (2-) -N) -( (2,3,4,5-η)-2, 4-пентадиен) титана (53)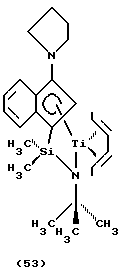
В сухом боксе в 30 мл гексана растворяли 0,50 г (1,16 ммоль) дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η) -3- (1-пирролидинил) -1Н-инден-1-ил)силанаминато(2-)-N)-титана. К полученному раствору прибавляли 1,14 мл пиперилена (11,6 ммоль), сразу все количество, и затем прибавляли по каплям 1,28 мл n-BuMgCl (2 М в гексанах, 2,55 ммоль). Смесь нагревали с обратным холодильником в течение 3 часов и затем удаляли в вакууме растворитель. Остаток растворяли в 15 мл пентана, раствор фильтровали через фритту, покрытую Целитом, и удаляли под вакуумом растворитель. Получили продукт в виде слегка влажного темно-коричневого твердого вещества (0,47 г, выход 95%).
1H (С6D6) δ 8,10 (д, 1Н, 3Jн.н =8,4 Гц), 7,82 (д, 1Н, 3Jн.н = 8,6 Гц), 7,13 (м, 2Н), 6,81 (м, 4Н), 5,60 (с, 1Н), 5,16 (с, 1Н), 4,07 (дд, 1Н, 3Jн.н = 11,11 Гц), 3,77 (м, 4Н), 3,46 (дд, 1Н, 3Jн.н =8,8 Гц), 2,85 (м, 8Н), 2,12 (д, 3Н, 3Jн.н = 5,4 Гц), 1,8-1,4 (м, 4Н), 1,38 (d, 3Н, 3Jн.н = 5,4 Гц), 1,29 (м, 8Н), 1,17 (с, 9Н), 1,15 (с, 9Н), 1,02 (с, 3Н), 0,94 (с, 3Н), 0,83 (с, 3Н), 0,79 (с, 3Н) м.д.
Пример 22
Получение дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1, 2, 3, 3а, 7a-η) -3- (1-пирролидинил) -1Н-инден-1-ил) силанаминато-(2-)-N)циркония (54)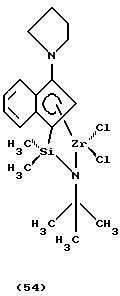
К суспензии ZrCl4, (1,80 г, 7,72 ммоль) в толуоле (100 мл) медленно прибавляли в виде твердого вещества N-(1,1- диметилэтил)-1,1-диметил-1-(3-(1-пирролидинил)-1Н-инден-1-ил)силанамин, дилитиевая соль (2,41 г, 7,72 ммоль). Полученной смеси давали перемешиваться всю ночь. По истечении времени реакции смесь фильтровали и удаляли летучие вещества, получив в результате целевой продукт в виде микрокристаллического твердого вещества золотистого цвета (1,7386 г, выход 48,9%).
1H ЯМР (С6D6) δ 0,51 (с, 3Н), 0,69 (с, 3Н), 1,33 (с, 9Н), 1,7-1,7 (м, 4Н), 3,1-3,2 (м, 2Н), 3,4-3,5 (м, 2Н), 5,59 (с, 1Н), 6,9-7,0 (м, 2Н), 7,6-7,7 (м, 1Н), 7,63 (д, 1Н, 3Jн.н. = 8,5 Гц).
13С ЯМР (С6D6) δ 2,28, 4,62, 25,68, 33,28, 50,68, 56,72, 82,15, 103,56, 122,56, 125,49, 125,62, 126,13, 129,28, 133,58, 142,98.
МСВР (EI, М+): вычислено 474,0432, найдено 474,0419.
Пример 23
Получение (N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7a-η) -3- (1-пирролидинил) -1Н-инден-1-ил) силанаминато (2-)-N)-диметилциркония (55)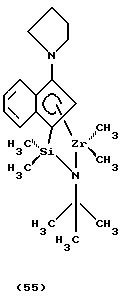
Дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)цирконий (0,99 г, 2,09 ммоль) перемешивали в диэтиловом эфире (50 мл), медленно прибавляя МеМgВr (4,60 ммоль, 1,53 мл 3,0 М раствора в диэтиловом эфире). Полученной смеси давали перемешиваться в течение ночи. По истечении времени реакции удаляли летучие вещества и остаток экстрагировали гексаном и фильтровали. Удалив гексан, получили целевой продукт в виде красного остатка (0,72 г, выход 79%).
1H ЯМР (С6D6) δ -0,58 (с, 3Н), 0,22 (с, 1Н), 0,51 (с, 3Н), 0,69 (с, 3Н), 1,37 (с, 9Н), 1,0-1,2 (м, 4Н), 3,1-3,2 (м, 2Н), 3,3-3,4 (м, 2Н), 5,60 (с, 1Н), 6,88 (т, 1Н, 3Jн.н=7,35 Гц), 6,96 (т, 1Н, 3Jн.н = 6,57 Гц), 7,54 (д, 1Н, 3Jн.н=8,49 Гц), 7,68 (д, 1Н, 3Jн.н = 8,58 Гц).
13С ЯМР (С6D6) δ 3,06, 5,11, 25,72, 34,54, 35,54, 40,32, 50,81, 55,17, 77,82, 103,10, 121,41, 122,96, 125,12, 125,25, 125,78, 132,33, 139,91.
Пример 24
Получение N,N-диметил-1Н-инден-3-амина (56)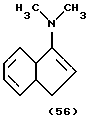
Это соединение получали, модифицируя общий метод Карлсона и Нильссона (Carlson, R.; Nilsson, A. Acta Chamica Scand. В 1984, 38, 49-53). В 3-горлую колбу емкостью 500 мл, снабженную навесной мешалкой и перегородкой и находящуюся под азотом вводили 150 мл сухого гексана. Растворитель охлаждали до температуры в пределах от -20 до -30oС, барботируя при этом в растворитель безводный диметиламин (12,6 г, 280 ммоль) без выпуска газа через барботер. К охлажденному и хорошо перемешанному раствору прибавляли TiCl4 (6,63 г, 35,0 ммоль) по каплям так, чтобы температура в колбе оставалась в пределах между -30 и -15oС (предупреждение: из-за образования амида титана рекомендуется мешалка Хершберга (Hershberg)). Полученную темно-коричневую суспензию перемешивали 15 минут с доведением до 0oС перед прибавлением сразу всего количества 1-инданона (4,32 г, 32,7 ммоль) в виде твердого вещества. Раствору давали согреться до комнатной температуры, после чего нагревали его до 60oС в течение 5 минут, после чего большая часть TiO2 выпадала из суспензии в осадок и раствор становился прозрачным. Суспензию фильтровали через слой высушенного в печи Целита толщиною 4 см под потоком азота и удаляли в вакууме растворитель, получив в результате указанный в заголовке енамин (3,8 г, 23,8 ммоль) с выходом 73% в виде темного масла, в котором не был обнаружен (ЯМР-анализ) кетон. ГХ-анализ показал, что чистота продукта составляла 98% (по площади).
1H ЯМР (CDCl3) δ 7,49 (д, 1Н, J=7,4 Гц), 7,42 (д, 1H, J=7,4 Гц), 7,30 (д, 1Н, J=7,4 Гц), 7,21 (д, 1Н, J=7,4 Гц), 5,46 (с, 1Н), 3,31 (с, 2Н), 2,83 (с, 6Н).
13С{ 1Н} ЯМР (CDCl3) δ 153,8, 144,6, 141,3, 125,6, 124,3, 123,8, 119,9, 107,8, 42,9, 35,6.
Получение (1-(диметиламино)-1H-инденил)лития (57)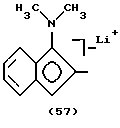
В сухом боксе смешивали 3,8 г (23,9 ммоль) N,N-диметил-1H-инден-3-амина с 100 мл гексана. К полученному раствору прибавляли по каплям 15 мл (23,9 ммоль) n-BuLi (1,6 М). По окончании прибавления n-BuLi раствор перемешивали всю ночь. Полученный осадок собирали путем фильтрования, промывали гексаном и сушили при пониженном давлении с получением 3,58 г продукта. Выход 91%.
Получение 1-(3-(диметиламино)-1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланамина (58)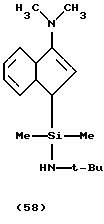
К раствору N-(трет-бутил)-N-(1-хлор-1,1-диметилсилил)-амина (3,59 г, 21,67 ммоль) в 80 мл ТГФ прибавляли в течение 30 минут раствор (1-(диметиламино)-1H-инденил)лития (3,58 г, 21,67 ммоль) в 40 мл ТГФ. По окончании прибавления реакционную смесь перемешивали всю ночь. Затем удаляли при пониженном давлении растворитель. Остаток экстрагировали гексаном и раствор фильтровали. Затем удаляли при пониженном давлении растворитель с получением 5,92 г продукта. Выход 95%.
1H (С6D6) δ -0,05 (с, 3Н), 0,03 (с, 3Н), 1,06 (с, 9Н), 2,68 (с, 6Н), 3,40 (с, 1Н), 5,63 (с, 1Н), 7,24 (м, 2Н), 7,56 (д, 1Н, 3Jн.н=7,4 Гц), 7,56 (д, 1Н, 3Jн.н=7,4 Гц).
13С{ 1Н} (С6D6) δ -0,46, 0,43, 34,08, 43,33, 44,00, 49,60, 111,20, 120,50, 123,84, 122,63, 123,84, 124,04, 124,75, 141,38, 146,44, 152,92.
Получение (3-(диметиламино)-1-(((1,1-диметилэтил)амино)-диметилсилил)-1H-инденил)лития, литиевая соль (59)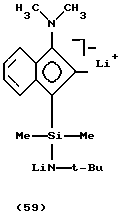
В сухом боксе смешивали 5,92 г (20,51 ммоль) 1-(3-(диметиламино) -1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланамина с 80 мл гексана. К полученному раствору прибавляли по каплям 25,6 мл (41,04 ммоль) n-BuLi (1,6 М). По окончании прибавления n-BuLi раствор перемешивали всю ночь. Полученный осадок собирали путем фильтрования, промывали 50 мл гексана и высушивали при пониженном давлении с получением 5,45 г продукта. Выход 88%.
Получение дихлор (1- ( (1,2, 3, 3а, 7a-η) -3- (диметиламино) -1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-) -N)титана (60)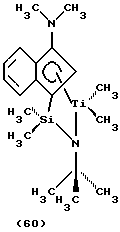
В 30 мл ТГФ растворяли (3-(диметиламино)-1-(((1,1-диметилэтил)амино)диметилсилил)-1H-инденил)литий, литиевая соль (5,45 г, 18,14 ммоль). К полученному раствору прибавляли ТiСl3(ТНF)3 (6,72 г, 18,14 ммоль) в виде твердого вещества. Через 1 час прибавляли PbCl2 (2,52 г, 9,07 ммоль) в виде твердого вещества. Затем реакционную смесь перемешивали еще час. Удаляли при пониженном давлении растворитель. Остаток экстрагировали 70 мл толуола и фильтровали. Удаляли при пониженном давлении толуол и остаток растирали с гексаном. Твердое вещество собирали путем фильтрования, промывали гексаном
и сушили при пониженном давлении с получением 4,00 г продукта. Выход 56%.
1H (С6D6) δ 0,48 (с, 3Н), 0,61 (с, 3Н), 1,06 (с, 9Н), 2,82 (с, 3Н), 5,74 (с, 1Н), 7,00 (м, 2Н), 7,14 (т, 2Н, 3Jн.н = 9,6 Гц).
13С{1Н} (С6D6) δ 2,43, 4,85, 34,73, 42,79, 50,17, 54,73, 107,25, 124,41, 124,98, 125,09, 137,0, 145,01.
Пример 25
Получение (1-( (1,2,3,3а, 7а-η)-3- (диметиламино) -lH-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)диметилтитана (61)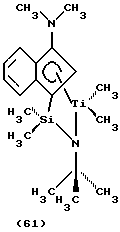
В 40 мл Et2O суспендировали 0,60 г дихлор(1-((1,2,3,3а, 7a-η) -3- (диметиламино) -1Н-инден-1-ил) -N- (1,1-диметилэтил) -1,1-диметилсиланаминато(2-)-N)титана (1,53 ммоль). К полученной суспензии прибавляли по каплям с перемешиванием в течение 20 минут 1,07 мл МеМgI (3,0 М). По окончании прибавления МеМgI раствор перемешивали в течение 40 минут. По истечении этого времени удаляли при пониженном давлении Et2O и остаток экстрагировали гексаном, раствор фильтровали и фильтрат выпаривали при пониженном давлении досуха с получением 0,43 г продукта. Выход 80%.
1H (С6D6) δ 0,03 (с, 3Н), 0,44 (с, 3Н), 0,63 (с, 3Н), 0,85 (с, 3Н), 1,49 (с, 9Н), 2,78 (с, 6Н), 5,56 (с, 1Н), 6,85 (т, 1Н, 3Jн.н = 7,5 Гц), 7,06 (т, 1Н, 3Jн.н = 7,5 Гц), 7,44 (д, 1Н, 3Jн.н =8,5 Гц), 7,63 (д, 1Н, 3Jн.н = 8,7 Гц).
Пример 26
Получение (1- ( (1,2, 3, 3а, 7а-η) -3- (диметиламино) -1H-инден-1-ил)-Н-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)-( (2,3,4,5-η)-2, 4-гексадиен) титана (62)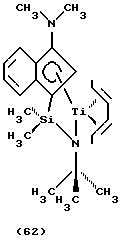
К 0,5490 г дихлор (1-( (1, 2, 3, 3а, 7a-η)-3-(диметиламино) -1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато-(2)-N)-титана (1,35 ммоль), суспендированного и растворенного в 50 мл гексана прибавляли 1,4 мл 2,4-гексадиена (12,3 ммоль), а затем 1,63 мл BuMgCl (2,0 М в Et2O) (3,26 ммоль) вместе с дополнительными 3 мл Et20. Реакционную смесь нагревали с обратным холодильником в течение 1,5 часов, после чего давали ей перемешиваться в течение ночи. Удаляли при пониженном давлении растворитель и остаток экстрагировали гексаном, раствор фильтровали и фильтрат выпаривали при пониженном давлении досуха. После прибавления гексана для растворения очень темного продукта раствор хранили всю ночь в холодильнике. Удаляли супернатант, получив в результате 0,0735 г черного кристаллического продукта. Супернатант концентрировали и опять охлаждали в холодильнике с получением дополнительного продукта.
1H (С6D6) δ 0,72 (с, 3Н), 0,94 (с, 3Н), 1,10 (с, 9Н), 1,26 (д, 3Н, 3Jн.н = 5,3 Гц), 1,60 (м, 1Н), 1,78 (м, 1Н), 2,10 (д, 3Н, 3Jн.н = 5,5 Гц), 2,37 (с, 6Н), 3,38 (м, 1Н), 3,97 (м, 1Н), 5,46 (с, 1Н), 6,68 (т, 1Н, 3Jн.н = 7,7 Гц), 6,94 (м, 2Н), 7,87 (д, 1Н, 3Jн.н = 8,5 Гц).
13С (С6D6) δ 142,9, 130,0 128,9, 123,2, 122,5, 121,8, 120,1, 112,4, 109,3, 99,0, 92,3, 79,6, 78,6, 56,4, 42,3, 35,0, 20,3, 15,7, 14,4, 6,4, 4,1. МС высокого разрешения: Вычислено для С23Н36N2SiТi: 416,2127. Найдено 416,2107.
Пример 27
Получение (1,1'-(η4-1,3-бутадиен-1,4-диил) бис (бензол)-(1-( (1,2,3, 3а, 7а-η) -3- (диметиламино) -1Н-инден-1-ил) -N- (1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)титана (63)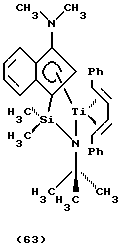
В сухом боксе смешивали 0,40 г дихлор(1-((1,2,3,3а,7а-η)-3-(диметиламино)-1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2)-N)титана с 0,21 г транс-1,4-дифенил-бутадиена и суспендировали в 30 мл гексана. К полученному раствору прибавляли 1,27 мл n-BuLi (1,6 М) и раствор нагревали с обратным холодильником в течение 2 часов. Затем раствор охлаждали до комнатной температуры, фильтровали и удаляли при пониженном давлении растворитель, получив в результате 0,23 г продукта. Выход 43%.
1H (С6D6) δ 0,68 (с, 3Н), 0,82 (с, 3Н), 1,25 (с, 9Н), 1,47 (с, 9Н), 3,45 (м, 1Н), 3,60 (м, 1Н), 4,15 (м, 1Н), 4,65 (м, 1Н), 5,20 (с, 1Н), 6,30-7,55 (м, 14Н).
Пример 28
Получение хлор (циклопентадиенил) (1-( (1, 2, 3, 3а, 7a-η)-3-(диметиламино)-1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)титана (64)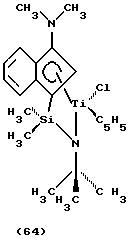
К раствору 0,312 г дихлор (1- ((1, 2, 3, 3а, 7а-η) -3- (диметиламино)-1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсилан-аминато(2-)-N)титана (0,77 ммоль) в примерно 35-40 мл Et2O медленно прибавляли 0,769 мл NaC5H5 (1,0 М в Et2O) (1,00 ммоль). Пурпурной реакционной смеси давали перемешиваться в течение полутора дней. Удаляли при пониженном давлении растворитель и остаток экстрагировали гексаном, раствор фильтровали и фильтрат выпаривали при пониженном давлении досуха. После прибавления гексана для растворения очень темного продукта раствор, весьма интенсивно окрашенный в пурпурный цвет, хранили всю ночь в холодильнике. После удаления супернатанта и сушки при пониженном давлении получили продукт в виде 0,1119 г кристаллов. Супернатант концентрировали и затем охлаждали в холодильнике, получив дополнительный продукт в виде микрокристаллов.
1H (С6D6) δ 0,50 (с, 3Н), 0,60 (с, 3н), 1,31 (с, 9Н), 2,73 (с, 6Н), 5,69 (с, 5Н), 5,78 (с, 1Н), 6,79 (т, 1H, 3Jн.н =7,4 Гц), 7,15 (м, 2Н), 7,33 (д, 1Н, 3Jн.н =8,2 Гц).
13С (С6D6) δ 170,8, 158,6, 126,6, 124,3, 121,3, 121,1, 115,4, 95,2, 88,4, 61,2, 42,5, 32,9, 3,9, 2,7. МСВР: Вычислено для C22H31ClN2SiTi: 434,14245. Найдено 434,1426.
Пример 29
Получение циклопентадиенил(N-(1,1-диметилэтил)-1,1-диметил-1- ((1,2,3, 3а, 7а-η) -3- (1-пирролидинил) -1Н-инден-1-ил) силанаминато(2-)-N)титана (65)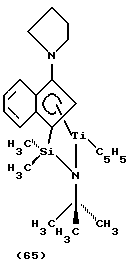
К хорошо перемешанному раствору 0,56 г трис(циклопентадиенил)титана (2,31 ммоль) в примерно 50 мл ТГФ медленно прибавляли 0,75 г дилитиевой соли (N-(1,1-диметилэтил)-1,1-диметил-1-(3-пирролидино-1Н-инден-1-ил)силанамина (2,31 ммоль) в виде порошка. Желтовато-зеленой (красноватой под проходящим светом) реакционной смеси давали перемешиваться всю ночь. Удаляли при пониженном давлении растворитель и остаток экстрагировали примерно 80 мл толуола, раствор фильтровали для удаления твердого вещества очень бледно-лилового цвета из темно-оливково-зелено-коричневого фильтрата. Обе продуктные фракции сушили при пониженном давлении. Темный продукт, растворимый в толуоле, экстрагировали гексаном, фильтровали и удаляли растворитель из темно-коричневого раствора с получением 0,9113 г продукта в виде кажущегося черным порошка (93%). Протонный ЯМР показал лишь широкие горбы (максимумы) в области 0,8-2,4 м. д. ЭСР (электронный спиновый резонанс) показал сигнал при g= 1,98, соответствующий комплексу Ti (III). Палевое твердое вещество, собранное на фильтре, экстрагировали ТГФ, фильтровали и удаляли при пониженном давлении растворитель, с получением 0,29 г бледно-пурпурно-розового твердого вещества (87%, на основе LiC5H5). К раствору 0,20 г "LiC5H5" (2,78 ммоль) в примерно 20 мл ТГФ прибавляли 0,179 г FeCl2 (1,40 ммоль). Раствор перемешивали в течение примерно 4-5 часов. Удаляли при пониженном давлении растворитель. Остаток экстрагировали толуолом, фильтровали и удаляли при пониженном давлении растворитель с получением 0,22 г оранжевого порошка, который идентифицировали как ферроцен. Выход 85%.
1H (C6D6) δ 4,00 (с).
13С (С6D6) δ 68,3. МСВР: Вычислено для С10Н10Fе: 186,0132. Найдено: 186,0124.
Пример 30
Получение хлор(циклопентадиенил)(N-(1,1-диметилэтил)-1,1-диметил-1- ( (1,2, 3, 3а, 7a-η) -3- (1-пирролидинил) -1Н-инден-1-ил)-силанаминато(2-)-N)титана (66)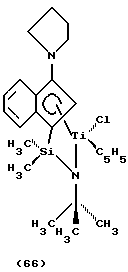
К раствору 0,0240 г циклопентадиенил(N-(1,1-диметилэтил) -1,1-диметил-1- ( (1, 2, 3, 3а, 7а-η) -3- (1-пирролидинил) -1Н-инден-1-ил)силанаминато(2-)-H)титана (0,056 ммоль), полученного так, как описано выше, в примерно 0,5-1 мл C6D6 в ЯМР-ампуле прибавляли 0,048 г PbCl2 (0,17 ммоль). Черный раствор сразу же приобретал пурпурный цвет. Через примерно 20-30 минут получали ЯМР-спектры неочищенной реакционной смеси.
1H (С6D6) δ 0,52 (с, 3Н), 0,64 (с, 3Н), 1,17 (ш, 4Н), 1,34 (с, 9Н), 3,16 (ш, 2Н), 3,52 (ш, 2Н), 5,73 (с, 5Н), 5,83 (с, 1Н), 6,83 (т, 1Н, 3Jн.н = 7,4 Гц), 7,2 (м, 2Н), 7,37, (д, 1Н, 3Jн.н = 8,0 Гц).
13С (С6D6) δ 167,7, 158,6, 127,3, 127,0, 126,6, 124,1, 121,1, 115,2, 93,6, 88,5, 61,0, 50,7, 32,9, 25,2, 4,0, 2,8. МСВР: Вычислено для C24H33ClN2SiTi: 460,1581. Найдено: 460,1580.
Пример 31
Получение (1- ( (1,2, 3, 3а, 7а-η) -3- (диметиламино) -1H-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-)-N)((2-диметиламино-N)фенил)метил-С)титана (67)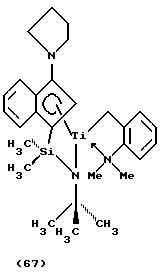
К раствору 0,3390 г цикдопентадиенил(N-(1,1-диметилэтил) -1,1-диметил-1- ( (1,2,3, 3а, 7а-η) -3- (1-пирролидинил) -1Н-инден-1-ил)силанаминато(2-)-N)титана (0,797 ммоль) в примерно 20 мл Et2O медленно прибавляли 0,1125 г (2- (N,N-диметиламино)бензил)лития (0,797 ммоль) в виде порошка. Реакционной смеси давали перемешиваться всю ночь. Из темно-коричневато-красного раствора удаляли при пониженном давлении растворитель и остаток экстрагировали гексаном, после чего из сильно растворимого красно-коричневого раствора отфильтровывали очень темное твердое вещество, намного менее растворимое в гексане. Обе продуктные фракции сушили при пониженном давлении. Протонные ЯМР-спектры обоих продуктов (в C6D6) показали широкие лишенные характерных черт пики, такие, как уже наблюдались для других соединений Ti (III). После окисления ЯМР-проб посредством PbCl2 определили путем 1Н ЯМР, что начальная реакция была неполной. Твердое вещество на фритте экстрагировали С6D6, фильтровали и объединяли с другой продуктной фракцией. Удаляли при пониженном давлении растворитель, остаток растворяли в примерно 15 мл Et2O и к полученному раствору прибавляли дополнительные 0,0170 г (2-(N, N-диметиламино)бензил)лития (всего 0,918 ммоль) в виде порошка. После перемешивания в течение ночи и удаления при пониженном давлении растворителя остаток экстрагировали гексаном, отфильтровывали из раствора твердый материал и очень темный фильтрат концентрировали. Твердое вещество, собранное на фритте, помещали в пузырек с примерно 0,075 г FeCl2 и примерно 3 мл ТГФ и оставляли стоять всю ночь. Удаляли при пониженном давлении растворитель и остаток экстрагировали С6D6 и фильтровали в ЯМР-ампулу. ЯМР-спектры показали присутствие Cp2Fe, по-видимому, в тетрагидрофурановом комплексе неорганического материала. 1H (С6D6) δ 2,00 (ш. с), 4,01 (с), 5,06 (ш. с). 13С (С6D6) δ 72,0, 68,2, 35,1. При концентрировании фильтрата начинало кристаллизоваться очень темное твердое вещество, в результате чего оставался темно-красный раствор цвета венозной крови. Твердое вещество отфильтровывали, промывали гексаном и сушили при пониженном давлении. Выход темно-красновато-коричневого продукта составлял 0,1718 г. Протонный ЯМР 0,0399 г вещества в С6D6 показал широкие пики неясной структуры. ЭСР показал сигнал при g=1,98, соответствующий комплексу Ti (III). Магнитная восприимчивость (метод Эванса): 1,57 mв.
Пример 32
Получение хлор (1- ( (1,2,3, 3а, 7a-η) -3- (диметиламино) -1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминато(2-) -N)((2-диметиламино)фенил)метил)титана (68)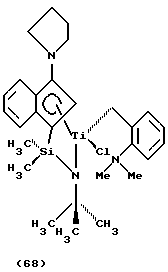
К раствору 0,0224 г (1-( (1, 2, 3, 3а, 7а-η)-3-(диметиламино) -1Н-инден-1-ил)-N-(1,1-диметилэтил)-1,1-диметилсиланаминатo-(2-)-N)((2-диметиламино-N)фенил)метил-С)титана (полученного так, как описано выше) в примерно 0,5-1 мл С6D6 в ЯМР-ампуле прибавляли примерно 0,070 г PbCl2. Реакционную смесь взбалтывали и затем оставляли стоять на ночь. ЯМР-спектры показали присутствие двух изомеров (в отношении приблизительно 1:2) вместе с очень небольшим количеством (хлор)(циклопентадиенильного) комплекса. 1H (С6D6) необычные пики одного изомера δ 0,67 (с, 1Н), 0,81 (с, 1Н), 1,63 (с, 9Н), 2,07 (д, 1Н, 3Jн.н = 12,6 Гц), 2,54 (с, 6Н), 2,64 (д, 1Н, 3Jн.н = 12,6 Гц), 3,17 (м, 2Н), 3,57 (м, 2Н), 5,53 (с, 1Н), 6,35 (с, 1Н).
Необычные пики другого изомера δ 0,71 (с, 1Н), 0,88 (с, 1Н), 1,61 (с, 9Н), 2,19 (д, 1Н, 3Jн.н = 13,5 Гц), 2,21 (м, 2H), 2,53 (с, 6Н), 2,76 (м, 2Н), 3,32 (д, 1Н, 3Jн.н = 13,5 Гц), 5,06 (с, 1Н), 7,90 (д, 1Н, 3Jн.н =7,4 Гц). Общие маловажные пики обоих изомеров δ 1,38 (ш, 4Н), 6,66 (м), 6,76 (м), 6,87 (м), 7,08 (м), 7,40 (м).
13С (С6D6) (оба изомера) δ 154,2, 153,5, 153,2, 152,9, 147,3, 142,8, 136,0, 133,4, 131,0, 130,0, 128,9, 125,8, 125,7, 125,6, 124,3, 123,4, 123,0, 122,7, 122,3, 122,1, 117,9, 114,3, 105,5, 130,8, 95,2, 95,0, 71,7, 69,6, 62,0, 61,3, 50,0, 49,9, 47,7, 47,4, 34,1, 34,1, 33,0, 31,9, 25,6, 14,4, 4,1, 2,8, 2,2, 1,3.
Пример 33
Получение N-метил-N-фенил-1H-инден-3-амина (89)
В сухую колбу, снабженную ловушкой Дина-Старка и холодильником, загружали 1-инданон (10,0 г, 75,7 ммоль), N-метил-анилин (15,1 г, 141 ммоль) и толуол (200 мл). Прибавляли каталитическое количество п-толуолсульфоновой кислоты (0,1 г) и смесь нагревали с обратным холодильником под азотом в течение 96 часов. Реакционную смесь охлаждали и удаляли при пониженном давлении толуол, после чего оставшийся материал перегоняли под вакуумом. Наиболее высококипящую фракцию (6,8 г, т. к. (точка кипения) 150-152oС/0,7 мм рт. столба) собирали в виде желтого масла, которое, постояв, затвердевало в желто-оранжевое твердое вещество. Этот материал хранили в мануальном боксе. ЯМР-анализ показал присутствие приблизительно 10% N-метиланилина продукте. Однако дополнительная перегонка другого образца перегнанного енамина не была успешной в снижении количества нежелательного амина в продукте.
13Н ЯМР (d8-PhMe) δ 6,78-7,25 (м, 9Н), 5,62 (т, 1Н), 3,24 (д, 2Н), 305 (с, 3Н).
13С{ 1Н} ЯМР (d8-PhMe) δ 149,84, 149,02, 144,30, 141,85, 129,05, 125,82, 124,98, 124,06, 121,79, 121,69, 121,19, 113,66, 42,01, 35,89.
Получение (3-(метилфениламино)-1H-инденил)лития (70)
N-метил-N-фенил-1Н-инден-3-амин (6,8 г, 30,7 ммоль) растворяли в 100 мл гексана и к полученному раствору прибавляли по каплям посредством шприца в течение 15 минут 12,3 мл 2,5 М n-BuLi (0,936 экв). При прибавлении n-BuLi в растворе появлялся желтый осадок с образованием суспензии, которой давали перемешиваться в течение ночи. По истечении этого времени твердое вещество отфильтровывали, промывали 50 мл гексана и сушили в вакууме всю ночь с получением целевого аниона в виде желто-оранжевого твердого вещества (5,83 г, 25,6 ммоль) с выходом 89% по литиевому реагенту.
Получение N-(1,1-диметилэтил)-1,1-диметил-1-(3-(метилфениламино)-1Н-инден-1-ил)силанамина (71)
К раствору трет-бутиламинодиметилсилилхлорида (2,17 г, 16,35 ммоль) в 35 мл ТГФ прибавляли по каплям в течение 30 минут раствор (3-(метилфениламино)-1H-инденил)лития (3,10 г, 13,64 ммоль) в 50 мл ТГФ, после чего реакционную смесь продолжали перемешивать 25 часов. Выпаривали растворитель и полученное масло подвергали воздействию вакуума в течение 4 часов. Это масло растворяли в 100 мл гексана и отфильтровывали от LiCl. Удаляли в вакууме растворитель, получив в результате вакуумного удаления летучих веществ в течение ночи продукт (4,66 г, 13,3 ммоль) в виде темно-красного масла с выходом 98%.
1H ЯМР (С6D6) δ 7,56 (д, 1Н, J=7,4 Гц), 7,15 (м, 4Н), 7,07 (д, 1Н, J = 7,4 Гц), 7,00 (д, 2Н, J=8,0 Гц), 6,83 (м, 1Н), 6,125 (д, 2Н, J = 2 Гц), 3,464 (д, 4Н, J= 2,0 Гц), 3,14 (с, 3Н), 1,08 (с, 9Н), 1,0 (ш.с, 1Н, N-H), 0,04 (с, 3Н), 0,00 (с, 3Н).
13С{ 1Н} ЯМР (С6D6) δ 149,3, 147,6, 145,7, 141,2, 129,3, 124,8, 124,3, 123,6, 121,4, 120,7, 120,3, 118,8, 68,1, 49,7, 44,9, 41,6, 34,1, 33,9, 33,6, 25,3, 0,54, -0,1.
Получение (1-(((1,1-диметилэтил)амино)диметилсилил)-3-(метилфениламино)-lH-инденил)лития, литиевая соль (72)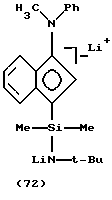
В сухом боксе смешивали 4,47 г (12,3 ммоль) N-(1,1-диметилэтил) -1,1-диметил-1-(3-(метилфениламино)-1Н-инден-1-ил)-силанамина с 80 мл гексана. К полученному раствору прибавляли по каплям 15,9 мл (25,5 ммоль) n-BuLi (1,6 М). По окончании прибавления n-BuLi раствор перемешивали всю ночь. Полученный осадок собирали путем фильтрования, промывали 50 мл гексана и высушивали при пониженном давлении с получением 4,25 г продукта. Выход 92%.
Получение дихлор(N-(1,1-диметилэтил)-1,1-диметил-1-((1, 2, 3, 3а, 7а-η) -3- (1-метилфениламино) -1Н-инден-1-ил) силанаминато(2-)-N)титана (73)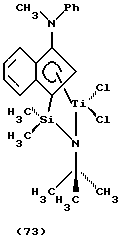
В 30 мл ТГФ растворяли (1-(((1,1-диметилэтил)амино)диметилсилил)-3-(метилфениламино)-1H-инденил)литий, литиевая соль (4,25 г, 11,72 ммоль). К полученному раствору прибавляли ТiСl3(ТНF)3 (4,34 г, 11,72 ммоль) в виде твердого вещества. Через 1 час прибавляли PbCl2 (1,63 г, 5,86 ммоль) в виде твердого вещества. Затем реакционную смесь перемешивали еще час. Удаляли при пониженном давлении растворитель. Остаток экстрагировали 70 мл толуола и фильтровали. Удаляли при пониженном давлении толуол и остаток растирали с гексаном. Твердое вещество собирали путем фильтрования, промывали гексаном и сушили при пониженном давлении с получением 1,57 г продукта. Выход 29%.
1H (С6D6) δ 0,47 (с, 3Н), 0,62 (с, 3Н), 1,30 (с, 9Н), 3,25 (с, 2Н), 5,97 (с, 2Н), 6,70 (д, 1Н, 3Jн.н = 8,1 Гц), 6,80 (м, 3Н, 3Jн.н =7,9 Гц), 7,06 (т, 2Н, 3Jн.н = 8,1 Гц), 7,33 (д, 2Н, 3Jн.н =7,9 Гц), 7,58 (д, 1Н, 3Jн.н =7,9 Гц).
13С{1Н} (С6D6) δ 1,44, 3,89, 33,01, 43,21, 61,72, 93,96, 108,97, 125,93, 126,21, 126,33, 127,51, 128,15, 128,51, 135,53, 146,83, 148,49.
Пример 34
Получение (N-(1,1-диметилэтил)-1,1-диметил-1-((1,2,3,3а, 7a-η) -3- (1-метилфениламино) -1Н-инден-1-ил) силанаминато (2-) -N)-диметилтитана (74)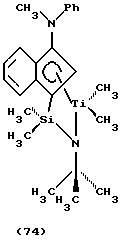
В 40 мл Et2O суспендировали 0,40 г дихлор(N-(1,1-диметилэтил) -1,1-диметил-1- ( (1,2,3,3а,7a-η)-3-( 1-метилфениламино)-1H-инден-1-ил) силанаминато (2-)-N) титана (0,80 ммоль). К полученной суспензии прибавляли по каплям с перемешиванием в течение 20 минут 0,57 мл МеМgI (3,0 М). По окончании прибавления МеМgI раствор перемешивали в течение 40 минут. По истечении этого времени удаляли при пониженном давлении Et2O и остаток экстрагировали гексаном, раствор фильтровали и фильтрат выпаривали при пониженном давлении досуха с получением 0,35 г продукта. Выход 96%.
1H (С6D6) δ 0,62 (с, 3Н), 0,70 (с, 3Н), 0,69 (с, 3Н), 1,04 (с, 3Н), 1,54 (с, 9Н), 3,29 (с, 3Н), 6,04 (с, 1Н), 6,88 (м, 2Н), 6,96 (т, 1Н, 3Jн.н=7,9 Гц), 7,16 (т, 4Н), 7,28 (д, 1Н, 3Jн.н=8,5 Гц), 7,55 (д, 1Н, 3Jн.н=8,5 Гц).
13С{ 1Н} (С6D6) δ 1,58, 4,00, 34,07, 41,48, 52,29, 54,13, 58,24, 83,55, 112,67, 121,05, 121,98, 124,76, 126,24, 129,03, 132,45, 140,91, 148,68.
Пример 35
Получение 1-(1-(хлордиметилсилил)-1H-инден-3-ил)пирролидина (75)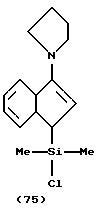
К раствору SiMe2Cl2 (8,1 г, 62,76 ммоль) в 50 мл ТГФ прибавляли в течение 30 минут раствор (1-(1-пирролидинил)-1Н-инденил)лития (2,00 г, 10,46 ммоль) в 25 мл ТГФ. По окончании прибавления реакционную смесь перемешивали всю ночь. Удаляли при пониженном давлении растворитель. Остаток экстрагировали гексаном и раствор фильтровали. Удалив при пониженном давлении растворитель, получили 2,40 г продукта. Выход 82%.
1H (С6D6) δ 0,03 (с, 3Н), 0,15 (с, 3Н), 1,52 (м, 4Н), 3,14 (м, 4Н), 3,43 (с, 1Н), 5,14 (с, 1Н), 7,24 (м, 2Н), 7,23 (м, 2Н), 7,60 (м, 2Н).
13С{ 1Н} (С6D6) δ -0,75, 0,48, 25,51, 42,72, 50,52, 100,02, 103,77, 121,18, 121,29, 124,30, 124,70, 125,58, 141,29, 144,61, 150,50.
Получение 1,1-диметил-N-(фенилметил)-1-(3-(1-пирролидинил)-1Н-инден-1-ил)силанамина (76)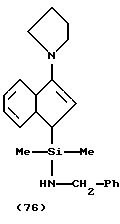
К раствору 1-(1-(хлордиметилсилил)-1H-инден-3-ил)пирролидина (2,40 г, 8,64 ммоль) в 150 мл ТГФ прибавляли в течение 30 минут раствор бензиламида лития (0,97 г, 8,64 ммоль) в 75 мл ТГФ. По окончании прибавления реакционную смесь перемешивали всю ночь. Затем удаляли при пониженном давлении растворитель. Остаток экстрагировали гексаном и раствор фильтровали. Затем удаляли при пониженном давлении растворитель с получением 2,99 г продукта. Выход 99%.
1Н (С6D6) δ -0,04 (с, 3Н), 0,06 (с, 3Н), 1,58 (м, 4Н), 3,22 (м, 4Н), 3,76 (д, 4Н), 5,32 (с, 1Н), 7,24 (м, 7Н), 7,47 (д, 1Н, 3Jн.н=7,7 Гц), 7,63 (д, 1Н, 3jн.н=7,7 Гц).
13С{ 1Н} (С6D6) δ -2,42, -3,16, 25,47, 43,84, 48,61, 50,91, 104,08, 121,65, 124,64, 126,65, 127,24, 128,46, 141,43, 144,42, 146,68, 148,87.
Получение (1-(((фенилметил)амино)диметилсилил)-3-(1-пирролидинил)-1H-инденил)лития, литиевая соль (77)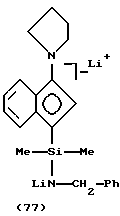
В сухом боксе смешивали 2,99 г (8,50 ммоль) 1,1-диметил-N-(фенилметил)-1-(3-(1-пирролидинил)-1Н-инден-1-ил)силанамина с 80 мл гексана. К полученному раствору прибавляли по каплям 11,25 мл (18,0 ммоль) n-BuLi (1,6 М). По окончании прибавления n-BuLi раствор перемешивали всю ночь. Полученный осадок собирали путем фильтрования, промывали 50 мл гексана и высушивали при пониженном давлении с получением 2,87 г продукта. Выход 93%.
Получение дихлор(1,1-диметил)-N-(фенилметил)-1-((1,2,3, 3а, 7a-η) -3- (1-пирролидинил) -1Н-инден-1-ил) силанаминато (2-) -N)титана (78)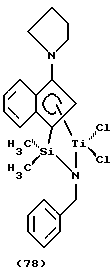
В 30 мл ТГФ растворяли (1-(((фенилметил)амино)диметилсилил)-3-(1-пирролидинил)-1H-инденил)литий, литиевая соль (2,87 г, 7,96 ммоль). К полученному раствору прибавляли ТiСl3(ТНF)3 (2,95 г, 7,96 ммоль) в виде твердого вещества. Через 1 час прибавляли PbCl2 (1,10 г, 3,98 ммоль) в виде твердого вещества. Затем реакционную смесь перемешивали еще час. Удаляли при пониженном давлении растворитель. Остаток экстрагировали 70 мл толуола и фильтровали. Удаляли при пониженном давлении толуол и остаток растирали с гексаном. Твердое вещество собирали путем фильтрования, промывали гексаном и сушили при пониженном давлении с получением 2,30 г продукта. Выход 62%.
1H (С6D6) δ 0,17, (с, 3Н), 0,27 (с, 3Н), 1,48 (м, 4Н), 3,19 (м, 2Н), 3,50 (м, 2Н), 5,25 (АВ кв, 2H, 2J=18,7 Гц), 7,03 (м, 5Н), 7,21 (м, 2H), 7,57 (д, 1Н, 3Jн.н=7,9 Гц), 7,61 (д, 1Н, 3Jн.н = 7,9 Гц).
Пример 36
Получение (1,1-диметил-N- (фенилметил) -1-( (1,2,3, 3а,7а-η)-3-(1-пирролидинил)-1Н-инден-1-ил)силанаминато(2-)-N)диметилтитана (79)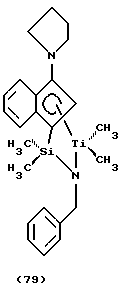
В 40 мл Et2O суспендировали 0,30 г дихлор(1,1-диметил)-N- (фенилметил) -1-( (1,2,3, 3а, 7а-η) -3- (1-пирролидинил) -1Н-инден-1-ил)силанаминато(2-)-N)титана (0,64 ммоль). К полученной суспензии прибавляли по каплям с перемешиванием в течение 20 минут 0,45 мл МеМgI (3,0 М). По окончании прибавления МеМgI раствор перемешивали в течение 40 минут. По истечении этого времени удаляли при пониженном давлении Et2O и остаток экстрагировали гексаном, раствор фильтровали и фильтрат выпаривали при пониженном давлении досуха с получением 0,23 г продукта. Выход 84%.
1H (С6D6) δ 0,12 (с, 3Н), 0,18 (с, 3Н), 0,36 (с, 3Н), 0,78 (с, 3Н), 1,52 (м, 4Н), 3,24 (м, 4Н), 5,20 (АВ кв, 2H, 2Jн.н=18,0 Гц), 5,48 (с, 1Н), 6,88 (т, 1Н, 3Jн.н= 9,0 Гц), 7,00 (т, 1Н, 3Jн.н=9,0 Гц), 7,15 (д, 1Н, 3Jн.н=9,0 Гц), 7,19 (т, 1Н, 3Jн.н=9,0 Гц), 7,30 (д, 1Н, 3Jн.н=9,0 Гц), 7,51 (д, 1Н, 3Jн.н=9,0 Гц), 7,78 (д, 1Н, 3Jн.н=9,0 Гц).
13С{1Н} (С6D6) δ -0,63, 1,44, 25,82, 49,57, 50,68, 54,28, 55,29, 105,19, 125,19, 125,21, 126,02, 127,08, 128,64, 128,73, 134,75, 142,57, 143,72, 146,24.
Данные полимеризации для каталитической системы, содержащей металлокомплексы по настоящему изобретению, представлены в табл. 2.
Рентгеновское определение структуры дихлор(N-(1,1-диметилэтил) -1,1-диметил-1- ( (1,2,3, 3а, 7а-η)-3-( 1-пиперидинил) -1Н-инден-1-ил)сиданаминато(2-)-N)титана.
СБОР ДАННЫХ
Темно-пурпурный брускообразный кристалл с размерами 0,22•0,21•0,19 мм погружали в масло (Paratone N. Еххоn) и закрепляли на тонком стеклянном волокне. Переносили кристалл в дифрактометр SMART PLATFORM (Siemens), снабженный графитовым монохроматическим кристаллом, источником излучения МоКα 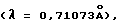 двухмерный детектор CCD (ПЗС - прибор с зарядовой связью), который держали на расстоянии 5,078 см от кристалла. На протяжении всего периода сбора данных кристалл омывали холодным потоком азота (-100oС). Три серии из 20 фреймов каждая собирали, охватив три перпендикулярных сектора пространства, с использованием метода ω-сканирования при времени экспозиции, равном десяти секундам. Интеграция фреймов с последующим индексированием отражений и уточнением по наименьшим квадратам дали ориентационную матрицу и моноклинную решетку кристалла.
двухмерный детектор CCD (ПЗС - прибор с зарядовой связью), который держали на расстоянии 5,078 см от кристалла. На протяжении всего периода сбора данных кристалл омывали холодным потоком азота (-100oС). Три серии из 20 фреймов каждая собирали, охватив три перпендикулярных сектора пространства, с использованием метода ω-сканирования при времени экспозиции, равном десяти секундам. Интеграция фреймов с последующим индексированием отражений и уточнением по наименьшим квадратам дали ориентационную матрицу и моноклинную решетку кристалла.
Сбор данных обеспечил сбор всего 1381 фреймов в четырех различных опытах, охвативших более одной полной полусферы данных. Параметры сканирования фреймов сведены в табл. 3.
Последний опыт ( 4) представляет собой повторное измерение первых 50 фреймов из опыта 1. Это сделано для контроля стабильности кристалла и дифрактометра и внесения поправки на какой-либо распад кристалла.
В состав дифрактометра входит 0,8-миллиметровый коллиматор, дающий рентгеновский пучок диаметром 0,8 мм. Мощность генератора была установлена на уровне 50 кВ и 30 мА. Для управления дифрактометром, фреймового сканирования, индексирования, вычислений ориентационной матрицы, уточнения по наименьшим квадратам параметров ячеек, измерений граней кристалла и сбора фактических данных использовали программу SMART1. Программы ASTRO SMART, SAINT и XPREP, являющиеся частью кристаллографического пакета программного обеспечения ф. "Siemens" для сбора, предварительного преобразования и подготовки данных об одиночном кристалле, использовали для создания методики сбора данных.
ПОДГОТОВКА ДАННЫХ
Все 1381 кристаллографические фреймы необработанных данных читали с помощью программы SAINT и интегрировали, пользуясь 3D алгоритмами профилирования. Полученные данные предварительно преобразовывали для получения отражений типа hkl и их интенсивностей и определяли среднеквадратичное отклонение. Данные корректировали, вводя поправку на эффект Лоренца и поляризационный эффект. Было собрано всего 16988 отображений, представляющих диапазон уровня резервирования 2,7-3,99 и имеющих значение Rsym в пределах от 3,3% (оболочка отражений при наименьшем угле 2θ) до 4,4% (оболочка отражений при наибольшем угле 2θ (55o)). Вводили поправку на распад кристалла, которая составляла менее 1%. Параметры элементарной ячейки уточняли методом наименьших квадратов установочных углов 7091 отражения. Параметры элементарной ячейки представляют собой: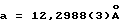 α=90o
α=90o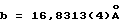 β=106,87(I)o
β=106,87(I)o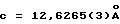 γ=90o
γ=90o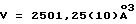
Вводили поправки на абсорбцию, пользуясь программой SADABS (Sheldrick, G.M., 1966). SADABS - это программа для ввода поправок на абсорбцию на основе psi разверток по Блессингу. Blessing, R.H. (1995), Acta Crist. A51, 33-38. Коэффициент поглощения составлял 0,617 мм-1, а минимальный и максимальный коэффициенты пропускания составляли 0,761 и 0,915 соответственно.
Подготовку данных осуществляли с использованием программы XPREP. Пространственная группа была определена на основе систематических отсутствий как P21/n (# 14). XPREP дала следующие кристаллографические параметры: 5659 уникальных отражений (Rint=3,65%) с индексами -13≤h≤15, -22≤k≤15, -16≤l≤15.
РЕШЕНИЕ И УТОЧНЕНИЕ СТРУКТУРЫ
Структуру решали непосредственными методами в SHELXTL5 (Sheldrick, G.M., 1995, пакет кристаллографического программного обеспечения, Siemens Analitical, Inc. , Madison, Wisconsin, USA), посредством которых были получены положения всех неводородных атомов. Структуру уточняли также с использованием SHELXTL5 согласно полноматричному уточнению методом наименьших квадратов. Неводородные атомы уточняли с использованием анизотропных термических параметров и все водородные атомы располагали в соответствии с разностной картой Фурье и уточняли без всяких ограничений. Молекулу толуола располагали в центре инверсии, занимающем центр кольца. Таким образом, это приводит в беспорядок местоположения метильных групп, занимающих параположения с 50%-ным коэффициентом заполнения позиций в кристаллической решетке для каждой. В конечном цикле уточнения было использовано 4206 наблюдаемых отражений с I>2σ(I) и полученные R1, wR2 и S (критерий согласия) составляли соответственно 3,59%, 8,38% и 1,023. Поправку на вторичную экстинкцию вносили с х= 0,0029(4). Максимальный и минимальный пики остаточной электронной плотности в окончательной разностной карте Фурье составляли 0,419 и -0,272 соответственно. Уточнение производили с использованием значений F2, а не F. R1 вычисляют со ссылкой на обычное значение R без минимизации (отыскания наименьшего значения) его функции. Кроме того, wR2 - это функции, которые минимизированы и не являются R1.
На фиг. 1 показана кристаллическая структура дихлор(N-(1,1-диметилэтил) -1,1-диметил-1- ( (1,2,3,3а,7a-η)-3-( 1-пиперидинил)-1Н-инден-1-ил)силанаминато(2-)-N)титана.
Рентгеновское определение структуры дихлор(N-(1,1-диметилэтил) -1,1-диметил-1- ( (1,2,3, 3а, 7a-η) -3-метокси-1H-инден-1-ил)силанаминато(2-)-N)титана.
СБОР ДАННЫХ
Темно-пурпурный брускообразный кристалл с размерами 0,30•0,21•0,09 мм погружали в масло (Paratone N. Exxon) и закрепляли на тонком стеклянном волокне. Переносили кристалл в дифрактометр SMART PLATFORM (Siemens), снабженный графитовым монохроматическим кристаллом, источником излучения МоКα 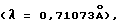 двухмерный детектор CCD (ПЗС - прибор с зарядовой связью), который держали на расстоянии 5,078 см от кристалла. На протяжении всего периода сбора данных кристалл омывали холодным потоком азота (-100oС). Три серии из 20 фреймов каждая собирали, охватив три перпендикулярных сектора пространства, с использованием метода ω-сканирования при времени экспозиции, равном десяти секундам. Интеграция фреймов с последующим индексированием отражений и уточнением по наименьшим квадратам дали ориентационную матрицу и моноклинную решетку кристалла.
двухмерный детектор CCD (ПЗС - прибор с зарядовой связью), который держали на расстоянии 5,078 см от кристалла. На протяжении всего периода сбора данных кристалл омывали холодным потоком азота (-100oС). Три серии из 20 фреймов каждая собирали, охватив три перпендикулярных сектора пространства, с использованием метода ω-сканирования при времени экспозиции, равном десяти секундам. Интеграция фреймов с последующим индексированием отражений и уточнением по наименьшим квадратам дали ориентационную матрицу и моноклинную решетку кристалла.
Сбор данных обеспечил сбор всего 1381 фреймов в четырех различных опытах, охвативших более одной полной полусферы данных. Параметры сканирования фреймов сведены в табл. 4.
Последний опыт ( 4) представляет собой повторное измерение первых 50 фреймов из опыта 1. Это сделано для контроля стабильности кристалла и дифрактометра и внесения поправки на какой-либо распад кристалла.
В состав дифрактометра входит 0,8-миллиметровый коллиматор, дающий рентгеновский пучок диаметром 0,8 мм. Мощность генератора была установлена на уровне 50 кВ и 30 мА. Для управления дифрактометром, фреймового сканирования, индексирования, вычислений ориентационной матрицы, уточнения по наименьшим квадратам параметров ячеек, измерений граней кристалла и сбора фактических данных использовали программу SMART. Для создания методики сбора данных использовали программу ASTRO.
ПОДГОТОВКА ДАННЫХ
Все 1381 кристаллографические фреймы необработанных данных читали с помощью программы SAINT и интегрировали, пользуясь 3D алгоритмами профилирования. Полученные данные предварительно преобразовывали для получения отражений типа hkl и их интенсивностей и определяли среднеквадратичное отклонение. Данные корректировали, вводя поправку на эффект Лоренца и поляризационный эффект. Было собрано всего 24545 отображений, представляющих диапазон уровня резервирования 2,59-3,76 и имеющих значение Rsym в пределах от 4,5% (оболочка отражений при наименьшем угле 2θ) до 6,0% (оболочка отражений при наибольшем угле 2θ (55o)). Вводили поправку на распад кристалла, которая составляла менее 1%. Параметры элементарной ячейки уточняли методом наименьших квадратов установочных углов 6109 отражений. Параметры элементарной ячейки представляют собой: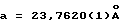 α=90o
α=90o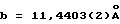 β=108,929(I)o
β=108,929(I)o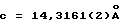 γ=90o
γ=90o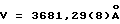 3
3
Вводили поправки на абсорбцию, пользуясь программой SADABS по Блессингу. Коэффициент поглощения составлял 0,821 мм-1, а минимальный и максимальный коэффициенты пропускания составляли 0,755 и 0,942 соответственно.
Подготовку данных осуществляли с использованием программ XPREP. Пространственная группа была определена на основе систематических отсутствий как С2/с (# 15). XPREP дала следующие кристаллографические параметры: 4203 уникальных отражений (Rint=3,06%) с индексами -31≤h≤30, -15≤k≤8, -18≤l≤19.
РЕШЕНИЕ И УТОЧНЕНИЕ СТРУКТУРЫ
Структуру решали непосредственными методами в SHELXTL5, посредством которых были получены положения всех неводородных атомов. Структуру уточняли также с использованием SHELXTL5 согласно полноматричному уточнению методом наименьших квадратов. Неводородные атомы уточняли с использованием анизотропных термических параметров и все водородные атомы располагали в соответствии с разностной картой Фурье и уточняли без всяких ограничений. В конечном цикле уточнения было использовано 3333 наблюдаемых отражений с I>2σ(I) для уточнения 292 параметров и полученные R1, wR2 и S (критерий согласия) составляли соответственно 3,00%, 6,93% и 1,026. Поправку на вторичную экстинкцию вносили с х=0,00037(9). Максимальный и минимальный пики остаточной электронной плотности в окончательной разностной карте Фурье составляли 0,342 и -0,295 соответственно. Уточнение производили с использованием значений F2, а не F. R1 вычисляют со ссылкой на обычное значение R без минимизации (отыскания наименьшего значения) его функции. Кроме того, wR2 - это функции, которые минимизированы и не являются R1.
На фиг. 2 показана кристаллическая структура дихлор(N-(1,1-диметилэтил) -1,1-диметил-1- ((1, 2, 3, 3а, 7а-η) -3-метокси-1Н-инден-1-ил)силанаминато(2-)-N)титана.
Рентгеновское определение структуры [N-(1,1-диметилэтил) -1,1-диметил-1- ( (1, 2, 3, 3а, 7a-η) -3- (1-пиперидинил) -1Н-инден-1-ил) силанаминато (2-)-N] [2,3,4,5-η)-2, 4-гексадиен) ] -титана.
СБОР ДАННЫХ
Темно-пурпурный брускообразный кристалл с размерами 0,28•0,24•0,21 мм погружали в масло (Paratone N. Exxon) и закрепляли на тонком стеклянном волокне. Переносили кристалл в дифрактометр SMART PLATFORM (Siemens), снабженный графитовым монохроматическим кристаллом, источником излучения МоКα 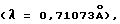 двухмерный детектор CCD (ПЗС - прибор с зарядовой связью), который держали на расстоянии 4,931 см от кристалла. На протяжении всего периода сбора данных кристалл омывали холодным потоком азота (-100oС). Три серии из 20 фреймов каждая собирали, охватив три перпендикулярных сектора пространства, с использованием метода ω-сканирования при времени экспозиции, равном десяти секундам. Интеграция фреймов с последующим индексированием отражений и уточнением по наименьшим квадратам дали ориентационную матрицу и моноклинную решетку кристалла.
двухмерный детектор CCD (ПЗС - прибор с зарядовой связью), который держали на расстоянии 4,931 см от кристалла. На протяжении всего периода сбора данных кристалл омывали холодным потоком азота (-100oС). Три серии из 20 фреймов каждая собирали, охватив три перпендикулярных сектора пространства, с использованием метода ω-сканирования при времени экспозиции, равном десяти секундам. Интеграция фреймов с последующим индексированием отражений и уточнением по наименьшим квадратам дали ориентационную матрицу и моноклинную решетку кристалла.
Сбор данных обеспечил сбор всего 1381 фреймов в четырех различных опытах, охвативших более одной полной полусферы данных. Параметры сканирования фреймов сведены в табл. 5.
Последний опыт ( 4) представляет собой повторное измерение первых 50 фреймов из опыта 1. Это сделано для контроля стабильности кристалла и дифрактометра и внесения поправки на какой-либо распад кристалла.
В состав дифрактометра входит 0,8-миллиметровый коллиматор, дающий рентгеновский пучок диаметром 0,8 мм. Мощность генератора была установлена на уровне 50 кВ и 30 мА. Для управления дифрактометром, фреймового сканирования, индексирования, вычислений ориентационной матрицы, уточнения по наименьшим квадратам параметров ячеек, измерений граней кристалла и сбора фактических данных использовали программу SMART1. Для создания методики сбора данных использовали программу ASTRO.
ПОДГОТОВКА ДАННЫХ
Все 1381 кристаллографические фреймы необработанных данных читали с помощью программы SAINT и интегрировали, пользуясь 3D алгоритмами профилирования. Полученные данные предварительно преобразовывали для получения отражений типа hkl и их интенсивностей и определяли среднеквадратичное отклонение. Данные корректировали, вводя поправку на эффект Лоренца и поляризационный эффект. Было собрано всего 8673 отображения, представляющих диапазон уровня резервирования 1,48-2,18 и имеющих значение Rsym в пределах от 2,5% (оболочка отражений при наименьшем угле 2θ) до 2,6% (оболочка отражений при наибольшем угле 2θ (55o)). Вводили поправку на распад кристалла, которая составляла менее 1%. Параметры элементарной ячейки уточняли методом наименьших квадратов установочных углов 6908 отражений. Параметры элементарной ячейки представляют собой: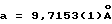 α=86,327(I)o
α=86,327(I)o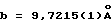 β=89,217(I)o
β=89,217(I)o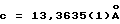 γ=82,840(I)o
γ=82,840(I)o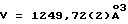
Вводили поправки на абсорбцию, пользуясь программой SADABS по Блессингу. Коэффициент поглощения составлял 0,405 мм-1, а минимальный и максимальный коэффициенты пропускания составляли 0,805 и 0,928 соответственно.
Подготовку данных осуществляли с использованием программы XPREP. Пространственная группа была определена на основе систематических отсутствий как PI (# 2). XPREP дала следующие кристаллографические параметры: 5563 уникальных отражений (Rint=1,59%) с индексами -12≤h≤10, -12≤k≤13, -15≤l≤18.
РЕШЕНИЕ И УТОЧНЕНИЕ СТРУКТУРЫ
Структуру решали непосредственными методами в SHELXTL5, посредством которых были получены положения всех неводородных атомов. Структуру уточняли также с использованием SHELXTL5 согласно полноматричному уточнению методом наименьших квадратов. Неводородные атомы уточняли с использованием анизотропных термических параметров и все водородные атомы располагали в соответствии с разностной картой Фурье и уточняли без всяких ограничений. В конечном цикле уточнения было использовано 4838 наблюдаемых отражений с I>2σ(I) для уточнения 432 параметров и полученные R1, wR2 и S (критерий согласия) составляли соответственно 3,13%, 7,17% и 1,023. Поправку на вторичную экстинкцию вносили с х=0,0018(7). Максимальный и минимальный пики остаточной электронной плотности в окончательной разностной карте Фурье составляли 0,324 и -0,368 соответственно. Уточнение производили с использованием значений F2, а не F. R1 вычисляют со ссылкой на обычное значение R без минимизации (отыскания наименьшего значения) его функции. Кроме того, wR2 - это функции, которые минимизированы и не являются R1.
Коэффициент линейной абсорбции, атомные факторы рассеяния и поправки на аномальную дисперсию вычисляли по значениям из Международных таблиц для рентгеновской кристаллографии (International Tables for X-ray Crystallography (1974), том IV, стр. 55, Birmingham, Kynoch Press; теперешний дистрибьютор: D. Reidel, Dordrecht.).
На фиг. 3 показана кристаллическая структура [N-(1,1-диметилэтил) -1,1-диметил-1- ( (1,2,3,3а,7а-η)-3-(1-пиперидинил) -1Н-инден-1-ил) силанаминато (2-)-N] [2,3,4,5-η)-2,4-гексадиен)]титана.
Ниже даны соответствующие функции, использованные для описанных выше определений структур.
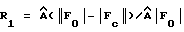
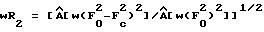
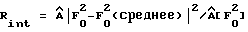
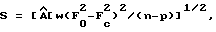
где n представляет число отражений и р представляет общее число уточненных параметров
w=1/[s2(F0 2)+(0,0370•p)2+0,31•p], р=[max(F0 2.0)+2•Fc 2]/3
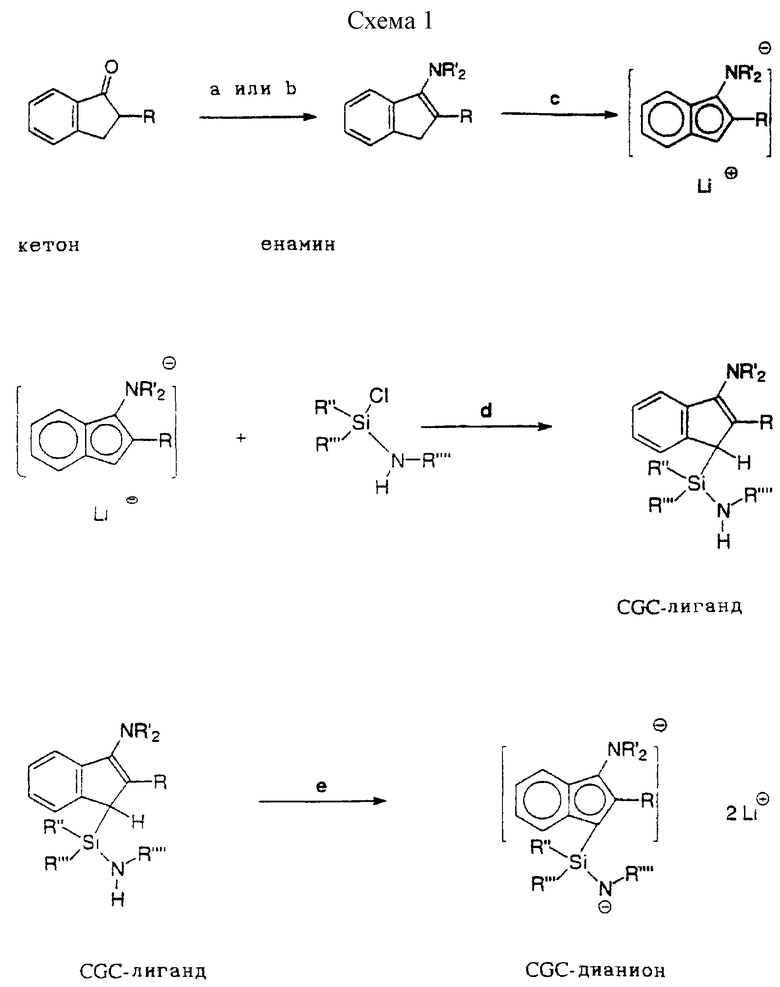
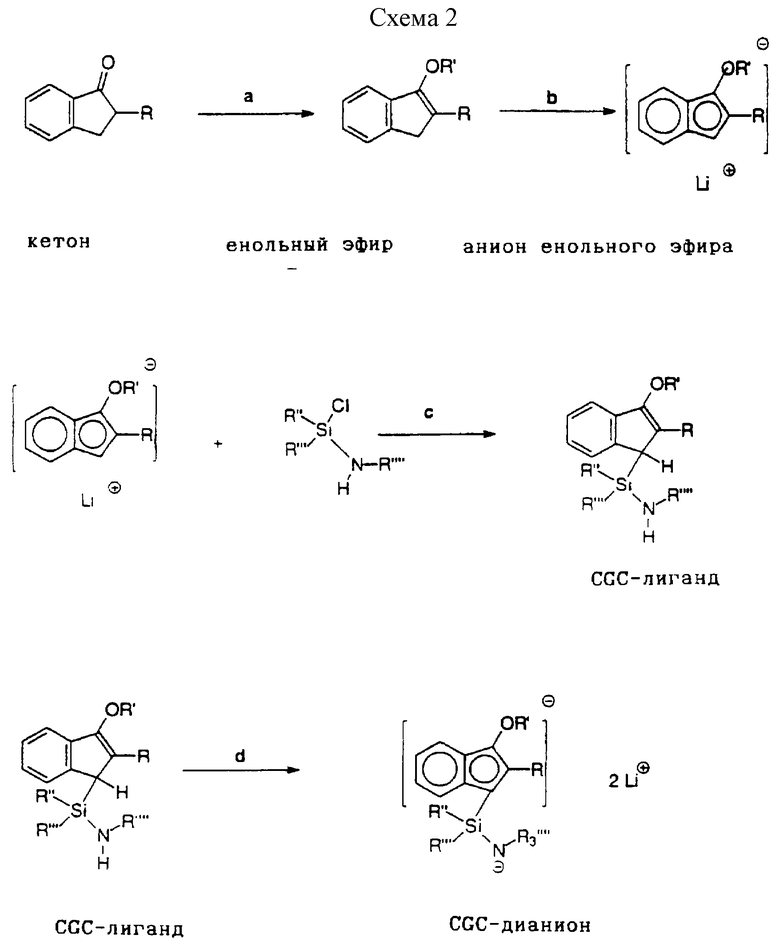
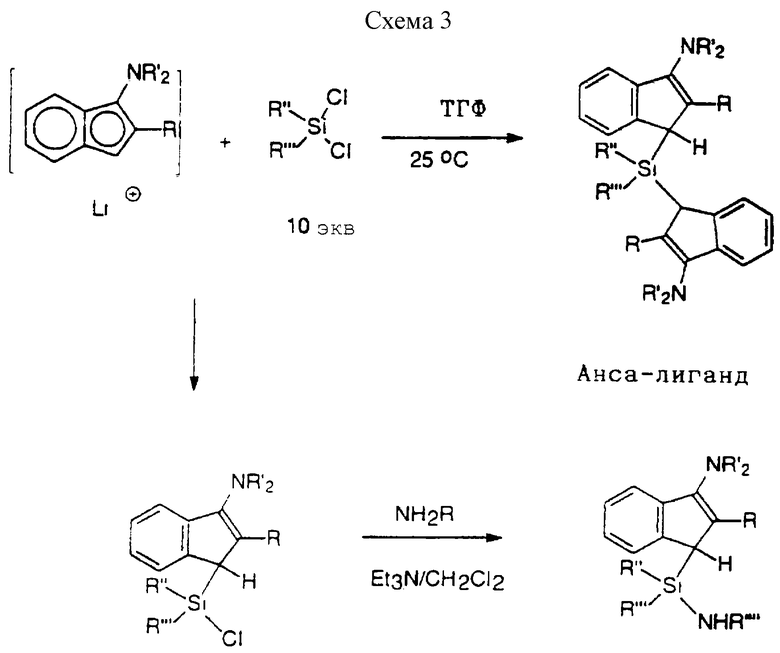

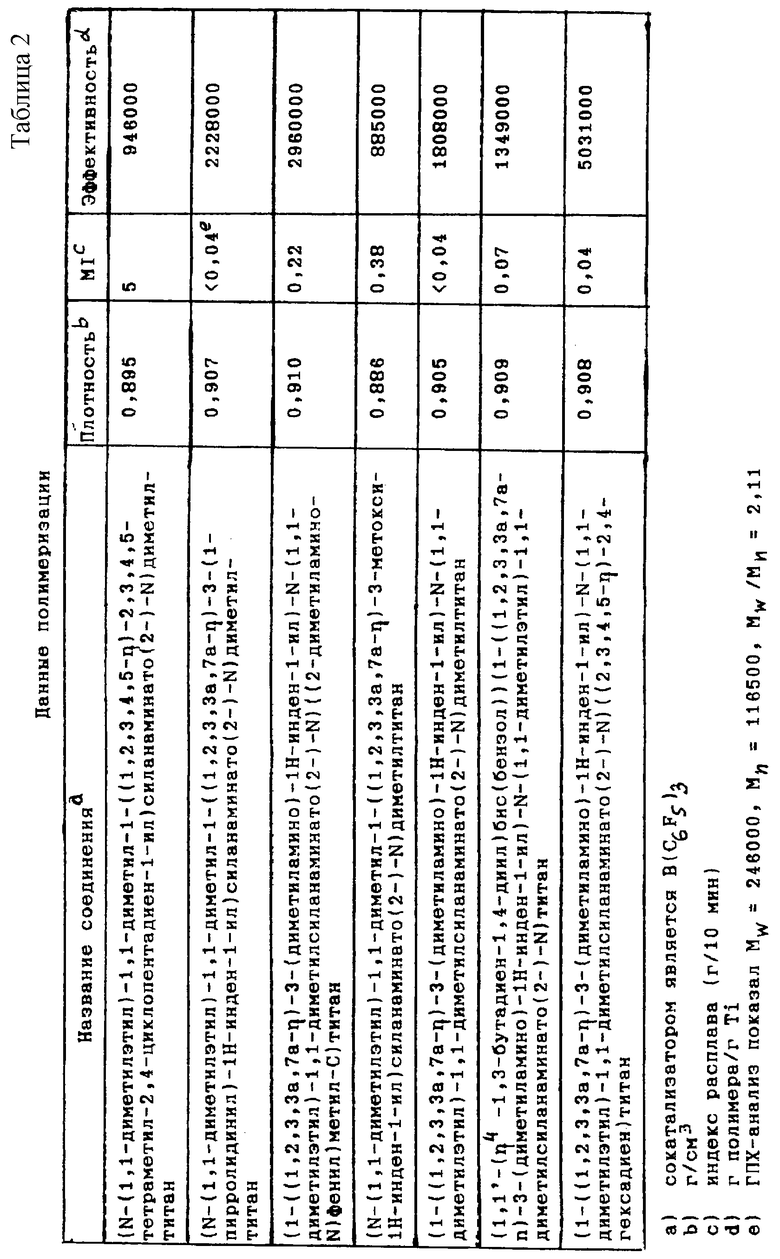
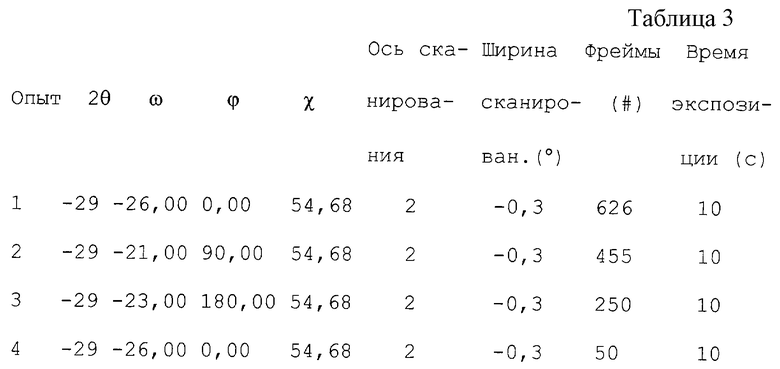
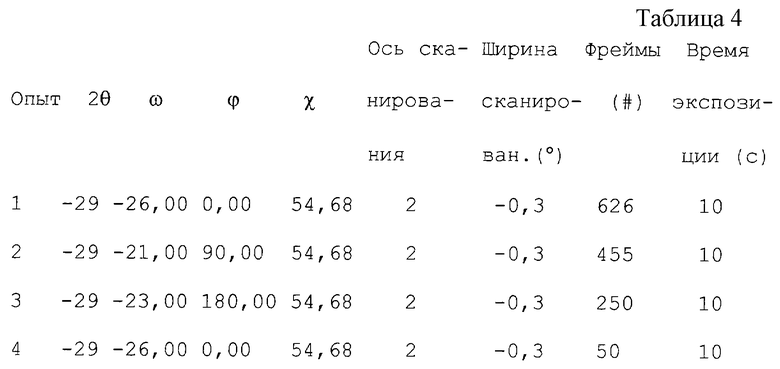
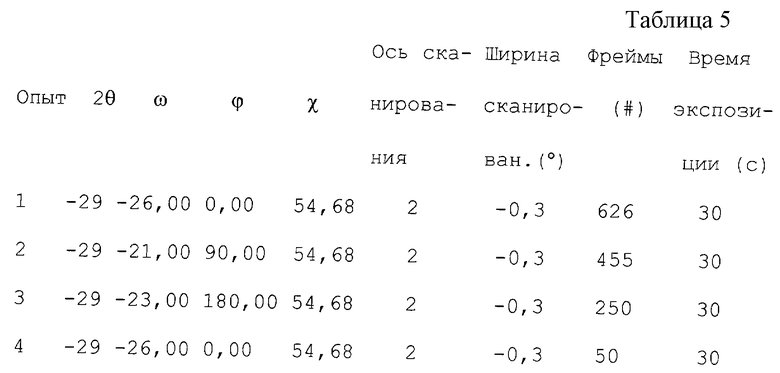
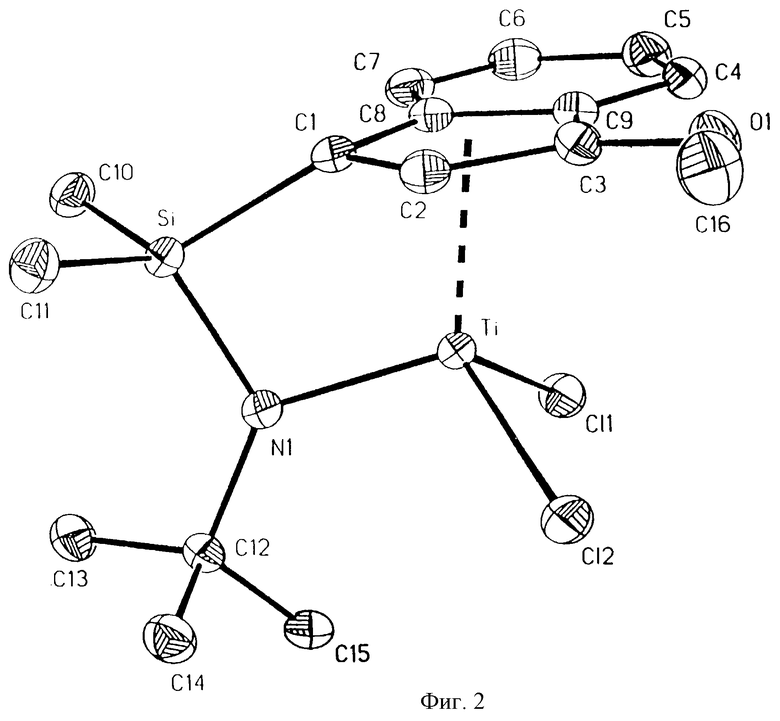
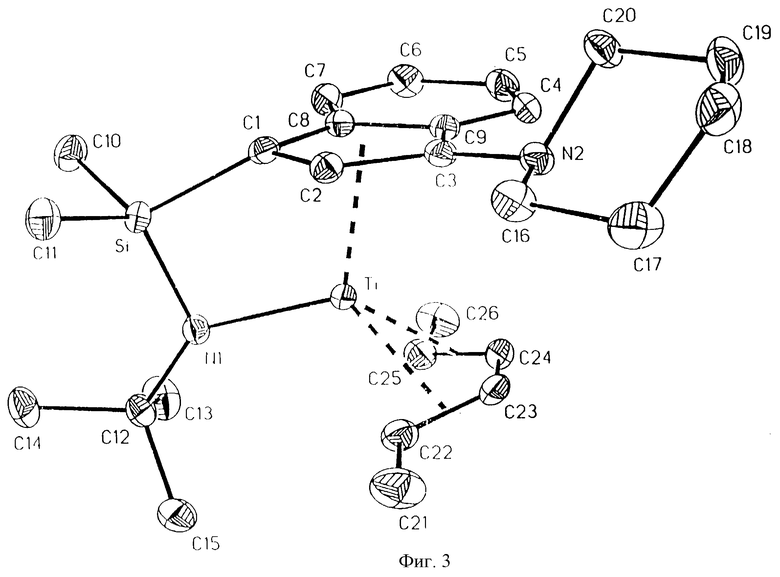
Описывается металлокомплекс, соответствующий формулам I и II, где М означает Ti, Zr или Hf; RA означает водород или низший алкил; RВ в каждом случае независимо означает метил или фенил; или, необязательно, обе группы RВ вместе с атомом N образуют 5-6-членное гетероциклическое кольцо; RX и RY означают независимо водород, или RX и RY ковалентно связаны друг с другом с образованием конденсированного кольца, необязательно, замещенного низшими алкильными группами; R* означает низший алкил или циклоалкил; Х независимо в каждом случае означает низший алкил, низший циклоалкилдиенил или бензил, возможно замещенный ди(низший)алкиламиногруппой; X' означает сопряженный диен с возможно концевым замещением фенильными радикалами, и способ полимеризации олефинов в присутствии каталитической системы, которая содержит указанный выше металлокомплекс. 2 с. и 7 з.п. ф-лы, 3 ил., 5 табл.
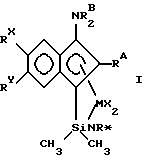
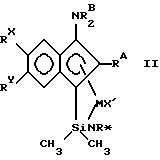
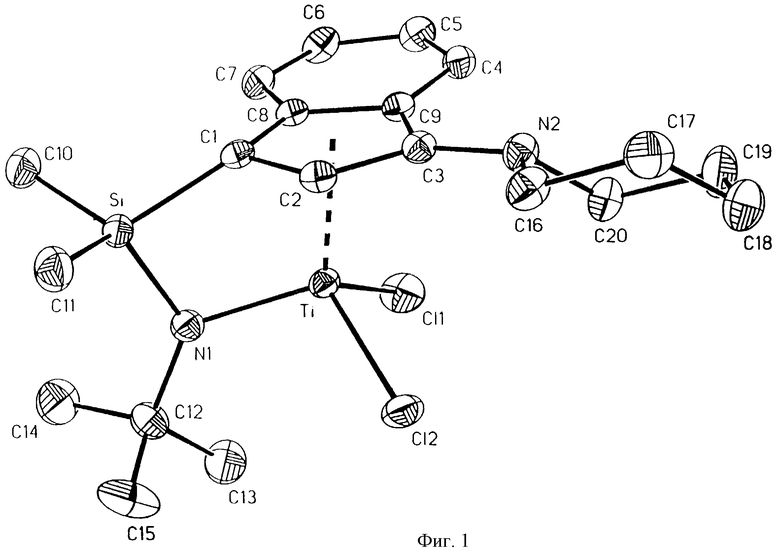
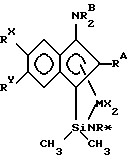
или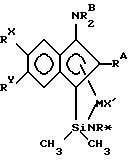
где М означает Ti, Zr или Hf;
RA означает водород или низший алкил;
RВ в каждом случае независимо означает метил или фенил; или, необязательно, обе группы RВ вместе с атомом N образуют 5-6 членное гетероциклическое кольцо;
RX и RY означают независимо водород, или RX и RY ковалентно связаны друг с другом с образованием конденсированного кольца, необязательно, замещенного низшими алкильными группами;
R* означает низший алкил или циклоалкил;
Х независимо в каждом случае означает низший алкил, низший циклоалкилдиенил или бензил, возможно замещенный ди(низший)алкиламиногруппой;
X' означает С4-6 сопряженный диен, с возможно концевым замещением фенильными радикалами.
(трет-бутиламидо)(3-(N-диметиламино)инден-1-ил)(диметилсилан)титан дихлорид;
(трет-бутиламидо)(3-(N-диметиламино)инден-1-ил)(диметилсилан)титан диметил;
(трет-бутиламидо)(3-(N-диметиламино)-5,6,7,8-тетрагидро-2,5,5,8,8-пентаметил-1Н-бенз(f)инден-1-ил)(диметилсилан)титан дихлорид;
(тpeт-бyтилaмидo)(3-(N-димeтилaминo)-5,6,7,8-тетрагидро-2,5,5,8,8-пентаметил-1Н-бенз(f)инден-1-ил)(диметилсилан)титан диметил;
(трет-бутиламидо)(2-метил-3-(1-пирролидино)-(1,2,3,3а, 8a-η)-1,5,6,7-тетрагидро-s-индацен-1-ил)(диметилсилан)титан дихлорид;
(трет-бутиламидо)(2-метил-3-(1-пирролидино)-(1,2,3,3а, 8а-η)-1,5,6,7-тетрагидро-s-индацен-1-ил)(диметилсилан)титан диметил;
(трет-бутиламидо)(3-(N-пиперидинил)-1Н-инден-1-ил)(диметилсилан)титан дихлорид;
(трет-бутиламидо)(3-(N-пиперидинил)-1Н-инден-1-ил)(диметилсилан)титан диметил;
(трет-бутиламидо)(3-(N-пиперидинил)-1Н-инден-1-ил)(диметилсилан)титан 2,4-гексадиен;
(тpeт-бyтилaмидo)(3-(N-пиppoлидинил)-1H-индeн-1-ил)(димeтилcилaн)титaн дихлорид;
(трет-бутиламидо)(3-(N-пирролидинил)-1Н-инден-1-ил)(диметилсилан)титан диметил;
(трет-бутиламидо)(3-(N-пирролидинил)-1Н-инден-1-ил)(диметилсилан)титан 1,3-пентадиен;
(трет-бутиламидо)(3-(N-пирролидинил)-1Н-инден-1-ил)(диметилсилан)цирконий дихлорид;
(трет-бутиламидо)(3-(N-пирролидинил)-1Н-инден-1-ил)(диметилсилан)цирконий диметил;
(трет-бутиламидо)(2-метил-3-(N-пирролидинил)-1Н-инден-1-ил)(диметилсилан)титан дихлорид;
(трет-бутиламидо)(2-метил-3-(N-пирролидинил)-1Н-инден-1-ил)(диметилсилан)титан диметил;
(циклoгeкcилaмидo)(3-(N-пиppoлидинил)-1H-индeн-1-ил)димeтилcилaн)титaн дихлорид;
(циклогексиламидо)(3-(N-пирролидинил)-1Н-инден-1-ил)(диметилсилан)титан диметил;
(трет-бутиламидо)(3-(N, N-диметиламино)-1Н-инден-1-ил)(диметилсилан)титан диметил;
(трет-бутиламидо)(3-(N, N-диметиламино)-1Н-инден-1-ил)(диметилсилан)титан 2,4-гексадиен;
(тpeт-бyтилaмидo)(3-(N, N-диметиламино)-1Н-инден-1-ил)(диметилсилан)титан 1,4-дифенилбутадиен;
(η5-циклопентадиенил)[(трет-бутиламидо)(3-(N, N-диметиламино)-1Н-инден-1-ил)(диметилсилан)] титан циклопентадиенил хлорид;
(η5-циклопентадиенил)[(трет-бутиламидо)(3-(N-пирролидинил)-1Н-инден-1-ил)(диметилсилан)] титан (III)(циклопентадиенил);
(η5-циклопентадиенил)[(трет-бутиламидо)(3-(N-пирролидинил)-1Н-инден-1-ил)(диметилсилан)] титан(циклопентадиенил)хлорид;
(трет-бутиламидо)(3-(N-пирролидинил)-1Н-инден-1-ил)(диметилсилан)титан(III)2-(N, N-диметиламино)бензил;
(трет-бутиламидо)(3-(N-пирролидинил)-1H-инден-1-ил)(диметилсилан)титан 2-(N, N-диметиламино)бензил хлорид;
(трет-бутиламидо)(3-(N-фенил-N-метиламино)-1Н-инден-1-ил)(диметилсилан)титан дихлорид;
(тpeт-бyтилaмидo)(3-(N-фeнил-N-мeтилaминo)-1H-индeн-1-ил)(димeтилcилaн)титaн диметил;
(бензиламидо)(3-(N-пирролидинил)-1Н-инден-1-ил)(диметилсилан)титан дихлорид;
или
(бензиламидо)(3-(N-пирролидинил)-1Н-инден-1-ил)(диметилсилан)титан диметил.
| Платформа подъемника | 1974 |
|
SU582195A2 |
| Катализатор для паровой конверсии углеводородного газа | 1975 |
|
SU670325A1 |
| RU 94043773 A1, 27.10.1996 | |||
| RU 94045143 A1, 27.10.1996. | |||
Авторы
Даты
2003-01-20—Публикация
1997-07-28—Подача