Изобретение относится к области органического синтеза, а именно к способу получения 5,51-(oкcиди)пeнтaнoнa-2 (1).
Указанное соединение представляет собой интерес в качестве полифункционального растворителя, экстрагента, как душистое вещество пряного запаха и как исходное сырье для синтеза гетероциклов.
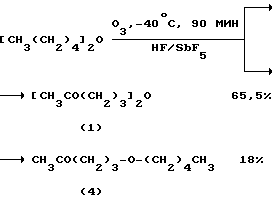
Известен способ получения 5,51-(oкcиди)пeнтaнoнa-2 окислением диамилового эфира (2) озоном катализируемый сверхкислотой НF/SbF5 (N. Yneda, T. Kinchi, T. Fukuhara, A. Suzuke, G. Olah "Chem. Lett", 1984, N 9, 1617-1618) [1].
В качестве исходного реагента для синтеза (1) используют диамиловый эфир, который получают этерификацией амилового спирта (3) в присутствии концентрированной серной кислоты. Амиловый спирт (1 моль) смешивают с серной кислотой (0,1 моль 95,7% Н2SО4), кипятят 7 часов, собирая воду в водоотделителе, дистиллат отгоняют с водяным паром, сушат и фракционируют. Выход эфира (2) 67% (И. Губен. Методы органической химии, т. 3, вып. 1, 1934, 165) [2].
Для окисления диамилового эфира в 5,51-(oкcиди)пeнтaнoн-2 через раствор (2) в HF/SbF5 (мольное соотношение SbF5/2=10) при -40oС в течение 90 мин пропускают поток кислорода, содержащий 2,5% озона. Выход (1) составляет 65,5%. Кроме (1) в реакционной массе содержится продукт неполного окисления эфира (2) пентил-5-оксопентиловый эфир (4) 18%.
Способ имеет существенные недостатки.
В качестве катализатора при получении (2) используется концентрированная серная кислота, а при синтезе (1) - очень агрессивный реагент HF/SbF5, что требует применения специального оборудования (Справочник сернокислотчика. М. : Химия, 1971, 157) [3].
Необходимость проведения реакции при -40oС создает дополнительные сложности в аппаратурном оформлении процесса.
Окисление (2) осуществляется озонированием (2,5% озона в кислороде), что обуславливает высокую пожаро- и взрывоопасность опыта.
Способ экологически опасен, так как реагенты HF и SbF5 являются весьма токсичными веществами с низкими значениями ПДК (ПДК HF=1,0 мг/м3, SbF5=0,3 мг/м3). (Вредные вещества в промышленности. Справочник. Л.: Химия, 1972, 28 [4], ГОСТ 121005-76) [5].
Необходимость применения больших количеств серной кислоты (мольное соотношение [3]:[95,7% H2SО4]=1:0,1) и десятикратного избытка HF/SbF5 создает проблему утилизации значительных объемов ядовитых отходов [3].
Авторами предлагается новый одностадийный каталитический метод получения 5,51-(оксиди)пентанона-2 (1). Сущность метода заключается в следующем: под действием солей меди происходит региоселективное раскрытие трехуглеродного цикла ацетилциклопропана (5) водой с последующим образованием (1).
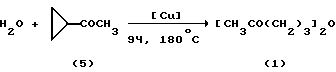
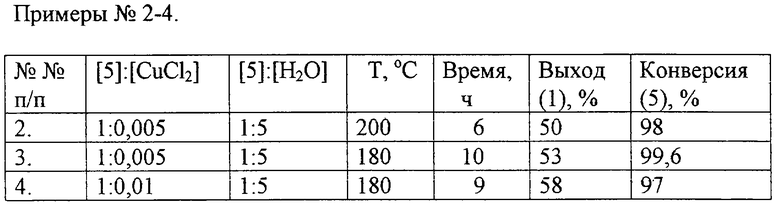
В качестве катализатора высокую активность проявляют следующие соединения меди: хлорид меди (II) CuCl2•2H2O и бромид меди (II) CuBr2 (см. таблицу).
Реакцию предпочтительно проводить в среде диэтилового эфира, взятого в мольном соотношении [3-5]:1 по отношению к (5).
Определены оптимальные мольные соотношения реагентов:
[5] :[катализатор]:[Н20]=1:[0,005-0,01]:5. Высокий выход целевого продукта достигается при температуре 180-200oС и продолжительности реакции от 6 до 10 часов (таблица).
Предлагаемый метод имеет следующие преимущества:
1. Легкодоступное исходное сырье.
2. Простота аппаратурного оформления.
3. Низкий расход катализатора и его дешевизна.
4. Отсутствие токсичных, экологически опасных отходов производства.
5. Высокая селективность реакции.
Способ поясняется примерами 1-4.
ПРИМЕР 1. Получение 5,51-(оксиди)пентанона-2 (1). В микроавтоклав емкостью 17 см3 поместили 0,46 г (5,5 ммоля) ацетилциклопропана, 0,5 г (28 ммолей) воды, 0,011 г (0,05 ммоля) СuВr2, 1,42 г (19 ммолей) диэтилового эфира. Герметично закрытый автоклав нагревали при 180oС в течение 9 ч. Реакционную массу после отгона диэтилового эфира перегоняли в вакууме. Выделено 0,32 г 5,5'-(оксиди)пентанона-2, выход 64%. Вычислено, %: С=64.50, Н=9.76 С10Н18О3. Найдено, %: С=64.59, Н=9.80.
5,51-(Окcиди)пeнтaнoн-2 (1) идентифицирован спектральными методами анализа. ЯМР 1Н зарегистрирован в CDCl3 на спектрометре "Tesla BS-567" (100 МГц, стандарт ТМС) и содержит следующие сигналы (δ): 1.72 (4Н, т), 2.05 (6Н, с), 2.41 (4Н, т), 3.29 (4Н, т), указанный спектр идентичен приведенному в литературе [1] 1.75 (4Н, м), 2.09 (6Н, с), 2.41 (4Н, т), 3.33 (4Н, т).
Спектр ЯМР 13С зарегистрирован в CDCl3 на спектрометре "JEOL FX 90G" (22.5 МГц) и по совокупности химсдвигов соответствует предложенной структуре: 29.95 (СН3), 208.59 (СО), 40.36 (СOCH2), 23.94 (СН2), 69.97 (CH2O).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 5-АЛКОКСИПЕНТАНОНОВ-2 | 1999 |
|
RU2171797C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОРАДАМАНТАНОНА-4 | 2000 |
|
RU2197468C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОРАДАМАНТАНА, 1- И 4-ХЛОРДИАМАНТАНОВ | 2000 |
|
RU2185364C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕКСАХЛОРЭТАНА | 2001 |
|
RU2185365C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3,5-ДИМЕТИЛ-2-ЭТИЛПИРИДИНА | 2001 |
|
RU2200156C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОР-3-АЦЕТИЛ- И 1,3-ДИХЛОР-5-АЦЕТИЛАДАМАНТАНОВ | 2000 |
|
RU2197467C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3-ДИХЛОРАДАМАНТАНА | 2000 |
|
RU2178401C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИЗОПРЕНОИДНЫХ ПРОИЗВОДНЫХ 2,3,5-ТРИМЕТИЛ-1,4-БЕНЗОХИНОНА | 2000 |
|
RU2197469C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АДАМАНТИЛАЛКИЛОВЫХ ЭФИРОВ | 1998 |
|
RU2145593C1 |
| КАТАЛИЗАТОР ДЛЯ ГИДРОХЛОРИРОВАНИЯ НЕНАСЫЩЕННЫХ СОЕДИНЕНИЙ | 1997 |
|
RU2151640C1 |
Изобретение относится к способу получения 5,5'-(оксиди)пентанона-2, который может быть использован в качестве полифункционального растворителя, экстрагента, как душистое вещество и как исходное сырье для синтеза гетероциклов. Способ заключается во взаимодействии ацетилциклопропана с водой в присутствии медьсодержащего катализатора: хлорида меди II - CuCl2•H2O или бромида меди (II) CuBr2 в мольном соотношении ацетилциклопропан : катализатор : вода, равном 1 : [0,005-0,01] : 5, при температуре 180-200oС в течение 6-10 ч, в среде диэтилового эфира. Продукт получают с выходом 50-64%. 1 табл.
Способ получения 5,5'-(оксиди)пентанона-2, отличающийся тем, что ацетилциклопропан взаимодействует с водой в присутствии медьсодержащего катализатора: хлорида меди (II) CuCl2•H2O или бромида меди (II) СuВr2 в мольном соотношении ацетилциклопропан: катализатор: вода, равном 1: (0,005-0,01): 5, при температуре 180-200oС, в течение 6-10 ч, в среде диэтилового эфира.
| Chem | |||
| Lett | |||
| Колосниковая решетка с чередующимися неподвижными и движущимися возвратно-поступательно колосниками | 1917 |
|
SU1984A1 |
| N | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Способ восстановления хромовой кислоты в сернокислую окись хрома | 1922 |
|
SU1617A1 |
| US 1083546 А, 10.08.2000. | |||
Авторы
Даты
2003-01-27—Публикация
2000-06-02—Подача