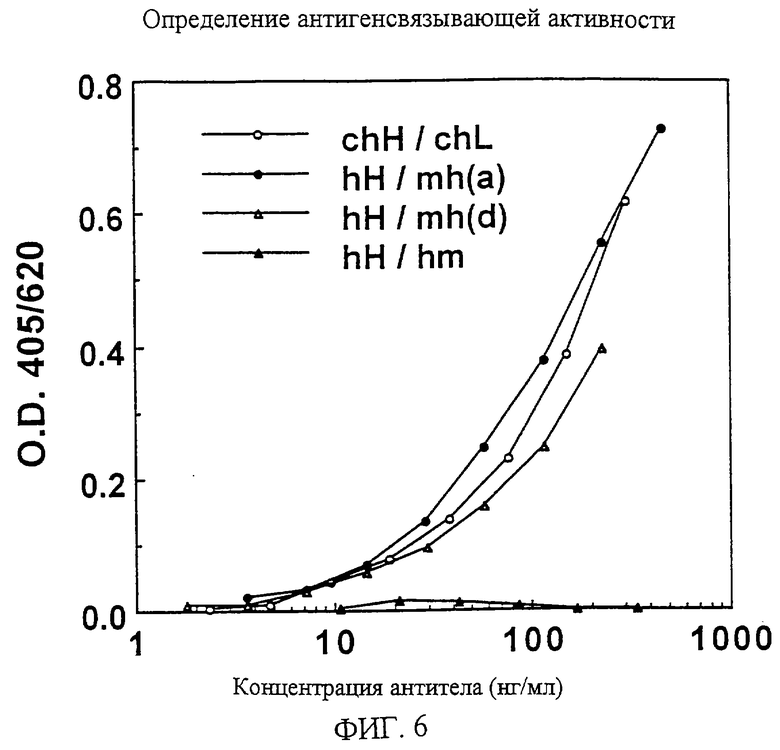
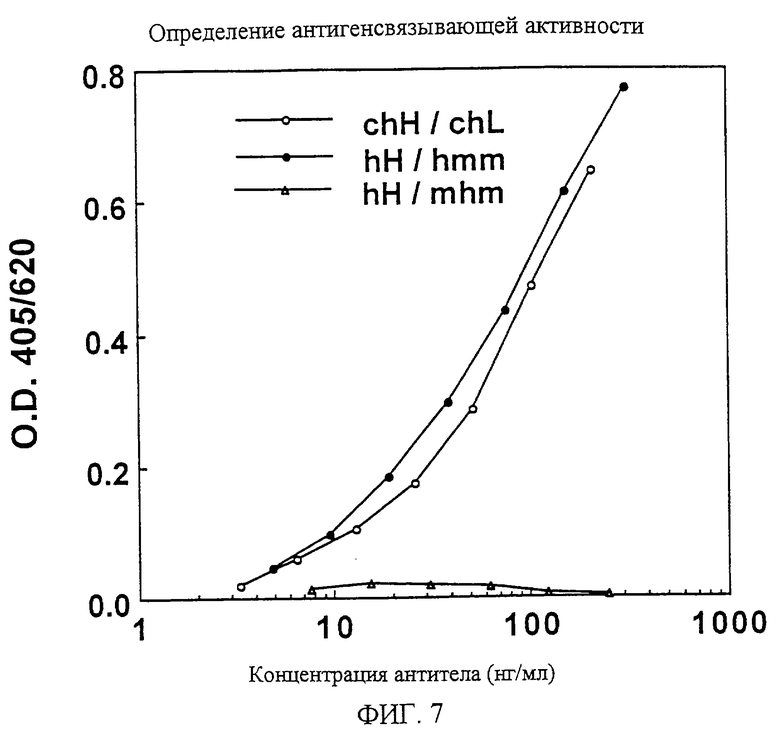
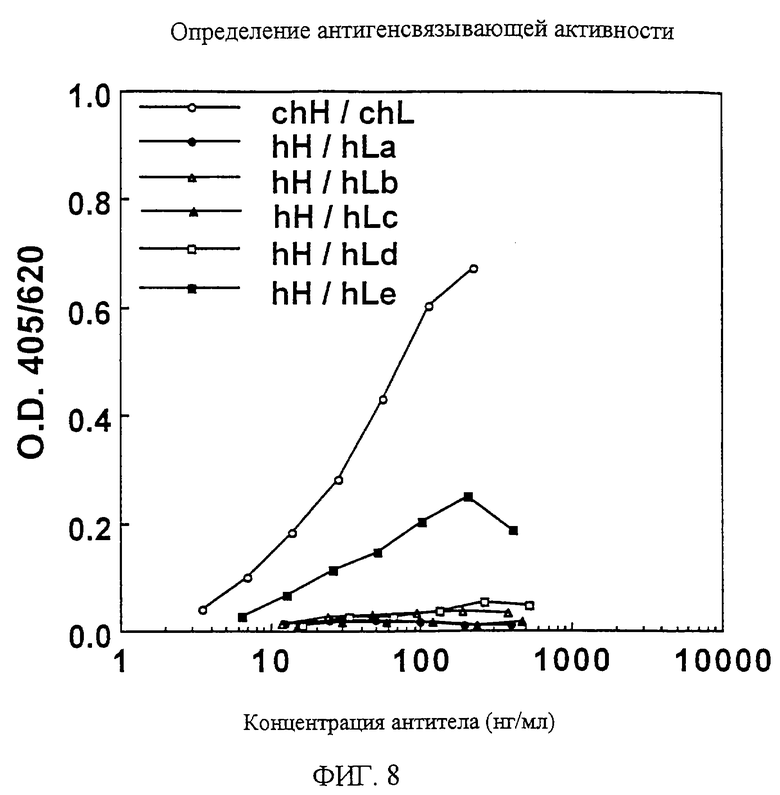
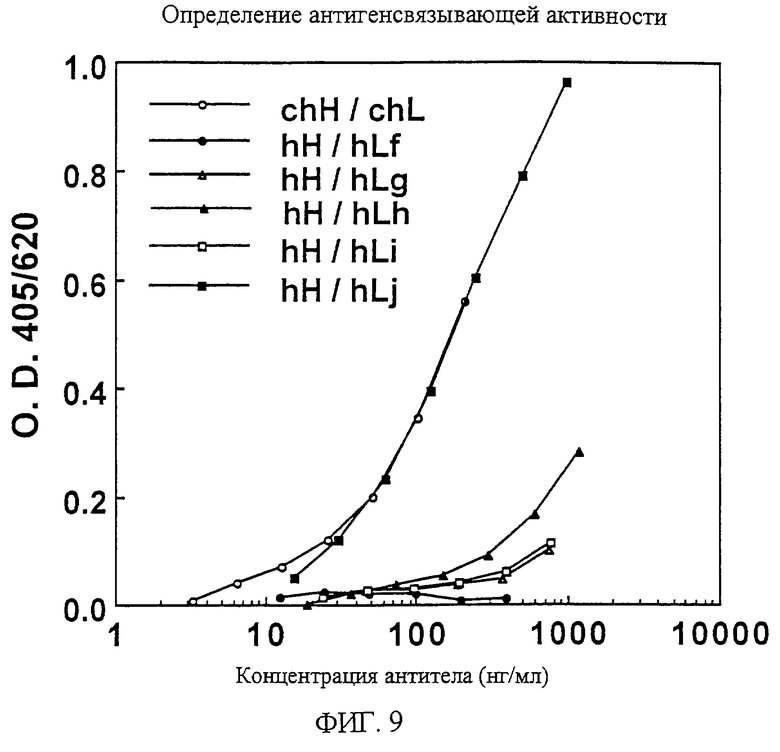
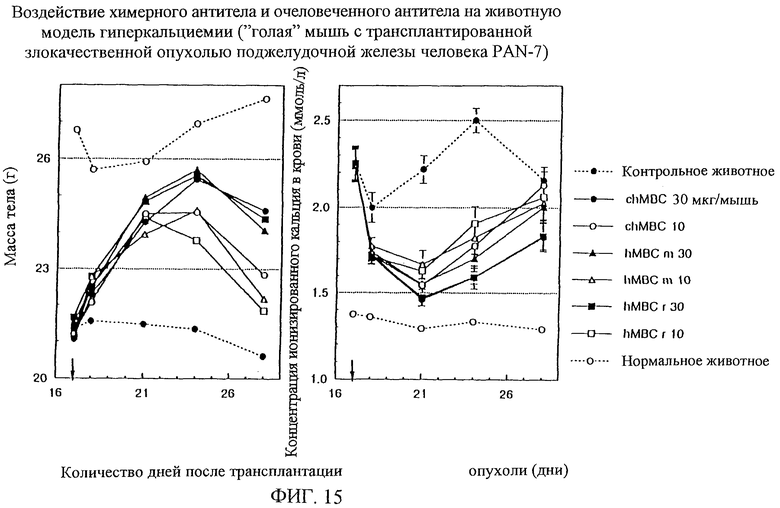
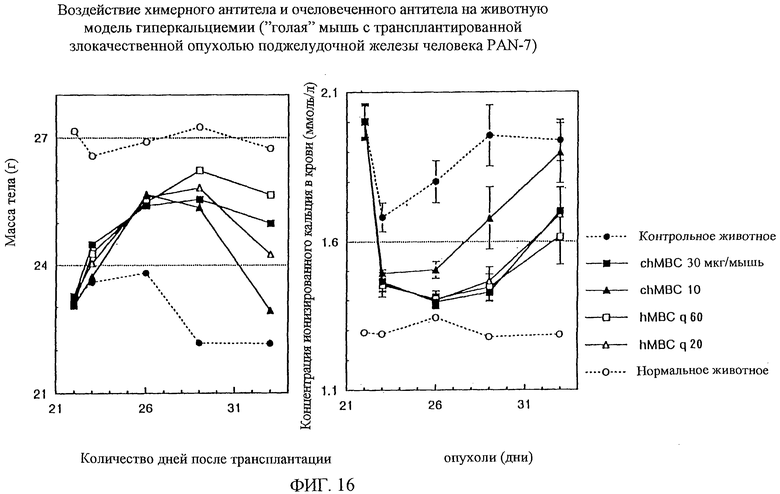
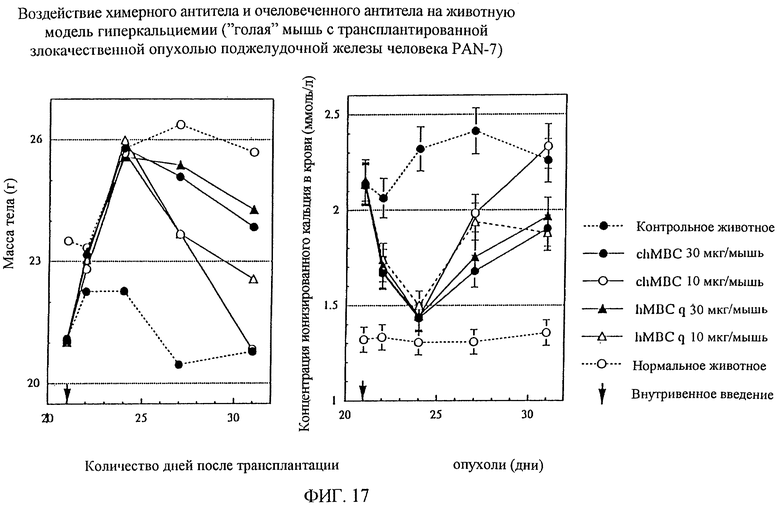
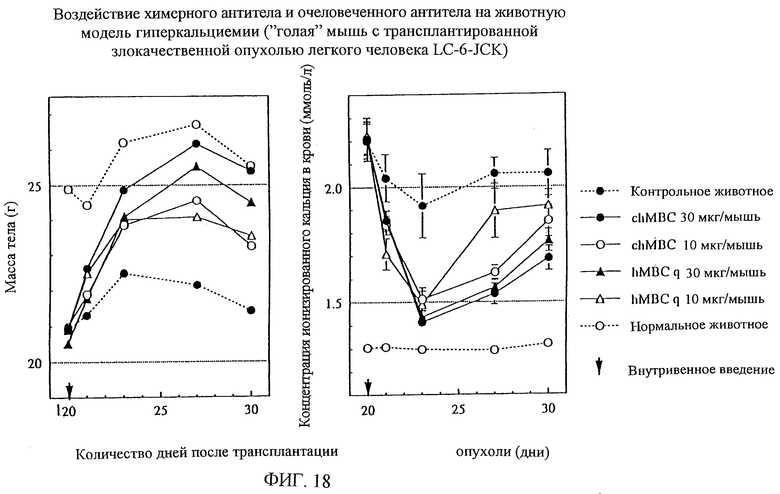
1. Химерная L-цепь, включающая С-область L-цепи антитела человека и V-область L-цепи моноклонального антитела мыши против белка, родственного паращитовидному гормону человека, в которой V-область L-цепи включает аминокислотную последовательность, показанную в SEQ ID NO:45. 2. Химерная L-цепь по п. 1, отличающаяся тем, что С-область является Сλ-цепью. 3. Химерная Н-цепь, включающая С-область Н-цепи антитела человека и V-область Н-цепи моноклонального антитела мыши против белка, родственного паращитовидному гормону человека, в которой V-область Н-цепи включает аминокислотную последовательность, показанную в SEQ ID NO:46. 4. Химерная Н-цепь по п. 3, отличающаяся тем, что С-область является Сγ1-цепью. 5. Химерное моноклональное антитело против белка, родственного паращитовидному гормону человека, включающее химерную L-цепь по п.1 или 2 и химерную Н-цепь по п.1 или 2 и химерную Н-цепь по п.3 или 4. 6. Полипептид, включающий V-область L-цепи гуманизированного антитела против белка, родственного паращитовидному гормону человека, где каркасные области 1-3 указанной V-области L-цепи получены из V-области L-цепи антитела человека HSU03868, и каркасная область 4 указанной V-области L-цепи получена из V-области L-цепи антитела человека S25755, и гипервариабельные участки 1-3 указанной V-области L-цепи включают аминокислотные последовательности, выбранные из группы последовательностей SEQ ID NO:59-61. 7. Полипептид, включающий V-область L-цепи гуманизированного антитела против белка, родственного паращитовидному гормону человека, где каркасные области 1-3 указанной V-области L-цепи по существу идентичны каркасным областям 1-3 антитела человека HSU03868, и каркасная область 4 указанной V-области L-цепи по существу идентичная каркасной области 4 антитела человека S25755, и гипервариабельные участки 1-3 указанной V-области L-цепи включают аминокислотные последовательности, выбранные из группы последовательностей SEQ ID NO:59-61. 8. Полипептид по п.7, отличающийся тем, что 36-я и 49-я аминокислоты каркасных областей по определению Кабата являются, соответственно, тирозином и аспарагиновой кислотой. 9. Полипептид по п. 8, отличающийся тем, что он включает любую одну аминокислотную последовательность, показанную в SEQ ID NO:48-51. 10. Полипептид по п.7, отличающийся тем, что 87-я аминокислота каркасных областей по определению Кабата является изолейцином. 11. Полипептид по п.7, отличающийся тем, что 45-я и 87-я аминокислоты каркасных областей по определению Кабата являются, соответственно, лизином и изолейцином. 12. Полипептид по п. 10, отличающийся тем, что он включает любую одну аминокислотную последовательность, показанную в SEQ ID NO:52-55. 13. Полипептид по п.11, отличающийся тем, что он включает аминокислотную последовательность, показанную в SEQ ID NO:52 или 54. 14. Полипептид, включающий V-область Н-цепи гуманизированного антитела против белка, родственного паращитовидному гормону человека, где каркасные области 1-4 указанной V-области Н-цепи получены из V-области Н-цепи антитела человека человеческой подгруппы III, и гипервариабельные участки 1-3 указанной V-области Н-цепи включают аминокислотные последовательности, выбранные из группы последовательностей SEQ ID NO:62-64. 15. Полипептид, включающий V-область Н-цепи гуманизированного антитела против белка, родственного паращитовидному гормону человека, где каркасные области 1-4 указанной V-области Н-цепи по существу идентичны каркасным областям 1-4 антитела человека человеческой подгруппы III, и гипервариабельные участки 1-3 указанной V-области Н-цепи включают аминокислотные последовательности, выбранные из группы последовательностей SEQ ID NO:62-64. 16. Полипептид по п.14 или 15, отличающийся тем, что антитело человека представляет собой антитело человека S31679. 17. Полипептид по п.14, отличающийся тем, что он включает аминокислотную последовательность, показанную в SEQ ID NO:56. 18. L-цепь гуманизированного антитела против белка, родственного паращитовидному гормону человека, включающая полипептид, включающий С-область L-цепи антитела человека, и полипептид по любому из пп.6-13. 19. L-цепь гуманизированного антитела по п.18, отличающаяся тем, что С-область является Сλ-цепью. 20. L-цепь гуманизированного антитела по п.18, отличающаяся тем, что С-область является Сλ-цепью, указанные каркасные области 1-3 по существу идентичны каркасным областям 1-3 антитела человека HSU03868, соответственно, и указанная каркасная область 4 по существу идентична каркасной области 4 антитела человека S25755, и гипервариабельные участки 1-3 включают аминокислотные последовательности, показанные соответственно в SEQ ID NO:59-61. 21. Н-цепь гуманизированного антитела против белка, родственного паращитовидному гормону человека, включающая полипептид, включающий С-область Н-цепи антитела человека, и полипептид по любому из пп.14-17. 22. Н-цепь гуманизированного антитела по п.21, отличающаяся тем, что С-область является Сγ1-цепью, указанные каркасные области 1-4 выделены, соответственно, из каркасных областей 1-4 антитела человека человеческой подгруппы III, и гипервариабельные участки 1-3 включают аминокислотные последовательности, показанные, соответственно в SEQ ID NO:62-64. 23. Гуманизированное антитело против белка, родственного паращитовидному гормону человека, включающее L-цепь гуманизированного антитела по любому из пп.18-20 и Н-цепь гуманизированного антитела по пп.21 или 22. 24. ДНК, включающая последовательность оснований, кодирующую V-область L-цепи моноклонального антитела мыши против белка, родственного паращитовидному гормону человека, в которой V-область L-цепи включает аминокислотную последовательность, показанную в SEQ ID NO:45. 25. ДНК, включающая последовательность оснований, кодирующую V-область L-цепи моноклонального антитела мыши против белка, родственного паращитовидному гормону человека, в которой последовательность оснований, кодирующая V-область L-цепи, показана в SEQ ID NO:65. 26. ДНК, включающая последовательность оснований, кодирующую V-область Н-цепи моноклонального антитела мыши против белка, родственного паращитовидному гормону человека, в которой V-область Н-цепи включает аминокислотную последовательность, показанную в SEQ ID NO:46. 27. ДНК, включающая последовательность оснований, кодирующую V-область Н-цепи моноклонального антитела мыши против белка, родственного паращитовидному гормону человека, в которой последовательность оснований, кодирующая V-область Н-цепи, показана в SEQ ID NO:57. 28. ДНК, кодирующая химерную L-цепь по п.1 или 2. 29. ДНК по п.28, отличающаяся тем, что ДНК, кодирующая химерную L-цепь, включает последовательность оснований, показанную в SEQ ID NO:65. 30. ДНК, кодирующая химерную Н-цепь по п.3 или 4. 31. ДНК по п.30, отличающаяся тем, что ДНК, кодирующая химерную Н-цепь, включает последовательность оснований, показанную в SEQ ID NO:57. 32. ДНК, включающая последовательность оснований, кодирующую полипептид по любому из пп.6-13. 33. ДНК по п.32, включающая одну из последовательностей оснований, показанных в SEQ ID NO:66-74. 34. ДНК, включающая последовательность оснований, кодирующую полипептид по любому из пп.14-17. 35. ДНК по п.34, включающая последовательность оснований, показанную в SEQ ID NO:58. 36. ДНК, кодирующая L-цепь гуманизированного антитела по любому из пп. 18-20. 37. ДНК, кодирующая L-цепь гуманизированного антитела, включающая последовательность оснований, кодирующую любую одну из аминокислотных последовательностей, показанных в SEQ ID NO:47-55. 38. ДНК по п.37, отличающаяся тем, что ДНК L-цепи гуманизированного антитела включает любую одну из последовательностей оснований, показанных в SEQ ID NO:66-74. 39. ДНК, кодирующая Н-цепь гуманизированного антитела по п.21 или 22. 40. ДНК Н-цепи гуманизированного антитела, включающая последовательность оснований, кодирующую аминокислотную последовательность, показанную в SEQ ID NO:56. 41. ДНК по п. 40, отличающаяся тем, что ДНК Н-цепи гуманизированного антитела включает последовательность оснований, показанную в SEQ ID NO:58. 42. Рекомбинантный вектор, включающий ДНК по любому из пп.24-41. 43. Рекомбинантный вектор по п.42, отличающийся тем, что он встроен в трансформант. 44. Способ получения химерного антитела против белка, родственного паращитовидному гормону, включающий культивирование трансформанта, трансформированного экспрессирующим вектором, включающим ДНК по любому из пп.24, 25, 28 и 29 и экспрессирующим вектором, включающим ДНК по любому из пп.26, 27, 30 и 31, и выделение из полученной культуры химерного антитела против белка, родственного паращитовидному гормону человека. 45. Способ получения гуманизированного антитела против белка, родственного паращитовидному гормону человека, включающий культивирование трансформанта, трансформированного экспрессирующим вектором, включающим ДНК по любому из пп.32, 33 и 36-38, и экспрессирующим вектором, включающим ДНК по любому из пп. 34, 35 и 39-41, и выделение из полученной культуры гуманизированного антитела против белка, родственного паращитовидному гормону человека. 46. Фармацевтическая композиция, для профилактики или лечения потери веса, для профилактики или улучшения сниженного приема пищи, анорексии, тошноты, метаболического алкалоза, нарушенного рН крови, для регулирования изменения температуры тела, для профилактики или улучшения сниженной температуры тела, сниженной спонтанной активности, сниженного состояния активности, сниженного QOL у пациента в связи со злокачественной опухолью, и для подавления гиперкальцемии, включающая гуманизированное антитело по п.23 в качестве активного ингредиента, и фармацевтически приемлемый носитель. 47. Средство для подавления гиперкальциемии или для улучшения при гипофосфатемии, включающее гуманизированное антитело по п.23 в качестве активного ингредиента. 48. Средство по п.47, отличающееся тем, что гиперкальциемия обусловлена злокачественной опухолью. 49. Средство по п.48, отличающееся тем, что злокачественная опухоль является по крайней мере одной, выбранной из группы, включающей рак поджелудочной железы, рак легкого, рак глотки, рак гортани, рак языка, рак десны, рак пищевода, рак желудка, рак желчных протоков, рак молочной железы, рак почек, рак мочевого пузыря, рак матки, рак предстательной железы и злокачественную лимфому. 50. Средство по п.47, отличающееся тем, что гипофосфатемия является гипофосфатемическим рахитом. 51. Средство по п.47, отличающееся тем, что гипофосфатемия является гипофосфатемическим рахитом, устойчивым к витамину D.