Изобретение относится к технологии производства калийных минеральных удобрений, а именно ионообменной технологии производства бесхлорных калийных удобрений, и может быть использовано в агрохимической промышленности и сельском хозяйстве.
Известны способы ионообменного получения бесхлорных калийных минеральных удобрений, включающие ионообменную конверсию хлорида калия в бесхлорное соединение калия путем контактирования раствора соли, не содержащей хлорид-ионов, с катионитом в К-форме с последующей регенерацией калийной формы катионита для его повторного использования раствором хлорида калия [Сафрыкин Ю. С., Букша Ю.В, Хентов В.И. Производство бесхлорных калийных удобрений в СССР и за рубежом: Обзорная информация, М., 1981, 180с.]. Наиболее известны ионообменные способы получения нитрата калия из хлорида калия с использованием азотной кислоты, нитрата кальция и нитрата аммония [Higgins I.R., Chem. Ing. Progr. , 1964, V. 60, N 11, Р. 60-61; Вулих А.И. Ионообменный синтез, М., 1973, 185 с. ; Федюшкин Б.Ф., Агатова О.И., Гавлина О.Т., Володкович В.Е, Получение бесхлорных калийсодержащих удобрений из хлорсодержащего сырья с применением ионного обмена. Деп.ВИНИТИ 0.12.85 N 516].
Недостатками указанных способов являются: загрязнение продукта используемым реагентом, необходимость использования избыточных количеств хлорида калия для регенерации ионита, получение смесей веществ в виде трудноутилизируемых смешанных растворов, образование сточных вод, низкая эффективность использования обменной емкости ионитов.
Наиболее близким к предложенному изобретению по технической сущности и достигаемому результату является ионообменный способ получения бесхлорного удобрения, позволяющий достигать высокой степени конверсии хлорида калия в бесхлорное удобрение без затрат избыточных количеств реагентов на каждой стадии процесса и получать конечный продукт с высокой чистотой без образования сточных вод [а. с. 1248650 СССР, кл. МКИ4 B 01 J 47/02, C 01 D 9/10, опубл. 1986 г.]. В указанном способе проводят циклический процесс получения концентрированного раствора бесхлорного калийного удобрения с помощью использования двух ионообменных колонн с катионитом, через одну из которых пропускают раствор хлористого калия и переводят катионит из ионной формы какого-либо вспомогательного компонента, например, аммония, в форму иона калия, одновременно с этим через вторую колонну, пропускают раствор, содержащий бесхлорную соль указанного вспомогательного компонента, например, нитрат аммония, с получением раствора бесхлорного калийного удобрения, и переводят катионит из калийной формы в форму вспомогательного иона, при этом катионит передвигают по замкнутому контуру в направлении, противоположном направлению пропускания растворов, а именно, перемещают катионит в калиевой форме из первой колонны во вторую, а катионит, например, в аммонийной форме, - из второй колонны в первую. Отсутствие затрат избыточных количеств реагентов и отсутствие сточных вод в указанном способе достигается за счет использования концентрированных растворов нитрата аммония, при котором наблюдается эффект обращения селективности катионита к ионам калия и аммония со смещением ионообменного равновесия в необходимом направлении, а также за счет обеспечения рециркуляции и возврата в процесс смесей веществ.
Указанный способ ограничен получением нитрата калия из нитрата аммония и не позволяет получать другие агрохимически ценные бесхлорные калийные удобрения, такие как сульфат калия или смешанные фосфаты калия и аммония. Получаемый в виде водного раствора продукт требует дальнейшей переработки для выделения бесхлорного калийного удобрения в твердой фазе. Другим недостатком указанного способа является то, что рециркуляция смесей веществ для исключения потерь реагентов и образования стоков осуществляется в нем возвратом в процесс смешанных ионных форм катионита с помощью передвижения сорбента по противоточной ионообменной схеме, что является существенно более трудоемкой операцией, чем рециркуляция растворов.
Задачей изобретения является расширение круга получаемых ионообменным способом бесхлорных калийных минеральных удобрений за счет обеспечения возможности получения сульфата калия, бикарбоната калия, смешанных фосфатов калия и аммония. Другой задачей является повышение эффективности и удешевление способа ионообменного получения бесхлорных калийных минеральных удобрений за счет получения конечных продуктов в виде твердых удобрений. Задачей изобретения является также обеспечение исключения потерь реагентов и образования стоков не за счет рециркуляции сорбента, а за счет рециркуляции образующихся смесей веществ в виде водных растворов.
Поставленные задачи решаются тем, что в способе ионообменного получения бесхлорных калийных минеральных удобрений, включающем использование, по крайней мере, двух ионообменных колонн с катионитом, через одну из которых пропускают раствор хлористого калия и переводят катионит из ионной формы какого-либо вспомогательного компонента в калиевую форму с получением раствора хлористого натрия, одновременно с чем через вторую колонну пропускают раствор, содержащий бесхлорную соль указанного вспомогательного компонента, и переводят катионит из калиевой формы в форму вспомогательного компонента с получением в качестве продукта бесхлорной соли калия и с возвратом в процесс смесей веществ, образуемых при пропускании растворов через указанные колонны, используют колонны с неподвижным слоем катионита, через которые попеременно пропускают раствор хлористого калия и раствор, содержащий бесхлорную соль вспомогательного компонента, при этом катионит выбирают таким образом, чтобы его селективность к вспомогательному компоненту была меньше селективности к калию, концентрацию указанной бесхлорной соли вспомогательного компонента в указанном растворе выбирают большей, чем концентрация насыщенного раствора бесхлорной калийной соли, попеременно на выходе из первой и второй колонн получают пересыщенный раствор бесхлорной калийной соли, который выдерживают для осуществления самопроизвольной кристаллизации бесхлорной калийной соли, раствор, полученный в каждом цикле после отделения осадка бесхлорной калийной соли, объединяют с раствором указанной бесхлорной соли вспомогательного компонента перед его пропусканием через каждую из колонн; пропускание через каждую из колонн раствора хлористого калия и объединенного раствора, содержащего бесхлорную соль вспомогательного компонента, проводят в противоположных направлениях, так, чтобы в пределах каждой колонны более плотный раствор находился ниже менее плотного раствора; пропускание через каждую из колонн раствора хлористого калия и последующее пропускание объединенного раствора, содержащего бесхлорную соль вспомогательного компонента, проводят при разной температуре; пропускание объединенного раствора, содержащего бесхлорную соль вспомогательного компонента, и кристаллизацию бесхлорной калийной соли проводят при разной температуре; раствор бесхлорной соли вспомогательного компонента, вытесняемый из каждой колонны в начале процесса пропускания раствора хлористого калия через указанную колонну, отделяют от раствора хлористого натрия, вытесняемого в конце процесса пропускания раствора хлористого калия через указанную колонну; раствор хлористого калия, вытесняемый из каждой колонны в начале процесса пропускания объединенного раствора бесхлорной соли вспомогательного компонента через указанную колонну, отделяют от раствора бесхлорной калийной соли, вытесняемого в конце процесса пропускания раствора бесхлорной соли вспомогательного компонента через указанную колонну; используют три колонны с неподвижным слоем катионита, при этом в каждом цикле процесса через две из трех колонн последовательно пропускают раствор хлористого калия, одновременно с чем через третью колонну в противоположном направлении пропускают раствор, содержащий бесхлорную соль вспомогательного компонента, причем в каждом последующем цикле колонна, использованная в предыдущем цикле как первая по ходу пропускания раствора хлористого калия, используется для пропускания раствора бесхлорной соли вспомогательного компонента, а колонна, использованная для пропускания раствора бесхлорной соли вспомогательного компонента, используется в последующем цикле для пропускания раствора хлористого калия как вторая колонна по ходу пропускания указанного раствора.
На фиг. 1 представлены выходные кривые ионообменных процессов получения пересыщенного раствора бесхлорного калийного удобрения и последующего перевода катионита КУ-2 в калиевую форму на одной колонне на примере установившегося циклического процесса получения сульфата калия из хлорида калия и сульфата натрия по предлагаемому способу. I - выход пересыщенного раствора сульфата калия: 1 и 2 - концентрация натрия и, соответственно, калия в выходящем растворе в процессе обработки калийной формы катионита объединенным циркулирующим раствором смеси сульфата натрия (3.2 г-экв/л) и сульфата калия (0.8 г-экв/л) при 35oС; 3 - остаточная концентрация калия в растворе после самопроизвольного разрушения пересыщенного раствора. II или III - перевод катионита в калийную форму пропусканием 0.125 н. раствора хлорида калия при 20oС: 4 и 5 - выходные кривые ионов натрия и, соответственно, калия.
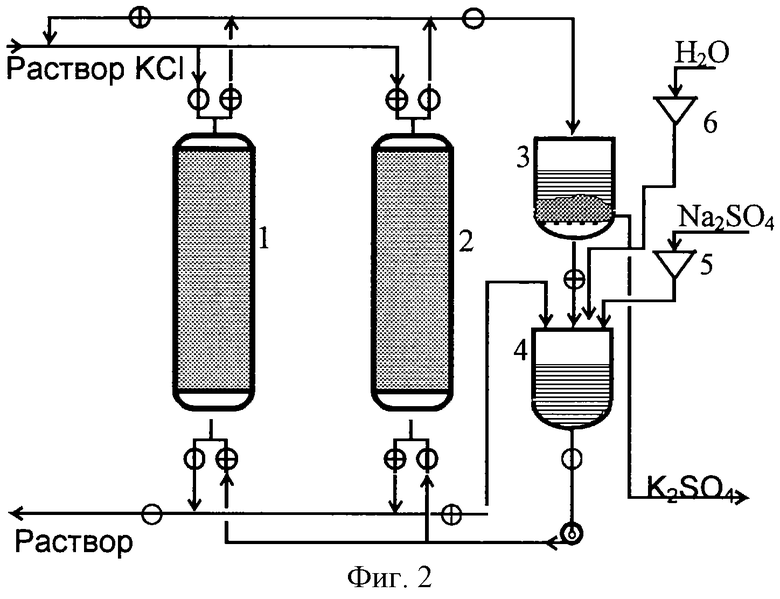
На фиг.2 представлена принципиальная технологическая схема процесса для осуществления предлагаемого способа получения бесхлорных калийных минеральных удобрений. 1, 2 - ионообменные колонны, 3 - емкость для сбора пересыщенного раствора и кристаллизации бесхлорного калийного удобрения, 4 - емкость для приготовления объединенного циркулирующего раствора, содержащего бесхлорную соль вспомогательного компонента, 5 - бункер-дозатор для подачи исходной бесхлорной соли вспомогательного компонента, 6 - емкость для подачи воды.
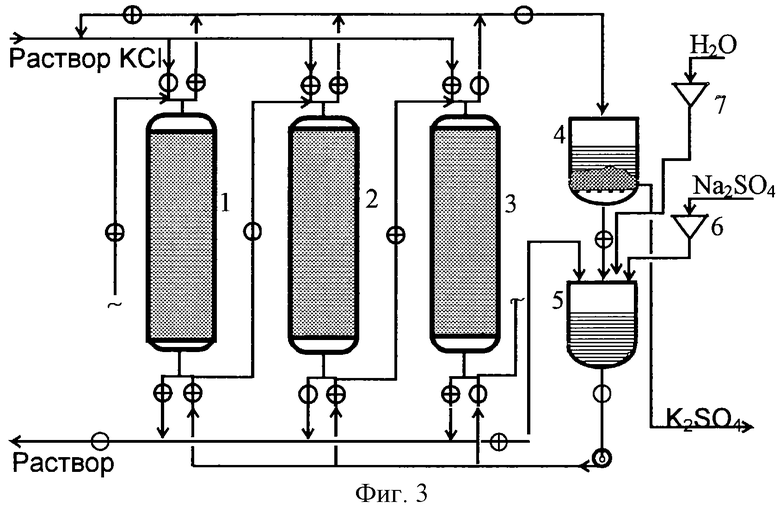
На фиг.3 представлена принципиальная технологическая схема процесса для осуществления предлагаемого способа получения бесхлорных калийных минеральных удобрений с использованием трех колонн с неподвижным слоем катионита. 1-3 - ионообменные колонны, 4 - емкость для сбора пересыщенного раствора и кристаллизации бесхлорного калийного удобрения, 5 - емкость для приготовления объединенного циркулирующего раствора, содержащего бесхлорную соль вспомогательного компонента, 6 - бункер-дозатор для подачи исходной бесхлорной соли вспомогательного компонента, 7 - емкость для подачи воды.
Отличительной особенностью предлагаемого способа ионообменного получения бесхлорных калийных минеральных удобрений является обнаружение и использование нового явления - изотермического пересыщения растворов неорганических веществ в ионном обмене (Хамизов Р.Х., Мясоедов Б.Ф., Тихонов Н.А., Руденко Б. А. , Об общем характере явления изотермического пересыщения в ионном обмене. Докл. АН, 1997 г.). Суть явления заключается в том, что при проведении в колонне ионообменной реакции, сопровождаемой образованием соединения с ограниченной растворимостью, в ионообменном слое образуется и стабилизируется пересыщенный раствор этого соединения, который после выхода из колонны самопроизвольно разрушается с кристаллизацией указанного соединения. Использование этого явления для ионообменного получения бесхлорных минеральных удобрений позволяет сдвигать равновесие процесса в нужном направлении, получать продукт в твердом виде без дополнительных переделов, использовать в цикле оборотные растворы, образуемые после кристаллизации продукта без потерь ценных химических веществ и без образования твердых отходов и сточных вод.
Целесообразно осуществлять пропускание через ионообменные колонны раствора хлористого калия и объединенного раствора, содержащего бесхлорную соль вспомогательного компонента в противоположных направлениях, так, чтобы в пределах каждой колонны более плотный раствор находился ниже менее плотного раствора. Это позволяет избежать перемешивания разнородных растворов и потери ценных компонентов.
Целесообразно осуществлять пропускание через ионообменные колонны раствора хлористого калия и последующее пропускание объединенного раствора, содержащего бесхлорную соль вспомогательного компонента, при разной температуре. Это позволяет влиять на растворимость (увеличивать растворимость) бесхлорной калийной соли в пересыщенном растворе в слое сорбента, с тем, чтобы обеспечить стабильный ионообменный процесс без осадкообразования в колонне.
Целесообразно осуществлять пропускание объединенного раствора, содержащего бесхлорную соль вспомогательного компонента, и кристаллизацию бесхлорной калийной соли при разной температуре. Это позволяет влиять на растворимость (уменьшать растворимость) получаемого продукта - бесхлорного калийного минерального удобрения и повышать его выход в каждом цикле процесса.
Целесообразно осуществлять процесс так, чтобы отделять раствор бесхлорной соли вспомогательного компонента, вытесняемый из каждой колонны в начале процесса пропускания раствора хлористого калия через ионообменную колонну, от раствора хлористого натрия, вытесняемого в конце процесса пропускания раствора хлористого калия через эту колонну. Это позволяет проводить процесс без образования сточных вод в виде трудноутилизируемых смешанных растворов и устранить потери ценного продукта.
Целесообразно осуществлять процесс так, чтобы отделять раствор хлористого калия, вытесняемый из каждой колонны в начале процесса пропускания объединенного раствора бесхлорной соли вспомогательного компонента через указанную колонну, от раствора бесхлорной калийной соли, вытесняемого в конце процесса пропускания раствора бесхлорной соли вспомогательного компонента через эту колонну. Это также позволяет проводить процесс без образования сточных вод в виде трудноутилизируемых смешанных растворов.
Целесообразно осуществлять процесс с использованием трех колонн с неподвижным слоем катионита, так, чтобы в каждом цикле процесса через две из трех колонн последовательно пропускать раствор хлористого калия, одновременно с чем через третью колонну в противоположном направлении пропускать раствор, содержащий бесхлорную соль вспомогательного компонента. В каждом последующем цикле, колонна, использованная в предыдущем цикле как первая по ходу пропускания раствора хлористого калия, может быть использована для пропускания раствора бесхлорной соли вспомогательного компонента, а колонна, использованная для пропускания раствора бесхлорной соли вспомогательного компонента, может быть использована в последующем цикле для пропускания раствора хлористого калия в качестве второй по ходу колонны для пропускания указанного раствора. Это позволяет, в случае применения концентрированных растворов хлорида калия в качестве источника калия, исключить возможность его потерь, а также возможность образования сточных вод в виде смешанных растворов.
Примеры осуществления предлагаемого способа.
Пример 1. Проводят процесс на лабораторной установке, собранной по схеме, показанной на фиг.2, и включающей две одинаковые ионообменные колонки с площадью внутреннего сечения 3.25 см2 и высотой 35 см, снабженные термостатирующей рубашкой, дренажными фильтрующими устройствами в верхней и нижней частях колонки и загрузочным устройством для ионита. Используют промышленный сильнокислотный сульфокатионит КУ-2х8, масса сорбента, загружаемого в каждую колонну, в воздушно-сухом состоянии - 50 г. Сорбент загружают в колонки в виде суспензии в 0.1 н. растворе NaCl. Параметры слоя сорбента в каждой колонне при различных условиях: в 0.1 н. NaCl: L=34 cм (объем слоя ω=110.5 см3); в 4 н. Na2SO4: L=31.5 см (ω=102.4 см3). Порозность плотного слоя в растворе хлорида натрия (доля объема между зернами ионита от объема его слоя в колонне) - ε= 35%, при этом объем порозного пространства в колонне - Vε = 38,5 см3; свободный объем в каждой колонке под слоем сорбента и в трубопроводах до нижнего выхода из каждой колонны - 31.5 см3; максимальный свободный объем в каждой колонке над слоем сорбента и в трубопроводах до верхнего выхода из каждой колонны - 31.5 см3. Процесс проводят следующим образом.
А. Через каждую из колонн при комнатной температуре пропускают по 2200 мл 0.125 н. раствора хлорида калия (КСl). Скорость пропускания раствора через каждую колонну - 550 мл/час, время пропускания - 4 часа. Полученный на выходе разбавленный 0.125 н. раствор хлорида натрия (NaCl) направляют на слив.
Б. Через первую колонну при температуре 35oС пропускают 240 мл 4 н. раствора Na2SO4 в направлении снизу наверх колонны. В начале процесса пропускания указанного раствора, а именно, 70 мл первых порций элюата, что соответствует объему разбавленного раствора КСl, остававшегося в порозном пространстве (38.5 мл) и в свободном объеме над слоем ионита (31.5 мл), направляют в линию подачи исходного раствора хлорида калия, что осуществляют с помощью клапанов, установленных в верхней части схемы на фиг.2. Дальнейшие порции элюата направляют в емкость 3, находящуюся при комнатной температуре и снабженную фильтрующим днищем. Скорость пропускания 4 н. раствора Na2SO4 - 120 мл/час, суммарное время пропускания 2 часа. Всего в емкости 3 собирают 240-70=170 мл раствора элюата. Этот раствор оставляют стоять (выдерживают) в течение 2 часов для кристаллизации сульфата калия (K2SO4).
В. Полученную суспензию разделяют тем, что оставшийся в емкости 3 раствор направляют в емкость 4, находящуюся при температуре 35oС. При этом раствор проходит через слой кристаллического осадка и фильтрующее днище емкости 3. Всего после указанных операций получают: в емкости 3 - влажный осадок, содержащий 12 г K2SO4 и 12 воды; в емкости 4 - 158 мл раствора, содержащего смесь сульфата калия и сульфата натрия в концентрациях: К2SO4 - 0.8 мг-экв/мл и Na2SO4 - 2.8 мг-экв/мл.
Г. В емкость 4 добавляют 9.68 г безводного сульфата натрия и 12 мл воды (или 22 г соли в виде кристаллогидрата - Na2SO4•10Н2О).
Д. Через первую колонну в направлении сверху вниз при комнатной температуре пропускают разбавленный (0.125 н. ) раствор КСl со скоростью 550 мл/час. Процесс пропускания продолжают в течение четырех часов. При этом первые порции элюата (всего 70 мл), соответствующие объему концентрированного раствора сульфата натрия, находящегося в порозном объеме и в свободном объеме над слоем ионита, направляют обратно в емкость 4, а последующие порции (всего 1030 мл) в виде разбавленного раствора хлорида направляют на слив. В процессе осуществления операций по п."Д" концентрации компонентов в выходящем из первой колонны растворе изменяются в соответствии с выходными кривыми 4 и 5, показанными на фиг.1.
Е. Одновременно с операциями по п."Д", через вторую колонну при температуре 35oС в направлении снизу вверх пропускают подаваемый из емкости 4 концентрированный раствор сульфата натрия (3.2 мг-кв/мл), смешанный с остаточным растворам сульфата калия (0.8 мг-экв/мл). Скорость и время пропускания, а также процедура пропускания полностью аналогичны тем, что описаны выше в п. "Б". В процессе пропускания концентрированного раствора через вторую колонну концентрации компонентов на выходе из верха указанной колонны изменяются в соответствии с выходными кривыми 1 и 2, показанными на фиг.1. Полученный пересыщенный по сульфату калия раствор собирают в емкости 4 и в течение 2 часов выдерживают для кристаллизации K2SO4. После кристаллизации сульфата калия остаточная концентрация ионов калия в растворе равна 0.8 мг-экв/мл и соответствует кривой 3 на фиг.1.
Ж. Полученную суспензию разделяют как описано в п. "В", а именно, оставшийся в емкости 3 раствор направляют в емкость 4, находящуюся при температуре 35oС. При этом раствор проходит через слой кристаллического осадка и фильтрующее днище емкости 3. Всего после указанных операций получают: в емкости 3 - влажный осадок, содержащий 17.6 г К2SO4 и 17.5 воды; в емкости 4 - 152.5 мл раствора, содержащего смесь сульфата калия и сульфата натрия в концентрациях: K2SO4 - 0.8 мг-экв/мл и Na2SO4 - 2.02 мг-экв/мл.
3. В емкость 4 добавляют 14 г безводного сульфата натрия и 17.6 мл воды (или 23.5 г соли в виде кристаллогидрата - Na2SO4 • 10H2O).
К. Повторяют все процессы в соответствии с п.п. "Д"-"З", за исключением того, что разбавленный раствор хлорида калия пропускают через вторую колонну в направлении сверху вниз, одновременно с чем концентрированный раствор смешанных сульфатов натрия и калия пропускают через первую колонну в направлении снизу вверх. В конце всех операций получают, отделяют и сушат 17.6 г сульфата калия.
Далее продолжают процесс в соответствии с приведенным описанием, используя в каждом цикле колонны 1 и 2 попеременно, то на стадии сорбции, то на стадии регенерации, с получением пересыщенного раствора сульфата калия. В каждом цикле (за 4 часа) получают 17.6 г сульфата калия и затрачивают 14 г безводного сульфата натрия. В процессе нет отходов кроме разбавленного 0.125 н. раствора хлорида натрия.
Пример 2. Проводят процесс на лабораторной установке, собранной по схеме, показанной на фиг.3, и включающей три одинаковые ионообменные колонки с площадью внутреннего сечения 3.25 см2 и высотой 35 см, снабженные термостатируюшей рубашкой, дренажными фильтрующими устройствами в верхней и нижней частях колонки и загрузочным устройством для ионита. Используют промышленный сильнокислотный сульфокатионит КУ-2х8, масса сорбента, загружаемого в каждую колонну, в воздушно-сухом состоянии - 50 г. Параметры слоя сорбента в каждой колонне аналогичны параметрам, приведенным в Примере 1. Процесс проводят следующим образом.
А. Через колонны 1, 2 и 3 последовательно пропускают при комнатной температуре 3 н. раствор (226.5 г/л) хлорида калия (КСl) до обнаружения "проскока" ионов калия через нижний выход колонны 3. Всего пропускают 168 мл. Скорость пропускания раствора 84 мл/час, время пропускания - 2 часа. Полученный на выходе концентрированный 3 н. раствор хлорида натрия (NaCl, 175.5 г/л) направляют на переработку (для получения сухой соли или в хлорное производство для получения хлора и щелочи методом мембранного электролиза).
Б. Через первую колонну при температуре 35oС пропускают 240 мл 4 н. раствора Na2SO4 в направлении снизу наверх колонны. В начале процесса пропускания указанного раствора, а именно, 70 мл первых порций элюата, что соответствует объему разбавленного раствора КСl, остававшегося в порозном пространстве (38.5 мл) и в свободном объеме над слоем ионита (31.5 мл), направляют в линию подачи исходного раствора хлорида калия, что осуществляют с помощью клапанов, установленных в верхней части схемы на фиг.3. Дальнейшие порции элюата направляют в емкость 4, находящуюся при комнатной температуре и снабженную фильтрующим днищем. Скорость пропускания 4 н. раствора Na2SO4 - 240 мл/час, суммарное время пропускания 1 час. Всего в емкости 4 собирают 240-70=170 мл раствора элюата. Этот раствор оставляют стоять (выдерживают) в течение 1 часа для кристаллизации сульфата калия (K2SO4).
В. Полученную суспензию разделяют тем, что оставшийся в емкости 4 раствор направляют в емкость 5, находящуюся при температуре 35oС. При этом раствор проходит через слой кристаллического осадка и фильтрующее днище емкости 4. Всего после указанных операций получают: в емкости 4 - влажный осадок, содержащий 12 г К2SO4 и 12 воды; в емкости 5 - 158 мл раствора, содержащего смесь сульфата калия и сульфата натрия в концентрациях: K2SO4 - 0.8 мг-экв/мл и Na2SO4 - 2.8 мг-экв/мл.
Г. В емкость 5 добавляют 9.68 г безводного сульфата натрия и 12 мл воды (или 22 г соли в виде кристаллогидрата - Na2SO4•10H2O).
Д. Через третью и первую колонну последовательно в направлении 3-->1, при этом в пределах каждой колонны в направлении сверху вниз, при комнатной температуре пропускают концентрированный 3 н. раствор КСl со скоростью 70 мл/час до "проскока" ионов калия через нижний выход первой колонны. Процесс пропускания продолжают в течение двух часов. При этом первые порции элюата (всего 70 мл), соответствующие объему концентрированного раствора сульфата натрия, находящегося в порозном объеме первой колонны и в свободном объеме над слоем ионита, направляют обратно в емкость 5, а последующие порции (всего 70 мл) в виде 3 н. раствора хлорида направляют на переработку.
Е. Одновременно с операциями по п. "Д", через вторую колонну при температуре 35oС в направлении снизу вверх пропускают подаваемый из емкости 4 концентрированный раствор сульфата натрия (3.2 мг-кв/мл), смешанный с остаточным растворам сульфата калия (0.8 мг-экв/мл). Скорость и время пропускания, а также процедура пропускания полностью аналогичны тем, что описаны выше в п. "Б".
Ж. Полученную суспензию разделяют как описано в п. "В", а именно, оставшийся в емкости 4 раствор направляют в емкость 5, находящуюся при температуре 35oС. При этом раствор проходит через слой кристаллического осадка и фильтрующее днище емкости 4. Всего после указанных операций получают: в емкости 4 - влажный осадок, содержащий 17.6 г К2SO4 и 17.5 воды; в емкости 5 - 152.5 мл раствора, содержащего смесь сульфата калия и сульфата натрия в концентрациях: K2SO4 - 0.8 мг-экв/мл и Na2SO4 - 2.02 мг-экв/мл.
З. В емкость 5 добавляют 14 г безводного сульфата натрия и 17.5 мл воды (или 23.5 г соли в виде кристаллогидрата - Na2SO4•10Н2О).
К. Повторяют все процессы в соответствии с п.п. "Д"-"З", за исключением того, что 3 н. раствор хлорида калия пропускают через первую и вторую колонну в направлении 1-->2 и в направлении сверху вниз в пределах каждой колонны, одновременно с чем концентрированный раствор смешанных сульфатов натрия и калия пропускают через колонну 3 в направлении снизу вверх. В конце всех операций получают, отделяют и сушат 17.6 г сульфата калия.
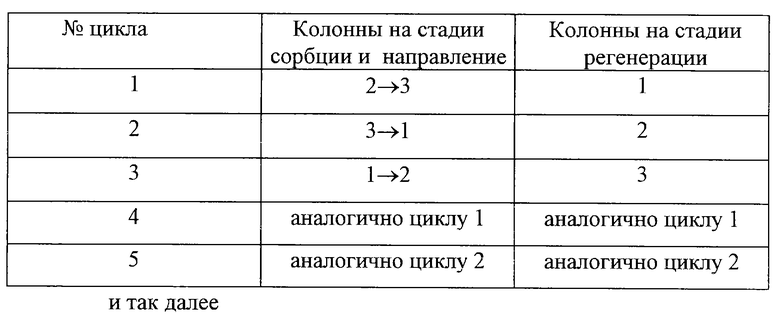
Далее продолжают процесс в соответствии с приведенным описанием, используя в каждом цикле колонны попеременно, причем две из трех колонн на стадии сорбции ионов калия из раствора хлорида калия, а одну из трех колонн, одновременно, на стадии регенерации с получением пересыщенного раствора сульфата калия. Указанные процессы проводят на колоннах в соответствии со следующей очередностью использования колонн в каждом цикле на стадиях сорбции и регенерации, начиная с первого цикла (см. таблицу).
В каждом цикле (за 2 часа) получают 17.6 г сульфата калия и затрачивают 14 г безводного сульфата натрия. В процессе нет отходов при условии полезной утилизации концентрированного раствора хлористого натрия.
Пример 3. Проводят процесс как описано в примере 2 за исключением того, что вместо концентрированного 4 н. раствора сульфата натрия используют 4 н. раствор нитрата аммония (320 г/л), стадию регенерации сорбента, предварительно насыщенного по калию указанным раствором нитрата аммония, ведут при комнатной температуре (температуре окружающей среды - 18-25oС), полученный пересыщенный раствор охлаждают до 0oС за счет поддержания в емкости 4 указанной низкой температуры, в емкости 5 поддерживают температуру окружающей среды. В каждом цикле процесса (за 2 часа) получают 20 г нитрата калия в расчете на сухую безводную соль. В каждом цикле процесса в оборотном регенерационном растворе после отделения осадка нитрата калия его остаточная концентрация составляет 1.25 г-экв/л (127.5 г/л). В каждом цикле оборотный регенерационный раствор доукрепляют добавлением 16 г нитрата аммония и 15 мл воды.
При проведении описанного процесса в каждом цикле на стадии сорбции калия получают 70 мл 3 н. раствора хлорида аммония (NH4Cl), который постепенно накапливают и перерабатывают вторично по методике, полностью аналогичной методике, описанной в Примере 2, за исключением того, что в качестве продукта получают сульфат аммония (13.2 г в каждом цикле). При этом в каждом цикле на стадии сорбции хлорида калия получают 70 мл 3 н. раствора хлорида натрия, который утилизирует в соответствии с Примером 2.
Получаемые в ходе всех описанных операций данного примера продукты - нитрат калия (20 г каждые два часа) и сульфат аммония (13.2 г каждые два часа) используют в качестве ценных минеральных удобрений по отдельности или в смешанном виде.
Пример 4. Проводят процесс, как описано в Примере 2, за исключением того, что вместо концентрированного 4 н. раствора сульфата натрия используют 3 н. (по аммонию) раствор дигидрофосфата аммония (NH4H2PO4, 354 г/л), получаемого продуванием через раствор ортофосфорной кислоты рассчитанного объема аммиака, стадию регенерации сорбента, предварительно насыщенного по калию указанным раствором дигидрофосфата аммония, ведут при комнатной температуре (температуре окружающей среды - 18-25oС), полученный пересыщенный раствор охлаждают до 10oС за счет поддержания в емкости 4 указанной низкой температуры, в емкости 5 поддерживают температуру окружающей среды. Другим отличием от примера 2 является то, что на стадии регенерации через колонну пропускают не 240 мл, а 300 мл концентрированного раствора. В каждом цикле процесса (за 2 часа) получают 27.5 г дигидрофосфата калия (КН2РO4) в расчете на сухую безводную соль. В каждом цикле процесса в оборотном регенерационном растворе после отделения осадка нитрата калия его остаточная концентрация составляет 1.1 г-экв/л (152 г/л). В каждом цикле оборотный регенерационный раствор доукрепляют добавлением 23.5 г дигидрофосфата аммония и 20 мл воды.
При проведении описанного процесса в каждом цикле на стадии сорбции калия получают 70 мл 3 н. раствора хлорида аммония (NH4Cl), который постепенно накапливают и перерабатывают вторично по методике, полностью аналогичной методике, описанной в Примере 2, за исключением того, что в качестве продукта получают сульфат аммония (13.2 г в каждом цикле). При этом в каждом цикле на стадии сорбции хлорида калия получают 70 мл 3 н. раствора хлорида натрия, который утилизирует в соответствии с Примером 2.
Получаемые в ходе всех описанных операций данного примера продукты - дигидрофосфат калия (27.5 г каждые два часа) и сульфат аммония (13.2 г каждые два часа) используют в качестве ценных минеральных удобрений по отдельности или в смешанном виде.
Предлагаемый способ, за счет использования нового явления открытого авторами - "Изотермического пересыщения в ионном обмене", а также за счет осуществления описанных выше отдельных операций и их специального сочетания друг с другом, обеспечивает: безотходность и экологическая чистоту процесса; возможность использования в качестве источника калия отходов калийного производства и других промышленных и сельскохозяйственных сточных вод; расширение круга получаемых бесхлорных калийных минеральных удобрений; удешевление способа ионообменного получения бесхлорных калийных минеральных удобрений за счет получения конечных продуктов в виде твердых удобрений и уменьшения энергоемкости, а также исключения потерь ценных химических реагентов за счет рециркуляции образующихся смесей веществ в виде водных растворов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения растворимых бесхлорных калийных удобрений (варианты) | 2016 |
|
RU2655211C1 |
| Способ переработки природных солоноватых вод с получением растворов сложных минеральных удобрений, установка для его осуществления и ионообменный узел | 2018 |
|
RU2682620C1 |
| Способ переработки природных солоноватых вод с получением растворов сложных минеральных удобрений и установка для его осуществления (варианты) | 2018 |
|
RU2680050C1 |
| Способ переработки природных солоноватых вод на ионитах с получением растворов сложных минеральных удобрений и установка для его осуществления (варианты) | 2018 |
|
RU2686147C1 |
| Способ получения растворимых бесхлорных калийных удобрений (варианты) | 2015 |
|
RU2608017C1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ МОРСКОЙ ВОДЫ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1996 |
|
RU2104969C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИСКУССТВЕННОЙ ПОЧВЫ НА ОСНОВЕ КЛИНОПТИЛОЛИТА | 1997 |
|
RU2115301C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА МИНЕРАЛЬНЫХ УДОБРЕНИЙ НА ОСНОВЕ МИНЕРАЛИЗОВАННОЙ И/ИЛИ ПРЕСНОЙ ВОДЫ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1998 |
|
RU2138149C1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ МОРСКОЙ ВОДЫ | 1995 |
|
RU2089511C1 |
| СПОСОБ ПРОВЕДЕНИЯ МАССООБМЕННЫХ СОРБЦИОННЫХ ПРОЦЕССОВ, АППАРАТ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ, ПРОМЫШЛЕННАЯ УСТАНОВКА ДЛЯ РАЗДЕЛЕНИЯ КОМПОНЕНТОВ ВОДНЫХ РАСТВОРОВ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ И АППАРАТ ДЛЯ ОТДЕЛЕНИЯ ОРГАНИЧЕСКИХ ЖИДКИХ ВЕЩЕСТВ ОТ ВОДНЫХ РАСТВОРОВ | 2010 |
|
RU2434679C1 |
Изобретение относится к технологии производства калийных минеральных удобрений, а именно ионообменной технологии производства бесхлорных калийных удобрений, и может быть использовано в агрохимической промышленности и сельском хозяйстве. В способе получения бесхлорных калийных минеральных удобрений, включающем использование по крайней мере двух ионообменных колонн с катионитом, через одну из которых пропускают раствор хлористого калия и переводят катионит из ионной формы какого-либо вспомогательного компонента в калиевую форму, одновременно с чем через вторую колонну пропускают раствор бесхлорной соли указанного вспомогательного компонента, и переводят катионит из калиевой формы в форму вспомогательного компонента, используют колонны с неподвижным слоем катионита, через которые попеременно пропускают раствор хлористого калия и раствор, содержащий бесхлорную соль вспомогательного компонента, при этом катионит выбирают таким образом, чтобы его селективность к вспомогательному компоненту была меньше селективности к калию, концентрацию указанной бесхлорной соли вспомогательного компонента в указанном растворе выбирают большей, чем концентрация насыщенного раствора бесхлорной калийной соли, попеременно на выходе из первой и второй колонн получают пересыщенный раствор бесхлорной калийной соли, который выдерживают для осуществления самопроизвольной кристаллизации бесхлорной калийной соли, раствор, полученный в каждом цикле после отделения осадка бесхлорной калийной соли, объединяют с раствором указанной бесхлорной соли вспомогательного компонента перед его пропусканием через каждую из колонн. Способ обеспечивает безотходность процесса, возможность использования в качестве источника калия отходов калийного производства и сточных вод, удешевления способа ионообменного получения калийных удобрений за счет получения конечных продуктов в виде твердых удобрений, а также исключение потерь ценных химических реагентов. 6 з.п.ф-лы, 3 ил., 1 табл.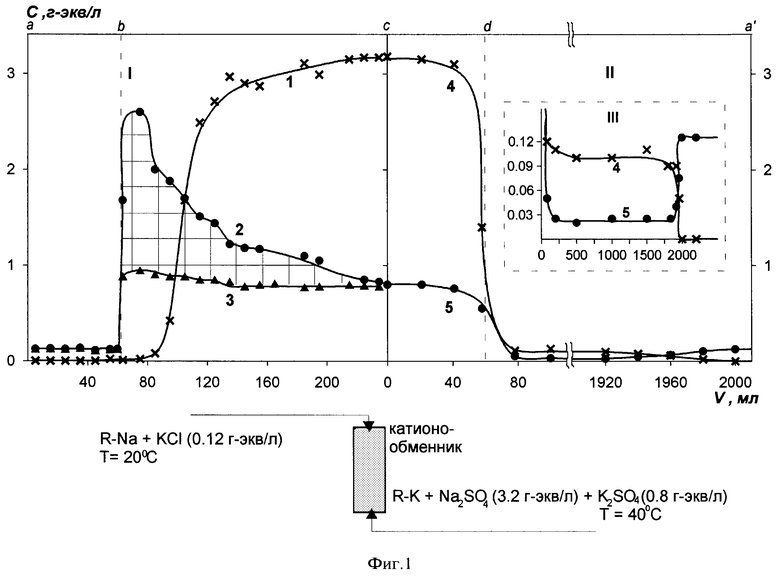
| Способ получения нитрата калия | 1984 |
|
SU1248650A1 |
| Способ получения бесхлорногокалийного удобрения | 1974 |
|
SU509568A1 |
| Умножитель частоты следования импульсов | 1986 |
|
SU1450096A1 |
Авторы
Даты
2003-03-27—Публикация
1998-07-30—Подача