Изобретение относится к области биологии и медицины и может быть использовано для лечения различных заболеваний, требующих улучшения кровоснабжения органа или региона.
Эфферентные методы лечебного воздействия, к которым относится гемосорбция (или гемоперфузия через различные сорбенты), широко используется в клинической практике [1, 2, 3, 4]. Традиционно в качестве основного механизма лечебного воздействия при сорбционной процедуре рассматривают удаление из крови агрессивных агентов, которые являются причиной экзогенной или эндогенной интоксикации организма [5].
В качестве аналогов данного изобретения можно принять процедуру гемосорбции в различных ее вариантах и с использованием сорбентов различной химической структуры.
Наиболее близким по сущности к заявляемому способу лечебного воздействия является метод аутотрансфузии гемосорбентообработанной крови (АГОК), который может быть выбран в качестве прототипа [6]. Метод заключается в эксфузии венозной крови в контейнер с гепарином. Кровь перфузируют в закрытом контуре через колонку с угольным сорбентом вне организма в течение 10 минут, а затем производят трансфузию сорбентообработанной крови (480 мл для пациента с массой тела 80 кг). Однако с позиции развития процессов активации и воздействия биоактивных молекул на патологические процессы АГОК обладает одним существенным недостатком. Дело в том, что биологически активные вещества, образующиеся в результате твердофазной контактной гемомодуляции, в основном короткоживущие (особенно активные формы кислорода (АФК) -l0-6-l0-12c), поэтому основная масса биоактивных молекул успевает инактивироваться, что сводит практически на нет активационный компонент воздействия АГОК.
Изобретение направлено на разработку способа улучшения кровоснабжения органов и тканей активированными гуморальными и клеточными элементами крови за счет артериальной гемоперфузии и исключения инактивации молекул (временной фактор).
В данном изобретении реализуется принцип твердофазной контактной гемомодуляции, основанный на активационных процессах [7]. Контакт крови с любой чужеродной поверхностью (в том числе и сорбентами различной химической структуры) приводит к инициации системы контактной активации, ключевым компонентом которой является фактор Хагемана (XII) [8]. Появление в кровотоке активной формы фактора XII приводит к запуску ограниченного протеолиза внутри всех ферментативных каскадных систем плазмы. Результатом активации ферментативных каскадов является появление в крови биоактивных молекул (брадикинин, С3а, С5а и др.), которые оказывают модулирующее воздействие на клетки крови и других тканей и органов. Такие активационные цепные реакции в организме возникают в результате контакта крови с сорбентом и составляют суть твердофазной контактной гемомодуляции. Именно они в конечном итоге переводят внутреннюю среду организма в иное функциональное "состояние".
Суть предлагаемого способа состоит в том, что в течение короткого промежутка времени осуществляется локальная перфузия конкретного органа или сосудистого региона, в котором локализован патологический процесс, активированными элементами крови после ее контакта с сорбентом. Для развития активационных процессов в отличие от классической гемосорбции используют малые объемы сорбента и крови. Локальность воздействия достигается внутриартериальной гемоперфузией соответствующей сосудистой области.
Изобретение отличается от прототипа тем, что кровь забирают из артерии через сорбент, а затем, не выходя из сосуда, ее сразу же возвращают через сорбент в артериальный кровоток. Оптимальный результат достигается, если кровь забирают в объеме 0,5 мл/100 г массы тела со скоростью 0,5 мл/мин и, не выходя из сосуда, с такой же скоростью возвращают обратно через сорбент, причем объем сорбента составляет 30% от объема перфузируемой крови. В результате таких манипуляций кровь дважды проходит через сорбент, активируется, а активированные элементы с током артериальной крови доставляются в очаг поражения.
Количественные отличительные признаки получены в результате экспериментальных исследований, выполненных авторами.
В качестве сорбента можно использовать сорбенты различной химической структуры, обычно используемые при гемосорбции.
Способ реализуется следующим образом.
Пример 1
Эксперименты проводили на нелинейных белых крысах-самцах массой 180-200 г. Процедуру выполняли следующим образом:
Всем животным, фиксированным к станку под наркозом (нембутал 30-40 мг/кг), катетеризировали наружную яремную вену. Свертывающую систему крови блокировали гепарином в дозе 500 Ед/кг. В качестве контроля I рассматривали животных, фиксированных на станке в течение 30 минут. Животным, составляющим контроль II и опытные группы I и II, катетеризировали бедренную артерию через общую сонную артерию. К катетеру подключали колонку (шприц объемом 2 мл) без сорбента (контроль II) или с сорбентом объемом 0,3 мл. В опыте I использовали угольный сорбент СКН-2К, а в опыте II - крупнозернистую агарозу 4Б с размером гранул 0,4-1,0 мм. Из бедренной артерии животного шприцем забирали кровь в объеме 0,5 мл/100 г массы тела со скоростью 0,5 мл/мин и с такой же скоростью возвращали ее в циркуляцию. Положение катетера в бедренной артерии контролировали при вскрытии животного. Предложенный способ может быть обозначен как метод целевой малообъемной гемоперфузии (ЦМОГ).
Эффективность ЦМОГ оценивали по реакции сердечно-сосудистой системы через 15 и 30 мин от проведения гемоперфузии. Регистрировали перераспределение фракций сердечного выброса и изменение микроциркуляции в перфузируемой и неперфузируемой конечности животного.
Для оценки регионарных перераспределений фракций сердечного выброса использовали макроагрегаты сывороточного альбумина (МАА) диаметром 10-13 мкм, меченые 1311 (г. Обнинск). В день опыта готовили рабочий раствор МАА, активность которого в 0,2 мл составила 10 мкКи. МАА вводили шприцем в левый желудочек сердца крысы в объеме 0,2 мл. Через 60 с после инъекции МАА внутривенным введением 0,6 мл насыщенного раствора KCl вызывали остановку сердца, осуществляли выделение тканей задних конечностей для радиометрического исследования [9,10].
Оценку регионарных изменений микроциркуляции осуществляли с помощью метода распределения в тканях водорастворимого хлорида рубидия 86Rb [11], введенного через наружную яремную вену в объеме 0,2 мл с аналогичной суммарной активностью. Остановку сердца вызывали внутривенным введением 0,6 мл насыщенного раствора KCl через 60 с после введения индикатора. Извлекали ткани задних конечностей, подсчитывали радиоактивность каждой пробы в течение 100 с с помощью радиометрической установки и пересчетного прибора ПСО-2-2УМ. Изменения фракций сердечного выброса и сосудистой проницаемости в каждой пробе рассчитывали с помощью показателя (% активности в пробе относительно общей введенной активности), нормированного по % массы исследуемой ткани относительно общей массы животного (% активности /% массы) [12].
Изменения гемодинамики, которые являются результатом проведения ЦМОГ, иллюстрируются следующими примерами.
Пример 2. Регионарное перераспределение фракций сердечного выброса в тканях нижних конечностей у крыс до и после ЦМОГ с использованием угля СКН-2К и Агарозы 4Б.
Результаты проведенных исследований представлены в табл.1. У фиксированных к станку животных (контроль 1) фракции сердечного выброса в левой и правой задних конечностях были практически одинаковыми. Проведение гемоперфузии без использования сорбента привело к незначительному усилению кровотока в обеих задних конечностях.
Проведение ЦМОГ через гемоконтактные препараты также увеличивало фракцию сердечного выброса в задних конечностях. Реакция сердечно-сосудистой системы на СКН-2К и агарозу была практически одинаковой, но в перфузируемой конечности фракция сердечного выброса была достоверно выше, чем в контроле 1. Эта реакция сохранялась на одном уровне в регистрируемые временные интервалы (15 и 30 мин).
Таким образом, целевая малообъемная гемоперфузия в бедренную артерию задней конечности крысы приводит к увеличению фракции сердечного выброса в данном регионе.
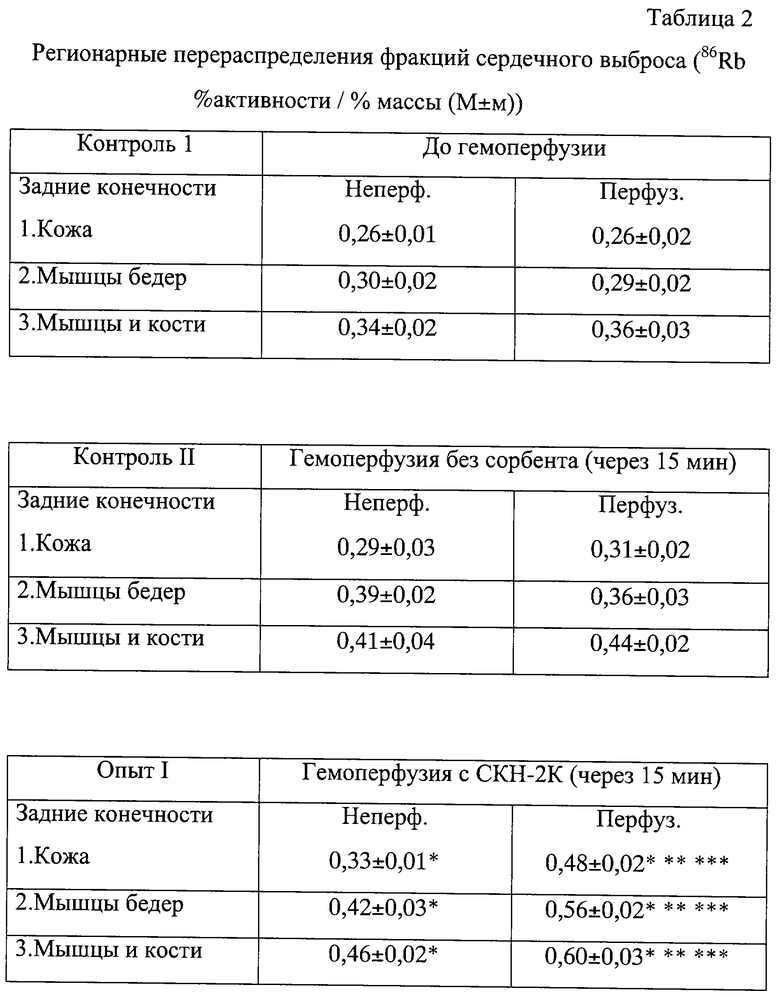
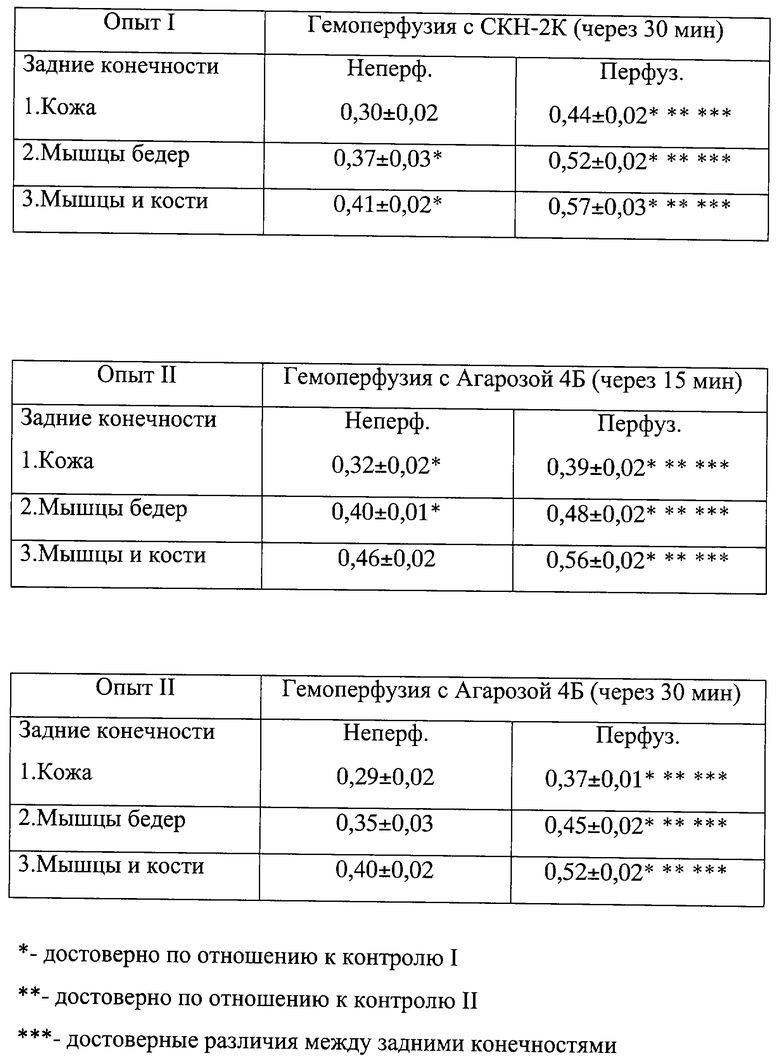
Пример 3. Изменение микроциркуляции в задних конечностях крыс после проведения ЦМОГ с использованием угля СКН-2К и агарозы
Реакция микроциркуляторного русла на ЦМОГ напоминала реакцию перераспределения фракций сердечного выброса у опытных и контрольных животных, но более выраженную (табл.2). Это вполне закономерно, т.к. биоактивный потенциал активированных элементов крови в первую очередь реализуется в перфузируемом регионе и в меньшей степени в других сосудистых областях. Усиление микроциркуляции наиболее выражено в перфузируемой конечности и достоверно отличается как от интенсивности микроциркуляции обеих контрольных групп, так и от сосудистой реакции в неперфузируемой конечности.
Апробация способа улучшения кровоснабжения тканей (метода ЦМОГ) в эксперименте позволила сделать заключение об изменении сосудистой реакции в перфузируемом регионе в сторону усиления кровоснабжения тканей. Данный эффект может быть использован в клинической практике для локального воздействия на патологические процессы, протекающие в конкретном участке или регионе.
ИСТОЧНИКИ ИНФОРМАЦИИ
1. Ветров В.В. Экстракорпоральная гемокоррекция в акушерстве. //Эфферентная терапия.-1999.- Т.5 - 3- С. 21-26.
2. Картель Н.Т. Возможности терапевтического действия медицинских сорбентов на основе активированных углей. //Эфферентная терапия.-1995.-T.1 - 4-С. 11-18.
3. Лопухин Ю.М. Методическое пособие для врачей. //Эфферентная терапия. - 1996. -Т.2- 4 - С. 3-35.
4. 0стапенко В.А. Возможности сорбционных технологий в медицинском обеспечении населения, пострадавшего в результате катастрофы на ЧАЭС. //Эфферентные методы в медицине. - М, 1992.- С. 78-79.
5. Лопухин Ю.М., Молоденков М.Н. Гемосорбция. - М.: Медицина.- 1985.-287 с.
6. Жидков К. П., Федорова Л.А., Полевщиков А.В., Назаров П.Г. Динамика показателей бласттрансформации лимфоцитов крови в процессе гемосорбции у больных язвенной болезнью. //Гематол. и трансфузиол.- 1992.-Т.37.- 3.-С. 15-17.
7. Кузнецов С.И. Эффекторные механизмы гемоперфузии. //Эфферентная терапия.-1998.-Т.4 - 4 -С. 28-32.
8. Wachfogel Y. T., De La Cadena R.A., Colman R.W. Structural biology, cellular interaction and pathophysiology of the contact system. //Thr.Res. -1993,- vol.72.,N1.- P. 1-30.
9. Rudolph A. M. , Heymann M.A. The circulation of the fetus in utero. //Circulat. Res.- 1967.-Vol.21.- P.163-184.
10. Ковалев О.А. Комплексная оценка изменений регионарного кровообращения в эксперименте. //Пат.физиол. и эксперим. терапия.- 1983.- 1.-С. 62-64.
11. Sapirstein L.A. The indicator fractionation technique for the study of regional blood flow. //Gastroenter.-1967.-Vol.57.-P.365-371.
12. Ковалев О.А. Особенности регистрации регионарных перераспределений крови в эксперименте. //Пат.физиол. и экспер.терапия. //1977.- 3.-С. 84-87.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РЕГУЛЯЦИИ ТКАНЕВОГО КРОВОТОКА ПУТЕМ ИНДУКЦИИ И СИНТЕЗА ЭНДОГЕННЫХ ВАЗОТРОПНЫХ ВЕЩЕСТВ ИЗ ГРУППЫ ЭЙКОЗАНОИДОВ | 2009 |
|
RU2414247C2 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ С КРИТИЧЕСКОЙ ИШЕМИЕЙ НИЖНИХ КОНЕЧНОСТЕЙ | 2002 |
|
RU2233178C2 |
| СПОСОБ ЛЕЧЕНИЯ ОЖОГОВЫХ РАН | 2002 |
|
RU2210391C1 |
| СПОСОБ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ И ГНОЙНО-НЕКРОТИЧЕСКИХ ЗАБОЛЕВАНИЙ ПАЛЬЦЕВ И КИСТИ | 2004 |
|
RU2282466C2 |
| СПОСОБ ОЦЕНКИ ИНДИВИДУАЛЬНОЙ ЧУВСТВИТЕЛЬНОСТИ БОЛЬНЫХ К ГЕМОКОНТАКТНЫМ ПРЕПАРАТАМ ДЛЯ ГЕМОСОРБЦИОННЫХ ПРОЦЕДУР | 1997 |
|
RU2122734C1 |
| СПОСОБ ПРОВЕДЕНИЯ ГЕМОСОРБЦИИ | 1997 |
|
RU2137508C1 |
| ИММУНОСОРБЕНТ ДЛЯ УДАЛЕНИЯ ИММУННЫХ КОМПЛЕКСОВ, ОБРАЗОВАННЫХ ИММУНОГЛОБУЛИНАМИ ЛОШАДИ ПОСЛЕ ВВЕДЕНИЯ ПРОТИВОДИФТЕРИЙНОЙ СЫВОРОТКИ, И СПОСОБ ПРОВЕДЕНИЯ ГЕМОСОРБЦИИ ПРИ ЛЕЧЕНИИ ДИФТЕРИИ | 1998 |
|
RU2161504C2 |
| Устройство для проведения малообъемной гемоперфузии | 2016 |
|
RU2631630C1 |
| Применение гранул сорбента из сверхсшитого полистирола марки "Стиросорб 516" в качестве контактного гемоактиватора клеточных элементов крови | 2019 |
|
RU2712630C1 |
| Устройство для проведения малообъемной гемоперфузии | 2022 |
|
RU2801672C1 |


Изобретение относится к медицине, а именно к эфферентной терапии. Способ заключается в следующем: осуществляют локальную перфузию конкретного органа или сосудистого региона, в котором локализован патологический процесс, для чего кровь забирают из артерии в объеме 0,5 мл/100 г массы тела со скоростью 0,5 мл/мин и, не выходя из сосуда, с такой же скоростью возвращают кровь через сорбент обратно в артериальный кровоток, причем объем сорбента составляет 30% от объема перфузируемой крови. Способ позволяет повысить эффективность процесса при локальном воздействии на конкретный регион. 2 табл.
Способ улучшения кровоснабжения тканей активированными гуморальными и клеточными элементами крови, заключающийся в том, что осуществляют забор крови, пропускают ее через гемосорбент вне организма с последующим введением в кровоток, отличающийся тем, что осуществляют локальную перфузию конкретного органа или сосудистого региона, в котором локализован патологический процесс, для чего кровь забирают из артерии в объеме 0,5 мл/100 г массы тела со скоростью 0,5 мл/мин и, не выходя из сосуда, с такой же скоростью возвращают кровь через сорбент обратно в артериальный кровоток, причем объем сорбента составляет 30% от объема перфузируемой крови.
| ЖИДКОВ К.П | |||
| и др | |||
| Динамика показателей бласттрансформации лимфоцитов крови в процессе гемосорбции у больных язвенной болезнью | |||
| - Гематология и трансфузиология, 1992, т.37, №3, с | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| УСТРОЙСТВО ДЛЯ ЭКСТРАКОРПОРАЛЬНОЙ ДЕТОКСИКАЦИИ | 1990 |
|
RU2006230C1 |
| СПОСОБ ПРОВЕДЕНИЯ ПЛАЗМОСОРБЦИИ | 1999 |
|
RU2162344C1 |
| RU 96113402 А, 20.02.1999 | |||
| WO 9302777 A1, 18.03.1993 | |||
| КУЗНЕЦОВ С.И | |||
| Эффекторные механизмы гемоперфузии | |||
| - Эфферентная терапия | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| ЛОПАТКИН Н.А | |||
| и др | |||
| Эфферентные методы в медицине | |||
| - М.: Медицина, 1989, с | |||
| Солесос | 1922 |
|
SU29A1 |
Авторы
Даты
2003-04-27—Публикация
2001-11-19—Подача