Изобретение относится к разделу медицины, посвященному биохимической лабораторной диагностике в клинической кардиологии.
Проблема возникновения и становления ГБ сохраняет свою актуальность, поскольку ГБ является одной из наиболее распространенных патологий сердечно-сосудистой системы и основным фактором риска в развитии ишемической болезни сердца, инфаркта миокарда, сосудистых катастроф и внезапной смерти. По данным выборочных исследований 25-30% населения России страдают артериальной гипертонией (АГ) (Арабидзе Г.Г. и др. - Кардиология. - 1990. - 7. - С.107-110; Оганов Р.Г. и др. - Тер. архив. - 1997. - 8. - С.66-69). Специальными исследованиями показано, что у пришлого населения Заполярья АГ диагностируется значительно чаще, чем у того же контингента в других климатогеографических зонах России. Среди основных особенностей АГ у пришлого населения Крайнего Севера выделяются: раннее начало, частота и выраженность кризов по церебральному и кардиальному типу, инсульты и инфаркты миокарда, высокие темпы увеличения массы миокарда левого желудочка (Казначеев В.П. Клинические аспекты полярной медицины. - М.: Медицина, 1986. - 206 с.). Исследования, проведенные непосредственно в экстремальных условиях Тюменского Заполярья, показали высокую распространенность АГ у лиц, занятых экспедиционно-вахтовой формой труда (Гапон Л.И., Вершинина А.М. - Материалы междунар. мед. конф. "Проблемы охраны здоровья и социальные аспекты освоения газовых и нефтяных месторождений в Арктических регионах". - Надым, 1993. -С. 37). Показано, что, помимо клинических особенностей, развитие и течение АГ в условиях Крайнего Севера сопровождается более выраженными мембранодестабилизирующими процессами, в частности чрезмерной активацией процессов перекисного окисления липидов (ПОЛ), ослаблением антиоксидантной защиты (АОЗ), более грубым нарушением липидного спектра клеточных мембран в сравнении с АГ умеренной климатической зоны (Вершинина А.М. и др. - Тер. архив. - 1998. - 12. - С. 24-28; Владимиров Ю. А. и др. Перекисное окисление липидов в биологических мембранах. - М: Медицина, 1972. - 204 с.). В связи с этим является актуальным вопрос ранней диагностики ГБ в условиях Крайнего Севера. Результаты проведенных эпидемиологических исследований показали, что у лиц, мигрировавших на Крайний Север из зон умеренной климатической зоны, уже в первые годы в процессе адаптации к экстремальным условиям региона отмечается повышение артериального давления (АД), не обусловленное на начальном этапе развитием ГБ как заболевания (Айдаралиев А.А. и др. Адаптация человека к экстремальным условиям, - Л.: Наука, 1988. - 125 с.). По данным рекомендаций экспертов Всемирной организации здравоохранения с целью выявления начальной стадии ГБ, так называемой пограничной артериальной гипертонии, необходимо проведение в амбулаторных условиях не менее трехкратного измерения АД с интервалом в неделю по стандартной методике (метод Короткова), а также исключение признаков гипертрофии левого желудочка по ЭКГ, гипертонических изменений на глазном дне, исключение симптоматического характера АГ в результате проведенного специального исследования (согласно рекомендации ВКНЦ) (Кушаковский М. С. Гипертоническая болезнь, С.-П.: Сотис, 1995. - 309 с.; Рекомендации по лечению гипертонии ВОЗ и МОГ. - Клин. фармакол. и терапия, 1999, 8 (3), с.18-23). Однако применение такого метода диагностики ГБ представляет большие практические сложности, особенно для лиц, работающих в сменном режиме по экспедиционно-вахтовому методу в условиях Севера. К тому же, результаты проведенных исследований показали возможность наличия начальных признаков гипертрофии левого желудочка у лиц с пограничной гипертонией, живущих в условиях Севера (Казначеев В.П. Клинические аспекты полярной медицины. -М.: Медицина, 1986. - 206 с.). Все это диктует необходимость поиска новых, совершенных, удобных в практической реализации и нетрудоемких методов диагностики ГБ у лиц, работающих в экспедиционно-вахтовом режиме на Крайнем Севере.
Согласно современным представлениям наиболее перспективными клеточными популяциями в плане изучения патогенетических механизмов ГБ являются нейтрофилы и тромбоциты в силу многогранности своих функциональных возможностей. В клинической практике последних лет имеются попытки применения биохимических методов для оценки структурно-функциональных изменений клеточных мембран в диагностике ГБ.
Для дифференциальной диагностики гипертонической болезни и симптоматических артериальных гипертензий с использованием выявления мембранных нарушений предложен Малишевским М. В. и соавт. (авторское свидетельство СССР 1527586) способ дифференциальной диагностики эссенциальной гипертензии и симптоматической нефрогенной артериальной гипертензии, взятый за прототип. Данный способ основан на определении содержания фракций фосфолипидов: лизофосфатидилхолина (ЛФХ), сфингомиелина (СМ), фосфатидилэтаноламина (ФЭА), а также уровня холестерина (ХС) в мембранах нейтрофилов, выделенных из периферической крови. Диагностический коэффициент (ДК) рассчитывают по формуле: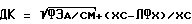
и при значении ДК от 0,1 до 1,8 диагностируют эссенциальную гипертензию, а при значении от 2,0 до 2,8 диагностируют симптоматическую артериальную гипертонию на фоне хронического пиелонефрита. Этот метод достаточно прост и доступен практически любой клинико-биохимической лаборатории. Однако он имеет ряд недостатков. Во-первых, метод предложен только для больных АГ и не позволяет дифференцировать между пациентами АГ и здоровыми лицами с транзиторным повышением АД. Во-вторых, изменения самих нейтрофилов не в полной мере отражают специфику происходящих в организме патологических сдвигов при развитии ГБ у лиц с транзиторным повышением АД.
Целью изобретения является повышение точности и информативности диагностики ГБ в отличие от лиц с транзиторным повышением АД, находящихся в экстремальных условиях Крайнего Севера, на основании использования мембранных тестов.
Суть предлагаемого нами метода диагностики ГБ в условиях Крайнего Севера заключается в заборе крови, выделении тромбоцитов, из мембран которых экстрагируют липиды и получают липидные экстракты, используемые для определения промежуточного продукта процессов перекисного окисления липидов (ПОЛ) - малонового диальдегида (МДА); параллельно проводится исследование внутриклеточного кальция в тромбоцитах с использованием стандартных наборов для определения кальция с последующим вычислением ДК по формуле:
ДК=0,001•МДА+0,05•Са++ - 5,6
и при значении ДК>0 диагностируют ГБ у лиц в условиях Крайнего Севера, при значении же ДК<0 пациент считается нормотензивным.
Предложенная формула получена на основе математического моделирования с использованием дискриминантного анализа. Для построения дискриминантной функции были взяты показатели с достоверным различием их средних значений между группами больных ГБ и здоровыми (см. таблицу). При этом фигурирующие в формуле постоянные величины являются результатом математической обработки измеренных данных с помощью ЭВМ.
Таким образом, предлагаемый диагностический коэффициент отличается от ДК в прототипе не только по используемым показателям, но и по способу математической обработки результатов, измерений.
Эти отличия позволяют сделать вывод о соответствии заявляемого технического решения критерию "новизна".
Признаки, отличающие заявляемое техническое решение от прототипа, не выявлены в других технических решениях при изучении данной и смежной областей медицины и, следовательно, обеспечивают заявляемому решению соответствие критерию "изобретательский уровень".
Способ диагностики ГБ у лиц в условиях Крайнего Севера осуществляется следующим образом.
Для исследования используется Венозная кровь, взятая из локтевой вены. Забор крови в количестве 5 мл производится натощак. В качестве антикоагулянта применяют 3,8% раствор цитрата натрия, смешивая его с кровью в пластиковой пробирке в отношении 1:9. Тромбоциты выделяют из плазмы дифференцированным центрифугированием. Для исследования используют обогащенную тромбоцитами плазму, предварительно отцентрифугированную при 1800 об/мин 10 мин. К осадку добавляют 5 мл буфера Тироде (рН 6,5; to - 37oС), центрифугируют при 1200 об/мин 10 мин, после чего к осадку вновь добавляют 2,5 мл буфера Тироде (рН 7,4; to - 37oС). Состав буфера Тироде: NaCl - 8,77 г, КСl - 0,20 г, NaH2PO4 - 0,74 г, Mg2SO4 - 0,12 г, глюкоза - 0,90 г, Н2О - до одного литра. Из тромбоцитарной взвеси готовят экстракты спирт-эфирной смесью (3:1), в которых определяют содержание МДА.
Определение МДА проводили путем растворения экстракта 0,8% ТБК (тиобарбитуровой кислоты) и 17% ТХУ в соотношении 1:2, после кипячения в течение 20 мин и центрифугирования 10 мин при 3000 об/мин производили замер на спектрофотометре СФ-46 при длине волны 532 нм. Расчет производили по формуле: Е•256,4. Результат выражали в тромбоцитах в нмоль/106 кл.
Определение внутриклеточного кальция тромбоцитов (с помощью набора реактивов фирмы "Лахема") проводят из тромбоцитарной взвеси. К 0,2 мл взвеси приливают 0,2 мл дистиллированной воды, тщательно перемешивают встряхиванием, затем приливают 0,2 мл 20% ТХУ и снова перемешивают. Одновременно ставят холостую и калибровочную пробы: в холостую - 0,2 мл дистиллированной воды и 0,2 мл ТХУ; в калибровочную - 0,02 мл стандартного раствора + 0,2 мл дистиллированной воды + 0,2 мл ТХУ. Опытную пробу центрифугируют 10 мин при 3000 об/мин и надосадочную часть (0,4 мл) переносят в новую пробирку. Во все пробирки приливают по 1,5 мл боратного буфера, затем через 1,5 мин. по 0,5 мл раствора ГБОА и еще через 1,5 мин по 1,0 мл смеси метанола с ацетоном. Замер проводят через 5-10 мин при 540 нм против холостой пробы.
Расчет:
Ео/Ек•0,25=нмоль/106 кл,
где Ео - экстинция опытной пробы;
Ек - экстинция калибровочной пробы.
Реактивы: 1.20% трихлоруксусная кислота (ТХУ): 20 г ТХУ растворить в 80 мл дистиллированной воды.
2. Боратный буфер рН 12,6: 10 г NaOH и 10 г тетрагидробората натрия (бура) растворяют в воде и добавляют объем до 1 л или 2 г едкого натра и 2 г буры растворить и довести до 200 мл дистиллированной водой.
3. 0,055 раствор ГБОА в метаноле (используют реактивы из набора): 10 мл ГБОА растворяют в 20 мл метанола. Раствор может храниться несколько дней в холодильнике, но лучше готовить небольшое количество реактива (на 1-2 дня работы).
4. Смесь ацетона с метанолом 1:9. Может быть использован чистый метанол.
5. Калибровочный раствор: 2,5 ммоль/л Са: 5 мл эталонного раствора из набора разбавляют в мерной колбе до 50 мл. Раствор устойчив при хранении.
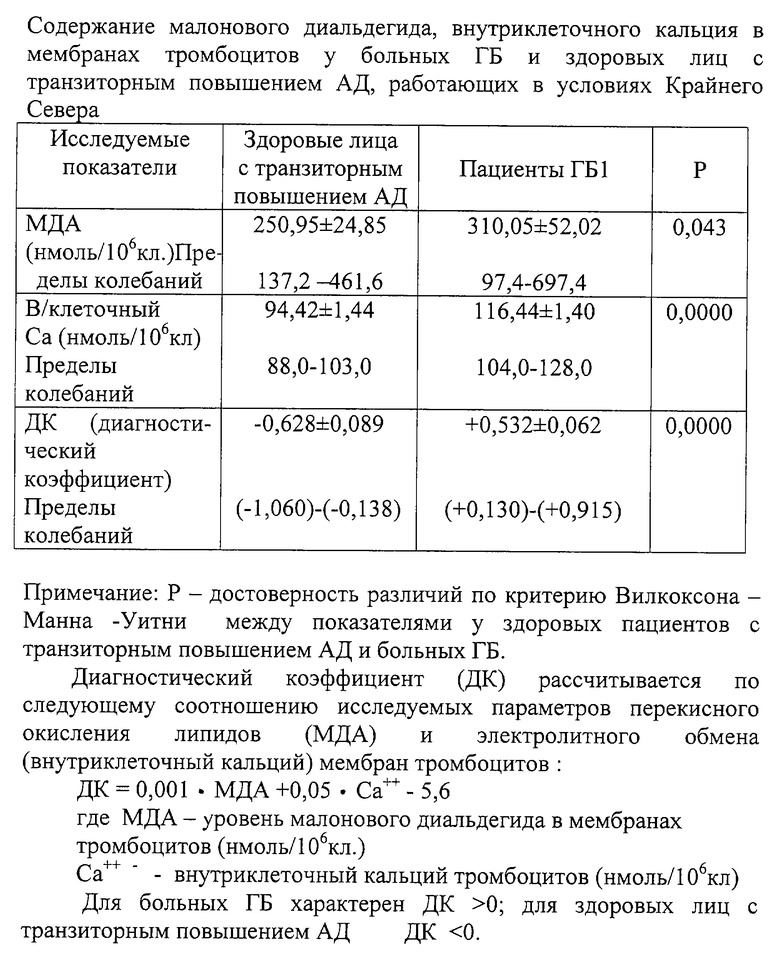
Нами непосредственно в экстремальных условиях Крайнего Севера (заполярный поселок Ямбург) в результате скриннинговых обследований отобрано 78 нелеченных лиц мужского пола, работающих в экспедиционно-вахтовом режиме, в возрасте 20-50 лет. Всем лицам проводилось анкетирование, клинический осмотр кардиолога с контролем АД по стандартизованной методике, электрокардиография, эхокардиография и ультразвуковое исследование внутренних органов. Проводился осмотр глазного дна, выполняли общий анализ крови и мочи. С целью исключения ИБС проводили велоэргометрическую пробу и тест чреспищеводной электрокардиостимуляции. В группе отобранных лиц гипертоническая болезнь (ГБ1) диагностирована у 52 человек, у 26 лиц, признанных практически здоровыми, отмечалось транзиторное повышение АД. Диагноз ГБ устанавливали на основании критериев ВОЗ (1978). Клиническое обследование на уровне 1-го этапа двухэтапной схемы диагностики АГ (Г.Г. Арабидзе и соавт., 1979) позволяло исключить у больных симптоматическую АГ. В последующем отобранные лица были госпитализированы в отделение артериальной гипертонии Тюменского кардиологического центра с целью детального обследования, подбора фармакотерапии согласно выполняемой научной программе. Симптоматический генез артериальной гипертонии исключался по общепринятой двухэтапной схеме с использованием современного лабораторного, инструментального, ультразвукового, радионуклеидного и рентгенологического обследования. Окончательный диагноз устанавливался на основе критериев классификации ВОЗ. Средние цифры АД в группе пациентов ГБ1 на момент обследования были 148,8±1,6/100,6±0,4 мм рт.ст., при этом среднее АД было равно 115,3±0,5 мм рт.ст. В группе практически здоровых лиц с явлениями транзиторного повышения АД цифры его соответственно составили 112,8±1,1/80,4±0,4 мм рт.ст. и 96,5±0,6 мм рт.ст.
В результате проведенных исследований выявлены следующие значения исследуемых параметров для пациентов с ГБ1 и здоровых лиц с транзиторным повышением АД (см. таблицу).
Клинические примеры
1. Больной К., 39 лет, работает по экспедиционно-вахтовому методу в условиях Заполярья в течение 6 лет (постоянное место жительства - Башкирия). На протяжении 2-х лет отмечает повышение АД до цифр 160-170/100 мм рт.ст. с возможной спонтанной нормализацией (четкого контроля АД не проводилось). Отягощена наследственность по ГБ. Убедительных клинико-анамнестических данных за симптоматический генез АГ нет. По результатам экспедиционного клинико-инструментального обследования предположено наличие у пациента ГБ.
При исследовании состояния продуктов перекисного окисления липидов (ПОЛ: МДА) и электролитного обмена (внутриклеточный кальций) мембран тромбоцитов выявлено: уровень МДА 588,6 нмоль/106 клеток, Са 115 нмоль/106кл. ДК=+0,739. Был сделан вывод о наличии у больного ГБ1 ст.
В дальнейшем в результате углубленного стационарного клинико-инструментального обследования в отделении артериальной гипертонии НИИ кардиологии по общепринятой двухэтапной схеме дифференциальной диагностики артериальных гипертензий с полным лабораторным исследованием биохимических параметров крови, комплексного исследования анализов мочи, ультразвуковым исследованием сердца и внутренних органов (включая надпочечники), радионуклеидных методов исследования с помощью гамма-камеры Омега - 500 (США), рентгенологических методов, гормональных исследований крови и мочи, с последующей консультацией окулиста, невропатолога, уролога, научного руководителя отделения артериальной гипертонии выставлен заключительный диагноз ГБ 1 стадии медленно-прогрессирующее течение.
2. Больной Н., 42 лет, уроженец г. Тюмени, работает в условиях Заполярья в экспедиционно-вахтовом режиме 5 лет. В течение 1,5 лет отмечает повышение АД до 160/100 мм рт.ст. Гипотензивной терапии не получал, АД спонтанно нормализуется в условиях пребывания в умеренной климатической зоне. Отягощена наследственность по ГБ. По результатам клинико-инструментального обследования в условиях Севера и исследования состояния продуктов ПОЛ и электролитного гомеостаза (уровень МДА 534,6 нмоль/106 кл. , Са - 114 нмоль/106кл. ДК= +0,6346) был сделан вывод о наличии у больного ГБ 1 ст.
В последующем результатами стационарного углубленного клинико-инструментального обследования в отделении артериальной гипертонии НИИ кардиологии подтвержден диагноз ГБ 1 ст.
3. Больной Л., 32 лет, работает в Тюменском Заполярье в условиях экспедиционно-вахтового режима в течение 4-х лет (уроженец южного района Тюменской области). В течение последнего года наблюдаются эпизодические подъемы АД до 150-160/80-85 мм рт.ст. с последующей спонтанной нормализацией (регулярный контроль АД отсутствует). Наследственность по ГБ не отягощена. В результате экспедиционного клинико-инструментального обследования при дополнительном исследовании состояния продуктов ПОЛ (МДА) и электролитного обмена (внутриклеточный кальций) мембран тромбоцитов (уровень МДА 204,8 нмоль/106 клеток, Са - 92 нмоль/106 кл. ДК=-0,795) было сделано заключение о диагнозе "практически здоров" с имеющими место транзиторными повышениями АД.
В последующем результатами углубленного клинико-инструментального обследования в условиях отделения артериальной гипертонии НИИ кардиологии г. Тюмени был подтвержден диагноз "практически здоров с транзиторными повышениями артериального давления" (диагноз артериальной гипертонии исключен на основании: нормальных цифр АД (110-115/70-75 мм рт.ст.) с первого дня стационарного наблюдения, отсутствие признаков гипертрофии миокарда левого желудочка по данным ЭКГ, ЭХОКГ, отсутствие изменений на глазном дне, отсутствие анамнестических указаний на повышение диастолического артериального давления).
Таким образом, разработанный способ диагностики ГБ у лиц, работающих в экспедиционно-вахтовом режиме на Крайнем Севере, является клинически высокоэффективным, технологически простым и доступным рядовой клинико-биохимической лаборатории практического здравоохранения, безопасен для пациентов, не требует больших затрат времени, дорогостоящей аппаратуры, дефицитных материалов и реактивов и, следовательно, является экономичным.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА У БОЛЬНЫХ АРТЕРИАЛЬНОЙ ГИПЕРТОНИЕЙ | 2006 |
|
RU2316995C1 |
| СПОСОБ ДИАГНОСТИКИ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА У БОЛЬНЫХ С ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНЬЮ | 1998 |
|
RU2145087C1 |
| КАРДИОПРОТЕКТОРНОЕ СРЕДСТВО | 2002 |
|
RU2216337C2 |
| СПОСОБ ОЦЕНКИ КЛИНИЧЕСКОЙ ЭФФЕКТИВНОСТИ ТЕРАПИИ У БОЛЬНЫХ АРТЕРИАЛЬНОЙ ГИПЕРТОНИЕЙ | 2006 |
|
RU2316996C1 |
| СПОСОБ ДИАГНОСТИКИ ХРОНИЧЕСКОЙ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 2001 |
|
RU2200951C2 |
| СПОСОБ ДИАГНОСТИКИ КОРОНАРНОЙ РЕПЕРФУЗИИ У БОЛЬНЫХ ИНФАРКТОМ МИОКАРДА | 2000 |
|
RU2190847C2 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 1995 |
|
RU2122732C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ЭССЕНЦИАЛЬНОЙ ГИПЕРТЕНЗИИ И СИМПТОМАТИЧЕСКОЙ НЕФРОГЕННОЙ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ | 1993 |
|
RU2081420C1 |
| СПОСОБ ДИАГНОСТИКИ ОТКРЫТИЯ КОРОНАРНОЙ АРТЕРИИ У БОЛЬНЫХ ОСТРЫМ ИНФАРКТОМ МИОКАРДА | 1999 |
|
RU2189173C2 |
| СПОСОБ ЛЕЧЕНИЯ МИОКАРДИАЛЬНОГО ДЕФЕКТА ПРИ ОСТРОМ ИНФАРКТЕ МИОКАРДА | 1999 |
|
RU2208399C2 |
Изобретение относится к медицине. Способ включает забор венозной крови, получение тромбицитарных мембран, экстрагирование из них липидов и последующий их анализ. В мембранах тромбоцитов определяют содержание малонового диальдегида (МДА), внутриклеточного кальция (Са++), затем рассчитывают диагностический коэффициент (ДК) по формуле: ДК=0,001•МДА+0,05•Са++ - 5,6, где МДА - уровень малонового диальдегида в мембранах тромбоцитов (нмоль/106кл), Са++ - внутриклеточный кальций тромбоцитов (нмоль/106кл). Для больных ГБ характерен ДК>0, для здоровых лиц с транзисторным повышением АД - ДК<0. Изобретение обеспечивает повышение точности диагностики. 1 табл.
Способ диагностики гипертонической болезни (ГБ), включающий забор крови, получение тромбоцитарных мембран, экстрагирование из них липидов и проведение последующего их анализа, отличающийся тем, что в мембранах тромбоцитов определяют содержание малонового диальдегида (МДА) и внутриклеточного кальция (Са++), затем рассчитывают диагностический коэффициент (ДК)
ДК+0,001•МДА+0,05•Са++ - 5,6,
где МДА - уровень малонового диальдегида в мембранах тромбоцитов (нмоль/106 кл);
Са++ - внутриклеточный кальций тромбоцитов (нмоль),
для больных ГБ характерен ДК больше нуля, для здоровых - с транзисторным повышением АД, ДК меньше нуля.
| Способ дифференциальной диагностики гипертонической болезни и артериальной гипертензии, обусловленной хроническим пиелонефритом | 1988 |
|
SU1527586A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 1995 |
|
RU2102756C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ЭССЕНЦИАЛЬНОЙ ГИПЕРТЕНЗИИ И СИМПТОМАТИЧЕСКОЙ НЕФРОГЕННОЙ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ | 1993 |
|
RU2081420C1 |
| СПОСОБ ДИАГНОСТИКИ ОБОСТРЕНИЯ ХОЛЕЦИСТИТА | 1995 |
|
RU2119670C1 |
| SU 1821743 A1, 15.06.1993 | |||
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 1995 |
|
RU2102756C1 |
| Способ измерения кальция сыворотки крови | 1989 |
|
SU1718116A1 |
Авторы
Даты
2003-04-27—Публикация
1999-12-27—Подача