Изобретение относится к процессу получения смесей водорода и оксида углерода путем каталитического превращения углеводородов в присутствии кислородсодержащих газов и/или паров воды и к катализаторам для этого процесса.
Смеси водорода и оксида углерода (синтез-газ) широко используются в крупнотоннажных химических процессах, таких как синтез метанола и высших спиртов и альдегидов, процесс Фишера-Тропша и других. Для каждого из этих процессов необходим синтез-газ с определенным соотношением концентраций водорода и оксида углерода (H2/CO). Для получения смесей водорода и оксида углерода с тем или иным соотношением Н2/СО используют различные реакции каталитического превращения парафинов [J.R.Rostrup-Nielsen, Production of synthesis gas. Catalysis Today, 1993, v.18, 305-324; B.C. Арутюнов, О.В. Крылов// Окислительные превращения метана. Москва, Наука, 1998]. Наиболее широко используется паровая конверсия природного газа (метана), при которой образуется синтез-газ с соотношением Н2/СО≥3, что удобно только для процесса синтеза аммиака. Кроме того, недостатками этого процесса являются высокая стоимость перегретого пара и образование избыточных количеств двуокиси углерода. При углекислотной конверсии метана можно получать смесь водорода и оксида углерода с соотношением Н2/СО~1, требующимся для реакций гидроформилирования, получения формальдегида и др. Реакции паровой и углекислотной конверсии метана являются эндотермическими, сопровождаются процессами коксообразования и требуют больших энергетических затрат.
Известен также способ получения синтез-газа с соотношением Н2/СО~2 путем селективного каталитического окисления углеводородов кислородом (СКО) [S.C. Tsang, J. B. Claridge and M.L.H.Green, Recent advances in the conversion of methane to synthesis gas, Catalysis Today, 1995, v.23, 3-15]. В отличие от паровой и углекислотной конверсии СКО имеет большую селективность, является экзотермичным процессом и эффективно протекает при малых временах контакта, что дает возможность проводить его в автотермическом режиме и уменьшить размеры реактора [D.A.Hickman, L.D.Schmidt, Synthesis gas formation by direct oxidation of methane, in "Catalytic Selective Oxidation", ACS Symposium series, 1993, p.416-426; P.M.Torniainen, X.Chu and L.D.Schmidt, Comparison of monolith-supported metals for the direct oxidation of methane to syngas. J. Catal., 1994, v.146, 1-10] и тем самым снизить как энергозатраты, так и капитальные вложения. Проведение одновременно экзотермической реакции СКО и эндотермической паровой конверсии природного газа на одном катализаторе позволяет осуществлять процесс получения смесей водорода и оксида углерода, обогащенных водородом, в автотермическом режиме [J.W.Jenkins and E. Shutt, The Hot SpotТМ Reactor, Platinum Metals Review, 1989, 33 (3), 118-127].
Изучение процесса СКО метана в пилотной установке на блочном катализаторе, содержащем Pt-Pd [J.К. Hoshmuth, Catalytic partial oxidation of methane over monolith supported catalyst, Appl. Catal., B: Environmental, v.1 (1992) 89], показало, что при времени контакта ~0.02 с в лобовом слое блока протекает полное окисление метана, а в последующих слоях - паровая и углекислотная конверсия метана. Поэтому для получения максимальных выходов целевого продукта - синтез-газа катализатор должен быть активным одновременно в этих трех реакциях. В соответствии с этим для эффективного протекания медленных реакций конверсии метана требуется катализатор с развитой поверхностью. Одновременно вследствие большого градиента температуры по длине блока катализатор должен иметь высокую термическую устойчивость.
Для проведения процесса СКО при малых временах контакта ~10-2 с используют Pt-Rh сетки или 10% Rh/блочный носитель, что очень дорого и экономически невыгодно [D.A.Hickman. L.D.Schmidt, Synthesis gas formation by direct oxidation of methane, in "Catalytic Selective Oxidation", ACS Symposium series, 1993, p.416-426. P.M.Torniainen, X.Chu and L.D.Schmidt, Comparison of monolith-supported metals for the direct oxidation of methane to syngas, J.Catal., 1994, v.146, 1-10].
Известен способ получения водорода [WO 99/48805, С 01 В 3/40, опубл. 30.09.00] путем проведения СКО и паровой конверсии углеводородов на одном катализаторе в автотермическом режиме: паровую конверсию проводят при введении пара в смесь углеводорода и кислородсодержащего газа после того, как начался процесс СКО и установился автотермический режим. В качестве катализаторов используют родий, нанесенный на термостойкий носитель, содержащий смесь оксидов церия и циркония при весовом отношении Ce/Zr от 0.05 до 19.
Известен способ СКО метана для получения оксида углерода и водорода [US 5149464, С 01 В 3/26, 1992] при температуре 650-900oС и объемной скорости 40000-80000 ч-1 (0,05-0,09 с) в присутствии катализатора, представляющего собой либо переходный металл или его оксид, нанесенный на термостабильный оксид одного из элементов (М): Mg, В, Al, Ln, Ga, Si, Ti, Zr, Hf, либо перовскитоподобный смешанный оксид общей формулы MxM'yOz со структурой пирохлора, где М' - переходный металл, в том числе элементы 8 группы. Атомное отношение элемента 8 группы к сумме неблагородных элементов в этих соединениях 1: 1 или 3:1 и содержание благородных металлов составляет 32,9-48 мас.%. Конверсия метана в присутствии смешанных оксидов Pr2Ru2O7, Eu2Ir2O7, La2MgPtO6 при объемной скорости 40000 ч-1 и 777o не превышает 94%, а увеличение объемной скорости до 80000 ч-1 приводит к снижению конверсии метана до 73% и селективности по СО и водороду до 82 и 90% соответственно.
В европейском патенте [ЕР 303438, С 01 В 3/38, 15.02.89] для получения смеси водорода и оксида углерода предлагают способ СКО углеводородов при контакте реакционной смеси, содержащей углеводород, кислород или кислородсодержащий газ и, необязательно, пары воды, с катализатором в зоне селективного каталитического окисления. Зона СКО содержит катализатор с соотношением: геометрическая поверхность/объем не менее 5 см2/см3. Катализатор может содержать благородные металлы, никель, кобальт, хром, церий, лантан и их смесь, нанесенные на термостойкий оксидный носитель, в том числе кордиерит, муллит, титанат алюминия, циркониевую шпинель, оксид алюминия. В то же время в патенте ЕР 303438 утверждают, что скорость реакции парциального окисления лимитируется скоростью массообмена и не зависит от химической природы катализатора, что позволяет в этом случае использовать материалы, не проявляющие каталитическую активность, но обеспечивающие необходимое соотношение: геометрическая поверхность/объем. Процесс проводят при температурах в интервале 760-1090oС и объемной скорости от 20000 до 500000 ч-1.
В патентах [RU 2115617, С 01 В 3/38, 20.07.98, RU 2136581, С 01 В 3/38, 10.09.99, RU 2137702, С 01 В 3/38, 20.09.99, RU 2123471, С 01 В 3/38, 20.12.98, US 5486313, С 07 С 1/02. 23.01.1996 и US 5639401, С 07 С 1/02, 17.06.97] предлагается способ СКО углеводородов, в том числе серусодержащих (0.05-100 ррм) [RU 2132299, С 01 В 3/38, 27.06.99, US 5720901, C 07 C 1/02, 24.04.98], в синтез-газ с использованием катализаторов, содержащих благородные металлы (до 10 мас.% Pt, Pd, Rh, Os), нанесенные на термостойкий носитель. В качестве носителей используют, например, α-Аl2О3, гексаалюминат бария (зерно размером ~1 мм) или ZrO2, термостабилизированный оксидами элементов групп III В или II А Периодической таблицы (пористые блоки в виде пенокерамики, устойчивые к термоударам). Процесс проводят в реакторе с неподвижным слоем катализатора, имеющим большую извилистость - отношение длины пути газа при прохождении через блок к его длине - в пределах 1.1-10 при температурах 950-1300oС и скорости потока газовой смеси 2-104-108 л/кг-ч. Недостатками такого способа являются большое гидравлическое сопротивление слоя катализатора с высокой извилистостью и высокая стоимость катализаторов вследствие большого содержания благородных металлов и использования в качестве носителя дорогостоящей пенокерамики на основе циркония, ограничивающая их практическое применение.
Известен процесс получения синтез-газа [US 5989457, С 07 С 1/02, 23.11.99] при взаимодействии метана или углеводородов или их смеси с двуокисью углерода в присутствии катализатора, содержащего от 0.1 до 7 мас.% Pt, Ni, Pd или Со на термостойком носителе, в состав которого входит не менее 80 мас. % ZrO2 и по крайней мере 0.5-10 мол.% одного из оксидов Y, La, Al, Са, Се или Sc. Процесс проводят на катализаторе с размером зерна 0.3-0.6 мм при 700-800oС и объемной скорости потока 12750 ч-1. При этих условиях конверсия метана составляет ~60-70%, выход СО ~30%.
Известен также способ получения смеси водорода и оксида углерода [US 5500149, С 07 С 1/02, 19.03.96] при контакте смеси, содержащей метан, кислород и СО2, при температурах 600-1000oС и объемной скорости ~5000-20000 ч-1 с твердым катализатором в виде зерен ~0.3 мм, отвечающим следующей формуле: MxM'yOz или MxOz или M'yOz на термостойком носителе, где М и М' представляют широкий круг щелочных, щелочноземельных, переходных и других элементов. Предлагаемые катализаторы эффективны как в углекислотной конверсии метана, так и при сочетании реакций селективного каталитического окисления и углекислотной конверсии метана. Вариация состава реакционной смеси позволяет варьировать состав получаемого синтез-газа и регулировать тепловой баланс процесса.
В патенте [US 5741440, С 01 В 3/38, 21.04.98] предлагают способ получения смеси водорода и оксида углерода при контакте реакционной смеси, содержащей двуокись углерода, водород, по крайней мере один углеводород и, необязательно, пар, с катализатором на основе Pt или Ni, нанесенных на термостабильный оксид (Аl2О3, MgO) при температурах 650-1450oС. Замена в исходной смеси, по крайней мере, части паров воды водородом позволяет увеличить количество синтез-газа и снизить содержание двуокиси углерода в конечном газе, а вариация состава исходной смеси - получать смесь водорода и оксида углерода с соотношением Н2/СО от 0.7 до 3. Отметим, что для смесей без воды для получения синтез-газа с Н2/СО≥2 необходима высокая концентрация водорода в исходной смеси, что увеличивает затраты на производство конечного продукта.
В патенте [US 5855815, С 07 С 1/02, 05.01.99] предлагают получать синтез-газ путем восстановления двуокиси углерода смесью природного газа, кислорода и пара в присутствии катализатора, содержащего никель и промоторы - щелочные или щелочно-земельные элементы, нанесенные на кремний-содержащий носитель, такой как силикагель, силикат, алюмосиликат или цеолит (пентасил). Последний носитель имеет поверхность от 300 до 600 м2/г. Процесс проводят при 600-1000oС и объемной скорости 1000-500000 ч-1, отношение Н2/СО изменяется в пределах 1/3-3/1.
Таким образом, для получения смеси водорода и оксида углерода с различным соотношением Н2/СО используют как процесс СКО, так и его комбинацию с эндотермическими процессами конверсии углеводородов при малых временах контакта реакционной смеси с катализатором, который должен отвечать жестким требованиям: иметь малое гидравлическое сопротивление, высокую термостабильность, обеспечивать высокие конверсии углеводородов и селективность по водороду и оксиду углерода и при этом не дезактивироваться из-за образования углерода на поверхности. Кроме того, природный газ часто содержит серусодержащие примеси и катализатор должен быть устойчивым к ним.
Известно, что высокая термостабильность и устойчивость к тепловым ударам материалов тем выше, чем ниже их коэффициент термического расширения [D.L. Trimm, Catalytic combustion (Review), Appl.Catal. 7(1983), 249-282]. Известные катализаторы процессов получения смеси водорода и оксида углерода, как правило, содержат оксиды, например α-Аl2О3, имеющий положительный коэффициент термического расширения. Известен способ снижения объемного коэффициента термического расширения (КТР) материалов [US 5919720, С 04 В 035/10, 06.07.99] , в котором используются композиции, включающие вещества с отрицательным или близким к нулю КТР общей формулы
А2-x 3+Аy 4+Мz 3+М3-y 6+РyО12,
где А3+ и М3+ - металл, имеющий состояние окисления 3+ (Al, Cr, Fe, Er, Ga, In, Lu, Sc, Tm, Y, Yb и их смесь, А4+ - металл, имеющий состояние окисления 4+ (Hf, Zr), M6+ - металл, имеющий состояние окисления 6+(W, Мо и их смесь), у - изменяется от 0 до 2, х=y+z и изменяется от 0,1 до 1,9.
Наиболее близким к заявленному по технической сущности и достигаемому эффекту является способ СКО для получения синтез-газа в присутствии катализаторов на основе смешанных оксидов со структурой перовскитов [Пат. РФ 2144844, B 01 J 23/10, С 01 В 31/18, 27.01.2000]. Процесс СКО метана проводят в присутствии перовскитов общей формулы АВОx или AB1-yMyOx, где А - редкоземельный элемент (например, La), В - переходный элемент (например, Ni), М - благородный металл, нанесенных на блоки сотовой структуры из α-Al2O3, при объемной скорости 25000-200000 ч-1. При температурах 700-850oС достигаются высокие конверсии метана и селективность по синтез-газу. Однако перовскиты - сложные оксиды, содержащие переходные металлы, в большой степени подвержены отравлению серусодержащими соединениями. Кроме того, носитель сотовой структуры подвержен растрескиванию вследствие положительного КТР корунда.
Изобретение решает задачу создания термостабильного катализатора для получения смеси водорода и оксида углерода, эффективного при малых временах контакта как в реакциях селективного каталитического окисления углеводородов кислородом, так и паровой и углекислотной конверсии углеводородов, в том числе в присутствии серусодержащих соединений, и процесса получения смеси водорода и оксида углерода с использованием этого катализатора.
Задача решается за счет использования катализатора, являющегося сложным композитом и содержащего смешанные оксиды со структурой перовскита или флюорита и переходные и/или благородные металлы и дополнительно компоненты с низким коэффициентом термического расширения и осуществления каталитического превращения смеси, содержащей углеводород или смесь углеводородов и/или воздух, или СО2, или пар, или их смесь, а также, необязательно, серусодержащие соединения, в присутствии этого катализатора. При этом сохраняются высокие конверсия метана и селективность, термостабильность катализатора, отсутствует его зауглероживание и отравление серусодержащими соединениями.
Указанный технический результат достигается использованием катализатора, имеющего состав, мас.%:
Переходный или благородный элемент - Не более 10
Смешанный оксид - Не менее 1
Материал с ультранизким коэффициентом термического расширения не выше 8•10-6 град-1 - Не более 95
Al2O3 - Остальное
Смешанный оксид включает оксид со структурой перовскита M1B1-yMyOz и/или оксид со структурой флюорита M1 xM2 1-xOz, где:
М - элемент 8 группы (Pt, Rh, Ir),
М1 - редкоземельный или щелочноземельный элемент,
М2 - элемент IV b группы Периодической системы (Zr, Hf),
В - переходный элемент - 3d элементы 4-го периода,
0,01<х<1,0≤y<1, z определяется степенью окисления катионов и их стехиометрическим соотношением.
Под термином "редкоземельный элемент" подразумевают элементы, относящиеся к группе редкоземельных элементов, включающей элементы группы III b Периодической системы и 4f элементы, например La, Ce, Nd.
Под термином щелочноземельный элемент подразумевают элементы группы II а Периодической системы, например Sr, Ca.
Введение в состав высокотемпературных катализаторов компонентов с низким или отрицательным КТР позволяет регулировать их коэффициент термического расширения и тем самым получать катализаторы с высокой термоустойчивостью. В качестве компонентов, имеющих низкий или отрицательный коэффициент термического расширения, используют кордиерит, муллит, сложные фосфаты циркония со структурой NZP, вольфраматы (M2W3O12, MW2O8), молибдаты, ванадаты (MV2O7), титанат алюминия.
Полученный сложный композит - катализатор имеет поверхность 2-200 м2/г. Катализатор имеет форму таблеток, колец, сфер, блоков сотовой структуры.
Процесс проводят путем последовательного пропускания газовой смеси, содержащей углеводород, или смесь углеводородов и/или воздух, или пар, или их смесь с температурой 20-500oС через неподвижный слой катализатора, который состоит из 1-20 рядов.
Для получения необходимого состава смеси водорода и оксида углерода варьируют состав исходной смеси. Исходная смесь содержит углеводород или смесь углеводородов и/или воздух, или СО2, или пар, или их смесь, а также, необязательно, серусодержащие соединения, процесс проводят при температурах 500-1000oС. В качестве углеводородного сырья используют, например, природный газ, метан, пропан-бутановую смесь, смесь более тяжелых углеводородов, керосин и т.д. В качестве кислородсодержащего газа - кислород, воздух, двуокись углерода, воду.
Предлагаемые катализаторы готовят с использованием методов смешения и пропитки с последующей сушкой и прокалкой. Процесс получения смеси водорода и оксида углерода проводят в проточном реакторе при температуре 550-1000oС, вариации времени контакта и состава реакционной смеси. Состав исходной реакционной смеси и продукты реакции анализируют хроматографически. Эффективность работы катализатора характеризуют степенью превращения метана, селективностью по СО и водороду, количеством полученной смеси водорода и оксида углерода и их соотношением. Материальный баланс по углероду во всех случаях составлял 100±2%.
Сущность изобретения иллюстрируется следующими примерами.
Пример. 1. Для приготовления блоков из Аl2О3 в лопастном смесителе объемом 5 л смешивают порошки гидроксида алюминия, содержащего 70 мас.% псевдобемита, и высокотемпературного оксида, содержащего 35 мас.% корунда, в количестве по 1000 г с добавлением 25 г структурообразующей добавки (древесной муки)* и 6 г поверхностноактивного вещества (глицерина)* в присутствии пептизатора - 6% азотной кислоты. Полученную пасту формуют в виде черенков или блоков сотовой структуры через специальную насадку. Далее Аl2О3 сушат и прокаливают при 800-1300oС. Удельная поверхность - 2-200 м2/г. Для определения КТР формуют трубочки с наружным диаметром 6 мм, внутренним - 2,5 мм и прокаливают при 1300oС. Средний КТР в интервале температур 20-1000oС составляет 5•10-6 град-1.
Пример 2. Для приготовления смешанного каркасного фосфата циркония, кальция и стронция со структурой NZP смешивают стехиометрические количества растворов нитратов кальция, стронция и оксинитрата циркония. Медленно, при непрерывном перемешивании приливают стехиометрическое количество раствора фосфорной кислоты. Полученный гель сушат и прокаливают при температуре 1300oС. Полученный порошок фосфата имеет состав Ca0,5Sr0,5Zr4P6O24 и структуру типа NZP. Этот порошок помещают в смеситель, добавляют исходный гель и перемешивают. Полученную массу формуют в виде блоков, сушат и прокаливают при 1300oС. Для определения КТР формуют трубочки с наружным диаметром 6 мм, внутренним - 2,5 мм. Средний КТР в интервале температур 20-1000oС составляет ~1•10-6 град-1.
Пример 3. В лопастном смесителе в присутствии азотной кислоты смешивают порошки Са0,5Sr0,5Zr4Р6O24, полученного, как в примере 2, и гидроксида алюминия, взятые в равном количестве. Полученную массу формуют, сушат и прокаливают при 1300oС. Для определения КТР формуют трубочки с наружным диаметром 6 мм, внутренним 2,5 мм. Средний КТР в интервале температур 20-1000oС составляет ~1•10-6 град-6.
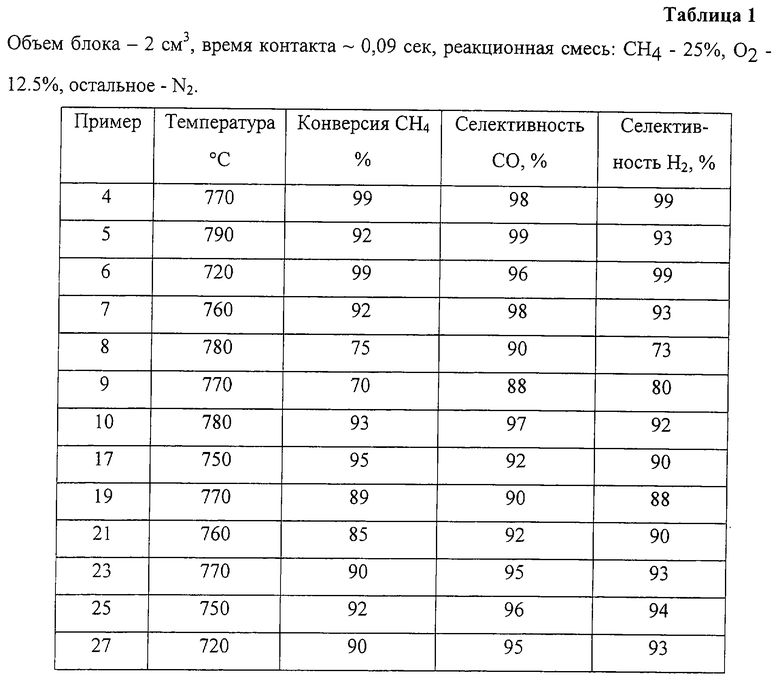
Пример 4. Al2O3 в виде микроблока с поверхностью 100 м2/г, приготовленный, как в 1, прокаливают при 800oС, пропитывают с учетом влагоемкости смешанным раствором солей церия и циркония с атомным соотношением Ce/Zr=0,8: 0,2. После пропитки катализатор сушат и прокаливают на воздухе при 900oС 2 часа. Полученный образец пропитывают раствором H2PtCl6, сушат и прокаливают при 900oС. Полученный катализатор, содержащий 10 мас.% смешанного оксида церия и циркония и 0,3 мас.% Pt, испытывают в проточном реакторе при составе реакционной смеси: СН4 - 25%, O2 - 12.5%, остальное - N2 и времени контакта ~0,09 с, активность приведена в табл. 1.
Пример 5. Аl2O3 в виде микроблока с поверхностью 100 м2/г, приготовленный, как в 1, пропитывают с учетом влагоемкости смешанным раствором солей церия и циркония с мольным соотношением церия и циркония 0,8:0,2. После пропитки катализатор сушат и прокаливают на воздухе при 900oС 2 часа. Процедуру пропитки повторяют. Полученный образец пропитывают совместным раствором H2PtCl6 и RhCl3, сушат и прокаливают при 900oС. Полученный образец содержит, мас. %: 16 смешанного оксида церия и циркония, 0,3 Pt, 0,3 Rh. Испытания проводят, как в 4, активность приведена в табл. 1.
Пример 6. Катализатор готовят, как в примере 4, за исключением того, что образец пропитывают раствором солей церия и циркония с мольным соотношением церия и циркония 0,5: 0,5. Полученный образец содержит 7 мас.% смешанного оксида церия и циркония, 0,3 мас.% Pt. Испытания проводят, как в примере 4, активность приведена в табл.1.
Пример 7. Аl2О3 в виде микроблока с поверхностью 2 м2/г, приготовленный, как в 1, прокаливают при 1300oС и пропитывают с учетом влагоемкости смешанным раствором солей с мольным соотношением церия и циркония 0,2:0,8. После пропитки катализатор сушат и прокаливают на воздухе при 900oС 2 часа. Полученный образец пропитывают раствором H2PtCl6, сушат, прокаливают и испытывают, как в примере 4, активность приведена в табл.1. Полученный образец содержит 8,5 мас.% смешанного оксида церия и циркония, 1 мас.% Pt.
Пример 8. Катализатор готовят, как в примере 7, за исключением того, что для пропитки используют смешанный раствор солей кальция и циркония с мольным соотношением Ca: Zr= 0,05: 0,95. Полученный образец содержит 7,5 мас.% смешанного оксида кальция и циркония, 1 мас.% Pt. Испытывают, как в примере 4, активность приведена в табл. 1.
Пример 9. Катализатор готовят и испытывают, как в примере 7, за исключением того, что для пропитки используют блок, приготовленный, как в 2. Полученный образец содержит 8 мас.% смешанного оксида церия и циркония, 1 мас.% Pt. Испытывают, как в примере 4, активность приведена в табл. 1.
Пример 10. Катализатор готовят и испытывают, как в примере 7, за исключением того, что для пропитки используют блок, приготовленный, как в 3. Полученный образец содержит 7,8 мас.% смешанного оксида церия и циркония, 1 мас.% Pt. Испытывают, как в примере 4, активность приведена в табл. 1.
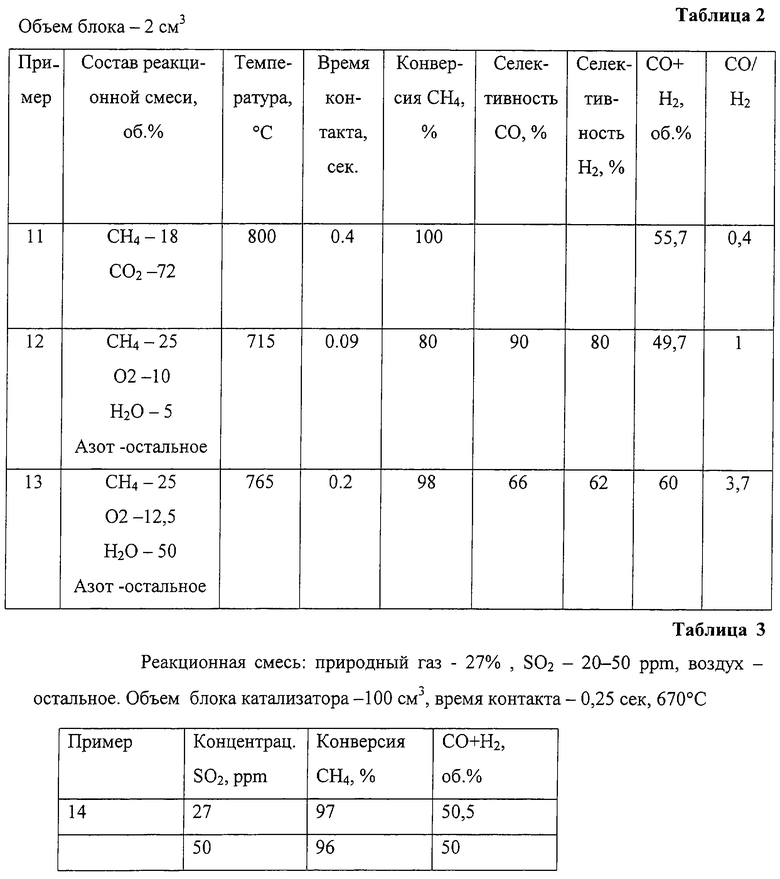
Пример 11. Катализатор готовят, как в примере 7, за исключением того, что для пропитки используют вместо H2PtCl6 раствор нитрата никеля. Образец содержит 8 мас.% смешанного оксида церия и циркония и 2,5 мас.% Ni и испытывают в реакции углекислотной конверсии метана. Условия испытаний и активность приведены в табл. 2.
Пример 12. Катализатор готовят, как в примере 4, и испытывают в реакции селективного окисления метана в присутствии паров воды. Условия испытаний и активность приведены в табл. 2.
Пример 13. Катализатор готовят, как в примере 7, и испытывают в реакции паровой конверсии метана. Условия испытаний и активность приведены в табл. 2.
Пример 14. Катализатор готовят, как в примере 7, за исключением того, что для пропитки вместо H2PtCl6 используют смешанный раствор H2PtCl6, нитратов лантана и никеля с атомным отношением катионов La:Ni:Pt=1:0,994:0,006. Полученный катализатор содержит 7 мас.% перовскита LaNi0,994Pt0,006 и 10 мас. % смешанного оксида церия и циркония. Катализатор испытывают в реакции селективного окисления природного газа в присутствии SO2. Активность приведена в табл. 3.
Пример 15. В реактор загружают два слоя катализатора: 1 слой - катализатор готовят, как в примере 14, второй слой - катализатор готовят, как в примере 7. Проводят реакцию селективного окисления природного газа. Активность приведена в табл. 4.
Пример 16. В лопастном смесителе в присутствии азотной кислоты смешивают порошки кордиерита и гидроксида алюминия, взятые в равном количестве. Полученную массу формуют в тонкостенные микроблоки, сушат и прокаливают при 1300oС. Для определения КТР формуют трубочки с наружным диаметром 6 мм, внутренним - 2,5 мм. Средний КТР в интервале температур 20-1000oС составляет ~0,9•10-6 град-1.
Пример 17. Катализатор готовят, как в примере 4, за исключением того, что в качестве носителя используют блок, приготовленный, как в примере 16. Полученный образец содержит 7 мас.% смешанного оксида церия и циркония, 0,3 мас. % Pt. Испытания проводят, как в примере 4, активность приведена в табл. 1.
Пример 18. В лопастном смесителе в присутствии азотной кислоты смешивают порошки высокодисперсного Al2TiO5, предварительно отожженного при 1500o, и гидроксида алюминия, взятые в равном количестве. Полученную массу формуют, сушат и прокаливают при 1300oС. Для определения КТР формуют трубочки с наружным диаметром 6 мм, внутренним - 2,5 мм. Средний КТР в интервале температур 20-1000oС составляет ~0,5•10-6 град-1.
Пример 19. Катализатор готовят, как в примере 4, за исключением того, что в качестве носителя используют блок, приготовленный, как в примере 18. Полученный образец содержит 7 мас.% смешанного оксида церия и циркония, 0,3 мас. % Pt. Испытания проводят, как в примере 4, активность приведена в табл. 1.
Пример 20. Носитель готовят, как в примере 16, за исключением того, что используют муллит и гидроксид алюминия. Средний КТР в интервале температур 20-1000oС составляет ~1•10-6 град-1.
Пример 21. Катализатор готовят, как в примере 4, за исключением того, что в качестве носителя используют блок, приготовленный, как в примере 20. Полученный образец содержит 7 мас.% смешанного оксида церия и циркония, 0,3 мас. % Pt. Испытания проводят, как в примере 4, активность приведена в табл. 1.
Пример 22. Носитель готовят, как в примере 16, за исключением того, что используют вольфрамат циркония и гидроксид алюминия. Средний КТР в интервале температур 20-1000oС составляет ~5•10-7 град-1.
Пример 23. Катализатор готовят, как в примере 4, за исключением того, что в качестве носителя используют блок, приготовленный, как в примере 22. Полученный образец содержит 7 мас.% смешанного оксида церия и циркония, 0,3 мас. % Pt. Испытания проводят, как в примере 4, активность приведена в табл. 1.
Пример 24. Носитель готовят, как в примере 16, за исключением того, что используют молибдат скандия и гидроксид алюминия. Средний КТР в интервале температур 20-1000oС составляет ~2•10-7 град-1.
Пример 25. Катализатор готовят, как в примере 4, за исключением того, что в качестве носителя используют блок, приготовленный, как в примере 24. Полученный образец содержит 7 мас.% смешанного оксида церия и циркония, 0,3 мас. % Pt. Испытания проводят, как в примере 4, активность приведена в табл. 1.
Пример 26. Носитель готовят, как в примере 16, за исключением того, что используют ванадат циркония и гидроксид алюминия. Средний КТР в интервале температур 20-1000oС составляет ~6•10-7 град-1.
Пример 27. Катализатор готовят, как в примере 4, за исключением того, что в качестве носителя используют блок, приготовленный, как в примере 26. Полученный образец содержит 7 мас.% смешанного оксида церия и циркония, 0,3 мас. % Pt. Испытания проводят, как в примере 4, активность приведена в табл. 1.
Как видно из приведенных примеров и таблицы, разработан термостабильный катализатор для получения смеси водорода и оксида углерода, эффективный при малых временах контакта как в реакциях селективного каталитического окисления углеводородов кислородом, так и паровой и углекислотной конверсии углеводородов, в том числе в присутствии серусодержащих соединений.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОР (ВАРИАНТЫ), СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ (ВАРИАНТЫ) И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2003 |
|
RU2248932C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2003 |
|
RU2248240C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2005 |
|
RU2292237C1 |
| СПОСОБ ОЧИСТКИ ВОДОРОДСОДЕРЖАЩЕЙ ГАЗОВОЙ СМЕСИ ОТ ОКСИДА УГЛЕРОДА | 2002 |
|
RU2211081C1 |
| КАТАЛИЗАТОР И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2010 |
|
RU2453366C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2003 |
|
RU2244589C1 |
| КАТАЛИЗАТОР И СПОСОБ ПОЛУЧЕНИЯ ЗАКИСИ АЗОТА | 2002 |
|
RU2212933C1 |
| КАТАЛИЗАТОР И СПОСОБ ПОЛУЧЕНИЯ ЗАКИСИ АЗОТА | 2002 |
|
RU2212932C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРОДА И УГЛЕРОДНОГО МАТЕРИАЛА | 1999 |
|
RU2160698C1 |
| КАТАЛИЗАТОР, НОСИТЕЛЬ КАТАЛИЗАТОРА, СПОСОБ ИХ ПРИГОТОВЛЕНИЯ (ВАРИАНТЫ) И СПОСОБ ОЧИСТКИ ОТХОДЯЩИХ ГАЗОВ ОТ ОКСИДОВ АЗОТА | 2001 |
|
RU2199389C1 |

Изобретение относится к процессу получения смесей водорода и оксида углерода путем каталитического превращения углеводородов в присутствии кислородсодержащих газов и/или паров воды. Описан катализатор, являющийся сложным композитом и содержащий смешанные оксиды со структурой перовксита или флюорита и переходные и/или благородные металлы, который дополнительно содержит компоненты с низким коэффициентом термического расширения. Описан способ каталитического превращения смеси, содержащей углеводород, или смесь углеводородов и/или воздух, или СО2, или пар, или их смесь, а также, необязательно, серусодержащие соединения. Технический результат: получен катализатор с улучшенной термостабильностью, устойчивый к зауглероживанию и отравлению серусодержащими соединениями. 2 с. и 4 з.п.ф-лы, 4 табл.
Переходный элемент и/или благородный элемент - Не более 10
Смешанный оксид - Не менее 1
Материал с ультранизким коэффициентом термического расширения не выше 8•10-6 см/град - Не более 95
Al2O3 - Остальное
при этом материал с ультранизким коэффициентом термического расширения выбран из группы: кордиерит, сложные фосфаты циркония со структурой NZP, титанат алюминия, муллит, вольфраматы, молибдаты, ванадаты, смешанный оксид включает оксид со структурой перовксита
M1B1-yMyOz
и/или оксид со структурой флюорита
Мx 1М1-x 2Оz,
где М - элемент 8 группы, например Pt, Rh, Ir;
М1 - редкоземельный элемент, например La, Ce, Nd или щелочноземельный, например Са, Sr;
М2 - элемент IVb группы Периодической системы, например Zr, Hf;
В - переходный элемент - 3d элементы 4-го периода, например Ni, Co;
0,01<х<1;
0<у<1;
z определяется степенью окисления катионов и их стехиометрическим соотношением.
| КАТАЛИЗАТОР (ЕГО ВАРИАНТЫ) И ПРОЦЕСС ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 1997 |
|
RU2144844C1 |
| RU 2058813 C1, 27.04.1996 | |||
| СПОСОБ КОРРЕКЦИИ ФИГУРЫ (ВАРИАНТЫ) | 2003 |
|
RU2239406C1 |
| US 5338488 A1, 16.08.1994. | |||
Авторы
Даты
2003-05-20—Публикация
2001-05-08—Подача