Изобретение относится к новым генам, кодирующим деацетилазы аминокислот со специфичностью к N-ацетил-L-фосфинотрицину, их выделению и применению.
Концепция химически индуцируемой обратимой мужской стерильности у растений путем пыльник-специфической экспрессии N-ацетил-фосфинотрицин далее (N-ацетил-ФФТ)-специфической деацетилазы описана в европейском патенте ЕР 531716. Применяемые при этом гены деацетилазы из Streptomyces viridochromogenes [N-ацетил-L-фосфинотрицил-аланил-аланин(N-ацетил-ФФТ)-деацетилаза, деа] или argE из Esterichia coli (N-ацетил-L-орнитин-деацетилаза) кодируют белки со специфичностью к N-ацетил-L-ФФТ. Для обоих генов могло быть показано при специфической экспрессии в оболочках растений появление цветов с мужской стерильностью после обработки отдельных почек N-ацетил-L-ФФТ. Для успешного применения этой системы, в частности при обработке целых растений N-ацетил-ФФТ в практически релевантных условиях, является предпочтительным использование деацетилазы с высоким сродством к субстрату. Поэтому были предприняты поиски других деацетилаз с высоким сродством к N-ацетил-ФФТ.
Задачей данного изобретения является, таким образом, получение в распоряжение молекул ДНК, кодирующих деацетилазы. С помощью таких деацетилаз можно получить растения с целенаправленной способность к разрушению частей растений. Особенный интерес вызывает получение растений с мужской или женской стерильностью. Эта задача решается путем изготовления форм, выполнения, описанных в формуле изобретения.
Данное изобретение относится к молекулам ДНК, которые кодируют деацетилазы или белки с биологической активностью деацетилазы. Ферментные свойства этих белков описаны в примерах. Изобретение относится также к молекулам ДНК, которые кодируют биологически активный частичный фрагмент или производное. Молекулы согласно изобретению охватывают также фрагменты, производные и все аллельные варианты. Под фрагментами понимают части, которые всегда проявляют биологическую активность деацетилазы.
Данное изобретение относится, кроме того, к трансгенным растительным клеткам, которые трансформировались под действием молекул ДНК согласно изобретению. Трансгенные растительные клетки могут быть получены по известным технологиям и регенерированы в целые растения.
Данное изобретение относится, кроме того, к молекулам ДНК, кодирующим белок с биологической активностью N-ацетил-ФФТ-деацетилазы.
Изобретение относится, в частности, к молекулам ДНК, кодирующим белок с биологической активностью N-ацетил-ФФТ-деацетилазы, выбранным из группы, состоящей из
а) молекул ДНК, которые кодируют белок с аминокислотной последовательностью, обозначенной SEQ ID 2, и его фрагменты и/или производные;
б) молекул ДНК, которые кодируют нуклеотидную последовательность, обозначенную SEQ ID 1, или последовательности, которые отклоняются от этой последовательности в рамках дегенерации генетического кода;
в) молекул ДНК, которые кодируют белок с аминокислотной последовательностью, обозначенной SEQ ID 4, или ее фрагментами, и/или производными и
г) молекул ДНК, которые кодируют нуклеотидного последовательность, обозначенную SEQ ID 3, или последовательности, которые отклоняются от этой последовательности в рамках дегенерации генетического кода.
Изобретение относится, кроме того, к идентифицированным и депонированным описанными в данной заявке способами микроорганизмам Stenotrophomonas sp. (DSM 9734) и Comamonas acidovorans (DSM 11070).
Предметом данного изобретения являются, в частности, растительные клетки или растения, которые содержат молекулы ДНК согласно изобретению.
Особенный интерес представляет способ получения растений со способными к целевому разрушению частей путем специфической экспрессии гена деацетилазы, а также способ получения растений с мужской или женской стерильностью путем специфической экспрессии гена деацетилазы.
Данное описание относится также к
(1) целевому концентрированию микроорганизмов с высокой N-ацетил-ФФТ-деацетилазной активностью;
(2) изоляции соответствующих генов деацетилазы;
(3) очистке и характеристике закодированных этими генами белков с высокой N-ацетил-ФФТ-деацетилазной активностью;
(4) экспрессии гена деацетилазы в растения.
Данное описание относится далее к
- молекулам ДНК, которые кодируют ферменты с высокой N-ацетил-ФФТ-деацетилазной активностью;
- белкам, закодированным такими генами;
- экспрессии таких генов деацетилазы в растения.
Из проб почвы в минеральной среде с хитином в качестве единственного С-источника подвергают концентрированию бактерии, которые способны расщеплять N-ацетил-ФФТ с высокой эффективностью. Таким образом могут быть выделены 2 штамма бактерий в виде чистых культур: Stenotrophomonas sp. (DSM-номер депонирования - DSM 9743) и Comamonas acidovorans (DSM-номер депонирования - 11070).
В соответствии с условиями, необходимыми при промышленном получении, может быть, однако, значительно выгоднее использовать очищенные ферменты.
Данная заявка охватывает новые L-N-ацетил-ФФТ-специфические деацетилазы, новый и эффективный способ очистки и характеристики этих ферментов из концентрированной культуры почвенных микроорганизмов, а также применение этих деацетилаз.
Изобретение также относится далее к
1. Деацетилазе с
- молекулярной массой от 20.000 до 100.000 дальтон;
- оптимуму рН - 6,5-10,0;
- субстратной специфичностью по отношению к L-N-ацетил-фосфинотрицину.
2. Способу получения деацетилазы, характеризующемуся тем, что неспорообразующий микроорганизм культивируют в среде, содержащей крабовый хитин, и деацетилазы выделяют из этих микроорганизмов.
3. Применению охарактеризованной в 1. деацетилазы для получения растений с мужской стерильностью, а также для стереоселективного получения L-фосфинотрицина.
Изобретение относится, в частности, к ферменту, который имеет температурный оптимум в пределах между 30oС и 50oС.
Способ получения деацетилаз согласно изобретению проводят предпочтительно с микроорганизмами, выбранными из группы, которая состоит из микроорганизмов, описанных в заявке.
Крабовый хитин может быть получен, как описано Shimahara, Kenzo и Takiguchi, Yasuyuki (Methods in Enzymology, том 161, стр.417-423, 1988) или может быть куплен в фирме Sigma.
Для очистки деацетилазы микроорганизмы культивируют в питательной среде, оптимальной для их роста. Размножение микроорганизмов происходит в аэробных условиях, например, погруженными при встряхивании или перемешивании в качалочных колбах или ферментерах, в случае необходимости при пропускании воздуха или кислорода. Ферментация может осуществляться в области температур от ≈20oC до 40oС, предпочтительно при от ≈25oС до 37oС, особенно при от 30oС до 37oС. Культивирование осуществляют в пределах рН между 5 и 8,5, предпочтительно между 5,5 и 8,0.
В этих условиях микроорганизмы дают обычно через от 1 до 3 дней обозначенное аккумулирование фермента. Синтез деацетилазы начинается с логарифмической фазы, Продуцирование фермента может контролироваться с помощью теста активности путем аналитической высокоэффективной жидкостной хроматографии или фотометрически. Используемая для продуцирования трансаминазы питательная среда содержит от 0,2 до 5%, предпочтительно от 0,5 до 2% крабового хитина, а также неорганические соли.
В качестве неорганической соли питательный раствор может содержать хлориды, карбонаты, сульфаты или фосфаты щелочного или щелочноземельного металла, железа, цинка и марганца, а также соли аммония и нитраты.
Согласно изобретению для дезацетилирования может быть введено активное количество деацетилазы в свободном виде или в иммобилизованной форме, предпочтительно в растения, которые экспрессируют гены деацетилазы.
Для фиксирования используют известные способы, такие как способы, описанные в немецких выложенных заявках 3237341 и 3243591.
Выделение и очистка ферментов может осуществляться согласно классическим способам путем отделения ультразвуком и French-Press (френч-прессованием), путем осаждения сульфатом аммония, путем ионообмена, путем аффинной хроматографии и путем гельпроникающей хроматографии.
Ферментный препарат характеризуется молекулярной массой от 20.000 до 100.000 дальтон, предпочтительно от 30.000 до 80.000, особенно от 40.000 до 70.000 дальтон. Оптимальная величина рН ферментного продукта составляет от 6,0 до 10,0, особенно от 7,0 до 8,0. Оптимальный температурный режим фермента расположен между 30 и 50oС, особенно между 35 и 45oС.
Кодирующие деацетилазу гены были клонированы в E. coli. В случае гена деацетилаза 1 из Stenotrophomonas sp. был проведен скрининг из фагового банка экспрессируемых генов из геномной ДНК в E.coli на N-ацетил-ФФТ-специфической деацетилазную активность. Ген деац.2 из Comamonas acidovorans был клонирован путем комплементации мутанта E. coli-argE с геномным банком.
Аминокислотные последовательности, произведенные из последовательностей ДНК обоих генов, подобны друг другу и, кроме того, гомологичны с гиппурат-гидролазой, как известно из банка данных белков.
Высокое сродство субстрата белка деац.-1 к N-ацетил-L-ФФТ (Кm=670 мкМ) в трансгенных растениях становится заметным благодаря высокой чувствительности тканей по отношению к этому веществу. Таким образом при конструктивной экспрессии деацетил-гена могут быть получены растения, листья которых еще могут чувствительно реагировать на концентрации до 0,4 мг/мл N-ацетил-D,L-ФФТ (= 0,2 мг/мл L-энантиомера). При специфической экспрессии в оболочках достигается индукция цветков с мужской стерильностью путем обработки почек 2 мг/мл N-ацетил-D,L-ФФТ (=1 мг/мл L-энантиомера). Описанные результаты относятся к тепличным растениям. Благодаря более низкой концентрации веществ возможна при необходимости в естественных природных условиях более высокая, 5-10-кратная дозировка.
Приведенные ниже примеры служат для дальнейшего прояснения данного изобретения. Процентные данные, если не оговорено иначе, относятся к весу. Далее данное изобретение определено в формуле изобретения.
Пример 1: Выделение и идентификация почвенных микроорганизмов с N-ацетил-ФФТ-специфической деацетилазной активностью
По 1 г почвы каждая (песчаной глины, дюны Шванхаймера) экстрагировали 10 мМ NaC1, 10 мМ натрийфосфатным буфером, рН 7,0, в течение 1 ч при комнатной температуре. Для селекции различных групп микроорганизмов производили пересев почвенных составов в следующие жидкие Среды:
(1) MSl-среда (для эубактерий): 5 мМ глюкоза; 5 мМ сукцинат; 10 мМ глицерин; 1 г/л NH4Cl; 50 мл/л раствора А; 25 мл/л раствора В; раствор А: 50 г/л К2НРО4; раствор В: 2,5 г/л MgSO4; 0,5 г/л NaCl; 25 мл/л микроэлементов.
(2) Хитиновая среда (для актино- и стрептомицетов, а также для хитиноворных бактерий): 10 г/л крабового хитина; 1 г/л (NH4)2SO4; 0,5 г/л MgSO4; 50 мл/л раствора А; 1 мл/л микроэлементов.
(3) Антибиотическая среда (для высших грибов): 20 г/л солодового экстракта; 10 г/л глюкозы; 2 г/л дрожжевого экстракта; 0,5 г/л (NH4)2SО4; 50 мкг/мл тетрациклина.
Все среды содержали 5 мМ N-ацетил-ФФТ и после пересева были инкубированы в течение 3-5 дней при 28oС.
Обогащенные культуры были дополнительно испытаны на дезацетилирование N-ацетил-ФФТ. Для этого клетки были отцентрифугированы при 10000 об/мин, и надосадочные жидкости были исследованы в аминокислотном анализаторе (Biotronic LC 5001) на образование ФФТ. Только культуры хитиновой среды оказались деацетилазопозитивными. После высева на хитин-агар из этих культур было выделено всего 40 отдельных колоний, рекультивировано в среде хитин-жидкость и снова исследовано на деацетилазную активность. При этом было обнаружено 6 позитивных изоляторов, из которых путем многоразовой смазки на агаровой пластинке и последующего культивирования отдельных колоний могли быть получены активные чистые культуры. Штамм с наивысшей деацетилазной активностью был идентифицирован как Stenotrophomonas sp. (DSM - номер депонирования DSM 9734).
Пример 2: Клонирование и секвенирование гена N-ацетил-ФФТ из Stenotrophomonas sp.
Используемые для работы стандартные методы молекулярной биологии описаны Maniatis и др. 1982, Molecular Cloning: a laboratory manual, Cold Spring Harbor Laboratoru, Cold Spring Harbor, N.Y.
Геномная ДНК из Stenotrophomonas sp. была препарирована по способу Meade и др., 1982, J. Bacteriol. 149:114-122. После парциального ферментирования с Sаu3А были выделены 5-10-т.п.н. большие фракции и лигированы в нарезанных с помощью BamHI ламбда-ZАР-вектора экспрессии Stratagene (стратагена) (Zap Express Vector Kit, каталог 239201, Instruction Manual). С упакованной лигированной смесью был получен первичный банк ламбда-фагов и затем амплифицирован. Из него с помощью pBK-CMV-фагемидной системы Stratagen (стратагена) (каталог 212209, Instruction Manual) был получен фаговый экспрессионный банк в Escherichia coli. Этот генный банк путем скрининга активности с [14С]-N-ацетил-L-ФФТ в качестве субстрата был испытан на наличие гена деацетилазы. Для этой цели 2000 отдельных клонов пересевали на пластинки для микротитрования и после выдержки в течение ночи переносили в LB-среду при 37oС с 0,2 мМ изопропилтиогалактазида в качестве индуктора и 50 мкг/мл канамицина в качестве стойкого маркера. Клетки были отцентрифугированы и инкубированы по 10 мкл 1 мМ [14С]-N-ацетил-L-ФФТ в течение ночи при 28oС. Наконец исходные смеси в восьмом пуле анализировали методами тонкослойной хроматографии и ауторадиографии на превращение N-ацетил-ФФТ в ФФТ (см. патент ЕР 531716, пример 8), и при позитивном результате отдельные клоны были дополнительно протестированы. Этим способом мог быть отделен позитивный клон с 6 т.п.н. включением из 1920 трансформантов. Эти фрагменты ДНК более близко были охарактеризованы ограниченным картированием. Путем субклонирования ограниченных фрагментов вставки в pUC 18/19 и трансформации рекомбинантных плазмид в E. coli с помощью вышеописанных анализов активности могли быть локализованы структурные гены деацетилазы на фрагментах SalI/SmaI длиной на 2,5 т.п.н. (2487 пар оснований) (фиг.1). Активность зависела от ориентации фрагмента относительно lac-промотора вектора.
Аминокислотные последовательности на обеих ветвях фрагмента длиной 2,5 т.п.н. были секвенированы по способу Зангера (Sanger и др. 1977, Proc. Natl. Acad. Sci USA 74: 5463-5468). Полный фрагмент имеет длину 2487 нуклеотидов (смотри SEQ ID 1). Открытые рамки считывания длиной 1494 нуклеотида начинаются с нуклеотида 367 и заканчиваются 1860.
Изучение экспрессии PCR-субфрагментов из этой области в E. coli показали, что активный белок деацетилазы закодирован областью длины 1365 нуклеотидов, начинающейся ATG-инициирующим кодоном в положении 496 и заканчивающейся TGA-терминирующим кодоном в положении 1860. Выведенная из последовательности ДНК аминокислотная последовательность представляет собой полипептид из 454 аминокислот (Seq ID 2) с рассчитанной молекулярной массой 48,1 кД.
Изучение гомологии в банках данных EMBL-, ДНК и белков показало сходство с описанными, впервые, в данной заявке N-ацетил-ФФТ-деацетилазой из Comamonas acidovorana (37,4% идентичных аминокислот), гиппуратгидролазой из Compylobacter jejuni (33,9%) и N-ацил-L-амидогидролазой из Bacillus stearothermophilus (33,7%). Следующий выделенный из Stenotrophomonas ген был обозначен как деац. 1. Соответствующий белок был обозначен как Деац.1. На основании гомологии можно заключить, что названные гиппуратгидролазы и амидогидролазы в сочетании со специфическими для тканей промоторами и последующей обработкой также могут быть с выгодой использованы для получения растений с селективно разрушенными тканями, в частности растений с мужской и/или женской стерильностью.
Пример 3: Характеристика белка Деац.1.
Для сверхэкспрессии и очистки деацетилазы из Stenotrophamonas sp. (деац. 1) была использована система глутатион-S-трансфераза (GST) - ген-вектор слияния из Pharmacia (каталог 27-4581-01, каталог 27-4570-01). Этот способ описан Smith и Johnson, 1988, Gene 67:31. Очистку слитых белков осуществляют путем аффинной хроматографии на глутатион-сефарозе-48.
Функциональный деац. -ген был переклонирован в качестве Bam-HI/SalI-PCR-фрагмента длиной 1,4 т.п.н. в вектор, кодирующий слитый GST-белок при контроле lac-промотором. Экспрессия рекомбинантного слитого белка была индуцирована путем прибавления 0,1 мМ IPTG. Путем SDS/полиакриламидного электрофореза неочищенных экстрактов трансформантов E. coli мог быть обнаружен слитый белок в виде 74-кД-полосы.
Для очистки белка клетки из 2 л культуры индуцированного позитивно экспрессирующего трансформанта E. coii обрабатывали ультразвуком, и затем экстракт солюбилизировали путем прибавления 1% тритона-Х-100. Надосадочную жидкость связывали на глутатион-сефарозе-4В. После многократного промывания ФСБ-буферным раствором (140 мМ NaCl, 3 мМ КСl, 10 мМ Na2HPО4, 2 мМ KH2PО4, pH 7,3) связанный на сефарозной матрице слитый белок расщепляли тромбином. Элюат содержал в виде отдельных белковых полос продукт расщепления 48-кД (после денатурирующего SDS/полиакриламидного электрофореза), который по данным ферментного анализа (смотри ниже) мог быть идентифицирован как N-ацетил-ФФТ-деацетилаза. При помощи описанного способа удается из 2 л культуры бактерий получить 200 мкг очищенного однородного белка деацетилазы.
Активность белка деацетилазы была измерена следующими двумя методами:
(1) Радиоактивный метод: по 2,5 мкг очищенного фермента инкубировали в 10 мкл смеси в ФСБ-буферном растворе с 0,1 Мм [14С] -N-ацетил-L-ФФТ в течение 15 мин при 37oС. После этого пробы разбавляли 1:6 5 мМ KH2PO4 в 10%-ном метаноле, рН 1,92, и анализировали методом высокоэффективной жидкостной хроматографии с детектором радиоактивности (разделительная колонка: сферисорб SAX, элюент: 5 мМ KH2PO4 в 10%-ном метаноле, рН 1,92, скорость потока: 0,5 мл/мин). В этих условиях элюируют [14С]-L-ФФТ на 4,5 мин и [14С] -N-ацетил-L-ФФТ при 6,5 мин. Специфическую деацетилазную активность обнаруживали в [нмоли [14С] -L-ФФТ/мин/мг белка]. Для определения оптимальной величины рН смеси инкубировали в буферной системе из 40 мМ Bis-Tris, Tns и Caps между рН 6 и 9. Для измерения значения Кm проводились 3-кратные определения концентраций [14С]-N-ацетил-L-ФФТ между 0,01 мМ и 1 мМ при рН 8,0 в присутствии 1 мМ CoCl2.
(2) Нерадиоактивный метод: Для исследования субстратной специфичности по 5 мкг каждого очищенного фермента инкубировали в 20 мкл надосадочной жидкости в ФСБ-буферном растворе каждая с по 25 мМ определенной N-ацетил- или N-ациламинокислоты в течение 60 мин при 28oС. Затем пробы измеряли на образование свободных аминокислот в аминокислотном анализаторе (Biotronic LC 5001). Специфическую активность обнаруживали в [нмоли аминокислоты /мин/мг белка]. Для N-ацетил-ФФТ-деацетилазы было определено оптимальное значение рН 8 (смотри таблицу 1) и температурный оптимальный режим 37oС (смотри таблицу 2). Кинетические измерения дали значение Кm 670 мкМ. Путем прибавления 1 мМ CoCl2 удавалось поднять активность фермента примерно на 20%.
Результаты измерений субстратной специфичности представлены в таблице 3.
Фермент обладает относительно широким спектром субстратов. Наиболее высокие взаимодействия были достигнуты с гиппуровой кислотой (N-бензоилглицином) и N-ацетил-L-глутаматом. Чувствительность N-ацетил-L-ФФТ примерно на 50% ниже, чем у обоих названных выше субстратов. Деацетилаза обладает исключительной специфичностью к N-ацетил-L-аминокислотам. С соответствующими D-энантиомерами никаких реакций не наблюдалось.
Пример 4: Конститутивная экспрессия деац.1-гена в табаке
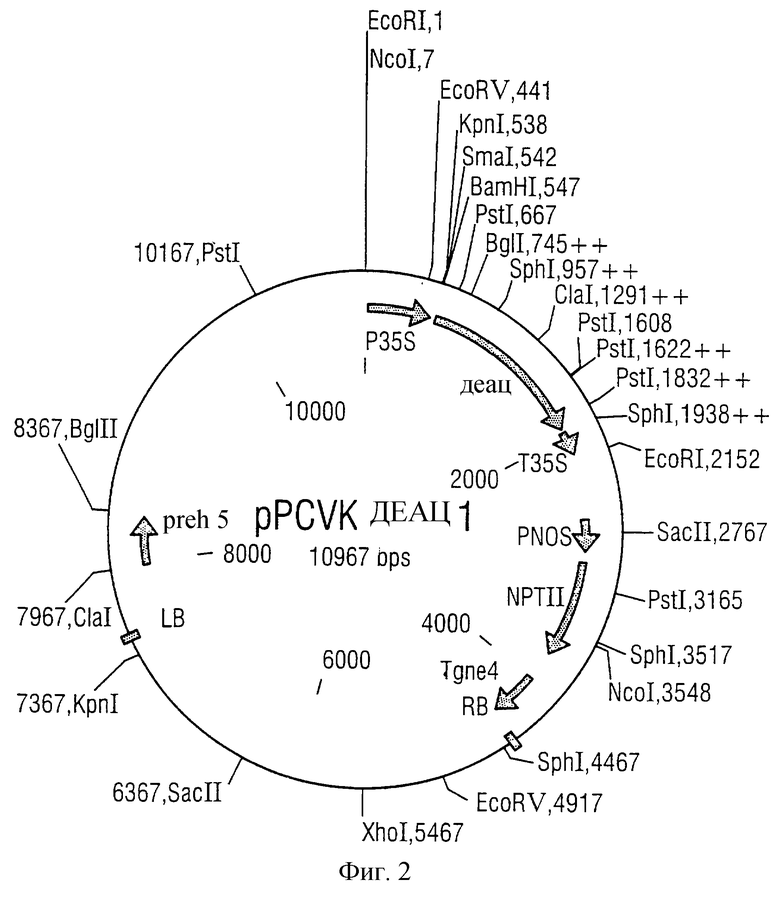
Структурный деац.1-ген был как фрагмент BamHI/SaLi-PCT длиной 1,4 т.п.н. переклонирован в бинарный вектор pPcv80l (Koncz и Schell, 1986, Mol. Gen. Genet. 204: 383-396) под контролем 35S-промоторов. Образующаяся плазмида pPCVKDEAC1 (фиг.2) с вектором экспрессии 35S-промотор-структурный деац.1-ген 35S-терминатор был с помощью стандартных способов трансформирован в Agrobacterium tumefaciens (штамм ATHV). Кусочки листьев табака (Nicotiana tabacum) были трансформированы рекомбинантными агробактериями по методу Horsch и др., 1985, Science 227% 1229-1231, и отобраны в среду с канамицином, 18 независимых трансформантов табака были регенерированы и испытаны на экспрессию деацетилазы в листьях. В этом случае активность белков в трансгенных растениях была рассчитана по чувствительности листьев к N-ацетил-ФФТ, тогда как это вещество в растении благодаря ферментативной активности деацетилазы далее превращалось в гербицидно активный фосфинотрицин.
В капельной пробе листья трансгенного растения, а также нескольких нетрансгенных контрольных растений обрабатывали по 5 мкл следующих концентраций N-ацетил-D, L-ФФТ: 4 мг/л (=15 мМ), 1 мг/л (=3,75 мМ), 0,4 мг/л (=1,5 мМ), 0,1 мг/л (-0,38 мМ). Места обработки через 1-2 недели исследовали на осветление или образование некрозов. Одновременно измеряли N-ацетил-ФФТ-специфическую деацетилазную активность трансформантов, а также контрольных растений в сырых экстрактах. Для этого по 100 мг листового материала гомогенизировали в 200 мкл ФСБ-буферного раствора, обломки клеток отцентрифугировали, и остаток подвергали диализу в течение ночи при 4oС в таком же буферном растворе. По 10 мкл этих проб каждая инкубировали с 0,1 мМ [14С]-]N-ацетил-L-ФФТ в течение ночи при 37oС. Надосадочную жидкость затем анализировали методом высокоэффективной жидкостной хроматографии, как описано выше, на образование [14С]-L-ФФТ.
Результаты капельных проб и проб активности для выбранных растений представлены в таблице 4. Показано, что 60% трансформантов экспрессируют функциональный белок деацетилазы и отображают соответствующий фенотип.
Пример 5: Тапетум-специфическая экспрессия деац.1-гена в табаке
С применением стандартных способов были слиты тапетум-специфический промотор tap-1-гена из львиного зева (Antirrhinum majus) в форме фрагмента EcoRi/BamHI длиной 2,2 т. п.н. со структурным геном деац.1 (фрагмент BamHI/SalI-PCR длиной 1,4 т.п.н.) и 353-терминатор в вектор pUC 18. Полученная таким образом экспрессионная кассета tap-1-промотор-структурный ген деац. -35S-терминатор была клонирована как фрагмент EcoRI длиной 3,8 т.п.н. на место области 35S-промотора/терминатора в бинарный вектор pPCV801 (плазмида pPCVTDEACI, фиг.3). Трансформация табака была проведена, как описано в примере 4.
В случае тапетум-специфической экспрессии деацетилазы должны были быть индуцированы путем обработки цветочных почек N-ацетил-ФФТ цветы с мужской стерильностью. Превращение ФФТ-производных в гербицидно активное вещество фосфинотрицин ведет к селективному повреждению тканей тапетума, благодаря чему затрудняется развитие функциональной пыльцы.
Всякий раз, когда была обработана только одна сторона Iyfloreszenzen (инфлоресценции) (вся область развивающихся цветочных почек) с помощью N-ацетил-ФФТ, другая сторона инфлоресценции оставалась необработанной для того, чтобы обеспечить, чтобы наблюдаемое явление не приводило к уродствам соответствующего растения. Обработку проводили к моменту, когда отдельные почки были не более 5 мм (активная фаза для тапетум-промотора). Трансформанты табака, так же как и несколько NT Sam NN-контрольных растений, были обработаны в течение недели трижды 0,2% N-ацетил-D,L-ФФТ (=7,5 мМ)/0,1% генаполем (смачивающий агент). После распускания почек (примерно 9-11 дней после окончания обработки) растения были исследованы на наличие мужской стерильности цветков.
Одновременно была измерена N-ацетил-ФФТ-специфичная деацетилазная активность незрелой пыльцы трансформантов, а также контрольных растений. Для этого пыльцу из цветочных почек величиной примерно 5 мм препарировали и инкубировали в течение ночи при комнатной температуре в растворе 50 мкМ [14С]-N-ацетил-L-ФФТ. Затем пыльцу промывали один раз в 500 мкл ФСБ-буферного раствора и гомогенизировали в 50 мкл ФСБ-буферного раствора. После отделения путем центрифугирования обломков клеток надосадочную жидкость концентрировали в Speed-Vac (быстром вакууме), и гранулы извлекали в 30 мкл КФЖ(НРLС)-буферного раствора (5 мМ KH2P04, 10% метанол, рН 1,92). Надосадочную жидкость затем анализировали в КФЖ-буферном растворе, как описано выше для образования [14C]-L-ФФТ.
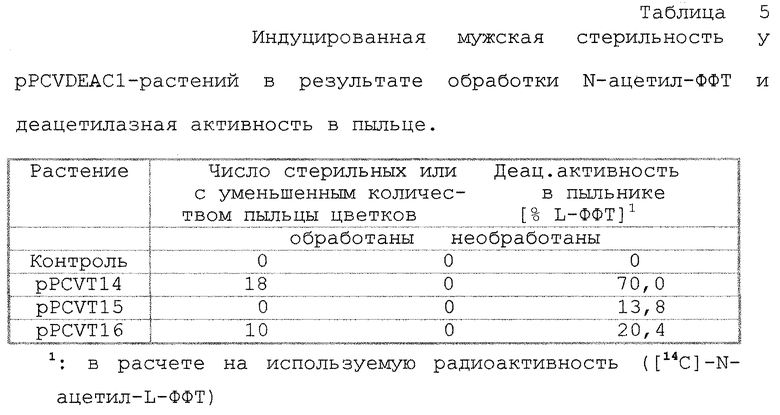
Результаты обработки цветков и пробы активности для выбранных растений представлены в таблице 5. Почти во всех трансформантах смогла быть установлена специфичная деацетилазная активность в пыльце. В 3 трансформантах на обработанной N-ацетил-ФФТ стороне цветочные грозди обладали мужской стерильностью, то есть пыльца не образовалась или наблюдались цветки с сильно уменьшенным количеством пыльцы. Действие на новые, зрелые почки останавливается примерно через 3 недели. Необработанные цветки трансформантов, а также обработанные цветки контрольных растений во всех случаях были фертильными. У цветков с мужской стерильностью невозможно образование семян. При целевом перекрестном опылении цветков с мужской стерильностью, однако, возможно, как было показано, сохранение полной функциональной способности женской части цветков (Nacken и др., 1991, Mol. Gen. Genet. 229: 129-136).
Пример 6: Выделение и идентификация деацетилазы со специфичностью к N-ацетилфосфинотрицину из Comamonas acidovorans
Почвенную пробу из Бангкока суспендировали в среде минеральных солей (0,5 г К2НРО4, 0,2 г МgSО4, 2 г (NH4)2SО4, 0,01 г FeSО4 в 980 мл Н2О), содержащей в качестве единственного источника углерода хитин (2 г/л), и затем инкубировали 48 часов при 30oС. Затем производили пересев в свежую среду минеральных солей и после дальнейшего инкубирования в течение 48 часов производили ряд разбавлении в LB-среде (Miller, Experiments in molecular genetics, Cold Spring Harbor Laboratory Press).
Среди выросших колоний находился также такой штамм бактерий, который в виде чистой культуры, путем очень хорошего использования N-ацетилглутамата характеризовался как единственный источник углерода (смазывание на минеральносолевой среде N-ацетилглутаматом (2 г/л; добавление в качестве стерильно-фильтрующего раствора к автоклавированной минерально-солевой среде 14 г/л агара), ведет в течение 12 часов инкубирования при 30oС к образованию отчетливо видимой колонии). Дезацетилирование N-ацетил-ФФТ было обнаружено, как описано выше. Штамм под лабораторным обозначением В6 был идентифицирован по DSM как Comamonas acidovorans (DSM 11070).
Пример 7: Клонирование гена деацетилазы из Comamonas acidovorans
Целая ДНК была выделена из Comamonas acidovorans, обработана EcoRI и лигирована с также обработанной EcoRI ДНК вектора pACYC184 (Cang и Cohen, 1978, J. Bacteriol. 134, 1141-1156). Лигированная смесь была применена для электропорации argE-мутанта E. coii XSID2 (Mountain и др., 1984, Mol. Gen. Genet. 197, 82-89). Путем селекции на комплементацию аргинин-ауксотрофности удается выделить фрагмент EcoRI длиной 8,9 т.п.н. из генома С. acidovorans, обогащенного для комплементации. Путем субклонирования удается ограничить комплементарную область до фрагмента величиной 1,4 т.п.н. Последний представляет собой обозначенное pGK83 производное вектора последовательности pSVB30 (Arnold и Punier, 1988, Gene 70, 172-178).
Пример 8: Секвенирование гена деацетилазы из Comamonas acidovorans
Комплементарный фрагмент величиной 1,4 т.п.н. (1387 пар оснований) был полностью секвенирован двойными полосами известными способами.
Пример 9: Анализ области кодирования и сравнение гомологии секвенированных областей
Анализ области кодирования дал открытую область считывания с положения 1 до 1206 (SEQ ID 3), которые кодируют белок величиной в 402 аминокислоты (SEQ ID 4).
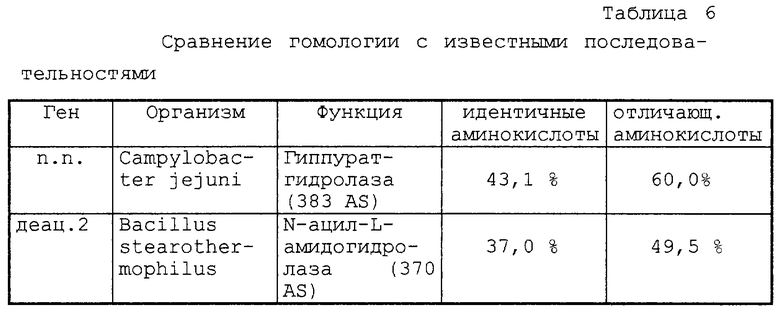
Сравнение гомологии с известными генами из банка данных показывает четкую гомологичность с N-ацил-L-амидогидролазной из Bacillus atearothermophilus (ama, Sakanyan и др., 1993, Appl. Environ. Microbiol. 59, 3878-3888) и гиппуратгидролазой из Compylobacter jejuni (до сих пор нет публикации). При сравнении белков гиппуратгидролаза обнаруживает 43%. идентичных аминокислот (таблица 6). Кроме того, ген на плоскости ДНК и белка проявляет поразительную гомологичность с геном деацетилазы, выделенным из Stenotrophomonas spec. В дополнение к обозначению гена из Stenotrophomonas sp. идентифицированный из С. acidovorans ген был обозначен деац.2.
Пример 10: Сверхэкспрессирование деац.2-гена из Comamonas acidovorans - растительные конструкции
Для анализа субстратной специфичности деац.2-генного продукта из Comamonas acidovorans, он был сверхэкспрессирован. Для этого ген был клонирован в вектор с высоким числом копий под контролем lacZ-промотора. Эффективность экспрессии была ограничена, однако, одновременно происходящей в другой рамке считывания трансляцией lacZ-альфа. Поэтому этот процесс прерывался введением стоп-кодона, так что вектор pGK81 делал возможным независимую от lac-Z-гена сверхэкспрессию дац.2-гена. Это смогло также быть фенотипически обнаружено, так как эта конструкция проявляет четкую комплементарность аrgE-мутанта Е. coil.
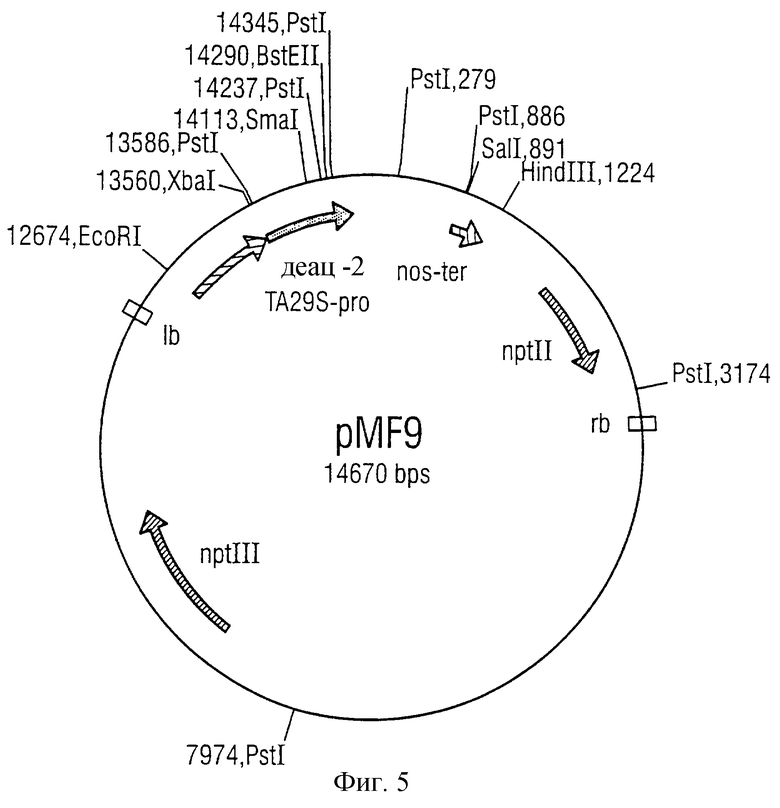
Для трансформации растений структурный деац.2-ген с применением бинарного вектора pROKl (Baulcombe и др., 1986, Nature, 321: 446-449) был переклонирован вслед за конструктивным 35S-промотором или специфическим промотором в оболочках ТА-29. Полученные экспрессионные плазмиды pGK83 и pMF9 представлены на чертежах.
Пример 11: Изучение субстратной специфичности деац.2-генных продуктов из Comamonas acidovorans.
Для изучения субстратной специфичности деац.2-генных продуктов из Comamonas acidovorans была использована обработка толуолом/этанолом проницаемых клеток Е. coli, штамма XLI-синего, в присутствии или в отсутствие вектора pGK81. Индукции гена деац.2, репримированного находящимся в этом штамме Lас1-репрессором, удается достигнуть путем обработки IPTG. Проницаемые клетки были инкубированы с различными N-ацилироваными аминокислотами (конечная концентрация 25 мМ) 3 часа при 30oС, и смесь была исследована с помощью аминокислотного анализатора. При этом оказалось, что более 20% представленных в распоряжение N-ацетил-орнитинов подверглись превращению. Для N-ацетил-фосфинотрицина, также аналогично используемым концентрациям N-ацетил-фосфинотрицина, удалось установить возрастающее дезацетилирование до фосфинотрицина (таблица 7).
Даны концентрации взятых N-ацетилированных аминокислот и полученных в результате дезацетилирования аминокислот.
Пример 12: Способ получения женских стерильных сельскохозяйственных растений с использованием гена деацетилазы Stenotrophomanas под контролем промотора, регулирующего экспрессию в женском репродуктивном органе растения.
Промоторы, регулирующие экспрессию в женском репродуктивном органе растения, описаны в предшествующем уровне техники, например, специфические промоторы рыльца (Robert et al., 1994, Plant Molecular Biology 26:1217-1222) или специфические промоторы пестика (Sato et al., 1991, The Plant Cell 3: 867-876; Dzelkalns et al., 1993, The Plant Cell 5:855-863, WO 94/25613).
Ген деацетилазы вида Stenotrophomanas гибридизуют со специфическим промотором пестика и вносят в клетки табака путем опосредованной Agrobacterium трансформации диска листа. Перед цветением растения, которые были регенерированы из этих клеток, обрабатывали N-ацетил-ФФТ. Было показано, что N-ацетил-ФФТ стабилен в растительной клетке, и он доставляется во все клетки. Этот субстрат не имеет существенных отрицательных характеристик, присущих растению дикого типа. Как только образуются первые клетки пестика, они начинают экспрессировать ген деацетилазы. N-ацетил-ФФТ, нанесенный на растение, деацетилируется под действием фермента и превращается в ФФТ-активную форму. Он подавляет глутаминсинтазу клеток пестика, обуславливая тем, самым гибель клеток. Женский гаметофит не может развиваться, следовательно оплодотворение не может иметь место. Растения становятся стерильными по женскому типу, при этом окружающие ткани не повреждаются.
Фиг.1 Рестрикционная карта 2,5- kb SalI/BamHI-фрагмента, который способствует N-ацетил-ФФТ-специфичной деацетилазной активности. Положения и ориентация структурного гена деац.1 обозначены стрелками (ВР-пара оснований).
Фиг. 2 Карта плазмиды pPVCKDEAC1 для конститутивной экспрессии гена деацетилазы в растениях.
Фиг.3 Карта плазмиды pPCVTDEAC1 для тапетум-специфической экспрессии гена деацетилазы в растениях.
фиг.4 Карта плазмиды pGK83.
Фиг.5 Карта плазмиды pPMF9.














Изобретение относится к генетической инженерии и может быть использовано в селекции растений. Введение в геном растения молекулы ДНК, кодирующей белок, обладающий активностью N-ацетил-фосфинотрицин-деацетилазы, вызывает нарушение метаболизма в отдельных частях растений. Например, могут быть получены растения с мужской или женской стерильность. 2 с. и 7 з.п. ф-лы, 5 ил., 7 табл.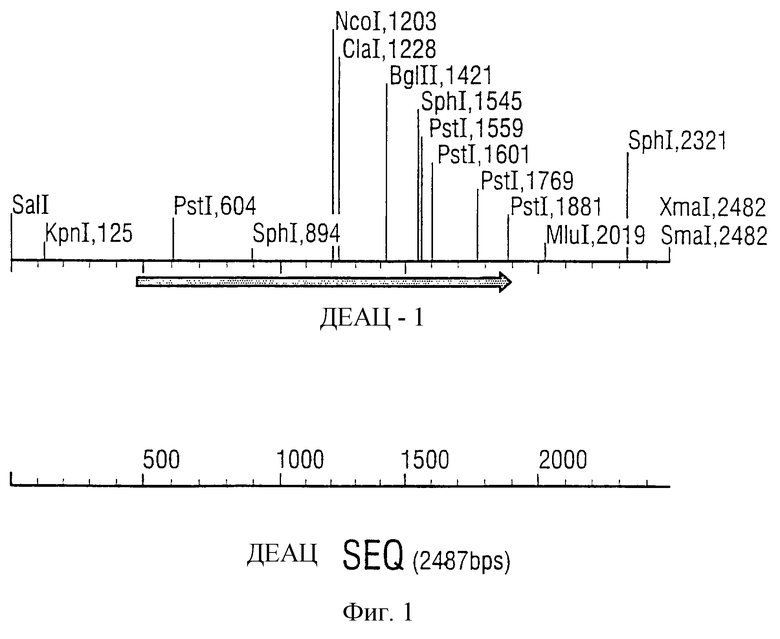
| RU 940333345 A, 10.05.1996 | |||
| RU 94023241 A,10.09.1996 | |||
| Устройство для полирования изделий | 1974 |
|
SU531716A1 |
| DE 4308061 A, 15.09.1994. | |||
Авторы
Даты
2003-05-27—Публикация
1997-12-03—Подача