Изобретение относится к способу получения доксорубицина из даунорубицина с использованием фермента, полученного из трансформированных рекомбинантной ДНК клеток.
Антрациклины группы даунорубицина, такие как доксорубицин, карминомиин и аклациномицин, относятся к наиболее часто используемым в противоопухолевой терапии средствам [F. Arcamone, Doxorubicin, Academic Press, New York, 1981, pp. 12-25; A. Grein. Process Biochem., 16, 34, 1981; T. Kaneko, Chimicaoggi May, 11, 1988; C. E. Myers et al., "Biochemical mechanisms of tumor cell kill". In: Antracycline and Antracenedione - Based Anti-Cancer Agents (Lown J.W., ed.), Elsevier, Amsterdam, pp.527-569, 1988; J.W.Lown, Pharmac. Ther., 60, 185-214, 1993].
С помощью химического синтеза были получены усовершенствованные с точки зрения усиления противоопухолевой активности производные доксорубицина, в частности, в случае их перорального введения, а также в плане снижения острой токсичности и хронической кардиотоксичности, возникающих при использовании таких препаратов для лечения рака [Penco, Process Biochem., 15, 12, 1980; T.Kaneko, Chimicaoggi May, 11, 1988]. 4'-эпидоксорубицин (эпирубицин), 4-деметоксидаунорубицин (идарубицин) и метоксиморфолинодоксорубицин представляет собой примеры таких аналогов.
Антрациклины относятся к натуральным соединениям, продуцируемым различными штаммами Streptomyces (S. peucetius, S. coeruleorubidus, S. galilaeus, S. griseus, S. griseoruber, S. insignis, S. viridochromogenes, S. bifurcus и Streptomyces sp., штамм С5) и Actinomyuces carminata.
Доксорубицин продуцируется большей частью S. peucetius, тогда как даунорубицин продуцируется S. peucetius и представителями Streptomyces, приведенными выше. Штаммы S. peucetius subsp. caesius IMRU 3920 (который идентичен АТСС 27952 и будет впоследствии обозначаться как "S. peucetius 3920"), S. peucetius АТСС 29050 ("S. peucetius 29050"), S. peucetius substr. caesius АТСС 27952 ("S. peucetius 27952"), а также не продуцирующий даунорубицин мутант S. peucetius dnrN: aphiI ("S. peucetius dnrN"; S.L. Otten, J. Ferguson and C.R. Hutchinson, J. Bacteriol., 177, 1216-1224, 1995] описаны в литературе. В частности, штамм S. peucetius АТСС 27952 описан в патенте США US -А-3 590 028, S. peucetius 29050 описан в US - A - 4 012 284, S. peucetius dnrN депонирован в Американской Коллекции культур, в Роквилле, США (American Type Culture Collection, Rockville, MD USA) под индексным номером АТСС 55607. S. peucetius АТСС 55607 получен из штамма S. peucetius АТСС 29050 замещением гена dnrN мутантным геном dnrN, в котором в сайт SalI для нарушения функции dnrN введен ген aphil из Тn 5 (J.M. Ward et al., Mol. Gen. Genet. , 203, 468-475, 1986). По результатам исследования роста штамма S. peucetius АТСС 55607 на среде ISP 4 (Difco Laboratories Detroit, MI), содержащей 50 мкг/мл канамицина, был сделан вывод об устойчивости этого штамма к неомицину или канамицину, а также о том, что он не продуцирует доксорубицин, даунорубицин или какие-либо другие интермедиаты на пути их биосинтеза (S.L. Otten et al., работа подписана к публикации). Антрациклиновый доксорубицин синтезируется в S. peucetius 27952 из малоновой кислоты, пропионовой кислоты и глюкозы по пути, описанному в наиболее полном виде в работах Грейна и Эккардта и Вагнера (Grein, Advan. Appl. Microbiol., 32, 203, 1987; Eckardt and Wagner, J. Basic Microbiol., 28, 137, 1988). Установлено, что в упомянутом пути интермедиатами являются ∈-родомицинон, карминомицин и даунорубицин. Последняя стадия в этом пути включает гидроксилирование даунорубицина до доксорубицина, который, как было показано, имеется только в S. peucetius 27952 (F. Arcamone et al., Biotechnol. Bioeng., 11, 1101, 1969). В патенте ЕР - А - 61737 описан способ биоконверсии даунорубицина в доксорубицин примерно на 30% с использованием не продуцирующего даунорубицин мутанта S. peucetius АТСС 31847, полученного в результате обработки штамма АТСС 27952 N-метил-N'-нитро-N-нитрозогуанидином. При этом указанная конверсия осуществляется обычно в промышленном масштабе в соответствии со способом, описанным в US - A - 3 803 124.
Гены биосинтеза даунорубицина и устойчивости к даунорубицину были получены из S. peucetius 29050 и S. peucetius 27952 в экспериментах по клонированию (Stutzman - Ergwall and Hutchinson, Proc. Natl. Acad. Sci. USA, 86, 3135, 1988; Otten et al., J. Bacteriol., 172, 3427, 1990). Эти исследования показали, что клонированные гены при введении в Streptomyces lividans 1326 придают им способность продуцировать ∈-родомицинон и делают их устойчивыми к даунорубицину и доксорубицину.
Настоящее изобретение относится к выделению молекулы ДНК, кодирующей даунорубицин-14-гидроксилазу. Даунорубицин-14-гидроксилаза превращает даунорубицин в доксорубицин. В типичном случае молекула ДНК состоит по существу из последовательности SEQ ID 1, которая будет далее называться как "dxrA" последовательность. В виде последовательности SEQ ID 2. представлена укороченная аминокислотная последовательность даунорубицин-14-гидроксилазы, кодируемая последовательностью SEQ ID 1.
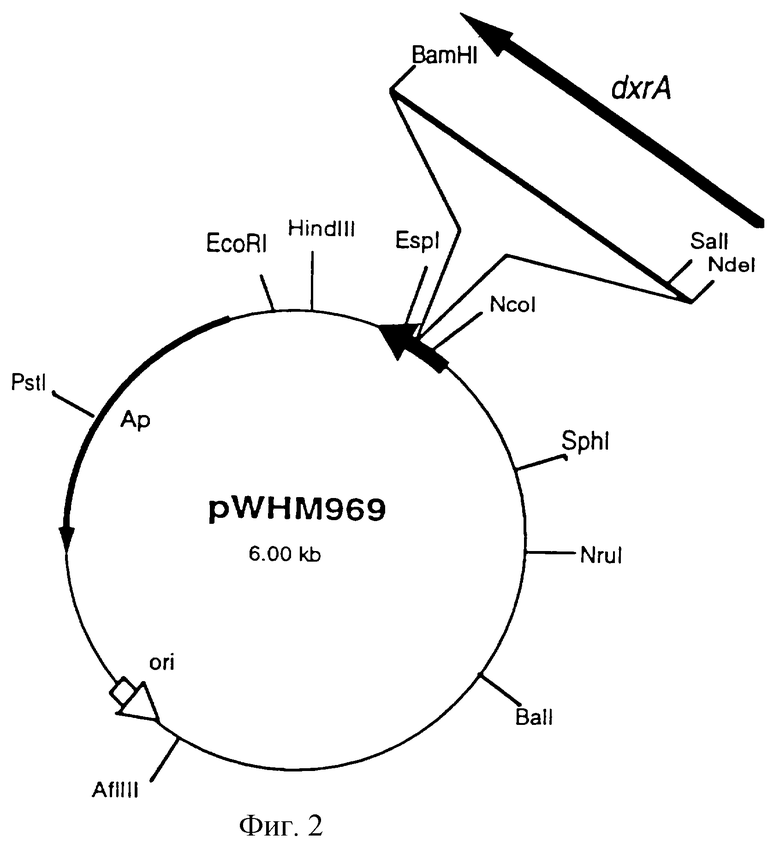
Молекула ДНК настоящего изобретения может включать либо полностью, либо только часть SрnI фрагмента размером 3,4 Kb, приведенного на фиг.1. Последовательность, кодирующая даунорубицин-14-гидроксилазу, находится между KpnI и BamHI сайтами XphI фрагмента. Молекула ДНК настоящего изобретения может также включать полностью или только Nde - BamHI фрагмента, приведенного на фиг.2, который был получен из несколько большего по размеру фрагмента KpnI - BamHI, приведенного на фиг.1.
В том случае, когда молекула ДНК настоящего изобретения включает только часть SpHI фрагмента размером 3,4 Kb или Nde - BamHI фрагмент эта часть должна функционировать как даунорубицин-14-гидроксилаза (т.е. должна превращать даунорубицин в доксорубицин). В типичном случае длина этой части составляет по крайней мере 1,2 Kb, предпочтительно от 1,2 до 3,4 Kb, более предпочтительно от 1,2 до 1,4 Kb. Часть может представлять собой фрагмент, полученный при расщеплении рестрикционным ферментом, в частности Nde - BamHI фрагмент, показанный на фиг.1.
Изобретение включает в свои рамки молекулу ДНК, кодирующую даунорубицин-14-гидроксилазу, которая имеет последовательность, идентичную, по крайней мере, на 60% последовательности SEQ ID 2. Изобретение включает также даунорубицин-14-гидроксилазу, аминокислотная последовательность которой, по крайней мере, на 60% идентична последовательности SEQ ID 2.
Последовательность может быть не менее чем на 80%, не менее чем на 90%, не менее чем на 95%, не менее чем на 98% или не менее чем на 99% идентична последовательности SEQ ID 2.
Последовательность SEQ ID 2 может быть модифицирована с помощью замещения, делеции, вставки, расширения, функционализации или посредством химической модификации. Замещение, делеция, вставка или расширение могут вовлекать одну или более аминокислот, например одну, две, три, четыре, пять, восемь, пятнадцать или двадцать аминокислот. В общем случае, модифицированная последовательность должна сохранять физико-химическую природу SEQ ID 2. Модифицированная последовательность должна быть при этом близкой к исходной по заряду, характеристикам гидрофобности/гидрофильности и по размеру. Приемлемыми видами замещения являются такие, которые приводят к замещению аминокислоты из одной из приведенных ниже групп другой аминокислотой из той же группы:
Н, R и К
I, L, V и M
А, G, S и Т
D, E, P и N.
Молекулы ДНК, кодирующие модифицированные последовательности, могут быть получены с помощью традиционной техники. Так, например, они могут быть получены с помощью обычного синтеза ДНК, сайт-направленного мутагенеза и с применением техники рекомбинантной ДНК. Подходящие для этого методы описаны в книге Самбрука с соавт. Sambrook et al., 1989, Molecular Cloning: A Laboratory Manual, 2nd Ed. , Cold Spring Harbor Laboratory, Cold Spring Harbor, NY). Белки, несущие такие производные последовательности, могут быть легко проверены на наличие активности даунорубицин-14-гидроксилазы, с использованием, например, метода, приведенного ниже в разделе Примеров.
Для синтеза даунорубицин-14-гидроксилазы, которую кодируют экспрессируемые молекулы ДНК настоящего изобретения, упомянутая ДНК может нести свою собственную последовательность, регулирующую транскрипцию, и, в частности, свой собственный промотор, который оперативно связан с кодирующей последовательностью и распознается РНК-полимеразой хозяйской клетки. Альтернативно, ДНК может быть лигирована с гетерологичной последовательностью регуляции транскрипции в правильном направлении или клонирована в векторе в сайте рестрикции, расположенном соответствующим образом, вблизи последовательности регуляции транскрипции вектора.
Молекула ДНК, кодирующая даунорубицин-14-гидроксилазу, может представлять собой рекомбинантную клонируемую ДНК или вектор экспрессии. Это может быть любой автономно реплицирующийся и/или интегрируемый агент, включающий молекулу ДНК, к которой могут быть добавлены один или более сегментов. Однако в типичном случае вектор является плазмидой. Предпочтительной плазмидой является мультикопийная плазмида pWHM3 или pIJ 702 Kаtz et al., J. Gen. Microbiol. , 129, 2703, 1983). К числу других предпочтительных плазмид относятся pIJ 385 (Mayeri et al. , J, Bacteriol., 172, 6061, 1990), pIJ 680 (Hopwood et al., Genetic Manipulation of Streptomyces. A Laboratory Manual, John Innes Foundation, Norwich, UК, 1985), pWHM 601 (Guilfoile and Hutchinson, Proc. Natl. Acad. Sci. USA, 88, 8553, 1991) или pSET 152 (Bierman et al. , Gene, 116, 43-49, 1992). Для введения ДНК в вектор может быть использована любая подходящая техника. Вставка может быть осуществлена при лигировании ДНК в соответствующем сайте рестрикции в линеаризованном векторе. Для этой цели применяют метод непосредственного соединения тупых и липких концов, гомополимерного наращивания или используют молекулу адаптера или линкера.
Рекомбинантный вектор может использоваться для трансформации или трансфекции подходящей хозяйской клетки. Хозяйские клетки могут быть как даунорубицин- и доксорубицин-чувствительные, т.е. не способные расти в присутствии определенного количества даунорубицина или доксорубицина, так и даунорубицин- или доксорубицин-устойчивыми. Организм хозяина может быть представлен микроорганизмом, таким как бактерия. При этом не продуцирующие антрациклины штаммы S. peucetius, в частности S. peucetius dnrN, и другие штаммы вида Streptomyces, могут быть трансформированы. Трансформанты Streptomyces получают при проведении трансформации протопластов. Векторы могут экспрессироваться в клетках, отличных от Streptomyces, например в E.coli.
Белок даунорубицин-14-гидроксилаза, полученный с помощью трансформированной хозяйской клетки, может быть применен далее для проведения биоконверсии даунорубицина в доксорубицин. Этот метод позволяет получать высокоочищенный доксорубицин из клеточного экстракта, продуцируемого в процессе ферментации и содержащего даунорубицин.
Процесс биоконверсии может быть осуществлен либо с использованием непосредственно свободных или иммобилизованных трансформированных клеток или посредством выделения белка даунорубицин-14-гидроксилазы, который может использоваться либо в свободном виде, либо при иммобилизации по известным методикам на смолах, стекле, целлюлозе или аналогичных веществах с помощью ионных или ковалентных связей или при перенесении на волокна, проницаемые для субстрата или же при придании свойств нерастворимости за счет образования поперечной сшивки. Белок даунорубицин-14-гидроксилаза может также использоваться в виде грубого клеточного экстракта. Рекомбинантный вектор настоящего изобретения может также использоваться для трансформации подходящей хозяйской клетки, которая продуцирует даунорубицин, с целью повышения биоконверсии даунорубицина в доксорубицин. Хозяйские клетки могут быть даунорубицин- или доксорубицин-устойчивыми, т.е. могут расти в присутствии любого количества даунорубицина или доксорубицина. Штаммы S. peucetius, в частности S. peucetius 29050 и другие штаммы видов Streptomyces, продуцирующие антрациклины, могут быть трансформированы. Трансформанты штаммов Streptomyces получают в типичном случае при трансформации протопластов.
Изобретение относится к способу получения доксорубицина, который включает:
(i) культивирование хозяйской клетки, трансформированной или подвергшейся трансфекции вектором настоящего изобретения в присутствии даунорубицина в условиях, при которых даунорубицин превращается в доксорубицин, и
(ii) выделение доксорубицина из культуры.
В соответствии с настоящим способом, хозяйская клетка может культивироваться при температуре от 20 до 40oС, например при температуре от 30 до 37oС. Длительность выдерживания культуры в присутствии даунорубицина может варьировать от 6 до 96 часов, например от 12 до 72 часов. Культура выращивается предпочтительно при перемешивании. Концентрация даунорубицина в культуре может составлять от 2 до 200 мкг/мл, например от 10 до 100 мкг/мл. Даунорубицин может добавляться к культуральной среде в начале культивирования или же он может продуцироваться хозяйскими клетками в ходе культивирования.
Молекулы ДНК настоящего изобретения могут быть получены из геномной ДНК S. peucetius 29050. Указанный штамм был депонирован в Американской Коллекции культур, в Роквилле, США (American Type Culture Collection, Rockville, MD, USA) под номером АТСС 29050. Штамм, полученный из S. peucetius 29050, такой как S. peucetius 27952, который в типичном случае тоже обладает способностью превращать даунорубицин в доксорубицин, также может использоваться. Молекулы ДНК могут быть получены с помощью:
(а) создания библиотеки геномной ДНК из S. peucetius 29050 или полученного из него штамма;
(б) отбора из библиотеки клона, обладающего способностью превращать даунорубицин в доксорубицин, и
(в) выделения из отобранного клона молекулы ДНК настоящего изобретения.
Библиотека может быть получена на стадии (а) с помощью частичного расщепления геномной ДНК из S. peucetius 29050 или полученного из него штамма; или при скрининге библиотеки из геномной ДНК S. peucetius, которая обогащена или имеет характерное для нее содержание кластера генов биосинтеза даунорубицина. В случае геномной ДНК используется предпочтительно рестрикционный фермент MboI, однако в случае библиотеки, содержащей кластер генов биосинтеза даунорубицина, предпочтительны рестрикционные ферменты BamHI или SpHI. Полученные таким образом фрагменты ДНК могут быть фракционированы по размеру; при этом фрагменты размером от 3 до 5 Kb предпочтительны для случая геномной ДНК, а для фрагментов ДНК из библиотеки, содержащей кластер генов биосинтеза даунорубицина, предпочтительны BаmHI фрагменты размером 13,5 Kb или SphI фрагменты размером от 3,4 до 4,9 Kb. Эти фрагменты лигируют в линеаризованном векторе, таком как pWHM3, pIJ 702 или рKC 505 (M. A. Richardson et al., Gene, 61, 231, 1987). Хозяйские клетки трансформируют смесью для лигирования. В типичном случае, хозяйские клетки не способны продуцировать даунорубицин и могут быть даунорубицин- и доксорубицин-чувствительными; например, чувствительными к присутствию даунорубицина или доксорубицина в количестве 10 микрограмм или меньше на мл. Так, например, могут быть трансформированы протопласты S. Lividans JI 1326 (Hopwood et al., Genetic Manipulation of Streptomyces. A Laboratory Manual., John Innes Foundation, Norwich, UК, 1985).
На стадии (б) проводят скрининг полученных трансформантов на их способность поглощать даунорубицин, превращать его в доксорубицин и далее выделять доксорубицин. Клоны, способные превращать даунорубицин в доксорубицин, идентифицируют хроматографией экстрактов культуральной среды, содержащей даунорубицин, в присутствии доксорубицина. Такие клоны выделяют и проводят экстракцию рекомбинантных векторов, содержащих их. При расщеплении на стадии (в) рекомбинантных векторов подходящими рестрикционными ферментами может быть идентифицирована с определением размера и картирована введенная в каждый вектор ДНК из S. peucetius 29050. Таким образом, может быть проверено и выявлено, что вектор содержит молекулу ДНК настоящего изобретения.
Кроме того, могут быть выделены две или более перекрывающихся вставки, которые полностью или частично соответствуют ДНК настоящего изобретения. Они могут быть слиты друг с другом при расщеплении на общем сайте рестрикции, с получением при последующем лигировании ДНК настоящего изобретения и, если нужно, объединением их попарно в длину при помощи подходящих рестрикционных ферментов. Рестрикционные фрагменты ДНК вставки, содержащие ген, кодирующий белок даунорубицин-14-гидроксилазу, могут быть получены на стадии (в) также при расщеплении вставочной ДНК соответствующими ферментами.
Приведенные ниже примеры иллюстрируют настоящее изобретение.
Краткое описание чертежей
Фиг. 1 показывает карту рестрикции ДНК настоящего изобретения. Она представляет собой вставку в рекомбинантной плазмиде pIS 70, которая была сконструирована с помощью инсерции в SphI сайте pWHM3 плазмиды - шаттл-вектора Escherichia coli - Streptomyces - SphI фрагмента ДНК размером 3,4 Kb, содержащего ген даунорубицин-14-гидроксилазы (dxrA), который получен из рекомбинантной плазмиды pIS62 путем частичного расщепления ее SphI (Vara et al. , J. Bacteriol. , 171, 5872, 1989). Представленная на фиг.1 карта не обязательно показывает все имеющиеся в сегменте ДНК сайты рестрикции. Однако указанных сайтов достаточно для однозначного распознавания сегментов.
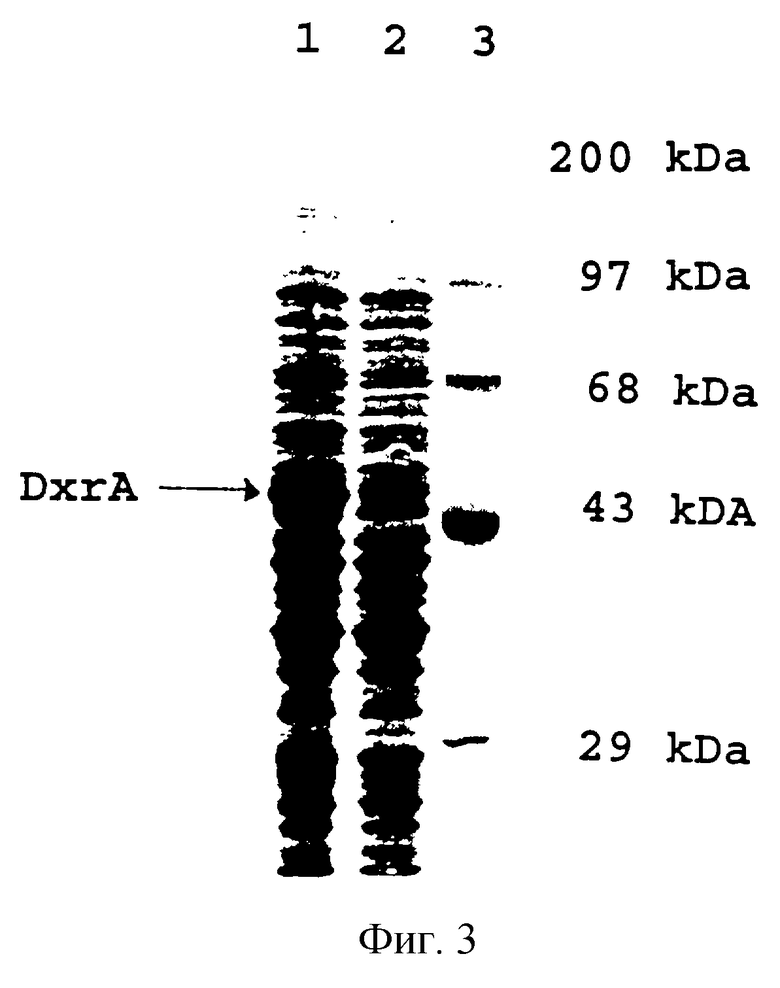
Фиг. 2 показывает карту рестрикции ДНК настоящего изобретения. Она представляет собой вставку в рекомбинантной плазмиде рWНМ969, которая была сконструирована с помощью инсерции в NdeI и BamHI сайты рЕТ14В - плазмидного вектора экспрессии E. coli - NdeI/BamHI фрагмента ДНК размером 1,33 Кb, который получен из KpnI/BamНI фрагмента ДНК рIS70 размером 1,36 Kb путем сайт-специфичного мутагенеза (Novagen, Madison, WI). В частности, NdeI сайт рестрикции (5'ЦАТ АТГ-3') был введен в KpnI/ВаmHI фрагмент ДНК размером 1,36 Kb путем мутагенеза ГТГ стартового кодона гена даунорубицин-14-гидроксилазы, а также двух нуклеотидов, вплотную предшествующих этому стартовому кодону, для репродуцирования целевой мишени, распознаваемой NdeI рестриктазой. С целью достижения эффективной экспрессии гена даунорубицин-14-гидроксилазы в E. coli, последовательность дикого типа, представленная на SEQ ID 1 соответствующим образом - для использования кодона E.coli - подвергают мутагенезу. Представленная на фиг.2 карта не обязательно показывает все имеющиеся в сегменте ДНК сайты рестрикции. Однако указанных сайтов достаточно для однозначного распознавания сегмента.
Фиг. 3 показывает окрашенный кумасси ДСН (SDS)-полиакриламидный гель клеточных экстрактов Escherichia coli, трансформированных векторами экспрессии dxrА и индуцированных с помощью ИПТГ (изопропилтиогалактозида) (IPTG) в течение 4 часов.
Полоса 1 - E. coli, трансформированная вектором экспрессии pWHM969 (молекулярный вес DxrA - 42280); полоса 2 - E.coli, трансформированная с применением рЕТ-14b (негативный контроль); полоса 3 - молекулярные веса стандартов.
Материалы и Методы
Бактериальные штаммы и плазмиды: штамм E.coli DH5α, чувствительный к ампициллину и апрамицину, используют для субклонирования фрагментов ДНК. S. Lividans ZX1 (Zhou et al., Nucleic Acids Res., 16, 4341, 1988) и S. peucetius dnrN (S. L. Otten, J. Ferguson and C.R. Hutchinson, J. Bacteriol., 177, 1216-1224, 1995) используют для экспрессии dxrA гена. Плазмидные векторы клонирования представляют собой pUCl8/19 (Yanisch - Perron et al., Gene, 33, 103, 1985) и pWHM3 (Vara et al., J. Bacteriol., 171, 5872, 1989).
Среды и буферы: E.coli DH5α поддерживают на LB агаре (Sambrook et al., Molecular Cloning. A Laboratory Manual, 2nd ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY, 1989). При отборе трансформантов добавляют ампициллин или апрамицин в концентрациях соответственно 100 мкг/мл и 50 мкг/мл. S. lividans для получения спор и регенерации протопластов поддерживают на R2YE агаре (Hopwood et al., Genetic Manipulation of Streptomyces, A Laboratory Manual, John Innes Foundation, Norwich, UК, 1995.
Субклонирование фрагментов ДНК: образцы ДНК после расщепления соответствующими рестриктазами разделяют с применением стандартных методик на агарозных гелях (Sambrook et al., Molecular Cloning. A Laboratory Manual, 2nd ed. , Cold Spring Harbor Press, Cold Spring Harbor, NY, 1989). С использованием ГЕНЕКЛИН (GENECLEAN) (Bio 101, LaJolla, СА) или эквивалентного устройства вырезают из геля агарозные слои, содержащие интересующие фрагменты ДНК. Выделенные фрагменты ДНК субклонируют в E.coli и E.coli/Streptomyces шаттл-векторах для проведения экспериментов соответственно по экспрессии и биотрансформации с использованием стандартной техники (Sambrook et al. , Molecular Cloning, A Laboratory Manual, 2nd ed., Cold Spring Harbor Press, Cold Spring Harbor, NY, 1989).
Трансформация видов Streptomyces и E.coli: Компетентные клетки E.coli получают кальций-хлоридным методом (Sambrook et al., Molecular Cloning, A Laboratory Manual, 2nd ed., Cold Spring Harbor Press, Cold Spring Harbor, NY, 1989) и трансформируют их далее с помощью стандартных методик (Sambrook et al., Moleсular Cloning. A Laboratory Manual, 2nd ed., Cold Spring Harbor Press, , Cold Spring Harbor, NY, 1989). Мицеллий S. lividans ZX1 выращивают на YEME среде (Hopwood et al., Genetic Manipulation of Streptomyces. A Laboratory Manual, John Innes Foundation, Norwich, UК, 1985) и собирают через 48 часов. Мицеллярный осадок промывают дважды 10,3% раствором сахарозы и используют для получения протопластов по методу, приведенному в руководстве Хопвуда (Hopwood et al., Genetic Manipulation of Streptomyces. A Laboratory Manual, John Innes Foundation, Norwich, UК, 1985). Протопластный осадок суспендируют примерно в 300 мкл Р-буфера (Hopwood et al., Genetic Manipulation of Streptomyces. A Laboratory Manual, John Innes Foundation, Norwich, UК, 1985) и используют для каждой трансформации 50-мкл аликвоту этой суспензии. Протопласты трансформируют плазмидной ДНК по микрометоду трансформации Хопвуда с соавт. (Hopwood et al., Genetic Manipulation of Streptomyces. A Laboratory Manual, John Innes Foundation, Norwich, UК, 1985). После проведения при 30oС 17-часовой регенерации на среде Р2УЕ на чашки наслаивают тиострептон в концентрации 50 мкг/мл и оставляют их расти при 30oС до спорообразования.
Биоконверсия даунорубицина в доксорубицин
Трансформанты S. lividans ZX1 и S. peucetius dnrN, несущие плазмиду настоящего изобретения, инокулируют в жидкую среду Р2УЕ, содержащую 10 мкг/мл тиострептона. После 2-х дней выращивания при температуре 30oС переносят 2,5 мл этой культуры в 25 мл среды, используемой для продуцирования (McGuire et al. , Process Biochem., 14, 2-5, 1979), которая содержит тиострептон в количестве 20 мкг/мл. Культуры выращивают в колбах Эрленмейера на роторной качалке со скоростью перемешивания 280 об/мин при температуре 30oС в течение 72 часов, после чего добавляют даунорубицин (в виде водного раствора с концентрацией 5 мг/мл) на каждые 10 мл культур до достижения конечной концентрации в 20 мкг/мл. После 24 часов последующей инкубации на качалке в культуры добавляют щавелевую кислоту для гидролиза гликозидных форм антрациклиновых метаболитов в количестве 25 мг/мл и продолжают инкубирование на водяной бане при температуре 55oС в течение 60 минут. Далее на качалке при температуре 30oС и скорости перемешивания 280 об/мин с помощью 10 мл смеси ацетонитрил: метанол (1:1) проводят в течение 30 минут экстракцию метаболитов из культур. Экстракты фильтруют, а полученный фильтрат анализируют методом высокоэффективной жидкостной хроматографии с обращением фаз (ВЭЖХ-ОФ). ВЭЖХ-ОФ осуществляют с использованием колонки Видак С18 (Vydak C18 column) (4,6•250 мм; частицы размером 5 мкм) с поддержанием скорости течения 0,385 мл/мин. Подвижная фаза А представляет собой 0,1% трифторуксусную кислоту [ТФУ, получаемую от Пиерс Кемикал Ко. (Pierce Chemical Co.)] в Н2О, а подвижная фаза В представляет собой 0,078% ТФУ в ацетонитриле [получаемую от Дж.Т.Бэйкер Кемикал Ко. (J.T. Baker Chemical Co.)]. Элюцию проводят при создании в течение 33 минут линейного градиента с содержанием от 20 до 60% фазы В в фазе А, осуществляя мониторинг с помощью диодного детектора при длине волны 488 нм (ширина полосы 12 мкм). Даунорубицин и доксорубицин используют в качестве внешних стандартов для определения количества исследуемых метаболитов, выделенных из культур.
Пример 1.
Клонирование гена dxrA, кодирующего даунорубицин-14-гидроксилазу
Несколько космидных клонов, описанных Штутцман-Энгваллом и Хатчинсоном (Stutzman - Engwall and Hutchinson, Proc. Natl. Acad. Sci. USA, 86, 3135, 1989), такие как рWНМ337 и pWHM338, или сходные клоны, получаемые из эквивалентных штаммов, несущие примерно от 20 до 90 кb геномной S. peucetius 29050, частично расщепляют рестриктазой ВаmНI, ДНК объединяют и снова лигируют, а полученную смесь плазмид (содержащих вектор рКС505 или эквивалентный вектор, способный к репликации как в E.coli, так и в видах Streptomyces) используют для трансформации E.coli DH5 с целью придания им устойчивости к апрамицину (или другого вида устойчивости соответственно выбранному вектору). Плазмидные ДНК из шестнадцати апрамицин-устойчивых клонов E.coli вводят в S. lividans ZX1, а в полученных трансформантах с помощью метода, описанного в разделе "Материалы и Методы" исследуют биоконверсию даунорубицина в доксорубицин. Плазмиду рIS23 выделяют из трансформанта, который осуществляет 3% конверсию внесенного даунорубицина в доксорубицин, при этом было показано, что она содержит вставку размером 13,5 Kb, охватываемую картой рестрикции, представленной на фиг. 1. Вставка в рIS23 используется для субклонирования Bg1 II/CiaI сегмента ДНК размером 4,9 Kb в pUC18, расщепленной рестриктазами BamHI и AccI. Из полученной плазмиды выделяют EcoRI/Hind III cегмент и субклонируют его в рWНМ3, расщепленную рестриктазами EcoRI и Hind III с получением плазмиды pIS 62. Трансформанты S. lividans ZX1 (pIS 62) получают по методу, описанному в разделе "Материалы и Методы", с последующим тестированием их на способность осуществлять биоконверсию даунорубицина в доксорубицин. Они оказались способными превращать до 16% внесенного даунорубицина в доксорубицин. SphI фрагмент ДНК размером 3,4 Kb клонируют из рIS62 в SphI сайт рWНМ3 с получением плазмиды рIS 70 (фиг.1). Трансформанты S. lividans ZX1 (pIS 70) получают по методу, описанному в разделе "Материалы и Методы", с последующим тестированием их на способность осуществлять биоконверсию даунорубицина в доксорубицин. Они оказались способными превращать до 22% внесенного даунорубицина в доксорубицин.
Пример 2.
Конверсия даунорубицина в доксорубицин клетками, которые содержат ген для синтеза даунорубицин-14-гидроксилазы, но не имеют продуктов других даунорубициновых генов
В штамм S. peucetius dnrN трансформацией по методу, описанному в разделе "Материалы и Методы", вводят плазмиды pIS 62 и pIS 70 с последующей селекцией на устойчивость к тиострептону. Полученные трансформанты S. peucetius dnrN (pIS 62) тестируют на способность осуществлять биоконверсию даунорубицина в доксорубицин. Было показано, что они обладают способностью превращать до 58% введенного даунорубицина в доксорубицин. Полученные трансформанты S. peucetius dnrN (pIS 70) также тестируют на способность осуществлять биоконверсию даунорубицина в доксорубицин. Оказалось, что они способны превращать до 100% введенного даунорубицина в доксорубицин.
Пример 3.
Экспрессия dxrA в Escherichia coli
Фактор экспрессии рЕТ-14b [коммерчески доступный от Новаген-Мэдисон WI (Novagen - Madison, WI)] основан на системе промотора из Т7. При использовании сайта рестрикции NdeI в рЕТ-14b возможна экспрессия клонированного белка, слитого с His-Nag на N-конце.
KpnI- BamHI фрагмент из вектора pIS 70 размером 1373 Kb (фиг.1), содержащий полностью dxrA ген, клонируют в pUC19 (Yanisch - Perron C., et al., Gene, 1985, 33, 103-119). Из полученной плазмиды удаляют SalI - BanHI фрагмент, затем проводят лигирование с KpnI - SalI линкером, который был получен с использованием двух олигонуклеотидов (51-мер SEQ ID 3 и 59-мер SEQ ID 4), синтезированных таким образом, что первый кодон в dxrА был изменен на АТГ, с созданием NdeI сайта, а третье положение четвертого, шестого и седьмого кодонов были изменены так, чтобы отражать наиболее часто используемый кодон в высокоэкспрессируемых генах E.coli, представляя собой средство усиления экспрессии dxrA. Полученный NdeI - BamHI фрагмент клонируют в pET-14b.
E. coli, используемая в качестве хозяйской клетки в экспериментах по экспрессии dxrA гена, представляет собой λ DE3 лизоген штамма BL 21 [коммерчески доступен от Новаген-Мэдисон WI (Novagen - Madison WI)]. Экспрессия dxrA при добавлении ИПТГ [изопропилтиогалактозида (IPTG)] в соответствии с приведенной ниже процедурой. Единичную колонию pWHM969 из свежей штриховки на чаше Петри инокулируют в 100 мл 2хУТ и ампициллин (50 мкг/мл) (фиг.2). Клетки выращивают при температуре 37oС до достижения величины оптической плотности ОП600=0,4-1,0. Экспрессию dxrА индуцируют добавлением 4 мМ ИПТГ и продолжают инкубацию в течение 3-4 часов.
0,5 мл культуры центрифугируют со скоростью 14000 об/мин в микроцентрифуге в течение 1 минуты, отбрасывают супернатант, а осадок ресуспендируют в 50 мкл буфера Лэммли (Laemmli, Nature, 227, 680, 1970) и кипятят полученную суспензию в течение 5 минут. Содержащиеся в прокипяченном образце белки анализируют стандартными методами с применением 10% ДСН-агарозного геля (фиг. 3) (Laemmli, Nature, London, 227, 680, 1970) при сравнении результатов анализа с данными, полученными с использованием вектора рЕТ 14b, не содержащего dxrA ген.
По данным миграции белка даунорубицин-14-гидроксилазы его относительная молекулярная масса (Мr) была оценена как 42280.






Изобретение относится к области генетической инженерии и может быть использовано для промышленного получения антибиотика доксорубицина, обладающего противоопухолевой активностью. В результате скрининга геномной библиотеки штамма Streptomyces peucetius (АТСС 29050) клонирован фрагмент ДНК, который включает ген, кодирующий даунорубицин-14-гидроксилазу. Путем трансформации штаммов Streptomyces и Е.coli вектором, содержащим названный ген, получены рекомбинантные штаммы, обладающие способностью при культивировании в присутствии даунорубицина эффективно превращать его в дексорубицин. 3 с. и 3 з.п. ф-лы, 3 ил.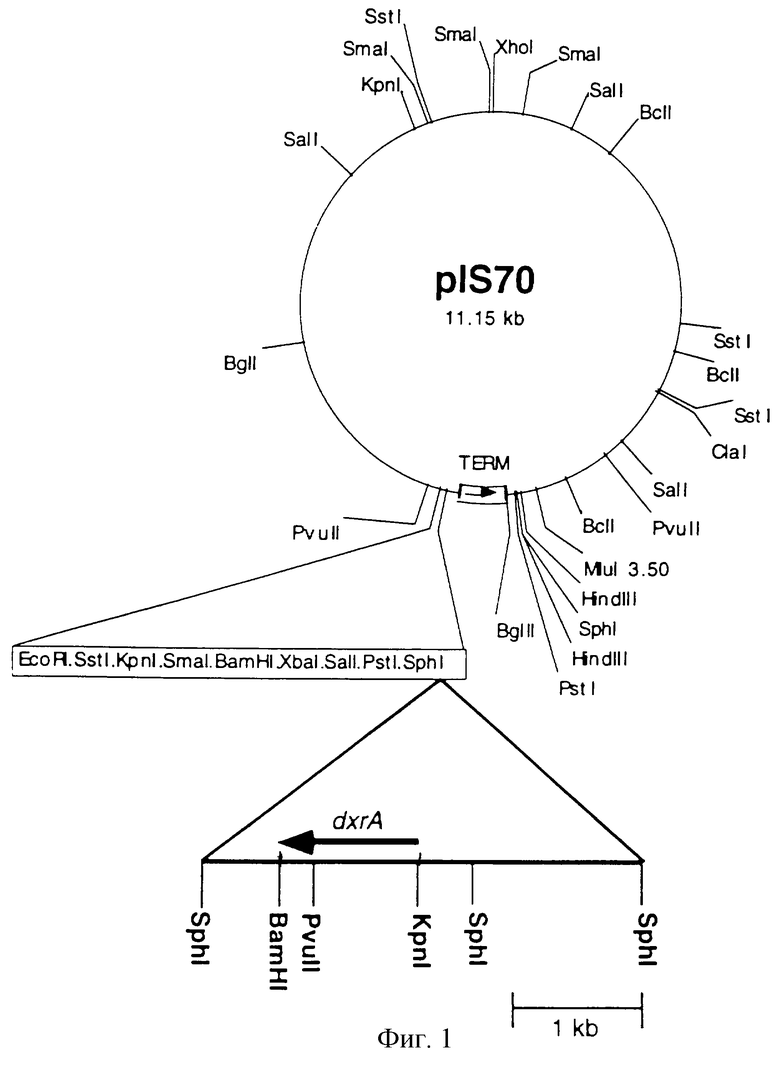
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| OTTEN S.L | |||
| et al | |||
| Journal of Bacteriology, v.172, № 6, 3427-3434, 1990 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| STUTZMAN-ENGWALL K.J | |||
| et al | |||
| Proc | |||
| Natl | |||
| Acad | |||
| Sci | |||
| USA, v.86, № 9, 3135-3139, 1989 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ непрерывного получения бромистого этила | 1939 |
|
SU61737A1 |
Авторы
Даты
2003-05-27—Публикация
1996-02-20—Подача