Настоящее изобретение относится к конъюгату, содержащему антагонист фолиевой кислоты и носитель, способу получения такого конъюгата, а также к его применению.
Фолиевая кислота является встречающимся в природе соединением, имеющим важное значение для переноса метильных групп в клетках, а тем самым и для роста клеток. Фолиевая кислота имеет следующую структурную формулу: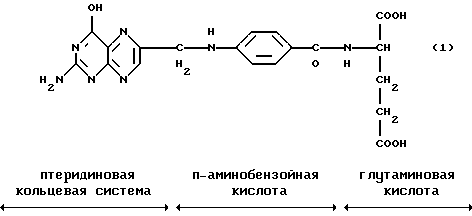
СН-группа глутаминовой кислоты содержит асимметричный атом. Следовательно, фолиевая кислота существует в двух энатиомерных формах, а именно в виде D- и L-энантиомеров.
Однако из этих энантиомерных форм только L-энантиомер находится в клетках, благодаря чему только эта форма фолиевой кислоты, но не D-энантиомер, ответственна за ее действие. Причина этого заключается в том, что фолиевая кислота поглощается клетками через фолатный рецептор, который, однако, поглощает только L-энатиомер фолиевой кислоты, но не поглощает ее D-энантиомер.
Антагонистами фолиевой кислоты являются соединения, которые представляют собой производные фолиевой кислоты, но которые противодействуют ей именно в том месте, куда она стремится, т.е. в клетках. Поэтому антагонисты фолиевой кислоты существуют в виде L-энатиомеров, а не в виде D-энатиомеров. Примерами антагонистов фолиевой кислоты являются аминоптерин и аметоптерин, который имеет и другое название - метотрексат.
Метотрексат, т. е. L-энантиомер аметоптерина, часто применяется для лечения опухолей и воспалений. При этом, однако, имеют место значительные побочные действия, поскольку метотрексат поглощается также здоровой тканью, для которой он токсичен. Конъюгаты из метотрексата и альбумина, которые более интенсивно поглощаются опухолями, чем здоровой тканью, и тем самым являются менее токсичными, описаны только в DE-A 4122210.5. Тем не менее существует необходимость в разработке средств, которые обладали бы еще меньшими побочными действиями.
Исходя из вышеизложенного, в основу настоящего изобретения была положена задача разработать средство для лечения больных тканей, в частности для терапии опухолей, которое обладало бы минимальным побочным действием.
Согласно изобретению указанная цель достигается с помощью технических решений, представленных в формуле изобретения.
Объектом настоящего изобретения является, следовательно, конъюгат, содержащий D-энантиомер антагониста фолиевой кислоты и носитель.
Настоящее изобретение основано на полученных заявителем результатах исследований, которые свидетельствуют о том, что D-энантиомер антагониста фолиевой кислоты в конъюгате, содержащем носитель, предпочтительно поглощается больной тканью, в частности опухолевыми клетками, и в них проявляет свое действие против заболевания. Далее было установлено, что D-энантиомер антагониста фолиевой кислоты как таковой, т.е. существующий не в конъюгате по изобретению, не оказывает побочных действий на здоровую ткань.
Понятие "конъюгат" указывает на то, что антагонист фолиевой кислоты и носитель связаны ковалентно, например, через амидные и/или сложноэфирные связи, соответственно через линкер.
Понятие "D-энантиомер антагониста фолиевой кислоты" включает соединения любого типа, которые являются производными фолиевой кислоты, действуют в качестве антагониста фолиевой кислоты и существуют в виде D-энантиомера. D-энантиомер антагониста фолиевой кислоты содержит в качестве компонентов птеридин, в частности птерин, п-аминобензойную кислоту и D-аминокислоту, прежде всего D-глутаминовую кислоту, которые химически изменены, т.е. модифицированы относительно имеющихся в фолиевой кислоте компонентов. Эти изменения включают, например, замещения, такие как замещение атомов водорода С1-С4 алкильными группами, в частности метильной группой, атомами галогена, такими как F, Cl, Вr и I, ОН- и NH2-группами, замещение ОН-групп вышеуказанными алкильными группами, NH2-группами, атомами водорода и галогена, а также замещение NH2-групп вышеуказанными алкильными группами, ОН-группами, атомами водорода и галогена. Далее, одна или обе карбоксильные группы глутаминовой кислоты могут присутствовать в виде кислотного производного, например в виде эфира или амида. Из вышеупомянутых модификаций одна или несколько могут присутствовать в применяемых согласно изобретению антагонистах фолиевой кислоты.
Антагонистами фолиевой кислоты предпочтительно являются D-аметоптерин (ниже называемый D-метотрексатом)
D-аминоптерин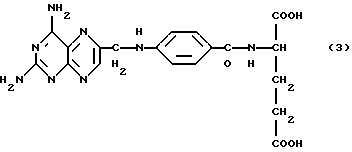
и D-e,t-ФМТК (аналог метотрексата, у которого глутаминовая кислота (Glu) заменена на D-эритро,трео-4-фторо-Glu).
Конъюгат по изобретению может содержать в своем составе один или несколько антагонистов фолиевой кислоты. Если он содержит несколько антагонистов, то последние могут быть как одинаковыми, так и отличными друг от друга.
Понятие "носитель" включает соединения любого типа, которые пригодны для обогащения конъюгата в больной ткани, например в опухоли или очаге воспаления. Примеры таких носителей включают белки, которые не рассматриваются как чужеродные для организма, и простые полиэфиры.
Белки предпочтительно присутствуют в нативной форме. В нативной форме белки не имеют межмолекуляных и/или внутримолекулярных поперечных связей. Предпочтительно белки имеют молекулярную массу до 100000 дальтон, в частности от 30000 до 100000 дальтон. Далее, целесообразно использовать белки человека. Примеры белков включают альбумин, фибриноген, трансферрин, иммуноглобулины и липопротеины, причем предпочтителен человеческий альбумин. Могут применяться также фрагменты вышеуказанных белков. Кроме того, последовательность белков, соответственно их фрагментов может иметь модификации одной или нескольких аминокислот в сравнении с известной последовательностью белков, соответственно их фрагментов.
Примерами простых полиэфиров являются полиэтиленгликоли, в частности таковые с молекулярной массой от 100 до 20000 дальтон. Предпочтительны полиэтиленгликоли, которые этерифицированы до сложного или простого эфира по концевой гидроксильной группе С1-С12алкильной группой, прежде всего метильной группой.
Предлагаемый конъюгат может иметь один или несколько, в частности два, вышеуказанных носителя. Если он содержит несколько носителей, то последние могут быть как одинаковыми, так и отличными друг от друга. В случае нескольких полиэфиров последние предпочтительно выбирают таким образом, чтобы молекулярная масса всех полиэфиров составляла приблизительно 20000 или более дальтон.
В предлагаемом конъюгате антагонист фолиевой кислоты может быть ковалентно соединен с носителем непосредственно или через линкер, т.е. между носителем и антагонистом фолиевой кислоты присутствует линкер. В качестве линкера пригодны все соединения, способные соединять антагонист фолиевой кислоты с носителем.
Предпочтительно, чтобы линкер обладал способностью расщепляться в клетке. Термин "клетка" включает отдельные клетки и состоящие из клеток структуры. Примерами первых являются эндогенные клетки, не объединенные в общую структуру с другими клетками. Примерами объединенных в общую структуру клеток являются ткани, органы и опухоли.
Линкер вышеуказанного типа известен специалистам в данной области техники. Специалистам известны также факторы, например ферменты, которые обусловливают расщепление определенных химических связей в клетках. Поэтому специалист в данной области техники может сконструировать расщепляемые в клетке линкеры. Особенно предпочтительно, чтобы такой линкер включал азогруппу. Более предпочтительно, если линкер имеет следующую структуру:
-Y-R-N=N-
где R обозначает органическую группу, предпочтительно ароматическую, особенно предпочтительно фенилен или его производное, и
Y обозначает группу, выбранную из С(О), S(O)2, P(O)OH и As(О)ОН.
Вышеуказанная структура предпочтительного линкера соответствует той, которую имеет линкер в конъюгате по изобретению. Кроме того, эта структура, по меньшей мере если R представляет собой фенилен или его производное, включает активное соединение, которое наиболее пригодно для лечения опухолевых, воспалительных и аутоиммунных заболеваний. После расщепления линкера и при определенных условиях разложения еще связанного с линкером белка это соединение может в полной мере проявить свою активность.
Предлагаемые согласно изобретению конъюгаты могут быть получены путем ковалентного связывания антагониста фолиевой кислоты с носителем и при необходимости с линкером. Пригодные для этой цели способы, а также необходимые материалы известны специалистам в данной области техники.
Если антагонист фолиевой кислоты имеет по меньшей мере одну карбоксильную группу, например карбоксильную группу глутаминовой кислоты, конъюгаты можно получать путем взаимодействия антагониста фолиевой кислоты с карбодиимидом и гидроксисукцинимидом с образованием реакционноспособных сложных сукцинимидиловых эфиров и взаимодействия последних с носителем. В случае конъюгатов с несколькими антагонистами фолиевой кислоты сукцинимидиловые эфиры можно получать совместно или раздельно.
Взаимодействие антагонистов фолиевой кислоты с карбодиимидом и гидроксисукцинимидом проводят в полярном апротонном растворителе, предпочтительно диметилформамиде (ДМФ). Молярное отношение антагонист фолиевой кислоты : карбодиимид : гидроксисукцинимид составляет приблизительно 1:1,5:10. Образовавшийся сложный сукцинимидиловый эфир затем подвергают взаимодействию в водном буферном растворе, предпочтительно NаНСО3, с носителем, таким как альбумин. Концентрация носителя составляет приблизительно от 10 до 70 мг/мл. Активированная таким образом карбоксильная группа может затем реагировать с ОН- и NH-группами носителя с образованием амидных и эфирных связей кислоты, причем в результате этой реакции получают предлагаемые в изобретении конъюгаты. Эти конъюгаты можно подвергать многократной очистке, например, путем ультрафильтрации, и затем стерилизовать фильтрацией, после чего они готовы для применения.
Предлагаемые согласно изобретению конъюгаты отличаются тем, что они остаются в течение длительного времени в системе кровообращения пациента. Далее, они накапливаются в больной ткани, в частности в опухолях и очагах воспаления. Кроме того, конъюгаты по изобретению отличаются тем, что они обладают еще меньшим побочным действием, чем конъюгаты с антагонистами L-фолиевой кислоты, известными из DE-A 4122210.5, причем их действие на больные ткани, прежде всего опухоли и очаги воспаления, сохраняется.
Таким образом, предлагаемые согласно изобретению конъюгаты наиболее пригодны для лечения опухолей, таких как гематологические и солидные опухоли, воспалений, например заболеваний ревматичесого характера, таких как хронический полиартрит, или псориаза, и аутоиммунных заболеваний.
Ниже изобретение проиллюстрировано на примерах.
Пример 1: Получение предлагаемого в изобретении конъюгата из D-метотрексата и человеческого сывороточного альбумина.
D-метотрексат (D-MTK) растворяли в концентрации 20 мг/мл в диметилформамиде. К прозрачному желтому раствору добавляли 1,5 моля дициклогексилкарбодиимида и приблизительно 10 молей гидроксисукцинимида. По истечении приблизительно 12 ч реакции превращение в сложный сукцинимидиловый эфир (D-MTK-ГСИЭ) завершалось, что можно было установить по выпавшему в кристаллический осадок количеству дициклогексилмочевины (ДЦМ). Аналитический контроль реакции проводили с помощью тонкослойной хроматографии:
пластинки: силикагель 60 с флуоресцентным индикатором;
система растворителей: этилацетат/МеОН в соотношении 75/25;
значения Rf: для D-MTK 0,0; для D-MTK-ГСИЭ 0,35-0,38.
Прозрачный желтый раствор D-MTK-ГСИЭ в ДМФ медленно, при постоянном перемешивании добавляли к раствору белка (50-70 мг человеческого сывороточного альбумина в 0,17-молярном растворе NаНСО3, рН 8,5), при этом по истечении некоторого времени появлялось помутнение, обусловленное взвесью из непрореагировавшего дициклогексилкарбодиимида и еще растворенной в диметилформамиде ДЦМ. По истечении по меньшей мере 30 мин реакции взвесь отделяли фильтрованием через стерилизационный фильтр (0,22 мкм), а диметилформамид удаляли путем ультрафильтрации с соответствующим мембранным фильтром (YM30, фирма Amicon).
Контроль чистоты проводили с помощью жидкостной хроматографии высокого разрешения (ЖХВР):
предварительная колонка: Zorbach Diol размером 50•4 мм;
колонки: 1-я: Zorbach GF 450, 2-я: Zorbach GF 250;
элюент: 0,2М фосфатный буфер, рН 7,4;
скорость потока: 1,0 мл/мин;
давление: около 65 бар.
В результате получили конъюгат по изобретению из D-метотрексата и человеческого сывороточного альбумина.
Пример 2: Сравнение токсичности конъюгата по изобретению, полученного из D-метотрексата и человеческого сывороточного альбумина, с конъюгатом, полученным из метотрексата и человеческого сывороточного альбумина.
Для этого опыта применяли конъюгат по изобретению из D-метотрексата и человеческого сывороточного альбумина (D-MTK-ЧCA) из примера 1. Далее применяли известный из DE-A 4122210.5 конъюгат, полученный из метотрексата и человеческого сывороточного альбумина (МТК-ЧСА).
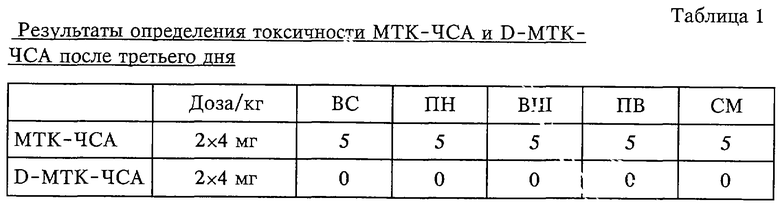
Группам из пяти здоровых крыс линии Sprague-Dawley вводили D-MTK-ЧCA, соответственно МТК-ЧСА. Крысам инъицировали по 4 мг конъюгата (в пересчете на долю МТК, соответственно D-MTK в конъюгатах) на килограмм веса тела с двухдневным интервалом. Полученные результаты представлены в таблице 1.
Использованные в таблице 1 сокращения имеют следующие значения: ВС означает "воспаление слизистой оболочки"; ПН означает "понос"; ВШ означает "взъерошенная шерсть"; ПВ означает "потеря веса"; СМ означает "смерть".
Как видно из таблицы 1, крысы при введении им конъюгата МТК-ЧСА, уже начиная с третьего дня, испытывали сильные побочные действия. На четвертый день две крысы были найдены мертвыми в клетке. Остальных трех крыс пришлось умертвить, поскольку они страдали от сильных побочных действий. В отличие от этого ни у одной из крыс, которым вводили конъюгат D-MTK-ЧCA по изобретению, не отмечалось побочных действий.
Таким образом, конъюгаты по изобретению оказывают лишь незначительные побочные действия.
Пример 3: Терапия опухолей конъюгатом по изобретению, полученным из D-метотрексата и человеческого сывороточного альбумина, в сравнении с коньюгатом, полученным из метотрексата и человеческого сывороточного альбумина.
Для этого опыта применяли указанные в примере 2 конъюгаты. В качестве подопытных животных использовали крыс-носителей карциносаркомы линии Walker-256. Лечение начинали на шестой день после пересадки опухоли объемом от 1000 до 2500 мм3 (диаметр опухоли от 1•1 до 1•2 см). Пяти крысам вводили МТК-ЧСА (3 инъекции с двухдневным интервалом дозой по 2 мг МТК-ЧСА в пересчете на долю МТК на килограмм веса тела). Предлагаемый в изобретении конъюгат D-MTK-ЧCA вводили двойной дозой согласно вышеприведенному протоколу. При указанных дозах в случае МТК-ЧСА имели место значительные побочные действия, тогда как при введении предлагаемого конъюгата D-MTK-ЧСА побочных действий не наблюдалось (см. пример 2). Полученные результаты представлены в таблице 2.
Использованные в таблице 2 сокращения имеют следующие значения: ПД означает "побочные действия"; СМ означает смерть в результате рецидива опухоли.
Результаты, приведенные в таблице 2, показывают, что в группе, в которой животным вводили МТК-ЧСА, опухоль спадала у трех животных (ремиссия). В этой группе у двух крыс имел место рецидив, и их пришлось умертвить. У трех крыс наблюдались побочные действия. В отличие от этого в группе, в которой животным вводили конъюгат D-MTK-ЧСА по изобретению, все животные излечивались от опухоли и при этом не наблюдалось побочных действий, хотя в сравнении с группой, которой вводили МТК-ЧСА, применяли двойную дозу конъюгата.
Таким образом, конъюгаты по изобретению обладают минимальными побочными действиями, причем с помощью этих конъюгатов возможно достижение исключительно высоких результатов в терапии опухолей.

Изобретение относится к медицине и касается конъюгата, содержащего D-энантиомер антагониста фолиевой кислоты и носитель, используемого для терапии опухолей. Конъюгат обладает повышенной активностью. 2 с. и 11 з.п.ф-лы, 2 табл.
| КОНЪЮГАТЫ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ С α -ФЕТОПРОТЕИНОМ, ОБЛАДАЮЩИЕ ИЗБИРАТЕЛЬНЫМ ДЕЙСТВИЕМ ПО ОТНОШЕНИЮ К РАКОВЫМ ОПУХОЛЯМ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1996 |
|
RU2071351C1 |
| ЗАГРУЗЧИК ЗАГОТОВОК ПРОТЕКТОРОВ КРУПНОГАБАРИТНЫХ ШИН | 0 |
|
SU251455A1 |
| Устройство для выпрямления опрокинувшихся на бок и затонувших у берега судов | 1922 |
|
SU85A1 |
Авторы
Даты
2003-06-10—Публикация
1998-05-08—Подача