Изобретение относится к области ветеринарной вирусологии, в частности к инактивированной вакцине против коронавирусного энтерита собак.
Известна инактивированная вакцина, содержащая в основе инактивированный вирус гастроэнтерита свиней (TGEV) (1).
Известна также вакцина против коронавирусного энтерита собак, содержащая в основе инактивированную и осажденную на гидрате окиси алюминия вирусную суспензию штамма Canine coronavirus 1-743 (2).
Известные вакцины на территории Российской федерации не использовались, а приводимая информация в указанных патентных источниках не позволяет сделать суждение об их преимуществах по сравнению с предлагаемой. Вакцина, содержащая в своей основе вирус трансмиссивного гастроэнтерита свиней (ТГЭС), менее эффективна из-за того, что используемый штамм ТГЭС не является близкородственным коронавирусу собак.
Целью изобретения является вакцина для профилактики коронавирусного энтерита собак, обладающая безвредностью и высокой иммуногенной активностью.
Цель достигается использованием в составе вакцины в качестве антигена коронавирусного энтерита собак инактивированной и осажденной на гидрате окиси алюминия вирусной суспензии штамма Coronavirus canine "Карат" ВГНКИ 29-ДЕП с титром инфекционной активности 105,5-106,5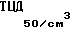 и дополнительно гидролизата лактальбумина в растворе Хенкса при следующем соотношении компонентов (мас.%):
и дополнительно гидролизата лактальбумина в растворе Хенкса при следующем соотношении компонентов (мас.%):
Инактивированная и осажденная на гидрате окиси алюминия вирусная суспензия штамма Coronavirus canine "Карат" ВГНКИ 29-ДЕП с титром инфекционной активности 105,5-106,5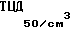 - 50-70
- 50-70
Гидролизат лактальбумина в растворе Хенкса - 30-50
Штамм Coronavirus canine "Карат" ВГНКИ 29-ДЕП является известным и используется для контроля иммуногенной активности вакцин и получения сывороток для лечения и диагностики коронавирусной инфекции собак (3).
Изобретение иллюстрируется следующими примерами.
Пример 1.
Изготавливают вакцину для профилактики коронавирусного энтерита собак. Для получения вирусного материала штамма "Карат" коронавирусного энтерита собак используют первично-трипсинизированную культуру клеток почек собак 1-3 месячного возраста. В качестве ростовой среды применяют среду, содержащую гидролизат лактальбумина - 50%, среду Игла с глутамином - 20%, среду 199 - 20%, сыворотку крови крупного рогатого скота - 10% и антибиотики (гентамицин 0,1 мг на 1 см3 среды).
Для получения вируса из матрасов со сформированным клеточным монослоем удаляют ростовую питательную среду, клеточный монослой аккуратно дважды ополаскивают теплой питательной средой без сыворотки в объеме 50 см3 и заражают штаммом "Карат" с активностью вируса 105,5-106,5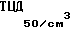 в дозе 20 см3 на полуторалитровые матрасы. Зараженную культуру клеток выдерживают для адсорбции вируса в течение 1 ч при температуре 37oС, после чего добавляют поддерживающую среду в объеме 200 см3 и инкубируют в условиях термостата в течение 5-7 сут. В качестве поддерживающей используют среду, содержащую те же компоненты, что и ростовая, но без добавления сыворотки. Размножение вируса оценивают по цитопатическому действию. Поражение 70% клеточного монослоя свидетельствует о высоком уровне накопления вируса и необходимости прекращения его культивирования. Цитопатическое действие в чувствительных культурах клеток характеризуется округлением и скоплением эпителиоподобных клеток, а фибробластоподобные клетки удлиняются, образовывая своеобразные тяжи. Монослой принимает вид узорчатого кружева. На 4-5 сут зараженные клетки начинают отделяться от стекла. Для более полного выхода вируса из зараженных клеток матрасы с вирусной суспензией трехкратно замораживают при -40oС и оттаивают при 20oС. Полученную вируссодержащую культуральную суспензию штамма "Карат" с титром инфекционной активности 105,5-106,5
в дозе 20 см3 на полуторалитровые матрасы. Зараженную культуру клеток выдерживают для адсорбции вируса в течение 1 ч при температуре 37oС, после чего добавляют поддерживающую среду в объеме 200 см3 и инкубируют в условиях термостата в течение 5-7 сут. В качестве поддерживающей используют среду, содержащую те же компоненты, что и ростовая, но без добавления сыворотки. Размножение вируса оценивают по цитопатическому действию. Поражение 70% клеточного монослоя свидетельствует о высоком уровне накопления вируса и необходимости прекращения его культивирования. Цитопатическое действие в чувствительных культурах клеток характеризуется округлением и скоплением эпителиоподобных клеток, а фибробластоподобные клетки удлиняются, образовывая своеобразные тяжи. Монослой принимает вид узорчатого кружева. На 4-5 сут зараженные клетки начинают отделяться от стекла. Для более полного выхода вируса из зараженных клеток матрасы с вирусной суспензией трехкратно замораживают при -40oС и оттаивают при 20oС. Полученную вируссодержащую культуральную суспензию штамма "Карат" с титром инфекционной активности 105,5-106,5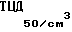 сливают в одну стерильную емкость. Для удаления клеточного детрита полученную вирусную суспензию подвергают фильтрации на системе "Миллипор" с диаметром фильтра 293 мм и размером пор 0,22 мкм при давлении 15 Пси. Вирус инактивируют формалином сначала в условиях термостата, а затем при комнатной температуре.
сливают в одну стерильную емкость. Для удаления клеточного детрита полученную вирусную суспензию подвергают фильтрации на системе "Миллипор" с диаметром фильтра 293 мм и размером пор 0,22 мкм при давлении 15 Пси. Вирус инактивируют формалином сначала в условиях термостата, а затем при комнатной температуре.
К инактивированному формалином вирусу добавляют, тщательно перемешивая, стерильный раствор гидроокиси алюминия (ГОА) и оставляют для отстаивания при комнатной температуре, после чего 30-50% надосадка удаляют и вносят до первоначального объема питательную среду гидрализат лактальбумина на растворе Хенкса.
Получают 3 серии вакцины следующего состава: (см. табл.A).
Готовая вакцина представляет собой жидкость розового или красновато-розового цвета с рыхлым осадком, легко разбивающимся при встряхивании в гомогенную взвесь.
Пример 2.
Безвредность вакцины серии 3 против коронавирусного энтерита собак проверяют на лабораторных животных (морских свинках массой 250-300 г и на мышах массой 14-16 г) и естественно восприимчивых животных.
Вакцину вводят подопытным животным и проводят наблюдения в течение 10 дней.
Результаты проверки представлены в табл. 1.
Из табл. 1 видно, что вакцина является безвредной. За период наблюдения воспалительной реакции на месте введения препарата и случаев заболевания животных не отмечают.
Пример 3.
Проверяют безвредность вакцины против коронавирусного энтерита собак серии 1 и 2 аналогично, как в примере 2, на 10 морских свинках и 20 белых мышах.
Устанавливают безвредность указанных серий на лабораторных животных.
Пример 4.
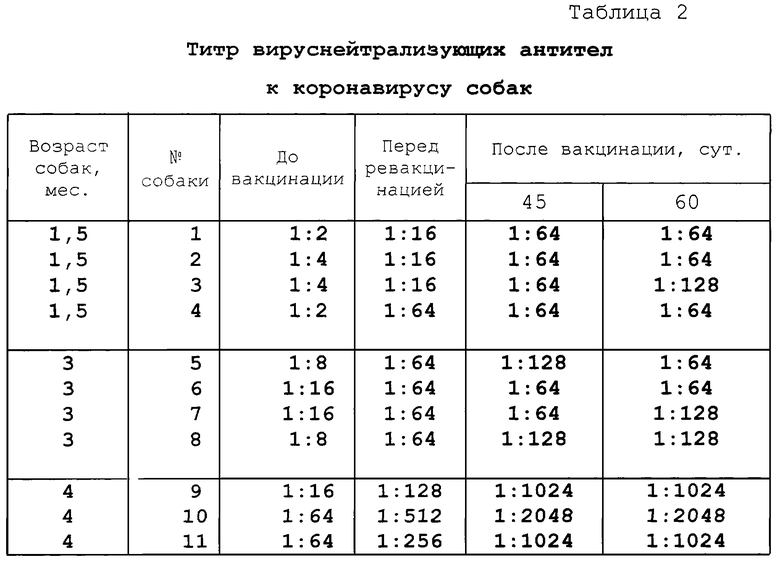
Изучение оптимальных сроков применения вакцины против коронавирусного энтерита собак серии 3 проводят на 3-х группах щенков в возрасте 1,5, 3 и 4 месяцев. Животных вакцинируют внутримышечно двукратно с интервалом 14 сутб в дозе 0,5 см3. Динамика накопления антител к коронавирусу собак в реакции - непрямой гемагглютинации показана в табл. 2.
Из табл. 2 следует, что предложенная вакцина позволяет создать напряженный иммунитет у щенков не только 3-х и 4-х месячного возраста, но и у щенков 1,5 месячного возраста - у щенков раннего возрастного периода, особенно подверженных заболеванию коронавирусным энтеритом.
Пример 5.
Оценку иммунологической эффективности вакцины против коронавирусного энтерита собак проводят на 12 подопытных и 4 контрольных щенках собак 3-х месячного возраста путем их экспериментального заражения контрольным штаммом "Карат".
Подопытных животных (по 4 гол. в группе) предварительно прививают вакциной против коронавирусного энтерита собак серий 1, 2, 3 внутримышечно в дозе 1 см3.
На 21 сутки от начала эксперимента всех животных заражают контрольным штаммом в дозе 106,0 ТЦД50/см3.
Все серии предложенной вакцины у подопытных щенков не вызывают поствакцинальных осложнений и создают высокий защитный эффект при контрольном заражении.
На 3 сутки после заражения у щенков контрольной группы наблюдают угнетенное состояние, учащенную дефекацию, фекалии жидкой консистенции. На 7 сутки 3 щенка контрольной группы пали с признаками тяжелой формы диареи. На вскрытии у павших животных отмечают обезвоживание, увеличение лимфоузлов кишечника. Слизистая оболочка кишечника утолщена, гиперемирована, с точечными кровоизлияниями и участками некроза.
Пример 6.
Антигенную активность вакцины определяют на щенках собаки 3-х месячного возраста и кроликах. Животных вакцинируют внутримышечно или подкожно вакциной против коронавирусного энтерита собак серии 1 в дозе 1 см3 и на 1, 14 и 21 день проводят взятие крови для определения уровня индуцированных вакциной гуморальных антител.
Антитела к коронавирусу собак определяют в реакции непрямой гемагглютинации. Результаты представлены в табл. 3.
По данным табл. 3 видно, что возрастание уровня антител к антигену, входящему в вакцину, наиболее выражено через 2 недели после 2-й вакцинации.
Данная серия вакцины обладает антигенной активностью, так как титр антител в сыворотке крови привитых щенков собак и кроликов к коронавирусу собак возрастает в 2-4 и более раз.
Использование кроликов вместо щенков собак для контроля антигенной активности данной вакцины позволит упростить и удешевить проведение исследований.
Использование вакцины на основе штамма Coronavirus canine "Карат" ВГНКИ 29 ДЕП позволяет в короткий срок сформировать у собак иммунитет высокой напряженности и до минимума снизить заболеваемость собак данной инфекцией.
Источники информации
1. US 5911999, 15.06.99.
2. US 5464621, 07.11.95.
3. RU 2100433, 27.11.97.



Изобретение относится к области ветеринарной вирусологии. Вакцина содержит инактивированную и осажденную на гидрате окиси алюминия вирусную суспензию штамма коронавируса собак "Карат" с титром инфекционной активности 105,5-106,5 ТЦД50/см3. Для инактивации вируса используют формалин. Дополнительно вакцина содержит гидролизат лактальбумина на растворе Хенкса при следующем соотношении компонентов, мас. %: вирусная суспензия штамма "Карат" 50-70, гидролизат лактальбумина на растворе Хенкса 30-50. Вакцина безвредна, позволяет в короткий срок создать у собак иммунитет высокой напряженности, до минимума снизить заболеваемость данной инфекцией. 4 табл.
Вакцина против коронавирусного энтерита собак, содержащая инактивированный и осажденный на гидрате окиси алюминия антиген коронавирусного энтерита собак, отличающаяся тем, что она в качестве антигена коронавирусного энтерита собак содержит инактивированную и осажденную на гидрате окиси алюминия суспензию штамма Coronavirus canine "Карат" ВГНКИ 29 ДЕП с титром инфекционной активности 105,5-106,5 ТЦД50/см3 и дополнительно гидролизат лактальбумина на растворе Хенкса при следующем соотношении компонентов, мас. %:
Инактивированная и осажденная на гидрате окиси алюминия суспензия штамма Coronavirus canine "Карат" ВГНКИ 29 ДЕП с титром инфекционной активности 105,5-106,5 ТЦД50/см3 - 50 - 70
Гидролизат лактальбумина на растворе Хенкса - 30 - 50
| US 5911999 А, 15.06.1999 | |||
| US 5464621 А, 07.11.1995 | |||
| ШТАММ CORONAVIRUS CANINE, ИСПОЛЬЗУЕМЫЙ ДЛЯ КОНТРОЛЯ ИММУНОГЕННОЙ АКТИВНОСТИ ВАКЦИН И ПОЛУЧЕНИЯ СЫВОРОТОК ДЛЯ ЛЕЧЕНИЯ И ДИАГНОСТИКИ КОРОНАВИРУСНОЙ ИНФЕКЦИИ СОБАК | 1996 |
|
RU2100433C1 |
Авторы
Даты
2003-09-10—Публикация
2001-12-21—Подача