Область техники
Настоящее изобретение относится к твердому диспергирующему агенту некристаллического цефуроксим-аксетила, способу его получения и к содержащей этот агент композиции для перорального введения, которая имеет улучшенную биодоступность и стабильность цефуроксим-аксетила.
Предпосылки изобретения
Цефуроксим-аксетил представляет собой цефалоспориновый антибиотик, обладающий высокой активностью против широкого спектра грамположительных и грамотрицательных микроорганизмов. Он проявляет полиморфизм в трех формах: в кристаллической форме, имеющей температуру плавления приблизительно 180oС, в по существу аморфной форме, имеющей температуру плавления приблизительно 135oС, и в по существу аморфной форме, имеющей температуру плавления приблизительно 70oС. Кристаллическая форма цефуроксим-аксетила, которая плохо растворима в воде и образует гель при контакте с водной средой, с трудом абсорбируется в желудочно-кишечном тракте, что делает ее биодоступность при пероральном применении очень низкой.
В патенте США 4820833 раскрыт способ получения очень чистой по существу аморфной формы цефуроксим-аксетила из кристаллической формы с целью улучшения растворимости лекарства. По существу аморфная форма цефуроксим-аксетила с низкой температурой плавления имеет более высокую растворимость в воде, чем кристаллическая форма. Однако она образует очень густой гель при контакте с водной средой, создавая в результате проблемы при работе в процессе получения из нее фармацевтической композиции. Более того, в описанном выше способе из-за липкости аморфного продукта возникает проблема низкого выхода, составляющего приблизительно 70%.
Кроме того, в корейской патентной публикации 94-233 описана легко распадающаяся таблетка с пленочным покрытием, содержащая ядро из аморфного цефуроксим-аксетила и покрывающую пленку, имеющую время разрыва менее чем 40 с, которая разработана с целью предупреждения желатинизации цефуроксим-аксетила в водной среде, а также для маскировки горького вкуса лекарства. Эта таблетка коммерчески доступна как таблетка Zinnat®, продаваемая фирмой Glaxo Group Limited (London, England). Однако в случае такой таблетки имеет место проблема, заключающаяся в том, что биодоступность цефуроксим-аксетила может ухудшаться, когда время разрыва покрывающей пленки не строго отрегулировано.
В международной публикации PCT WO 99/08683 описан продукт соосаждения, содержащий низкоплавкую аморфную форму цефуроксим-аксетила и растворимый в воде наполнитель, например повидон. Продукт соосаждения полезен при получении таблетки, которая не ограничена временем разрыва покрывающей пленки. Однако такой продукт соосаждения подвержен нежелательному изменению свойств, так как он легко абсорбирует влагу из-за присутствия растворимого в воде наполнителя. Кроме того, с продуктом соосаждения, который имеет высокую адгезивность и плохую текучесть, трудно работать при проведении распылительной сушки, и, следовательно, выход получаемого описанным способом продукта соосаждения является низким, например приблизительно 70%.
Обычно молекула воды, абсорбированная лекарством, может существовать в трех формах: вода, слабо абсорбированная на поверхности лекарства, которая легко испаряется; вода, связанная с лекарством более прочно, чем поверхностная вода, что приводит к изменению физико-химических свойств, например температуры плавления лекарства; и кристаллическая вода, входящая в структуру кристаллической решетки лекарства.
Проведенный термический анализ позволил установить, что продукт соосаждения в соответствии с международной публикацией РСТ WO 99/08683 показывает смещение температурного пика поглощения при влажных условиях, и этот смещенный пик возвращается в исходное положение в сухих условиях. Соответственно, можно сделать вывод, что вода, абсорбированная на продукте соосаждения, является связанной водой, которая вызывает изменение физико-химических свойств лекарства. Кроме того, несмотря на использование растворимого в воде наполнителя растворение цефуроксим-аксетила из продукта соосаждения существенно не улучшается и, следовательно, биодоступность цефуроксим-аксетила, содержащегося в продукте соосаждения, является относительно низкой.
В этой связи были предприняты попытки для решения проблем, связанных с существованием по существу аморфной формы цефуроксим-аксетила с низкой температурой плавления, которые увенчались успехом в разработке улучшенной композиции некристаллического цефуроксим-аксетила, которая обладает высокой стабильностью и биодоступностью.
Сущность изобретения
Таким образом, задачей настоящего изобретения является обеспечение твердого диспергирующего агента некристаллического цефуроксим-аксетила, имеющего улучшенную биодоступность и стабильность.
Другая задача настоящего изобретения состоит в обеспечении способа получения указанного диспергирующего агента.
Еще одной задачей настоящего изобретения является обеспечение композиции для перорального введения указанного диспергирующего агента.
В соответствии с одним из аспектов настоящего изобретения разработан твердый диспергирующий агент некристаллического цефуроксим-аксетила, содержащий цефуроксим-аксетил, поверхностно-активное вещество и нерастворимый в воде неорганический носитель.
Краткое описание чертежа
Описанные выше объекты и признаки настоящего изобретения станут понятны из последующего описания предпочтительных вариантов осуществления изобретения, рассматриваемых вместе с чертежом, где представлены данные дифференциальной сканирующей калориметрии (ДСК) твердого диспергирующего агента некристаллического цефуроксим-аксетила настоящего изобретения.
Подробное описание изобретения
Твердый диспергирующий агент некристаллического цефуроксим-аксетила настоящего изобретения содержит в качестве активного ингредиента цефуроксим-аксетил, поверхностно-активное вещество и нерастворимый в воде неорганический носитель.
Цефуроксим-аксетил, который может быть использован при получении заявляемого диспергирующего агента, представляет собой любую форму цефуроксим-аксетила, например кристаллическую форму, низкоплавкую по существу аморфную форму и высокоплавкую по существу аморфную форму, из которых предпочтительной является кристаллическая форма цефуроксим-аксетила.
Поверхностно-активное вещество, используемое в настоящем изобретении, играет ключевую роль при образовании некристаллического твердого диспергирующего агента цефуроксим-аксетила. Типичными примерами поверхностно-активного вещества являются:
(1) полиоксиэтиленсорбитановые эфиры жирной кислоты, где жирная кислота представляет собой моно- или три-лауриновую, пальмитиновую, стеариновую или олеиновую кислоту (Tween®, ICI);
(2) полиоксиэтилированные гликолированные натуральные или гидрированные растительные масла, такие как полиоксиэтилированное гликолированное натуральное или гидрированное касторовое масло (Cremophor®, BASF);
(3) полиоксиэтилированные эфиры жирной кислоты, такие как полиоксиэтилированный эфир стеариновой кислоты (Myrj, ICI);
(4) полиоксиэтилен-полиоксипропиленовый блок-сополимер (Poloxamer®, BASF);
(5) диоктилсульфосукцинат натрия или лаурилсульфат натрия;
(6) фосфолипиды;
(7) сложные эфиры пропиленгликоля и моно- или ди-жирной кислоты, такие как дикаприлат пропиленгликоля, дилаурат пропиленгликоля, изостеарат пропиленгликоля, лаурат пропиленгликоля, рицинолеат пропиленгликоля, пропиленгликолевый диэфир каприловой-каприновой кислоты (Miglyol® 840, Huls);
(8) продукты перекрестной этерификации триглицеридов натурального растительного масла и полиалкиленполиолов (Labrafil®M, Gattefosse);
(9) моно-, ди- или моно/ди-глицериды, такие как моно- и ди-глицериды каприловой/каприновой кислоты (Imwitor®, Gattefosse);
(10) сорбитановые эфиры жирных кислот, такие как сорбитанмонолаурат, сорбитанмонопальмитат и сорбитанмоностеарат (Span®, ICI).
Из поверхностно-активных веществ, описанных выше, предпочтительными являются полиоксиэтиленсорбитановые эфиры жирных кислот, полиоксиэтилен-полиоксипропиленовый блок-сополимер и их смеси, и наиболее предпочтительными являются сложные эфиры полиоксиэтиленсорбитана и жирной кислоты.
Нерастворимый в воде неорганический носитель, используемый в настоящем изобретении, уменьшает адгезивные свойства диспергирующего агента цефуроксим-аксетила, повышая за счет этого его выход при проведении распылительной сушки, и также предупреждает желатинизацию цефуроксим-аксетила, когда последний вступает в контакт с водной средой. Типичными примерами нерастворимого в воде неорганического носителя являются диоксид кремния, гидротальцит (hydrotalcite), алюмосиликат магния, гидроксид алюминия, диоксид титана, тальк, алюмосиликат, алюмометасиликат магния, бентонит и их смесь, из которых предпочтительным является диоксид кремния.
Твердый диспергирующий агент настоящего изобретения содержит от 1 до 50 мас. частей, предпочтительно от 2 до 30 мас. частей поверхностно-активного вещества; и от 1 до 200 мас. частей, предпочтительно от 3 до 50 мас. частей нерастворимого в воде неорганического носителя, из расчета на 100 мас. частей цефуроксим-аксетила.
Помимо некристаллического цефуроксим-аксетила, поверхностно-активного вещества и нерастворимого в воде неорганического носителя твердый диспергирующий агент настоящего изобретения может дополнительно содержать нерастворимую в воде добавку. Типичными примерами нерастворимой в воде добавки являются микрокристаллическая целлюлоза, поперечно-сшитый повидон (поперечно-сшитый поливинилпирролидон), поперечно-сшитая натрий-карбоксиметилцеллюлоза, а также их смеси, из которых предпочтительной является поперечно-сшитая натрий-карбоксиметилцеллюлоза. Нерастворимая в воде добавка может быть использована в количестве 100 мас. частей или менее, предпочтительно 50 мас. частей или менее, из расчета на 100 мас. частей цефуроксим-аксетила.
Твердый диспергирующий агент настоящего изобретения обладает повышенной растворимостью в воде и высокой биодоступностью цефуроксим-аксетила. Кроме того, цефуроксим-аксетил в твердом диспергирующем агенте настоящего изобретения является термодинамически стабильным даже при влажных условиях и устойчив к желатинизации при контакте с водной средой, благодаря его взаимодействию с нерастворимым в воде неорганическим носителем.
Твердый диспергирующий агент настоящего изобретения может быть получен путем (а) растворения цефуроксим-аксетила и поверхностно-активного вещества в подходящем органическом растворителе, например в спирте, таком как метанол или этанол, в ацетонитриле, тетрагидрофуране, дихлорметане, хлороформе и их смеси; (б) суспендирования нерастворимого в воде неорганического носителя в полученном растворе и (в) сушки полученной суспензии для удаления органического растворителя в соответствии с обычным способом, например распылительной сушкой, сушкой вымораживанием и упариванием при пониженном давлении. Нерастворимая в воде добавка может быть также суспендирована в растворе, полученном на стадии (а) перед сушкой.
Заявляемый способ дает твердый диспергирующий агент изобретения с высоким выходом 90% и более, благодаря пониженной адгезивности и хорошей текучести диспергирующего агента.
Твердый диспергирующий агент настоящего изобретения может быть введен перорально. Следовательно, фармацевтическая композиция настоящего изобретения содержит твердый диспергирующий агент некристаллического цефуроксим-аксетила в сочетании с фармацевтически приемлемым носителем. Фармацевтическая композиция может быть приготовлена в виде различных фармацевтических препаратов для перорального применения, например, в форме порошка, гранулы, таблетки и препарата с покрытием, в соответствии с любой из обычных методик. Например, твердая капсула может быть приготовлена путем добавления фармацевтических добавок к заявляемому твердому диспергирующему агенту цефуроксим-аксетила, переработки смеси в порошок или гранулы и заполнения порошком или гранулами твердой желатиновой капсулы; таблетка может быть получена путем добавления подходящей добавки к твердому диспергирующему агенту цефуроксим-аксетила и таблетирования смеси; препараты с покрытием могут быть получены путем нанесения покрытия на таблетку заявляемого диспергирующего агента с помощью пленочной композиции в соответствии с обычными способами нанесения покрытия. Терапевтически эффективное количество цефуроксим-аксетила может находиться в интервале от 250 до 1000 мг на 1 кг веса тела, как это хорошо известно в данной области техники.
Следующие примеры предназначены для дополнительной иллюстрации настоящего изобретения и не ограничивают его объем.
Кроме того, проценты, приведенные ниже, для твердых компонентов в смеси твердых компонентов, жидкости в жидкости и твердого вещества в жидкости приведены из расчета на мас./мас., об./об. и мас./об., если не оговорено особо.
Пример 1: Получение твердого диспергирующего агента
Растворяли в ацетоне 100 мас. частей кристаллического цефуроксим-аксетила и 16,63 мас. частей Tween 80® (ICI), и в растворе диспергировали 16,63 мас. частей диоксида кремния (площадь поверхности: 200±25 м2/г, размер частиц 30 мкм или менее). Затем диспергирующий агент подвергали распылительной сушке с использованием распылительной сушилки (Minispray dryer В-191, Büchi, Switzerland) при температуре на входе 45oС и температуре на выходе 37oС для получения твердого диспергирующего агента. Твердый диспергирующий агент дополнительно сушили при температуре от 30 до 40oС в течение приблизительно 3 ч для удаления оставшегося растворителя.
Пример 2: Получение твердого диспергирующего агента
Повторяли методику примера 1 за исключением того, что использовали 3,33 мас. частей 80® и 9,98 мас. частей диоксида кремния. Получали высушенный твердый диспергирующий агент.
Пример 3: Получение твердого диспергирующего агента
Повторяли методику примера 1 за исключением того, что использовали 4,99 мас. частей 80® и 13,30 мас. частей диоксида кремния. Получали высушенный твердый диспергирующий агент.
Пример 4: Получение твердого диспергирующего агента
В ацетоне растворяли 100 мас. частей кристаллического цефуроксим-аксетила и 6,65 мас. частей 80® (ICI), и в растворе диспергировали 9,98 мас. частей поперечно-сшитой натрий-карбоксиметилцеллюлозы и 26,60 мас. частей диоксида кремния. Затем диспергирующий агент подвергали распылительной сушке с использованием распылительной сушилки (Minispray dryer B-191, Büchi, Switzerland) при температуре на входе 45oС и температуре на выходе 37oС, для получения твердого диспергирующего агента. Твердый диспергирующий агент дополнительно сушили при температуре от 30 до 40oС в течение приблизительно 3 ч для удаления остающегося растворителя.
Пример 5: Получение твердого диспергирующего агента
Повторяли методику примера 4 за исключением того, что использовали 16,65 мас. частей Poloxamer® (BASF) вместо Tween 80®. Получали высушенный диспергирующий агент.
Сравнительный пример 1: Получение продукта соосаждения
Растворяли в ацетоне 100 мас. частей кристаллического цефуроксим-аксетила и 9,98 мас. частей повидона, и раствор подвергали распылительной сушке с использованием распылительной сушилки (Minispray dryer B-191, Büchi, Switzerland) при температуре на входе 45oС и температуре на выходе 37oС, для получения продукта соосаждения. Продукт соосаждения сушили затем при температуре от 30 до 40oС в течение приблизительно 3 ч для удаления оставшегося растворителя.
Сравнительный пример 2: Получение по существу аморфного цефуроксим-аксетила
Кристаллический цефуроксим-аксетил растворяли в ацетоне до концентрации 10% (мас./об.), и полученный раствор подвергали распылительной сушке, получая низкоплавкий по существу аморфный цефуроксим-аксетил.
Пример испытания 1: Исследование термодинамической стабильности
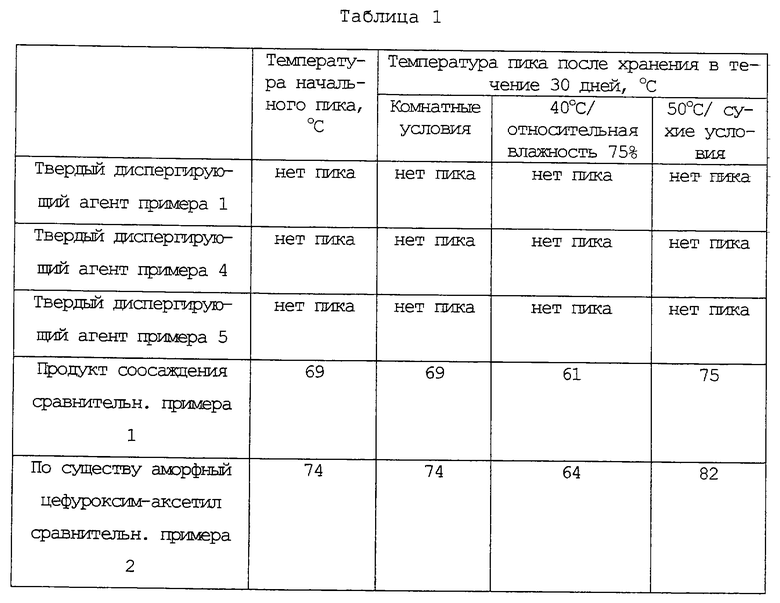
Приготовленные в примерах 1, 4 и 5 твердые диспергирующие агенты, продукт соосаждения, полученный в сравнительном примере 1, и низкоплавкий по существу аморфный цефуроксим-аксетил, полученный в сравнительном примере 2, хранили в течение 30 дней при трех условиях хранения: при комнатных условиях, при 40oС и относительной влажности 45%, и в сухих условиях при 50oС, при этом оценивали пики поглощения теплоты с использованием термоаналитического прибора для дифференциальной сканирующей калориметрии (ДСК, Rheometric Scientific DSC Plus, Англия).
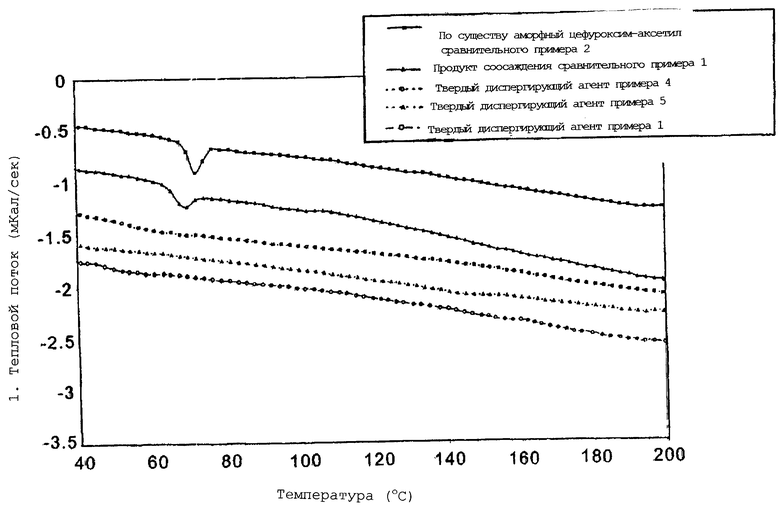
На чертеже приведены данные ДСК указанных выше композиций, записанные на 30 день, а в таблице 1 (см. в конце описания) приведены температуры плавления (температура пика поглощения) до и после хранения в течение 30 дней.
Как видно из чертежа и таблицы 1, твердые диспергирующие агенты настоящего изобретения не имеют пика поглощения при всех условиях хранения, что говорит о том, что диспергирующие агенты настоящего изобретения содержат устойчивый некристаллический цефуроксим-аксетил. Напротив, продукт соосаждения, полученный в сравнительном примере 1, и низкоплавкий по существу аморфный цефуроксим-аксетил, приготовленный в сравнительном примере 2, дают отчетливые максимумы поглощения, которые сдвигаются в сторону высоких температур при хранении при 50oС и в сторону более низких температур при хранении при 40oС и высокой влажности. Это наблюдение подтверждает тот факт, что и продукт соосаждения и низкоплавкий по существу аморфный цефуроксим-аксетил становятся более кристаллическими при 50oС, в то время как их физико-химические свойства изменяются при поглощении воды в условиях высокой влажности.
Пример 6: Получение таблетки с пленочным покрытием
Ингредиенты - Количество (мг/таблетка)
Твердый диспергирующий агент
Твердый диспергирующий агент, полученный в примере 1 - 400,72 (250 мг - цефуроксима)
Фармацевтические наполнители
Микрокристаллическая целлюлоза - 50
Поперечно-сшитый повидон - 110
Стеарат магния - 5
Ингредиенты покрывающей пленки*
Гидроксипропилметилцеллюлоза 2910 (15 сПз) - 8
Гидроксипропилцеллюлоза (10 сПз) - 1,34
Этилцеллюлоза (10 сПз) - 1,34
Концентрированный глицерин - 0,69
Тальк - 0,07
Диоксид титана - 0,42
* Для получения покрывающего раствора суспендировали в смеси 260 мг метиленхлорида и 108 мг этанола
Если описывать более конкретно, то каждую одну половину предписанных количеств микрокристаллической целлюлозы и поперечно-сшитого повидона добавляли к твердому диспергирующему агенту, полученному в примере 1, и приготовленную смесь прессовали. Добавляют стеарат магния и оставшиеся количества наполнителей. Полученную смесь повторно прессовали в таблетки с помощью таблетирующей машины. Затем по обычной методике на поверхность таблетки наносили предписанное пленочное покрытие с использованием покрывающего раствора.
Пример 7: Получение таблетки
Ингредиенты - Количество (мг/таблетка)
Твердый диспергирующий агент
Твердый диспергирующий агент, полученный в примере 2 - 340,72 (250 мг цефуроксима)
Фармацевтические наполнители
Микрокристаллическая целлюлоза - 50
Поперечно-сшитый повидон - 150
Стеарат магния - 5
Повторяли методику примера 6 с использованием приведенных выше ингредиентов, получали таблетки.
Пример 8. Получение твердой капсулы
Ингредиенты - Количество (мг/таблетка)
Твердый диспергирующий агент
Твердый диспергирующий агент, полученный в примере 3 - 355,72 (250 мг цефуроксима)
Фармацевтические наполнители
Микрокристаллическая целлюлоза - 20
Поперечно-сшитый повидон - 50
Стеарат магния - 5
Фармацевтические наполнители добавляли к полученному в примере 3 твердому диспергирующему агенту и полученной смесью заполняли твердые капсулы.
Пример 9: Получение таблетки с пленочным покрытием
Ингредиенты - Количество (мг/таблетка)
Твердый диспергирующий агент
Твердый диспергирующий агент, полученный в примере 4 - 430,72 (250 мг цефуроксима)
Фармацевтические наполнители
Поперечно-сшитая натрий-карбоксиметилцеллюлоза - 40
Микрокристаллическая целлюлоза - 50
Поперечно-сшитый повидон - 50
Стеарат магния - 5
Ингредиенты покрывающей пленки*
Гидроксипропилметилцеллюлоза 2910 (15 сПз) - 8
Гидроксипропилцеллюлоза (10 сПз) - 1,34
Этилцеллюлоза (10 сПз) - 1,34
Концентрированный глицерин - 0,69
Тальк - 0,07
Диоксид титана - 0,42
* Для получения покрывающего раствора суспендировали в смеси 260 мг метиленхлорида и 108 мг этанола
Повторяли методику примера 6 с использованием приведенных выше ингредиентов, получали таблетки с пленочным покрытием.
Пример 10: Получение таблетки с пленочным покрытием
Ингредиенты - Количество (мг/таблетка)
Твердый диспергирующий агент
Твердый диспергирующий агент, полученный в примере 5 - 460,72 (250 мг цефуроксима)
Фармацевтические наполнители
Поперечно-сшитая натрий-карбоксиметилцеллюлоза - 40
Микрокристаллическая целлюлоза - 50
Поперечно-сшитый повидон - 50
Стеарат магния - 5
Ингредиенты покрывающей пленки*
Гидроксипропилметилцеллюлоза 2910 (15 сПз) - 8
Гидроксипропилцеллюлоза (10 сПз) - 1,34
Этилцеллюлоза (10 сПз) - 1,34
Концентрированный глицерин - 0,69
Тальк - 0,07
Диоксид титана - 0,42
* Для получения покрывающего раствора суспендировали в смеси 260 мг метиленхлорида и 108 мг этанола
Повторяли методику примера 6 с использованием приведенных выше ингредиентов, получали таблетки с пленочным покрытием.
Сравнительный пример 3
Ингредиенты - Количество (мг/таблетка)
Продукты соосаждения
Продукт соосаждения, полученный в сравнительном примере 1 - 330,72 (250 мг цефуроксима)
Фармацевтические наполнители
Поперечно-сшитая натрий-карбоксиметилцеллюлоза - 40
Микрокристаллическая целлюлоза - 50
Поперечно-сшитый повидон - 50
Стеарат магния - 5
Ингредиенты покрывающей пленки*
Гидроксипропилметилцеллюлоза 2910 (15 сПз) - 8
Гидроксипропилцеллюлоза (10 сПз) - 1,34
Этилцеллюлоза (10 сПз) - 1,34
Концентрированный глицерин - 0,69
Тальк - 0,07
Диоксид титана - 0,42
* Для получения покрывающего раствора суспендировали в смеси 260 мг метиленхлорида и 108 мг этанола
Повторяли методику примера 6 с использованием приведенных выше ингредиентов, получали таблетки с пленочным покрытием.
Пример испытания 2: Изучение растворимости
Определяли скорости растворения цефуроксим-аксетила в случае таблеток с пленочным покрытием, полученных в примерах 6, 9 и 10 и в сравнительном примере 3, а также в случае таблетки Zinnat® (Glaxo Group Limited, Англия) в качестве контроля, в соответствии с методикой изучения растворимости, описанной в разделе для цефуроксим-аксетила Фармакопеи Соединенных Штатов при приведенных ниже условиях:
Прибор для испытания: Erweka DT80 (Erweka, Германия).
Раствор для проведения испытания: 900 мл 0,07 н. НС1.
Температура раствора для проведения испытания: 37±0,5oС.
Скорость вращения: 55±4 об/мин.
Аналитический метод: жидкостная хроматография
- колонка: Cosmosil C18 (150 мм • 4,6 мм; Nacalai Tecque, Япония),
- подвижная фаза: 0,2 М монофосфат аммония : метанол = 620:380,
- вводимый объем: 10 мкл,
- скорость потока: 1,2 мл/мин,
- детектор: УФ, 278 нм.
Определяли соотношение изомеров цефуроксим-аксетила (R и S), высвобождающихся из каждой таблетки с пленочным покрытием, а также определяли время разрыва покрывающей пленки.
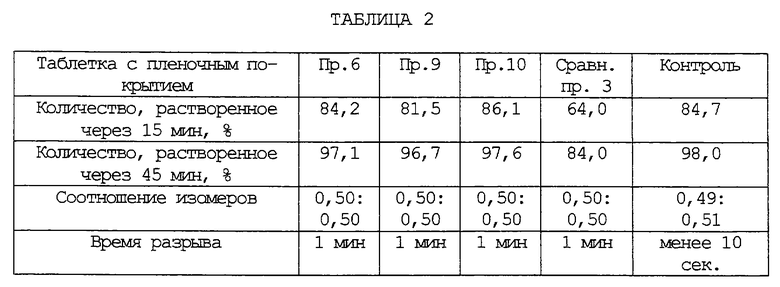
Результаты приведены в таблице 2 (см. в конце описания).
Как видно из таблицы 2, таблетки с пленочным покрытием композиции настоящего изобретения, содержащие некристаллический цефуроксим-аксетил, имеют скорость растворения, сравнимую со скоростью растворения контрольной таблетки Zinnat®, несмотря на значительно улучшенное время разрыва 1 мин и более. Рецептура сравнения, содержащая продукт соосаждения цефуроксим-аксетила с повидоном, наоборот, имеет низкую скорость растворения. Таким образом, композиция настоящего изобретения, имеющая высокую скорость растворения, характеризуется отличной биодоступностью цефуроксим-аксетила, которая не ограничивается временем разрушения покрывающей пленки.
Изобретение относится к фармации и касается твердого диспергирующего агента некристаллического цефуроксим-аксетила, который получают путем а) растворения цефуроксим-аксетила и поверхностно-активного вещества в органическом растворителе; (б) суспендирования нерастворимого в воде неорганического носителя в полученном растворе и (в) сушки полученной суспензии для удаления органического растворителя, причем указанный твердый диспергирующий агент обладает улучшенной биодоступностью и стабильностью цефуроксим-аксетила и может быть полезен при получении фармацевтической композиции для перорального применения. 3 с. и 7 з.п. ф-лы, 2 табл., 1 ил.
| Способ получения суспоэмульсии примицина | 1989 |
|
SU1837870A3 |
| БЕНЗИЛБЕНЗОАТ В ВОДНО-ЭМУЛЬСИОННОЙ ФОРМЕ | 1997 |
|
RU2098081C1 |
| СОДЕРЖАЩАЯ ГИДРАТИРОВАННЫЙ ЦЕФТИБУТЕН ПОРОШКОВАЯ АНТИБАКТЕРИАЛЬНАЯ КОМПОЗИЦИЯ, ПРЕДНАЗНАЧЕННАЯ ДЛЯ ОРАЛЬНОГО ИСПОЛЬЗОВАНИЯ В ВИДЕ СУСПЕНЗИИ | 1993 |
|
RU2123863C1 |
| US 5013833, 07.05.1991. | |||
Авторы
Даты
2003-11-10—Публикация
2000-07-25—Подача