Настоящее изобретение относится к новой группе производных 3-тетрагидропиридин-4-илиндола формулы (I)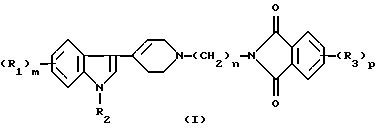
где R1 представляет галоген, СF3, алкил(1-3С), алкокси(1-3С), CN или SСН3,
m равно величине 0, 1 или 2,
R2 представляет Н или алкил (1-3С),
n равно величине 3, 4, 5 или 6,
R3 представляет галоген, алкил(1-4С) или алкокси(1-4С),
р имеет величину 0, 1 или 2,
и их солям.
Было обнаружено, что соединения, имеющие формулу (I), проявляют высокое сродство к D2-рецептору допамина и являются хорошими ингибиторами повторного поглощения серотонина (SRI).
Предпочтительными соединениями изобретения являются соединения, имеющие формулу (I), где R1 представляет водород (т.е. m=0) или F, Сl, СН3 или CN и m= 1, R2 представляет Н или СН3, n=4, R3 представляет водород (т.е. р=0) или F, или алкил(1-4С), р= 1, и их соли. Особенно предпочтительно соединение, имеющее формулу (I), где (R1)m представляет F, R2 представляет водород, n=4 и р=0, и его соли.
Было обнаружено, что соединения по данному изобретению проявляют высокое сродство как к D2-рецептору допамина, так и к сайту повторного поглощения серотонина. Это сочетание полезно для лечения шизофрении и других психотических нарушений и может предоставить возможность для полного лечения всех симптомов заболеваний (как положительных симптомов, так и отрицательных симптомов).
Данные соединения проявляют активность в качестве антагонистов D2-рецепторов допамина, так как они потенциально создают антагонизм апоморфин-индуцированному поведению мышей, проявляющемуся в карабкании. Данные соединения проявляют также активность в качестве ингибиторов повторного поглощения серотонина, поскольку они делают возможным 5-НТР-индуцированное поведение у мышей.
Данные соединения активны в терапевтических моделях, восприимчивых к клинически уместным антипсихотикам (например, условному рефлексу избегания; Van der Heyden and Bradford, Behav. Brain Res., 1988, 31:61-67) и антидепрессантам или анксиолитикам (например, угнетению индуцированных стрессом органов, образующих звук; Van der Poel et al., Psychopharmacology, 1989, 97: 147-148).
В противоположность клинически уместным антагонистам D2-рецептора допамина описанные соединения имеют низкую предрасположенность к индуцированию каталепсии у грызунов и как таковые, вероятно, индуцируют более слабое экстрапирамидальное побочное действие, чем существующие антипсихотические агенты.
Ингибирующая активность в отношении повторного поглощения серотонина, присущая данным соединениям, может быть ответственна за терапевтические действия, наблюдаемые в поведенческих моделях, восприимчивых либо к антидепрессантам, либо к анксиолитикам.
Данные соединения можно использовать для лечения поражений или заболеваний центральной нервной системы, вызванных расстройством либо в допаминергической, либо серотонергических системах, например агрессии, нарушений типа тревожных состояний, аутизма, головокружения, депрессии, нарушения познавательной способности или памяти и, особенно, шизофрении и других психотических нарушений.
Фармакологически приемлемыми кислотами, с которыми соединения данного изобретения могут образовывать кислотно-аддитивные соли, являются, например, хлористовородная кислота, серная кислота, фосфорная кислота, азотная кислота и органические кислоты, такие как лимонная кислота, фумаровая кислота, малеиновая кислота, винная кислота, уксусная кислота, бензойная кислота, п-толуолсульфоновая кислота, метансульфоновая кислота и нафталинсульфоновая кислота.
Данные соединения и их кислотно-аддитивные соли можно превращать в формы, приемлемые для введения, при помощи подходящих способов с использованием вспомогательных веществ, таких как жидкие и твердые материалы-носители.
Соединения, имеющие формулу (I), можно получить следующим образом:
а) взаимодействием соединения формулы (II)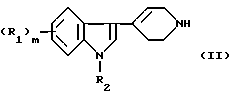
с соединением формулы (III)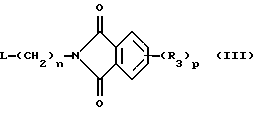
где символы имеют вышеуказанные значения и L представляет так называемую уходящую группу, например бром.
Данное взаимодействие проводят в растворителе, таком как ацетонитрил, в присутствии триэтиламина или K2СО3 и KI при температуре флегмы (кипячение с обратным холодильником). Или
b) (i) восстановлением цианогруппы в соединении формулы (IV)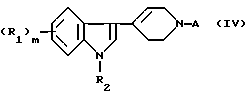
где А представляет группу -(CH2)n-1-CN, в соответствующую группу -(СН2)n-NH2 и
(ii) взаимодействием полученного амина с необязательно замещенным фталевым ангидридом формулы (V)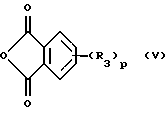
причем в данной формуле символы имеют значения, приведенные выше.
Реакцию стадии b (i) можно проводить, например, с LiAlH4 в органическом растворителе, таком как тетрагидрофуран, при температуре флегмы.
Реакцию стадии (ii) можно проводить, например, в органическом растворителе, таком как тетрагидрофуран и толуол, при температуре флегмы.
Используемые в способе а) исходные соединения формулы II можно получить способом, известным per se, взаимодействием необязательно замещенного производного индола с 4-пиперидоном.
Исходные соединения, используемые в способе b) и имеющие формулу (IV), можно получить взаимодействием соединения, имеющего формулу (II), с бромалкилнитрилом формулы Br-(CH2)n-1-CN способом, известным per se.
Получение соединений, имеющих формулу (I), теперь будет описано более подробно в следующих примерах.
Пример 1.
Получение 1-метил-3-(1,2,3,6-тетрагидропиридин-4-ил)индола.
К раствору 4-пиперидон•Н2О•НСl (50 г, 0,32 моль) в 100 мл уксусной кислоты и 150 мл трифторуксусной кислоты добавляют по каплям раствор 1-метилиндола (11,5 мл, 0,09 моль) в 100 мл уксусной кислоты при комнатной температуре. После перемешивания в течение 1 часа реакционную смесь концентрируют (в вакууме, температура приблизительно 30oС), добавляют воду, смесь делают основной карбонатом калия и экстрагируют этилацетатом. Органический слой отделяют, сушат и очищают хроматографией на колонке с силикагелем (дихлорметан/метанол/гидроксид аммония = 84/15/1) с получением 9 г (47%) указанного в заголовке соединения.
Пример 2.
Получение 5-фтор-3-(1,2,3,6-тетрагидропиридин-4-ил)индола.
К раствору натрия (60 г, 2,6 моль) в 1000 мл метанола добавляют 5-фториндол (49 г, 0,36 моль) и 4-пиперидон•Н2O•НСl (170 г, 1,11 моль). Смесь нагревают при кипячении с обратным холодильником в течение 18 часов, затем концентрируют, добавляют воду и экстрагируют этилацетатом. Объединенный органический слой сушат над сульфатом натрия и затем концентрируют. Получаемое твердое вещество растворяют в метаноле (приблизительно 200 мл) и затем разбавляют водой (приблизительно 1000-1500 мл). Осадок собирают, промывают водой и петролейным эфиром и затем сушат в вакуумном сушильном шкафу при 60oС. Выход 74 г (95%) желтого твердого вещества.
Пример 3.
Получение N-[4-[4-[(5-фтор-1Н-индол-3-ил)-1,2,3,6-тетрагидропиридин-1-ил]бутил]фталимид•НСl (cоединение 1).
Раствор 5-фтор-3-(1,2,3,6-тетрагидропиридин-4-ил)индола (7,5 г, 34,7 ммоль), N-(4-бромбутил)фталимида (10,8 г, 38,3 ммоль), триэтиламина (4,5 мл) и иодид калия (5,5 г) в 150 мл ацетонитрила нагревают при кипячении с обратным холодильником в течение 18 часов. Реакционную смесь концентрируют и очищают хроматографией на колонке с силикагелем (дихлорметан/метанол/гидроксид аммония = 92/7,5/0,5) с получением 8,3 г указанного в заголовке соединения в виде свободного основания, т.пл. 186oС. Гидрохлорид получают растворением вышеуказанного свободного основания в 20 мл 1М НСl в этаноле. Раствор концентрируют и получаемое твердое вещество промывают простым эфиром. Выход 8,4 г (54%) соединения 1, т.пл. 224oС (разложение).
Пример 4.
Получение 5-фтор-3-[1-(3-цианопропил)-1,2,3,6-тетрагидропиридин-4-ил] индола.
Раствор 5-фтор-3-(1,2,3,6-тетрагидропиридин-4-ил)индола (10 г, 46 ммоль), 4-бромбутиронитрила (5,6 мл, 56 ммоль), карбоната калия (6,3 г) и иодида калия (7,6 г) в 100 мл ацетонитрила нагревают при кипячении с обратным холодильником в течение 18 часов. Смесь фильтруют и остаток на фильтре промывают смесью дихлорметан/метанол/гидроксид аммония = 84/15/1. Органический слой концентрируют с получением 10,9 г (83%) указанного в заголовке соединения, т.пл. 152oС.
Пример 5.
Получение 5-фтор-3-[1-(4-аминобутил)-1,2,3,6-тетрагидропиридин-4-ил]индола.
К раствору 5-фтор-3-[1-(3-цианопропил)-1,2,3,6-тетрагидропиридин-4-ил] индола (10 г, 35 ммоль) в 300 мл сухого ТГФ медленно добавляют LiAlH4 (2,0 г). Смесь перемешивают и нагревают при кипячении с обратным холодильником в течение 2 часов. Затем реакционную смесь охлаждают и медленно добавляют воду (1,9 мл) в ТГФ (10 мл), затем 2 н. гидроксид натрия (1,9 мл). Указанную смесь нагревают при кипячении с обратным холодильником в течение 0,25 часов, фильтруют через Хайфло (hyflo) и концентрируют с получением 8,76 г (88%) указанного в заголовке соединения.
Пример 6.
Получение N-[4-[4-(5-фтор-1Н-индол-3-ил)-1,2,3,6-тетрагидропиридин-1-ил] бутил]-4-фторфталимида (соединение 19).
К раствору 5-фтор-3-[1-(4-аминобутил)-1,2,3,6-тетрагидропиридин-4-ил] индола (1,46 г, 5 ммоль) в 20 мл ТГФ добавляют 4-фторфталевый ангидрид и 50 мл толуола. ТГФ удаляют перегонкой и получаемую смесь нагревают при кипячении с обратным холодильником в течение 18 часов с азеотропным удалением воды (устройство Дина и Старка). Реакционную смесь концентрируют и очищают хроматографией на колонке с силикагелем (дихлорметан/метанол/гидроксид аммония = 92/7,5/0,5) с получением 1,52 г (69%) указанного в заголовке соединения 19, т.пл. 197-199oС.
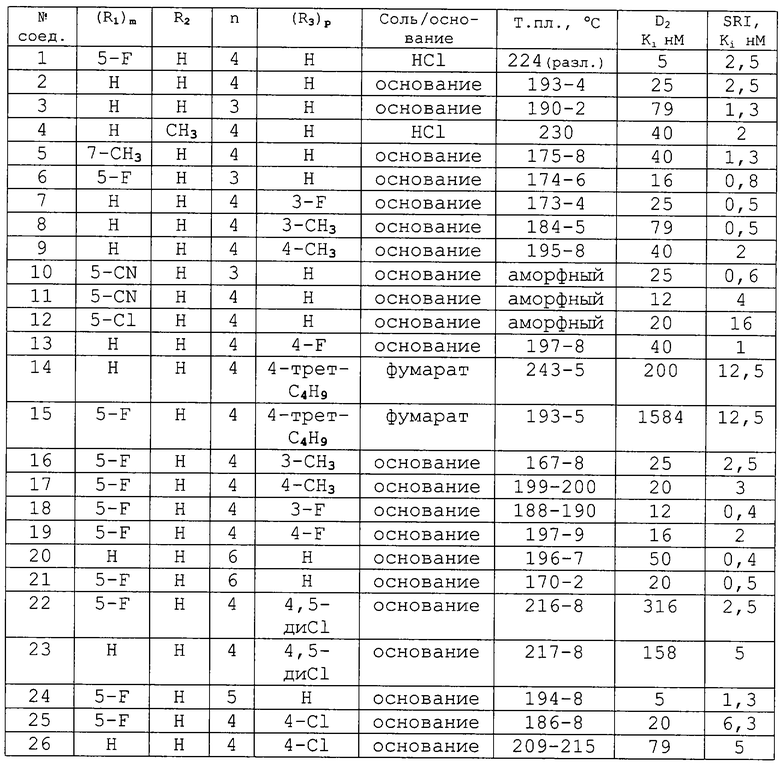
В соответствии со способом а), как показано в примерах 1-3, или способом b), как показано в примерах 4-6, были получены соединения, перечисленные в следующей таблице.
| название | год | авторы | номер документа |
|---|---|---|---|
| АЛКИЛ-ПИПЕРАЗИНИЛ БЕНЗОКСАЗОЛОНОВЫЕ И АЛКИЛ-ПИПЕРИДИНИЛ БЕНЗОКСАЗОЛОНОВЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ | 1999 |
|
RU2225406C2 |
| НОВЫЕ ФЕНИЛПИПЕРАЗИНЫ | 2000 |
|
RU2246494C2 |
| ПРОИЗВОДНЫЕ СУЛЬФОНАМИДА, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2002 |
|
RU2293082C2 |
| НОВЫЕ ПИПЕРИДИНЗАМЕЩЕННЫЕ ИНДОЛЫ ИЛИ ИХ ГЕТЕРОПРОИЗВОДНЫЕ | 2004 |
|
RU2382037C2 |
| ПРОИЗВОДНЫЕ ОКСИМА ПИПЕРАЗИНА, ОБЛАДАЮЩИЕ АНТАГОНИСТИЧЕСКОЙ АКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К РЕЦЕПТОРУ НЕЙРОКИНИНА-1 (НК-1). | 2002 |
|
RU2273639C2 |
| ПРОИЗВОДНЫЕ 4-АРИЛ-1-(ИНДАНМЕТИЛ ИЛИ ДИГИДРОБЕНЗОТИОФЕНМЕТИЛ)ПИПЕРИДИНА,- -ТЕТРАГИДРОПИРИДИНА ИЛИ ПИПЕРАЗИНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2142458C1 |
| ИНДОЛЫ, ПОЛЕЗНЫЕ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С АНДРОГЕНОВЫМИ РЕЦЕПТОРАМИ | 2003 |
|
RU2328484C2 |
| СОЕДИНЕНИЕ 4-ФЕНИЛПИПЕРАЗИНА, 4-ФЕНИЛПИПЕРИДИНА И 4-ФЕНИЛ-1,2,3,6- ТЕТРАГИДРОПИРИДИНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОЯВЛЯЮЩАЯ 5-HT И D АКТИВНОСТЬ | 1995 |
|
RU2140920C1 |
| ПРОИЗВОДНЫЕ ТЕТРАГИДРОПИРИМИДИН-2-ОНА И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2334741C2 |
| ПРОИЗВОДНЫЕ ПИРИМИДОБЕНЗИМИДАЗОЛА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АГОНИСТОВ ИЛИ АНТАГОНИСТОВ РЕЦЕПТОРОВ МЕЛАНОКОРТИНОВ | 2005 |
|
RU2392279C2 |
Изобретение относится к соединениям формулы (I)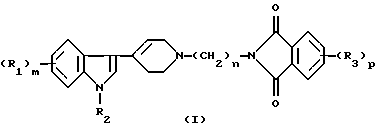
где R1 представляет собой водород, галоген, CF3, алкил(1-3С) или CN; m равно 0, 1 или 2; R2 представляет собой водород или алкил (1-3С); n равно 3, 4, 5 или 6; R3 представляет собой водород, галоген или алкил(1-4С); р равно 0, 1 или 2, или его фармакологически приемлемым кислотно-аддитивным солям. Соединения по п.1 получают путем взаимодействия соединения формулы (II)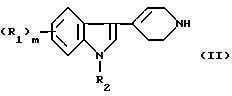
с соединением формулы (III)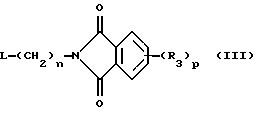
где L представляет собой удаляемую группу, такую как бром. Соединения по п.1 также могут быть получены путем восстановления соединения формулы (IV)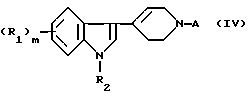
где А представляет собой группу -(CH2)n-1-CN, в соответствующее соединение, где А представляет собой группу -(CH2)n-NH2, и полученное аминопроизводное подвергают взаимодействию с производным фталевого ангидрида формулы (V)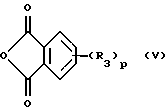
Технический результат - 3-тетрагидропиридин-4-илиндолы, проявляющие высокое сродство к D2-рецептору допамина и ингибирующие повторное поглощение серотонина (SRI). 3 с. и 2 з.п. ф-лы, 1 табл.
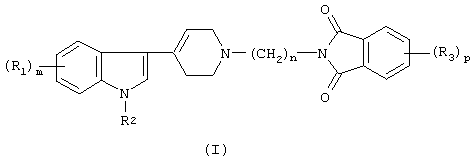
где R1 представляет собой водород, галоген, СF3, алкил(1-3С) или CN;
m равно 0, 1 или 2;
R2 представляет собой водород или алкил (1-3С);
n равно 3, 4, 5 или 6;
R3 представляет собой водород, галоген или алкил(1-4С);
р равно 0, 1 или 2,
или его фармакологически приемлемые кислотно-аддитивные соли.
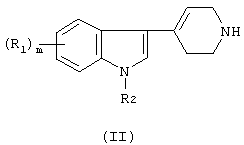
подвергают взаимодействию с соединением формулы (III)

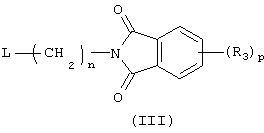
где L представляет собой удаляемую группу, такую, как бром.
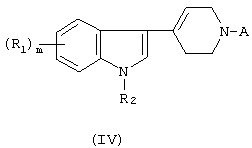
где А представляет собой группу -(СН2)n-1-CN,
восстанавливают в соответствующее соединение, где А представляет собой группу -(CH2)n-NH2, и (ii) полученное аминопроизводное подвергают взаимодействию с производным фталевого ангидрида формулы (V)
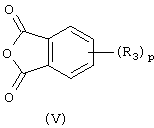
в указанных формулах R1, m, R2, n, R3 и р имеют значения, приведенные в п.1.
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| DE 4414113 Al, 26.10.1995 | |||
| Приработочное масло | 1978 |
|
SU722941A1 |
| Способ получения производных N-(4-индолилпиперидиноалкил)-бензимидазолона или их солей с кислотами | 1982 |
|
SU1088665A3 |
Авторы
Даты
2004-01-27—Публикация
1999-10-15—Подача