Изобретение относится к области медицины, биоорганической химии и генной инженерии, конкретно оно относится к композиции рекомбинантных белков, фармацевтического набора на ее основе для профилактики и лечения хронической палилломовирусной инфекции, приводящей к генитальному инвазийному раку, а также лечения неоплазий и инвазийного рака, ассоциированных с вирусами палилломы человека. Изобретение относится также к разработанному способу иммунотерапии и профилактической вакцинации и способу получения композиции рекомбинантных белков.
У около 500000 женщин в мире ставится диагноз цервикальный рак, который занимает второе место в мире как причина смерти от раковых заболеваний среди женщин. Несмотря на программы скрининга, принятые в США и выявляющие рак шейки матки на ранней стадии, число случаев инвазийного цервикального рака не уменьшается. За последние 15 лет эпидемиологические и вирусологические исследования однозначно подтверждают связь этой патологии с вирусами папилломы человека (ВПЧ) (Sexually transmitted diseases. "Vaccines, prevention and control", 2000, Edited by D.I.Bernstein, Academic Press). Установлена также взаимосвязь между неоплазиями и инвазийньм раком матки, наружных половых органов, ануса с вирусами папилломы человека (Lorine J. et all "Obstet Gynecol." 79:328-337, 1992).
Папилломавирус является вирусом с двойной замкнутой спиралью ДНК, состоящей из 7800-7900 пар оснований, с безоболочным вирионом и с 20-гранным икосаидральным капсидом из 72 капсомеров. Геном состоит из трех главных районов. Один кодирует поздние гены, другой - ранние; третий район - некодирующий. Он состоит из 400 пар оснований и содержит связывающие сайты для различных транскрипционных факторов, контролирующих экспрессию поздних и ранних генов. Район поздних генов имеет две рамки считывания и кодирует белок L1, являющийся основным калсидным белком ВПЧ, и белок L2, являющийся минорным капсидным белком. Район ранних генов включает шесть рамок считывания и кодирует соответственно белки Е1, Е2, Е3, Е4, Е5, Е6 и Е7. Белки Е6 и Е7 являются онкобелками и играют решающую роль в вирусной репликации, а также они необходимы для иммортализации и трансформации клеток. Белки Е1, Е2 и Е4 также играют важную роль в репликации. Белок Е4 необходим для созревания вируса. Роль белка Е5 пока до конца не выяснена.
Накопившиеся к настоящему времени данные свидетельствует о том, что капсидные белки ВПЧ способны индуцировать высокие титры специфических антител (гуморальный иммунитет) и являются перспективными кандидатами для создания профилактических вакцин (Lowy D.R., Schffler J.T. Papillomaviruses: Prophylactic vaccine prospects. Biochim. Biophys. Acta, 1999, 1423:M 1-8; Патент России №2173170, заявка РСТ 86/05816) либо диагностических наборов для определения вирусов папилломы (ЕР №№386734, 375555).
Однако при использовании данных белков для терапевтической иммунизации при устоявшейся, хронической папилломавирусной инфекции не удалось получить сколько-нибудь значительного эффекта. Для лечебной иммунизации необходима другая стратегия, а именно индукция антигенспецифического Т-клеточного иммунитета. Основное требование к терапевтическим вакцинам состоит в том, что они должны стимулировать клеточную составляющую специфического иммунитета и блокировать развитие неопластических процессов. Клеточная реакция должна быть направлена на клеточные и вирусные белки, участвующие в малигнации эпителия. Несмотря на интенсивные исследования, довольно мало известно о клеточных мишенях при опухолевой трансформации, поэтому большинство экспериментальных вакцин направлены на продукты генов Е6 и Е7 ВПЧ, роль которых в онкогенезе доказана однозначно.
Имеется большое количество рекомбинантных белков, которые могут быть использованы в качестве вакцинных препаратов и которые содержат наряду с белками Е6 или Е7 другие белки ВПЧ (Е1, Е2, Е4, L1, L2, и др.), (см. например, заявку РСТ 99/48518 и др.). Однако такие конструкции имеют слабые перспективы для лечения неоплазий и рака ввиду того, что раковая клетка в процессе химио- или иммунотерапии способна мутировать - терять многие менее важные для ее существования белки - мишени для иммунологической атаки. Включение таких белков в состав гибридных конструкций малоэффективно еще и потому, что подстегнуть в достаточной степени специфический клеточный иммунитет на Е6 и/или Е7 в силу недостаточной иммуногенности белков ВПЧ они не могут. Более перспективными конструкциями следует признать те, которые содержат в качестве антигенных детерминант только белки Е6 и/или Е7 ВПЧ и которые более близки к конструкциям гибридных белков предлагаемого изобретения.
Самой ранней такой работой является патент по заявке РСТ 92/10513, в которой описана конструкция на основе пептидной последовательности из иммуногенной части белка Е7 ВПЧ 16, связанной непосредственно или опосредованно с аминокислотной последовательностью, соответствующей В эпитопу Е7 ВПЧ 16 или ВПЧ 18. С помощью такой конструкции удалось преодолеть онкогенность белков Е7 и Е6 и вызвать стимуляцию гуморального иммунитета. Конструкция требует адъюванта.
В международной заявке №96/19496 описана конструкция гибридного белка на основе белка Е6 или Е7 ВПЧ (16, 18, 6, и 11 типов), которые вызывают гуморальный и/или клеточный иммунный ответ и не опасны для клеток реципиента, так как не способны вызывать их трансформацию. Для этого белки Е7 или Е6 ВПЧ 16 связывают ковалентно с белком или пептидным фрагментом, которые, например, облегчают очистку рекомбинантного белка (например 6His, GST фрагмент или глютадион-s-трансфераза), либо увеличивают его иммуногенность, для чего могут быть использованы дифтерийный или холерный токсин или их нетоксичные производные. (Однако описания таких слитых белков с дифтерийным или холерным токсином в материалах заявки нет). Конструкция, предусмотренная по этому изобретению, также нуждается в адъюванте.
В международной заявке 97/06821 впервые показана возможность использования белков теплового шока для возбуждения клеточной составляющей иммунитета. В примере 10 описана конструкция, представляющая собой комплекс, образованный in vitro из белка теплового шока и гибридного белка из Е7 ВПЧ и пептидного сайта, который и способен образовывать комплекс с белком теплового шока. Для индукции иммунного ответа конструкция нуждается в адъюванте.
Следует сделать отступление и отметить, что был сделан ряд сообщений о том, что химический коньюгат белков теплового шока микобактерий hsp65 или hsp70 (или hsp65 или hsp70 бактерий Escherichia coli) с частью малярийного антигена способны индуцировать образование специфических антител (гуморального иммунитета) в отсутствие какого-либо адъюванта. (Ваrrios at all Eur. J. Immunol. 22.1365-1372, 1994. Barrios et all Clin. Exp. Immunol. 98:224-228, 1994). В работе K.Suzue и R.Young ("The journal of immunology", "Adjuvant-free hsp70 fusion protein system elicits memoral and cellular immune responses to HIV1h24") показано, что коньюгат индуцирует в отсутствие какого-либо адъюванта в 10 раз более интенсивную клеточную и гуморальную составляющую иммунитета, чем антигенный белок р24 ВИЧ1 в свободном виде.
Этот подход использован в международной заявке 99/07860 (принятой нами за прототип), в которой предложены композиции какого-либо белка ВПЧ (в качестве антигенной детерминанты), соединенного со стрессовым протеином (белком теплового шока), с приемлемым фармакологическим компонентом. Композиция гибридного белка способна индуцировать клеточный, клеточно-медиируемый цитолитический иммунный ответ. Большинство фактического материала заявки посвящено композициям на основе слитых или рекомбинантных белков Е7 и/или Е6 ВПЧ 16 с белком теплового шока Hsp65, относящегося к белкам теплового шока класса Hsp60. Конъюгаты могут быть получены экспрессией соответствующих генов в векторе под контролем промотора Р Т7 в E.coli.
В примерах 5, 6, 8 показано, что регрессия индуцированных опухолей у иммунизированных этими композициями мышей введением им раковых клеток линии ТС-1, экспрессирующих белки Е7 и Е6, происходит с той же, либо немного меньшей эффективностью, что и при их иммунизации белком Е7 в полном адъюванте Фрейда (так называемый положительный контроль).
Это очень важный результат. Методы современной биохимии, генетической инженерии позволяют получить практически любой антиген, но заставить его работать, т.е. сделать так, чтобы он не был выведен из организма макрофагами печени и почек, которые не формируют иммунный ответ, а был представлен иммунокомпетентым клеткам так, чтобы образовалась цепь клеточных взаимосвязанных реакций или событий, т.е. чтобы сформировался клеточный иммунитет - это требует не меньших усилий и является объектом многих научных работ и изобретений (см., например, пат. США №№20010031262, 5997900, 6419920, 5965125, 5906817, РСТ 01/41809 и многие другие). По сути это и есть предмет изобретения-прототипа: разработана в общем виде работающая конструкция для выработки клеточной составляющей иммунного ответа для белков вируса папилломы человека в качестве антигенных детерминант. Однако широта защиты является обратной стороной непроработанности частных решений, ставящих перед собой более определенные, конкретные задачи. Ее использование напрямую для иммунотерапии и вакцинации раковых заболеваний сомнительно ввиду того, что, как было отмечено ранее, раковые клетки способны терять многие свои детерминанты, которые к тому же являются слабыми иммуногенами.
Изобретательской задачей является создание в рамках предложенных конструкций таких рекомбинантных белков, их композиций и набора реагентов для иммунотерапии и вакцинации опухолевых заболеваний аногенитальной сферы, которые бы реально отвечали требованиям на такие препараты: были эффективны для подавляющего контингента больных, отличались технологичностью получения и для которых была бы разработана схема лечения и вакцинации.
Изобретательская задача решается тем, что предлагается композиция рекомбинантных белков для иммунотерапии и профилактической вакцинации опухолевых заболеваний аногенитальной сферы, ассоциированных с вирусами папилломы человека, отличием в которой является то, что она содержит в эффективном количестве гибридные белки, состоящие из аминокислотных последовательностей онкобелка Е7 вируса папилломы человека 16 и 18 типов, которые ковалентно присоединены с аминокислотой последовательностью белка теплового шока 70 (Hsp70) из М. tuberculosis при следующем соотношении белков Е7 16-Hsp70 и Е7 18-Hsp70 - (1-2):1.
Предлагаемая композиция может дополнительно содержать фармакологически приемлемые компоненты.
Изобретательская задача решается также тем, что предлагается фармацевтический набор реагентов для иммунотерапии и профилактической вакцинации опухолевых заболеваний аногенитальной сферы, ассоциированных с вирусом папилломы человека, содержащий композицию рекомбинантных белков Е7 16-Hsp70 и Е7 18-Hsp70 из M.tuberculosis в соотношении (1-2):1 и противотуберкулезную вакцину БЦЖ.
Предлагается также способ получения композиции рекомбинантных белков, отличающейся тем, что экспрессию соответствующих генов осуществляют в векторных плазмидах рТНЕ 716 и рТНЕ 718 под контролем Т7 промотора.
Предлагается также способ иммунотерапии и профилактической вакцинации опухолевых заболеваний аногенитальной сферы, ассоциированных с вирусами папилломы человека, отличающийся тем, что осуществляют предварительную стимуляцию иммунитета введением пациенту противотуберкулезной вакцины БЦЖ, после чего в сроки повторной вакцинации вводят композицию рекомбинантных белков Е7 16-Hsp70 и Е7 18-Hsp70 (из М. tuberculosis).
В основе изобретения лежат два новых вещества, рекомбинантные белки Е7 16-Hsp70 (из M.tuberculosis) и Е7 18-Hsp70 (из M.tuberculosis), которые в эксперименте с индуцированными опухолями показали эффективность большую, чем у белка Е7 16 в полном адъюванте Фрейда (см. пример 6), т.е. эти вещества оказались более эффективными антигенными конструкциями, чем соответствующие гибридные белки в способе прототипе. Так как белки теплового шока содержатся в любой ткани и в любом организме, a Hsp70 класс - в клетках млекопитающих, бактерий и микобактерий, таких как M.leprae, M.tuberculosis, M.vaccae, M.S.megmetis, M.bovis, a взаимосвязь между структурой химического соединения и его свойствами устанавливается только опытным путем, то изобретение уже на этом этапе соответствует критерию изобретательский уровень.
В качестве антигенной детерминанты ВПЧ в композиции использован только белок Е7 (в прототипе наряду с Е7 равноценно используется белок Е6). Наш опыт, а также анализ соответствующих научных и клинических данных, свидетельствует, что только белок Е7 является надежной мишенью для иммунологической атаки при цервикальном раке и др. опухолевых заболеваниях аногенитальной сферы. В композицию входят два гибридных онкобелка: Е7 16 и Е7 18, и только в этом случае композиция будет эффективна для большего контингента больных (до 70-80% против 40-50% по прототипу).
Выбор Hsp70 из M.tuberculosis привел не только к получению более эффективной антигенной конструкции, чем в прототипе, но был сделан не случайно еще и потому, что заявитель надеялся использовать известную противотуберкулезную вакцину БЦЖ (разрешенную в России и которая делается новорожденным) для стимуляции иммунного ответа к Hsp 70 M.tuberculosis, за счет чего происходит резкое усиление иммунного ответа на весь гибридный белок. Как оказалось, такой подход был правомерен, что показано в примере 6. Он реализован через фармакологический набор и способ иммунотерапии и вакцинации, которые являются новыми и отвечающими критерию “изобретательский уровень”.
Следует отметить, что получаемые гибридные белки отвечают требованию технологичности: на N-конце они содержат последовательность из 6His, что облегчает их очистку и обеспечивает требуемую чистоту реагента. Была также подобрана плазмида и промотор, обеспечивающий экспрессию соответствующих генов, с наибольшим уровнем синтеза белка. Уровень синтеза гибридных белков в клетках E.coli под контролем промотора Т7 полимеразы составил 30% от суммарного клеточного белка, тогда как использовавшийся также в экспериментах по оптимизации получения гибридных белков промотор PL (бактериофаг λ) и lac промотор давали синтез белка соответственно 12 и 15%. Как понятно, композиция рекомбинантных белков не нуждается в адъюванте за счет конъюгации с Hsp70, что тоже является большим удобством в использовании, т.к. адьювант Фрейда часто дает осложнения в виде нарывов, свищей и остающихся шрамов, а новых адьювантов практическая медицина пока не имеет (прогресс в этой области коснулся в основном пока только вакцин для ветеринарных целей).
Изобретение иллюстрируется следующими примерами. Примеры 1,2,3 посвящены получению и выделению гибридных белков. В примерах 4 и 5 дано описание композиции и фармакологического набора реагентов. В примере б показана эффективность использования гибридного белка Е7 16-Hsp70 и совместного его использования с вакциной БЦЖ по сравнению с “позитивным контролем” в экспериментальной иммунотерапии опухолей у мышей. В примере 7 показана эффективность использования композиции гибридных белков на группе добровольцев (на базе ЦКВ диспансера).
Пример 1. Последовательности клонированных генов (см. в конце текста).
Пример 2.
Создание продуцента DnaK (HSP70)
Ген dnaK M. tuberculosis был амплифицирован с использованием праймеров dnaK-1 (gc gga tcc gct cgt ggg gtc ggg atc g) и dnaK-2 (gtc cgt cac ttg gcc tcc). Полученный фрагмент был обработан рестриктазой BamHI и клонирован между BamHI и Smal сайтами экспрессирующего вектора pQE30 (Qiagen). Данная конструкция позволяет экспрессировать DnaK, слитый с 6 гистидинами на N-конце, под контролем lacI-регулируемого промотора. Наличие 6 гистидиновых аминокислот облегчает очистку белка. Полученную рекомбинантную плазмиду pQESO-dnaK поддерживали в штамме E.coli DLT1270, содержащем хромосомноинтегрированную копию lacI - репрессора.
Корректность процедуры клонирования была подтверждена при помощи рестрикционного анализа и ПЦР.
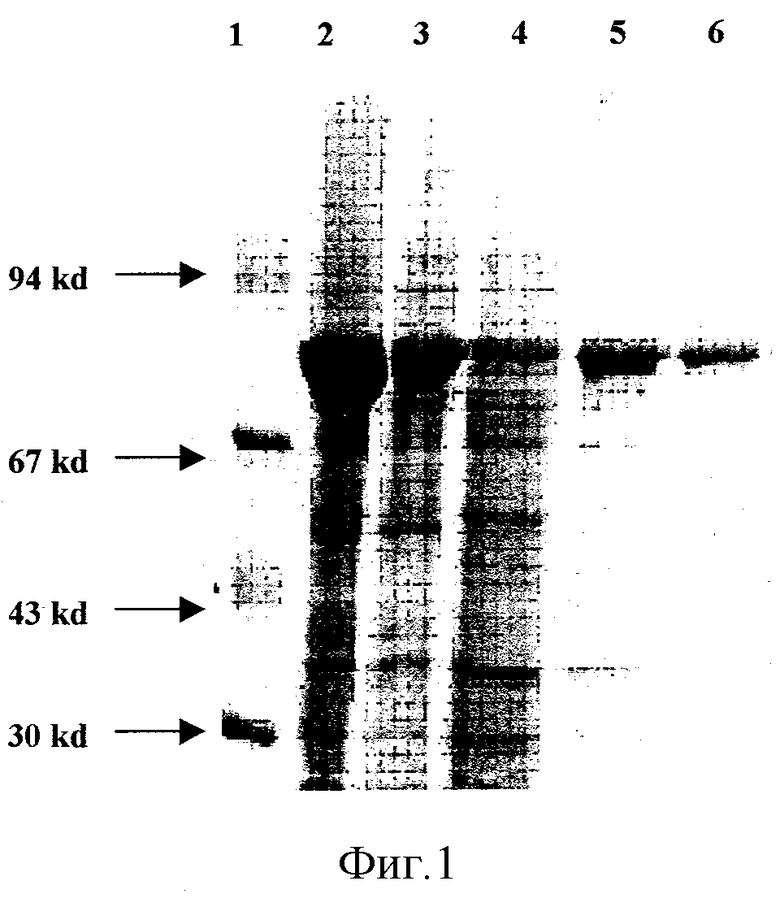
Синтез DnaK индуцировали при помощи IPTG. Ночную культуру DLT1270/pQE30-dnaK, выращенную в LB-бульоне, разводили 1:100 и выращивали в LB-бульоне на качалке до OD600=0.5 Затем вносили IPTG (оптимальная доза 0.1 мМ) и продолжали выращивание в течение 3-4 часов. Продукцию белка контролировали при помощи SDS-PAGE, выход продукта в данных условиях составлял 40-70% растворимых белков. (Фигура.1, где показан электрофорез белков в ПААГ 13% с SDS, где
1. Маркеры молекулярного веса.
2. Лизат клеток E.coli, содержащих плазмиду pQE30 (ген hsp70+6 His).
3. Супернатант из рекомбинантного штамма E.coli с плазмидой pQE30 после разрушения ультразвуком.
4. Осадок из рекомбинантного штамма E.coli, содержащего плазмиду pQE30 после разрушения ультразвуком.
5. Белок Hsp70 после одноступенчатой хроматографии на хелатном носителе.
6. Белок Hsp70 после второй стадии очистки.)
рSКЕ16
Содержит ген Е7 Human papillomavirus type 16, амплифицированный из ДНК клинических изолятов при помощи геноспецифических праймеров. Фрагмент длиной 303 п.н. клонирован по сайгам ЕсоRi-ВаmHI в плазмиде pBluescriptSK(+) (Stratagene). Последовательность гена соответствует данным GenBank (например, AF125673). Особенности конструкции: 1) перед инициирующим кодоном сохранен триплет АТС для оптимизации эукариотической экспрессии; 2) отсутствие терминирующего кодона, поскольку ген планировался для получения гибридного белка.
pSKE18
Содержит ген Е7 Human papillomavirus type 18, амплифицированный из ДНК клинических изолятов при помощи геноспецифических праймеров. Фрагмент 324 п.н. клонирован по сайгам ЕсоRI-ВаmHI в плазмиде pBluescnptSK(+) (Stratagene). Последовательность содержит нуклеотидные замены по сравнению с GenBank (например, HPU89349; PAPHPV18), однако аминокислотная последовательность белка при этом сохраняется.
Терминирующий кодон также отсутствует. Перед инициирующим кодоном - триплет AGT.
рТЕ716
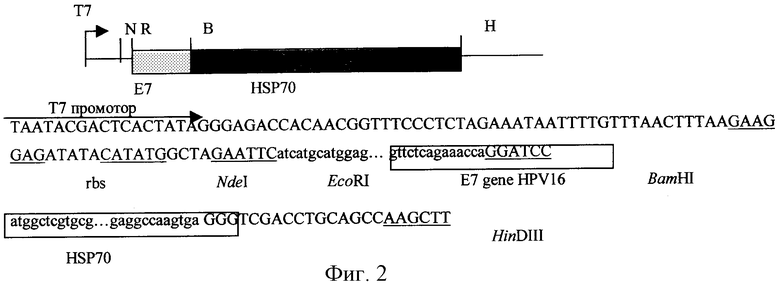
Плазмида получена путем клонирования ЕсоRI-ВаmHI фрагмента плазмиды pSKE16, содержащего ген Е7 HPV16, совместно с BamHI-HinDIII фрагментом плазмиды pQE-HSP70 (новый вариант с правильной 3'-концевой последовательностью гена hsp70) в вектор, полученный расщеплением плазмиды pKS70 EcoRI и HinDIII и выделения фрагмента, соответствующего векторной части. Фактически в качестве вектора была использована плазмида рТ7-7. Экспрессия гибридного гена E7-HSP70 находится под контролем Т7 промотора и индуцируется ИПТГ в клетках Е. coli BL21(DE3) - см. Фигуру 2.
РТНЕ716
получена путем клонирования олигонуклеотидного дуплекса His1+His2, в вектор, полученный путем расщепления плазмиды рТЕ716 NdeI и EcoRI.

Кодирует гибридный белок Н16: Met(His)6-GluPheIle-E7/16-GlySer-Hsp70 (736 а.о., 79,3 кДа, ИЭТ 4,7).
рТНЕ718
получена путем клонирования ÅсоRI-BamHI. фрагмента плазмиды pSKE18, содержащего ген E7 HPV18, совместно с олигонуклеотидным дуплексом His1+His2, в вектор, полученный путем расщепления плазмиды рТЕ716 Ndel и BamHI. Кодирует гибридный белок Н18: Met(His)6-GluPheSer-E7/18-GlySer-Hsp70 (743 а.о., 80,3 кДа, ИЭТ 4,8).

Пример 3. Выделение белков Н16 и Н18
Клетки Е. coli штамма BL21(DE3) трансформировали ДИК плазмид рТНЕ716(718) и выращивали в течение ночи при 37°С в среде LB с добавлением ампициллина (100 мкг/мл) и глюкозы (0,2%). Затем разбавляли ночную культуру в 25 раз свежей средой LB с ампипиллином и подращивали 2-3 часа до мутности около 0,5, после чего добавляли раствор ИПТГ до 0,2 мМ. Растили еще 3 часа, центрифугировали культуру при 5 тыс. об/мин 10 мин, супернатант отбрасывали.
Осадок после центрифугирования суспендировали в буфере 20 мМ трис-HC1, рН 8, 0,3 М NaCl (1 мл на осадок из 50 мл культуры) и озвучивали 6 импульсов по 15 с. Центрифугировали 10 тыс. об/мин, 10 мин, осадок промывали тем же буфером с добавлением 0,1% Тритон Х-100 (0,5 мл), после чего суспендировали с помощью гомогенизатора в 5 мл буфера А (10 мМ трис-HCl, рН 8, 6М мочевина, 0,4М NaCl, 10 мМ β-меркаптоэтанол, 5 мМ имидазол). Перемешивали в течение 1 часа при комнатной температуре, отделяли супернатант центрифугированием при 10 тыс. об/мин 10 мин, осадок отбрасывали.
Колонку с IDA-агарозой (1 мл) заряжали раствором NiSO4, уравновешивали буфером А с 5 мМ имидазолом. Супернатант наносили на колонку, промывали 5 мл буфера А, затем 10 мл буфера В (буфер А с 20 мМ имидазола). Элюцию проводили буфером С (10 мМ трис-HC1, рН 8, 2М мочевина, 0,4М NaCl, 10 мМ β-меркаптоэтанол, 0,3 М имидазол). Этот буфер добавляли по 0,5 мл, собирая соответствующие фракции. Обычно белки H16 и H18 обнаруживались во фракциях 1-3.
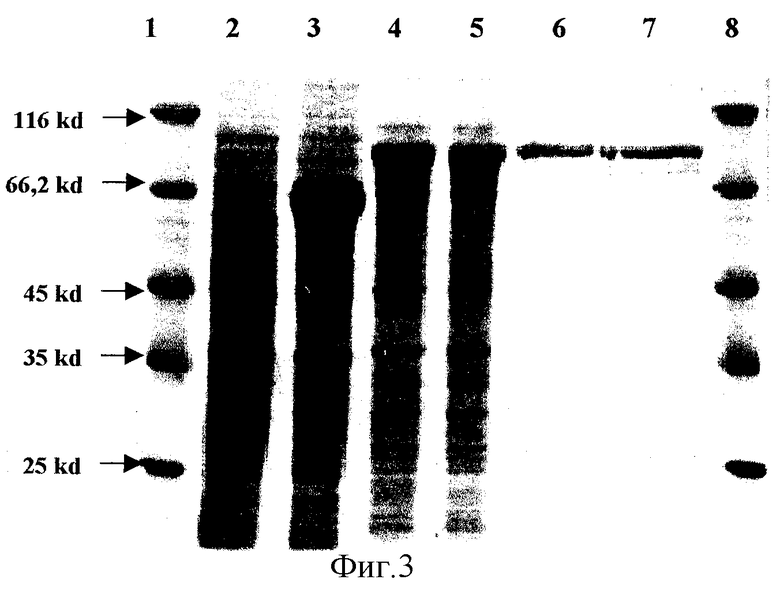
Объединенные фракции диализовали в течение ночи против 100-кратного объема буфера 10 мМ трис-HC1, рН 8, 150 mM NaCl. (Фигура 3, на которой представлен электрофорез белков в ПААГ 13% с SDS, где
1,8 - Маркеры молекулярного веса
2 - Лизат клеток E.coli, содержащих плазмиду рQЕ30 до индукции IPTG
3 - Лизат клеток E.coli, содержащих плазмиду рQЕ30 после индукции IPTG
4 - Лизат клеток E.coli, содержащих плазмиду рТНЕ716 после индукции IPTG
5 - Лизат клеток E.coli, содержащих плазмиду рТНЕ718 после индукции IPTG
6 - Гибридный белок E716-Hsp70 после одноступенчатой хроматографии
7 - Гибридный белок E718-Hsp70 после одноступенчатой хроматографии.)
Пример 4
Композиция гибридных белков, содержащих белки Е7 16-Hsp70 (M.tuberculosis) и Е7 18-Hsp70 (M.tuberculosis) в соотношении (1-2):1.
Смесь представляет собой белый порошок, хорошо растворимый в воде, в физиологическом растворе и фосфатно-буферном физиологическом растворе Дильбекко. Композицию хранят в асептических условиях в запаянных стеклянных капсулах в отсутствие кислоты, в сухом или растворенном в указанных растворителях виде.
Композицию при соотношении белков 1:1 используют для иммунотерапии по примеру 7.
Пример 5
Фармацевтический набор
Фармацевтический набор состоит из двух реагентов: композиции гибридных белков, описанной в примере 4, и известной вакцины БЦЖ. Вакцина БЦЖ представляет собой живые микобактерии вакцинного штамма БЦЖ, модифицированные в 1,5% растворе глутамината натрия. Прививочная доза содержит 0,05 мг в 0,1 мл растворителя. Препарат хранится при температуре не выше 8°С.
Пример 6
Иммунотерапия экспериментальных опухолей, экспрессирующих белок Е7 ВПЧ-16 с помощью гибридного белка Е716 - Hsp 70.
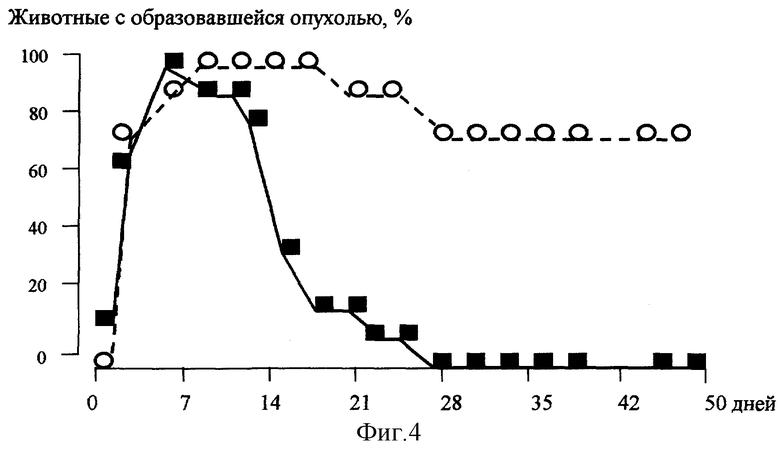
Для индукции опухолей использовали клеточную мышиную линию ТС-1, содержащую интегрированный геном ВПЧ-16, в которой активно экспрессируются вирусные онкогены Е6 и Е7. Для оценки противоопухолевого иммунитета мышам С57В1/6 вводили подкожно по 100 мкг очищенных белков Е7 (в полном адьюванте Фрейда), Hsp 70 и E7-Hsp 70 в фосфатно-буферном физиологическом растворе Дильбекко. На третий день после иммунизации вводили 1,3×105 клеток ТС-1. В течение 7 дней у всех подопытных животных развивалась подкожно пальпируемая опухоль. На Фигуре 4 представлены суммирующие результаты этих экспериментов, где продемонстрирована профилактическая иммунизация рекомбинантными белками Е7 в полном адъюванте Фрейда ( ) и Е7- Hsp 70 (
) и Е7- Hsp 70 ( ) в дозе 100 мкг. На третий день после иммунизации мышам подкожно вводили клетки ТС-1 в количестве 1,3×105. Наблюдение за мышами вели в течение 50 дней.
) в дозе 100 мкг. На третий день после иммунизации мышам подкожно вводили клетки ТС-1 в количестве 1,3×105. Наблюдение за мышами вели в течение 50 дней.
Как следует из представленных данных, к 30 дню у всех мышей, иммунизированных гибридным белком E7-Hsp 70, наблюдалась полная регрессия опухоли. Частичная регрессия (10-15% животных) наблюдалась в случае иммунизации белком Е7 и Hsp 70 (данные не представлены). В контрольной группе (неиммунизированные мыши) наблюдался прогрессивный рост опухоли.
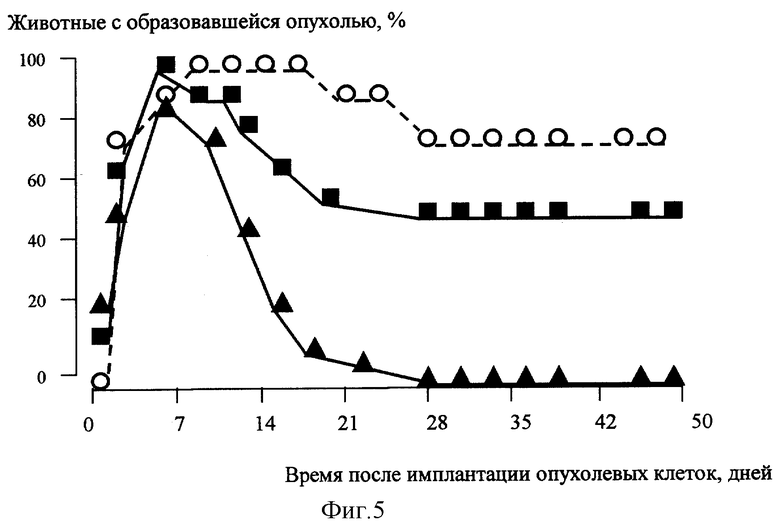
Проводилась иммунотерапия экспериментальных опухолей гибридным белком Е7-16-hsp70 на фоне предварительной иммунизации БЦЖ с концентрацией гибридного белка в 6,5 раз (15 мкг) меньшей, чем в экспериментах без предварительной сенсибилизации животных БЦЖ. Данные представлены на Фигуре 5, где представлена профилактическая иммунизация рекомбинантными белками Е7 в полном адъюванте Фрейда ( ) и E7-Hsp 70 (
) и E7-Hsp 70 ( ) и E7-Hsp70 на фоне предварительной иммунизации БЦЖ (
) и E7-Hsp70 на фоне предварительной иммунизации БЦЖ ( ). Доза для всех реагентов 15 мкг. На третий день после иммунизации мышам подкожно вводили клетки ТС-1 в количестве 1,3×105. Наблюдение за мышами вели в течение 50 дней.
). Доза для всех реагентов 15 мкг. На третий день после иммунизации мышам подкожно вводили клетки ТС-1 в количестве 1,3×105. Наблюдение за мышами вели в течение 50 дней.
Пример 7.
Двум группам добровольцев (по 30 женщин в каждой с диагнозом дисплазия шейки матки I степени) вводили подкожно дважды с интервалом в 14 дней композицию из белков Е7 16-Hsp70 и Е7 18-Hsp70 и белок Е7 16-Hsp70 соответственно в физиологическом растворе в дозе 0,3 мг на 1 инъекцию. Через месяц наблюдения у первой и второй групп был произведен профилактический осмотр. Положительная динамика наблюдалась в обеих группах. Однако в первой группе этот процент составил 75%, тогда как во второй он отмечался только у 54% пациенток.


| название | год | авторы | номер документа |
|---|---|---|---|
| МУКОЗАЛЬНАЯ ВАКЦИНА ДЛЯ ИММУНОТЕРАПИИ ЗАБОЛЕВАНИЙ, ОБУСЛОВЛЕННЫХ ВИРУСАМИ ПАПИЛЛОМЫ ЧЕЛОВЕКА, И СПОСОБ ЛЕЧЕНИЯ С ЕЕ ИСПОЛЬЗОВАНИЕМ (ВАРИАНТЫ) | 2008 |
|
RU2377305C1 |
| РЕКОМБИНАНТНЫЙ ГИБРИДНЫЙ БЕЛОК, ПРЕПАРАТ ДЛЯ ИММУНОТЕРАПИИ НА ЕГО ОСНОВЕ И СПОСОБ ИММУНОТЕРАПИИ РЕЦИДИВИРУЮЩЕГО ПАПИЛЛОМАТОЗА ГОРТАНИ | 2005 |
|
RU2290204C1 |
| ВАКЦИННАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ТУБЕРКУЛЕЗНОЙ ИНФЕКЦИИ И ГЕНЕТИЧЕСКИЕ КОНСТРУКЦИИ ДЛЯ ПОЛУЧЕНИЯ ДЕЙСТВУЮЩИХ КОМПОНЕНТОВ ЭТОЙ КОМПОЗИЦИИ | 2003 |
|
RU2262351C1 |
| ВАГИНАЛЬНЫЕ СУППОЗИТОРИИ ДЛЯ ЛЕЧЕНИЯ РАКА ШЕЙКИ МАТКИ | 2008 |
|
RU2404794C2 |
| СПОСОБ МИКРОБИОЛОГИЧЕСКОГО СИНТЕЗА ГИБРИДНОГО БЕЛКА Е7-HSP70 (ВАРИАНТЫ) | 2013 |
|
RU2546917C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ШЕЙКИ МАТКИ, АССОЦИИРОВАННЫХ С ВИРУСОМ ПАПИЛЛОМЫ ЧЕЛОВЕКА, В ВИДЕ ВАГИНАЛЬНОГО СУППОЗИТОРИЯ | 2010 |
|
RU2438703C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ШЕЙКИ МАТКИ, АССОЦИИРОВАННЫХ С ВИРУСОМ ПАПИЛЛОМЫ ЧЕЛОВЕКА, В ВИДЕ ВАГИНАЛЬНЫХ КАПСУЛ | 2010 |
|
RU2438702C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ШЕЙКИ МАТКИ, АССОЦИИРОВАННЫХ С ВИРУСОМ ПАПИЛЛОМЫ ЧЕЛОВЕКА, В ВИДЕ ВАГИНАЛЬНОГО РАСТВОРА ДЛЯ ОРОШЕНИЯ, НАБОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2010 |
|
RU2438652C1 |
| ВАКЦИННАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ, РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК, ОБЕСПЕЧИВАЮЩАЯ СИНТЕЗ ГИБРИДНОГО БЕЛКА, СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2316342C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКА E7-HSP70 И ШТАММ ДРОЖЖЕЙ Saccharomyces cerevisiae ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2012 |
|
RU2489481C1 |
Изобретение относится к области медицины и касается композиции рекомбинантных белков, способа получения композиции, фармацевтического набора реагентов для иммунотерапии и профилактической вакцинации опухолевых заболеваний аногенитальной сферы и способа иммунотерапии и профилактической вакцинации. Сущность изобретения включает гибридные белки, состоящие из аминокислотных последовательностей онкобелка Е7 вируса папилломы человека 16 и 18 типов, которые ковалентно соединены с аминокислотной последовательностью белка теплового шока с м.м. 70 кДа (Hsp70) из M.tuberculosis, соответственно E716-Hsp70 и E718-Hsp70. Преимущество изобретения заключается в усилении активности. 4 с. и 2 з.п. ф-лы, 5 ил.
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| JABBAR I.A | |||
| et al., Jmmune responses induced by BCG recombinant for human papilloma virus LI и Е7 proteins plasmid pY07L1 and plazmid pY60Е7 - mediated gene transfer and expression for vector expression in mouse for nucleic acid vaccene., Vaccine, 2000, v.l8, №22, pp.2444-2453 | |||
| SCHWEIGHOFFER Т., Tumor cells expressing a recall antigen are powerful cancer vaccines, Eur | |||
| J.Jmmunol., 1996, v.26, №11, p.p.2559-2564. | |||
Авторы
Даты
2004-05-27—Публикация
2002-10-22—Подача