Изобретение относится к генетической инженерии, конкретно к генетической конструкции, кодирующей синтез α2-интерферона человека, и которая может быть использована для его промышленного получения в штаммах E.coli.
Интерфероны впервые привлекли внимание благодаря своей способности вмешиваться в репликацию и продукцию разного рода вирусов. Это семейство мультифункциональных цитокинов, среди которых наиболее изученными являются интерферон-альфа (IFN-α), -бета (IFN-β), -гамма (IFN-γ).
Все интерфероны - продукты различных генов. IFN-α представляет целое семейство, белки которого кодируются как минимум 23 различными генами. Это 19-23 кДа полипептиды длиной от 156 до 172 аминокислот. Все IFN-α высокогомологичны и различаются лишь одной-двумя аминокислотами. В белковой последовательности имеются сайты потенциального гликозилирования, однако большинство подтипов IFN-α негликозилированы. Пространственная структура интерферонов состоит исключительно из альфа-спиралей и относится к классу "четырехспиральный бочонок". Биологической активностью обладают мономеры этого белка.
Интерфероны обладают множеством активностей, которые способствуют активации Т-клеточного иммунитета, что необходимо для естественной защиты организма от вирусных и бактериальных инфекций. Эти цитокины активирут другие иммунокомпетентные клетки - Т-клетки, NK-клетки, активированные макрофаги, стимулируя ранний неспецифический иммунный ответ. Они усиливают экспрессию рецепторов и антигенов эффекторными клетками, регулируют транскрипцию новых генов, стимулируют экспрессию белков комплекса гистосовместимости класса II (МНС II). Интерфероны обнаруживают антипролиферативную, цитостатическую и цитотоксическую активности на некоторых опухолевых клетках.
Эти белки также принимают участие в регуляции гемопоэза, в результате чего усиливается продукция и активация нейтрофилов, моноцитов, тромбоцитов, что, в свою очередь, является ключевым событием воспалительного процесса. И это лишь малая часть активностей, которыми обладают интерфероны.
Суммируя вышесказанное, можно сделать вывод, что использование экзогенных интерферонов для лечения многих заболеваний - воспалительных, опухолевых и многих других, где необходима иммуномодулирующая активность, более чем оправдано. В связи с вышеописанными свойствами интерферона многими исследователями были разработаны штаммы-продуценты для наработки рекомбинантного аналога этого белка (патенты WO 01/42301 А1, WO 01/25438 А2, WO 00/69913, WO 01/57217 A1, WO 87/06616, WO 88/09673, EP 0032134 В1, ЕР 0626448 А2, ЕР 0538300 B1, US 5710027, SU 1092176 A).
Наиболее близкой по технической сущности является рекомбинантная ДНК, ее штамм-продуцент на базе Е.соli, которые пригодны для промышленного получения α2-интерферона (US 5710027, кн. 435-69.51, 1998).
Рекомбинантная ДНК содержит нуклеотидную последовательность, α2-интерферон-гена, слитую с нуклеотидной последовательностью сигнального пептида теплоустойчивого энтеротоксина E.coli, под контролем Е.соli фосфотазного промотора (phoA).
Вектор, содержащий рекомбинантную ДНК, устойчиво экспрессируется в E.coli, обеспечивает стабильную секрецию белка в преплазматическое пространство клетки и дает правильно сформированный с аутентичным N-терминаторным концом и правильными дисульфидными связями α2-интерферон (то есть биологически активный α2-интерферон) с промышленно пригодным выходом - 15-20% от общего клеточного белка.
Однако известная рекомбинантная ДНК, вектор, ее содержащий, и используемый штамм дают продукт, который требует многостадийной очистки, включающей последовательную хроматографию на силикагеле, хроматографию с гидрофобным взаимодействием, катионно-обменную и анионно-обменную хроматографии.
Изобретательской задачей является повышение выхода и упрощение очистки биологически активного (то есть с сохраненными структурными особенностями, отмеченными выше) α2-интерферона.
Изобретательская задача решается тем, что предложена рекомбинантная плазмидная ДНК pASIF-62, кодирующая синтез α2-интерферона, которая имеет размер 4200 т.п.о. и состоит из следующих элементов: lac-промотор, АТГ-кодон, ген α2-интерферона размером 642 нуклеотида, инвертированный фрагмент ДНК-гена htpR размером 350 нуклеотидов, ген устойчивости к ампициллину и сайты для рестриктаз Pst, Hind III, BamHI, а также содержит 18 нуклеотидных остатков, оперативно связанных с lac-промотором и геном интерферона и кодирующих 6 гистидиновых остатков.
Предлагается также способ получения человеческого α2-интерферона экспрессией его гена в составе рекомбинантной ДНК в Е.соli, отличием которого является то, что экспрессию осуществляют в рекомбинантной плазмиде pASIF-62 в ростовой среде до ее мутности 0,4-0,6 ОД, после чего в нее добавляют 0,1-0,3 мМ изопропил-b-тиогалактозида - индуктора lас-промотора (ИПТГ) и экспрессию продолжают под контролем индуцированного lac-промотора рекомбинантной плазмиды. Очистку целевого продукта, полученного в плазмидной ДНК pASIF-62 осуществляют в одну стадию методом катионно-обменной хроматографии на агарозном носителе. В способе предполагается в виде предпочтительного варианта использовать штаммы Е.соli, дефектные по гену htpR.
По предлагаемому способу экспрессия интерферона осуществляется в цитоплазматическую среду Е.соli, что создает определенные трудности в правильном фолдинге белка, а также в подборе лидера стабильной экспрессии, который не должен менять аутентичность терминаторного конца.
Другой проблемой цитоплазматической экспрессии гетерологичных белков в E.coli является проблема многостадийной очистки, требующей на первой стадии дорогостоящей очистки с помощью иммуноаффинной хроматографии (ЕР 396555).
Предложенная рекомбинантная плазмида для получения α2-интерферона и способ получения с ее использованием обходят все эти проблемы за счет использования Заявителем нового подхода, предложенного ниже и доказывающего “изобретательский уровень” предложенного изобретения.
Известно, что за агрегацию чужеродных рекомбинантных полипептидов в клетках E.coli отвечают “шапероны”, то есть белки “теплового шока” (БТШ). К их числу относятся белки DNAK, groES и groEL, которые вызывают агрегацию чужеродных полипептидов, и Lon-протеаза, осуществляющая их избирательную деградацию. Регуляция транскрипции генов, кодирующих белки “теплового шока”, осуществляется белком htpR, который является альтернативной δ-субъединицей РНК-полимеразы и при встраивании в голофермент обеспечивает избирательную транскрипцию генов БТШ в условиях синтеза аномальных белков. Ранее нами было установлено, что в клетках E.coli, дефектных по БТШ, наблюдается более интенсивное накопление рекомбинантных белков, а из “телец включения”, полученных в этих штаммах, существенно выше выход белков с природной конформацией (с правильным фолдингом).
Эти наблюдения позволяют сделать вывод, что нарушение функции шаперонов в клетках E.coli придает клеткам весьма полезные с биотехнологической точки зрения свойства, так как значительно повышается “выход” рекомбинантных продуктов.
Однако известные мутации, которые нарушают функцию шаперонов и снижают протеолитическую активность клеток, существенно нарушают ростовые свойства клеток E.coli, стимулируют образование слизи, что затрудняет промышленное культивирование рекомбинантных штаммов.
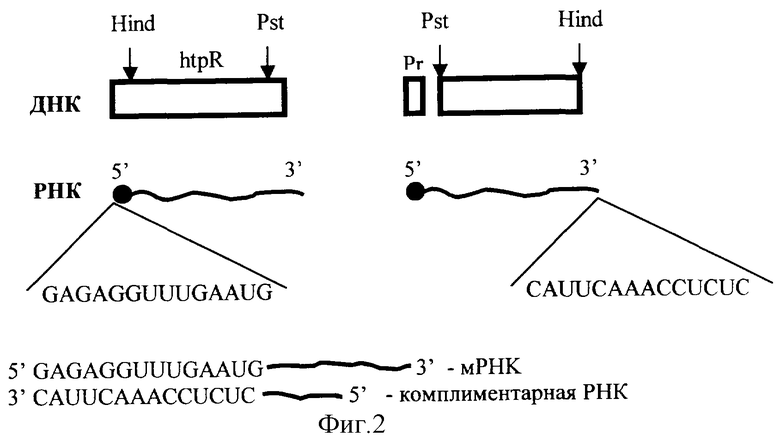
Нами предложено другое решение этой проблемы, состоящее в том, что рекомбинантная плазмида, кодирующая синтез α2-интерферона, за последовательностью гена IFN содержит короткую инвертированную последовательность гена htpR-регулятора экспрессии генов БТШ. Молекулы РНК, синтезирующиеся при транскрипции этой последовательности, имеют структуру, комплиментарную структуре mРНК гена htpR и могут выполнять функцию антисмысловой РНК, блокируя синтез БТШ посредством инактивации белка HtpR.
Сделанный Заявителем выбор лидерной последовательности из шести гистидиновых остатков отвечает в наибольшей степени основным биотехнологическим требованиям, которые могут быть к нему предъявлены.
Это, в первую очередь, надежная экспрессия слитого вместе с ним α2-интерферона, отсутствие необходимых в таких случаях точечных замен для адаптации к белоксинтезирующему аппарату клетки-хозяина, упрощение конечного выделения и очистки слитого белка, а также отсутствие препятствий для корректного фолдинга зрелого белка.
Для получения рекомбинантной ДНК был использован вектор pQE30, содержащий lac-промотор, участок инициации трансляции, область, кодирующая 6 гистидиновых остатков, и полилинкер, содержащий 6 сайтов рестрикции.
Изобретение иллюстрируется следующими примерами.
Пример 1.
Клонирование гена α2-интерферона человека.
В качестве источника генов α2-интерферона были использованы:
1. Библиотека генов человека
2. Плазмида из промышленного штамма-продуцента α2-интерферона на основе Pseudomonas Putida
3. Плазмида из промышленного штамма-продуцента α2-интерферона на основе Escherichia coli.
Фрагмент гена IFN2, соответствующий зрелой части белка, был выделен из трех выше перечисленных источников методом амплификации с помощью праймеров:
IFNA2-L gc gga tcc atg tgt gat ctg cct caa ace
IFNA2-R ccc aag ctt tea ttc ctt act tct taa.
Фрагмент был обработан рестриктазами BamHI+HindIII и клонирован между BamHI и HindIII сайгами трех типов векторов для экспрессии.
В каждом случае получено и проанализировано по 20 независимых клонов.
Индукция синтеза интерферона оценивалась в 10 мл IPTG-индуцированных культур (выращивание до OD600=0.5, внесение IPTG до 0.2 мМ, затем 3 часа при 37С на качалке). Продукция белка ожидаемого размера проверена по SDS-PAGE.
В качестве клеток-“хозяев” были использованы штаммы E.coli BL21, DLT1270, DSK-41. Штамм DSK-41 получен в лаборатории молекулярной биологии ВНЦМДЛ путем внесения мутации в ген htpR, в результате чего в штамме наблюдается пониженный уровень протеолиза, что повышает выход любых рекомбинантных белков. Другая особенность штамма DSK-41 состоит в том, что в стационарной фазе роста в этом штамме наблюдается спонтанная дерепрессия генов, находящихся под контролем lac-промотора и lac-репрессора, вероятно, за счет деградации lac-репрессора.
Праймеры:
IFNA2-L gc gga tcc atg tgt gat ctg cct caa асc
IFNA2-R ccc aag ctt tca ttc ctt act tct taa
На фиг.1 показана последовательность гена human IFNA2, где начало гена - 69 нт (ATG), конец - 635 нт (TGA), зрелая часть белка соответствует участку 138-635 нт. Начало гена, начало зрелой части и стоп-кодон подчеркнуты. Для экспрессии взята зрелая часть. Вставляли между BamHI/HindIII сайтами pQE30.
Пример 2.
Клонирование последовательности гена htpR.
Фрагмент гена htpR выделяли из плазмиды pKV3, содержащей полимеразный ген htpR из генома E.coli. Плазмидную ДНК обрабатывали рестриктазами Hind III и Pst I и после фракционирования в агарозном геле выделяли фрагмент гена htpR размером 350 нуклеотидных пар. Фиг.2 представляет собой гипотетическую схему взаимодействия мРНК гена htpR с антисмысловой РНК.
Пример 3
Исследование протеолитической активности в штаммах E.coli, содержащих плазмиду pASIF62.
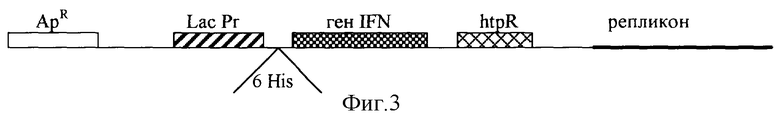
Для конструирования плазмиды, кодирующей синтез α2-интерферона, использовали вектор pQE30, куда встраивали ген IFN под контроль lас-промотора, таким образом, что на N-концевой последовательности белка синтезировались 6 остатков гистидина. Затем в 3’-концевую область гена после терминирующих кодонов встраивали фрагмент гена htpR в обратной ориентации, описанный в примере 2. Общая схема генетической конструкции представлена на фиг.3 (Рекомбинантная плазмида pASIF62).
Предполагается, что в результате индукции синтеза интерферона в клетках E.coli в присутствии IPTG будет образовываться антисмысловой транскрипт инвертированного фрагмента гена htpR, который при взаимодействии с mРНК htpR будет блокировать синтез БТШ и, следовательно, снижать уровень протеолиза в клетках E.coli.
Определение протеолитической активности штаммов
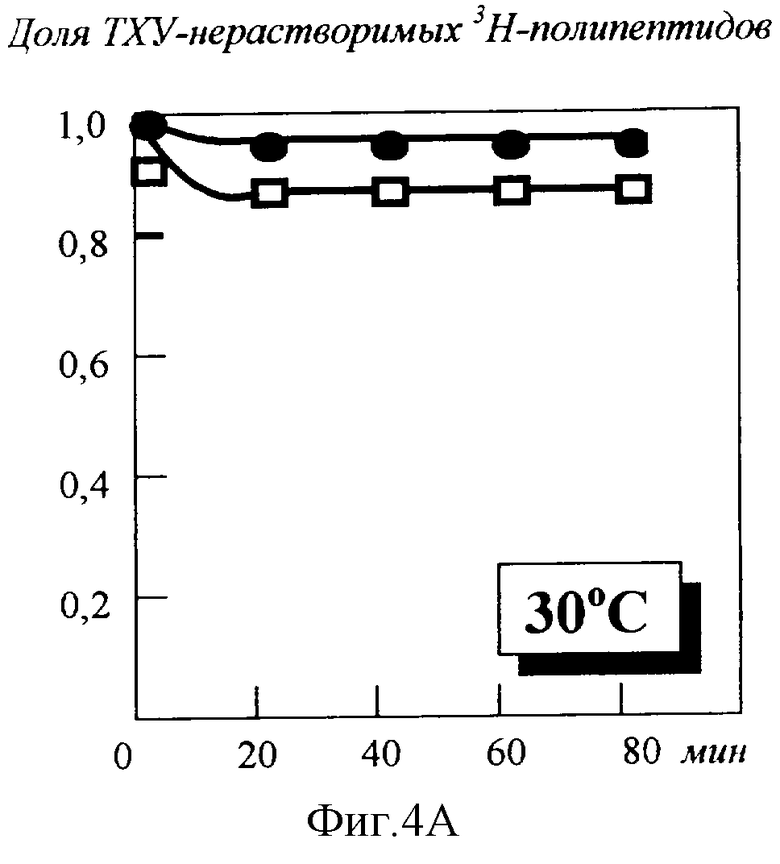
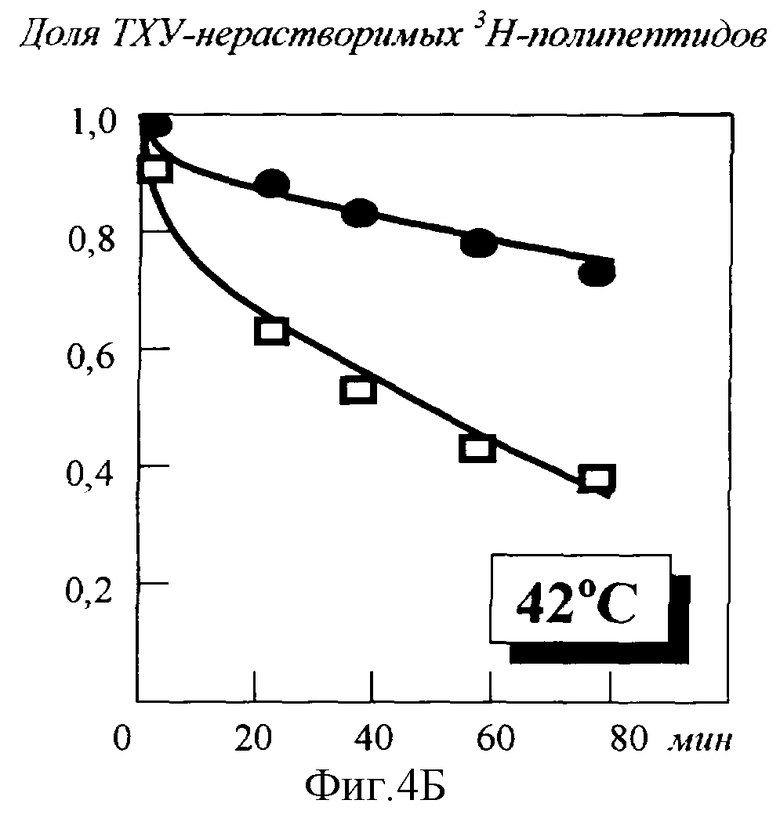
Скорости протеолитической деградации белков измеряли согласно методу Гольдберга. Бактериальные клетки выращивали при 30°С в минимальной среде М9, содержащей необходимые добавки. При достижении оптической плотности культуры при 550 нм = 0,4-0,5 в среду вносили пуромицин до конечной концентрации 300 мкг/мл и спустя 15 мин L-3Н-лейцин до конечной концентрации 0,2 Ки/мл. После этого клетки выращивали еще в течение 10 мин, собирали центрифугированием, отмывали дважды в среде М9, содержащей “холодный” лейцин в концентрации 75 мкг/мл для предупреждения повторного включения 3H-лейцина, высвобождающегося из белков. Клетки суспендировали в концентрации 2,5×105 мл. Скорость деградации аномальных пуромициновых полипептидов определяли по накоплению меченых свободных аминокислот в ТХУ-растворимой фракции. Как следует из результатов, представленных на фиг.4А и 4Б (скорость деградации 3H-пуромициновых полипептидов в штаммах:  -BL21c плазмидой pASIF62,
-BL21c плазмидой pASIF62,  -BL21 без плазмиды pASIF62) - в штамме Е.соli BL21, не содержащем плазмиду pASIF62, наблюдается значительное усиление протеолиза при температуре +42°С, тогда как в штамме, содержащем плазмиду, уровень протеолиза в аналогичных условиях существенно ниже.
-BL21 без плазмиды pASIF62) - в штамме Е.соli BL21, не содержащем плазмиду pASIF62, наблюдается значительное усиление протеолиза при температуре +42°С, тогда как в штамме, содержащем плазмиду, уровень протеолиза в аналогичных условиях существенно ниже.
Пример 4
Синтез α2-интерферона человека в штаммах E.coli
Уровень синтеза α2-интерферона определяли в штаммах E.coli, содержащих плазмиду pIF62 (не содержащую последовательность гена htpR и имеющую нормальный уровень протеолиза) и плазмиду pASIF62, ингибирующую синтез протеаз.
Клетки E.coli выращивали до плотности ОД-05, вносили IPTG до концентрации 0,2 мМ для индукции синтеза интерферона. Клеточные белки фракционировали в 13% SDS ПААГе.
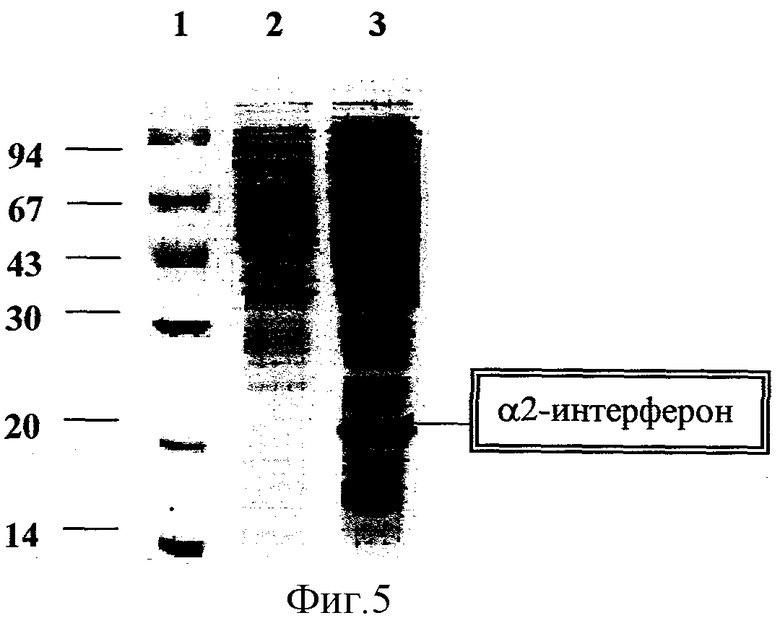
Из данных, представленных на фиг.5, следует, что в идентичных условиях роста клетки E.coli, содержащие плазмиду pASIF62, синтезируют рекомбинантный α2-интерферон. На фиг.5 представлен электрофорез белков штаммов E.coli в полиакриламидном геле, где
1 - маркеры молекулярного веса,
2 - штамм E.coli, содержащий рекомбинантную плазмиду pIF62 с геном α2-интерферон,
3 - штамм E.coli с рекомбинантной плазмидой.
Пример 5
Выделение рекомбинантного α2-интерферона
Клетки Е.coli штамма DLT1270 трансформировали плазмидой pASIF62 и выращивали в течение ночи при 37°С в среде LB с добавлением ампициллина (100 мкг/мл) и глюкозы (0,2%). Затем разбавляли ночную культуру в 25 раз свежей средой LB с ампициллином и подращивали 2-3 часа до мутности около 0,5, после чего добавляли раствор ИПТГ до 0,2 мМ. Растили еще 3 часа, центрифугировали культуру при 5 тыс. об/мин 10 мин, супернатант отбрасывали.
Осадок после центрифугирования суспендировали в буфере 20 мМ трис-НСl, рН 8, 0,3 М NaCl (1 мл на осадок из 50 мл культуры) и озвучивали 6 импульсов по 15 сек. Центрифугировали 10 тыс. об/мин, 10 мин, осадок промывали тем же буфером с добавлением 0,1% Тритон Х-100 (0,5 мл), после чего суспендировали с помощью гомогенизатора в 5 мл буфера А (10 мМ трис-НСl, рН 8, 6М мочевина, 0,4М NaCl, 10 мМ р-меркаптоэтанол, 5 мМ имидазол). Перемешивали в течение 1 часа при комнатной температуре, отделяли супернатант центрифугированием при 10 тыс. об/мин 10 мин, осадок отбрасывали.
Колонку с IDА-агарозой (1 мл) заряжали раствором NiSO4, уравновешивали буфером А с 5 мМ имидазолом. Супернатант наносили на колонку, промывали 5 мл буфера А, затем 10 мл буфера В (буфер А с 20 мМ имидазола). Элюцию проводили буфером С (10 мМ трис-HCl, рН 8, 2М мочевина, 0,4М NaCl, 10 мМ р-меркаптоэтанол, 0,3 М имидазол). Этот буфер добавляли по 0,5 мл, собирая соответствующие фракции. Обычно белки HI 6 и HI 8 обнаруживались во фракциях 1-3.
Объединенные фракции диализовали в течение ночи против 100-кратного объема буфера 10 мМ трис-HCl, рН 8, 150 mM NaCl.
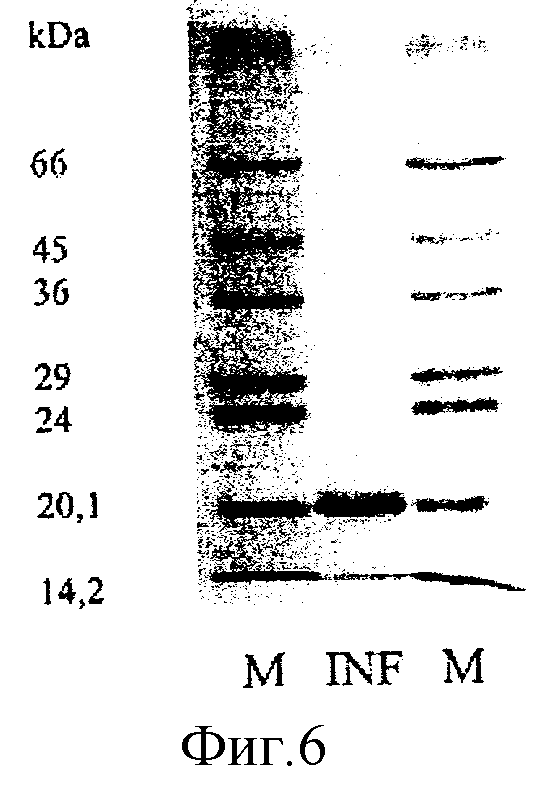
Выделенный α2-интерферон был охарактеризован методом жидкостной хроматографии и электрофорезом в ПААГе. На фиг.6 представлены данные электрофоретического анализа рекомбинантного α2-интерферона в полиакриламидном геле, где М - маркеры; INF-α2-интерферон.
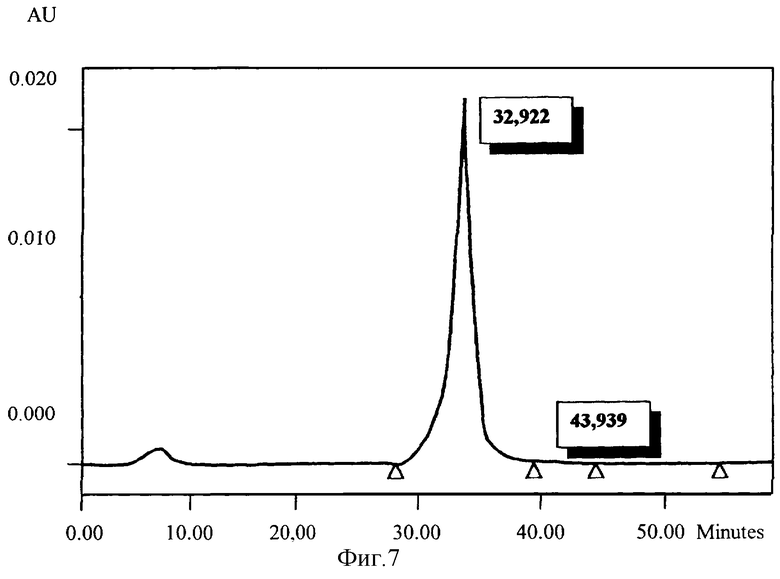
На фиг.7 представлена хроматографическая характеристика рекомбинантного α2-интерферона человека.
Предлагаемое изобретение поясняется таблицей.
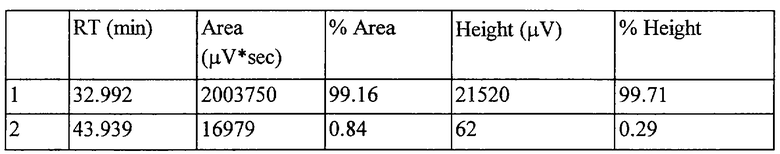
Выход составил 30% от общей массы клеточного белка.
Как следует из представленных данных, описанный метод выделения позволяет получить гомогенный белок, лишенный дополнительных примесей.
Пример 6
Иммунохимическая характеристика рекомбинантного α2-интерферона.
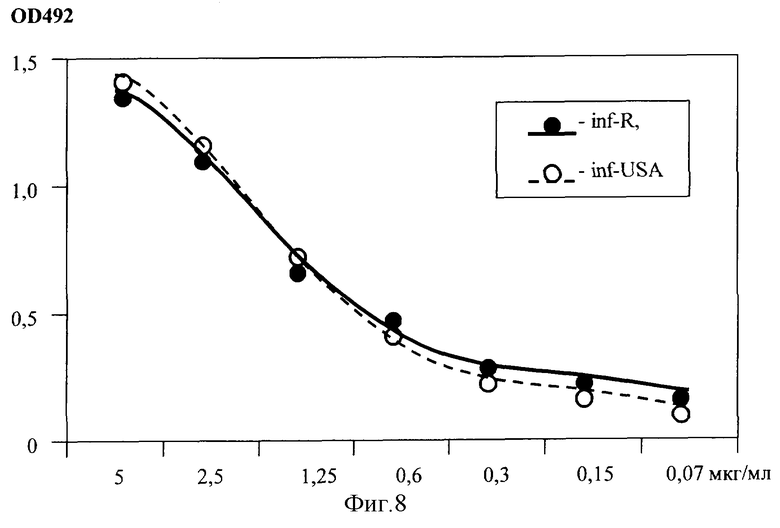
С целью идентификации рекомбинантного белка были проведены иммунологические исследования методом непрямого иммуноферментного анализа, с помощью моноклональных антител к α2-интерферону человека. В качестве стандарта был использован коммерческий препарат α2-интерферона (Интрон), производимый фирмой Шеринг-Плау (США). На фиг.8 приведены результаты экспериментов, подтверждающие полную идентичность двух белков.
Изобретение относится к области генной инженерии и биотехнологии. Путем встройки в вектор pQE30 гена α2-интерферона и инвертированного гена htpR сконструирована рекомбинантная плазмидная ДНК pASIF62. Также предложен способ биосинтеза α2-интерферона в клетках E.coli с последующей очисткой целевого продукта, заключающийся в том, что E. coli трансформируют плазмидной ДНК pASIF62, а культивирование проводят до достижения мутности 0,4-0,6 ОД, после чего в среду добавляют 0,1-0,3 мМ изопропил-b-тиогалактозида. Применение изобретения обеспечивает повышенный выход α2-интерферона. 2 с. и 2 з.п. ф-лы, 8 ил., 1 табл.

| US 5710027, 20.01.1998 | |||
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК PIF16, КОДИРУЮЩАЯ ЗРЕЛЫЙ ЛЕЙКОЦИТАРНЫЙ ИНТЕРФЕРОН α ЧЕЛОВЕКА, ШТАММ ESCHERICHIA COLI - ПРОДУЦЕНТ ЗРЕЛОГО ЛЕЙКОЦИТАРНОГО ИНТЕРФЕРОНА α ЧЕЛОВЕКА | 1992 |
|
RU2054041C1 |
| US 5391713, 21.02.1995 | |||
| US 4765903, 23.08.1988 | |||
| US 5200341, 06.04.1993 | |||
| US 4758512, 19.07.1988. | |||
Авторы
Даты
2004-06-10—Публикация
2002-10-22—Подача