Изобретение относится к области молекулярной биофармакологии, а именно к созданию способа получения препарата белка из семейства стрессовых и препарата белка из этого семейства (белок теплового шока HSP70), полученного разработанным способом. Полученные препараты белков из семейства стрессовых, например белки теплового шока, могут служить основой для создания профилактических, терапевтических и диагностических агентов при различных заболеваниях, связанных с нарушением обмена этих белков.
Белки из семейства стрессовых, например белки теплового шока (HSP), представляют собой полифункциональные белки, метаболизм которых в клетках живых организмов нарушается в ответ на действие неблагоприятных условий. Внутриклеточный уровень стрессовых белков (в том числе HSP) повышается в условиях теплового стресса, ацидоза, гипоксии или гипероксии, энергетического истощения клетки, а также при вирусных и микробных инфекциях [1]. Основными функциями белков HSP являются повышение клеточной термотолерантности, участие в ренатурации и поддержание целостности структуры клеточных белков, участие в деградации белков с нарушенной структурой, участие в процессах ассоциации-диссоциации белков, а также их транслокации через мембраны внутриклеточных компартментов и органелл [2, 3]. Важнейшими функциями белков HSP являются их способность к улучшению презентации антигена на поверхности дендритных клеток и макрофагов, а также способность выступать в роли носителей иммуногенных пептидов [4, 5, 6, а также патент РФ 2229307]. Одними из наиболее важных представителей белков HSP являются белки семейства HSP 70. В настоящее время известно более 10 представителей HSP 70 эукариот [7]. Описаны также дрожжевые (Kar 2, Ssa 1-4) и бактериальные (DnaK) белки HSP. Структура и функции HSP 70 в настоящее время активно изучаются. Молекулярная масса HSP 70 составляет ˜70 кДа; аминоконцевая часть молекулы содержит консервативный АТФазный домен (44 кДа), в карбокситерминальной части молекулы локализован субстрат-связывающий домен (˜25 кДа), обеспечивающий прочное взаимодействие шаперона с полипептидами. В отличие от большинства других стрессовых белков HSP функционируют в виде мономеров и обладают способностью к связыванию крупных пептидных фрагментов. Обеспечение эффективного источника получения высокоочищенного HSP 70 является одной из важных задач, возникающих при создании современных вакциноподобных препаратов. В связи с этим возникает необходимость разработки и использования новых технологий для получения таких белков и получения целевых продуктов с минимальным количеством примесей. В качестве основного компонента новых препаратов наиболее предпочтительным является использование HSP 70 из Mycobacterium tuberculosis, поскольку этот белок вызывает наиболее мощную стимуляцию клеточного иммунологического ответа к связанным с ним антигенным пептидам.
Рядом исследователей были разработаны продуценты для наработки рекомбинантных аналогов белков теплового шока HSP 70 [пат. США №№6,524,825; 5,919,620].
Известны также работы в области создания противоопухолевых препаратов на основе гибридных, слитых и других белков HSP. Например, в опубликованной заявке на изобретение РФ №2003101965/14, опубл. 07.2004 г., описан способ лечения заболеваний, связанных с вирусом папилломы человека (бородавки, рак шейки матки и прямой кишки и т.д.) с помощью композиции, содержащей гибридный белок, включающий микобактериальный белок теплового шока (HSP 65 или HSP 70 из Mycobacterium bovis) и белок вируса палилломы. Лечение может осуществляться либо путем введения субъекту рекомбинантного гибридного белка, либо путем введения нуклеиновой кислоты, кодирующей гибридный белок, которая содержится в вирусном векторе.
Наиболее близкой по технической сущности является разработка, где описана рекомбинантная ДНК и ее штамм-продуцент Е.coli, которые способны обеспечить получение рекомбинантного микобактериального HSP 70 в виде конъюгата с белком р24 вируса иммунодефицита человека. По известному способу экспрессия HSP 70 осуществляется в виде химерного белка с р24 [8].
Однако в данной работе решалась узкая задача - получение химерного белка с определенными свойствами, который не может служить компонентом для других вакцинных препаратов.
Технической задачей настоящего изобретения является разработка универсального способа получения белка из семейства стрессовых в препаративных количествах и высокоочищенных для использования в составе вакциноподобных препаратов.
Техническая задача достигается тем, что разработан способ получения препарата белка из семейства стрессовых (белка теплового шока) путем экспрессии гена такого белка в клетках E.coli с последующим выделением, рефолдингом и очисткой, отличающийся тем, что экспрессию гена осуществляют в составе векторной кДНК, содержащей Т7 промотор, ген устойчивости к канамицину, репликативный ориджин pUC ori, и ген, кодирующий lac-индуктор, векторную ДНК культивируют в составе клеток E.coli BL21 в питательной среде с добавлением канамицина (100 мкг/мл) и глюкозы (0.2%) до уровня мутности 0,5-0,6 OD600, в среду добавляют 0.2 мМ изопропил бета-D-тиогалактозид (ИПТГ) и продолжают культивировать в течение 1-3 часов до накопления конечного продукта, а очистку конечного продукта осуществляют методом анионообменной хроматографии. В способе используют векторную кДНК любого гена, кодирующего белок из семейства стрессовых белков: HSP 100-200; HSP 100; HSP 90; Lon; HSP 70; HSP 60; TF 55; HSP 40; FKBP; циклофилин; HPS 20-30; CIpP; GrpE; HSP 10; убиквитин; калнексин. ДНК гена из семейства стрессовых белков в вектор операбельно встраивают между сайтами рестриктаз ВатН I и Hind III. При этом встроенная кДНК каждого из используемых белков может быть модифицирована лидерной последовательностью, кодирующей 6 гистидиновых остатков. Разработанный способ может быть, в частности, использован для получения препарата из семейства стрессовых белков - белка теплового шока HSP70.
Изобретение поясняется некоторьми примерами.
Пример 1. Получение препарата белка из семейства стрессовых - белка HSP 40.
Изобретательской задачей является обеспечение высокого выхода и упрощение процедуры получения биологически активного HSP 40.
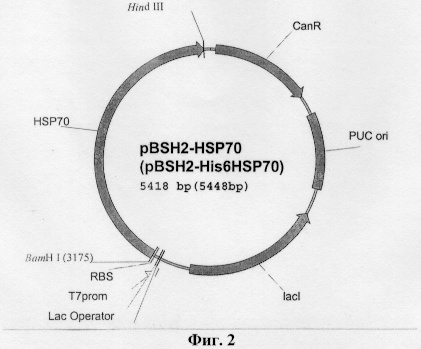
Для решения поставленной задачи разработана рекомбинантная плазмидная ДНК pBSH2-HSP40, кодирующая синтез HSP 40, которая состоит из следующих элементов: кДНК гена HSP 40 под контролем Т7 промотора, гена устойчивости к канамицину, репликативного ориджина pUC ori, гена, кодирующего lac-индуктор, и последовательностей, необходимых для успешного начала трансляции белка в клетках Е.coli.
В качестве экспрессионной системы нами взята система, применяемая в векторах рЕТ. Разработанный нами вектор pBSH2-HSP40 несет ген белка HSP40 под контролем Т7 промотора, который может быть транскрибирован только Т7 РНК-полимеразой. Ген Т7 полимеразы должен быть расположен в составе бактериального генома штамма под контролем lac-промотора, например, как в штамме BL21. Т.е. транскрипция целевых генов, находящихся под контролем Т7 промотора, возможна только после индукции lac-промотора изопропил-бета-D-тиогалактозидом (ИПТГ). В состав вектора входит копия гена lac I, кодирующего lac-репрессор. lac оператор находится между промотором Т7 и кодирующей частью гена HSP 40. lac репрессор супрессирует базальную экспрессию белка в отсутствие индуктора ИПТГ. Связывание индуктора с репрессорной молекулой нарушает ее взаимодействие с операторным участком, делая возможным посадку на этот участок РНК-полимеразы с последующей транскрипцией.
Данный вектор также может быть использован для экспрессии других рекомбинантных белков.
Рекомбинантная плазмидная ДНК может содержать последовательность, кодирующую 6 гистидиновых остатков, и сайт узнавания энтерокиназой, связанный с геном HSP 40 (рекомбинантная плазмидная ДНК pBSH2-His6HSP40).
Плазмидная ДНК применяется в способе получения HSP40 путем экспрессии его гена в составе рекомбинантной ДНК в Е.coli, отличием которого является то, что экспрессию осуществляют в рекомбинантной плазмиде pBSH2-HSP40 или pBSH2-His6HSP40 в ростовой среде до ее мутности 0,4-0,6 OD, после чего в нее добавляют 0,1-0,3 мМ ИПТГ - индуктора lac-промотора - и экспрессию продолжают под контролем индуцированного lac-промотора рекомбинантной плазмиды.
Непосредственно связанным с этим изобретением является описание методов и способов, которыми HSP 40, содержащийся как главный компонент во внутриклеточных тельцах экспрессионных систем - клеток бактерий, может быть переведен в растворимое состояние, после чего очищен и с помощью рефолдинга возвращен к нативной структуре, благодаря которой реализуется его биологическая активность.
После стадии ренатурации (рефолдинга) очистку целевого продукта, полученного в плазмидной ДНК pBSH2-HSP40, осуществляют методом аффинной хроматографии на колонке с АТФ-агарозой. Дополнительную очистку целевого продукта осуществляют с помощью анионообменной хроматографии с помощью системы FPLC. Очистку целевого продукта, полученного в плазмидной ДНК pBSH2-His6HSP40, осуществляют в одну стадию методом катионообменной хроматографии на агарозном носителе.
Использование в конструкции pBSH2-His6HSP40 лидерной последовательности, кодирующей шесть гистидиновых остатков, позволяет обеспечить надежную экспрессию слитого с ней HSP 40, отсутствие необходимых в таких случаях точечных замен для адаптации к аппарату биосинтеза белка клетки-хозяина, упрощение конечного выделения и очистки слитого белка. Присутствие гистидиновой последовательности не создает препятствий для корректной ренатурации зрелого белка.
Описанный способ может быть использован при получении других белков семейства стрессовых путем культивирования клеток Е.coli, при этом используют векторную кДНК соответствующего гена, кодирующего получаемый белок из семейства стрессовых: HSP 100-200; HSP 100; HSP 90; Lon; HSP 70; HSP 60; TF 55; HSP 40; FKBP; циклофилин; HPS 20-30; ClpP; GrpE; HSP 10; убиквитин; калнексин. Векторную кДНК гена из семейства стрессовых белков в вектор операбельно встраивают между сайтами рестриктаз BamH I и Hind III.
Другой технической задачей настоящего изобретения является разработка препарата белка HSP70, полученного нашим способом, более высокоочищенного, упрощенным и доступным способом.
Техническая задача решается тем, что разработан препарат стрессового белка (белка теплового шока HSP70), представляющий собой рекомбинантный белок HSP с М.м. около 70 кДа, полученный с помощью заявленного способа из трансформированных плазмидным вектором клеток - хозяев E.coli с последующим выделением, рефолдингом и очисткой, отличающийся тем, что препарат выделен после инкубации клеток E.coli BL21 (D3) на ростовой среде LB в течение 12 ч при 37°С с добавлением канамицина (100 мкг/мл) и глюкозы (0.2%) до уровня мутности 0,5-0,6 OD600, при этом трансформированная клетка содержит плазмидную ДНК pBSH2-HSP70, несущую кДНК гена белка теплового шока HSP70, которая характеризуется размером 5118 п.н. и представляет собой вектор pBSH2, содержащий Т7 промотор, ген устойчивости к канамицину, репликативный ориджин pUC ori, ген, кодирующий lac-индуктор, а конечный белковый препарат характеризуется чистотой не менее 98%. Встроенная рекомбинантная плазмидная ДНК pBSH2-HSP70 дополнительно может быть модифицирована лидерной последовательностью, кодирующей 6 гистидиновых остатков. При использовании рекомбинантной плазмиды pBSH2-HSP70 очистку конечного продукта осуществляют методом аффинной хроматографии на колонке с АТФ-агарозой, с последующей очисткой методом анионообменной хроматографии. При использовании рекомбинантной плазмиды pBSH2-HSP70 с лидерной последовательностью, кодирующей 6 гистидиновых остатков, очистку осуществляют в одну стадию методом катионообменной хроматографии на агарозном носителе. Подробнее получение и свойства препарата описаны в примерах.
Пример 2. Клонирование гена HSP 70.
В качестве источника гена HSP 70 была использована кДНК библиотека генов М.tuberculosis. Ген HSP 70 М.tuberculosis был выделен методом амплификации с помощью следующих праймеров:
HSP70-BamH 5'
GGATCCATGGCTCGTGCGGTCGGGATCGACCTCGGGACCACCA
HSPTO-Hind 5'
ACAAAGCTTATTATCACTTGGCCTCCCGGCCGTCGTCGACCAC
His6HSP70-Bam 5'
ACAGGATCCATGCATCATCATCACCATCATGATGATGATAAAGCTCGTGCGGTCG
GGATCGACCTCGGGACCACCA
Праймер His6HSP-BamH 5' предназначен для синтеза гена HSP 70 с лидерной последовательностью 6-His и эпитопом узнавания энтерокиназой.
Подчеркнутые последовательности вносят сайты рестрикции Bam HI и Hind III для клонирования в вектор для секвенирования последовательности гена HSP70.
Фрагмент был обработан рестриктазами BamHI -+- Hind III и клонирован между BamHI и Hind III сайтами вектора pBS+.
Фрагмент, синтезированный с помощью праймеров HSP-70_HIND и 6-HIS HSP70 ВАМН содержит в себе лидерную последовательность, кодирующую 6-His, и эпитоп узнавания энтерокиназой. Его обработали рестриктазами HIND3 и BAMHI, и клонировали в вектор pBS+, между сайтами рестрикции HIND3 и BAMHI. Полученные клоны были проанализированы с помощью автоматического секвенатора.
Была получена следующая нуклеотидная последовательность, соответствующая гену HSP 70 (фиг.1). Последовательность вставили по сайтам рестрикции ВатН I и Hind III в вектор pBSH. Полученный вектор назвали pBSH2-HSP70 (pBSH2-His6HSP70, в случае с 6-His) (фиг.2).
Индукция синтеза HSP70 оценивалась в 10 мл ИПТГ-индуцированных культур (выращивание до OD600 0.5, внесение ИПТГ до 0.2 мМ, затем 3 часа при 37°С на качалке). Продукция белка ожидаемого размера проверена по SDS-PAGE.
Для экспрессии рекомбинантных белков был использован штамм Е.coli BL21(DE3).
Пример 3. Синтез HSP 70 в штаммах Е.coli.
Уровень синтеза HSP 70 определяли в штамме Е.coli, содержащем плазмиды pBSH2-HSP70 или pBSH2-His6HSP70. В качестве контроля использовали штамм Е.coli с рекомбинантной плазмидой рВSН2, не несущей гена HSP 70. Клетки Е.coli штамма BL21(DE3) трансформировали плазмидой pBSH2-HSP70, либо плазмидой pBSH2-His6HSP70 и выращивали в течение 12 ч при 37°С в среде LB с добавлением канамицина (100 мкг/мл) и глюкозы (0.2%). Затем разбавляли культуру в 25 раз свежей средой LB с канамицином и подращивали 2-3 ч до плотности OD600=0.5, затем вносили ИПТГ до конечной концентрации 0.2 мМ для индукции синтеза HSP 70. Растили еще 3 часа, центрифугировали культуру при 5 тыс. об/мин в течение 10 мин, супернатант отбрасывали.
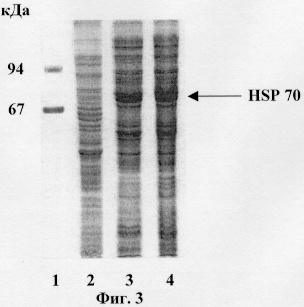
Как следует из данных, представленных на фиг.3, клетки Е.coli, содержащие плазмиды pBSH2-HSP70 и pBSH2-His6HSP70, поддерживают экспрессию HSP 70. На фиг.3 представлены результаты электрофоретического разделения белков тотальных клеточных лизатов штаммов Е.coli в ДСН-ПААГ,
где: 1 - маркеры молекулярной массы;
2 - штамм Е.coli BL21(DE3), не несущий плазмиды pBSH2-HSP70 или pBSH2-His6HSP70;
3 - штамм Е.coli, содержащий рекомбинантную плазмиду pBSH2-HSP70;
4 - штамм Е.coli, содержащий рекомбинантную плазмиду pBSH2-His6HSP70.
Пример 4. Очистка препарата HSP 70 из клеток Е.coli, содержащих плазмиду pBSH2-HSP70.
Осадок клеток, полученный из культуры Е.coli, ресуспендировали в буфере для обработки ультразвуком (50 мМ трис-HCl, рН 8.0, 20 мМ ЭДТА), после чего добавляли лизоцим до конечной концентрации 50 мкг/мл и инкубировали в этом буфере на льду в течение 30 мин. Затем обработанные лизоцимом клетки подвергали воздействию ультразвука с помощью ультразвукового дезинтегратора в течение 1 мин при 0°С. Полученную суспензию центрифугировали в течение 5 мин при 10 000 об/мин. Далее проводили процедуру отмывки телец включения. Для этого осадок ресуспендировали в буфере, содержащем 20 мМ трис-HCl, рН 8.0, 2 мМ ЭДТА, 0.1 М NaCl, 0.5% Нонидет Р40, и подвергали действию ультразвука, как описано выше, с последующим центрифугированием (10000 об/мин, 5 мин). Процедуру отмывки телец включения повторяли еще два раза. Полученный препарат телец включения HSP 70 был солюбилизирован в буфере, содержащем 10 мМ трис-HCl, 10 мМ ЭДТА, 5М гуанидинхлорид. Ренатурацию целевого белка проводили последовательным диализом препарата против буфера для солюбилизации, содержащего гуанидинхлорид в убывающих концентрациях: 2 М, 1 М, 0.5 М, 0.25 М. Последнюю стадию диализа проводили против буфера, содержащего 100 мМ трис-HCl, рН 7.5,100 мМ MgCl2, 0.5 М ЭДТА.
Далее проводили аффинную хроматографию на колонке с АТФ-агарозой ("Sigma"), уравновешенной буфером, содержащим 100 мМ трис-HCl, рН 7.5, 10 мМ MgCl2, 0.1 М NaCl, 0.1% Нонидет Р40.
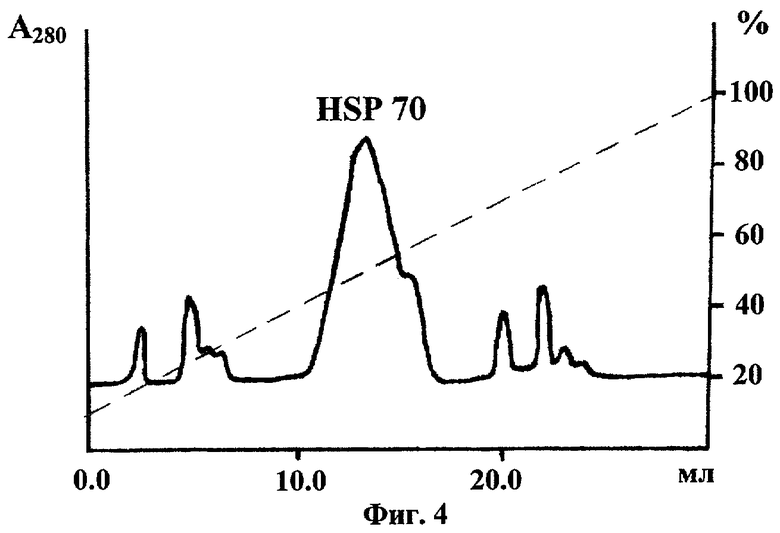
После нанесения препарата колонку промывали буфером для уравновешивания, содержащим 0.5 М NaCl, а затем тем же буфером, содержащим 100 мМ NaCl и 5 мМ АТФ. Элюцию белка проводили буфером для уравновешивания колонки, содержащим 30 мМ АТФ. Фракции анализировали с помощью ДСН-электрофореза. Содержащие целевой белок фракции объединяли и диализировали против буфера, содержащего 20 мМ трис-HCl, рН 8.0, 1 мМ MgCl2. Дальнейшую очистку белка проводили с помощью высокоэффективной хроматографии при умеренном давлении (FPLC) на анионообменной колонке MonoQ HR 5/50 ("Pharmacia"), уравновешенной буфером, содержащим 20 мМ трис-HCl, рН 8.0, 2 мМ MgCl2. После нанесения препарата колонку промывали тем же буфером, дополнительно содержащим 50 мМ NaCl. Целевой белок элюировали линейньм градиентом NaCl (50-500 мМ) в том же буфере. Профиль элюции HSP 70 с колонки MonoQ представлен на фиг.4. Наличие во фракциях целевого белка и степень его чистоты определяли с помощью ДСН-электрофореза. Фракции, содержащие целевой белок, объединяли, диализировали против PBS и хранили при -70°С. После заключительной стадии очистки был получен белок высокой степени чистоты (см. фиг.5). Выход белка составил ˜10 мг белка HSP 70 из 1 л клеточной культуры.
Пример 5. Очистка препарата HSP 70 из клеток Е.coli, содержащих плазмиду pBSH2-His6HSP70.
Стадии дезинтеграции клеток и рефолдинга HSP 70 проводили, как описано в примере 3. Очистку целевого продукта, полученного в плазмидной ДНК pBSH2-His6HSP70, осуществляли методом катионообменной хроматографии на агарозном носителе. Колонку, заполненную сорбентом IDA-агарозой (объем около 1 мл), уравновешивали раствором никеля (II) сульфата, затем буфером, содержащим 10 мМ трис-HCl, рН 8.0, 6 М мочевины, 400 мМ NaCl, 10 мМ 2-меркаптоэтанола, 5 мМ имидазола. Супернатант, полученный после рефолдинга, как описано в этом разделе ранее, наносили на колонку, промывали последнюю 5-ю объемами того же буфера, затем 10-ю объемами буфера, содержащего 10 мМ трис-HCl, рН 8.0, 6 М мочевины, 400 мМ NaCl, 10 мМ 2-меркаптоэтанола, 20 мМ имидазола. Элюцию проводили буфером, содержащим 10 мМ трис-HCl, рН 8.0, 2 М мочевину, 400 мМ NaCl, 10 мМ 2-меркаптоэтанола, 300 мМ имидазола. Наличие во фракциях целевого белка и степень его чистоты определяли с помощью ДСН-электрофореза (см. фиг.5). Фракции, содержащие HSP 70, объединяли и диализировали против PBS и хранили при -70°С.
Уровень продукции HSP 70 в клетках Е.coli, трансформированных плазмидой pBSH2-HSP70, составлял около 20 мг/л культуры.
Пример 6. Электрофоретический анализ конечных препаратов HSP 70 из М.tuberculosis.
На фиг.5 представлены данные электрофоретического анализа рекомбинантного HSP 70 в 12% полиакриламидном геле в присутствии 0.1% додецилсульфата натрия:
1 - маркеры молекулярных масс;
2 - препарат HSP 70 из штамма с плазмидой pBSH2-HSP70 после заключительной стадии очистки;
3 - препарат HSP 70 из штамма с плазмидой pBSH2-His6HSP70 после заключительной стадии очистки.
Из фиг.5 видно, что оба препарата представляют собой практически гомогенные белки (чистота более 98%) с молекулярной массой, соответствующей природному HSP 70.
Таким образом, разработан удобный, доступный универсальный способ получения рекомбинантных препаратов белка семейства стрессовых и получен препарат белка HSP70, высокоочищенный, который может быть компонентом при изготовлении вакциноподобных иммуногенных комплексных препаратов.
Литература
1. Kregel K.C., J.Appl. Physiol. 92: 2177-2186, 2002.
2. Mizzen L.A. and Welch W.J., J.Cell Biol. 106: 1105-1116, 1988.
3. Schlessinger M.J., J.Biol. Chem. 265: 12111-12114, 1990.
4. Gaston J.S.H., Clin. Exp. Immunol. 127: 1-3, 2002.
5. Khlebodarova T.M., Genetika 38: 437-452, 2002.
6. Lussow A.R. et al., Eur. J. Immunol. 21: 2297-2302, 1991.
7. Bernelli-Zazzera A. et al., Ann. N.Y.Acad. Sci. 663: 120-124, 1992.
8. Suzue К. and Young R.A., J.Immunol. 156: 873-879, 1996.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИННАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ, РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК, ОБЕСПЕЧИВАЮЩАЯ СИНТЕЗ ГИБРИДНОГО БЕЛКА, СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2316342C1 |
| ШТАММ E.coli BL21(DE3)/pET-hHSP70 - ПРОДУЦЕНТ БЕЛКА ТЕПЛОВОГО ШОКА ЧЕЛОВЕКА HSP70 | 2006 |
|
RU2333956C1 |
| ПРЕПАРАТ ЧЕЛОВЕЧЕСКОГО ЭНДОСТАТИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2278688C1 |
| БЕЛКОВОПЕПТИДНЫЙ ПРОТИВООПУХОЛЕВЫЙ КОМПОЗИТ, КЛЕТОЧНЫЙ ПРЕПАРАТ, АКТИВИРОВАННЫЙ ЭТИМ КОМПОЗИТОМ, И СПОСОБ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ОПУХОЛЕЙ | 2004 |
|
RU2283129C1 |
| ПЛАЗМИДНАЯ ДНК pBSH2EGF, КОДИРУЮЩАЯ СИНТЕЗ ЭПИДЕРМАЛЬНОГО ФАКТОРА РОСТА ЧЕЛОВЕКА, И СПОСОБ ЕГО ПОЛУЧЕНИЯ С ПОМОЩЬЮ ДАННОЙ ДНК | 2004 |
|
RU2289623C2 |
| ВАКЦИННЫЕ КОМПОЗИЦИИ, СПОСОБЫ ИХ ПРИМЕНЕНИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ МЕЛАНОМЫ И ГЕНЕТИЧЕСКИЕ КОНСТРУКЦИИ ДЛЯ ПОЛУЧЕНИЯ ДЕЙСТВУЮЩИХ КОМПОНЕНТОВ КОМПОЗИЦИИ | 2006 |
|
RU2333767C2 |
| ШТАММ БАКТЕРИЙ Escherichia coli - ПРОДУЦЕНТ БЕЛКА ТЕПЛОВОГО ШОКА 70 И СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА БЕЛКА ТЕПЛОВОГО ШОКА ЧЕЛОВЕКА | 2013 |
|
RU2564120C2 |
| КОМПОЗИЦИЯ РЕКОМБИНАНТНЫХ БЕЛКОВ, СПОСОБ ПОЛУЧЕНИЯ ТАКОЙ КОМПОЗИЦИИ, ФАРМАЦЕВТИЧЕСКИЙ НАБОР РЕАГЕНТОВ ДЛЯ ИММУНОТЕРАПИИ И ПРОФИЛАКТИЧЕСКОЙ ВАКЦИНАЦИИ ОПУХОЛЕВЫХ ЗАБОЛЕВАНИЙ АНОГЕНИТАЛЬНОЙ СФЕРЫ, СПОСОБ ИММУНОТЕРАПИИ И ПРОФИЛАКТИЧЕСКОЙ ВАКЦИНАЦИИ НА ЕГО ОСНОВЕ | 2002 |
|
RU2229307C1 |
| ВАКЦИННАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ТУБЕРКУЛЕЗНОЙ ИНФЕКЦИИ И ГЕНЕТИЧЕСКИЕ КОНСТРУКЦИИ ДЛЯ ПОЛУЧЕНИЯ ДЕЙСТВУЮЩИХ КОМПОНЕНТОВ ЭТОЙ КОМПОЗИЦИИ | 2003 |
|
RU2262351C1 |
| ПЛАЗМИДНЫЙ ВЕКТОР pE-Lc-LTP, ШТАММ БАКТЕРИИ Escherichia coli ДЛЯ ЭКСПРЕССИИ ЛИПИД-ТРАНСПОРТИРУЮЩИХ БЕЛКОВ ЧЕЧЕВИЦЫ Lens culinaris И СПОСОБ ПОЛУЧЕНИЯ УКАЗАННЫХ БЕЛКОВ | 2009 |
|
RU2415940C1 |

Изобретение относится к области молекулярной биофармакологии. Сущность изобретения составляет способ получения препарата стрессового белка (белка теплового шока) путем экспрессии гена такого белка в клетках E.coli с последующим выделением, рефолдингом и очисткой, при этом экспрессию гена осуществляют в составе векторной кДНК, содержащей Т7 промотор, ген устойчивости к канамицину, репликативный ориджин pUC ori, и ген, кодирующий lac-индуктор, векторную ДНК культивируют в составе клеток E.coli BL21 в питательной среде с добавлением канамицина (100 мкг/мл) и глюкозы (0.2%) до уровня мутности 0,5-0,6 OD600, в среду добавляют 0.2 мМ изопропил бета-D-тиогалактозид (ИПТГ) и продолжают культивировать в течение 1-3 часов до накопления конечного продукта, а очистку конечного продукта осуществляют методом анионообменной хроматографии. В способе используют векторную кДНК любого гена, кодирующего белок из семейства стрессовых белков: HSP 100-200; HSP 100; HSP 90; Lon; HSP 70; HSP 60; TF 55; HSP 40; FKBP; циклофилин; HPS 20-30; CIpP; GrpE; HSP 10; убиквитин; калнексин. Другим объектом изобретения является препарат стрессового белка (белка теплового шока HSP70), полученный вышеуказанным способом. Белок представляет собой рекомбинантный белок HSP с М.м. около 70 кДа, который выделен после инкубации клеток E.coli BL21 (D3) на ростовой среде LB в течение 12 ч при 37°С с добавлением канамицина (100 мкг/мл) и глюкозы (0.2%), инкубирован до уровня мутности 0,5-0,6 OD600, при этом трансформированная клетка содержит плазмидную ДНК pBSH2-HSP70, несущую кДНК гена белка теплового шока HSP70, которая характеризуется размером 5118 п.н. и представляет собой вектор pBSH2, содержащий Т7 промотор, ген устойчивости к канамицину, репликативный ориджин pUC ori, ген, кодирующий lac-индуктор, а конечный белковый препарат характеризуется чистотой не менее 98%. Технический результат - повышение чистоты высокоактивных стрессовых белков. 2 н. и 6 з.п. ф-лы, 5 ил.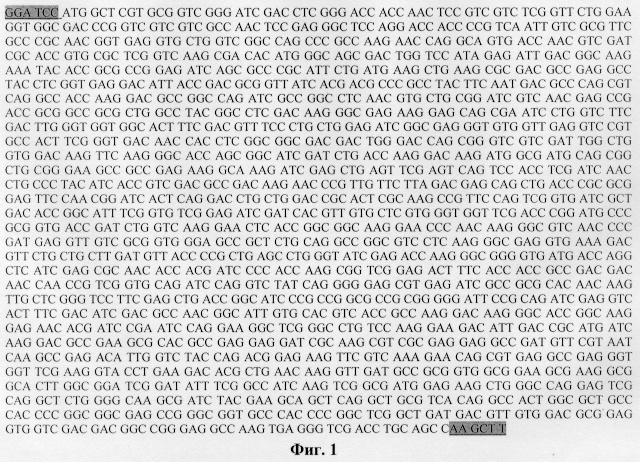
| US 6524825 А, 25.02.2003 | |||
| US 6797491 A, 28.09.2004 | |||
| COX A.L | |||
| et al | |||
| «Science», 264, 716-719, 1997. |
Авторы
Даты
2006-09-10—Публикация
2005-04-05—Подача