Изобретение относится к медицине и может быть использовано для профилактики, диагностики, лечения и иммунореабилитации контингентов “беременная женщина-плод”, роженица-плод”, “родильница-новорожденный”, “кормящая мять-грудной ребенок”, “женщина-мать-ребенок 0-15 лет”.
Аналитическая оценка основных тенденций в области материнства и младенчества позволяет констатировать ухудшение качественных показателей здоровья женщин и детей, о чем свидетельствуют высокая частота патологических родов, увеличение частоты анемии беременных, формирование акушерство-гинекологической патологии. Одновременно прослеживается ухудшение качественных показателей здоровья детей: частота патологии органов дыхания, болезней нервной системы, увеличение частоты гипоксии и асфикции в родах, болезней эндокринной системы, увеличение частоты инфекций перинатального периода, задержки внутриутробного развития плода, развитие врожденных пороков и количество детей-инвалидов, увеличение частоты развития гидроцефалии, дисгенезии почек и т.д.
Возрастает частота урогенитального хламидоза.
Недооценка роли внутриутробных инфекций и TORCH-синдрома, представленного широким спектром инфекций с вертикальным механизмом передачи от матери к плоду, включающих вирусы герпеса (HSV) 1, 2 типов, цитомегаловирусные (ЦМВ или CMV) инфекции, токсоплазмоз, уреаплазмоз, микоплазмоз и их ассоциации, серьезно влияет на качественные показатели здоровья матери и ребенка.
Рост заболеваний, передающихся половым путем, увеличение количества заболеваний перинатального периода и неврологической патологии у детей раннего возраста свидетельствуют о необходимости изучения причинно-следственных факторов, формирующих патологию матери и ребенка.
В формировании стратегии, направленной на снижение инвалидизации детей, первостепенное значение принадлежит выявлению и изучению причинно-следственных факторов, определяющих развитие патологии центральной нервной системы (ЦНС).
Заболеваемость органов мочевой системы также является актуальной проблемой, поэтому необходимо своевременное изучение и выявление причинно-следственных факторов, определяющих генез развития поражения почек в периоды закладки и формирования органов мочевыводящей системы плода.
Работами последних лет доказана инвалидизирующая роль ЦМВ-инфекции и ее значение в развитии патологии ЦНС с формированием детского церебрального паралича (ДЦП), атрофии коры головного мозга, задержки психомоторного развития и вторичной иммунологической недостаточности, иммуносупрессии с CD2 и CD4 популяциями лимфоцитов, с персистенцией ЦМВ в иммунокомпетентных клетках-моноцитах.
Недостаточно изученной остается роль вирусных ЦМВ, HSV-инфекций и урогенитальных инфекций в развитии патологии почек матери и ребенка, а также роль иммунологических факторов защиты беременных и их потомства.
Несмотря на интенсивные исследования, не раскрыты клинические, иммунологические и молекулярно-генетические критерии диагностики репликативной и латентной форм ЦМВ-инфекции у детей.
Остаются нераскрытыми вопросы о влиянии реактивированной и внутриутробно приобретенной ЦМВ-инфекции на течение вирусно-бактериально-ассоциированного поражения ЦНС у детей раннего возраста. В научной литературе не обнаружено данных по влиянию ЦМВ-инфекции на течение нейроинфекционного бактериального процесса по механизмам иммунного ответа при микстовых формах заболеваний.
Технической задачей изобретения является повышение эффективности профилактики диагностики и лечения контингентов “беременная женщина-плод”, “роженица-плод”, “родильница-новорожденный”, “кормящая мать-грудной ребенок”, “женщина-мать-ребенок 0-15 лет” с целью сохранения здоровья семьи и детей в семьях с урогенитальными инфекциями при репликативных и латентных формах ЦМВ-инфекций и урогенитальных инфекциях (хламидийной, урогенитальной, герпетической, цитомегаловирусно-хламидийно-бактериальных ассоциациях).
Анализ известных источников информации
Известен способ иммунологической оценки адаптации новорожденных детей (пат. РФ на изобретение №2152619, C 01 N 33/53), включающий исследование сыворотки венозной крови путем определения общего уровня иммуноглобулинов класса G и уровней субклассов G1 и G2 в 1-3 дни жизни.
Известен способ оценки состояния плода (пат. РФ на изобретение №2086981, G 01 N 33/53) путем исследования иммунологических показателей в крови матери, причем в сроки гестации 5-20 недель определяют абсолютное содержание нейтрофилов с рецепторами к CD3-компоненту компонента (ЕАС-РОН).
Известен способ диагностики постнатальной ЦМВ-инфекции и токсоплазменной инфекции (пат. РФ на изобретение №2077057, G 01 N 33/53) путем определения в крови детей от серопозитивных матерей специфических антител, причем у детей несколько раз определяют наличие антител против токсоплазм и ЦМВ, и если в первые шесть месяцев жизни титр антител снижается вплоть до исчезновения, а в последующие месяцы жизни вновь появляются специфические антитела, диагностируют соответствующую постнатальную инфекцию.
Известен способ диагностики перинатальных нефропатий на стадии предболезни (пат. РФ на изобретение №2110799, G 01 N 33/493), заключающийся в сборе мочи за определенный промежуток времени и последующем анализе характера хемилюминесценции мочи.
Известен способ ранней диагностики внутриутробного инфицирования (пат. РФ на изобретение №2110800, G 01 N 33/53), включающий определение уровня плацентарного альфа-1-микроглобулина (ПАМГ-1) с помощью иммуноферментного анализа сыворотки крови беременной женщины, бактериологического и цитологического исследования мазков из цервикального канала шейки матки и заднего свода влагалища и иммунологическое исследование сыворотки крови на наличие С-реактивного белка (СРБ).
Известно использование репортерской клеточной линии, несущей интегрированную плазму, для определения ЦМВ-инфекций и идентификации модуляторов экспрессии вирусного типа в биологических образцах (пат. США №5945276, С 12 Q 1/70).
Известна вириоционная цитомегалловирусная вакцина (пат. РФ №2181295, А 61 К 39/12, 39/245), содержащая инактивированную суспензию цитомегаловируса, полиоксидоний, гиалуроновую кислоту и суппозиторную основу (кондитерский жир, парафин, эмульгатор).
Известно использование аминопуриновых противовирусных соединений для лечения и профилактики латентных инфекций, вызванных вирусом герпеса (пат. РФ №2181049, А 61 К 31/521).
Известно использование противовирусных и иммуномодулированных препаратов для лечения рецидивирующих генитальных герпесов (пат. РФ №2179849, А 61 К 31/19, 35/74). Больным назначают валтрекс по 0,5 г 2 раза в сутки и неовир по 250 мг внутримышечно, 10 инъекций в два этапа.
Известен противовирусный фармацевтический состав (пат. РФ №2179851, А 61 К 31/522), содержащий в качестве активного вещества ацикловир, в качестве вспомогательных веществ спирт, воду и консервант, а также производные целлюлозы и моно- или дисахарид или их смеси.
Известен способ интегрированной оценки здоровья семьи (пат. РФ на изобретение №2122832, А 61 В 10/00), включающий формирование обследуемых контингентов, клинико-лабораторные обследования сформированных контингентов, регистрацию результатов обследования, причем контингенты формируют по маркерам TORCH-ассоциируемой патологии матери и ребенка, определяют комплекс связанных функциональным действием информационно-значимых параметров, а именно: параметров иммунодиагностики, иммунного профиля матери и ребенка, эндокринного профиля, иммуногенетической диагностики, невропатологических параметров, зарегистрированные параметры преобразуют в графическую форму, по которой определяют прогностические маркеры, проводят сравнительный анализ значений параметров, диагностируют состояние обследуемых, по результатам диагностики определяют тактику ведения сформированных контингентов (прототип).
Для решения поставленной задачи предлагается способ восстановления и сохранения здоровья семьи, включающий формирование контингентов “беременная-плод”, “роженица-плод”, “родительница-новорожденный”, “кормящая мать-грудной ребенок”, “женщина-мать-ребенок 0-15 лет”, клинико-лабораторные обследования сформированных контингентов, регистрацию результатов обследования, причем контингенты формируют по маркерам TORCH-ассоциируемой патологии матери и ребенка, определяют комплекс связанных функциональным действием информационно-значимых параметров, а именно: параметров иммунодиагностики, иммунного профиля матери и ребенка, эндокринного профиля, иммуногенетической диагностики, невропатологических параметров, зарегистрированные параметры преобразуют в графическую форму, по которой определяют прогностические маркеры, проводят сравнительный анализ значений параметров, диагностируют состояние обследуемых, по результатам диагностики определяют тактику ведения сформированных контингентов, отличающийся тем, что в клинико-лабораторные исследования вводят исследование пуповинной крови, околоплодных вод, крови и мочи, молекулярно-генетическую диагностику репликативной и латентной форм ЦМВ-инфекции у детей раннего возраста, в комплекс информационно-значимых параметров вводят дополнительно параметры диагностики полиорганной патологии при поражении вилочковой железы, почек, сердца с дополнительными поражениями органов дыхания, центральной нервной системы моно-ЦМВ, ЦМВ-хламидийно-уреаплазменной, хламидийной, уреаплазменной инфекциях, параметры диагностики полиантигенного воздействия, параметры иммунного ответа при репликативной и латентной форме ЦМВ-инфекции, определяемые по максимальной индикации ДНК - ЦВМ в моче и обнаружением в крови ДНК-ЦВМ, IgM к ЦВМ, параметры иммунного ответа у детей раннего возраста с ЦМВ-бактериальными ассоциациями с сочетанным поражением ЦНС по варианту менингоэнцефалита, параметры уровня CD23-лимфоцитов, влияющие на формирование бронхообструктивного синдрома, ассоциированного с TORCH-инфекциями у детей, параметры иммунофенотипических маркеров и цитокинового профиля у беременных женщин с хроническим пиелонефритом, в тактику ведения сформированных контингентов дополнительно вводят фамвир в качестве противовирусной терапии врожденной моно- и микстовой ЦМВ-инфекции у детей в дозе 125 мг/сут курсом 7-10 дней, в качестве комбинированной терапии при поражениях ЦСН детей вводят дополнительно цефтриаксон в дозе 100 мг/кг, но не более 4 г, один раз в день внутривенно медленно курсом 7-10 дней; в качестве адаптагенного регулятора биодинамики нормальной и патологической клетки у детей с нейроинфекцией вводят гипербарическую оксигенацию курсом 8-10 сеансов, в качестве превентивной технологии женщин с урогенитальными хламидийной и уреаплазменной инфекциями на этапах планирования и течения беременности вводят ровамицин в обычных дозах.
Для решения поставленной задачи проведена оценка клинико-иммунологических особенностей течения нейроинфекций при ЦМВ-бактериальных ассоциациях у 63 детей первого года жизни, эффективность применения в терапии цефалоспориновых препаратов III поколения и иммуноглобулинов парентерального применения II генерации, а также использование немедикаментозных методов, таких как метод гипербарической оксигенации (ГБО); выполнены клинико-иммунологические исследования у 142 детей, из них ЦМВ-хламидийно-уреаплазменая ассоциация диагностирована у 54, ЦМВ-инфекция - у 47, хламидийная - у 30, уреаплазменная - у 11. Иммунофенотипирование лимфоцитов проведено у 30 детей с определением CD3, CD4, CD8, CD19, CD23, CD16/56-антигена на проточном цитометре Facs Can наборами Becton Dickinson, уровень IgM, IдА - по G. Mancini. Этиологическая расшифровка TORCH-инфекций проведена методом ИФА с определением IgM и IgG, индикация ДНК-ЦМВ в моче и крови PCR (ПЦР), диагностика хламидий выполнена PCR в соскобах с конъюнктивы, уретры, вагины и в моче; определены особенности формирования иммунного ответа при репликативной форме ЦМВ-инфекции, при латентной форме ЦМВ-инфекции, доказана эффективность превентивных технологий для лечения женщин с урогенитальными хламидийной и уреаплазменной инфекции на этапе планирования и течения беременности ровамецином, дан анализ препаратов противовирусной терапии врожденной моно- и микстовой ЦМВ-инфекции и определено приоритетное использование в данном случае фамвира; дан анализ противовирусных и иммунотропных препаратов комплексной терапии (виферон, циклоферон, неовир, фамвир, валтрекс, цитотек, пентоглобин) при лечении очагового поражения ЦНС и определено приоритетное использование в данном случае цефтриаксона. Раскрыты варианты развития иммунологической недостаточности у детей, рожденных в семьях с микстовой, урогенитальной инфекцией. Предложена тактика лечения менингоэнцефалитов с ЦМВ-бактериальной ассоциацией комбинированной терапией препаратом III поколения (цефтриаксон) и пентоглобином, что позволило добиться снижения летальности с 38 до 8,3% в клинике, сократить сроки лечения, уменьшить тяжесть процесса и риск развития токсикоза по сравнению с традиционными методами лечения.
Назначение в комплекс иммунореабилитационной терапии баротерапии позволило добиться улучшения качественных показателей здоровья детей, перенесших менингоэнцефалит смешанной этиологии.
Доказана роль полиантигенного воздействия в развитии осложненного течения беременности с угрозой невынашиваемости у 42% обследованных женщин, анемии беременных в сроки 20 недель - у 44,6% женщин.
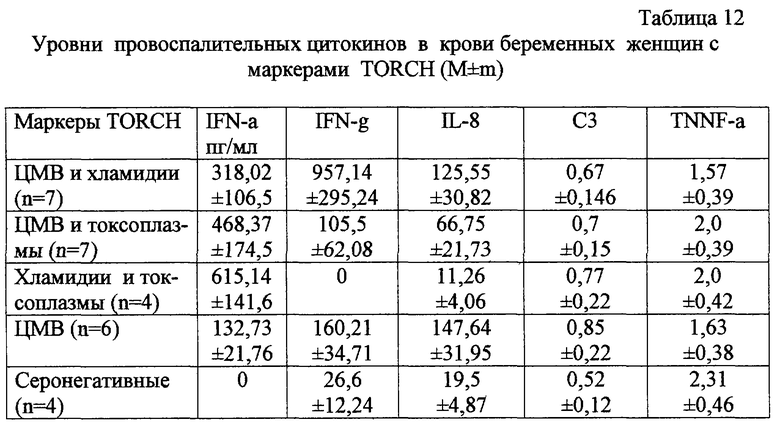
В крови беременных женщин уровень IFNα при CMMV, ЦМВ-токоплазменной инфекции превышает значение при физиологическом течении, а уровень IFNγ снижен в крови беременных с токсоплазмом.
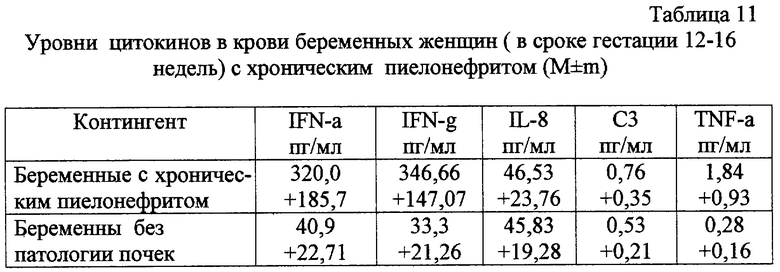
Наличие хронического пиелонефрита у беременных женщин проявляется высокими значениями IFNα (3201±85,7) IIF/мл, IINγ (435,6±147,07) и INF (1,84±0,93 пг/мл) по сравнению со значениями у женщин без патологии, что является дополнительным критерием прогноза течения беременности.
Полиантигенные воздействия у беременных увеличивают риск развития угрозы невынашивания беременности и риск развития токсикоза по сравнению с неинфицированными женщинами. У 67% матерей, родивших детей с патологией почек, регистрируется пиелонефрит, а 16% имеют врожденную патологию почек. Наличие полиантигенного воздействия у матери увеличивает в 10 раз риск развития патологии почек у детей. Сочетание почечного синдрома с гепатомегалией доказано у 50% детей с патологией почек, со спленомегалией - у 16%.
Выделены критерии прогноза внутриутробного инфицирования, риска формирования обструктивных бронхитов, пиелонефритов, анемии.
Предложены индивидуальные алгоритмы подбора противовирусных и иммунотропных препаратов на основании изучения особенностей формирования иммунного ответа по уровню сывороточных иммуноферментов Ig, A, G, M, частоте и глубине развития иммунологической недостаточности в клеточном и гуморальном звене иммунитета, фагоцитарных реакций, риску развития селективной недостаточности IgA, а также активности репликации вирусных инфекций в PCR, CMV, MSV, HCV, HBV и определения вирусных нагрузок и степени антигенности в крови и моче и характера полиорганной недостаточности, топологии поражения ЦНС.
Предлагаемый способ оптимального выбора иммунотерапии позволяет добиться стойкого иммунореабилитета.
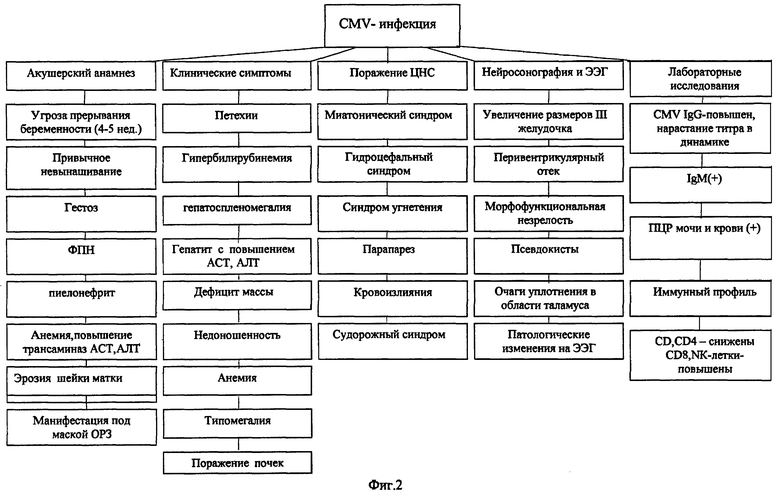
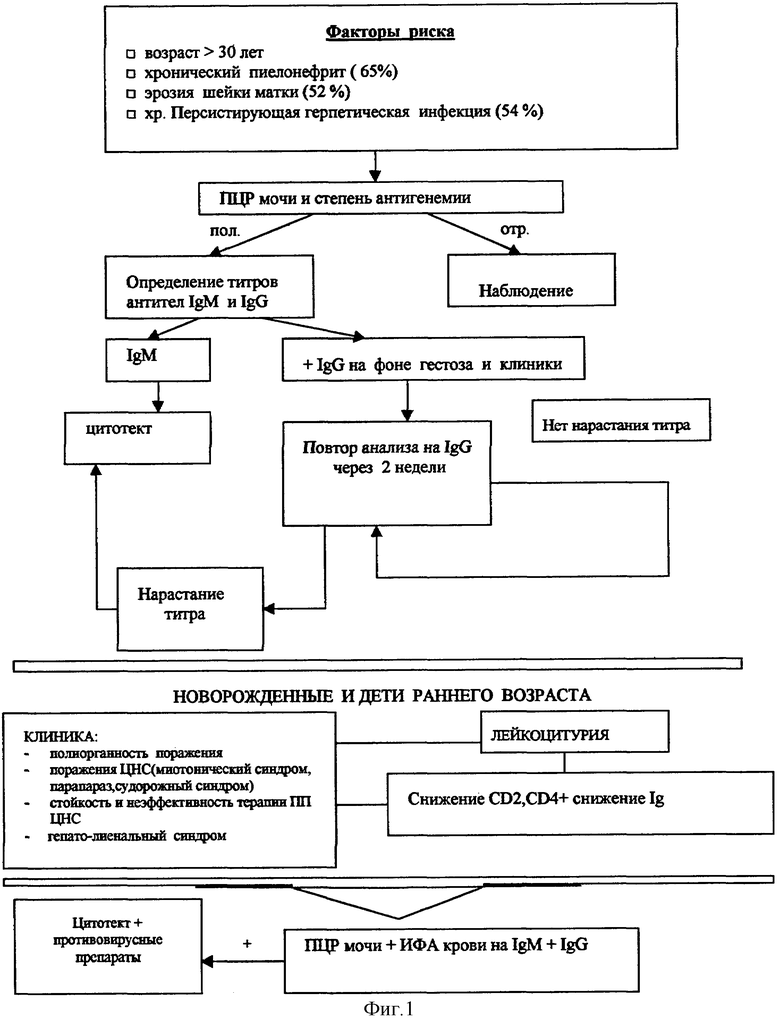
На фиг.1 представлен алгоритм ведения беременных и новорожденных с ЦМВ-инфекцией; на фиг.2 - алгоритм клинической и лабораторной диагностики врожденной ЦМВ-инфекции.
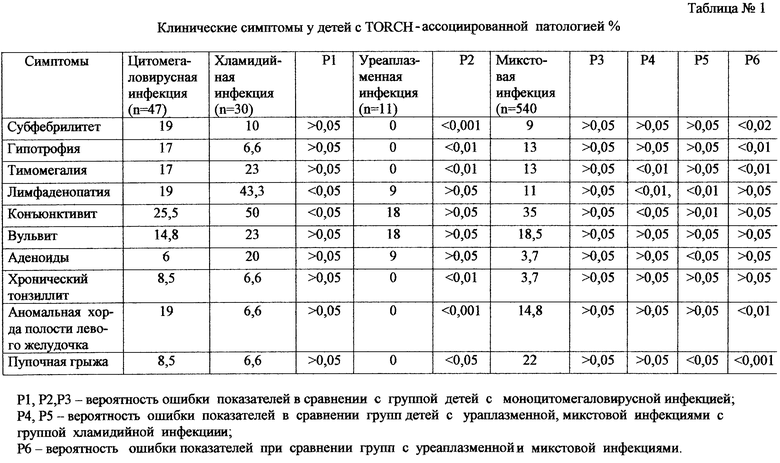
В табл.1 показаны клинические симптомы у детей с TORCH-ассоциированной патологией;
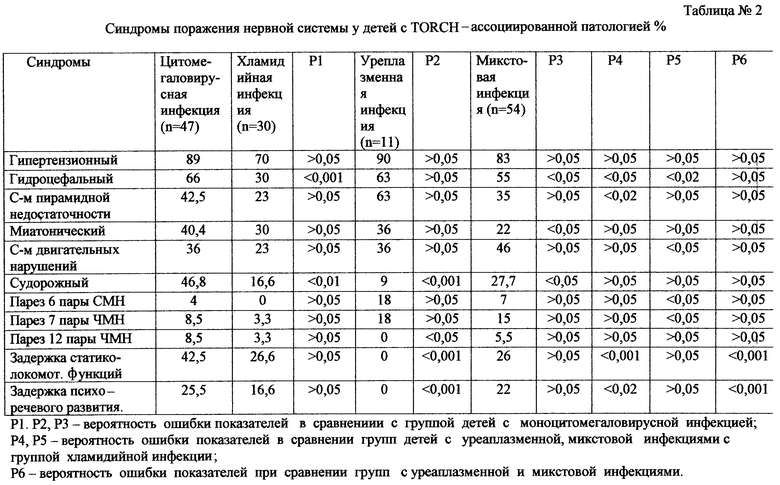
в табл.2 - синдромы поражения нервной системы у детей с TORCH-ассоциированной патологией;
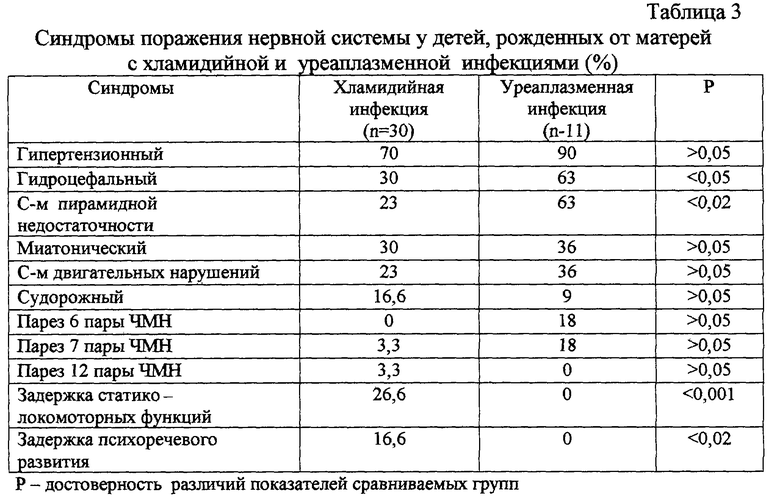
в табл.3 - синдромы поражения нервной системы у детей, рожденных от матерей с хламидийной и уреаплазменной инфекциями;
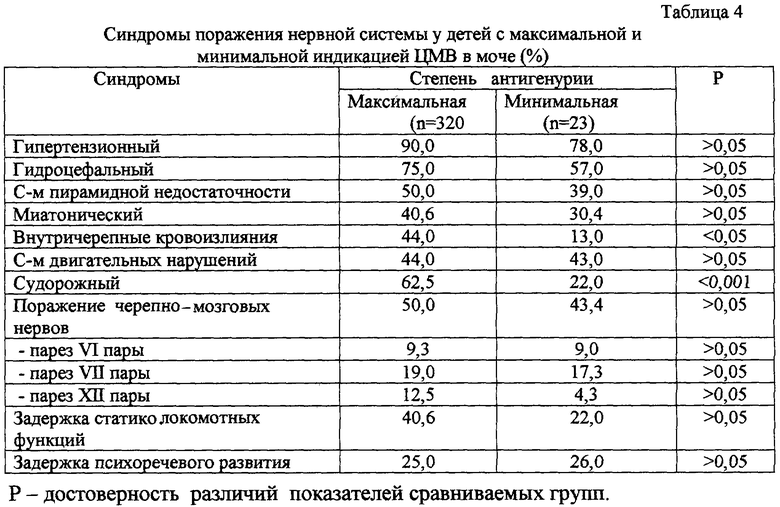
в табл.4 - синдромы поражения нервной системы у детей с максимальной и минимальной индикацией ЦМВ в моче;
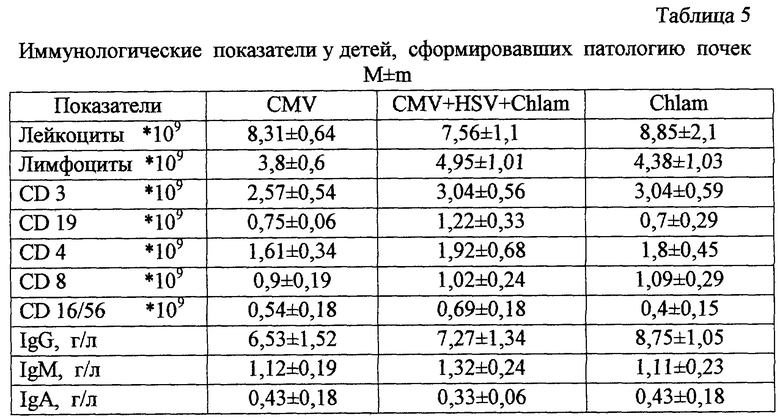
в табл.5 - иммунологические показатели у детей, сформировавших патологию почек;
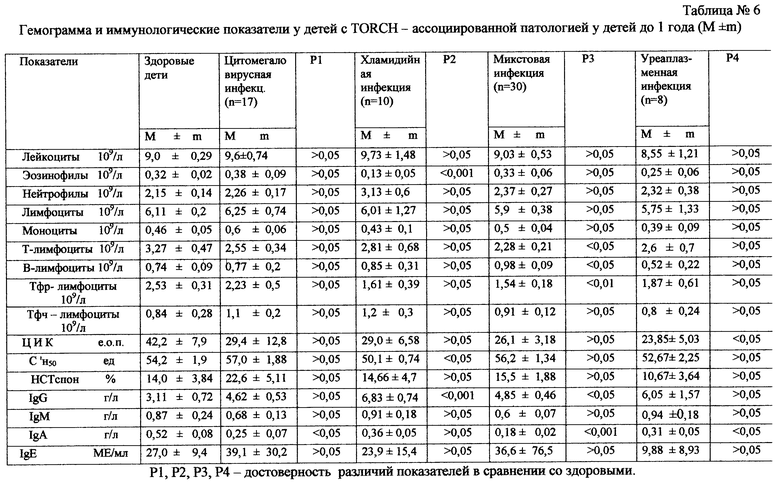
в табл.6 - гемограмма и иммунологические показатели у детей с TORCH-ассоциированной патологией у детей до 1 года;
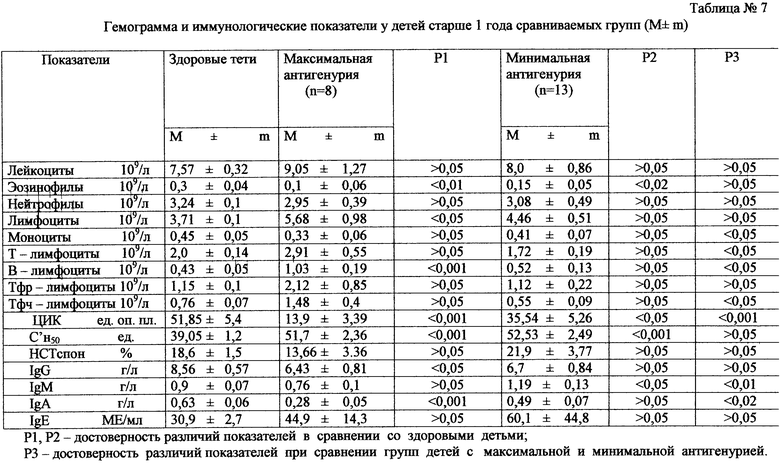
в табл.7 - то же. у детей старше 1 года;
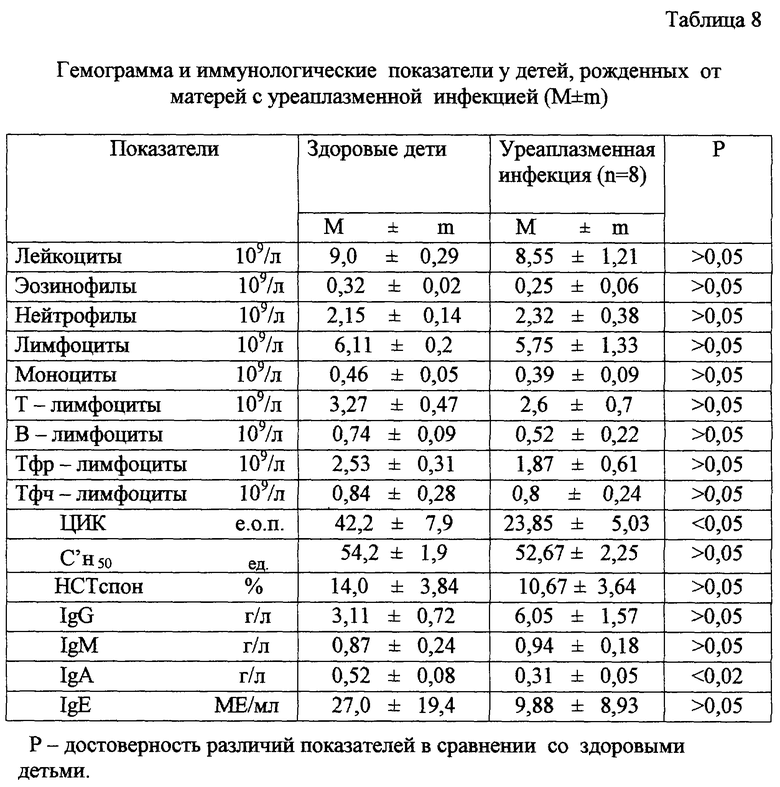
в табл.8 - гемограмма и иммунологические показатели у детей, рожденных от матерей с уреаплазменной инфекцией;
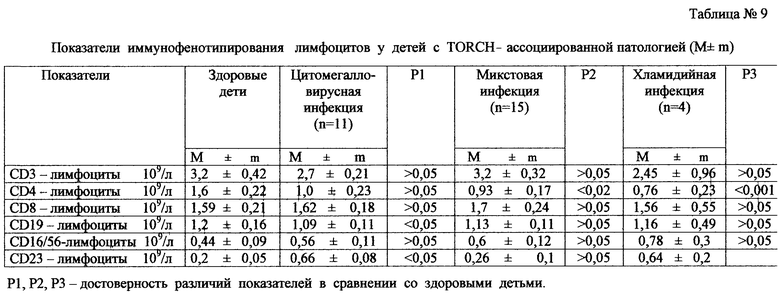
в табл.9 - показатели иммунофенотипирования лимфоцитов у детей с TORCH-ассоциируемой патологией;
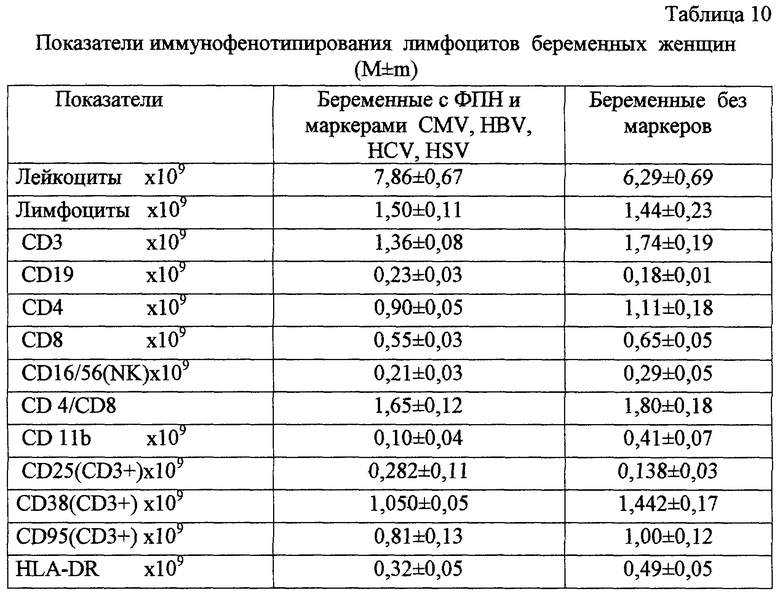
в табл.10 - то же, у беременных женщин;
в табл.11 - уровни цитокинов в крови беременных женщин в сроке гестации 12-16 недель с хроническим пиелонефритом;
в табл.12 - то же, с маркерами TORCH;
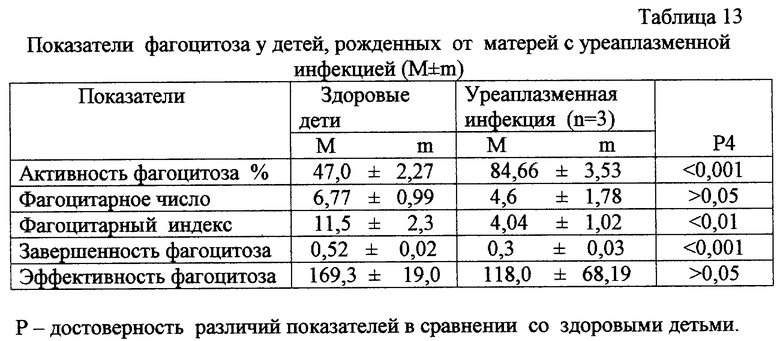
в табл.13 - показатели фагоцитоза у детей, рожденных от матерей с уреаплазменной инфекцией;
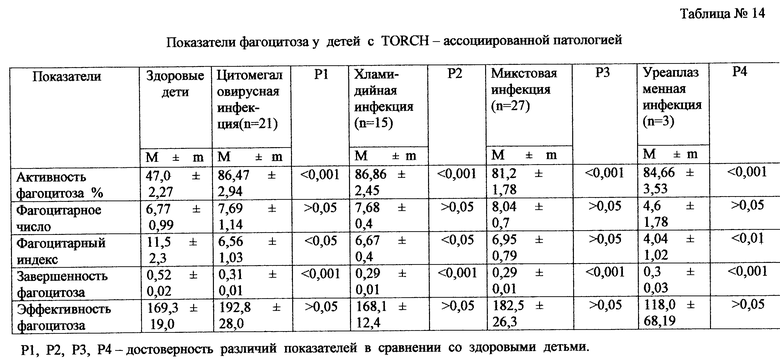
в табл.14 - показатели фатоцитоза у детей с TORCH-ассоциированной патологией;
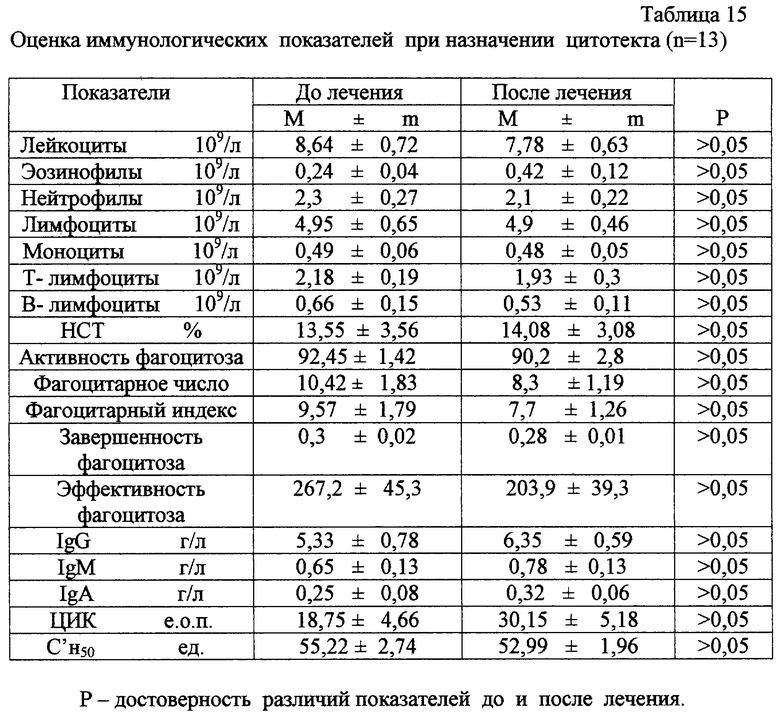
в табл.15 - оценка иммунологических показателей при назначении цитотекта;
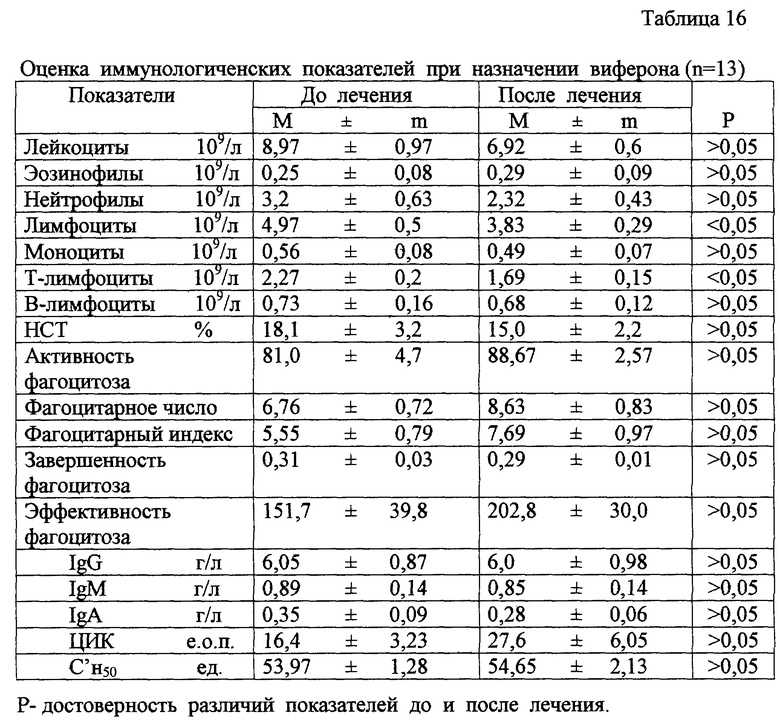
в табл.16 - оценка иммунологических показателей при назначении виферона;
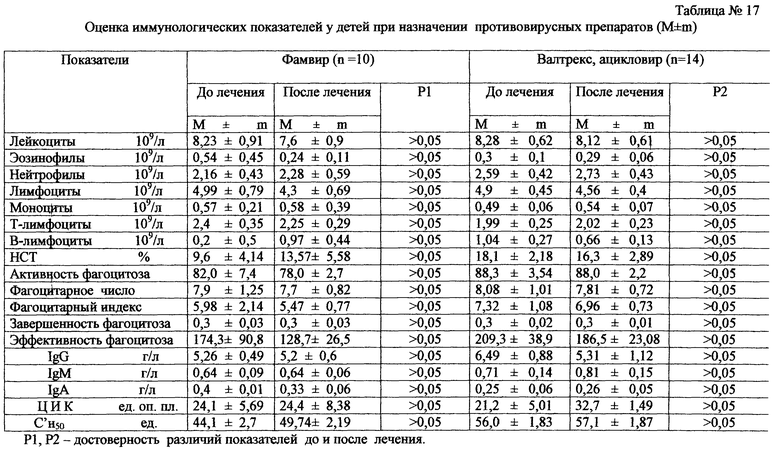
в табл.17 - оценка иммунологических показателей у детей при назначении противовирусных препаратов;
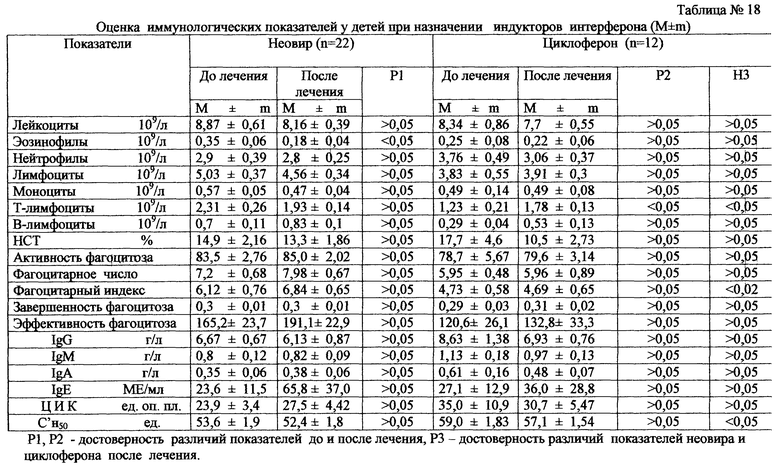
в табл.18 - оценка иммунологических показателей при назначении индукторов интерферона;
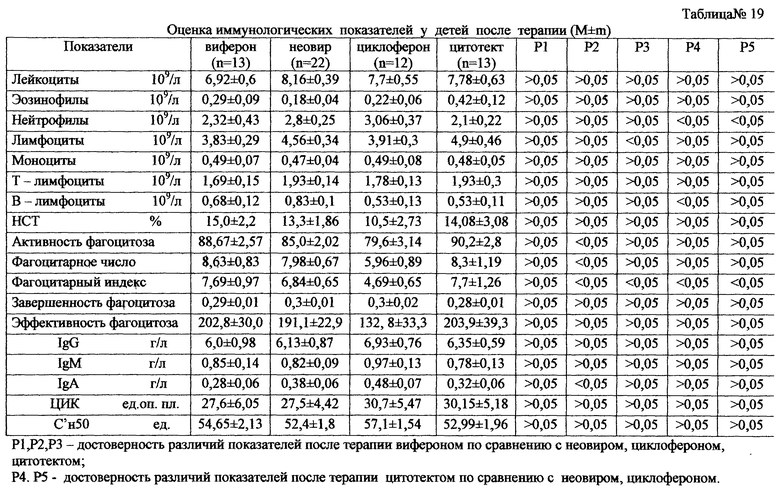
в табл.19 - оценка иммунологических показателей у детей после терапии;
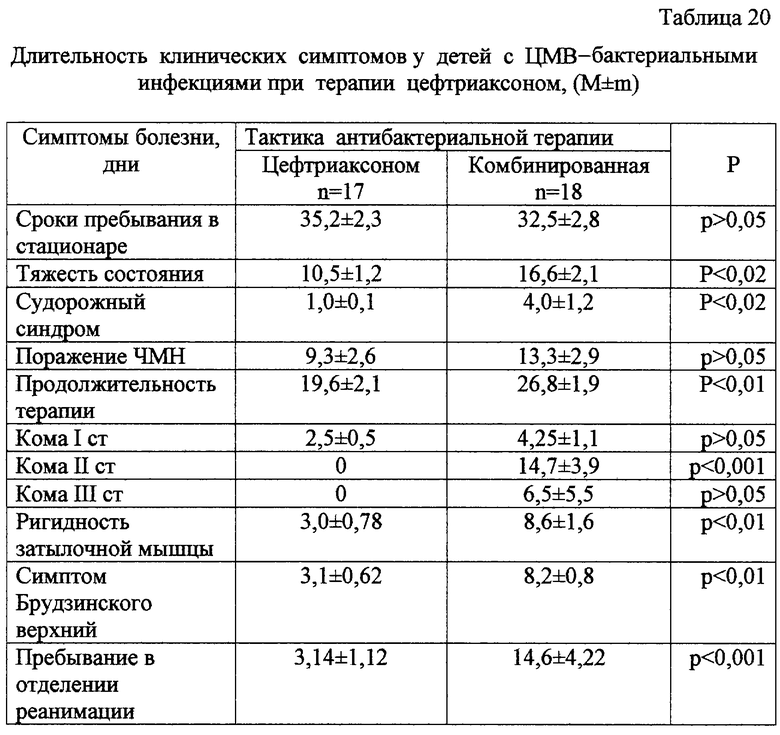
в табл.20 - длительность клинических симптомов у детей с ЦВМ-бактериальными нейроинфекциями при терапии цефтриаксоном;
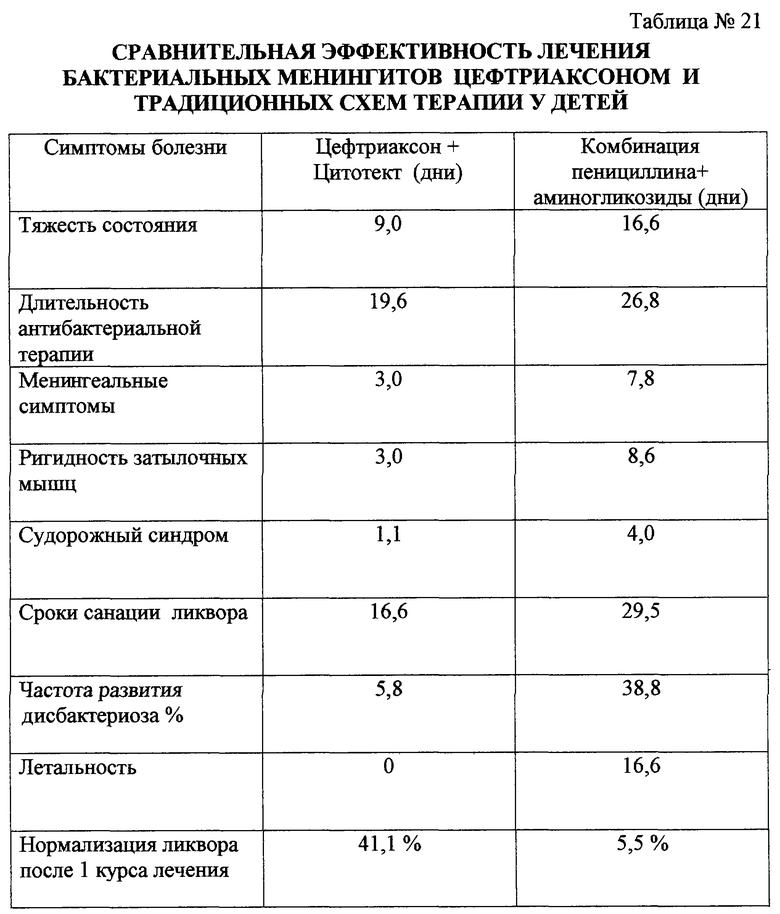
в табл.21 дана сравнительная эффективность лечения бактериальных менингитов цефтриаксоном и традиционных схем терапии детей;
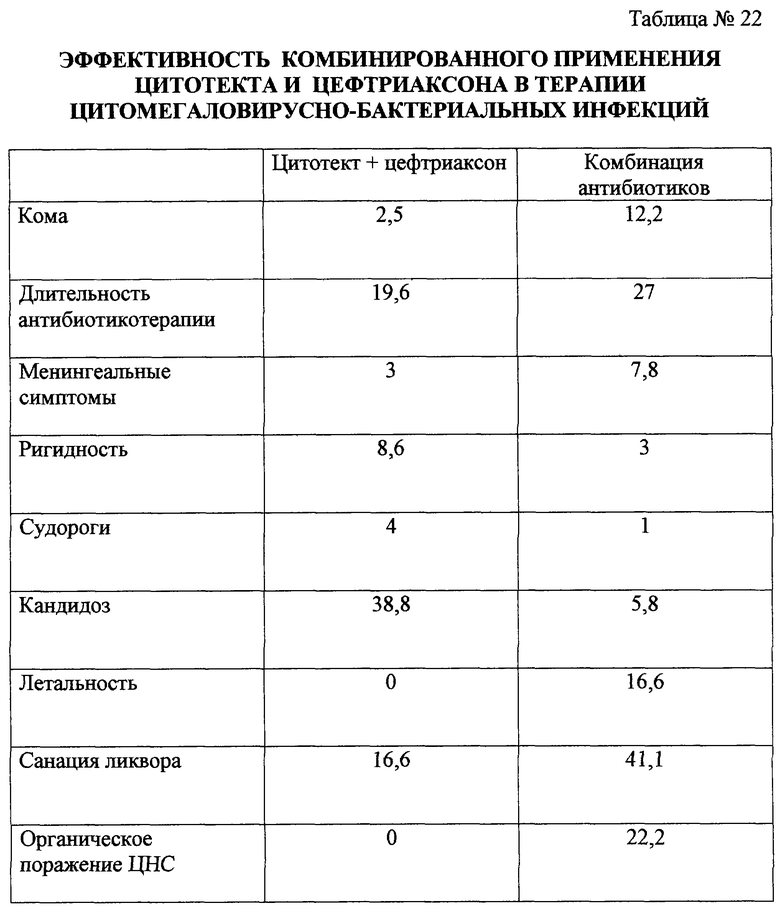
в табл.22 показана эффективность комбинированного применения цитотека и цефтриаксона в терапии ЦМВ-инфекций;
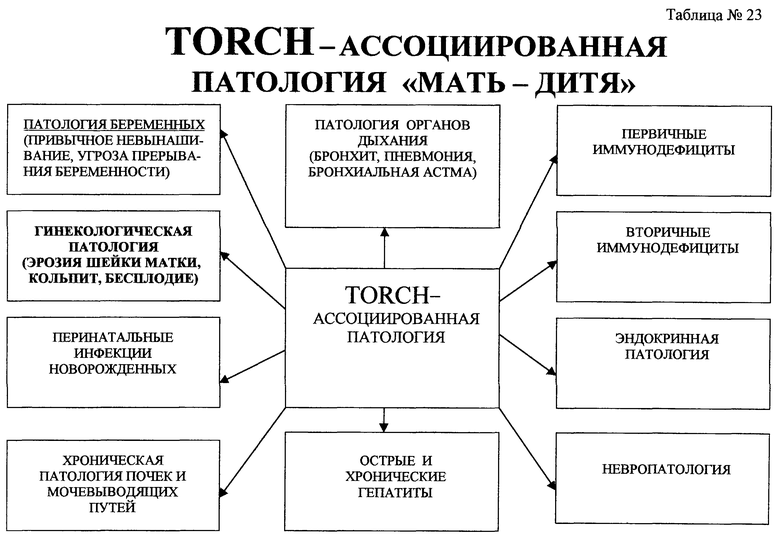
в табл.23 показана TORCH - ассоциированная патология “Мать-дитя”;
в табл.24 показана структура почек у новорожденных от матерей с ЦМВ-инфекцией;
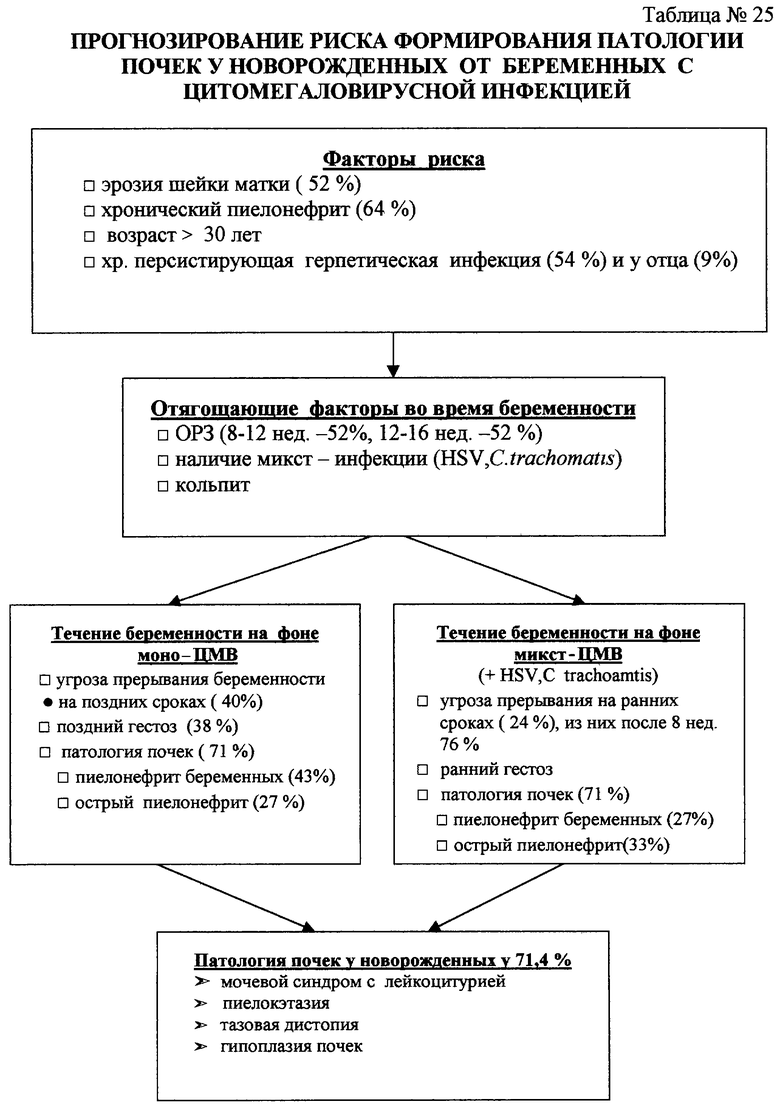
в табл.25 показано прогнозирование риска формирования патологии почек у новорожденных от беременных с ЦМВ-инфекцией.
Изучены результаты клинического и лабораторного обследований 142 детей, рожденных от матерей с урогенитальными инфекциями. Наблюдение на детьми проводилось на базе Академического медицинского центра “Семья и здоровое поколение” Уральской государственной медицинской академии (г.Екатеринбург, 1999-2001 г.) и отделения клинической иммунологии муниципального учреждения “Детская инфекционная больница” (г.Екатеринбург, 1998-2001 г.).
По этиологическому фактору выделены следующие группы пациентов: 1 - дети с цитомегаловирусно-хламидийно-уреаплазменной ассоциацией (n=54); 2 - дети, рожденные от женщин с ЦМВ-инфекцией (n=47); 3 - дети с хламидийной инфекцией (n=30); 4 - дети, рожденные от матерей с уреаплазменной инфекцией (n=11). В возрастной структуре пациентов доминировали дети до 1 года - 56% (80 чел.), дети раннего возраста от 1 до 3 лет - 26% (37 чел.), старше 3 лет - 18% (25 чел.).
В соответствии с целями и задачами всем пациентам проведено комплексное клинико-иммунологическое обследование. Длительность наблюдения и обследования пациентов в катамнезе составила: 80,9% (115 чел.) осмотрены однократно, из них в течение одного года наблюдалось 68% (78 чел.), от 1 до 3 лет - 27% (31 чел.) и более 3 лет - 5% (6 чел.).
Антитела классов IgM, IgG к питомегаловирусу выявляли иммуноферментным анализом с помощью тест-системы фирмы Hoffman La RocHe (Швейцария) на аппарате Cobas Core II.
Индикацию ДНК-вирусов выполняли молекулярно-генетическим методом диагностики с определением цитомегаловируса в моче, методом цепной полимеразной реакции (ЦПР) наборами для ЦПР. ДНК ЦМВ в сроки определяли ЦПР с помощью диагностических тест-систем Литех на ДНК-ампликаторе “Терцик” МС-2 в лаборатории молекулярной генетики УГМА. Обнаружение хламидий проводили в соскобах с конъюнктивы, уретры, вагины и в моче методом цепной полимеразной реакции наборами ПЦР.
Иммунологические исследования проводили на базе городского центра лабораторной диагностики болезней матери и ребенка (г.Екатеринбург) и НИИ ОММ.
Функциональные методы исследования представлены: нейросонографическое исследование головного мозга, ультразвуковое исследование внутренних органов с помощью аппарата “Echographe ECH 200В”. Электрофизиологические исследования составили: М-ЭХО (аппарат ЭХО-ЭС 12) и магнитно-резонансная томография в двух проекциях в режиме Т1ω1. Биохимические исследования проводили на аппарате “DR. Lange LP-700”. Исследованы: нервная система, головной мозг, почки, брюшная полость, сердце (с обнаружением дополнительных хорд в виде микро-макроаномалий), УЗИ вилочковой железы и определение размеров тимуса, поражений печени. Исследованы биологически активные жидкости: пуповинная кровь ребенка, матери, околоплодные воды беременной женщины и новорожденного, моча матери и ребенка, кровь матери и ребенка.
При оценке иммунологических показателей учитывали относительные и абсолютные значения. Абсолютные значения (Т-лимфоциты, В-лимфоциты, их субпопуляции, НСТ-спонтанный) рассчитывали через лейкоцитарную формулу общего анализа крови, взятой в день исследования иммунограммы. Результаты приведены в Международной системе единиц СИ.
Идентификацию Т-лимфоцитов, теофиллинрезистентных лимфоцитов (Тфр) проводили в реакции спонтанного розеткообразования с эритроцитами барана (Е-РОК), В-лимфоцитов - с эритроцитами мыши (М-РОК), количество Тфр вычисляли посредством вычитания числа Тфр-клеток из общего содержания Е-РОК.
Оценка поверхностных структур лимфоцитов методом иммунофенотипирования с применением моноклональных антител к фенотипическим маркерам лимфоцитов-CD-антигенам проведена у 30 детей. В работе использованы диагностические наборы фирмы Becton Dickin-Son. Окрашенные флуорохромом клетки анализировали на проточном цитометре Facs CAN по величине светорассеяния. CD3-антиген является пан-Т-клеточным маркером, антиген CD19 обнаруживается практически на всех В-клетках, антиген CD4 экспрессирован преимущественно на Т-лимфоцитах с хелперно-индукторной, a CDS - с супрессорно-цитотоксической функцией, CD 16/56 - антиген-маркер натуральных киллеров, CD23 - низкоаффинный рецептер для IgE-FcεRII, экспрессируемый на зрелых В-клетках.
Иммунофенотипирование CD23 - низкоаффинного рецептора для IgE-FcεRII выполнено у 15 детей.
Уровень иммуноглобулинов изучали методом радиальной иммунодиффузии в агаровом геле (метод G. Manchini, 1965 г.), концентрацию иммуноглобулина класса Е определяли методом иммунофлюоресценции с помощью диагностических тестовых наборов фирмы “Техносума” (Куба).
Содержание циркулирующих иммунных комплексов изучали методом прецепитации в растворе полиэтиленгликоля (ПЭГ-6000) по V.Haskova в модификации Гриневича Ю.А. (1981 г.). Результаты оценивали в единицах экстенции. Определение уровня комплементарной активности сыворотки крови проводили методом титрования по 50% гемолизу эритроцитов барана. Результаты оценивали в условных единицах гемолитической активности.
Изучение окислительно-восстановительных процессов нейтрофилов выполняли с помощью реакции восстановления нитросинего тетразолия (Маянский А.Н., 1981 г.). Для оценки поглотительной и переваривающей функции сегментоядерных нейтрофилов использовали метод изучения фагоцитоза по Берману В.М. - Славянской Е.М. в модификации Олейниковой Е.А. (1981) с оценкой активности фагоцитоза, фагоцитарного индекса, фагоцитарного числа, завершенности и эффективности фагоцитоза.
Обработку полученных данных проводили методом вариационной статистики с вычислением средних величин (М), ошибки средней (m), квадратичного отклонения (G). Показатель достоверности различий (Р) определяли по таблицам Стьюдента - Фишера. Различия считались достоверными при р<0,05. Вычисления коэффициента корреляции проводили по формуле Н. Бейли (1963 г.), уровень значимости оценивали по таблице для значений коэффициента корреляции.
Все статистические параметры вычисляли с использованием ПК IBМ-486, пакета прикладных программ Microsoft office.
Сопоставление показателей иммунитета проводили с иммунологическими показателями, представленными в методических рекомендациях “Клиническая оценка показателей периферической крови и иммунного статуса”. - Екатеринбург, УГМА, 1993 (табл.1, 2, 3, 4, 5).
Сравнение показателей фагоцитоза проводили со средними значениями показателей детей контрольной группы, результаты иммунофенотипирования лимфоцитов методом многоклональных антител сопоставлены с показателями контрольной группы здоровых детей без маркеров ЦВМ-инфекций (табл.13, 14).
В настоящее время накоплен опыт лечения цитомегаловирусной инфекции препаратами иммуноглобулинового ряда (питотект, пентаглобин), интерферонами (виферон) и индукторами интерферона (неовир, циклоферон), противовирусными препаратами (валтрекс, ацикловир), гипериммунными препаратами (цитотект), (табл.15, 16, 17, 18).
В комплексной терапии у 23 детей раннего возраста с цитомегаловирусной инфекцией и цитомегаловирусно-хламидийно-уреаплазменной ассоциацией применяли виферон, который назначали детям в возрастной дозе 2 раза в день через 12 часов ректально в течение 5 дней, двумя-тремя курсами с перерывом 5-7 дней.
На фоне терапии вифероном в гемограмме выявлено снижение уровня лимфоцитов (р<0,05), у 7,6% детей наблюдался транзиторный агранулоцитоз в течение 6 месяцев. В иммунном профиле после окончания курса отмечено снижение уровня Т-лимфоцитов по сравнению с исходными показателями (р<0,05).
В результате применения виферона в комплексной терапии больных с цитомегаловирусной и микстовой инфекцией получена положительная динамика в неврологическом статусе. Эпизоды судорог прекратились и стали регистрироваться реже у 50% детей, по данным ЭХО-энцефалоскопии дилятация 3-го желудочка уменьшилась у 43% и пульсация сосудов у 60% пациентов.
Клинически выявлено уменьшение гепатомегалии у 70% детей; купирование синдрома цитолиза - у 78%; снижение уровня аланиновой и и аспаргиновой аминотрансферазы - у 11%; по данным ультразвукового исследования (УЗИ) восстановление нормальной эхогенности печени обнаружено у 36% детей; сохранялось изменение структуры печеночной ткани у 45% детей; выявлено повышение эхогенности структуры печени у 22% детей; частота острых респираторных заболеваний (ОРЗ) снизилась на 50%.
Применением неовира и циклоферона у 42 детей выявлено:
Неовир вводили внутримышечно из расчета 6 мг/кг однократно через день, курсом 5 инъекций.
Циклоферон использовали 2,0 мл один раз в день по схеме, внутримышечно, курсом 10 инъекций.
В гемограмме при использовании неовира отмечено снижение уровня эозинофилов (р<0,05).
При использовании циклоферона в иммунном профиле выявлено достоверное повышение уровня популяции Т-лимфоцитов.
В клинике после курса терапии неовиром и циклофероном наблюдалась положительная динамика в неврологическом статусе в виде прекращения и урежения эпизодов судорог у 83%. Данные ЭХО-энцефалоскопии показали уменьшение дилятации третьего желудочка и пульсации сосудов у 30%. Уменьшение гепатомегалии выявлено у 75%. Купирование синдрома цитолиза - у 64%, снижение аланиновой и аспаргиновой аминотрансферазы - у 18%, по данным УЗИ наблюдение за эхоструктурой печеночной ткани выявило положительный результат лишь у 14%. Повышение эхогенности печени - у 22%. Частота возникновения ОРЗ снизилась на 76,5%.
Применение противовирусных препаратов у 32 детей раннего возраста позволило выявить:
При использовании ацикловира, фамвираи валтрекса при оценке иммунного профиля отсутствовали данные о влиянии указанных препаратов (таблица на иммунный профиль) у пациентов с цитомегаловирусной инфекцией и циломегалловирусно-хламидийно-уреаплазменной ассоциацией.
У пациентов с цитомегаловирусной и микстовой инфекциями отмечено клинически улучшение в неврологическом статусе на 34%. В клинике уменьшение гепатомегалии выявлено у 80% пациентов, принимавших фамвир, и у 62,5% пациентов, принимавших валтрекс и ацикловир. Купирование синдрома цитолиза и снижение уровня аланиновой и аспаргиновой аминотрансферазы после курса терапии фамвиром наблюдалось соответственно у 50 и 25% пациентов.
Применение гипериммунного иммуноглобулина направленного действия - цитотекта у 18 детей позволило выявить:
У пациентов с цитомегаловирусной инфекцией и цитомегаловирусно-хламидийно-уреаплазменной ассоциацией при оценке иммунного статуса на фоне терапии цитотектом не выявлено достоверного влияния на параметры иммунитета (табл.49).
Внутривенное введение цитотекта у 72% детей с эпилептиформными пароксизмами привело к прекращению и стойкому урежению судорог, у 28% после проведения лечения цитотектом впервые возникли судорожные пароксизмы.
В клинике уменьшение гепатомегалии наблюдалось у 60% детей, купирование синдрома цитолиза и снижение уровня аланиновой и аспаргиновой трансферазы отмечено у 66%. УЗИ эхогенности печени показало восстановление нормальной структуры печеночной ткани у 37,5% детей, динамика отсутствовала у 62,5%. Частота ОРЗ уменьшилась у 83% пациентов.
Пример 1. Иллюстрацией схемы терапии ЦМВ-инфекции с включением противовирусного препарата "Фамвир" является история болезни ребенка, дата рождения 14.10.98 г.
Ребенок рожден от второй беременности, протекавшей на фоне субфебрилитета в течение всей беременности, анемии I и II половины, гестоза с 12 недель, дрожжевого кольпита с 30 недель, хронической гипоксии плода в 38 недель. Гинекологический анамнез отягощен наличием хронического аднексита, эрозией шейки матки. Первая беременность сопровождалась субфебрилитетом, что послужило причиной для медицинского аборта. Роды первые, срок 38,5 недель, оперативные. Масса при рождении 3276 г. Оценка по шкале Апгар 6/7 баллов, искусственная вентиляция легких (ИВЛ) в течение нескольких часов. Из родильного дома на 7 сутки ребенок переведен в неврологическое отделение детской больницы, выписан через 20 дней с клиническим диагнозом: перинатальное положение центральной нервной системы (ЦНС) гипоксического генеза с нарушением мозговой гемоликвородинамики. Гипертензионно-гидроцефальный синдром. Парез VII, ХII пар слева. Экзофтальм слева. Синдром пирамидной недостаточности до стадии нижнего спастического парапареза, больше слева. Баланит. Кандидоз. Анемия смешанного генеза. Острый ринит. Дисбактериоз кишечника. Острый аллергоз. НСГ от 23.10.98: расширение межполушарной щели, дилятация 3-го желудочка, усиление пульсации сосудов. В 2,5 мес на фоне приема фенобарбитала после курса церобролизина внутримышечно, электрофореза, парафина появились приступы “замираний” до 5-6 раз в день, в связи с чем обратились к эпилептологу, был поставлен диагноз: эписиндром, назначен радедорм и обследование на внутриутробные инфекции. На фоне приема радедорма “замирания” прекратились, повторный эпизод отмечен на фоне повышения температуры в 7 месяцев. На амбулаторный прием впервые обратились в возрасте 4 мес. На момент осмотра диагностированы гипертензионный, гидроцефальный синдромы, задержка моторного развития, синдром двигательных нарушений, эписиндром, гепатоспленомегалия, дисбактериоз кишечника, паратрофия. В биохимическом анализе крови отмечен синдром цитолиза: билирубин общий - 4,0 мкмоль/л, прямой - 0, непрямой - 4,0 мкмоль/л, тимоловая проба - 2,1 ед., АЛТ -58,8 ед./л, ACT - 68,9 ед./л. УЗИ органов брюшной полости показало повышение эхогенности печени. ЯМРТ показало: очаговых изменений в белом веществе мозга не выявлено, легкая наружная гидроцефалия. ЭХО-ЭС показало: умеренная внутричерепная гипертензия со значительным расширением 3-го желудочка. УЗИ тимуса: гипертензия тимуса II степени. В крови методом ПЦР обнаружен геном ЦМВ, в моче - геном ЦМВ +++++, серологическое исследование крови методом ИФА показало: IgM к ЦВМ не обнаружены. OAK: Нв - 116 г/л, ЭР - 3,6·1012/л, лейкоциты - 10,2·109/л, эозинофилы - 1,43·109/л, нейтрофилы - 1,73·109/л, лимфоциты - 6,22·109/л, моноциты - 0,82·109/л. Иммунограмма: Е-РОЛ - 2,426·109/л, М-РОЛ-0,5·109/л, НСТ - 3%, активность фагоцитоза - 88%, фагоцитарное число - 4,86, фагоцитарный индекс - 4,28, завершенность фагоцитоза - 0,26, эффективность фагоцитоза - 98, IgG - 5,5 г/л, IgM - 0,3 г/л, IgA - 0,2 г/д, ЦИК - 14 ед., CH50 - 54,2 ед.оп.пл.
Установлен клинический диагноз: внутриутробная ЦМВ-инфекция, генерализованная: поражение ЦНС в виде гипертензионного, гидроцефального синдромов, эписиндрома, синдрома двигательных нарушений, поражения III пары черепно-мозговых нервов, гепатит, дисбактериоз кишечника, паратрофия, репликативная форма, хроническое течение. Тимомегалия. Вторичная иммунная недостаточность с недостаточностью клеточного иммунитета, нарушение антителопродукции с дефектом фагоцитарной системы.
В комплекс патогенетической терапии ЦМВ-инфекции был включен противовирусный препарат "Фамвир" в дозе 125 мг/сут, 7 дней.
Клинический осмотр после указанной терапии показал стойкое исчезновение эпипароксизмов, анизокории, восстановление статиколокомоторных функций (стал самостоятельно сидеть), сокращение размеров печени и селезенки. В биохимическом анализе крови отмечена нормализация уровня трансминад, ACT - 27,94, АЛТ - 17,46, билирубин общий 05,0 мкмоль/л, прямой - 0, непрямой - 5,0 моль/л, тимоловая проба - 3,4 ед., УЗИ органов брюшной полости: эхоструктура печени однородная, обычная, УЗИ тимуса: органической патологии не выявлено, УЗИ сердца: аномальная хорда левого желудочка (апикальная косая). В крови методом ПЦР: геном ЦМВ не обнаружен, в моче методом ПЦР: уменьшилась антигенурия - геном ЦМВ ++++, серологическое исследование крови методом ИФА: IgG к ЦМВ - 0,9 (отр.), OAK: Нв - 115 г/л, эр - 3,67·1012/л, лейкоциты - 114·109/л, эозинофилы - 0,456·109/л, нейтрофилы - 3,99·109/л, лимфоциты - 6,27·109/л, моноциты - 0,684·109/л, иммунограмма: Е-РОЛ - 2,13·109/л, М-РОЛ - 1,06·109/л, НСТ - 33%, активность фагоцитоза - 76%, фагоцитарное число - 8,13, фагоцитарный индекс - 6,18, завершенность фагоцитоза - 0,28, эффективность фагоцитоза - 132, IgG - 5,4 г/л, IgM - 0,6 г/л, IgA - 0,2 г/л, ЦИК - 60 ед., СН50 - 59,6 ед. оп.пл. Метод моноклональных антител: лимфоциты - 3,66·109/л, CD3 - 2,6·109/л, CD19 - 0,8·109/л, CD4 - 1,6·109/л, CD8 - 0,8·109/л, CD16/56 - 0,3·109/л, CD23 - 0,69·109/л.
Пример 2. Иллюстрацией схемы терапии больных с бактериальными менингитами является обследование 63 детей в отделении нейроинфекций и отделении реанимации и интенсивной терапии городской детской инфекционной больницы №4 г.Екатеринбурга. Возраст детей от 1 мес до 1 года.
Были выделены две группы. В первую группу (30 человек) были включены дети с серологическими (IgM, IgG) и молекулярно биологическими маркерами (верификация ДНК ЦВМ в реакции ДОТ-гибридизации и ЦПР). Вторая группа (24 человека) - контрольная.
Для исключения микстовых инфекций все дети были обследованы на маркеры герпетической, токсоплазменной инфекций и краснухи и не имели серологических и молекулярно-биологических маркеров данных инфекций.
Изучение эффективности антибактериальной терапии цефтриаксоном выполнено у 17 больных с острыми бактериальными нейроинфекциями, контрольная группа (18 человек) получала традиционную комбинированную антибактериальную терапию.
Этиологическая структура менингитов расшифрована у 67,8% больных и с учетом идентификации возбудителя из спинномозговой жидкости распределилась следующим образом: менингококковые менингиты - 46,6%, менингиты, вызванные H.influenzae - 8,3%, пневмококковые менингиты - 3,3%, менингиты прочей этиологии - 32,2%.
Сопоставляя две группы больных и оценивая эффективность терапии, видно, что в группе детей, получавших цефтриаксон, состояние оценивалось как тяжелое в течение 10,5±1,2 дней, а в группе контроля - 16,6±2,1 дней. Назначение в терапии нейроинфекций цефтриаксона привело к сокращению длительности неврологической симптоматики (табл.20).
Помимо традиционных медикаментозных методов лечения нейроинфекций как монобактериальных, так и при вирусно-бактериальных ассоциациях, находят применение и нетрадиционные методы. Один из них - гипербарическая оксигенация (ГБО), где кислороду отводится роль универсального адаптогенного регулятора биодинамики нормальной и патологической клетки.
Хотя метод ГБО известен давно и находит широкое применение в основном в реабилитационной терапии, но использование ГБО в остром периоде нейроинфекций заявителю не известно.
Таким образом, при проведении мероприятий по востановлению и сохранению здоровья сформированных контингентов впервые предложены клинические, молекулярно-генетические и иммунологические критерии диагностики репликативной и латентной форм ЦМВ-инфекции у детей раннего возраста.
Выявлены особенности формирования иммунного ответа по максимальной индикации ДНК-ЦМВ в моче с обнаружением в крови ДНК-ЦМВ, IgM к ЦМВ.
Применение фамвира в противовирусной терапии подавляет репликации вируса эффективнее других препаратов.
Использование ревамицина на этапах планирования и течения беременности снимает риск рождения детей в асфикции с оценкой по шкале Апгар до нулевых параметров, а также снижает риск формирования патологии органов дыхания у детей.
Включение в схему ведения нейроинфекций цефтриаксона позволяет сократить длительность проявления неврологической симптоматики и тяжесть состояния больных детей.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ЦМВ-ИНФЕКЦИИ У ДЕТЕЙ РАННЕГО ВОЗРАСТА | 2004 |
|
RU2272645C2 |
| ИНТЕГРИРОВАННЫЙ МОДУЛЬ ОЦЕНКИ ЗДОРОВЬЯ СЕМЬИ | 1996 |
|
RU2125829C1 |
| СПОСОБ ИНТЕГРАЛЬНОЙ ОЦЕНКИ ЗДОРОВЬЯ СЕМЬИ | 1996 |
|
RU2122832C1 |
| СПОСОБ ПРОВЕДЕНИЯ ПРЕВЕНТИВНЫХ МЕРОПРИЯТИЙ, НАПРАВЛЕННЫХ НА ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ У ДЕТЕЙ РАННЕГО ВОЗРАСТА, РОЖДЕННЫХ ОТ МАТЕРЕЙ С ОППОРТУНИСТИЧЕСКИМИ ИНФЕКЦИЯМИ | 2007 |
|
RU2355447C1 |
| СПОСОБ ЛЕЧЕНИЯ АТОПИЧЕСКОГО ДЕРМАТИТА У ДЕТЕЙ ПРИ ДИАГНОСТИРОВАННОЙ ЦИТОМЕГАЛОВИРУСНОЙ ИНФЕКЦИИ | 2007 |
|
RU2402776C2 |
| СПОСОБ ЛЕЧЕНИЯ СИАЛОАДЕНИТА | 2007 |
|
RU2413507C2 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ ЦИТОМЕГАЛОВИРУСНОЙ ИНФЕКЦИИ У НОВОРОЖДЕННЫХ | 2006 |
|
RU2317550C1 |
| СПОСОБ ПРОФИЛАКТИКИ ВНУТРИУТРОБНЫХ ИНФЕКЦИЙ У ДЕТЕЙ | 2003 |
|
RU2239442C1 |
| СПОСОБ ЛЕЧЕНИЯ НЕВРОЛОГИЧЕСКИХ ПОВРЕЖДЕНИЙ У ДЕТЕЙ | 2005 |
|
RU2314817C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЧАСТЫХ ОРВИ НА ПЕРВОМ ГОДУ ЖИЗНИ У ДЕТЕЙ, ПЕРЕНЕСШИХ ЦИТОМЕГАЛОВИРУСНУЮ ИНФЕКЦИЮ В ПЕРВЫЕ ДВА МЕСЯЦА ЖИЗНИ | 2012 |
|
RU2484474C1 |

Изобретение относится к медицине и может быть использовано для профилактики, диагностики и лечения TORCH-инфекций с целью оздоровления различных контингентов, характеризующих семью - мать и ребенка. Для этого проводят комплексную диагностику указанных инфекций у матери и ребенка и в тактику ведения детей дополнительно вводят фамвир в дозе 125 мг/сутки курсом 7-10 дней, цефтриаксон в дозе 100 мг/кг/сутки курсом 7-10 дней. Женщинам на этапах планирования и течения беременности вводят ровамицин. Детям с нейроинфекцией дополнительно проводят 8-10 сеансов ГБО. Способ обеспечивает оздоровление семьи “мать-ребенок” за счет предупреждения и лечения внутриутробных инфекций и их последствий. 25 табл., 2 ил.
Способ восстановления и сохранения здоровья семьи, включающий формирование контингентов “беременная - плод”, “роженица - плод”, “родительница - новорожденный”, “кормящая мать - грудной ребенок”, “женщина мать - ребенок 0-15 лет”, клинико-лабораторные обследования сформированных контингентов, регистрацию результатов обследования, причем контингенты формируют по маркерам TORCH-ассоциированной патологии матери и ребенка, определяют комплекс информационно значимых параметров, связанных функциональным действием, а именно: параметров иммунодиагностики, иммунного профиля матери и ребенка, эндокринного профиля, иммуногенетической диагностики, невропатологических параметров, зарегистрированные параметры преобразуют в графическую форму, по которой определяют прогностические маркеры, проводят сравнительный анализ значений параметров, диагностируют состояние обследуемых, по результатам диагностики определяют тактику ведения сформированных контингентов, отличающийся тем, что в клинико-лабораторные исследования дополнительно вводят исследование пуповинной крови, околоплодных вод, крови и мочи, молекулярно-генетическую диагностику репликативной и латентной форм ЦВМ-инфекции у детей раннего возраста, в комплекс информационно значимых параметров дополнительно вводят параметры диагностики полиорганной патологии при моно - ЦВМ, ЦВМ - хламидийно-уреаплазменной, хламидийной и уреаплазменной инфекциях, параметры диагностики полиантигенного воздействия, параметры иммунного ответа при репликативной и латентной формах ЦМВ-инфекций, определяемые по максимальной индикации ДНК - ЦВМ в моче и обнаружением в крови ДНК - ЦВМ, IgM, IgM к ЦВМ, параметры иммунного ответа у детей раннего возраста с ЦВМ-бактериальными ассоциациями с сочетанным поражением ЦНС по варианту менингоэнцефалита, параметры уровня CD23-лимфоцитов, влияющих на формирование бронхообструктивного синдрома, ассоциированного с TORCH-инфекциями у детей, параметры иммунофенотипических маркеров и цитокинового профиля у беременных женщин с хроническим пиелонефритом, в тактику ведения сформированных контингентов дополнительно вводят Фамвир - в качестве противовирусного препарата, который назначают детям в дозе 125 мг/сут, курсом 7-10 дней, дополнительно вводят Цефтриаксон - в качестве комбинированной терапии, который назначают детям в дозе 100 мг/кг, но не более 4 г, внутривенно медленно, один раз в сутки, курсом 7-10 дней, дополнительно вводят ровамицин - в качестве превентивного лечения женщинам на этапах планирования и течения беременности, в обычных дозах, дополнительно вводят детям с нейроинфекцией курс гипербарической оксигенации 8-10 сеансов - в качестве адаптагенного регулятора биодинамики нормальной и патологической клетки.
| СПОСОБ ИНТЕГРАЛЬНОЙ ОЦЕНКИ ЗДОРОВЬЯ СЕМЬИ | 1996 |
|
RU2122832C1 |
| СПОСОБ ИММУНОЛОГИЧЕСКОЙ ОЦЕНКИ АДАПТАЦИИ НОВОРОЖДЕННЫХ ДЕТЕЙ | 1999 |
|
RU2152619C1 |
| RU 2000107001 A, 10.01.2002 | |||
| БЕЛОБОРОДОВА Н.В | |||
| и др | |||
| Роцефин в неонатологии | |||
| Педиатрия, 1997, №4, с.136-140 | |||
| МИХАЙЛОВА И.В | |||
| Клинико-иммунологические особенности ЦМВ - бактериальной ассоциации при нейроинфекции у детей и оптимизация антибактериальной терапии | |||
| Автореф | |||
| канд | |||
| дисс., Екатеринбург, 2000, с.39 | |||
| ГЛАЗКОВА Л.К | |||
| и др | |||
| Опыт применения ровамицина в терапии беременных с урогенитальной хламидийной инфекцией | |||
| Вестник дерматологии и венерологии, 1997, №5, с.75-76. | |||
Авторы
Даты
2004-06-20—Публикация
2002-08-19—Подача